Цирроз ассоциированный с вирусом с

Цирроз печени (ЦП), осложненный портальной гипертензией (ПГ), нередко развивается на фоне вирусного гепатита С (HCV). Он является одной из актуальных медико-социальных проблем современной гепатологии. Способность возбудителя оказывать прямое цитопатическое действие на гепатоциты, его репликация в моноцитах и макрофагах часто приводят к развитию первично-хронического течения гепатита, трансформации в цирроз и первичную гепатокарциному и является причиной развития стойкой иммунной недостаточности [13,16,20,21,22]. Длительная вирусная инфекция (гепатит С) приводит к истощению иммунных механизмов, в частности к дефициту и истощению функций Th1 лимфоцитов, ответственных за выработку интерлейкина-2 [4,18,20,21]. Отмеченная особенность наиболее важна при хронической и тяжело протекающей патологии, когда применение традиционных иммуномодуляторов или синтетических индукторов синтеза цитокинов бессмысленно из-за истощения компенсаторных возможностей иммунной системы при необходимости дальнейшей хирургической коррекции внутрипеченочной ПГ [2,5,6,7,11,14,15,19]. Также нельзя не учитывать у данной категории пациентов явлений эндотоксемии, ишемию кишечника с микробной транслокацией, фармакологический анамнез и инвазивные манипуляции – как последовательность событий в формировании системного воспалительного ответа [1,3,8,12].
Появление синдрома портальной гипертензии (ПГ) имеет чрезвычайно важное значение в течение заболевания. Являясь приспособительным явлением в начале заболевания, ПГ с прогрессированием процесса приобретает роль ведущего патогенетического клинического фактора [23].
Асцит, рефрактерный к медикаментозным мероприятиям, встречается примерно у 10 % больных с ЦП [9]. С момента появления асцита у пациентов летальность составляет 42–70 % в течение года [17].
В ряде исследований последнего десятилетия установлена роль и значение гипопротеинемии как одного из основных факторов неблагоприятного исхода хирургического лечения больных с синдромом портальной гипертензии [10].
Наличие свободной жидкости в животе на фоне цирроза печени нередко сопровождается ее инфицированием – спонтанным бактериальным перитонитом. За последние годы частота этого осложнения значительно возросла и достигла 12–21 % [24,25].
Целью работы является улучшение результатов лечения пациентов с вирус-ассоциированнымHCV циррозом печени путём ликвидации гипо- и диспротеинемии, а также необходимостью предотвращения инфекционных осложнений и опасности развития генерализованной инфекции с проведением опережающего лечения, а именно – раннего применения интерлейкина-2 человеческого рекомбинантного при дальнейшей хирургической коррекции внутрипеченочной портальной гипертензии одним из известных способов.
Материалы и методы. В клинике хирургии Ростовского государственного медицинского университета с 1997 года пролечен 341 пациент с портальной гипертензией. Внутрипеченочная форма ПГ была у 297 (87,1 %) больных и у 2 (0,6 %) пациентов носила смешанный характер (внутрипеченочный и надпеченочный).
Из 299 больных внутрипеченочной ПГ у 287 был выявлен цирроз печени (у 227 из них в анамнезе выявлен вирусный гепатит), у 6 пациентов выявлена альфа-1-антитрипсиновая недостаточность, у одного редко встречающаяся гепатоцеребральная дистрофия (болезнь Вильсона – Коновалова), приведшие к развитию фиброза печени, у ребенка 8 лет ПГ развилась, как осложнение врожденного фиброза печени. У одного пациента регенеративный узел печени вызвал ПГ. Трем пациентам был поставлен диагноз полинодулярной трансформации печени. У двоих из них ПГ носила смешанный характер за счет гипоплазии нижней полой вены в области впадения печеночных вен с деформацией и стенозом их устьев в одном случае и сдавления печеночных вен и нижней полой вены в другом.
Из 297 пациентов с внутрипеченочной ПГ было выполнено 79 операций спленоренального венозного шунтирования (СВШ) и 128 операций трансъюгулярного внутрипеченочного портосистемного шунтирования (ТВПШ). Помимо этого больным выполнялся лапароцентез с реинфузией концентрата асцитической жидкости (38).
Из 207 пациентов, которым выполнялась коррекция ПГ одним из вышеуказанных способов, у 79 (38,2 %) вирусный гепатит не был выявлен. У 9 (4,3 %) в анамнезе присутствовал вирусный гепатит А, у 26 (12,6 %) – вирусный гепатит В, у 75 (36,2 %) – вирусный гепатит С, различное сочетание двух или трех вирусных гепатитов было у 18 (8,7 %) больных. Подробная характеристика представлена на рис.1.
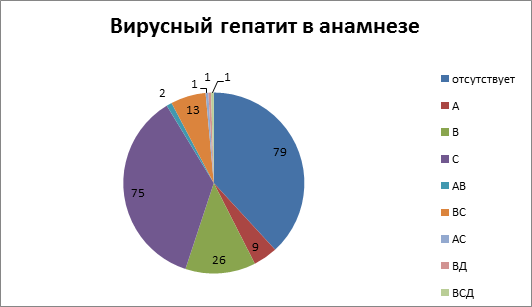
Рис.1. Этиология цирроза печени
Таким образом, вирус-ассоциированный цирроз печени присутствовал у 119 (67,5 %) больных, из них хронический вирусный гепатит С был выявлен у 89 (43,0 %) пациентов.
Сущность метода заключается в том, что внутривенно со скоростью перфузии 60 капель в минуту вводят 500 мл приготовленного концентрата асцитической жидкости с добавлением в него интерлейкина-2 человеческого рекомбинантного в дозе 500 МЕ, при необходимости оставшуюся часть концентрата вводят дробно по 500 мл интраоперационно и в первые сутки после хирургического лечения.
Результаты. 12 пациентам с вирус-ассоцированнымHCV циррозом печени и признаками иммунной недостаточности по клеточному типу с дефицитом CD3⁺- и CD4⁺-позитивных лимфоцитов, снижением содержания CD4⁺CD25⁺-лимфоцитов и NK-клеток, дисиммуноглобулинемией в предоперационном периоде была выполнена реинфузия концентрата асцитической жидкости по ранее заявленной методике.
Состав асцитической жидкости был исследован кроме данной группы еще у 26 больных с ЦП, всего у 38 пациентов. При биохимическом исследовании определялось содержание общего белка и белковых фракций, мочевины, креатинина и билирубина. Количество общего белка в асцитической жидкости составляло от 17,6 до 42,8 г/л (28,2±9,6 г/л). Низкое его содержание было у больных, которым ранее неоднократно выполнялся лапароцентез. Содержание альбумина в процентах составило 49,4±5,3, α-глобулина –14,1±2,4, β-глобулина – 13,4±1,9, γ-глобулина – 24,5±3,6, средние молекулы были в пределах 0,386±0,045 у.е.
В среднем показатели цитоза составляли 297±174 клеток в 1 мм3. Основную часть клеток при микроскопии осадка составляли лимфоциты (69 %), меньшую – сегментоядерные нейтрофилы (10 %), моноциты (2 %), макрофаги (2 %), мезотелиальные клетки (6 %), а также мононуклеары (11 %).
После ультрафильтрации объем асцитической жидкости уменьшался от 5 до 10 раз, содержание общего белка возрастало до 49,3±18,4 г/л. Фракция альбумина повышалась до 52,2±6,8 %, а количество γ-глобулина снижалось.
После выполнения реинфузии концентрата асцитической жидкости показатели общего белка плазмы крови составили 52,4±9,3 г/л до переливания и 58,8±8,4 г/л после, % содержание альбумина - 41,7±14,4 и 47,2±6,4 соответственно. Процент содержания гамма-глобулина – 32,6±7,5 до переливания и 28,4±5,4 после переливания. Коэффициент (отношение альбуминов к глобулинам) составил 0,62±0,04 и 1,1±0,03 соответственно.
После выполнения реинфузии перед операцией спленоренального венозного шунтирования (8) или трансъюгулярного внутрипеченочного портоситемного шунтирования (4) ни одному из 12 пациентов не понадобилось дополнительное введение альбумина, не было выявлено признаков гнойных осложнений, послеоперационные раны в 8 наблюдениях после СВШ зажили первичным натяжением, стабилизировались показатели биохимического анализа крови (табл.1).
Изменения показателей крови больных ЦП до и после лечения
Основные факты
- Вирус гепатита D (HDV) представляет собой вирус, для репликации которого необходим вирус гепатита B (HBV). Инфицирование HDV происходит только одновременно с HBV или в виде суперинфекции по отношению к HBV.
- Передача вируса чаще всего происходит перинатальным путем от матери ребенку, а также при контакте с кровью или другими биологическими жидкостями.
- Вертикальная передача от матери ребенку происходит редко.
- Не менее 5% всех людей с хронической инфекцией также инфицированы HDV. Другими словами, во всем мире число инфицированных HDV составляет 15-20 млн. человек. Тем не менее, это только приблизительная цифра, поскольку многие страны не ведут учета распространенности гепатита D.
- С 1980 г. наблюдается снижение общего числа случаев инфекции гепатита D в мире. Эта тенденция, главным образом, связана с успехами глобальной программы вакцинации против гепатита В.
- Коинфекция HDV-HBV считается самой тяжелой формой хронического вирусного гепатита ввиду более быстрого смертельного исхода от болезней печени и гепатоклеточной карциномы.
- В настоящее время показатели эффективности курсов лечения, в целом, невысоки.
- Инфекцию гепатита D можно предотвратить посредством иммунизации против гепатита В.
Гепатит D — это болезнь печени, протекающая как в острой, так и хронической форме, вызываемая вирусом гепатита D (HDV), для репликации которого необходим вирус HBV. Заражение вирусом гепатита D происходит только в присутствии вируса гепатита B. Коинфекция HDV-HBV считается наиболее тяжелой формой хронического вирусного гепатита гепатита ввиду более быстрого смертельного исхода от болезней печени и гепатоклеточной карциномы.
Единственным способом предотвращения инфекции HDV является вакцина против гепатита B.
Острый гепатит: одновременное инфицирование HBV и HDV может приводить к гепатиту в умеренной или тяжелой форме или даже к фульминантному гепатиту, но обычно за этим следует полное выздоровление, и хронический гепатит D развивается редко (менее чем в 5% случаев острого гепатита).
Суперинфекция: HDV может инфицировать человека, уже имеющего хроническую инфекцию HBV. Суперинфекция HDV при хроническом гепатите B ускоряет развитие более тяжелых форм болезни в любом возрасте у 70-90% людей. Суперинфекция HDV ускоряет развитие цирроза почти на 10 лет по сравнению с моноинфекцией HBV, несмотря на то, что HDV подавляет репликацию HBV. Механизм, ввиду которого HDV вызывает более тяжелый гепатит и ускоренное развитие фиброза по сравнению с моноинфекцией HBV остается неясным.
Риску инфицирования HDV подвержены хронические носители HBV.
Люди, у которых нет иммунитета к HBV (как естественного после болезни, так и в результате иммунизации вакциной против гепатита B), подвергаются риску инфицирования HBV, что сопряжено с риском инфицирования HDV.
Высокая распространенность гепатита D среди людей, употребляющих инъекционные наркотики, указывает на то, что употребление наркотиков является серьезным фактором риска коинфекции HDV.
Сексуальные контакты с высоким уровнем риска (например, у работников секс-индустрии) – также фактор повышенного риска инфекции HDV.
Миграция из стран с высокой распространенностью HDV в страны с низкой его распространенностью может оказывать влияние на эпидемиологическую ситуацию в принимающей стране.
Инфекция HDV диагностируется путем выявления высоких титров иммуноглобулина G (IgG) и иммуноглобулина M (IgM), антител к HDV, и подтверждается путем выявления РНК HDV в сыворотке.
Однако широкий доступ к диагностике HDV отсутствует, как и стандартизированный подход к анализу на наличие РНК HDV, который используется для мониторинга ответа на противовирусную терапию.
При отсутствии возможности количественного анализа РНК HDV целесообразным маркером для мониторинга реакции на лечение является HBsAg. Снижение титра HBsAg часто свидетельствует об исчезновении поверхностного антигена и клиренсе HDV, хотя исчезновение поверхностного антигена редко встречается при лечении.
В текущих руководствах обычно рекомендуется прием пегилированного интерферона альфа в течение как минимум 48 недель независимо от форм ответа на лечение. Общий уровень устойчивого вирусологического ответа низкий, однако это лечение является независимым фактором, ассоциированным с меньшей вероятностью прогрессирования заболевания.
Для пациентов с фульминантным гепатитом и болезнью печени на последних стадиях может рассматриваться возможность трансплантации печени. Необходимы новые терапевтические средства и стратегии. Новые препараты, такие как ингибитор пренилирования или ингибиторы входа HBV, дали предварительные положительные результаты.
ВОЗ не публиковала конкретных рекомендаций в отношении гепатита D. Тем не менее, рекомендованные меры по предотвращению передачи HBV, такие как иммунизация против гепатита B, безопасная практика инъекций, обеспечение безопасности крови и услуги по снижению вреда, заключающиеся в предоставлении стерильных игл и шприцев, эффективны для предотвращения передачи HDV.
В мае 2016 г. Всемирная ассамблея здравоохранения приняла первую “Глобальную стратегию сектора здравоохранения по вирусному гепатиту на 2016-2021 гг.”. В этой стратегии подчеркивается решающая роль всеобщего охвата услугами здравоохранения, а задачи стратегии находятся в соответствии с задачами в рамках Целей в области устойчивого развития. Главной целью стратегии является ликвидация вирусного гепатита в качестве проблемы общественного здравоохранения, и это отражено в глобальных задачах по сокращению числа новых случаев инфекции вирусного гепатита на 90% и сокращению смертности от вирусного гепатита на 65% к 2030 году. Действия, которые должны проводить страны и Секретариат ВОЗ для выполнения этих задач, изложены в стратегии.
Для оказания поддержки странам в ходе выполнения глобальных целей по гепатиту в рамках Повестки дня в области устойчивого развития на период до 2030 г. ВОЗ проводит работу по следующим направлениям:
- повышение осведомленности, укрепление партнерств и мобилизация ресурсов;
- разработка основанной на фактических данных политики и сбор данных для информационного обеспечения практических действий;
- предотвращение передачи инфекции;
- расширение услуг в области скрининга, ухода и лечения.
Кроме того, ежегодно 28 июля ВОЗ проводит Всемирный день борьбы с гепатитом для повышения осведомленности о вирусном гепатите и более глубокого осмысления связанных с ним проблем.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Ключевые слова: хронический гепатит С, цирроз печени, гепатоцеллюлярная карцинома.
Для цитирования: Макашова В.В., Омарова Х.Г., Хохлова О.Н., Лукашенко Т.Н. Хронический вирусный гепатит С с исходом в цирроз и гепатоцеллюлярную карциному (клиническое наблюдение). РМЖ. Медицинское обозрение. 2018;8(II):92-96.
Chronic hepatitis C virus with the outcome of cirrhosis and hepatocellular carcinoma (clinical observation)
V.V. Makashova 1,2 , H.G. Omarova 1 , O.N. Hohlova 1 , T.N. Lukashenko 3
1 Central Research Institute of Epidemiology, Moscow
2 Clinical Hospital for the Infectious Diseases, Moscow
3 Outpatient Clinic № 5, Moscow
The article presents a clinical case of a patient with a diagnosis of liver cirrhosis of Child-Pugh class B in the outcome of chronic hepatitis C, treated with interferon and ribavirin for 18 months. In the course of antiviral therapy, RNA of the hepatitis C virus became negative after 8 weeks and remained steadily negative for 2 years. Subsequently, on the background of stress, 3 months after the end of treatment, a relapse of chronic hepatitis C appeared with moderate biochemical and virological activity. 6 months after the relapse, a liver cancer was suspected during an ultrasound examination and histological confirmation was obtained. After a few months, hemorrhage from esophageal varicose veins dilatation (EVVD) occurred in the patient, and after another 1 month, there was repeated hemorrhage from EVVD. The patient was monitored and treated in the intensive care department. Ascites, bilateral pneumonia, fever, leukocytosis appeared. The patient’s condition progressively worsened and with increasing psychomotor agitation, progressive respiratory and cardiovascular insufficiency, biological death was recorded.
There was a divergence of diagnoses, category II. The cause of the fatal outcome was purulent intoxication, as a result of ulcers perforation of the esophagus, purulent mediastinitis with pleural empyema on the left.
Key words: chronic hepatitis C, cirrhosis, hepatocellular carcinoma.
For citation: Makashova V.V., Omarova H.G., Hohlova O.N., Lukashenko T.N. Chronic hepatitis C virus with the outcome of cirrhosis and hepatocellular carcinoma (clinical observation) // RMJ. Medical Review. 2018. № 8(II). P. 92–96.
Пациент Т., 1948 г. р., 22.01.2009 г. обратился в поликлинику к инфекционисту в связи с лейкопенией (до 3,2×10 9 /л), тромбоцитопенией (60–120×10 9 ). Со слов пациента, антитела к HCV впервые выявлены в 1998 г. Не обследовался, не лечился. Впервые обследовался в поликлинике ФСБ № 5 в 2009 г., выявлена РНК HCV+, 1в генотип, вирусная нагрузка — 1,3×10 6 коп/мл.
Жалобы на периодически возникающую слабость и утомляемость.
Перенесенные заболевания: 1972 г. — аппендэктомия, 1992 г. — острый вирусный гепатит А, 1995 г. — оперирован по поводу синдрома Меллори — Вейса. В это же время были гемотрансфузии. 1996 г. — грыжесечение, 1997 г. — повторное грыжесечение, 2004 г. — язвенная болезнь 12-перстной кишки, 2005 г. — правостороннее воспаление легких, хронический бронхит, 2007 г. — повторная пневмония, 2007 г. — сильное кровотечение при удалении зубов, гипертоническая болезнь, сахарный диабет 2-го типа.
Аллергоанамнез — не отягощен.
Наследственность: у отца — цирроз печени алкогольного генеза, у матери — инсульт, у брата — хронический вирусный гепатит В.
Вредные привычки: не курит, алкоголь употреблял часто, но немного (со слов), крепкие напитки (виски, коньяк).
Объективно при осмотре: сосудистые звездочки в области грудной клетки, умеренная пальмарная эритема, иктеричность склер. Печень пальпаторно и перкуторно увеличена — выступает на 4–5 см ниже реберной дуги, селезенка не пальпируется.
Рост — 173 см, вес — 80 кг.
Динамика основных показателей общего и биохимического анализов крови, данные ПЦР-диагностики представлены в таблице 1.
, MD, MPH, Harvard Medical School
Last full review/revision January 2019 by Anna E. Rutherford, MD, MPH
Гепатит длительностью > 6 мес. обычно называют хроническим гепатитом, хотя эта продолжительность выбрана произвольно.
Есть 6 основных генотипов вируса гепатита С (ВГC), которые различаются по их ответной реакции на лечение. Генотип 1 более распространен, чем генотипы 2, 3, 4, 5 и 6. На его долю приходится 70–80% случаев хронического гепатита С в США.
Острый гепатит С переходит в хроническую форму примерно у 75% пациентов. По оценкам ЦКЗ около 2,7 - 3,9 миллионов человек в США имеют хроническую инфекцию гепатита C. По оценкам 71 миллион человек во всем мире имеют хронический гепатит C (1).
Хронический гепатит С у 20–30% пациентов прогрессирует в цирроз; на формирование цирроза печени часто уходят десятилетия. Гепатоклеточная карцинома может развиться на фоне цирроза, вызванного ВГС, без цирроза данный вирус редко вызывает гепатоцеллюлярную карциному (в отличие от ВГВ-инфекции).
Общие справочные материалы
1. World Health Organization: Hepatitis C. По состоянию на 13.12.2018 г.
Клинические проявления
У многих пациентов заболевание протекает бессимптомно и без желтухи, хотя у некоторых проявляется недомогание, анорексия, утомляемость и неспецифический дискомфорт в верхней части живота. Часто первые проявления являются признаками хронического заболевания печени (например, спленомегалия, звёздчатые гемангиомы, ладонная эритема) или осложнений цирроза (например, портальная гипертензия, асцит, энцефалопатия).
Хронический гепатит C иногда ассоциирован с красным плоским лишаем, кожно-слизистым васкулитом, гломерулонефритом, поздней кожной порфирией, криоглобулинемией смешанного типа и, возможно, неходжкинской В-клеточной лимфомой. Симптомы криоглобулинемии включают утомляемость, миалгию, артралгию, нейропатию, гломерулонефрит и высыпания (крапивница, пурпура, лейкоцитокластический васкулит); чаще встречается бессимптомная криоглобулинемия.
Скрининг
Люди с определенными характеристиками должны быть проверены на наличие гепатита С, не зависимо от того, имеют они симптомы, указывающие на заболевание, или нет. Одноразовый скрининг рекомендуется для людей со следующими характеристиками (1,2):
Родились между 1945 и 1965 годами, независимо от страны рождения
В настоящее время используют или когда-либо вводили запрещенные препараты, даже если это имело место только один раз или только в далеком прошлом
Использовали интраназальные запрещенные препараты
Получали концентраты фактора свертывания крови, произведенные до 1987 года
Получали переливание крови или пересадку органов до июля 1992 года
В настоящее время или когда-либо лечились с применением долгосрочного гемодиализа
Имеют аномальные уровни АЛТ или хроническое заболевание печени невыясненной этиологии
Работают в области здравоохранения или общественной безопасности и подвергались воздействию ВГС-положительной крови через иглоукалывание, другие повреждения острым предметом или контакт со слизистой оболочкой
Когда-либо были заключены в тюрьму
Являются детьми ВГС-инфицированных женщин
Такое тестирование важно, поскольку симптомы могут не развиваться до тех пор, пока гепатит С сильно не повредит печень, что происходит спустя годы после первичной инфекции.
2. CDC: Testing recommendations for hepatitis C virus infection. По состоянию на 13.12.2018 г.
Диагностика
(См. Практическое руководство Американской ассоциации по изучению заболеваний печени [AASLD] Диагностика, ведение и лечение гепатита С [Diagnosis, Management, and Treatment of Hepatitis C] и Клинические рекомендации Целевой группы профилактических услуг США [U.S. Preventive Services Task Force] по скринингу взрослого населения на гепатит С [Screening for Hepatitis C in Adults]).
Диагноз хронического гепатита С следует подозревать при наличии у пациента любого из следующих признаков:
Наличие клинических симптомов и признаков, характерных для заболевания
Случайное обнаружение повышенных уровней аминотрансфераз
Ранее диагностированный острый гепатит
Диагноз подтверждается при обнаружении положительного анти-ВГC и положительного РНК ВГC через ≥ 6 мес после начальной инфекции (см. таблицу Серологический анализ на гепатит С [Hepatitis C Serology]).
Острой инфекции ВГC
Хронической инфекции ВГC
Предполагаемой инфекции ВГС*
* Пациенты с инфекцией ВГC, спонтанно выздоровевшие или успешно вылеченные.
анти-ВГC = антитела к вирусу гепатита С; ВГC означает вирус гепатита С.
Биопсия печени применяется с целью (1 или более из перечисленных пунктов):
Определения активности воспалительного процесса;
Определения стадии фиброза или прогрессирования заболевания (что иногда помогает определить каких пациентов леченить и когда);
Исключения других причин заболевания печени;
Тем не менее, роль биопсии печени при гепатите С находится на стадии развития, ее вытесняют методы неинвазивной визуализации (напр., ультразвуковая эластография, магнитно-резонансная эластография), сывороточные маркеры фиброза, а также системы оценки фиброза на основе серологических маркеров.
Генотип ВГС определяется до начала лечения, так как от него зависит курса, продолжительность, и успех лечения.
Выявление и количественное определение РНК-ВГС помогает диагностировать гепатит C и оценивать эффективность во время и после лечения. Для большинства существующих в настоящее время количественных РНК-ВГС тестов нижний предел чувствительности составляет не менее 50 МЕ/мл. Если количественный тест не имеет такого уровня чувствительности, то может быть использован качественный. Качественные анализы могут обнаруживать очень низкие уровни РНК-ВГС, часто
Функциональные пробы печени необходимы в том случае, если они ранее не проводились. Они включают определение АЛТ, АСТ, щелочной фосфатазы и билирубина в сыворотке.
Также необходимо провести другие исследования для определения степени тяжести заболевания. Они включают сывороточный альбумин, количество тромбоцитов и ПВ/МНО.
Пациентов следует обследовать на ВИЧ и инфекцию гепатита B, потому что передача этих инфекций подобна.
Если при хроническом гепатите C имеются симптомы криоглобулинемии, то необходимо измерить уровни ревматоидного фактора и криоглобулинов. Высокий ревматоидный фактор и низкий уровень комплемента характерны для криоглобулинемии.
Пациенты с хронической инфекцией ВГС и прогрессирующим фиброзом или циррозом должны обследоваться каждые 6 мес. с применением УЗИ и измерением сывороточного альфа-фетопротеина на гепатоцеллюлярный рак, хотя целесообразность этой практики, в частности, измерения альфа-фетопротеина, спорна.
Прогноз
Прогноз зависит от того, есть ли у пациентов УВО (т. е. РНК ВГС не обнаруживается на 12 и 24 неделе после завершения лечения, в зависимости от использованной схемы лечения).
У пациентов, которые достигли УВО вероятность остаться РНК-ВГС отрицательными составляет > 99%, и они, как правило, считаются вылеченными. Почти у 95% пациентов с УВО улучшились гистологические признаки, в том числе фиброз и индекс гистологической активности; Кроме того, риск развития цирроза, печеночной недостаточности и смерти от заболеваний печени снизился. У пациентов с циррозом печени и портальной гипертензией, которых лечили по схеме с использованием интерферона, УВО показал снижение портального давления, значительное снижение риска развития печеночной декомпенсации, общей смертности и смертности по причине болезни печени, случаев гепатоцеллюлярной карциномы (1).
Достижение УВО при лечении интерфероном, более вероятно, когда присутствует ≥ 1 из ниже перечисленных факторов:
Любой генотип, кроме 1;
Низкая вирусная нагрузка до начала лечения;
1. van der Meer AJ, Veldt BJ, Feld JJ, et alvan der Meer AJ, Veldt BJ, Feld JJ, et al: Association between sustained virological response and all-cause mortality among patients with chronic hepatitis C and advanced hepatic fibrosis. JAMA 308 (24):2584–2593, 2012.
Лечение
Антивирусные препараты прямого действия
(См. в Практическом руководстве Американской ассоциации по изучению заболеваний печени [the American Association for the Study of Liver Disease’s [AASLD] practice guidelines] Рекомендации по диагностике, контролю течения и лечению гепатита С [Recommendations for testing, managing, and treating Hepatitis C] и Положения Американской ассоциации исследований заболеваний печени/Американского общества инфекционистов [AASLD/Infectious Disease Society of America guidelines] "Когда и кому начинать лечение ВГС" [When and in Whom to Initiate HCV Therapy]).
Лечение хронического гепатита С назначается, когда присутствуют оба из ниже перечисленных факторов:
Уровни аминотрансферазы повышены;
Биопсия выявляет активное воспалительное заболевание с развитием фиброза.
Основная цель лечения – стойкая элиминация РНК-ВГС (т.е. УВО), что сопровождается стабильной нормализацией уровня сывороточных трансаминаз и улучшением гистологической картины. Результаты лечения являются более обнадеживающими у пациентов с умеренным фиброзом и вирусной нагрузкой 800000 МЕ/мл.
До конца 2013 года, пациентов с любыми генотипами лечили пегилированным ИФН-альфа в сочетании с рибавирином. В настоящее время большинство пациентов лечатся противовирусными препаратами (противовирусные препараты прямого действия [ПППД]), которые поражают специфические мишени ВГC, такие как протеазы или полимеразы (см. также Генотип 1 вируса гепатита С [HCV genotype 1] и Генотипы 2, 3, 4, 5 и 6 вируса гепатита С [HCV genotypes 2, 3, 4, 5, and 6]).
ПППД используемые для лечения ВГС включают:
Телапревир и боцепревир: ингибитор протеазы 1 поколения с активностью против генотипа 1;
Симепревир: ингибитор протеазы 2 поколения с активностью против генотипа 1;
Софосбувир: ингибитор полимеразы с активностью против ВГC всех генотипов от 1 до 6;
Паритапревир: ингибитор протеазы;
Ледипасфир: ингибитор протеазы;
Дасабувир: ингибитор полимеразы;
Омбитасвир: ингибитор вирусного неструктурного белка 5А (ингибитор NS5A);
Даклатасвир: ингибитор NS5A
Элбасвир: ингибитор NS5A
Гразопревир: ингибитор протеазы
Велпатасвир: ингибитор NS5A с активностью в отношении всех генотипов ВГС
Глекапревир: ингибитор протеазы с активностью в отношении всех генотипов ВГC
Пибрентасвир: ингибитор NS5A с активностью в отношении всех генотипов ВГC
Воксилапревир: ингибитор протеазы NS3/4A
Телапревир, боцепревир и симепревир традиционно спользовали вместе с пэгилированным ИФН и рибавирином, но схемы лечения на основе интерферона больше не считаются стандартом лечения.
Софосбувир можно применять без интерферона; его можно назначать с рибавирином (для генотипов 1–6), симепревиром (для генотипа 1) или даклатасвиром (для генотипов 1–3) в пероральных схемах лечения. Ледипасфир и софосбувир доступны в одной таблетке для лечения ВГС генотипа 1, 4 и 6.
Комбинированный препарат элбасвир/гразопревир используют для лечения пациентов с вирусным гепатитом С 1-го и 4-го генотипа.
Велпатасвир и софосбувир доступны в одной таблетке для лечения ВГС генотипов от 1 до 6.
Глекаправир и пибрентасвир доступны для лечения ВГС, вызванного генотипами 1, 4 и 6, в форме одной таблетки.
Ниже приведена 5-ти компонентная схем лечения, эффективная против генотипов 1 и 4:
Паритапревир/ритонавир/омбитасвир (одной таблеткой) 1 раз/день;
Дасабувир 2 раза/день;
Рибавирин 2 раза/день;
Паритапревир/ритонавир/омбитасвир в комбинации с дасабувиром, доступны в одном препарате.
Ритонавир повышает уровень паритапревира, но обладает прямой противовирусной активностью. Рибавирин часто используется с ПППД.
Одна комбинированная таблетка софосбувира 400 мг, велпатасвира 100 мг и воксилапревира 100 мг используется для повторного лечения хронической инфекции, вызванной вирусом гепатита С (ВГС) у взрослых с генотипом 1, 2, 3, 4, 5 или 6, пролеченных до этого по схеме, содержащей ингибитор NS5A, или с генотипом 1a или 3, предварительно пролеченных по схеме, содержащей софосбувир без ингибитора NS5A (1).
Так как в настоящее время разрабатываются все больше и больше ПППД, текущие рекомендации для лечения ВГС быстро развиваются. Recommendations for Testing, Managing, and Treating Hepatitis CРекоммендации по диагностике, контролю течения и лечению гепатита С (Recommendations for Testing, Managing, and Treating Hepatitis C) Американской ассоциации по изучению заболеваний печени (AASLD) и Американского общества инфекционистов (IDSA) доступны в интернете и часто обновляются.
Декомпенсированный цирроз вследствие гепатита С является наиболее частым показанием для трансплантации печени в США. Рецидив после трансплантации, вызванный ВГС, возникает практически всегда без применения ПППД. Срок жизнеспособности трансплантата менее благоприятен, чем при трансплантации по другим показаниям. Однако, у пациентов. после пересадки печени, при использовании ПППД уровень УВО поднимается до 95%, вне зависимости от того есть у них цирроз или нет. Поскольку показатели частоты устойчивого вирусологического ответа очень высоки, трансплантация органов среди пациентов с положительным результатом на вирус гепатита C становится более распространенной, в частности среди реципиентов, которые также имеют положительный результат на вирус гепатита C, что, в свою очередь, расширяет круг потенциальных доноров. Если и реципиент, и донор имеют положительный результат анализа на гепатит С, лечение может быть отложено на период после проведения трансплантации. В результате можно избежать нежелательного предтрансплантационного курса лечения.
В настоящее время считается, что схемы приема эльбасвира/гразопревира или глекапревира/пибрентасвира имеют хороший профиль безопасности и эффективны у пациентов с терминальной стадией заболевания почек, включая пациентов, находящихся на диализе. Лечение гепатита С у пациентов с декомпенсированным циррозом следует назначать при консультации с гепатологами, в идеале в центре по пересадке печени. Схемы лечения ВГС, включающие ингибиторы протеазы, не должны использоваться у пациентов с декомпенсированным циррозом печени, поскольку у пациентов с нарушениями функции печени уровни ингибиторов протеазы повышены.
Все пациенты с гепатитом С, получающие противовирусные препараты прямого действия (ПППД), должны быть проверены на наличие хронического или ранее перенесенного гепатита В; тесты должны включать следующее:
Поверхностный антиген гепатита В (HBsAg)
Поверхностное антитело гепатита В (анти-HBs)
Антитела к сердцевинному антигену вируса гепатита В класса IgG (анти-НВс IgG)
О реактивации гепатита В сообщалось во время или после лечения ВГС с помощью ПППД; таким образом, пациенты с хроническим гепатитом B или признаками перенесенного гепатита B должны наблюдаться на предмет реактивации во время и после лечения ВГС.
Генотип 1 более устойчив к традиционной двухкомпонентной терапии с помощью пегилированного ИФН-альфа в сочетании с рибавирином, чем другие генотипы. Однако теперь с использованием схем лечения противовирусными препаратами прямого действия (ПППД) без ИФН уровень УВО увеличился с
Для генотипа 2 рекомендуется одна из следующих комбинаций:
Фиксированная доза софосбувир 400 мг/велпатасвир 100 мг 1 раз/день в течение 12 недель
Комбинацию препаратов с фиксированными дозировками глекапревира 300 мг/пибрентасвира 120 мг 1 раз/день в течение 8–12 недель
Альтернативной схемой для генотипа 2 является
Софосбувир 400 мг перорально 1 раз/день в комбинации с даклатасвиром 60 мг перорально 1 раз/день от 12 до 24 нед, в зависимости от степени фиброза печени
При генотипе 3, терапия первой линии включает:
Фиксированная доза софосбувир 400 мг/велпатасвир 100 мг 1 раз/день в течение 12 недель
Комбинацию препаратов с фиксированными дозировками глекапревира в 300 мг/пибрентасвира в 120 мг 1 раз/день в течение 8-16 недель
Альтернативной схемой для генотипа 3 является
Софосбувир 400 мг перорально 1 раз/день в комбинации с даклатасвиром 60 мг перорально 1 раз/день с или без рибавирина от 500 до 600 мг перорально 2 раза/день от 12 до 24 нед, в зависимости от степени фиброза печени
При генотипе 4 терапия первой линии включает:
Ледипасвир 90 мг/софосбувир 400 мг перорально 1 раз/день в течение 12 недель
Элбасвир 50 мг/гразопревир 100 мг перорально 1 раз/день в течение 12 недель
Велпатасвир 100 мг/софосбувир 400 мг 1 раз/день в течение 12 недель
Комбинацию препаратов с фиксированными дозировками глекапревира 300 мг/пибрентасвира 120 мг 1 раз/день в течение 8–12 недель
Альтернативной схемой для генотипа 4 является
Паритапревир 150 мг/ритонавир 100 мг/омбитасвир 25 мг перорально 1 раз/день плюс рибавирин 500–600 мг перорально 2 раза/день в течение 12–16 недель
Для генотипов 5 и 6 терапия первой линии включает:
Ледипасвир 90 мг/софосбувир 400 мг перорально 1 раз/день в течение 12 недель
Велпатасвир 100 мг/софосбувир 400 мг 1 раз/день в течение 12 недель
Комбинацию препаратов с фиксированными дозировками глекапревира 300 мг/пибрентасвира 120 мг 1 раз/день в течение 8–12 недель
1. Bourlière M, Gordon SC, Flamm SL, et al: Sofosbuvir , Velpatasvir, and Voxilaprevir for Previously Treated HCV Infection. N Engl J Med 376 (22):2134-2146, 2017. doi: 10.1056/NEJMoa1613512.
Основные положения
Хронический инфекционный гепатит С развивается в 75% случаев острой инфекции и приводит к циррозу печени в 20 - 30% случаев; у некоторых пациентов с циррозом печени развивается гепатоцеллюлярная карцинома.
Диагноз подтверждает выявление положительного анти-ВГС и положительного ВГC-РНК. Позднее проводят биопсию и определяют генотип.
Лечение зависит от генотипа, но так или иначе включает один или несколько противовирусных препаратов прямого действия, иногда с рибавирином.
Пегилированные нтерфероны больше не рекомендуют для лечения хронического гепатита С.
Новые методы лечения могут окончательно ликвидировать РНК-ВГС у > 95% пациентов.
Пациенты с декомпенсированным циррозом печени должны лечиться гепатологами, а схемы лечения, содержащие ингибиторы протеазы, не должны использоваться.
Читайте также:


