Билиарные гепатиты и циррозы печени
По этиологии и патогенезу выделяют следующие формы хронического гепатита:
- хронический вирусный гепатит В,
- хронический вирусный гепатит С,
- хронический вирусный гепатит D,
- аутоиммунный гепатит,
- лекарственный гепатит,
- криптогенный хронический гепатит.
Кроме того, ряд других заболеваний печени может иметь клинико-лабораторные и гистологические признаки хронического гепатита - это болезнь Вильсона-Коновалова, альфа 1-антитрипсиновая недостаточность, начальные стадии первичного билиарного цирроза, первичного склерозирующего холангита.
Хронический вирусный гепатит В, С - воспалительное заболевание печени, обусловленное инфекцией вируса гепатита В (HBV) или С (HCV), способное прогрессировать до цирроза печени. Хронический гепатит В развивается приблизительно у 5% больных с желтушной формой острого гепатита. НСV -инфекция является причиной 70% случаев хронического вирусного гепатита, 40% - цирроза печени и 60% - гепатоцеллюлярной карциномы в мире. Основные пути передачи HBV и HCV-инфекций - парентеральный (контакт с кровью или инфицированным медицинским инструментарием), половой, перинатальный.
Хронический вирусный гепатит В и С характеризуется клиническими проявлениями, складывающимися из поражения печени и/или признаков внепеченочных поражений. Первые клинические симптомы часто проявляются спустя годы или десятилетия после инфицирования. Выделяют астенический, диспепсический, желтушный синдромы, увеличение печени и селезенки. Среди внепеченочных проявлений определяется кожная пурпура, артриты, миалгии, нефротический и мочевой синдромы и другие.
Аутоиммунный гепатит - хронический процесс в печени неизвестной этиологии, механизм развития которого связан с агрессией собственной иммунной системы против компонентов ткани печени.
Аутоиммунный гепатит характеризуется пери-портальным или более обширным воспалительным процессом, наличием гипер- g -глобулинемии и тканевых аутоантител, который в большинстве случаев отвечает на иммунносупрессивную терапию. В качестве основного фактора патогенеза аутоиммунного гепатита рассматривается генетическая предрасположенность. Для реализации процесса необходимы запускающие агенты - вирусы, лекарственные препараты и другие факторы окружающей среды. Выделяют аутоиммунный гепатит 3 типов соответственно профилям выявляемых аутоантител. Аутоиммунный гепатит характеризуется широким спектром клинических проявлений - от бессимптомного до тяжелого, иногда фульминантного гепатита с наличием или отсутствием внепеченочных признаков. При первичном обследовании клинические признаки цирроза печени обнаруживают у 25% больных. Внепеченочные проявления аутоиммунного гепатита - лихорадка, кожные васкулиты, артралгии и артриты, миалгии, полимиозит, лимфоаденопатия, плеврит, перикардит, миокардит, тиреодит Хашимото, гломерулонефрит, язвенный колит, сахарный диабет, гемолитическая анемия и др.
Дефицит α1-антитрипсина является первым по частоте врожденным метаболическим дефектом с аутосомно-кодоминантным типом наследования, вызывающим поражение печени с холестазом и цирроз печени у детей.
Дефицит ингибитора трипсина α1-антитрипсина приводит к повышению активности протеаз, что вызывает повреждение тканей легких, поджелудочной железы, почек. Механизм хронического поражения печени при дефиците α1 -антитрипсина до конца не изучен, его связывают с накоплением α1 -антитрипсина в ткани печени.
Дефицит α1 -антитрипсина клинически характеризуется следующими симптомами - гепатомегалия, реже спленомегалия, желтуха в раннем возрасте. В ряде случаев выявляется патология со стороны легких, поджелудочной железы, почек.
Дефицит α1 -антитрипсина - диагностика:
- исследование функциональных проб печени;
- определение 1-антитрипсина, α1 -глобулинов в сыворотке крови;
- ультразвуковое исследование органов брюшной полости;
- гистологические исследование биоптата печени;
- выявление мутаций гена, ответственного за дефицит α1 -антитрипсина в гомозиготном состоянии при приведении генетического исследования.
Цирроз печени - хроническое диффузное прогрессирующее заболевание печени. Анатомически характеризуется фиброзом, образованием узлов-регенератов, нарушающих дольковую архитектонику органа, и перестройкой внутрипеченочного сосудистого русла.
Этиологические факторы цирроза печени следующие:
- вирусы гепатита В,С, D;
- генетически обусловленные метаболические нарушения - гемохроматоз, болезнь Вильсона-Коновалова, дефицит α1 -антитрипсина, гликогеноз IV типа, галактоземия, наследственная тирозинемия;
- длительный внутри- и внепеченочный холестаз;
- нарушение венозного оттока из печени - синдром Бада-Киари, вено-окклюзионная болезнь и др.;
- токсины и лекарства;
- шунтирующие операции на кишечнике с выключением значительной части тонкой кишки.
Первичный билиарный цирроз представляет собой хроническое воспалительное холестатическое заболевание печени неизвестной (предположительно иммунной) этиологии, ведущее к прогрессирующей необратимой деструкции мелких внутридольковых и септальных желчных протоков. Как и другие аутоиммунные заболевания, первичный билиарный цирроз ассоциируется с внепеченочными аутоиммунными синдромами - тиреоидитом, коллагеновыми болезнями, гломерулонефритом, язвенным колитом. Клинически первичный билиарный цирроз проявляется гепатос-пленомегалей, астеническим синдромом, кожным зудом, позднее желтухой, гиперпигментацией кожных покровов с ксантелазмами и ксантомами.
Первичный склерозирующий холангит - хроническое холестатическое заболевание печени предположительно аутоиммунной природы, характеризующееся воспалением и фиброзом внутри- и внепеченочных желчных протоков. Поражение желчных протоков является необратимым и приводит к выраженному холестазу, формированию цирроза печени и развитию печеночной недостаточности. Первичный склерозирующий холангит может осложняться бактериальным холангитом, стриктурами желчных ходов, желчно-каменной болезнью, высок риск развития холангиокарциномы. Клинически первичный склерозирующий холангит характеризуется астено-вегетативными проявлениями, кожный зудом, желтухой. Первичный склерозирующий холангит более чем у 75% больных сочетается с воспалительными заболеваниями кишечника: язвенным колитом или болезнью Крона.
Резюме. Практические рекомендации для врачей, медицинских сестер и пациентов
Терапия при первичном билиарном холангите включает урсодезоксихолевую кислоту и обетихолевую кислоту наряду с экспериментальными и ранее одобренными фармацевтическими средствами. Лечение ориентировано на применении урсодезоксихолевой кислоты и стратификации риска на основе исходных и терапевтических факторов, включая ответ на лечение. При непереносимости урсодезоксихолевой кислоты или высоком риске заболевания, о чем свидетельствует неэффективность лечения с применением урсодезоксихолевой кислоты (обычно проявляющаяся повышением уровня щелочной фосфатазы >1,67 × верхнюю границу нормы и/или повышением концентрации билирубина в крови), возможна терапия второй линии, включающая обетихолевую кислоту.
Характеристиками первичного билиарного холангита являются устойчивое повышение (продолжительностью более 6 мес) уровня щелочной фосфатазы в сыворотке крови, довольно часто наличие гранулематозного воспаления портальных трактов, сопутствующим лимфоцитарно опосредованным повреждением (и деструкцией) мелких внутрипеченочных желчных протоков, холестазом и типичным набором сывороточных и секреторных аутоантител. У большинства пациентов описанное состояние прогрессирует с развитием билиарного фиброза и, в конечном счете — цирроза. Скорость цирротических изменений вариабельна и поддается модификации путем применения урсодезоксихолевой кислоты.
Первичный билиарный холангит соответствует критериям редких заболеваний (распространенность менее 50 на 100 тыс. населения) во всех изученных популяциях. Осведомленность об этой патологии коррелирует с распространенностью, показатель которой обычно стабилизируется после нескольких лет роста. Заболеваемость характеризуется асимметричностью с более высокими показателями среди женщин (в 10 раз выше, чем среди мужчин). Первичный билиарный холангит чаще наблюдается у пациентов пожилого возраста (средний возраст выявления заболевания — 65 лет). Самый молодой пациент с зарегистрированным первичным билиарным холангитом — девочка в возрасте 15 лет. Существуют потенциально важные различия в клиническом проявлении первичного билиарного холангита между мужчинами и женщинами и между пациентами пожилого и более молодого возраста, хотя базовый подход к управлению одинаков во всех демографических группах. Семейная история первичного билиарного холангита характерна для прочих аутоиммунных процессов. Более половины пациентов имеют еще одно аутоиммунное состояние (целиакию, склеродермию, заболевание щитовидной железы, синдром Шегрена и др.), что отражает общую генетическую предрасположенность.
Первичный билиарный холангит этиологически является иммуноопосредованным повреждением билиарных путей в результате взаимодействия иммуногенетических и экологических триггеров с наличием точек кластеризации болезни. Подтвержденными факторами риска являются курение и рецидивирующие инфекции мочевыводящих путей. Холестаз и/или зуд в период предыдущей беременности также связан с повышением риска развития первичного билиарного холангита. Необходимо документировать рецидивирующие инфекции мочевыводящих путей и связанные с беременностью холестазы, а также рекомендовать прекращение курения, учитывая его прямую взаимосвязь с прогрессированием заболевания.
Диагностическая точность сочетания холестатических сывороточных тестов и специфических серологических маркеров достигает >95% по своей чувствительности и специфичности, поэтому анализ крови лежит в основе диагностики первичного билиарного холангита. Подозрение на первичный билиарный холангит справедливо по отношению к пациентам с иначе необъяснимым повторным повышением щелочной фосфатазы в сыворотке крови, а также гамма-глутамилтрансферазы.
Во всех подобных случаях следует проверять наличие аутоантител с помощью теста ELISA в соответствии с местной практикой, что является достаточным для подтверждения диагноза у большинства пациентов без применения биопсии. При подозрении на альтернативное аутоиммунное заболевание тест ELISA может обладать большей чувствительностью и менее подвержен неспецифичной реактивности, возникающей в результате высокого титра поликлональных иммуноглобулинов IgM, наблюдаемого при первичном билиарном холангите. Наличие специфических антинуклеарных или антицентромерных антител чаще всего бывает достаточным для диагностики серонегативного первичного билиарного холангита, однако достоверно о наличии серонегативного заболевания можно судить лишь при наличии материалов биопсии.
Учитывая доброкачественный прогноз при наличии антимитохондриальных антител и нормальных результатов печеночных проб, для таких пациентов не рекомендуется ни биопсия, ни применение урсодезоксихолевой кислоты. Однако рекомендуется ежегодно на первичном медико-санитарном уровне проводить повторные печеночные пробы.
Нет никаких доказательств того, что концентрация антимитохондриальных антител, превышающая диагностический порог, имеет какое-либо прогностическое значение. Поэтому после установления четкого диагноза повторное измерение не рекомендуется. Кроме того, титр аутоантител может снижаться под влиянием урсодезоксихолевой кислоты. Иммунофлуоресцентный метод, также используемый для диагностики первичного билиарного холангита, позволяет выявить тонкие вариации специфичности аутоантител.
Роль визуализации в диагностике первичного билиарного холангита в значительной степени исключает альтернативные диагнозы. Для большинства пациентов достаточно скрининга ультразвуковой визуализации. Особое внимание уделяется исключению первичного склерозирующего холангита и похожих на него заболеваний у пациентов с серонегативным холангитом при помощи магнитно-резонансной холангиопанкреатографии. Наличие желчных камней у пациентов с первичным билиарным холангитом довольно часто является потенциальной причиной задержки диагностики. На терминальной стадии первичного билиарного холангита визуализация цирротических осложнений выполняется так же, как при циррозе печени любой другой этиологии.
Адекватность любой биопсии обусловлена клинической задачей, но в целом биопсийный материал печени должен иметь достаточный объем для визуализации паренхимы и количества портальных трактов (предлагается более 11). Картина первичного билиарного холангита включает деструктивный гранулематозный лимфоцитарный холангит, ведущий к прогрессирующей потере желчных протоков, а также хроническому холестазу, фиброзу и циррозу. Другие видимые особенности включают лимфоцитарную активность, паренхиматозное некротизирующее воспаление и узловатую регенеративную гиперплазию. Точные критерии прогностической биопсии печени при первичном билиарном холангите еще предстоит установить, равно как и роль конкретных систем оценки.
Биопсия периферических лимфатических узлов, увеличение которых довольно часто отмечают при первичном билиарном холангите (и вообще при заболеваниях печени), обычно выявляет наличие реактивно-воспалительных изменений, которые предположительно являются частью основного патологического процесса.
Определение диагноза первичного билиарного холангита обычно вызывает небольшую путаницу из-за специфичности и чувствительности аутоантител. Следует проявлять осторожность при серонегативном типе холангита, для которого основным дифференцируемым заболеванием является первичный склерозирующий холангит. Другие возможные диагнозы включают саркоидоз, болезнь трансплантата против хозяина, идиопатическое нарушение кровообращения, вызванное лекарственным повреждением печени, и варианты генетических холестатических синдромов. Также следует осторожно интерпретировать низкий титр антимитохондриальных антител из-за возможности ложной позитивности аутоантител при воспалительных состояниях, в частности неалкогольной жировой болезни печени.
Первичный билиарный холангит в основном ассоциирован с другими аутоиммунными состояниями, отражающими общую иммуногенетическую восприимчивость (наиболее сильная ассоциация с синдромом Шегрена). У пациентов с выраженной слабостью следует учитывать наличие заболеваний щитовидной железы (присутствует у 25% пациентов) или анемии с иммунной/аутоиммунной этиологией (включая пернициозную анемию, аутоиммунную гемолитическую анемию и целиакию).
Остеопороз также часто отмечают при первичном билиарном холангите, хотя его правильнее рассматривать в качестве осложнения метаболических изменений, наблюдаемых при холестазе, включая снижение абсорбции жирорастворимых витаминов.
До сих пор не установлено, связаны ли повторные инфекции мочевыводящих путей при первичном билиарном холангите с основным заболеванием или агрессивное лечение инфекции мочевыводящих путей оказывает влияние на естественную историю первичного билиарного холангита. Однако рецидивирующие инфекции мочевыводящих путей являются потенциальной причиной снижения качества жизни.
Наличие у пациента антимитохондриальных или специфических антиядерных антител в титре 1:40 или выше (при соответствующих признаках холестаза по биохимическим показателям и отсутствии альтернативного объяснения) обычно является достаточным основанием для установления диагноза первичного билиарного холангита (сильные рекомендации с высоким уровнем доказательности).
Все пациенты с первичным билиарным холангитом нуждаются в пожизненном наблюдении, причем различное течение болезни у разных пациентов может потребовать различной интенсивности наблюдения (сильные рекомендации, умеренный уровень доказательности).
Оценка риска должна учитывать тяжесть заболевания и его активность в начальном и последующих этапах, молодой возраст наступления болезни (младше 45 лет) и мужской пол. При этом рекомендуется комплексное исследование: печеночные пробы, ультразвуковая визуализация для выявления открытого цирроза и спленомегалии, переходная эластография (сильная рекомендация, умеренный уровень доказательности).
Выявление пациентов с наибольшим риском прогрессирования заболевания осуществляется на основании показателей биохимического анализа после одного года терапии с применением урсодезоксихолевой кислоты (сильная рекомендация, высокий уровень доказательности).
Предполагается, что если пациенты при лечении урсодезоксихолевой кислотой имеют уровень щелочной фосфатазы в крови >1,67 × верхнюю границу нормы и/или повышенную концентрацию билирубина 1,67 × верхнюю границу нормы и/или концентрацией билирубина в сыворотке крови 1,67 × верхнюю границу нормы и/или содержанием билирубина 50 мкмоль/л (включая тех, которые принимали урсодезоксихолевую кислоту), или доказательством декомпенсированного заболевания печени, необходимо рассмотреть вопрос о трансплантации печени (сильная рекомендация, высокий уровень доказательности).
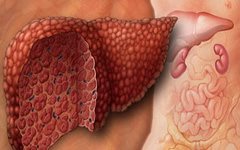
Избыточное образование фиброзной ткани нарушает структуру печени и в конечном счете приводит к циррозу.
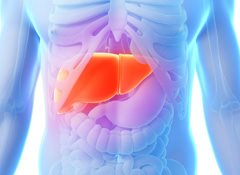
Фиброзная ткань образуется вследствие воспалительных процессов в печени.
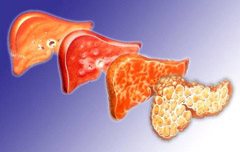
Развитие цирроза может долгое время протекать бессимптомно.
Сочетание глицирризиновой кислоты и эссенциальных фосфолипидов способствует устранению воспаления печени и уменьшению степени фиброза.

- оптимальный состав активных компонентов;
- достоверное уменьшение воспаления в печени и степени фиброза;
- благоприятный профиль безопасности.
Использование гепатопротекторов, обладающих фиксированной доступной ценой, — возможность не переплачивать в процессе лечения.
Цирроз печени — это серьезное заболевание, требующее тяжелого и длительного лечения. Однако, причинами данной патологии могут быть совершенно разные факторы, многие из которых поддаются если не лечению, то контролю. В данной статье мы подробно разберем причины возникновения цирроза печени и методы его профилактики.
Характеристика заболевания и стадии развития цирроза печени
Это поражение является конечной стадией различных хронических заболеваний печени. Данный диагноз ставится, когда патологические изменения в клетках органа (гепатоцитах) становятся необратимыми. При циррозе гепатоциты погибают вследствие воспалительного процесса, а на их месте образуется фиброзная (соединительная) ткань. В целом данный процесс можно назвать иммуновоспалительным. В результате структура печени серьезно нарушается.
Разрушение гепатоцитов — крайне опасный процесс, так как данные клетки выполняют множество важных функций: они участвуют в обменных процессах и секреторной деятельности (выделение желчи и переработанных веществ в кишечник), обезвреживают токсины и другие вредные вещества. В результате печень перестает выполнять свои функции в полной мере: вредные вещества попадают в кровеносную систему, вызывая интоксикацию организма.
Гепатоциты — клетки паренхимы печени (печеночной ткани), на основе которых формируются печеночные дольки — структурно-функциональные единицы печени.
В развитых странах цирроз печени входит в шестерку основных причин смерти пациентов от 35 до 60 лет. Во всем мире от него ежегодно умирают 40 миллионов человек, в Европе — порядка 170 тысяч. За последнее десятилетие количество смертельных исходов возросло на 12%. В России частота возникновения цирроза печени составляет 20–35 случаев на 100 000 населения. Стоит сказать, что это в первую очередь мужская болезнь. Сильный пол страдает ей в три раза чаще, чем женщины. Данное заболевание обычно развивается после 40 лет.
Цирроз печени имеет стадийное течение. Каждая стадия отличается степенью патологических изменений, симптомами и необходимым лечением. Для определения стадии используется специально разработанная для этого шкала по Чайлд-Пью. Для верной оценки требуется сдать некоторые анализы, а также учесть клинические проявления заболевания на текущий момент времени.
Первая степень практически не имеет симптомов, так как болезнь компенсирована. Анализы крови характеризуются снижением уровня билирубина, а также уменьшением протромбинового индекса до 60–80 единиц. При этом воспалительные процессы уже начались и погибшие гепатоциты замещаются соединительной тканью.
На второй стадии заболевания начинают появляться первые неспецифичные симптомы: слабость, апатия, головные боли, тошнота и поносы, слабый аппетит, дискомфорт в правом подреберье, кровотечения из носа и кровоточивость десен. У мужчин возможно облысение и увеличение молочных желез. Начинают проявляться печеночная энцефалопатия и асцит. Данная стадия называется субкомпенсированным циррозом, так как болезнь еще можно вернуть в стадию компенсации.
Печеночная недостаточность — комплекс симптомов, который характеризуется нарушением одной или нескольких функций печени.
Асцит — одно из осложнений цирроза, проявляется скоплением свободной жидкости в брюшной полости.
Далее следует терминальная стадия, на которой энцефалопатия и асцит прогрессируют, кожные покровы обретают желтоватый цвет, наблюдается мышечная атрофия и анемия. Данная стадия опасна развитием серьезных осложнений, которые могут привести к летальному исходу. Среди таких осложнений: печеночная кома, тромбоз воротной вены, рак печени, внутренние кровотечения, а также инфекционные осложнения.
Как можно узнать о состоянии печени? Раньше для этого требовалось проведение биопсии, однако сейчас оценка возможна с помощью специального комплекса расчетных тестов, в которых используются результаты исследований крови и минимальные анамнестические данные, однако золотым стандартом остается биопсия. Специально разработанные алгоритмы определяют стадию фиброза (F0, F1, F2, F3, F4) и степень некровоспалительного процесса (А0, А1, А2, А3) по международной общепринятой системе METAVIR. Данная шкала включает в себя анализ 6 показателей: возраст, индекс массы тела, гипергликемия, количество тромбоцитов, уровень альбумина, отношение ферментов аспартатаминотрансферазы и аланинаминотрансферазы.
В зависимости от степени цирроза печени можно спрогнозировать продолжительность жизни пациента. В среднем более 7 лет живут около половины всех заболевших. При компенсированной стадии цирроза не менее 50% пациентов живут 7–10 лет. Субкомпенсированная стадия дает показатель пятилетней выживаемости около 40%. На стадии декомпенсации около 3 лет живут 10–40% пациентов.
Цирроз может быть вызван разными причинами, а самая распространенная из них — вирусы гепатита. Наиболее опасным для печени является гепатит С, так как он приводит к развитию цирроза в 97% случаев. Алкогольная форма развивается в результате неконтролируемого употребления спиртных напитков. Лекарственный тип возникает из-за длительного употребления гепатотоксических препаратов. Врожденная форма цирроза — результат некоторых генетических патологий (гемохроматоз, тирозиноз, галактоземия и др.). При недостаточном кровообращении и длительном венозном застое в печени диагностируется застойная форма заболевания. Обменно-алиментарный цирроз развивается в результате метаболических нарушений. Вторичный билиарный цирроз — следствие нарушения оттока желчи (болезнь развивается через 3–18 месяцев после нарушения проходимости желчных протоков). Если причина болезни не выяснена, такой цирроз называется криптогенным. Первичный билиарный цирроз также относится к категории заболевания неясной этиологии.
Как уже упоминалось, симптомы цирроза печени зависят от стадии заболевания. Основными из них, независимо от этиологии, являются: пониженная трудоспособность, неприятные ощущения в животе, повышенная температура тела, боли в суставах. При осмотре выявляется умеренное увеличение селезенки, увеличение и уплотнение печени, деформация ее поверхности. На более серьезных стадиях наблюдается вздутие живота, тошнота и рвота, возможна диарея при употреблении жирной пищи, тяжесть и боль в правом подреберье. На терминальной стадии могут возникать желтуха, асцит, отеки ног, варикозное расширение вен пищевода. В некоторых случаях развивается геморрой. При обнаружении тех или иных заболеваний печени необходимо обращаться к врачу гастроэнтерологу-гепатологу.
Лечение цирроза — процесс длительный, и он представляет собой не столько лечение, сколько вторичную профилактику. При этом назначается специальная диета, гепатопротекторные препараты и комплекс витаминов, исключается прием гепатотоксических лекарственных средств, алкоголя. В целом сформировавшийся цирроз печени является необратимым состоянием и считается неизлечимым. Этиотропная терапия для большинства форм цирроза печени на данный момент отсутствует, исключением является вирусный гепатит, при котором могут назначаться противовирусные препараты.
При заболеваниях печени пациентам, как правило, назначают так называемую диету № 5, направленную на нормализацию функций органа и улучшение желчеотделения. Пищу необходимо принимать небольшими порциями 5–6 раз в день, при этом следует полностью исключить жареное и жирное. Предпочтение следует отдать вареной и приготовленной на пару пище. Обязательно употреблять достаточное количество воды — не менее 1,5 литров в день. Следует полностью отказаться от алкоголя. Количество белков ограничивается сотней граммов в день, соли —10-ю граммами в день. При асците назначают бессолевую диету.
Продукты, запрещенные к употреблению:
- любые химические пищевые добавки, в том числе консервы;
- жареное, соленое, маринованное, копченое;
- кондитерские изделия, шоколад, мороженое;
- животные жиры, маргарин, жирные мясо и мясные бульоны;
- соленые сыры, молочные продукты с высокой жирностью;
- бобовые, редька, шпинат, редис, щавель, чеснок, лук;
- кислые фрукты и ягоды;
- сладкие газированные напитки, крепкий чай и кофе.
Наиболее популярны при лечении заболеваний печени такие гомеопатические средства, как:
- Phosphor 6, 12;
- Magnesia Muriatica 6;
- Lycopodium 6;
- Nux Vomica 6;
- Mercur dulcis 6 и др.
Кроме того, в гомеопатических препаратах можно встретить вытяжки из майского чистотела Chelidonium majus. Действительно, взятые за основу растения известны как народные средства для восстановления печени. Однако не стоит забывать, что гомеопатия как таковая официальной доказательной медициной не признана, и ее методы не проходят серьезных клинических испытаний. До сих пор не существует веских доказательств того, что она действует за счет заявленных полезных компонентов, а не за счет эффекта плацебо. Далеко не все пациенты гомеопатов отмечают улучшение своего самочувствия. В любом случае, гомеопатическое лечение печени — процесс длительный, занимающий не один месяц. Распад гепатоцитов и рост фиброзной ткани могут развиваться быстрее. Если говорить о циррозе печени, то у больного просто нет времени на рискованное лечение.
При компенсированном и субкомпенсированном циррозе назначается поддерживающая терапия – строгая диета и гепатопротекторы (лекарства на основе глицирризиновой кислоты, фосфолипидов, аминокислот, расторопши (Silybum marianum Carduus marianus) и других компонентов, способствующих восстановлению функций печени). При вирусном циррозе используется противовирусная терапия (ПВТ). Однако, справедливо заметить, что специфического лечения цирроза нет.
Глицирризиновая кислота — это биологически активное вещество, которое в природе встречается в корне солодки (Glycyrrhiza glabra), по имени этого растения оно и получило свое название. Однако гепатопротекторные функции глицирризиновой кислоты были изучены не так давно, поэтому до сих пор ее можно встретить далеко не в каждом лекарственном препарате против заболеваний печени. Особенно эффективен комплекс глицирризиновой кислоты и фосфатидилхолина — многочисленные клинические исследования показали его противовоспалительное, гепатопротекторное и антифибротическое действие.
На декомпенсированной стадии цирроза медикаментозная терапия мало эффективна и необходимо ставить вопрос о трансплантации (пересадке) печени. , Таким образом, лечение цирроза – крайне непростая задача, поэтому лучше его предотвратить. С этой целью при заболевании печени невирусной природы или вирусном гепатите и недоступной ПВТ, врачи могут назначить российский препарат на основе глицирризиновой кислоты, который приемлем по цене и почти не имеет противопоказаний (за исключением стандартных: аллергических реакций на компонент, беременности и периода лактации). Компоненты препарата защищают печеночные клетки от повреждения, уменьшают воспаление, разрастание соединительной ткани и способствуют восстановлению органа.
Если вышеуказанные методы лечения не помогают, проводят трансплантацию (пересадку) печени. Хирургическое вмешательство необходимо на последней, декомпенсированной, стадии заболевания, когда печень уже не выполняет своих функций. Кроме того, часть печени может быть взята у родственника больного или другого человека, который выразил свое согласие на эту операцию.
К числу профилактических мероприятий можно отнести любые процедуры по предупреждению заражения гепатитом, который является частой причиной цирроза печени. Рекомендуется вести здоровый образ жизни, отказаться от алкоголя и соблюдать сбалансированную диету, не увлекаться жареными и жирными продуктами. Следует с осторожностью относиться к чрезмерному приему лекарственных средств, многие из которых являются токсичными для печени. Стоит также позаботиться о нивелировании неблагоприятных экологических условий окружающей среды, которые могут оказывать негативное влияние на клетки печени — больше отдыхайте на свежем воздухе.
Один из эффективных методов предупреждения цирроза — прием гепатопротекторных препаратов при заболеваниях печени. Они защищают клетки печени, восстанавливают их структуру, уменьшают степень воспаления, нормализуют белковый и липидный обмены, приостанавливают развитие фиброза. Так, глицирризиновая кислота обладает антиоксидантной и мембраностабилизирующей активностью, потенцирует действие эндогенных глюкокортикостероидов, оказывая противовоспалительное действие при неинфекционных поражениях печени. Положительный эффект данного соединения был доказан в ходе 54 клинических исследований, из них 31 — рандомизированное. Испытания проводились на разных категориях пациентов, в том числе больных гепатитом и алкогольной болезнью печени. Во всех этих исследованиях профиль безопасности глицирризиновой кислоты был оценен как благоприятный, что позволило включить ее в рекомендации Азиатско-Тихоокеанской ассоциации по изучению печени (APASL) и разрешить для медицинского применения человеком Европейским медицинским агентством (EMA).
Итак, прием современных гепатопротекторов — надежный и безопасный способ улучшить клиническую картину болезни печени, однако любое самолечение недопустимо, и, несмотря на то, что многие лекарственные препараты допущены к продаже без рецепта, обязательно проконсультируйтесь с врачом.

Цирроз печени — тяжелое заболевание, негативно влияющее на работу всего организма, требующее длительного и сложного лечения. Поэтому, если у вас выявлено то или иное заболевание печени, необходимо сделать все возможное, чтобы затормозить патологические процессы и максимально восстановить функции печени. Многое зависит от вас. Начните с самодисциплины, взяв под тотальный контроль ваше питание, распорядок дня и прием лекарств, назначенных врачом — уже только это способно значительно улучшить прогноз.
Читайте также:


