Avxs-101 вирус вектор что нового
Компания Новартис сообщила о планах регистрации в России препарата Золгенсма для лечения СМА

Компания Новартис также поясняет, что в настоящий момент говорить о точных сроках получения регистрационного удостоверения пока преждевременно.
Также Новартис сообщает о том, что в настоящее время компанией ведутся переговоры с медицинскими центрами на территории России для улучшения доступа к терапии путем ввоза препарата до его регистрации по жизненным показаниям.
О препарате: AVXS-101 (onasemnogene abeparvovec-xioi, Zolgensma®) является препаратом генной терапии, разработанным для лечения больных проксимальной спинальной мышечной атрофией, вызванной нарушением в гене SMN1. AVXS-101 доставляет синтетическую функциональную копию гена SMN1 в клетки двигательных нейронов, используя адено-ассоциированный вирус-вектор 9 серотипа (scAAV9). Препарат AVXS-101 изучался в трех программах клинических исследований на нескольких десятках больных СМА 1 и показал многообещающую эффективность и безопасность. На основании полученных данных препарат был одобрен Американским регулирующим органом (FDA) 24 мая 2019 года для применения у больных со СМА возрастом до 2 лет. В настоящее время ожидается решение Европейского регулятора в области обращения лекарственных средств и регуляторные рассмотрения в других странах.
Компания в своем письме подчеркивает, что понимает срочность получения терапии нуждающимися пациентами и заверяет, что регистрация и доступ к терапии являются приоритетами для компании Новартис.
Источники:
Данный материал носит исключительно информационный характер и не может служить рекламой. Рекомендации относительно индивидуального применения любого лекарственного препарата следует получать у вашего лечащего врача.
Объявлено о временной приостановке исследований интратекального применения AVXS-101
- FDA частично приостановило интратекальные клинические испытания AVXS-101 для пациентов со СМА на основании результатов небольшого доклинического исследования на животных
- При тщательном анализе данных о безопасности для человека из всех доступных на сегодняшний день источников, неблагоприятные события, которые можно ожидать от доклинических результатов, не были замечены
- Новые данные не влияют на уже одобренное внутривенное применение Zolgensma® (onasemnogeneabeparvovec-xioi), также известного как AVXS-101: внутривенное введение остается доступным в США.
- Novartis\Avexisработает с FDA, чтобы определить следующие шаги для решения вопросов возобновлению дозирования в интратекальных испытаниях AVXS-101.
30 октября 2019 года компания Novartis\Avexis объявила, что Управление по контролю за продуктами и лекарствами США (FDA) частично приостановило клинические испытания для интратекального введения препарата AVXS-101. Это решение последовало после сообщения AveXis для органов здравоохранения о результатах небольшого доклинического исследования, инициированного AveXis, в котором у животных были обнаружены воспаления мононуклеарных клеток дорсальных корешковых ганглиев (DRG), иногда сопровождающиеся дегенерацией нервных клеток или их потерей.
Это частичное ограничение от FDA не влияет на ранее одобренное регулятором внутривенное введение Zolgensma® (или AVXS-101) для пациентов возрастом до 2 лет.
AveXis в настоящее время изучает интратекальное введение AVXS-101 у пациентов со вторым типом спинальной мышечной атрофии в своем исследовании STRONG (многоцентрового исследования с контролем дозировки, предназначенного для оценки эффективности, безопасности и переносимости однократного интратекального введения AVXS-101).
Введенное ограничение влияет на набор пациентов в когорту высокой дозировки исследования STRONG. Набор пациентов в когорту, получающих низкие и средние дозировки препарата, был ранее завершен, и уже были представлены промежуточные результаты.
Клиническое значение воспаления DRG, наблюдаемого в указанном доклиническом исследовании на животных, неизвестно и не наблюдалось в предыдущих исследованиях на животных с AVXS-101. Воспаление DRG может быть связано с сенсорными эффектами.
В настоящее время AveXis и Novartis по-прежнему продолжают исследование и разработку генной терапии для спинальной мышечной атрофии, редкого и разрушительного генетического заболевания. Мы будем продолжать следить за последними новостями и сообщать вам по мере появления новой информации.
Данный материал носит исключительно информационный характер и не может служить рекламой препарата. Рекомендации относительно индивидуального применения лекарственного препарата следует получать у вашего лечащего врача.
Авексис поделился планами о дальнейшей регистрации Золгенсма

- Пациент болен тяжелым, угрожающим жизни заболеванием или находится в состоянии, и не доступно никакое другое альтернативное лечение, либо все альтернативные методы лечения заболевания или состояния пациента уже исчерпаны.
- Пациент не имеет возможности доступа к действующим клиническим исследованиям AveXis.
- Существует достаточно оснований полагать, что потенциальная польза от лечения препаратом выше потенциального риска заболевания или состояния больного.
- AveXis имеет достаточное количество препарата, и предоставление препарата не нарушит действующие клинические исследования и программы разработки препарата.
- Пациент отвечает другим важным медицинским критериям, установленными медицинскими экспертам, работающими над программой развития продукта.
- Пациент младше двух лет, а также соответствует следующим критериям:
◦Подтвержденный ДНК-диагноз СМА — анализе мутации гена SMN1 (делеция или точечная мутация).
◦Вес: ≥ 2.6 кг на момент дозирования
◦Anti Adeno Associated Virus Serotype 9 (AAV9) титр антител
Инструкция к препарату Золгенсма

Как мы сообщали ранее, 24 мая 2019 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило ZOLGENSMA® (оназемноген abeparvovec-xioi) (производитель — AveXis Inc. [группа Новартис])— первый препарат для генной терапии спинальной мышечной атрофии (СМА) у детей младше 2 лет.
Мы понимаем, что в настоящее время у медицинских специалистов и семей со СМА возникает большое количество вопросов о препарате и его применению.
Поэтому подготовили в целях информирования русскоязычный перевод американской инструкции к препарату Золгенсма.
ОБРАТИТЕ ВНИМАНИЕ! Данный материал и перевод инструкции не является официальным источником информации и не одобрен регуляторными органами, не может использоваться для применения Золгенсма где-либо и служит только ознакомительным целям для тех, кто не может ознакомиться и инструкцией на английском языке.
- 24756
- 8,9
- 8
- 3



Спонсором приза зрительских симпатий выступила компания BioVitrum.
Что такое СМА?
Спинально-мышечной атрофией, или СМА, называют смертельно опасное нейродегенеративное заболевание, в процессе развития которого у пациента происходит постепенная атрофия скелетной мускулатуры. В результате человек теряет или так и не приобретает способности ходить, самостоятельно стоять, сидеть без поддержки. Со временем возникает сколиоз и другие ортопедические проблемы. Также СМА-пациенты, если они не получают должного ухода и лечения, постепенно утрачивают способность самостоятельно дышать, глотать, кашлять. Пациенты с первым, самым тяжелым, типом СМА еще несколько лет назад, как правило, не доживали и до двух лет [1].
СМА возникает из-за потери участка хромосомы или точечной мутации гена SMN1, расположенного в пятой хромосоме. В результате этого нарушается синтез SMN-белка, недостаток которого приводит к гибели моторных нейронов и атрофии скелетной мускулатуры [2].
Для того чтобы болезнь проявилась, носителем рецессивной мутации в гене SMN1 должны быть оба родителя. Примерно каждый 40-й житель Земли является таким носителем.
До недавнего времени методы лечения СМА сводились к поддерживающей терапии. Больным рекомендовали специальное питание, витамины, умеренные физические нагрузки, при необходимости — хирургическое вмешательство, искусственная вентиляция легких. К сожалению, до сих пор значительная часть СМА-пациентов получает лишь такое лечение.

Стоимость препарата составляет несколько сот тысяч долларов в год, поэтому его закупка осуществляется не за счет пациента. Одна за другой страны разных континентов одобрили препарат и стали применять для спасения жизней своих сограждан. В некоторых государствах этот процесс сильно затянулся из-за бюрократических проволочек и нехватки финансирования.
Происходит это следующим образом: препарат содержит функционально полноценный ген SMN1, который находится внутри вектора. Задача вектора — быстро доставить его в мотонейроны тела (рис. 3).
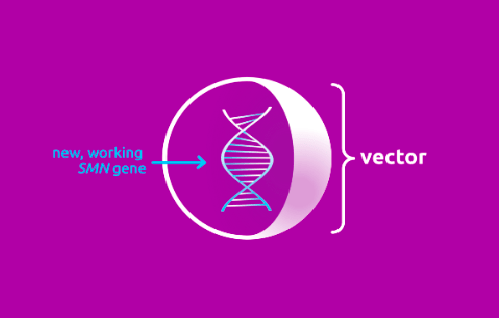
Для создания вектора использовали аденоассоциированный вирус (adeno-associative virus 9, или AAV9). Это представитель семейства парвовирусов, который способен инфицировать клетки человека и других приматов, но при этом не является патогенным. Все это делает AAV9 отличным генетическим вектором. Собственный генетический материал вируса удалили и вместо него поместили функционально полноценный ген SMN1 (рис. 4).
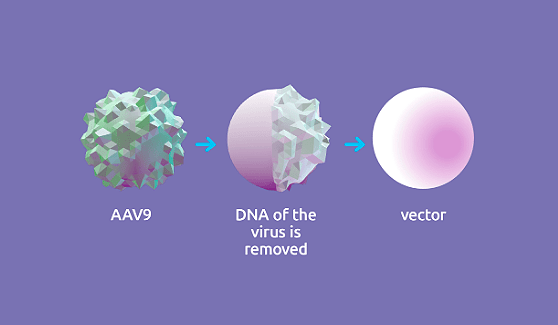
Рисунок 4. Условная схема механизма создания вектора
После того, как ген прибывает в нужную локацию, вектор разрушается и выводится из организма.
- рвота;
- повышение уровня аминотрансфераз;
- тромбоцитопения;
- нарушение функций печени, вплоть до острого тяжелого поражения.
Следующий шаг

Рисунок 5. Рисдиплам — препарат для лечения спинально-мышечной атрофии, который находится на стадии клинических испытаний на людях
Уже в конце 2019 года компания Roche планирует подать документы на одобрение препарата в FDA и EMA (Европейское медицинское агентство) [13].
Почему карантин не может сдержать пандемию, а российские власти — не очень-то и хотят
Фото: РИА Новости

Судя по всему, эпидемию коронавируса в России не будут — не считая косметических мер — сдерживать. Коронавирус убивает стариков и больных, а не молодых и здоровых.
Cтарики и больные вымрут по максимально жесткому варианту, и в стране быстро сформируется иммунная прослойка с минимальными для экономики потерями. Кстати, с точки зрения экономики это — совершенно правильная стратегия.
Читайте также

Но, конечно, одной из основных ее примет является феерическая история с монополией на тесты на коронавирус.
Что такое тестирование и почему оно необходимо?
Возьмем историю Во. Во — небольшой городишко на севере Италии. И 21 февраля там умер первый в Италии человек, ставший жертвой коронавируса. После чего мэр запер город и протестировал все 3300 его жителей. Выяснилось, что 3% жителей уже заражены, причем половина от зараженных не имела никаких симптомов. Зараженных изолировали. И болезнь в Во сошла на нет.
Первая — хорошая — новость из Во заключалась в том, что тотальное тестирование сократило летальность коронавируса до 1%. Это в 10 раз больше, чем у обычного гриппа, но намного меньше, чем 3,4% летальности COVID-19, о которых в настоящий момент говорит глава ВОЗ.
Вторая — плохая — новость заключается в том, что пандемию невозможно остановить без всеобщего тестирования, потому что нельзя иначе установить инфицированных людей без симптомов. В этом особенность нынешней пандемии —
ее трудно остановить не потому, что она тяжелая, а ровно потому что она легкая по форме протекания у большинства больных.
Кейс города Во диаметрально противоположен кейсу круизного лайнера Diamond Princess. Японские власти держали в карантине всех, тестировали только тех, кто уже заболел. Перезаразились несколько сот человек. В конце концов на судне начали тестировать всех подряд, больных и здоровых, и в результате сейчас ученые оценили летальность вируса на Diamond (с учетом поправки на возраст) в 1,2%, — цифра, почти идентичная выборке в Во.
Читайте также

Ровно это же мы видим в Южной Корее. Там тестируют по 10 тысяч человек в день, и летальность там низкая. Напротив, в Италии тестов долго не хватало. И летальность там чудовищная: в Ломбардии она на порядок (!) выше, чем в Во.
По какому пути идут США? По пути Во.
Штат Теннеси с населением в 6,7 млн на прошлой неделе получил 500 000 тестов. Дональд Трамп обещал нации, что в течение месяца частные компании обеспечат американцев не меньше, чем 5 миллионами тестов. FDA на прошлой неделе срочно одобрило тесты, разработанные компанией Roche, — они позволяют получать результаты через четыре часа.
Еще 17 января ВОЗ опубликовала открытый протокол, позволяющий любой компании начать производство тестов. Сотни частных компаний и научных учреждений бросились конкурировать друг с другом.
Не так в России.
Понятно, что такая ситуация не позволяет контролировать эпидемию. Зато она позволяет отрицать ее существование.
Нету тестов — нет и диагнозов. Нет диагнозов — нет и эпидемии.
Читайте также

Россия, несомненно, получила хорошую фору, рано закрыв границы с Китаем, и эпидемия у нас развивается с заметным отставанием от Европы. Но царского пути не бывает — ни в геометрии, ни в биологии, и когда нам сообщают, что в России за сутки выявлено 52 новых больных в 23 регионах, мы должны понимать, что этого не может быть.
Это значит, что больным считают не того, кто болен, а того, кого выявили.
В ближайшее время нам предстоит столкнуться с эпидемией, которую мы переживем, как наркоманы у Ройзмана, — всухую. С переполненными больницами, с хрипящими стариками, с ИВЛ, которых не хватает.
А теперь вопрос: с чего вы взяли, что для власти, которая только что обесценила рубль и обесценила этим пенсии, коронавирус — это беда?
Это просто дальнейшее уменьшение социальных обязательств. Кто умирает-то? Больные и пенсионеры.
Вам кажется, что плохо, что турфирмы разорятся? Так и хорошо. Нечего за границу ездить, ездите в Крым.
Еще раз — для власти, которая не ценит человеческую жизнь и не зависит от избирателя, эпидемия коронавируса не представляет никакой опасности. И с точки зрения экономики — как это ни чудовищно звучит — это оправдано.
Наши власти готовы грохнуть экономику ради своих представлений о мировом порядке, но не готовы грохать ее ради жизни своих граждан.
На этом фоне спасение утопающих — дело рук самих утопающих. Когда вам говорят — самоизолируйтесь — самоизолируйтесь. Носите маски, протирайте руки. Помните, что в России иммунная прослойка действительно сформируется быстро. От вас зависит, вы будете лежать в ее основании или будете ее бенефициарами.
В конце концов, могло быть хуже. Могли всех закрыть в больницу, похожую на концлагерь, где все бы заболели наверняка, — чтобы кормить там за бюджетный счет завтраками Пригожина.
Почему это важно
Читайте также:


