Возбудители туберкулеза и дифтерии имеют форму
Роберт Кох — немецкий микробиолог, один из основоположников современной бактериологии и эпидемиологии. Впервые выделил чистую культуру возбудителя сибирской язвы, доказал ее способность к спорообразованию. Предложил способы дезинфекции. Сформулировал критерии этиологической связи инфекционного заболевания с микроорганизмом (триада Коха).
Роберт Кох родился 11 декабря 1843 года в крохотном немецком городке Краустале. В детстве он очень любил ломать, а затем чинить свои игрушки. За этим занятием он проводил долгие часы. Когда он подрос и пошел в гимназию, то, как и положено ребенку его возраста, стал мечтать о далеких странах и великих открытиях. Он хотел стать судовым врачом и проплыть вокруг земного шара. Но по окончании в 1866 году медицинского факультета Геттингенского университета его ждала скромная должность младшего врача в доме умалишенных в Гамбурге. Лечение лишенных разума людей энтузиазма у Коха не вызывало. Казалось, что в перспективе его ждет только скучная рутинная врачебная практика. Он переезжал с места на место и наконец оказался в роли уездного врача в Вольштейне (Восточная Пруссия). Кох быстро завоевал уважение сельских жителей, и врачебная практика стала приносить ему ощутимый доход. В то же время мысли о романтических путешествиях и свершениях Коха не покидали.
Невеста его, девушка милая, простая, согласилась выйти за него замуж при одном условии: никаких джунглей, фрегатов: дом, семья, тихая, всеми уважаемая профессия сельского лекаря. Он смирился. Не смирился его дух. В день 28‑летия Коха Эмми Фраац, его жена, на радостях подарила ему микроскоп. Она и подумать, конечно же, не могла, что этот прибор поможет мужу завоевать мировую славу. Микроскоп, купленный как игрушка, стал вскоре причиной супружеских разногласий. Коху стоило большого труда оторваться от любимого инструмента. Насколько он был теперь увлечен занятиями микробиологией, настолько потерял интерес к врачебной практике. Он не любил врачевать, он любил исследовать.
Опыты Луи Пастера, утверждавшего, что все болезни вызываются бактериями, будоражили воображение молодого доктора. И Кох организовал примитивную домашнюю лабораторию и провел свои первые микробиологические исследования. Он ничего не знал еще о дрожжевом бульоне, придуманном Пастером, и его опыты отличались такой же примитивной оригинальностью, как попытки первого пещерного человека получить огонь. Бесстрашный исследователь невидимого мира убийц мог легко заразиться смертельной болезнью. Предохраняться было нечем: не было ни инструмента, ни индивидуальных средств защиты.
Благодаря микроскопу и красителям Коху открылся удивительный мир невероятно маленьких живых существ — микробов. Пользуясь разработанным им методом культивирования бактерий, открытых ранее в крови больных сибирской язвой, Кох доказал, что они являются возбудителями сибирской язвы и способны к образованию устойчивых спор. Это открытие врача объяснило пути распространения болезни. Когда он разобрался с сибирской язвой, ему и в голову не приходило что-то об этом опубликовать, кому-то доложить. В 1876 году, по настоянию своего профессора Кона, Кох отправился из своего медвежьего угла в Бреславль, чтобы объявить миру о том, что микробы действительно являются причиной болезни. Тогда в это мало кто верил. Собравшиеся светила науки в течение трех дней, затаив дыхание, сидели и слушали никому неизвестного врача. Это была победа! Профессор Конгейм, один из самых талантливых в Европе патологов, не мог больше сдерживаться. Он выскочил из зала как ошпаренный и бросился в лабораторию проверять, прав ли этот безвестный доктор.
Доктор Кох вернулся в Вольштейн, где, начиная с 1878 по 1880 год, добился новых больших успехов, открыв и изучив особый вид маленьких негодников, вызывающих смертельное нагноение ран у людей и животных. В работе, посвященной раневым инфекциям, Кох выдвинул известных три требования (триада Коха), на основании которых можно установить связь заболевания с определенным микробом: 1) обязательное выявление микроба во всех случаях данной болезни; 2) число и распределение микробов должно объяснить все явления болезни; 3) в каждой отдельной инфекции должен быть определен свой возбудитель в виде хорошо морфологически охарактеризованного микроорганизма. Для выполнения этих требований (впоследствии во многом переработанных и измененных) Кох создал ряд новых методов приготовления препаратов, окрашивания и др., которые прочно вошли в медицинскую практику.
Далее Кох горячо взялся за поиски бактерий туберкулёза — болезни, которая уносила, да и сейчас еще уносит, множество человеческих жизней. Начал Кох с микроскопического исследования внутренних органов тридцатишестилетнего рабочего, погибшего от скоротечной чахотки — туберкулёза легких. Но никаких микробов разглядеть не удалось. Вот тогда его и осенило использовать окраску препаратов. Это произошло в 1877 году, который стал историческим для медицины. Сделав мазок легочной ткани больного на предметном стекле, Кох высушил его и поместил в раствор красителя. Рассматривая под микроскопом препарат, окрашенный в синий цвет, он отчетливо увидел между легочной тканью многочисленные тоненькие палочки…
Подобное решение было принято и в Германии. Правительство назначило Коха главой комиссии, которая 24 августа прибыла в Александрию. Местом работы был выбран греческий госпиталь. Еще за год до этого Кох наблюдал в присланной ему из Индии части кишки умершего от холеры большое количество бактерий. Он, однако, не придал этому особого значения, так как в кишках всегда находится множество бактерий.
В 1885—1891 годах Кох был профессором Берлинского университета. С 1891 года он возглавлял Институт инфекционных болезней больницы Шаритэ, а с 1901 года — Институт инфекционных болезней в Берлине, впоследствии названный именем Коха.
В 1904 году Кох отказался от должности директора Института инфекционных болезней, чтобы заняться только исследовательской деятельностью. Через год ему одновременно с Адольфом Байером, выдающимся исследователем красителей, была присуждена Нобелевская премия, а еще через пять лет, 27 мая 1910 года, Роберт Кох умер. Он ушел из жизни так же тихо и скромно, как и жил.
Ученики Коха немало потрудились. Страшная болезнь, дифтерит, уносила каждый день сотни, тысячи детских жизней. Лечили от удушья трахеотомией (вскрытием дыхательного горла). Некоторые бесстрашные врачи, рискуя умереть от смертельного яда, жертвовали собой и высасывали ложные перепонки, находящиеся в только что открытом дыхательном горле. Так погиб врач-писатель М.А. Булгаков. И вот в 1884 году Фридрих Лёфлер (1852—1915) открыл возбудителя дифтерии и описал этиологию дифтерита, что дало возможность Э. Берингу и Э. Ру приготовить антитоксическую сыворотку. Георг Гафки (1850—1918), с 1904 года директор Института инфекционных болезней в Берлине, описал этиологию брюшного тифа, впервые выделил чистые культуры брюшнотифозной палочки и дал в 1884 году подробное ее описание. Особенно заметным был Рихард Пфейфер (Pfeiffer), автор большого числа работ по различным вопросам микробиологии и иммунитета. В 1890 году описал возбудителя инфлюэнцы в мазках, а в 1892 году получил чистую культуру микроба, считавшегося возбудителем гриппа; в 1894 году одновременно с русским врачом В.И. Исаевым открыл и изучил бактериолиз холерных вибрионов; в 1896 году открыл эндотоксины возбудителя брюшного тифа. В объяснении механизма иммунитета пытался противопоставить явления бактериолиза фагоцитозу. Пфейфер внес много нового в изучение малярии, чумы, холеры и других инфекционных болезней.

Философы ничего не прячут, кроме веса и мер, то есть пропорций ингредиентов, что очевидно, поскольку никто из них не согласен в этом с другими, в чем причина великой ошибки.
Сайт СТУДОПЕДИЯ проводит ОПРОС! Прими участие :) - нам важно ваше мнение.
Представители семейства микобактерий имеют вид тонких, иногда ветвистых палочек, чем напоминают мицелий гриба. Медленный рост на питательных средах также сближает их с грибами. Эти особенности объясняют название семейства, рода – Mycobacterium.
Микобактерии кислото-, щёлоче- и спиртоустойчивы, что обусловливается наличием в оболочках их клеток жировосковых веществ.
Род микобактерий включает патогенных и непатогенных представителей. Патогенными для человека являются возбудители туберкулеза и возбудитель лепры (проказы).
Туберкулез широко распространен среди крупных животных, птиц, грызунов.
Существуют несколько видов туберкулезных палочек:
1. Человеческий (М. tuberculosis (лат. – бугорчатка))
2. Бычий (M. bovis)
5. Встречаются микобактерии, вызывающие заболевания у холоднокровных. К ним относится особая группа атипичных микобактерий, некоторые также могут вызывать заболевания у человека.
Морфология. Возбудители туберкулеза были открыты Р. Кохом в 1882г.
§ тонкие палочки, очень полиморфны: встречаются прямые, изогнутые, колбовидные;
§ спор и капсул не образуют;
§ грамположительны, однако они плохо окрашиваются.
Обычно окрашивают кислотоустойчивые микобактерии по методу Циля-Нильсена, где используются концентрированные красители и подогревание.
Культивирование. Возбудители туберкулеза – аэробы. Растут при температуре 37-38 о С и рН среды 5,8-7,0. Отличительными культуральными особенностями туберкулезной палочки являются медленный рост и требовательность к питательным средам.
Поскольку глицерин стимулирует рост микобактерий, их можно выращивать на глицериновом бульоне, глицериновом агаре, глицериновом картофеле.
ВОЗ в качестве стандартной среды для выращивания туберкулезных палочек рекомендована среда Левенштейна-Йенсена. В настоящее время пользуются также средой Финна II. Туберкулезные палочки можно культивировать и на синтетических средах, например среде Сотона.
На плотных питательных средах через 2-3 недели возбудители туберкулеза образуют сухие морщинистые колонии кремового цвета с чуть приподнятым центром и изрезанными краями, напоминающие бородавки или цветную капусту. В жидких питательных средах микобактерии туберкулеза вырастают на 10-15 день в виде пленки, которая постепенно утолщается, становится грубой, морщинистой, ломкой, желтоватой и в силу тяжести иногда падает на дно. Бульон под пленкой остается прозрачным.
Ферментативные свойства. Возбудители туберкулеза биохимически мало активны. К тому же, свойства эти непостоянны, поэтому изучение ферментов не имеет диагностического значения.
Токсинообразование. Возбудители туберкулеза образуют эндотоксин – это белковое вещество впервые выделил Р. Кох (1890) и назвал его туберкулином. Туберкулин обладает свойствами аллергена. Он не оказывает токсического действия на здоровый организм. Его действие проявляется только в зараженном организме. Поэтому введение туберкулина используют с диагностической целью, в постановках аллергических проб (проба Манту - в/к вводят 0,5 мл очищенного туберкулина. Учет через 72 часа. Положительная реакция – покраснение и припухлость 5-10 мм – имеется иммунитет Для этой цели туберкулин готовят из бычьего типа микобактерий туберкулеза.)
Вирулентные штаммы возбудителей туберкулеза содержат особый липид корд-фактор, который способствует склеиванию микобактерий и росту их в виде кос и тяжей.
Антигенная структура. Микобактерии туберкулеза содержат О-антиген.
Устойчивость к факторам окружающей среды. Микобактреии туберкулеза самые устойчивые из неспороносных форм бактерий. Температуру 100 о С они переносят в течение 5 мин. УФ-лучи вызывают их гибель только через несколько часов.В высохшей мокроте они живут до 10 мес. При низких температурах микобактерии туберкулеза длительно сохраняются. Дезинфицирующие растворы губят их только через сутки. Наиболее чувствительны к хлорамину и хлорной извести.
Источники инфекции. Человек. Реже животные.
Пути передачи. Наиболее частые пути передачи – воздушно-капельный и воздушно-пылевой; реже пищевой (с молоком больных животных). Возможно внутриутробное инфицирование через плаценту.
Заболевания у человека и патогенез. Заболевание туберкулезом характеризуется многообразием клинических форм. Различают:
1. легочную форму (наиболее часто встречающуюся);
2. внелегочные формы: туберкулез желудка и кишечника, почек, мозговых оболочек, костей и других органов.
Каждая из этих форм заканчивается генерализацией процесса. При воздушно-капельном и воздушно-пылевом заражении первичный очаг возникает в легком. В пораженном органе образуется бугорок – туберкула (гранулёма). Бугорок представляет собой скопление лейкоцитов и гигантских клеток, внутри которых находятся микобактерии туберкулеза. При хорошей сопротивляемости организма соединительная ткань окружает бугорок, он обызвествляется и бактерии, оставаясь жизнеспособными, не выходят за пределы бугорка (закрытый процесс). При закрытом процессе палочки туберкулеза не выделяются с мокротой, мочой и др.
Таким образом, даже при доброкачественном течении процесса организм не освобождается от возбудителей туберкулеза. Считают, что 80% людей инфицированы туберкулезными бактериями. Однако клинически они здоровы. Когда организм попадает в неблагоприятные условия, защитные функции его снижаются, бугорок подвергается некрозу, бактерии высвобождаются и вовлекают в процесс новые участки, наступает обострение, образуются каверны – открытый процесс. Иногда может быть генерализация процесса, которая приводит организм к гибели. Чаще туберкулез протекает в хронической форме (закрытый процесс). Большое значение при обострении имеют условия труда и быта.
Иммунитет. Человек обладает определенной резистентностью, т.е. при заражении не всегда возникает заболевание, а образуется инфекционный (нестерильный) иммунитет, который обусловливается комплексом защитных факторов: гуморальных, клеточных, а также резистентностью органов и тканей.
Профилактика. Ранняя диагностика, изоляция и т.д.
Для специфической профилактики используется живая вакцина БЦЖ, полученная французскими учеными Кальметтом и Гереном. Эту вакцину вводят новорожденным на 5-7 день жизни однократно, внутрикожно в наружную поверхность плеча. Ревакцинацию проводят в 7, 11 лет.
Лечение. Проводится после определения антибиотикочувствительности возбудителя, поскольку микобактерии отличаются крайне высокой устойчивостью к антибиотикам. Антибактериальные препараты: стрептомицин, рифампицин, ПАСК, фтивазин и др.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Лекция по микробиологии.
ВОЗБУДИТЕЛИ ДИФТЕРИИ И ТУБЕРКУЛЕЗА.
Дифтерия поражает детские коллективы и все вновь создаваемые коллективы (1, 9 классы школы и училищ, армейские коллективы). Сегодня дифтерия очень актуальна.
Семейство Corinobacteriaceae объединяет порядка 60 видов из них примерно 20 патогенны для человека и животных.
Corinobacterium Difteriae -- микроб патогенный только для человека. Слово Corine обозначает булава. На обоих концах бактерии есть булавовидные утолщения. Считается что эти булавидные утолщения связаны с накоплением на обоих концах питательных веществ в зернах волютина, что выявляется окраской по Нейсеру. Волютин -- это полиметафосфаты, окрашиваются в синий цвет. Коринобактерии довольно мелкие, полиморфные, располагаются в мазке под углом друг к другу, изображая букву L.
Впервые выделил и описал коринобактерии дифтерии Лефлер. При делении они делятся вдоль. Дифтерийная палочка -- аэробы, имеют набор сахоролитических ферментов, расщепляют глюкозу, иногда крахмал и сахарозу.
Они хорошо устойчивы во внешней среде и на предметах (они могут передаваться через посуду, предметы). Протеолитических ферментов у возбудителя дифтерии нет вообще, потому применяются сложные питательные Среды. Они содержат аминокислоты, витамины и как правило кровь. Основная плотная Среда -- Среда Клауберга, жидкая Среда -- Среда Костюковой. В среду Клауберга входит и эритрацитарная масса и гемолизированная кровь. Обе Среды содержат гелурит калия или натрия. Рост дифтерийной палочки на них -- потемнение (черные полоски на среде Клауберга, а Среда Костюковой-- темнеет) это очень удобно при массовых исследованиях.
Дифтерийные коринобактерии вирулентны в R-форме. Для R-формы характерны шероховатые колонии. По культуральным свойствам выделяют 2 типа: 1) gravis (тяжелый), 2)mitio (легкий). Gravis описывается как цветок маргаритки: круглый выпуклый центр и фестончатый край, радиальная исчерченность по периферии. Mitio -- гладкая выпуклая ко. с ровными краями. Раньше считалось что gravis вызывает более тяжелое заболевание чем mitio, но это не так такой зависимости нет (зависит только от токсина).
Дифтерийные палочки имеют большое количество антигенов. В нашей стране наиболее распространены 7 антигенных типов. Их можно фаготипировать. Есть циногенные культуры (коринобактерии продуцируют цины 2 типов). Существуют циночувствительные культуры.
Ген токсигенности дифтерийной палочки не находится в хромосоме, а находится в ДНК умеренного фага. Если ДНК такого фага интегрируется в геном дифтерийная палочка начинает продуцировать токсин. Это явление было открыто в 1951 году (сейчас это доказано для возбудителя ботулизма, для некоторых энтеротоксигенных кишечных палочек, для холерного вибриона). Такое явление называется фаговая конверсия. Вообще лизогенная конверсия -- это привнесение профагом информации в бактериальную клетку. Если же профаг приносит факторы вирулентности, то такая конверсия называется фаговой. Токсин дифтерийной палочки -- истинный экзотоксин. Это белок состоящий из 2 субъединиц А и В. А имеет меньшую молекулярную массу, а В большую. Субъединица В отвечает за рецепцию. Когда субъединица В соединилась с клеткой, она остается снаружи, а А -- проникает внутрь клетки где находит фермент амитрансферазу-2, участвующий в синтезе белка. Он характерен для эукариотов. Этого фермента в каждой клетке 1-2 молекулы. Таким образом 1-2 молекулы экзотоксина достаточно чтобы остановить синтез белка в клетке. Токсин дифтерийной палочки очень ядовит. Его минимальная летальная доза для морской свинки весом где-то 235 гр составляет 0.06 микрограмма. Высокая ядовитость противоположна малой
инвазивности. Дифтерийная палочка имеет фактор похожий на гиалуронидазу, гемолизины, корд-фактор. Корд-фактор находят и у туберкулезных палочек. Это вещество которое не дает микробам расходиться друг от друга, склеивает их. Инвазивность дифтерийной палочки несмотря на наличие этих факторов считается нулевой, т.е. палочка попала в организм и не двигается с места.
Самая частая форма дифтерии -- дифтерия зева. На втором месте -- дифтерия зева и носа. На 3 м месте -- дифтерия носа. Остальные формы дифтерии -- редкие: дифтерия раны, пупочного кольца, половых органов, ануса, глаза. Лизоцим на дифтерийные палочки вообще не действует. Есть коринобактерия -- нормальный обитатель глаза -- Corinobacterium xerosis. Там где размножается дифтерийная палочка образуется пленка. Эта пленка состоит из чистой культуры дифтерийных микробов которые связаны корд-фактором и фибрином. Микробы в составе этой пленки никуда не распространяются, а распространяется только токсин. Если дифтерийная палочка попала на орган покрытый многослойным эпителием (зев, глотка) то развивается дифтерийное воспаление. При этом пленка плотно связана с подлежащими тканями (при удалении пленки - слизистая разрушается). Если дифтерийная палочка попала на орган покрытый однослойным плоским эпителием (более низкие отделы - гортань, трахея, бронхи) то воспаление будет крупозное. Пленка будет легко отделятся от подлежащей ткани (сама) и может перекрывать дыхательные пути и вызывать асфиксию. Дифтерия опасна также тем что происходит отек гортани и дыхательные пути перекрываются. Есть третья причина асфиксии -- дифтерийный токсин действует на дыхательный центр угнетающе. Пленки надо отсасывать (раньше врачи это делали ртом, сами при этом заражались).
Токсин действует еще на надпочечники и сердечную мышцу, которые фактически не функционируют. Вылечить такого ребенка можно только с помощью противодифтерийных сывороток. Противодифтерийная сыворотка - антитоксическая. Применение ее является противопоказанием для серодиагностики. Применяют для лабораторной диагностики бактериоскопический метод (можно покрасить любой краской, отличия сразу видны) и бактериологический. Сыворотка лошадиная, применяется в огромных дозах до 30000 МЕ. Это примерно 30 мл. Поэтому возможно развитие сывороточной болезни. Поэтому она вводится по Безредко, дают антигистаминные препараты.
ПРЕПАРАТЫ ДЛЯ АКТИВНОЙ ПРОФИЛАКТИКИ ДИФТЕРИИ.
1. Основной препарат -- дифтерийный анатоксин (АД-анатоксин). Он получен из дифтерийного токсина по Романову 0.4% формалином. Он обязательно сорбируется на гидроокиси Al. Так как анатоксин легко растворяется, рассасывается , то нужно создать депо. Вводится под лопатку, т.к медленнее всего рассасывается. 2. АДС-анатоксин -- адсорбированный дифтерийно-столбнячный анатоксин. 3. АДСМ-анатоксин (М-- минимальный,т.е в очень маленьких дозах антиген (в 4 раза меньше доза). Применяется при аллергии. Вместо одного введения делают два. 4. АКДС - вакцина. Сюда прибавляется убитые коклюшная вакцина, которая создает антимикробный иммунитет. Здесь “А” -- ассоциированная. Очень реактогенный препарат. Если ребенок на 2 м году жизни не привит, то ему не нужно прививать коклюшную вакцину, т.к коклюш уже не опасен., прививают АДС. Промежуток между вакцинациями АКДС вакцины должен быть не более 6 месяцев. Прививку нельзя делать если ребенок простужен.
Относится к семейству Micobacterioceae к порядку Actinomycetoles. Актиномицеты имеют сходство с грибами : они медленно растут на питательных средах, малый диаметр гиф, способны давать ветвящийся рост. Однако есть общее и с бактериями -- во-первых это прокариоты, во-вторых у актиномицетов клеточное стенка такая же как у бактерий, рибосомы, жгутики бактериального типа.
Семейство микобактерий включает около 200 видов. У человека заболевание вызывают Mycobacterium tuberculosis, M. Bovis, M. Afrecanus, M.lepra (возбудитель проказы).
Все микобактерии характеризуются кислотоустойчивостью, которая обусловлена высоким содержанием жировосковых веществ в клеточной стенке микобактерий: это миколовая, туберкулостеариновая, туберкулопальмитиловая кислоты. Эти кислоты встречаются только у туберкулезных палочек. Эти вещества позволяют микобактериям быть устойчивыми в агрессивных средах, устойчивы к высушиванию. В пыли, высохшей мокроте возбудители туберкулеза могут сохранятся до 6 месяцев. Окрасить микобактерии вследствие их кислотоустойчивости также очень трудно. Открыл микобактерию туберкулеза Кох. Красят их по Цилю-Нильсону (окрашиваются в красный цвет).палочки Коха также чуть изогнутые.
Микобактерии облигатные анаэробы, растут в виде поверхностной пленки. У них есть сахаро- протео- и липолитические ферменты. Требовательны к питательным средам, которые должны содержать аспарагин и глицерин. Основная Среда -- Левенштейна-Нейсена. Плотная желточная Среда, содержит малахитовую зелень. Растут микобактерии крайне медленно -- первые признаки роста обнаруживаются к концу 3 ей недели.
Существует большая группа условнопатогенных микобактерий которые вызывают микобактериозы. Микобактероизы часто похожи на туберкулез и на проказу. Есть и группы условно-патогенных микобактерий по способности продуцировать пигмент:
фотохромогенные - образуют пигмент на свету
нехромогенные и быстрорастущие - вырастают в пределах одной недели. Пигмент оранжево-желтого цвета продуцируется на свету. К быстрорастущим относится М.smegmatis представитель нормальной микрофлоры.
ПАТОГЕНЕЗ. Основное действующее вещество микобактерий туберкулеза -- эндотоксин-аллерген, названный Кохом туберкулином. Основная защита макроорганизма -- клеточная на уровне фагоцитов, на уровне специфических Т-лимфоцитов.
Источник инфекции - больной человек или животное (для М.bovis). механизм передачи аэрозольный, может быть и алиментарным. Почти в 100% туберкулезная палочка вызывает туберкулез легких, иногда ЖКТ, мочеполовой системы, кости - это вторичные процессы.
Если фагоцитоз микобактерий завершенный -- очаг обезвествляется и процесс заканчивается ( в корне правого легкого у каждого из нас есть так называемый очаг Гона). Если фагоцитоз незавершен, образуется специфическая гранулема, появляются гигантские многоядерные клетки Пирогова-Ланганса, в которых много туберкулезных палочек, развивается некроз. В центре гранулемы -- творожистый некроз. Образуется полость --каверна, если она сообщается с наружной средой то туберкулезная палочка будет выходить наружу -- это открытая форма туберкулеза (исследуют мокроту на содержание палочек при открытой форме туберкулеза).
Фтизиатры делят туберкулез на активный и неактивный. Активный туберкулез -- это когда обнаруживается антитела в РСК или в РНГА (реакция связывания комплимента или нагрузочной гемагглютинации). Титр антител очень маленький: диагностический титр 1: 5. Антитела не играют защитной роли.
Также для аллергодиагностики применяют пробу с туберкулином (Манту). Официальное название туберкулина -- протеин-туберкулин-дериват (т.е прозводное кожи) Линкинова.
Проба Манту проводится внутрикожно.
Специфическая профилактика -- вакцина BCG.
Лечение - использавание ПАСК, изониазида, антибиотиков (стрептомицин, канамицин).
Родовое название Mycobacterium (грибовидные бактерии) предложено Леманом и Нойманом в 1896 г., обративших внимание на плесневидную пленку, которая образуется при росте туберкулезной палочки на поверхности жидких сред (аэробы!). Вскоре коллекция микобактерий была дополнена видами, изолированными из внешней среды. Оказалось, что именно свободно живущие сапрофиты составляют большинство этой своеобразной группы прокариот, а истинно паразитические микобактерии представлены всего несколькими видами, патогенными для человека и животных. Впрочем, известную опасность представляют и некоторые микобактерии-сапрофиты (рис. 1). Они вызывают оппортунистические инфекции (микобактериозы) у иммунокомпрометированных лиц, а при заражении в раннем детстве могут извращать реактивность организма к возбудителям туберкулеза.
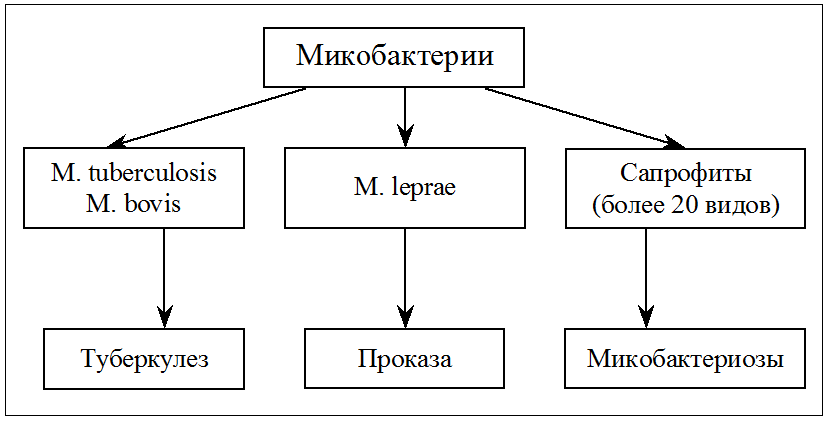
Рис. 1. Микобактерии, патогенные для человека
Известно более 60 видов микобактерий. Они объединены в род Mycobacterium семейства Mycobacteriaceae, которое относится к порядку Actinomycetales. В этом есть логика. Подобно актиномицетам, микобактерии образуют ветвящиеся клетки (особенно in vitro). Но сходство имеет и более глубокие корни, по крайней мере с соседями по порядку — нокардиями и коринебактериями. И те и другие содержат липиды, которые напоминают миколовые кислоты, хотя и уступают микобактериям по сложности строения этих уникальных компонентов клеточной стенки.
Микобактерии туберкулеза представляют собой тонкие, прямые или слегка изогнутые палочки, длиной 1—4 мкм и около 0,3 мкм в ширину (рис. 2). Они неподвижны, не образуют спор и капсулы, если не считать микозидной оболочки, которую иногда сравнивают с микрокапсулой. Они плохо окрашиваются по Граму, но, восприняв окраску, не обесцвечиваются этанолом, поэтому их считают грамположительными, хотя правильнее не относить ни к тем, ни к другим. С трудностями окраски туберкулезной палочки впервые столкнулся Кох, сумевший разглядеть их в мазках из мокроты лишь после 24—30-часовой (!) инкубации в щелочном растворе метиленовой синьки.
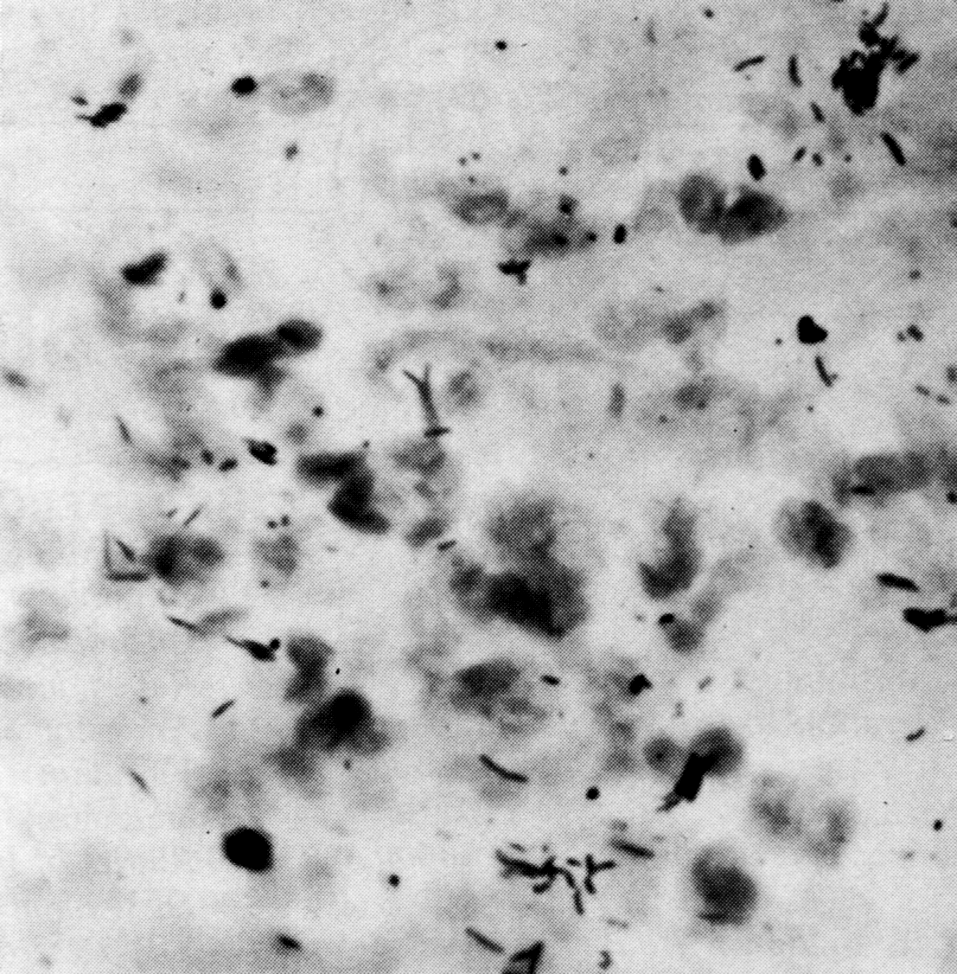
Рис. 2. M. tuberсulosis. Мазок из мокроты больного туберкулезом легких. Окраска по Цилю—Нильсену, х1050
Избирательная окраска основана на так называемой кислотоустойчивости микобактерий и включает два основных этапа. Сначала повышают проницаемость клеточной стенки для насыщенного раствора красителя (расплавление восковидного слоя путем прогревания или протравливания детергенами), а затем окрашенный препарат промывают разведенными кислотами. Обесцвечивая большинство бактерий, это сохраняет окраску микобактериальных клеток. По классической методике Циля—Нильсена на фиксированный мазок наливают карболовый фуксин, нагревают до отхождения паров, промывают закисленным этанолом (3% НСl в 85% растворе этанола) и докрашивают метиленовой синькой. Микобактерии удерживают фуксин и выглядят как красные палочки на голубом фоне; остальные бактерии теряют фуксин и окрашиваются в синий цвет. Этанол здесь не обязателен, но делает фон более чистым. Устойчивость к обесцвечиванию (она связана с образованием прочных комплексов между красителем и миколовыми кислотами клеточной стенки) проявляется не только в отношении кислот, но также щелочей и спиртов. Поэтому с равной справедливостью микобактерии можно называть также щелоче- и спиртоустойчивыми.
Морфологические и тинкториальные признаки микобактерий имеют много исключений, породивших немало споров о природе возбудителя. Туберкулезная палочка может терять кислотоустойчивость и хорошо окрашиваться по Граму, превращаться в филаментозные и даже мицелиоподобные формы, распадающиеся на палочки и кокки (гранулы/зерна Муха). Некоторые из них настолько малы, что проходят через бактериальные фильтры (фильтрующиеся формы). Теперь ясно: речь идет о фенотипической изменчивости, которая отражает экологическую пластичность возбудителя и его способность выживать в неблагоприятных условиях. Отсюда не удивительно, что плеоморфизм туберкулезной палочки сильнее проявляется в инвитровых культурах, т.е. в неестественной среде обитания.
Туберкулезные микобактерии — строгие аэробы и мезофилы, т.е. растут в диапазоне 30—42° С, лучше всего при 37°С. Размножение происходит очень медленно: период генерации составляет 14—16 ч (типичные бактерии делятся каждые 15 мин). Поэтому для получения обильного роста требуется не менее 4—6 нед, хотя миниатюрные колонии могут появиться через 7—10 дней. Туберкулезная палочка принадлежит к числу наиболее вяло реплицирующихся микобактерий. Большинство сапрофитических видов размножаются быстрее, их рост заметно отстает от других прокариот и хорошо заметен не ранее чем через 5—7 дней. Одной из причин отсроченного размножения микобактерий является высокая гидрофобность, связанная с обилием липидов в клеточной стенке. Это затрудняет поступление в бактерии питательных веществ, снижая их метаболическую активность.
Выделение первичных культур (т.е. непосредственно от больного) проводят на специальных средах, самые сложные из которых содержат яйца, картофельную муку и глицерин. Для подавления сопутствующей микрофлоры добавляют малахитовый зеленый или генцианвиолет. При субкультивировании туберкулезная палочка становится менее прихотливой и растет на обычных средах с добавкой глицерина.
В жидких средах рост происходит на поверхности (аэроб!). Нежная сухая пленка со временем утолщается, становится бугристо-морщинистой и обретает желтоватый оттенок, часто сравниваемый с цветом слоновой кости. Бульон остается прозрачным и добиться диффузного роста удается только в присутствии детергентов, например твина-80. В микроколониях (они образуются на ранних сроках и заметны только под микроскопом) формируются структуры, напоминающие жгуты — признак, который связывают с так называемым корд-фактором М. tuberculosis (рис. 3).

Рис. 3. Образование жгутов в микрокультуре М. tuberculosis
Морфотинкториальная изменчивость, о которой говорилось выше, весьма характерна для туберкулезной палочки, но это — фенотипические варианты, которые не переходят в генетически закрепленные биовары. Попытки выявить устойчивые серотипы М. tuberculosis и М. bovis не увенчались успехом, прежде всего из-за спонтанной агглютинации клеток, которая является следствием их высокой гидрофобности (см. ниже). Более удачным оказался опыт фаготипирования, но и он не закрепился в лабораторной практике.
В современных исследованиях много внимания уделяется дифференцировке (клонированию) микобактериальных штаммов по генетическим маркерам, прежде всего по особенностям хромосомного профиля ДНК. Генотипирование обычно проводится на основе вставочных генов — инсерционных последовательностей (англ. insertion sequences — IS). Они отличаются структурным полиморфизмом, позволяя классифицировать штаммы по степени генетического родства. Чаще используется анализ последовательности IS6110. Применяются и другие, дополнительные методы, основанные на особенностях генетического аппарата М. tuberculosis. К их числу относится сполиготипирование (от англ. spacer oligotyping), сравнение по числу прямых повторов и полиморфной G-С-обогащенной повторяющейся последовательности.
Полная идентичность возможна лишь внутри одного клона бактерий. Отсюда сравнение с отпечатками пальцев — англ. DNA fingerprinting. Каждое очередное поколение (т.е. каждый новый клон) несет хотя бы небольшие генетические различия. Накапливаясь со временем, они ведут к формированию клоногрупп, объединяемых в семейства. Тенденцию к распространению имеют клональные кластеры, еще не достигшие статуса группы. Наиболее изученным и распространенным (в том числе в России) является W-Beijing-семейство штаммов микобактерий туберкулеза. Оно включает более десятка клоногрупп — генетических ответвлений, эволюционировавших по IS6110 в различных географических зонах. Факторы, содействующие селекции штаммов W-Beijing, не известны. Возможно, это связано с повышенной контагиозностью, устойчивостью во внешней среде, резистентностью к антибиотикам. Именно первый W-штамм (акроним выбран произвольно), изолированный в 1990 г. в США, открыл тревожную эру лекарственной полирезистентности микобактерий туберкулеза. Есть мнение, что W-Beijing-штаммы более удачливы в преодолении барьера, создаваемого BCG-вакцинацией. Впрочем, каждая из перечисленных позиций встречает возражения.
Большую озабоченность вызывает эволюция лекарственной устойчивости на основе генетически закрепленных мутаций М. tuberculosis. Распространение резистентных биоваров может обезоружить в борьбе с туберкулезом или, по крайней мере, заметно снизить ее эффективность. Не случайно в системе лабораторий США, работающих с возбудителями особо опасных инфекций, организован центр, единственная задача которого — изучение штаммов туберкулезной палочки с множественной устойчивостью к антибиотикам.
Разгадка своеобразия микобактерий связана с необычностью их поверхностных структур. В клеточной стенке, устроенной сложнее, чем у других бактерий, преобладают липиды (более 60% сухой массы), в том числе специфичные для микобактерий. Именно они определяют нестандартность тинкториальных, физиологических и экологических свойств туберкулезной палочки (см. таблицу). Разнообразие микобактериальных липидов, в которых с трудом ориентируются даже искушенные биохимики, заставляет пользоваться такими собирательными понятиями, как миколовые кислоты, микозиды, сульфолипиды, корд-факторы и пр.
| Признак | Причина |
| Тинкториальные свойства: | |
| неокрашиваемость обычными способами | Слабая проницаемость клеточной стенки |
| кислото-, щелоче-, спиртоустойчивость | Связывание красителей миколовыми кислотами |
| Медленное размножение | Низкая скорость внутриклеточной диффузии питательных веществ |
| Культуральные свойства (сухие, морщинистые колонии), спонтанная агглютинация бактериальных клеток | Гидрофобность клеток |
| Устойчивость во внешней среде | Защита от высыхания |
| Устойчивость к дезинфектантам | Медленное проникновение антисептиков в клетку |
| Взаимоотношения с макрофагами: | |
| поглощение | Гидрофобность клеток |
| внутриклеточное выживание | Блокада образования фаголизосом, нейтрализация антимикробных факторов, ускользание в цитоплазму (повреждение фагосомальных мембран) |
| Цитотоксичность | Повреждение митохондриальной мембраны |
| Особенности иммунитета, иммунопатогенез | Иммуноадъювантная активность, CD1-зависимое представление антигенов (гликолипидов) |
Читайте также:


