Ревматоидный артрит на фоне туберкулеза легких
Туберкулезный артрит –инфекционный артрит, сопровождающийся деструкцией костно-хрящевых и околосуставных тканей. Туберкулезный артрит является одной из наиболее частых локализаций внелегочного туберкулеза. Среди других форм экстрапульмональной инфекции на долю туберкулезного артрита приходится более 20%. Костно-суставной туберкулез чаще развивается у детей в возрасте 7-14 лет; во взрослой популяции обычно болеют мужчины старше 50-60 лет. В большинстве случаев инфекция поражает позвоночник (40%), тазобедренные и коленные суставы (по 20%), реже — голеностопные суставы, кости стопы и верхних конечностей, плоские кости.
Симптоматика туберкулезного артрита крайне схожа с проявлениями бактериального артрита, но все же у этого вида заболевания имеются свои особенности, по которым устанавливается точный диагноз. Чаще всего туберкулезный артрит поражает один сустав (примерно в восьмидесяти пяти процентах случаев), и очень редко болезнь поражает два и более суставов.
Развивается туберкулезный артрит фазово. Всего наблюдает три фазы его развития, каждая из которых имеет свои проявления и симптомы.
- В первой фазе – преартритической – симптоматика крайне слаба. При этом можно заметить незначительную боль в суставе и небольшую припухлость. А признаков туберкулезной интоксикации практически нет в первой стадии развития болезни.
- Во второй фазе – артритической – симптоматика становится более выраженной. Пораженный сустав напухает, в нем отчетливо локализуется болевой синдром, нарушается функциональность сустава, пациент начинает прихрамывать, развивается атрофия мышцы.
- И в третьей фазе туберкулезного артрита – постартритической – происходит развитие вторичного деформирующего остеоартроза и полного сращения поверхностей сустава.
Диагностика туберкулезного артрита
Основанием для предполагаемого диагноза могут служить данные анамнеза, сведения о вакцинации БЦЖ, результаты рентгенологических и лабораторных исследований, туберкулинодиагностики. Важную роль имеет выявление первичного очага инфекции: туберкулеза легких, туберкулеза почек, генитального туберкулеза; положительные туберкулиновые пробы. В рамках диагностического поиска выполняется рентгенография легких, анализ мокроты на КУБ, бактериологический посев мочи, микроскопия и ПЦР-исследование урогенитальных мазков, ИФА крови на ВИЧ.
При туберкулезном артрите производится исследование синовиальной жидкости и отделяемого свищевых ходов, артроскопия, биопсия синовиальной оболочки. При рентгенографии суставов выявляются признаки остеопороза (разрежение костной ткани); сужение суставной щели, нарушение целостности кортикального слоя. В сомнительных случаях выполняется магнитно-резонансная или компьютерная томография суставов, МРТ и КТ позвоночника.
Туберкулезно-аллергические синовиты и артриты — следствие параспецифических аллергических поражений синовиальной оболочки сустава, проявляющихся ее иммунным воспалением, вызванным отдаленным туберкулезным очагом. К туберкулезно-аллергическим синовитам относится прежде всего болезнь Понсе в различных ее проявлениях. Заболевание развивается на фоне туберкулеза внутренних органов, однако источник инфекции может быть скрытым. Клиническая картина схожа с проявлениями реактивного воспаления сустава, возникающего при первичных оститах, но отличается упорным волнообразным течением с ремиссиями и сезонными обострениями. В классической форме болезнь Понсе протекает в виде полиартрита, причем чаще поражаются мелкие суставы. Однако в последние годы заболевание нередко начинается с поражения одного крупного сустава и моноартрит в течение длительного периода времени может быть единственным проявлением болезни. Это рассматривают как следствие выраженного патоморфоза болезни Понсе, наблюдаемого в последние десятилетия. Высказано мнение о том, что первичных синовиальных форм туберкулеза суставов не существует, так как возможность первичного поражения туберкулезом синовиальной оболочки сустава не доказана. Первичные синовиальные формы туберкулеза суставов на самом деле являются либо вторичными синовитами, характеризующимися клинической картиной, схожей с наблюдаемой в стадии начала артритической фазы, либо относятся к туберкулезно-аллергическим артритам — атипично протекающая болезнь Понсе. Осложнения туберкулеза суставов — деформации, натечные абсцессы, свищи, амилоидоз внутренних органов — возникают в разные периоды развития болезни, но чаще всего — в артритической фазе.
- КЛЮЧЕВЫЕ СЛОВА: артрит, заболевания суставов, жесткое дыхание, бронхоэктазы
Поражение дыхательной системы является одним из наиболее часто встречающихся системных проявлений ревматоидного артрита (РА). В то же время их своевременное выявление и дифференциальная диагностика представляют собой достаточно сложную задачу. Типичные клинические симптомы, как и используемые рутинные методики, позволяют диагностировать в основном лишь далеко зашедшие изменения. Наибольшей информативностью обладает дорогостоящая методика КТ высокого разрешения (50–80%) и биопсия легких [1, 4, 6]. В то же время информативность рутинной рентгенограммы составляет не более 6% [4, 6]. Специфические клинические симптомы поражения легких выявляются лишь у 6,5–10% пациентов [4, 5]. Основные формы поражения легких и соответствующие им клинические синдромы представлены на рисунке 1. Согласно литературным данным, наиболее часто диагностируются поражения плевры, большая часть которых бессимптомны (40–75% аутопсий и 20% – рентгенологические изменения) или сопровождаются умеренным болевым синдромом (около 25%) [6]. Вторым по частоте заболеванием паренхимы легких является ассоциированная с ревматоидным артритом интерстициальная болезнь легких (RA-ILD) [1–7]. Наиболее часто встречается обыкновенная интерстициальная пневмония – UIP, один из самых неблагоприятных вариантов RA-ILD [6–8]. Реже диагностируется неспецифическая интерстициальная пневмония, в большей степени типичная для системных заболеваний соединительной ткани [7, 8]. Встречаются также смешанные варианты с элементами лимфоцитарной интерстициальной пневмонии [6, 7]. Указанным состояниям сопутствуют рестриктивные изменения. Ранняя клиническая симптоматика RA-ILD в этих случаях может включать сухой кашель и одышку инспираторного типа. При некоторых вариантах RA-ILD (криптогенная организующая пневмония – СОР [9] и крайне редко ассоциирующаяся с ревматоидным артритом респираторная бронхиолит-интерстициальная болезнь легких – RB-ILD) одышка может быть смешанной или экспираторной, а при физикальном обследовании могут определяться признаки обструкции (жесткое дыхание, коробочный перкуторный тон). Обструктивный и бронхитический синдромы при RA-ILD могут быть следствием развития тракционных бронхоэктазов на фоне значительного фиброза легочной ткани [6]. Реже RA-ILD развивается как осложнение базисной терапии (метотрексат, препараты золота, D-пеницилламин) [1, 2, 6, 7]. Достаточно редко встречается эозинофильная пневмония (острая или хроническая), в том числе в дебюте заболевания [10].
Другой наиболее частый вариант поражения паренхимы – ревматоидные узелки – в подавляющем большинстве случаев является бессимптомным [1, 2]. При рутинной рентгенографии они выявляются всего у 1% пациентов, в то время как при КТ высокого разрешения частота выявления достигает 22% случаев. По данным аутопсии, узелки в легких обнаруживаются у 32,5% умерших больных с РА [4, 6]. Осложнениями ревматоидных узелков может быть развитие некроза с образованием полости, кровохарканьем, спонтанным пневмотораксом или эмпиемой плевры. Описаны случаи микозного поражения узелка с развитием мицетомы [4]. Дифференциальная диагностика очаговых изменений в легких у больных РА представляет особую диагностическую проблему в связи с высоким риском туберкулезного процесса не только у больных, получающих биологическую терапию (в 30 раз выше, чем в общей популяции), но и пациентов, получающих традиционное лечение метотрексатом и преднизолоном (в 4–8 раз выше, чем в популяции) [11, 12]. Некоторыми авторами обсуждается проблема роста ревматоидных узелков на фоне биологической терапии (инфликсимаб, этанерцепт) или лечения лефлюнамидом, однако в других публикациях этот феномен не подтверждается, тем более что продолжение терапии не приводит к клиническому ухудшению состояния пациента [13, 14, 20]. Редкой причиной очаговых изменений в легких при РА может быть перекрест-синдром с ограниченными легочной паренхимой проявлениями гранулематоза Вегенера [16]. Необходимо отметить, что как интерстициальная болезнь легких, так и ревматоидные узелки значительно чаще обнаруживаются у курящих пациентов по сравнению с некурящими [6]. Тем не менее наличие соответствующего анамнеза не должно рассматриваться как фактор, позволяющий полностью объяснить имеющиеся пульмонологические симптомы и исключить наличие поражения дыхательных путей, обусловленное РА.
Несколько реже встречаются поражения дыхательных путей, проявляющиеся обструктивным и бронхитическим синдромом. К ним относятся бронхоэктазы (в большинстве случаев тракционного характера на фоне RA-ILD), облитерирующий бронхиолит, фолликулярный бронхиолит и бронхоцентрический гранулематоз [6]. В целом частота развития патологии бронхиального дерева (включая тракционные бронхоэктазы) составляет около 30% [1–3, 6]. Обструктивные нарушения функции внешнего дыхания диагностируются примерно у 38% пациентов с нормальными результатами рентгенограммы [15]. Достаточно редки, но опасны начальные проявления легочного васкулита – кровохарканье, одышка или легочная гипертензия – и его потенциально фатальное осложнение – диффузное альвеолярное кровотечение, клинически и морфологически сходное с аналогичным состоянием при системной красной волчанке и обусловленное некротизирующим капилляритом с отложением иммунных комплексов. Клинические симптомы диффузного альвеолярного кровотечения включают острое развитие выраженной инспираторной одышки с резкой гипоксемией, кровохаркание, анемии [6].
При анкилозирующем спондилоартрите пульмонологические симптомы встречаются реже – примерно у 10% пациентов. Рестриктивный характер изменений обнаруживается при наиболее типичном осложнении – двустороннем апикальном фиброзе верхних долей, развитии буллезных изменений (как правило, той же локализации), а также при анкилозе костовертебральных суставов. Описаны случаи развития интерстициальной болезни легких, сходной с таковой при РА, однако в этих публикациях отсутствуют сведения о вариантах данного заболевания. Обструктивный синдром и смешанный характер изменений могут быть обусловлены тракционными бронхоэктазами или парасептальной эмфиземой [16–18]. У больных псориатическим артритом могут встречаться узловые образования в легких, сходные с таковыми у пациентов с РА. Подобные узелки, так же как и при РА, могут осложняться некрозом и спонтанным пневмотораксом [19].
Таким образом, при РА и серонегативных спондилоартритах (ССА) достаточно часто встречается поражение дыхательной системы. При этом ранняя диагностика указанных изменений затруднена в связи с неспецифичностью симптомов и поздним появлением изменений, определяемых рутинными методами, доступными практическому здравоохранению. В связи с этим представляется актуальным анализ диагностической значимости неспецифических пульмонологических симптомов (кашель, одышка, изменения перкуторной или аускультативной картины легких), позволяющих заподозрить вовлеченность легких в патологический процесс и, соответственно, планировать дальнейшее обследование пациентов с помощью высокотехнологичных методов.
С целью поиска наиболее информативных клинических симптомов, определяемых рутинной диагностикой, проведен анализ историй болезни 29 больных ревматоидным артритом и 24 пациентов с серонегативными артритами, находившихся на лечении в клинике госпитальной терапии в период с 2006 по 2009 г. Средний возраст больных составлял 51,4 года, средняя длительность заболевания – 7,6 лет. Средний показатель активности заболевания составил 2,23, значения индекса DAS4 – 3,3 DAS28 – 4,9. Из 28 пациентов отрицательные значения ревматоидного фактора отмечались у 6, у 2 серонегативных пациентов не выявлялись антитела к циклическому цитруллиновому пептиду (АЦЦП). Системные проявления отмечались у 18 серопозитивных и 3 серонегативных пациентов. Наиболее частыми проявлениями у серопозитивных пациентов были лихорадка [9] и лимфаденопатия [5]. Анемия выявлена у 3 больных, еще у 3 – ревматоидные узелки и полинейропатия. У 2 пациентов документировано поражение дыхательной системы (интерстициальная болезнь легких и выпотной плеврит), у 1 – синдром Шегрена. В целом 3 и более системных проявлений имели место у 4 пациентов. У серонегативных пациентов имели место лихорадка [2], лимфаденопатия [2], амиотрофия и синдром Рейно [1]; 3 и более системных проявлений отмечалось у 1 пациента. Несмотря на то что диагностированное поражение легких отмечалось лишь у 2 серопозитивных пациентов с высокой степенью активности заболевания, такие симптомы, как кашель, одышка, отмечались у 8 пациентов (28,6%), объективные изменения в легких (коробочный тон, жесткое дыхание) – у 20 (71%). Реже указанные симптомы наблюдались у больных ССА. Одышка, затруднение дыхания и кашель встречались у 7 (29,1%), объективные изменения в легких зарегистрированы у 11 (45,8%) пациентов (рис. 2).
Обращает на себя внимание тот факт, что 10 больных РА и 4 ССА, у которых выявлялись объективные симптомы со стороны легких, не курили (рис. 3). Таким образом, примерно у половины пациентов с РА и более чем у 3 с ССА наличие симптомов не может быть объяснено ХОБЛ. Кроме того, как уже указывалось выше, пульмонологические симптомы при РА чаще отмечаются у курящих больных, что требует включения таких пациентов в диагностический поиск.
Анализируя связь перечисленных симптомов с активностью заболевания, было обнаружено, что у больных РА, предъявляющих пульмонологические жалобы, по сравнению с пациентами, не имеющими симптомов поражений легких, отмечались более высокие показатели активности заболевания – 2,8 и 2,0 – и значения индекса DAS4 – 4 и 2,9 соответственно. Эти больные были старше по возрасту – 55,9 и 49,6 – и имели большую длительность заболевания – 8,6 и 7,6 лет соответственно. Та же тенденция отмечалась и у пациентов с ССА: больные, предъявляющие пульмонологические жалобы, отличались большей активностью заболевания, у 49,5% из них определялось 2 и более системных проявлений против 26,7% пациентов без жалоб.
Из 12 пациентов с РА, которым производилось рентгенологическое исследование в клинике, только у 4 не было диагностировано каких-либо изменений. Изменения плевры обнаружены у 2 больных (экссудативный плеврит, плевральные шварты), у 5 – паренхиматозные изменения (диффузные интерстициальные изменения с субплевральным фиброзом, множественные субплевральные округлые образования в нижней доле, лимфаденопатия, субплевральный тяж в паренхиме одного из сегментов, диск-ателектаз, посттуберкулезные изменения). У одного пациента выявлены перибронхиальные изменения (подчеркнутость структуры бронхов). Таким образом, только у 2 пациентов были выявлены достоверные признаки, позволяющие диагностировать ревматоидное поражение легких. В то же время наличие множественных очаговых образований, плевральных шварт, лимфаденопатии и субплеврального тяжа требовали проведения дифференциальной диагностики между специфическим процессом (туберкулез), проявлениями ревматоидного артрита (в том числе последствиями криптогенной организующей пневмонии) и неспецифическими постпневмоническими изменениями (плевральные шварты). Наличие дисковидного ателектаза у больной 49 лет с высокой (3-я степень) активностью заболевания и ревматоидными узелками без признаков варикозной болезни нижних конечностей может быть обусловлено эпизодом тромбоэмболии на фоне активации эндотелия и внутрисосудистой гемокоагуляции. Из 12 пациентов ССА, у которых производилось рентгенологическое исследование, не обнаружены изменения в легких у 7 (58,3%), у 3 (25%) определялись паренхиматозные (посттуберкулезные у 2, диск-ателектазы у 1), у 1 (8,3%) – перибронхиальные изменения. Ни у одного из пациентов не были определены признаки поражения плевры. Таким образом, как при РА, так и, в меньшей степени, при ССА достаточно часто выявляются как клинические пульмонологические симптомы, так и рентгенологические изменения в паренхиме легких. При этом у пациентов, предъявляющих жалобы со стороны дыхательной системы, отмечается более высокая активность заболевания, чаще диагностируются системные проявления. В связи с этим можно предположить, что неспецифические пульмонологические симптомы могут быть начальными проявлениеми поражения легких в рамках РА или ССА, что требует проведения у этих пациентов углубленного обследования дыхательной системы, в том числе с применением высокотехнологичных методов.
Необходимо отметить, что при наличии рентгенологических изменений в легких (фиброзные тяжи, шварты, очаговые образования) требуется проведение дифференциальной диагностики с туберкулезным процессом, в том числе определение уровня антител к туберкулезной микобактерии. У 24,1% пациентов с РА и 18,1% больных ССА был контакт с больными туберкулезом в анамнезе и/или выявлены признаки, свидетельствующие об активации туберкулезной инфекции (посттуберкулезные изменения на рентгенограмме или положительная реакция Манту на пробу с 2ТЕ ППД-Л). С учетом приведенных ранее литературных данных о повышенном риске развития туберкулеза у больных РА (в том числе не получающих биологическую терапию), это свидетельствует о возможности развития у данных пациентов осложнений на фоне терапии биопрепаратами. Профилактический курс лечения изониазидом в противотуберкулезном диспансере по месту жительства проводился у 10% больных РА и 13,6% ССА. Ни у одного пациента не обнаружено признаков активации туберкулезной инфекции на фоне лечения инфликсимабом. Таким образом, при правильном отборе пациентов для проведения терапии антагонистами ФНО применение биологической терапии является достаточно безопасным и не приводит к активизации туберкулезной инфекции.
Меня зовут Женя, мне 31 год, из них 6 лет у меня диагноз: ревматоидный артрит. Сейчас многие знают, что такое рак или СПИД, а вот о РА говорят не очень часто.
Все началось в 2012 году.

Хуже стало год спустя, когда ни с того ни с сего я стала ощущать жуткие боли не только в руках, но и в ногах, по утрам ступить на ногу было невозможно, буквально. Первые 20–40 минут после пробуждения казались каким-то кошмаром, к тому времени боли в руках разошлись до такой степени, что надеть одежду самостоятельно я не могла, пока не подействует обезболивающее. Боль похожа на ту, когда очень сильно ушибся, — и эта первая звенящая боль не проходит.
Походы по врачам и анализы привели меня к ревматологу. Врач пенсионного возраста тогда сказала, что не видит у меня РА и мне стоило бы одеваться теплее. Тогда я еще не понимала масштаб бедствия, которое наступит после того, как я со спокойной душой выйду из кабинета.
Очередной московский ревматоидный центр (я тогда жила в столице и могла выбрать центр). На приеме у врача я рыдала — у меня кончились силы терпеть боль.
Так что, когда я пришла к [своему нынешнему врачу] Т. А., она сказала, что назначает гормоны и будет вводить лекарство в мое лечение постепенно, — а я всё ревела.
Гормоны — это результат затянутого начала лечения, точнее, его отсутствия, длительный воспалительный процесс просто так не затихнет, а основное лекарство — только в уколах — раз в неделю, строго по расписанию. Обезболивающее и мази, примочки из странных растворов — дополнительные помощники.
Боли начали утихать, пришли побочные эффекты от сложных лекарств: тошнота, головокружение и другие…

Ревматоидный артрит — хроническое заболевание, при котором воспаляется синовиальная мембрана, из-за чего суставы теряют подвижность и опухают. Постепенно воспаление разрушает концы кости и покрывающий суставные поверхности хрящ. Нарушаются структура и функции связок, придающих суставу прочность, и он начинает деформироваться.
Чаще всего болезнь поражает несколько суставов и обычно начинается на одном из мелких — кисти или стопы. Как правило, заболевание развивается симметрично. В воспалительный процесс могут быть вовлечены глаза, легкие, сердце и кровеносные сосуды. Болезнь обычно развивается медленно, но клинически проявляется резко.
Ревматоидный артрит — аутоиммунное заболевание; синовиальную мембрану, а в ряде случаев и другие части тела повреждают свои же антитела.
Ревматоидный артрит не свойствен молодому возрасту, да и вообще мало изучен.
Единственное, что известно наверняка, — сегодня ревматоидный артрит не излечивается, он на всю жизнь.
Я боялась этого заболевания. Видела, что оно делает с суставами и как люди впадают в отчаяние. Оно и понятно, изменения настолько уродливы, а ты настолько беспомощен…
Однажды я почувствовала, что мне нужна поддержка, и зашла на форум для людей с РА. С тех пор я больше не посещала таких форумов. Вероятно, у русского человека фокус внимания смещен больше на страдания и на то, как ему плохо. Я же искала, скорее, поддержку, рецепты того, как люди справляются, уверенность, что нам всё посильно.
Один раз пошла к психотерапевту, рассказала ему, как переживаю и нервничаю, ведь знаю, что это заболевание со мной на всю жизнь, а жизнь на глазах рушится. Он выписал мне лекарство. Я его приняла и ощутила упадок сил, мне ничего не хотелось делать. Чтобы не навредить себе больше и не впасть в апатию, я не стала больше его пить и к этому врачу больше не ходила. Моральную поддержку я стала искать в себе сама.
Ты молода, у тебя много планов, и вдруг ты уже не можешь жить полноценно, врачи говорят, что тебе нельзя заниматься активными видами деятельности и работа твоя тебе не подходит — слишком большая физическая нагрузка. Поэтому о своей особенности я молчала.
За несколько месяцев до того, как у меня развился ревматоидный артрит, я сменила сферу деятельности и стала работать бариста. Мне хотелось развиваться в кофейной индустрии, у меня был план на несколько лет. И вот ты приходишь на работу и понимаешь, что не можешь сжать руку, чтобы приготовить кофе, тебе просто не хватает сил делать то, что ты любишь.
Сейчас я просыпаюсь в 6 утра, принимаю таблетку метипреда и продолжаю спать. Так начинается каждое мое утро с 2014 года. Раз в неделю ставлю укол основного лекарства. Таких страшных болей, как раньше, нет, лекарства помогают. Но я всё же боюсь просто удариться пальцем или локтем — суставы реагируют. Несмотря на то что мне стало легче, мне нельзя бегать, под запретом ударные нагрузки, нельзя заниматься активным спортом в принципе. Так что пробежать марафон или проехать на велосипеде длительный маршрут я не смогу.
Но я прошла этап принятия.
Я не разлюбила прогулки, я научилась быть спокойнее. Ведь сначала казалось, что все вокруг бодрые и сильные и только ты такой слабак. Но потом ты учишься быть более плавным и летящим, узнаешь, как можешь сбалансировать самого себя.

Но пока центра нет, я могу лишь дать несколько советов:
— Если у вас ревматоидный артрит либо есть подозрение на него, сразу идите к врачу, ищите хорошего специалиста — вам с ним долго по пути.
В какие-то моменты я прекращала терапию без одобрения врача: мне казалось, что я выздоровела, — не делайте так, РА — коварное заболевание, потом может быть хуже.
— Надо помнить: как бы больно ни было, наступит день, когда боли не будет, главное — не опускать руки и подобрать лечение!
— Еще нужно делать зарядку. По утрам ты чувствуешь себя настолько скованно, будто твое тело сжалось в комок. Но проходит время — обязательно нужно сделать зарядку, очень медленную, прощупать все косточки и мышцы. Это помогает.
Ну и одевайтесь теплее, конечно! Говорят, это защищает от многих заболеваний.

Фиброз легких — это процесс образования в легких фиброзной (рубцовой) ткани, что приводит к нарушениям дыхательной функции. При фиброзе снижается эластичность и растяжимость легочной ткани, затрудняется прохождение кислорода и углекислого газа через стенку альвеол (легочных пузырьков, в которых происходит контакт вдыхаемого воздуха с кровью).
Причины заболевания
Фиброз легкого может возникнуть вследствие развития воспаления на альвеолах интерстициальных легочных тканей. В результате это становится причиной образования рубцов и дальнейшего разрастания тканей.
К основным причинам образования можно отнести:
• Наследственный фактор – первая и основная причина
• Курение
• Пребывание в загрязненной местности или в промышленном районе, на вредном производстве
• Осложнение таких заболеваний, как сахарный диабет, красная системная волчанка, ревматоидный артрит
• Осложнение заболеваний легких – такие как альвеолит, саркоидоз, асбестоз, туберкулез
• Длительное вдыхание частиц органических веществ или минералов
• Интоксикация химическими веществами
• Радиоактивное излучение на участке грудной клетки
Виды легочного фиброза
• Идиопатический легочный фиброз – когда определить болезнь, которая его вызвала, невозможно
• Интерстициальный легочный фиброз – когда причину заболевания можно обнаружить
Формы
Фиброз может быть односторонним и двусторонним, очаговым (поражается небольшой участок легкого) и тотальным (распространяется на все легкое).
• фиброз (пневмофиброз) – умеренное тяжистое разрастание соединительной ткани, чередующееся с неизмененной легочной тканью;
• склероз (пневмосклероз) – грубое замещение участков легочной ткани соединительной с уплотнением легких;
• цирроз легких – полное замещение легочной ткани соединительной с повреждением бронхов и сосудов легкого.
По причине развития выделяют:
• фиброз как следствие пылевых заболеваний легких (силикоз — профессиональное заболевание легких, развивающееся после длительного вдыхания пыли силикатов; асбестоз — профессиональное заболевание легких, возникающее после длительного вдыхания пыли асбеста);
• лекарственный фиброз (развивается на фоне длительного приема препаратов для лечения аритмии, химиотерапевтических препаратов (для лечения опухолей));
• фиброз при заболеваниях соединительной ткани (ревматоидном артрите, системной склеродермии, системной красной волчанке);
• фиброз инфекционной природы (после пневмонии или туберкулеза легких);
• идиопатический (первичный) фиброз (возникает без видимой причины).
Лечение заболевания
Специфического эффективного лечения фиброза легких нет. Среди основных рекомендаций выделяют следующие:
• исключить воздействие повреждающих факторов (профессиональные вредности);
• ограниченные участки пневмосклероза, не проявляющие себя клинически, в терапии не нуждаются;
• кислородотерапия (ингаляции кислорода с помощью специальных аппаратов);
• оперативное лечение: возможно удаление функционально неполноценного ограниченного очага, в случае тотального фиброза (распространяющегося на все легкое) – пересадка легких.
Сегодня в области медицины проводятся различные разработки препаратов, которые способствуют уменьшению таких рубцов. Также некоторые из них при различных типах фиброза способны уменьшать процессы, способствующие рубцеванию ткани. К таким препаратам относят кортикостероиды, которые могут подавить иммунную систему. В случае подавления иммунной системы уменьшается воспаление легких и последующее рубцевание ткани в легких. Кроме этого, прием кортикостероидов может вестись в комплексе с противовоспалительными и другими препаратами.
Осложнения и последствия
• Хроническая дыхательная недостаточность (недостаточность кислорода организму).
• Легочная гипертензия.
• Хроническое легочное сердце.
• Присоединение вторичной инфекции (с развитием пневмонии).
Профилактика фиброза легкого
• Использование средств индивидуальной защиты при работе с профессиональными вредностями, соблюдение правил техники безопасности.
• Своевременное лечение воспалительных заболеваний легких (пневмонии; туберкулеза).
• Отказ от курения.
• При приеме препаратов, способных привести к развитию фиброза легких (некоторые антиаритмические препараты), – периодический профилактический контроль за состоянием легких.
Врач общей практики (семейный врач), врач-терапевт Зиновенкова Елена Алексеевна
Ревматоидный артрит (РА) – аутоиммунное заболевание неясной этиологии, характеризующееся симметричным эрозивным артритом (синовитом) и широким спектром внесуставных (системных) проявлений. РА – распространенное заболевание, им традает примерно 1 процент населения земного шара; характерная его черта – неуклонное прогрессирующее поражение суставов (постоянные боли, деформация, нарушение функции) и внутренних органов, приводящее к инвалидизации (около 1/3 больных за 20 лет болезни становятся полными инвалидами) и снижению продолжительности жизни. Последнему в немалой степени способствует высокий риск развития сопутствующих заболеваний (инфекции, атеросклеротическое поражение сосудов, артериальная гипертензия – АГЮ остеопороз и др.).
Развитие и прогрессирование РА определяется сложным, плохо изученным сочетанием генетически детерминированных и приобретенных дефектов (дисбалансом) нормальных (иммуно)регуляторных механизмов, ограничивающих патологическую активацию иммунной системы в ответ на потенциально патогенные, а нередко и физиологические стимулы (схема 1). Этот дисбаланс ведет быстрой трансформации физиологической (защитной) острой воспалительной реакции в хронический неконтролируемый прогрессирующий воспалительный процесс, потенциально затрагивающий все органы и системы человека, в первую очередь – суставы.
Неизученность этиологии РА делает невозможной эффективную этиотропную терапию и ставит его лечение в ряд наиболее сложных проблем медицины. Тем не менее в последние годы в этом направлении достигнуты определенные успехи. Благодаря расшифровке механизмов, лежащих в основе эффективности и токсичности нестероидных противовоспалительных препаратов (НПВП), симптоматическая терапия РА была усовершенствована, чему во многом способствовало создание нового класса этих препаратов – так называемых ингибиторов циклооксигеназы (ЦОК-2), а расширение знаний о механизмах ревматоидного воспаления позволило оптимизировать патогенетическую (базисную) терапию РА. Прогресс, достигнутый за последние годы, особенно хорошо виден при сравнении рекомендаций Американской коллегии ревматологов по фармакотерапии РА, опубликованных в 1996 и 2002 гг.
— глюкокортикоиды – ГК (внутрисуставно, перорально);
— базисные препараты: гидроксихлорохин, сульфасалазин, метотрексат, золи золота (внутримышечно, перорально), азатиоприн, D-пеницилламин.
— ГК (внутрисуставно, перорально);
— базисные препараты: гидроксихлорохин, сульфасалазин, метотрексат, соли золота (внутримышечно, перорально), азатиоприн, D-пеницилламин, циклоспорин А, лефлюномид, миноциклин;
— биологические агенты: моноклональные акнтитела – МАТ – к фактору некроза опухоли (ФНО)-ά (ремикейд); растворимый ФНО-75-Fc lgG (этанерцепт); растворимый антагонист ИЛ-1 (анакинра); иммуноадсорбция с использованием белка А стафилококка.
Однако особое значение имеет разработка концепции ранней, агрессивной терапии, в основе которой лежат данные о том, что наиболее высокая скорость деструкции суставов, в конечном счете, и определяющая неблагоприятный (непосредственный и отдаленный) прогноз болезни, наблюдается именно в дебюте РА. Полагают, что, поскольку применение базисных препаратов при раннем РА позволяет модифицировать течение болезни, активное лечение РА (как и других хронических заболеваний человека – сахарного диабета, АГ, ИБС и др.) должно начинаться как можно раньше. Ранняя диагностика и ранняя терапия любыми базисными противоревматическими препаратами имеют важное значение для улучшения качества жизни и отдаленного прогноза у пациентов с РА.
Современные подходы к диагностике РА подробно освещены в специальной литературе, их обсуждение выходит за рамки задач данной публикации. Следует лишь напомнить, что характерными признаками ревматоидного синовита являются утренняя скованность, длительность которой составляет не менее 1 ч. И симметричное поражение суставов кистей (и стоп); реже бывают поражены коленные, голеностопные, плечевые, локтевые, плюснефаланговые суставы, включая сустав большого пальца стопы, а также шейный отдел позвоночника и тазобедренные суставы. Поскольку РА и другие заболевания опорно-двигательного аппарата распространены весьма широко, очевидно, что заподозрить РА должны еще на поликлиническом этапе врачи-терапевты. Именно поэтому группа авторитетных европейских и американских ревматологов с позиций доказательной медицины разработала алгоритм ранней диагностики РА для поликлинических врачей: более трех воспаленных суставов, поражение пястнофаланговых/плюснефаланговых суставов, утренняя скованность более 30 мин – показания для немедленной консультации ревматолога. Применение алгоритма в широкой клинической практике должно способствовать улучшению прогноза РА, так как при правильной диагностике можно раньше назначить активную терапию базисными противоревматическими препаратами.
После постановки диагноза РА всем больным необходимо провести базовое клиническое, лабораторное и инструментальное обследование.
В клиническое обследование входят выявление субъективных симптомов (выраженность болей в суставах, длительность утренней скованности, длительность общего недомогания, ограничение подвижности в суставах) и физическое обследование:
— определение числа воспаленных и болезненных суставов; оценка механических нарушений (нарушение подвижности, крепитация, нестабильность и/или деформации);
— обнаружение внесуставных проявлений;
— оценка функционального статуса или качества жизни (по стандартным опросникам);
— общая оценка активности врачом;
— общая оценка активности пациентом.
При лабораторном обследовании:
— определяют СОЭ и концентрацию С-реактивного белка (С-РБ); ревматоидный фактор;
— проводят общий анализ крови;
— оценивают уровень электролитов;
— выполняют общий анализ мочи;
— проводят биохимическое исследование на печеночные ферменты, креатин, альбумин;
— исследуют синовиальную жидкость;
— проводят анализ кала на скрытую кровь.
Инструментальное обследование состоит в рентгенографии суставов кистей и стоп, при необходимости – других пораженных суставов.
При каждом визите пациента врач-ревматолог должен оценить активность патологического процесса, эффективность терапии и клинической ремиссии с использованием международных критериев.
Оценка активности РА:
Во время каждого визита определяют:
— выраженность болей в суставах (визуальная аналоговая шкала);
— длительность утренней скованности, в мин;
— наличие воспаленных суставов (болезненные и припухшие суставы);
— прогрессирование заболевания: нарастание ограничения подвижности, нестабильности и/или деформации суставов;
— прогрессирование по данным рентгенографии;
— динамику минеральной плотности костной ткани (МПКТ) по данным костной денситометрии.
Определяют и другие параметры, характеризующие ответ на лечение:
— активность, по мнению врача;
— активность, по мнению пациента;
— функциональный статус или качества жизни (по стандартизованным опросникам).
В задачи терапии РА входят:
— снижение выраженности симптомов, включая недомогание, боли, отек и скованность суставов;
— предотвращение деструкции, нарушения функции и деформации суставов;
— сохранение качества жизни;
— достижение клинической ремиссии;
— увеличение продолжительности жизни.
Нестероидные противовоспалительные препараты
Основной метод симптоматического лечения РА – назначение НПВП с целью уменьшения боли и воспаления в суставах. Однако эти препараты недостаточно хорошо контролируют не только прогрессирование, но и субъективные симптомы у пациентов с РА и вызывают побочные эффекты, особенно у лиц пожилого возраста. У пациентов с факторами риска осложнений со стороны желудочно-кишечного тракта – ЖКТ (пожилой возраст, язвенный анамнез, сочетанное применение глюкокортикоидов – ГК, антикоагулянтов) препаратами выбора являются так называемые ингибиторы ЦОГ-2 – мелоксикам (мовалис), целекоксиб (целебрекс) и нимесулид. Для профилактики и лечения НПВП-индуцированных поражений ЖКТ следует использовать ингибиторы протонной помпы и мизопростол, но не антагонисты Н2-гистаминовых рецепторов и антациды. Следует помнить, что, хотя ингибиторы ЦОГ-2 существенно реже вызывают поражение ЖКТ, чем стандартные НПВП, на фоне их приема также могут возникать нежелательные явления : симптомы диспепсии, замедление заживления язв желудка и двенадцатиперстной кишки, задержка жидкости, повышение АД. Применять как стандартные НПВП, так и ингибиторы ЦОГ-2 следует с особой осторожностью у пациентов со сниженным внутрисосудистым объемом или отеками, связанными с застойной сердечной недостаточностью, нефротическим синдромом, циррозом печени или при повышении концентрации креатина до уровня более 2,5 мг%.
Лечение низкими ( Поделиться: Tweet
4 комментариев(-ия)
скажите пожалуйста от чево РА
Спасибо затакой подробный ответ!
А где в Новосибирске можно сдать кровь на антиССР?
Отвечает главный специалист по клинической лабораторной диагностике
Главного управления здравоохранения мэрии г. Новосибирска,
кандидат медицинских наук Обухов Александр Васильевич:
Определение в крови антител к цитрулинсодержащему белку или цитруллиновые антитела – современный, эффективный, а главное ранний метод клинической лабораторной диагностики ревматоидного артрита.
Выявление антикератиновых антител (АКА) важно для ранней диагностики ревматоидного артрита. Их присутствие может предшествовать клиническим проявлениям заболевания – в ретроспективных исследованиях на замороженных пробах сыворотки показано, что в четверти случаев АКА можно выявить за 5 лет и менее до дебюта ревматоидного артрита, в 10% случаев – за 5 — 9 лет, в 8% случаев – за 10 и более лет. Этот вид антител может встречаться у пациентов с серонегативным ревматоидным артритом. По сравнению с ревматоидным фактором, для АКА характерна более высокая специфичность (88 — 99%), при более низкой чувствительности (40 — 60%).
Необходимо помнить, что НПВП, а тем более глюкокортикоиды (ГК), могут маскировать диагностически важные клинические признаки РА, поэтому от их назначения до установления точного диагноза лучше воздерживаться. Крайне нежелательно проведение внутрисуставных инъекций ГК, поскольку эта манипуляция на несколько недель, а иногда и месяцев затушевывает клиническую симптоматику и поэтому является одной из наиболее частых причин запоздалой постановки правильного диагноза.
Оценка лабораторных показателей воспаления – СОЭ, С-реактивный белок (СРБ), белковые фракции – имеет второстепенное значение в диагностическом процессе, и отсутствие их изменений не должно препятствовать постановке диагноза. В первые 2-3 месяца величины этих параметров не менее чем у 50% больных не выходят за пределы нормальных значений. Кроме того, изменения острофазовых показателей совершенно неспецифичны для РА.
Гораздо большее значение имеет обнаружение в крови РФ в диагностических титрах. Известно также, что больные, позитивные по РФ, имеют худший прогноз течения заболевания. Однако РФ-фенотип имеет два существенных ограничения. Во-первых, специфичность этого теста для РА является достаточно низкой: РФ обнаруживается примерно у 5% здоровых людей, у 5-25% лиц пожилого возраста, а также у значительного числа больных с хроническими заболеваниями. Так, классический IgM-РФ выявляется у 30-35% больных с системной красной волчанкой и системной склеродермией, 20% больных с дерматомиозитом, узелковым полиартериитом и болезнью Бехтерева, 10-15% больных с псориатическим артритом, болезнью Рейтера, сифилисом, туберкулезом, саркоидозом, хроническим активным гепатитом. При наличии суставного синдрома IgM-РФ-позитивными оказываются 25-50% больных с инфекционным эндокардитом, 45-70% — с первичным билиарным циррозом печени, 20-75% — с гепатитом В или С, 15-65% — с другими вирусными инфекциями, 5-25% — с опухолями. Во-вторых, наличие РФ не является стабильным. Частота выявления РФ существенно зависит от длительности заболевания: в первые 6 месяцев он выявляется лишь у 15-43% больных РА, в последующем часть РФ-негативных пациентов становятся РФ-позитивными. Под влиянием лечения возможна и обратная трансформация.
Указанных ограничений лишен недавно внедренный в клиническую практику новый тест иммуноферментного определения антител к цитруллинсодержащим белкам – производным филаггрина, в котором в качестве антигенной субстанции используется синтетический циклический цитруллинированный пептид (ЦЦП), что значительно повысило эффективность лабораторной диагностики РА на ранних стадиях.
Установлено, что анти-ЦЦП являются более специфичными для РА и, по меньшей мере, так же чувствительны, как традиционный РФ: чувствительность анти-ЦЦП при диагностике РА составляет 70-80%, специфичность – 98-99%. Чувствительность теста для больных с ранним РА колеблется между 40 и 70%. Согласно результатам одного из исследований специфичность анти-ЦЦП при диагностике РА на ранних стадиях составляет 86%, комбинации анти-ЦЦП + СОЭ – 95%, анти-ЦЦП + РФ – 91%, анти-ЦЦП + СРБ – 97%, анти-ЦЦП + полиартикулярная боль – 95%, анти-ЦЦП + утренняя скованность – 99%. При этом на момент обследования только 27% больных соответствовали диагностическим критериям ACR. Показано, что наличие этих антител предвещает развитие РА у здоровых на момент обследования людей и прогрессию недифференцированного артрита в РА.
В крупномасштабных клинических исследованиях установлено, что анти-ЦЦП-статус остается стабильным по меньшей мере в течение первых 3-5 лет РА. Наличие анти-ЦЦП на момент установления диагноза предвещает более агрессивное течение заболевания и более выраженное рентгенологическое прогрессирование, несмотря на проводимую терапию. Последующие колебания уровня этих АТ не отражают изменения активности заболевания. Ни НПВП, ни ГК, ни большинство базисных препаратов не влияют на уровень анти-ЦЦП. Следовательно, в клинической практике определение анти-ЦЦП имеет важное значение не только в ранней диагностике РА, но и в планировании терапевтической стратегии. Однако для контроля эффективности лечения данный тест не пригоден.
Таким образом, анти-ЦЦП и РФ являются наиболее важными лабораторными параметрами в диагностике РА на ранних стадиях. При решении вопроса о целесообразности одновременного или последовательного назначения больному этих тестов необходимо учитывать следующее. До 90% анти-ЦЦП(+) больных являются также позитивными по РФ, а одновременное присутствие обеих разновидностей антител не является более специфичным для РА, чем каждый из этих показателей в отдельности. Как уже упоминалось, РФ — достаточно чувствительный, но относительно неспецифичный маркер РА. Поэтому на ранних стадиях заболевания диагностическое значение имеют только высокие титры РФ. Например, если согласно методике РФ определяется как позитивный при значениях >20 Ед/мл, то высокими титрами считаются величины ≥50 Ед/мл. Кроме того, анти-ЦЦП и высокие титры РФ имеют примерно одинаковое прогностическое значение в плане агрессивного, с быстрым рентгенологическим прогрессированием течения заболевания.
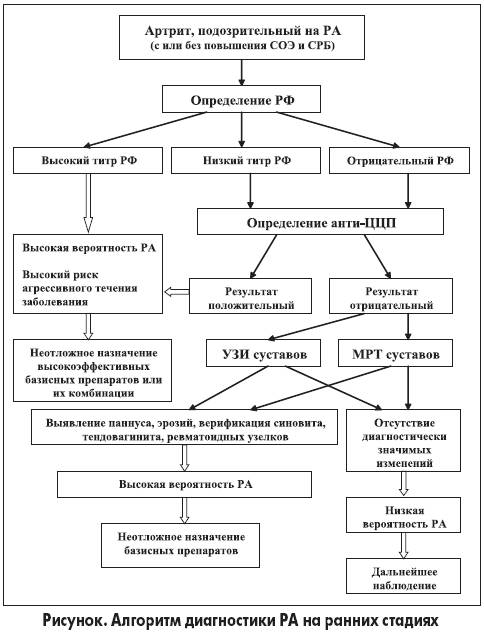
Из вышеизложенного вытекает, что дополнительное определение анти-ЦЦП у больных с высокими титрами РФ с учетом экономических соображений нецелесообразно, поскольку не позволяет получить новую диагностическую и прогностическую информацию. В то же время при низких титрах РФ или у РФ-негативных пациентов такое исследование является исключительно полезным. Этот подход отражен в предлагаемом алгоритме диагностики РА на ранних стадиях (рис.).
Расскажите пожалуйста о месте исследования в диагносике РА крови на Антитела к цитрулинсодержащему белку, или порекомендуйте источник, где можнооб этом почитать.
Читайте также:


