Беэр с а биология возбудителя описторхоза
Долгое время возбудитель описторхоза – широко распространенного паразитического заболевания, вызванного потреблением инфицированной рыбы, изучался главным образом медиками и паразитологами. Однако современные молекулярно-генетические методы в сочетании с биоинформационными подходами позволяют получить принципиально новые данные о биологии и структурно-функциональной организации генома этого паразита, в том числе определить молекулярные основы его патогенной и канцерогенной активности. Это открывает широкие перспективы для разработки новых методов профилактики и лечения описторхоза
Описторхоз – это тяжелое паразитическое заболевание, с очаговым характером распространения, которое вызывается печеночными сосальщиками. Эти паразитические трематоды (иначе – плоские черви) принадлежат к семейству Opishtorchiidae. Интерес к описторхозу не случаен – он продиктован высокой социальной значимостью этого заболевания для нашей страны, особенно для Западной Сибири.
Здесь, в Обь-Иртышском речном бассейне, еще в 1929 г. был обнаружен крупнейший природный очаг описторхоза. И за прошедшие десятилетия эпидемиологическая ситуация ничуть не улучшилась: по данным Роспотребнадзора, в 2010 г. в нижнем течении Иртыша и среднем течении Оби было заражено до 90—95 % сельского населения, в том числе дети дошкольного возраста. Показатели заболеваемости в разных населенных пунктах этого очага превышают общероссийские в 3—28 раз (О санитарно-эпидемиологической обстановке…, 2008 г.).
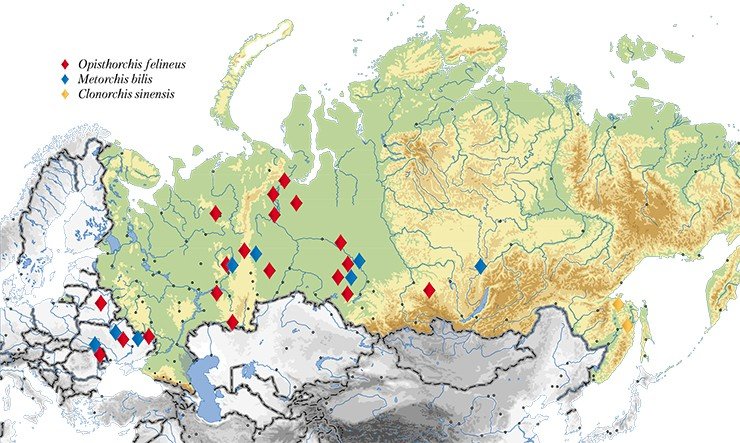
Учитывая широкую географию распространения паразита, для специалистов представляет несомненный интерес выяснить, существуют ли генетические различия, характеризующие популяции из разобщенных зон его ареала. Эти, с первого взгляда, сугубо теоретические исследования имеют и выраженный прикладной аспект. Поскольку именно генетические отличия между паразитами могут обусловливать такие значимые медицинские характеристики, как разнообразие клинических проявлений заболевания, разную вероятность формирования лекарственной устойчивости у паразита, а также его различную иммуногенность (способность вызывать наработку специфических антител). Все эти сведения будут полезны для прогнозирования течения заболевания и формирования иммунного ответа у зараженного человека, а также для разработки диагностических средств и создания вакцин.
Именно такое комплексное исследование проблемы описторхоза и его возбудителей проводится с 2005 г. в Институте цитологии и генетики СО РАН (Новосибирск). Работа по анализу популяционно-генетической структуры гельминтов началась с формирования уникальной коллекции описторхов из разных географических зон – Западной Сибири, европейской части России и Северного Казахстана. На сегодня в ней представлено около 300 образцов Opisthorchis felineus – основного возбудителя описторхоза в нашей стране, и около 300 других видов описторхид, включая эпидемиологически значимые.
Метод как основа
Для оценки генетического разнообразия гельминтов из разных мест обитания был использован метод сравнительного анализа геномных маркеров, в качестве которых выступают фрагменты ДНК. Этот метод, широко использующийся в современной молекулярной биологии, позволяет достаточно надежно судить о степени родства как отдельных индивидов, так и их групп. Поэтому его используют для определения близкородственных видов и реконструкции их эволюционной истории.
10 –8 —10 –12 на клетку за поколение. Поэтому в качестве геномных маркеров выбирают участки генома с высокой скоростью накопления мутаций, а это характерно для тех из них, которые по тем или иным причинам не попадают под действие отбора, т. е. селективно нейтральны.
Этому требованию отвечают не кодирующие белок последовательности ядерной ДНК, а также собственная ДНК клеточных органелл – митохондрий. Последняя наследуется строго по материнской линии с цитоплазмой яйцеклетки и не участвует в рекомбинационном процессе (обмене участками хромосом при клеточном делении). Скорость накопления нейтральных мутаций в митохондриальных генах в 5—10 раз выше, чем в генах ядерной ДНК.

Принято считать, что число накопленных однонуклеотидных замен в селективно нейтральных участках ДНК линейно зависит от времени. Следовательно, произведя подсчеты этих замен, можно получить приблизительную датировку эволюционных событий.
В результате было найдено восемь подходящих генетических маркеров, из них три (два митохондриальных и один ядерный) были выбраны для генотипирования коллекционных образцов описторхид. Нужно добавить, что хотя в последнее десятилетие аналогичные маркеры использовались при исследованиях популяционной структуры и филогеографии других паразитических трематод в Европе, Восточной и Юго-Восточной Азии, Африке, и Америке, исследования такого рода в отношении O. felineus ранее не проводились.
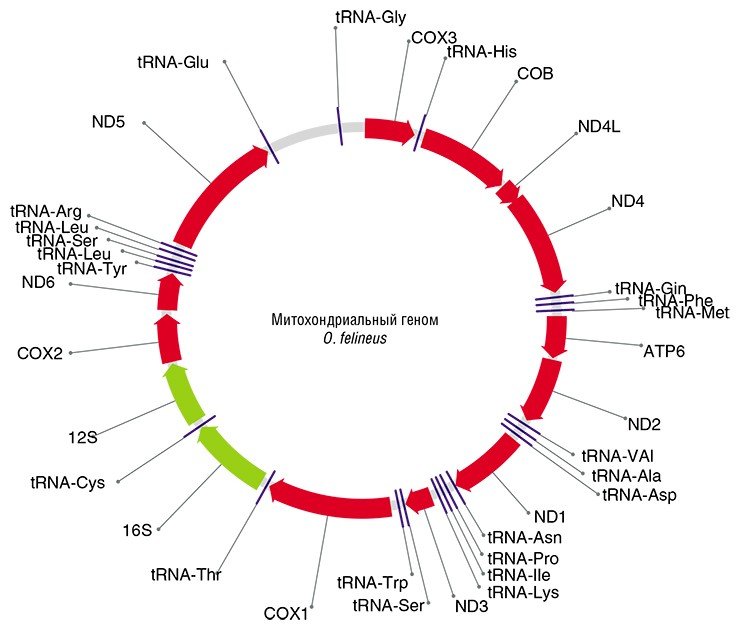
Последующая эволюционная история O. felineus, по-видимому, была весьма драматичной. Дело в том, что ранее было высказано предположение о существовании трех подвидов описторха – сибирского, казахского и восточно-европейского, обитающих соответственно в Обь-Иртышском и Енисейском, Нура-Сарысукском, Волжском, Донском и Уральском речных бассейнах (Беэр, 2005). Поэтому ожидалось, что коллекционные образцы из столь разнесенных в пространстве популяций продемонстрируют заметные генетические различия, поскольку экологически условия обитания также значительно разнятся. Но вопреки предположениям исследованные выборки описторхов характеризовались крайне низким генетическим разнообразием, в отличие от других уже изученных видов трематод (Брусенцов и др., неопубликованные данные).
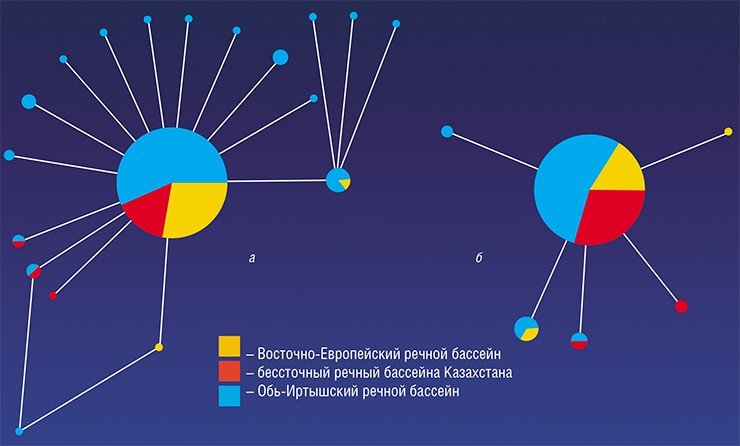
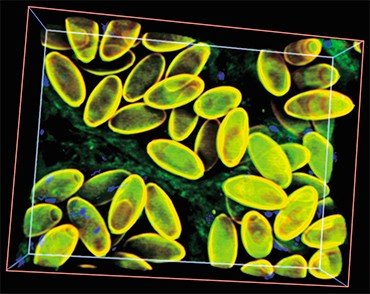
С наступлением потепления и формированием новых речных бассейнов последовало восстановление численности предковой популяции. Согласно расчетам, 21—25 тыс. лет назад в истории вида начался (и продолжается до сих пор) период демографического взрыва, которому, вероятно, в немалой степени способствовал факультативно гермафродитный способ размножения описторха.
К сожалению, проведенное исследование не дает возможности точно указать локализацию предковой популяции и проследить пути расселения паразита. Но, учитывая сложный жизненный цикл O. felineus, представляется очевидным, что направление и скорость его экспансии определялись миграционными способностями его хозяев. Тот факт, что описторхоз сегодня распространен только в некоторых географических зонах, во многом обусловлен средовыми предпочтениями его первого промежуточного хозяина – пресноводных моллюсков битиний, которые в морской воде погибают. Однако одним из окончательных хозяев описторха является человек, для которого географические изолирующие барьеры практически отсутствуют.
В одной пробирке
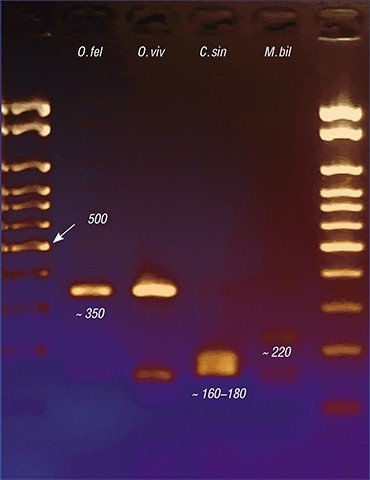
С помощью метода генетических маркеров удалось решить и актуальную медицинскую задачу точной видовой идентификации описторхид. Дело в том, что, наряду с описторхом, в России, а также в Казахстане и странах Восточной Европы встречается еще один эпидемиологически значимый вид – меторх (Мetorchis bilis). А на Дальнем Востоке – еще и клонорх (C. sinensis), о котором упоминалось выше, обычный для стран Юго-Восточной Азии.
Все эти трематоды вызывают заболевания с очень сходной клинической картиной, поэтому на основе одних лишь симптомов врач не может поставить точный диагноз. Под микроскопом же яйца этих гельминтов практически неразличимы между собой, так что результат микроскопического анализа фекалий или содержимого двенадцатиперстной кишки, взятого при дуоденальном зондировании, во многом зависит от квалификации лаборанта. Ситуацию усугубляет возможность одновременного заражения разными видами описторхид.
Сегодня наиболее точной является ДНК-диагностика трематодозов. За рубежом такие эффективные тест-системы начали интенсивно разрабатываться еще в 1990-е гг. Российские ученые начали подобную работу позже, но в последние годы и у нас, в частности в ИЦиГ СО РАН, активно идет процесс создания ПЦР-дигностикумов, с помощью которых можно выявлять в лабораторном материале генетические фрагменты, строго специфичные для определенного вида возбудителя. Поскольку метод позволяет использовать одновременно генетические маркеры на разных гельминтов, для точной диагностики паразитических агентов достаточно одного анализа.
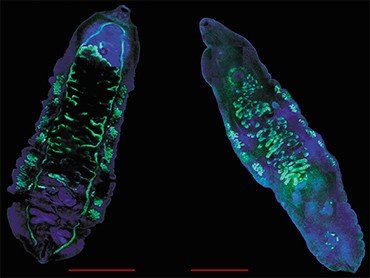
Установление вида паразита может иметь большое значение. Например, оно позволяет определить источник и место заражения. Но самое главное – возбудители описторхоза – меторхоза и клонорхоза различаются по ряду биологических характеристик, что может влиять на течение и прогноз заболевания, возникновение осложнений и степень чувствительности паразитов к лекарственным препаратам.
Так, недавно в эксперименте на золотистых хомячках было показано, что два вида описторхид – наш O. felineus и O. viverrini, встречающийся в странах Юго-Восточной Азии, различаются по агрессивности воздействия на организм хозяина (Lvova et al., 2012). Кстати сказать, в той же Юго-Восточной Азии помимо высокопатогенной O. viverrini широко распространена еще одна похожая трематода – Haplorchis taichui, заражение которой не вызывает тяжелого заболевания (Lovis et al., 2009). Этот пример показывает, насколько важна дифференциальная диагностика трематодозов для назначения адекватного лечения.
Кроме того, даже при низкой степени зараженности хроническая инвазия описторхидами может приводить к серьезным последствиям для здоровья. Однако, как правило, врачи бессильны обнаружить яйца описторхид в лабораторном материале таких пациентов с помощью обычной световой микроскопии, и диагноз зачастую ставится только посмертно (Müller et al., 2007). ПЦР-диагностика же является в этом случае гораздо более чувствительным методом.
Итак, несмотря на свою драматическую эволюционную историю, паразитическая трематода O. felineus не только выжила, но, даже потеряв часть своего генофонда, сегодня является весьма процветающим видом с высокими адаптационными способностями, в том числе высокой инвазионностью – способностью внедряться в организм хозяина.
Разработанные новосибирскими учеными наборы для ПЦР-диагностики описторхоза прошли стадию лабораторных испытаний, сейчас завершается их тестирование на клиническом материале. С их помощью уже удалось успешно выявить у группы пациентов случаи смешанных трематодных инвазий (Brusentsov et al., 2010), что, несомненно, говорит о необходимости их включения в арсенал методов лабораторной диагностики описторхоза. Ведется разработка производственной технологии выпуска диагностикумов.
Повысить точность ИФА можно путем клонирования генов, кодирующих специфичные для описторха антигены. В ИЦиГ СО РАН уже получены такие генно-инженерные белки-антигены О.felineus, пригодные для создания диагностикумов нового поколения. Их можно использовать для детекции даже незначительного количества специфических антипаразитарных антител в сыворотке крови. Однако в медицинскую практику такие ИФА-диагностикумы поступят еще не скоро.
Внедрение новых диагностических технологий, несомненно, повлияет на качество лечения и продолжительность реабилитации пациентов. Этому есть много примеров, наиболее яркие из которых связаны с диагностикой бактериальных инфекций, перешедшей из чашек Петри в пробирки для ПЦР. Новые технологии не отменят традиционные, но позволят намного повысить чувствительность и точность анализов, особенно в сложных клинических случаях.
Юрлова Н. И. Обская болезнь описторхоз // Наука из первых рук. 2008. №2 (20). С. 12—21.
Пальцев А. И. Системному заболеванию – системный подход // Наука из первых рук. 2008. №2 (20). C. 22—27.
Колчанов Н. А., Мордвинов В. А. Паразитоз от А до Т // Наука из первых рук. 2008. №2 (20). C. 28—41.
Беэр С. А. Биология возбудителя описторхоза. КМК, 2005. 336 с.
Брусенцов И. И., Катохин А. В., Сахаровская З. В. и др. ДНК-диагностика микст-инвазий Opisthorchis felineus и Metorchis bilis с помощью метода ПЦР // Медицинская паразитология и паразитарные болезни. 2010. № 2. С.10—13.
Федеральный исследовательский центр Институт цитологии и генетики Сибирского отделения РАН
630090, Россия, Новосибирск, проспект акад. Лаврентьева, 10
Описторхоз – инфекционное заболевание, возникающее при попадании личинок трематод семейства Opisthorchiidae в желудочно-кишечный тракт млекопитающих. Основным возбудителем описторхоза в Европе и РФ является представитель данного семейства – кошачья двуустка, Opisthorchis felineus (O. felineus).
В настоящее время описторхоз рассматривают как системное заболевание, при котором страдает не только печень, основное место локализации паразитов, и другие органы и системы, в том числе центральная нервная. Поэтому актуально исследование этой паразитарной инфекции и моделирование описторхоза на лабораторных животных.
На самцах мышей линии C57BL/6J моделировали хронический описторхоз при однократном и двукратном инфицировании животных метацеркариями трематоды O. felineus, полученными из инфицированных язей, выловленных из реки Обь в Новосибирской области. Все эксперименты проводили в SPF-виварии. Сравнивали 3 группы животных: 1-я – контрольные неинфицированные (n=10); 2-я – однократно инфицированные личинками O. felineus (n=12); 3-я – повторно инфицированные через 3 мес после 1-й инвазии (n=18).
Введение личинок осуществляли внутрижелудочно с помощью специализированных зондов. Через 6 мес от начала эксперимента было обнаружено большее количество гельминтов в печени мышей после двукратного инфицирования по сравнению с однократным. Причем увеличение числа гельминтов отмечено за счет неполовозрелых форм паразита, при этом размер половозрелых форм O. felineus варьировал от 1,5 до 3 мм.
На фоне двукратного инфицирования установлено усиление негативного воздействия гельминтов на физиологическое состояние хозяина паразита. У этих животных наблюдалась повышенная активность фермента аланинаминотрансферазы (АЛТ) в сыворотке крови, основного маркера воспалительных процессов в печени. Кроме того, у мышей снижалась масса тела к концу эксперимента и наблюдалась гепатоспленомегалия. При однократном инфицировании увеличения весовых индексов печени и селезенки были менее выраженными, а активность АЛТ не отличалась от контрольных значений.
Следовательно, мыши линии C57BL/6J могут быть использованы для моделирования описторхоза в лабораторных условиях, причем двойное инфицирование оказывает более выраженное негативное воздействие на организм хозяина.
Описторхоз — инфекционное заболевание, возникающее при попадании личинок трематод семейства Opisthorchiidae в желудочно-кишечный тракт млекопитающих. Инфицирование происходит при поедании недостаточно термически обработанной рыбы из семейства карповых (Cyprinidae), которая является носителем метацеркарий — личинок этого опасного для человека паразита. Основной возбудитель описторхоза в Европе и России — представитель данного семейства — кошачья двуустка, Opisthorchis felineus (O. felineus). В качестве дефинитивного хозяина O. felineus, кроме человека, зарегистрировано 33 вида рыбоядных млекопитающих [1]. Самый крупный очаг O. felineus-индуцированного описторхоза находится в Обь-Иртышском бассейне. Степень зараженности населения в прибрежных областях рек Обь и Иртыш, охватывающих 14 регионов РФ и 4 региона Казахстана с населением приблизительно 15 млн человек, равна 500 человек на 100 000 населения, при этом в некоторых сельских районах средней части реки Обь эта величина достигает 100% [2, 3].
Внедряясь в желчные протоки печени, личинки O. felineus способствуют развитию заболеваний, прежде всего печени. На фоне хронического описторхоза развиваются такие заболевания, как холангит, холангиохолецистит, холангиогепатит, холангитический цирроз печени [4]. Отмечают связь между описторхозом, вызванным O. felineus, и опухолями в печени [5, 6]. Кроме того, описторхоз рассматривают как системное заболевание, при котором происходят нарушения в других органах и системах организма, вплоть до центральной нервной системы (ЦНС) [7].
Актуальность исследования особенностей инвазии паразита и системных изменений в организме хозяина после заражения O. felineus обусловлена продолжающимся поиском эффективной терапии этого заболевания. Однако проведение этих исследований требует удобных, дешевых и легко воспроизводимых моделей описторхоза. Чаще всего описторхоз моделируют на сирийских хомячках, что объясняется лучшей приживаемостью описторхид у этих животных. Иногда исследования проводят на других представителях млекопитающих (лисицах, песчанках, крысах), еще реже используют мышей, хотя в природных популяциях гельминт O. felineus обнаруживается у разных мышеобразных грызунов (водяная и европейская рыжая полевка, малая лесная, желтогорлая, полевая и домовая мыши) [8]. Обнаружена равная степень заражения личинками O. felineus у сирийских хомячков и мышей линии C57BL/6 на острой стадии (2 нед) экспериментального описторхоза [9], тогда через 6 мес после инфицирования наблюдаются значительные межвидовые различия по количеству паразитов в желчных протоках печени. При равной дозе инфицирования (100 метацеркарий на 1 животное) у хомячков отмечалось 32,0±2,0 паразитов [10], тогда как у мышей только 10,9±4,0 [11]. Однако учитывая разницу в массе печени у инфицированных животных (около 2 г – у мышей и 6,5–7 г – у хомячков), паразитарная нагрузка (количество паразитов на 1 г печени) у 2 видов животных оказалась сопоставимой. На основании этих данных было высказано предположение, что мыши линии C57BL/6J также могут быть использованы для моделирования описторхоза в лабораторных условиях.
Поскольку в природных популяциях инфицирование млекопитающих происходит зачастую многократно, в нашей работе исследовали эффективность инфицирования и развитие паразитов при однократном и двукратном введении личинок трематоды O. felineus мышам линии C57BL/6J. При этом планировали оценить не только степень инфицирования животных, но и их состояние по ряду физиологических показателей, поскольку известно, что кратность заражения во многих случаях коррелирует со степенью проявления патологических признаков у хозяина паразита [12].
Получение метацеркарий O. felineus. Личинки O. felineus были получены из инфицированных язей, выловленных из реки Обь в Новосибирской области. Рыбный фарш подвергали ферментативной обработке (11 мл концентрированной HCl + 7 г пепсина на 1 л воды) и инкубировали при температуре 37°C в течение ночи с последующей фильтрацией и осаждением в 0,9% растворе хлористого натрия. Под микроскопом определяли жизнеспособность отобранных метацеркарий для дальнейшего внутрижелудочного введения животным.
Процедура эксперимента. Животные были разделены на 3 группы: 1-я – контрольные (неинфицированные) животные (n=10); 2-я – однократно инфицированные личинками гельминтов O. felineus в дозе 90 метацеркарий на каждую особь (n=12); 3-я – повторно инфицированные через 3 мес после 1-го введения личинок паразита (n=18). Введение личинок осуществляли внутрижелудочно с помощью зондов (Braintree Scientific, Inc.). Через 6 мес от начала эксперимента всех мышей умерщвляли декапитацией и производили забор крови для дальнейшего биохимического исследования. Кроме этого, определяли массу печени и селезенки, которую далее пересчитывали на 1 г массы тела. Печень с желчным пузырем помещали в физиологический раствор для подсчета в дальнейшем числа марит O. felineus, извлеченных из желчных протоков. Состояние зрелости гельминтов определяли, используя микроскоп Altami CM0745 при 10 – 40-кратном увеличении.
Статистика. Все показатели оценивали с помощью однофакторного дисперсионного анализа с последующим post hoc сравнением групп по критерию Fisher LSD, используя пакет программ Statistica 6.0. Корреляции между показателями в группах определяли непараметрическим анализом по Спирмену (Spearman rank correlation coefficient). Данные представлены как среднее ±SEM. Различия считались статистически значимыми при p 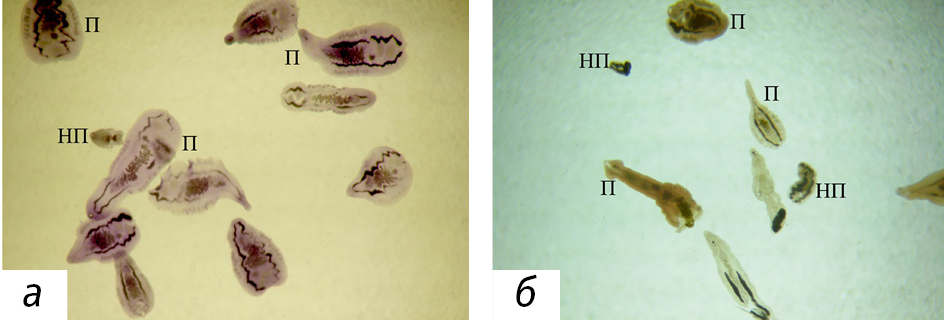
Рис. 1. Мариты‚ выделенные из желчных протоков печени мышей через 6 мес после однократного (а) и двукратного (б) инфицирования личинками трематоды O. felineus. У половозрелых марит (П) видна продукция яиц‚ у неполовозрелых (НП) – только 2 ветви кишечника
Таким образом, можно предположить, при каждом последующем инфицировании мышей время созревания паразитов увеличивается. Подсчет всех гельминтов показал, через 6 мес после однократного инфицирования в печени мышей присутствовали преимущественно взрослые мариты O. felineus (рис. 2). При повторном инфицировании через 3 мес после первого число мелких неполовозрелых марит в печени мышей было больше, чем после однократного (p 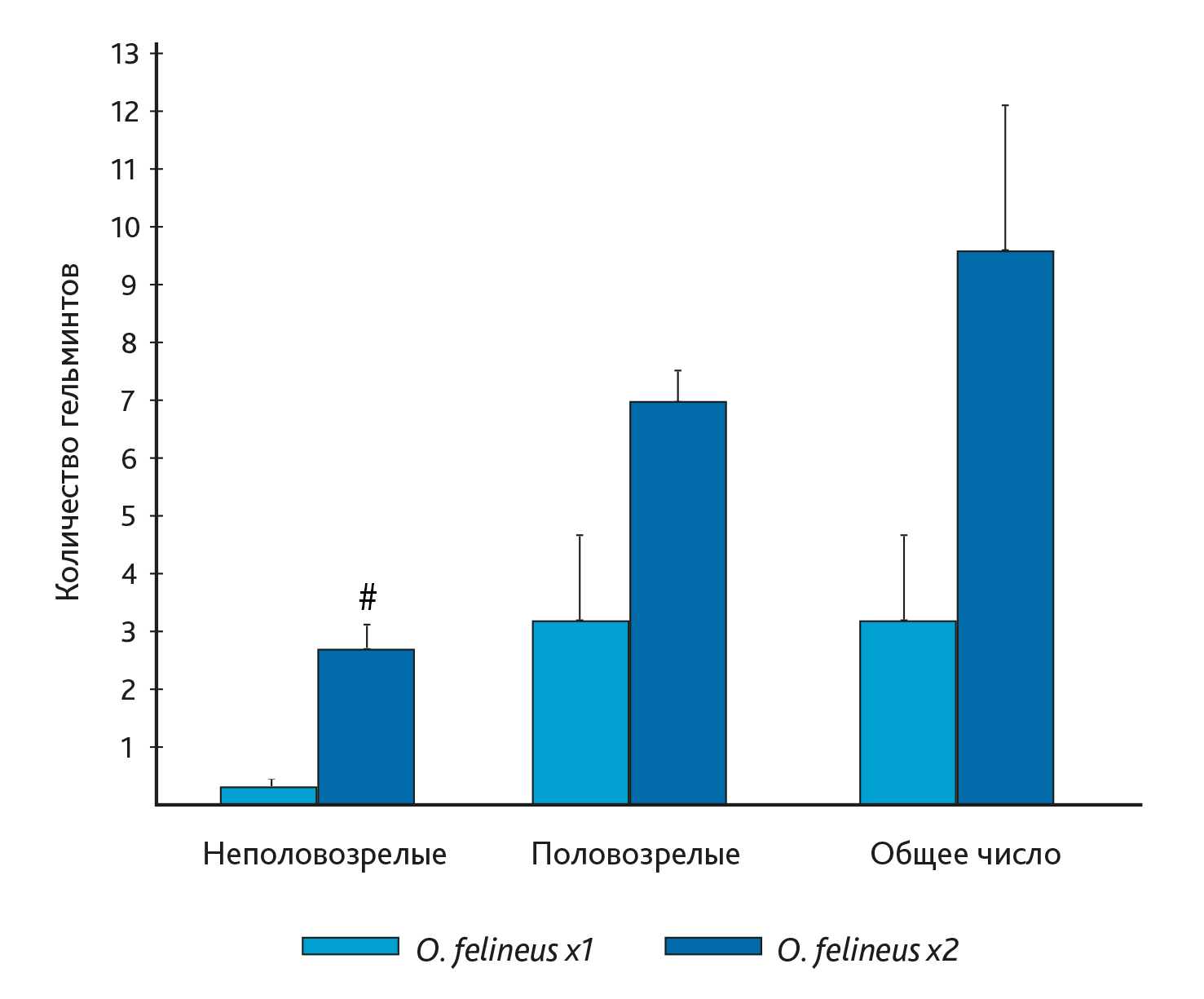
Примечание: # p Рис. 2. Количество гельминтов O. felineus разной степени зрелости‚ выделенные из желчных протоков печени мышей через 6 мес после однократного (х1) и двукратного (х2) инфицирования.
Примечание: # p
Согласно полученным данным можно заключить, что у мышей для созревания гельминтов требуется более 3 мес, причем повторное инфицирование животных увеличивает срок созревания вновь внедрившихся паразитов. Это отличает мышей от хомячков, у которых уже через 2 нед после инфицирования личинками O. felineus все мариты были половозрелыми [9]. Видимо, этим объясняется то, что при моделировании описторхоза в лабораторных условиях чаще всего используют сирийских хомячков и лишь в единичных случаях – мышей [14, 15]. Учитывая, что мыши – всеядные животные, а хомячки питаются преимущественно растительной пищей, не рыбой, которая является промежуточным хозяином для описторхид, можно предположить, что у мышей эволюционно выработались механизмы устойчивости против трематодных инфекций. Следует подчеркнуть, что выявление этих механизмов сопротивления трематодным инфекциям – не менее важная задача, чем изучение механизмов повышенной чувствительности к заражению. Оба этих направления исследования в равной степени актуальны в борьбе с описторхозной патологией у людей и животных. Возможно, устойчивость к инфекции O. felineus связана с высоким уровнем иммунной защиты у мышей. Так, по сравнению с сирийскими хомячками, у мышей C57BL/6J в крови значительно выше уровень лимфоцитов [9], главных клеток, осуществляющих контроль и иммунную защиту организма при инфекциях. Кроме того, у них почти в 2 раза больше относительная масса селезенки [9], основного органа периферической иммунной системы, в котором происходит пролиферация и дифференцировка T- и B-лимфоцитов крови. Как показали наши результаты, масса селезенки возрастает значительно на фоне инфицирования O. felineus у мышей обеих групп, причем в большей степени при двукратном инфицировании (рис. 3). При этом в обеих группах инфицированных животных относительные массы печени и селезенки коррелировали с общим число паразитов, извлеченных из печени (при однократном инфицировании: r=0,86, p=0,001 и r=0,73, p=0,011 соответственно; при двукратном инфицировании r=0,61, p=0,009 и r=0,71, p=0,001 соответственно). Учитывая то, что у мышей с двойным инфицированием снижалась масса тела и увеличивалась относительная масса печени и селезенки, можно говорить о более тяжелых последствиях повторного инфицирования личинками трематоды O. felineus у мышей C57BL/6J.
Результаты биохимических исследований подтверждают это предположение. Установлено, что у мышей после двукратного инфицирования повышается активность фермента АЛТ – главного маркера различных заболеваний печени (рис. 4). Поскольку этот показатель статистически значимо коррелировал с числом гельминтов как при однократном (r=0,81, p=0,004), так и при двукратном (r=0,66, p=0,015) инфицировании животных, можно говорить, что изменение этого показателя обусловлено развитием экспериментального описторхоза. Повышенный уровень активности другого фермента – АСТ – был обнаружен у мышей через 6 мес после однократного инфицирования, при двукратном инфицировании значение этого показателя было средним между показателем в контрольной группе мышей и у мышей с однократным инфицированием. Поскольку корреляционной связи между активностью АСТ и общим числом паразитов в печени в обоих случаях инфицирования не установлено (r=0,04, p=0,919 – при однократном и r=0,14, p=0,636 – при двукратном инфицировании), можно полагать, что АСТ в меньшей степени, чем АЛТ, отражает развитие патологического процесса. Тем более, что и в процентном отношении повышение уровня АЛТ при однократном и двукратном инфицировании было более выраженным (на 40 и 103% соответственно), чем повышение АСТ (на 25 и 11% соответственно). Фермент АЛТ находится в цитоплазме гепатоцитов, а АСТ является митохондриально-цитоплазматическим ферментом с выраженным преобладанием в митохондриях [16]. Повышение АСТ в крови свидетельствует о поражении преимущественно митохондрий, а повышение АЛТ – о более глубоких нарушениях в клетке, связанных с нарушением целостности плазматических мембран гепатоцитов. Таким образом, полученные биохимические данные свидетельствуют о более значимых нарушениях в печени у мышей на фоне двукратного инфицирования трематодой O. felineus, чем и обусловлена гибель гепатоцитов.
У людей хронический описторхоз приводит к изменению системы взаимодействий изучаемых биохимических показателей, в том числе обнаруживается значимая связь между активностью АЛТ и АСТ [17]. В нашем исследовании была получена высокая корреляционная связь между активностью 2 ферментов у мышей при двукратном инфицировании (r=0,57, p=0,041), тогда как у контрольных особей и у животных с однократным инфицированием таких значимых корреляций не обнаружено (r=-0,29, p=0,492 и r=0,20, p=0,580 соответственно). Это также свидетельствует о более выраженном развитии патологического процесса у мышей после двукратного инфицирования.
Как показали результаты проведенного исследования, мыши линии C57BL/6J, наравне с сирийскими хомячками, являются хорошим лабораторным объектом при моделировании O. felineus-вызванного описторхоза. Через 3 мес после инфицирования в желчных протоках печени животных обнаружены половозрелые и неполовозрелые мариты паразита. Повторное инфицирование мышей спустя 3 мес после 1-го увеличивало их количество преимущественно за счет числа неполовозрелых особей O. felineus. Двойное инфицирование оказывало более выраженное негативное воздействие на организм хозяина и сопровождалось повышением активности фермента АЛТ – основного маркера воспаления в печени. Кроме того, дважды инфицированные мыши характеризовались более выраженным снижением массы тела и увеличением весового индекса печени и селезенки, что является признаками описторхоза. Считаем, что мыши линии C57BL/6J могут быть использованы для исследования механизмов развития описторхоза, а также для преклинических исследований эффективности новых антигельминтных препаратов.
Работа выполнена при финансовой поддержке РФФИ (грант №17-04-00790) и бюджетного проекта ФИЦ ИЦиГ СО РАН (№0324-2019-0041). Исследования проведены с использованием оборудования Центра генетических ресурсов лабораторных животных ФИЦ ИЦиГ СО РАН, поддержанного Минобрнауки России (Уникальный идентификатор проекта RFMEFI62117X0015).
Читайте также:


