Когда начинают развиваться основные признаки интоксикации при синдроме длительного сдавливания
Ксения Скрыпник о синдроме длительного сдавления, который встречается у пострадавших во время боевых действий, при обвалах, землетрясениях, терактах, ДТП
Байуотерсу удалось выявить три последовательные стадии, приводящие к развитию краш-синдрома:
- сдавливание конечности и последующий некроз тканей;
- развитие отека в месте сдавливания;
- развитие острой почечной недостаточности и ишемического токсикоза.
Патогенез
Синдром Байуотерса возникает в результате сдавливания конечности, повреждения основных сосудов и магистральных нервов. Подобная травма встречается примерно у 30% людей, пострадавших в результате природных или техногенных катастроф.
В патогенезе этого заболевания ведущее значение имеют три фактора: регуляторный, связанный с болевым воздействием на организм, существенная плазмопотеря и, наконец, тканевая токсемия. Отметим, что подобные факторы в той или иной степени наблюдаются практически при любой травме, но при краш-синдроме они проявляются особенно ярко. Каждый из этих факторов дает свой вклад в клиническую картину синдрома длительного сдавления.
Болевое воздействие влияет на человека, попавшего под завал, наиболее сильно. Отмечается рефлекторный спазм сосудов периферических органов и тканей, что приводит к нарушению газообмена и последующей гипоксии тканей. Сосудистый спазм и развивающаяся гипоксия вызывают дистрофические изменения эпителия почечных извитых канальцев, существенно падает клубочковая фильтрация.
Плазмопотеря развивается вскоре после травмы и даже после устранения причины сдавливания.
Плазмопотерю связывают с увеличением проницаемости капилляров на фоне травмы, что ведет к выходу плазмы крови из кровяного русла.
Интоксикация организма выражена тем сильнее, чем больше масса сдавленных тканей и длительность компрессионного воздействия.
Степени тяжести краш-синдрома
В зависимости от объёма повреждения и длительности сдавления, выделяют 4 степени тяжести синдрома [2].
Легкая степень – сдавление небольшого сегмента конечности в течение не более чем двух часов. В этом случае токсемия выражена слабо, хотя отмечаются острая почечная недостаточность и нарушения гемодинамики. В большинстве случаев при проведении своевременной терапии улучшение наступает в течение недели.
Средняя степень возникает при сдавлении конечности целиком в течение четырех часов. Подобное состояние характеризуется интоксикацией, миоглобинурией и олигоурией.
Длительная компрессия конечностей (4–7 часов) ведет к проявлению симптомов, характерных для тяжелой степени синдрома Байуотерса. Отмечаются существенные нарушения гемодинамики, выражены симптомы интоксикации, быстро развивается острая почечная недостаточность.
Несвоевременное и неправильное оказание медицинской помощи в большинстве случаев ведет к летальному исходу.
Также важно правильно и быстро действовать, если у пациента диагностирована крайне тяжелая степень краш-синдрома. Такой диагноз ставят при сдавлении нижних конечностей в течение 8 и более часов. Развивающийся ишемический токсикоз окажется губительным для пациента вскоре после проведенной декомпрессии. Смертность таких больных крайне высока даже при проведении своевременного лечения.
Лечение
Выбор подхода к лечению начинают с оценки степени компрессии и длительности сдавления конечностей. Для специалистов, принимающих участие в спасательных операциях, важно постараться освободить максимальное число пострадавших в первые два часа после возникновения чрезвычайной ситуации. Именно в этом случае прогноз окажется благоприятным для большинства пациентов.
Во время землетрясения в Мармаре (Турция), произошедшего в 1999 году, пострадало много детей. Тогда был накоплен колоссальный опыт по устранению последствий компрессионной травмы у маленьких пациентов. Специфика лечения синдрома Байуотерса у детей обусловлена тем, что их травмы зачастую оказываются гораздо тяжелее, чем у взрослых [3].
С детьми сложнее коммуницировать в процессе спасательной операции, поэтому часто они проводят под завалами больше времени, чем взрослые. Детский организм в большей степени подвержен переохлаждению и потере жидкости, так что следует особое внимание уделить регидратации сразу же после спасения ребенка.
Вне зависимости от степени тяжести и возраста пациента проводят противошоковые мероприятия: вводят анальгетики, сердечно-сосудистые препараты для нормализации артериального давления. В большинстве случаев это делают еще до извлечения пострадавшего из-под завала.
Лечение, начатое еще до удаления пресса, дает возможность избежать развития ишемического токсикоза. В первую очередь это касается обширных компрессионных травм.
Соблюдение последовательности этапов лечения пациентов с компрессионными травмами очень важно. Своевременное использование инфузионной терапии, понимание патогенеза синдрома Байоутерса существенно увеличивает количество спасенных жизней.
При легкой степени синдрома хирургического лечения не проводят, нередко такие больные лечатся амбулаторно. При средней степени тяжести нарушения гемодинамики выражены достаточно ярко: отек нарастает, нарушается микроциркуляция, увеличивается количество микротромбозов, однако хирургическое лечение и в этом случае показано не всегда. Рекомендована инфузионная терапия, которая позволяет не допустить развития или же прогрессирования острой почечной недостаточности.
В случаях тяжелой и крайне тяжелой степени выраженности краш-синдрома консервативное лечение неэффективно, и необходимо хирургическое лечение. Проводят фасциотомию поврежденной конечности, которая способствует восстановлению кровообращения и дает возможность избежать полной некротизации конечности. Нередко приходится ампутировать дистальные отделы конечностей, чтобы спасти пациента.
Параллельно проводится терапия острой почечной недостаточности – назначается строгий питьевой режим, гемодиализ, плазмоферез и инфузионная терапия (введение растворов глюкозы, альбумина и т.п.).
В реабилитационном периоде следует уделять внимание физиопроцедурам (например, массажу) и лечебной физкультуре, которые способствуют более эффективному восстановлению конечности, минимизируя атрофию мышц и нервов.
Случай из практики
В результате автомобильной катастрофы 21-летний молодой мужчина провел 10 часов, будучи зажатым в поврежденном автомобиле. Он был доставлен в больницу города Низва (Оман), находясь в полном сознании [4]. Осмотр показал, что грудная клетка, брюшная полость, спина и таз не были повреждены. В то же время наблюдался отек правого плеча, правая верхняя конечность была обездвижена. Рентгеновское исследование выявило перелом правой ключицы.
Также отмечался отек правой нижней конечности, кожный покров поврежден не был. На левой ноге был диффузный отек, затрагивавший голень и бедро, а также глубокие ссадины. Обе ноги были практически неподвижны в голеностопных суставах, отмечались нарушения чувствительности в области голеней. Допплерографическое исследование показало нарушение венозного кровотока в стопе и голени. Дальнейшее наблюдение выявило быстрое накопление креатинина, миоглобина, калия в сыворотке крови, а также миоглобинурию.
Проводилась инфузионная терапия: физиологический раствор, глюкоза, бикарбонат натрия. Несмотря на это у пациента развилась анурия, а уровень калия в крови продолжал повышаться. Пострадавшему назначили гемодиализ и провели фасциотомию левого бедра и голени, в результате которой обнаружили, что часть бедренных мышц некротизирована. На 7-й день лечения в мазке из раны были обнаружены грамотрицательные бактерии – E.coli и бактерии рода Proteus. Пациенту назначили адекватную антибиотикотерапию, рана регулярно обрабатывалась антисептиками. Состояние пациента прогрессивно ухудшалось. Несмотря на прием антибиотиков, развилась бактериальная септицемия, в связи с чем была рекомендована ампутация левой ноги, от которой пациент и его семья отказались. Ими было принято решение продолжить лечение за границей, где пострадавший скончался от тяжелого сепсиса через три дня после прибытия.
Резюме
Синдром Байуотерса был выделен как нозологическая единица не так давно – лишь в середине 20 века. При спасении и последующем лечении пострадавших с тяжелыми компрессионными травмами важны координированные действия спасателей и врачей. Быстрое извлечение людей из-под завалов и оказание первой помощи еще до удаления пресса минимизирует тяжелые последствия синдрома длительного сдавления конечностей и помогает сохранить жизнь больного.
1.Bywaters EG. Crushing Injury. Br Med J. 1942 Nov 28; Vol.2 No.4273. P.643-6.
2.Рудаев В.И. Кричевский А.Л., Галеев И.К. Краш-синдром в условиях катастроф. - Методические рекомендации для реанимационно-противошоковых групп ВГСЧ, специализированных бригад постоянной готовности Службы медицины катастроф и реанимационных бригад скорой медицинской помощи. 1999.
3.Dario Gonzalez. Crush syndrome. Crit Care Med. 2005. Vol. 33, No. 1 (Suppl.). S.34-41.
4.Dinesh Dhar, TP Varghese. Crush Syndrome Case Report and Literature Review. Macedonian Journal of Medical Sciences. 2010 Sep 15; 3(3):319-323.
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.
Патологическое состояние, развивающееся после длительного сдавления большой массы мягких тканей. Встречается у пострадавших при землетрясениях, завалах в шахтах, обвалах и др . Как правило, синдром длительного сдавления наступает при компрессии, длительность которой свыше 4 ч (иногда меньше), и массе травмированных тканей, превышающей массу верхней конечности.
Наблюдается также синдром позиционной компрессии, или позиционного сдавления, возникающий в результате длительного неподвижного положения тела пострадавшего, находящегося в бессознательном состоянии (кома, отравление и т.п.) или в состоянии глубокого патологического сна. При этом ишемия развивается от сдавления релаксированных тканей массой собственного тела.
Патогенез
Длительное сдавление и травматизация нервных стволов обусловливают патологические нервно-рефлекторные влияния на центральную нервную систему, эндокринную систему, кровообращения, функцию почек. Пусковым фактором многих патофизиологических сдвигов в организме пострадавшего является боль. Плазмопотеря в поврежденных тканях достигает нередко катастрофических размеров. Объем циркулирующей крови в зависимости от продолжительного сдавления может снижаться на 27—52% от исходного уровня. Так, при отеке одной верхней конечности депонируется до 2—3 л, а нижней — до 3—5 л жидкости, в основном плазмы. Наблюдаемую при синдроме длительного сдавливания массивную плазмопотерю некоторые исследователи называют белым кровотечением, которое переносится организмом тяжелее, чем кровопотеря.
Большое значение в развитии синдрома длительного сдавления имеет токсемия. Интоксикация в начальных стадиях синдрома длительного сдавления обусловлена токсическими веществами, образующимися в тканях при их повреждении. В результате длительного сдавления конечности развивается ишемия всей конечности или ее сегмента в сочетании с венозным застоем.
Сдавливаются кровеносные сосуды, нервы и мышцы. Снижается количество кислорода в крови, не выводится углекислота и другие продукты молекулярного распада, которые накапливаются в сдавленной части тела. Как только сдавление тканей прекращается, токсические продукты поступают в кровеносное русло и вызывают тяжелейшую интоксикацию. Ведущими факторами токсемии являются: гиперкалиемия, достигающая нередко 7—12 ммоль/л; миоглобинурия, приводящая к блокаде канальцев почек; увеличение образования биогенных аминов и вазоактивных полипептидов (продуктов распада белков, гистамина, адениловой кислоты, креатинина и др.), а также протеолитических лизосомальных ферментов, освобождающихся при разрушении клеток: развитие аутоиммунного состояния.
В ранних стадиях синдрома длительного сдавления в первую очередь поражаются почки, что проявляется деструкцией эпителия канальцев, стазом и тромбозом как в корковом, так и мозговом веществе. Значительные дистрофические изменения развиваются в почечных канальцах, просветы которых заполняются продуктами распада клеток. Миоглобин и образующийся при гемолизе эритроцитов свободный гемоглобин усиливают ишемию коркового вещества почек, что способствует прогрессированию процесса и развитию острой почечной недостаточности.
Длительное сдавление сегмента конечности, развитие в его тканях кислородного голодания и гипотермии приводят к выраженному тканевому ацидозу. Гипоксия отрицательно влияет на функцию почек, печени, кишечника. Дефицит кислорода ведет к повышению проницаемости кишечной стенки и нарушению ее барьерной функции. Поэтому токсические вещества бактериальной природы свободно
проникают в портальную систему и блокируют элементы системы мононуклеарных фагоцитов печени. Нарушение антитоксической функции печени и ее аноксия способствуют освобождению вазопрессорного фактора — ферритина. Нарушения гемодинамики при этом состоянии связаны не только с образованием вазопрессорных веществ, но и с массивными разрушениями эритроцитов, что ведет к гиперкоагуляции и внутрисосудистому тромбозу.
Клиническая картина
Тяжесть клинических проявлений синдрома длительного сдавления зависит от степени и продолжительности сдавления конечности, объема и глубины поражения, а также от сочетанного повреждения других органов и структур (черепно-мозговой травмы, травмы внутренних органов, костей, суставов, сосудов, нервов и др.
Различают 3 периода синдром длительного сдавления:
I период (начальный) характеризуется локальными изменениями и эндогенной интоксикацией. Он продолжается 2—3 суток после освобождения от сдавления. Типичным является относительно благополучное состояние пострадавших сразу после извлечения из завала. Только через несколько часов возникают местные изменения в сегменте, подвергавшемся сдавлению. Конечность становится
бледной, появляется цианоз пальцев, быстро нарастает отек, кожа приобретает деревянистую плотность. Пульсация периферических сосудов не определяется. С углублением местных изменений ухудшается общее состояние пострадавшего. Преобладают проявления травматического шока: болевой синдром, психоэмоциональный стресс, нестабильность гемодинамики, гемоконцентрация, креатининемия. Состояние пострадавшего может стремительно ухудшаться с развитием острой сердечно-сосудистой недостаточности. Возрастает концентрация фибриногена, повышается толерантность плазмы к гепарину, снижается активность фибринолитической системы, т.е. повышается функция свертывающей системы крови, что ведет к тромбозам (см. Тромбогеморрагический синдром). Моча имеет высокую относительную плотность, в ней появляется белок, эритроциты, цилиндры. В периферической крови отмечаются сгущение, нейтрофильный сдвиг, лимфопения. Плазмопотеря приводит к существенному снижению объема циркулирующей крови и плазмы.
II период (промежуточный) — период острой почечной недостаточности — длится с 3—4-х до 8—12-ти суток. Усиливается отек конечности, подвергшейся сдавливанию, что сопровождается образованием пузырей с прозрачным или геморрагическим содержимым, плотных инфильтратов, локальным, а иногда и тотальным некрозом всей конечности. Гемоконцентрация сменяется гемодилюцией, нарастает анемия, резко снижается диурез, вплоть до анурии. В крови увеличивается содержание остаточного азота, мочевины, креатинина, калия, развивается классическая картина уремии. Повышается температура тела, состояние пострадавшего резко ухудшается, усиливаются вялость и заторможенность, появляются рвота и жажда, иктеричность склер и кожи. Летальность в этом периоде может достигать 35% несмотря на интенсивную терапию.
III период (восстановительный) начинается с 3—4-й недели. В этот период местные изменения преобладают над общими. Функция почек восстанавливается. На первый план выступают инфекционные осложнения открытых повреждений, а также ран после лампасных разрезов и фасциотомий. Возможна генерализация инфекции с развитием сепсиса. В неосложненных случаях отек конечности и боли в ней к концу месяца проходят. У пострадавших длительно сохраняются выраженная анемия, гипопротеинемия, диспротеинемия (гипоальбуминемия, гиперглобулинемия), гиперкоагуляция крови; изменения в моче (белок, цилиндры). Эти изменения являются стойкими и, несмотря на интенсивную инфузионную терапию, имеют тенденцию к нормализации в среднем к концу месяца интенсивного лечения. Выявляется резкое снижение факторов естественной резистентности и иммунологической реактивности. Снижается бактерицидная активность крови, активность лизоцима сыворотки. Длительное время остаются повышенными показатели лейкоцитарного индекса интоксикации, указывающие на наличие аутоиммунного состояния и выраженной интоксикации. У большинства пострадавших долго сохраняются отклонения в эмоционально-психическом статусе в виде депрессивных или реактивных психозов и истерий.
При бактериологическом исследовании у подавляющего большинства пострадавших от землетрясений выявляется высокая степень обсемененности ран клостридиями в ассоциации с энтеробактериями, псевдомонадами и анаэробными кокками. Этим обусловлен высокий риск развития у этих больных клостридиального мионекроза. В результате проводимых лечебных мероприятий раны обычно очищаются от клостридий через 7—10 дней. В более поздние сроки из ран выделяется синегнойная палочка в ассоциации с энтеробактериями, стафилококками и некоторыми другими бактериями.
Лечение
Должно быть комплексным, с соблюдением этапности и преемственности оказания лечебных пособий.
На догоспитальном этапе после освобождения пострадавшего первая помощь на месте происшествия должна включать введение обезболивающих (промедол, омнопон, морфин, анальгин), седативных и антигистаминных средств, при возможности — футлярную новокаиновую блокаду 0,25% раствором новокаина в проксимальном отделе сдавленной конечности, тугое бинтование конечности
эластичным или марлевым бинтом, транспортную иммобилизацию, местную гипотермию в виде обкладывания поврежденной конечности пузырями со льдом. При наличии ран осуществляют механическую их очистку, накладывают повязки с антисептическими и дегидратирующими свойствами. Во время эвакуации выполняют коррекцию иммобилизации, продолжают введения обезболивающих и
седативных средств, проводят инфузионную терапию (полиглюкин, реополиглюкин, 5% раствор глюкозы, 4% раствор натрия гидрокарбоната и др.). Для профилактики раневой инфекции применяют комбинации антибиотиков широкого спектра действия с обязательным включением в них антибиотика группы пенициллина (учитывая частое выделение из ран клостридиальной флоры).
На госпитальном этапе осуществляют интенсивные противошоковые и реанимационные мероприятия. Количество и состав вводимых внутривенно трансфузионных сред в объеме 2 000—4 000 мл и более в сутки регулируется по данным суточного диуреза и показателям гомеостаза. В состав вливаемых жидкостей входят свежезамороженная плазма, глюкозоновокаиновая смесь, 5% раствор глюкозы с витаминами, 5% или 10% раствор альбумина, 4% раствор натрия гидрокарбоната, раствор маннита из расчета 1 г на 1 кг массы тела, дезинтоксикационные средства (гемодез, неогемодез). Для стимуляции диуреза назначают фуросемид до 80 мг и более в сутки, папаверин, эуфиллин, с целью профилактики тромбозов вводят гепарин по 2 500 ЕД 4 раза в сутки, дезагреганты (дипиридамол, пентоксифиллин), по показаниям используют ретаболил или феноболин, сердечно-сосудистые средства, иммунокорректоры. В профилактике острой почечной недостаточности эффективно применение простагландина Е2 (простенона), который вводят внутривенно в течение 3—5 дней. Интенсивное консервативное лечение должно обеспечить мочеиспускание в количестве не менее 30 мл в час. При неэффективности проводимого лечения в течение 8—12 ч, а именно при снижении диуреза до 600 мл/сут. и ниже, повышении уровня гиперкалиемии более 6 ммоль/л, креатининемии выше 0,1 ммоль/л, появлении признаков отека мозга и легких, показано проведение гемодиализа в режиме ультрафильтрации. Инфузионную терапию в междиализный период осуществляют в объеме 1500—2000 мл. Пострадавшим с выраженной интоксикацией показано проведение плазмафереза (см Плазмаферез, цитаферез), обеспечивающего наиболее полное удаление из организма токсических продуктов метаболизма. Сеансы гипербарической оксигенации уменьшают степень гипоксии тканей. С целью дезинтоксикации ежедневно делают очистительные клизмы, назначают энтеродез по 1 чайной ложке в 1/2 стакане воды 3 раза в день или активированный уголь.
При кровоточивости вследствие уремии и диссеминированного внутрисосудистого свертывания показано экстренное проведение плазмафереза с последующим переливанием свежезамороженной плазмы до 1000 мл, назначение ингибитора протеаз (гордокса, контрикала) на фоне продолжающегося введения гепарина по 2 500 ЕД 4 раза в сутки.
Хирургическая тактика должна быть активной и зависит от состояния пострадавшего, степени ишемии поврежденной конечности, наличия или отсутствия размозженных ран и переломов костей. Выраженный отек и напряжение мягких тканей сдавленного сегмента конечности, появление пузырей с геморрагическим содержимым, быстрое нарастание цианоза свидетельствуют о грубых нарушениях
микроциркуляции и опасности развития обширного некротического процесса. Проведение широких фасциотомий с рассечением фасциальных футляров может восстановить кровоток и устранить сдавление тканей. После фасциотомий на кожу накладывают редкие швы с оставлением дренажных трубок. Нежизнеспособность подвергшейся сдавлению конечности является показанием к ее ампутации.
При наличии размозженных ран проводят тщательную первичную хирургическую обработку с широким раскрытием ран, иссечением явно нежизнеспособных тканей, удалением инородных тел и свободно лежащих костных отломков, обильным промыванием антисептиками. Наложение глухих швов и выполнение операции кожной пластики недопустимо, так как некроз тканей может продолжаться и в
последующие дни.
Фиксацию переломов костей следует осуществлять с помощью компрессионно-дистракционных аппаратов вначале даже без окончательной и полной адаптации отломков. При отсутствии возможностей или условий для наложения этих аппаратов фиксацию выполняют гипсовыми лонгетами (циркулярную гипсовую повязку накладывать нельзя!) или скелетным вытяжением (если не планируется эвакуация пострадавшего в другие специализированные учреждения). Погружной накостный или внутрикостный остеосинтез переломов костей конечностей, подвергшихся сдавлению, противопоказан. В последующие дни в зависимости от состояния пострадавшего проводят коррекцию положения отломков, этапные некрэктомии, интенсивное местное лечение с применением средств, обладающих антисептическими, ферментными и дегидратирующими свойствами. После очищения раневой поверхности от некротических тканей и появления свежих грануляций осуществляют свободную и несвободную кожную эластику.
В позднем восстановительном периоде пострадавшие нуждаются в реабилитационно-восстановительном лечении с применением ЛФК, физиотерапевтических методов и санаторно-курортного лечения. По показаниям выполняют реконструктивно-восстановительные вмешательства.

Что такое краш-синдром?
Перед тем, как начать рассуждать, можно дать определение данному состоянию.
Оно возникает вследствие длительного сдавления мягких тканей (в основном мышц), в основе которого лежат ишемический некроз и интоксикация продуктами некроза с развитием печеночно-почечной недостаточности.
Синдром начинает развиваться после освобождения конечности от сдавления, например после землетрясения, когда человека придавило обломками здания. В развитии самого синдрома играют определенные факторы - боль, увеличение количества токсических веществ в крови, вследствие некроза сдавленной конечности, а также кровопотеря.
Клиническая картина
Условно патология разделяется на три периода, которые последовательно сменяют друг друга в течение 14 дней.
Первый период характеризуется резким отеком и сосудистой недостаточностью, которая длится 1-3 дня. Освобожденная конечность выглядит резко опухшей, красной, больные предъявляют жалобы на боль, снижение двигательной способности, общее состояние (артериальное давление, пульс, частота дыхания) в первые часы и дни в пределах нормы, однако состояние резко начинает ухудшаться с геометрической прогрессией и проявляются клинические симптомы шока, то есть резко падает давление, учащается сердцебиение, резко снижается количество мочи (олигоурия), иногда даже процесс мочеобразования прекращается (анурия), моча приобретает темно-бурый цвет, так как в ней содержание белка повышено. 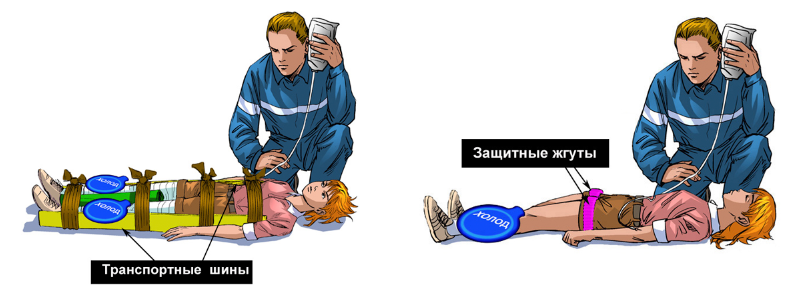
И синдром переходит во второй период - острая почечная недостаточность. Но почему же? По какой причине почки перестают работать? Для того, чтобы ответить на данный вопрос, следует немного коснуться строения почки. Данный орган состоит из нефронов. Это структурно-функциональная единица почки, то есть клетка. Данная структура играет огромную роль в процессе мочеобразования, и она состоит из капсулы и множества канальцев. Чтобы легче было понять, представьте себе маленькую трубку, вокруг которой обвиты виноградные лозы, и благодаря давлению в трубы попадают различные вещества из лоз, а далее они выводятся в сточные воды. В данном примере, виноградные лозы характеризуют капиллярные сети, а трубка характеризует канальцы нефрона, а те самые вещества, это и есть моча.
Теперь, когда процесс мочеобразования немного стал ясен, можно ответить на вопрос, почему же возникает почечная недостаточность при данном синдроме. Когда конечность освобождается от сдавления, все те ядовитые продукты распада некротизированных тканей попадают в кровь, а с ней и в почки для того, чтобы профильтроваться. Однако количество токсических веществ настолько велико, что они, попадая в канальцы (трубки), засоряют их, приводя к закупорке, а вследствие этого накоплению ядовитых веществ в самой почке и ее повреждению, а также системному токсикозу.
Лечение
Данная череда явлений может привести к смерти больного в кратчайшие сроки, если не будут предприняты мероприятия по дезинтоксикации, вплоть до диализа (искусственной почки).
Но как же избежать возникновения острой почечной недостаточности после освобождения конечности? И говоря про меры профилактики и лечения, сразу переходим к третьему периоду заболевания – излечению больного.
Каковы наши действия? В первую очередь после того, как человека освободили от сдавления, ему вводят анальгезирующие препараты во избежание возникновения болевого шока, далее следует туго перевязать поврежденную конечность. Возникает вопрос – зачем? Это делается для того, чтобы уменьшить отток крови, а значит и токсических веществ из области некроза в системный кровоток, и получить лишние часы для проведения дезинтоксикационных мероприятий. Если у больного возникают признаки сердечной недостаточности - ему вводят адреналин или норадреналин внутривенно. Данные выше описанные мероприятия чаще всего проводятся сразу на месте происшествия, для того, чтобы облегчить возможность доставки пострадавшего в стационар.
Далее уже в самом стационаре начинают противошоковую терапию, а также очищают кровь от различных опасных веществ. Также конечность циркулярно обкалывают новокаином и обкладывают льдом, дабы уменьшить отек. И самое главное в лечении, также назначение антибиотиков широкого спектра, дабы избежать возникновения вторичной инфекции, которая может осложнить и без того тяжелое состояние пострадавшего. Но бывают случаи, когда все эти действия не приводят к улучшению состояния больного, поэтому врачи прибегают к ампутации конечности.
Практика
Как пример можно привести Спитакское землетрясение, произошедшее в Армении 7 декабря 1988 года. Мощные подземные толчки амплитудой в 9-11 баллов практически полностью разрушили северную часть республики. 25 тысяч людей в тот злополучный день погибли, около полумиллиона остались без крова, и 20 тысяч стали инвалидами. Первыми, кто пришел на помощь республике - были подразделения Пограничных войск СССР, а также в тот же день в Армению вылетели из Москвы около сотни высококвалифицированных врачей разной специальности (терапевты, хирурги, анестезиологи, педиатры). Кроме этого, в течение одной недели со всего мира в республику были направлены сотни аппаратов искусственного гемодиализа (устройство, берущее на себя функцию почки), ведь на тот момент уже давно был известен синдром длительного сдавления, и он активно изучался.
Врачи прекрасно понимали, что освобождение пострадавших из-под завалов было лишь половиной дела, ведь сотни, а иногда и тысячи людей, которых вытащили из-под обломков, вначале ощущали себя удовлетворительно, однако буквально за неделю их состояние прогрессивно ухудшалось вследствие острой почечной недостаточности вплоть до смерти, и на тот момент единственным способом поддержания жизни таких больных была искусственная почка (аппарат гемодиализа) или же пересадка настоящей донорской почки.
Но, к огромному сожалению, даже аппаратов не хватало для спасения жизней людей, потому что пострадавших было слишком много, что уже говорить про дефицит донорских почек, и чаще всего на врачей падало великое и трагичное бремя, когда им приходилось выбирать между пациентами, кто получит возможность искусственного очищения крови, а кто нет. Чаще всего, акцент делался на возраст - старались спасти молодых людей, детей. И винить врачей в ужасных деяниях ни в коем случае нельзя, ведь они ценой своих моральных устоев, получая тяжелейшие психические и нравственные страдания, делали выбор, были спасателями и палачами одновременно. Профессия врача требует не только сострадания по отношению к ближнему, но зачастую гораздо важней иметь мужество в принятии своих решений. Ведь в большинстве своем, у нас нет времени на долгие обдумывания проблемы, потому что чаще всего время играет против нас.
Читайте также:


