Интоксикация при раке толстой кишки

Автор Александра Томберг | Врач международного отдела, основатель Clinics Direct | 9 декабря 2019 г.
Онкология кишечника входит в перечень наиболее часто диагностируемых злокачественных патологий с одинаковым уровнем распространённости по всему миру. Чаще всего данное заболевание поражает толстый кишечник, но и в зоне тонкого кишечника могут создаваться предпосылки для развития онкологического процесса.
Причины возникновения
К общим предрасполагающим факторам развития злокачественного процесса в области кишечника, относят:
- Наследственная предрасположенность к развитию онкологии кишечника.
- Семейный полипоз.
- Синдром Линча.
- Такие алиментарные факторы, как регулярное употребление алкоголя, злоупотребление жирной и жареной пищей.
- Ожирение.
- Введение малоподвижного образа жизни (гиподинамия).
- Хронические запоры.
- Табакокурение.
- Неспецифический язвенный колит.
- Болезнь Крона.
- Одиночные полипы в области толстого кишечника.
- Дивертикулярная болезнь толстого кишечника.
Кроме того, канцерогенное воздействие на кишечный эпителий оказывают метаболиты стероидных гормонов, производные тирозина и триптофана, амины и ароматические углеводороды.
Первые признаки рака кишечника
В зависимости от вовлечённости того или иного отдела кишечника в злокачественный процесс могут преобладать разные клинические симптомы. К общим клиническим симптомам онкологии кишечника, можно отнести:
- Отвращение к жареной и жирной пище.
- Снижение или полное отсутствие аппетита.
- Резкая потеря массы тела.
- Присутствие алой крови в кале.
- Постоянное ощущение тяжести в животе не связанное с перееданием.
- Чередование запоров и диареи.
- Снижение показателей гемоглобина в крови.
Признаки рака толстой кишки
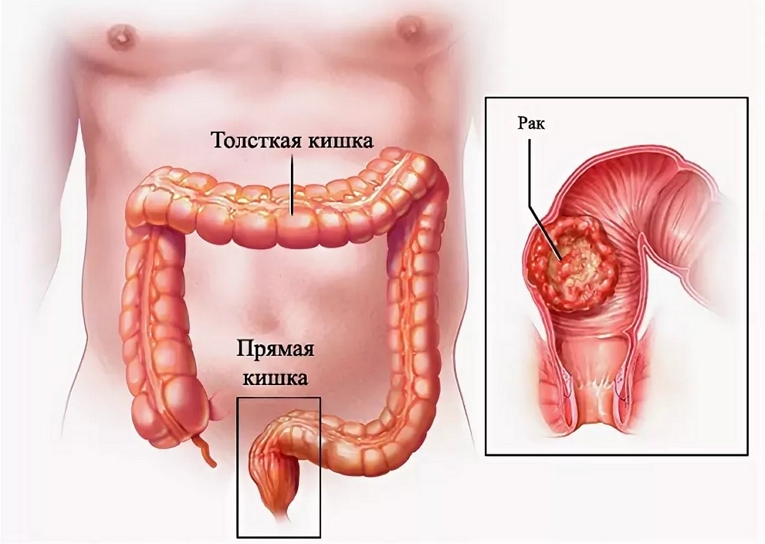
На развитие онкологии толстого кишечника указывает ряд таких клинических симптомов:
- Боль в правом подреберье или околопупочной области.
- Потеря аппетита.
- Тошнота и рвота.
- Повышенное газообразование в кишечнике.
- Хронические запоры, сменяющиеся диареей.
- Прогрессирующая анемия.
- Кишечная непроходимость.
- Появление в испражнениях примесей гноя, слизи или крови.
Признаки рака прямой кишки
На ранних стадиях данное заболевание протекает в бессимптомной форме. По мере прогрессирования онкологического процесса, клиническая картина патологии включает такие симптомы:
- Выделение алой крови из заднего прохода, примеси крови в кале.
- Стул имеет форму ленты или карандаша.
- Нарастающая анемия.
- Хронические запоры.
- Боль в области прямой кишки.
Признаки рака тонкой кишки
Онкология тонкой кишки сопровождается спастической болью в животе, возникающей с определенной периодичностью. Кроме того, на первый план выходят такие симптомы, как тошнота и рвота, метеоризм, неустойчивость стула, прогрессирующее снижение массы тела, интоксикация.
Стадии
В клинической практике выделяют такие стадии опухолевого процесса в области кишечника:
- 0 стадия. Возникают предраковые изменения.
- 1 стадия. Атипичные клетки начинают неконтролируемо делиться.
- 2 стадия. Наблюдается активный рост опухоли.
- 3 стадия. Опухоль выходит за пределы кишечника, наблюдаются признаки метастазирования.
- 4 стадия. Метастазы выявляются в других органах и лимфоузлах, развивается выраженная интоксикация организма.
Метастазы
Метастазирование при данном виде онкологии происходит в лимфатические узлы, легочную ткань, печень и кости таза.
Диагностика
План диагностики при подозрении на рак кишечника включает такие варианты осбледования:
Лечение
Радикальным методом лечения онкологии кишечника является оперативное вмешательство. Также, используются методики лучевого воздействия и химиотерапии.
Для лечения онкологии кишечника используются такие химиотерапевтические препараты, как Фторурацил, Луйковорин, Капецитабин, Иринотекан. С лечебной целью при онкологии кишечника используется дистанционный и контактный вид лучевого воздействия. Также, проводится предоперационное и послеоперационное облучение опухоли.
Прогноз для жизни
Прогноз относительно выживаемости и качества жизни при онкологии кишечника напрямую зависит от стадии, на которой был выявлен злокачественный процесс. Если лечение было проведено на 1 стадии онкологического процесса, то уровень пятилетней выживаемости составляет от 90 до 100%. Уровень пятилетней выживаемости на 2-3 стадии составляет не более 30%. На 4 стадии онкологического процесса, прогнозы менее благоприятные.
Профилактика
План профилактических мероприятий подразумевает регулярное диспансерное наблюдение пациентов из так называемой группы риска по возникновению рака кишечника. В группу риска попадают люди, имеющие так называемые предраковые заболевания. Также необходима коррекция образа жизни и рациона питания. Большое значение имеют скрининговые методы обследования (колоноскопия, анализ кала на скрытую кровь). Если у пациента ранее был диагностирован колоректальный рак, и было проведено оперативное вмешательство, то ему необходимо проходить комплексное обследование и получать консультацию врача онколога не реже 1 раза в 3 месяца. Регулярное обследование позволяет предупредить или своевременно выявить рецидив злокачественного процесса.
В зависимости от места локализации патологического очага, радикальное лечение рака кишечника предусматривает операцию с последующим наложением колостомы, реконструктивной операцией и закрытием кишечной стомы. Если злокачественный процесс локализуется в области восходящего отдела ободочной кишки или в области слепой кишки, то пациентам выполняется правосторонняя гемиколэктомия. Если новообразование располагается в восходящем отделе поперечно-ободочной кишки, то проводится ее резекция, а при раке нисходящего отдела — левосторонняя гемиколэктомия.
Остались вопросы? Вы можете позвонить нам или оставить заявку на нашей сайте и опытные врачи-координаторы ответят на все ваши вопросы по поводу лучших специалистов, клиник и цен на лечение!

Рак толстого кишечника в последние годы привлекает особое внимание ученых и клиницистов в связи с неуклонным ростом заболеваемости данной патологией, прежде всего в социально-экономических развитых странах. Каждый год на планете диагностируется более 800 тыс. вновь выявленных пациентов с колоректальным раком и 440 тыс. смертей от него, при этом общее количество больных составляет 3,5 млн человек [2, 3, 6]. Несмотря на внедрение новых медицинских технологий и значительные достижения в онкологии и хирургии, по-прежнему продолжается рост числа больных с осложненными формами колоректального рака. Так, в 2001 г. было зарегистрировано 24 849 вновь заболевших раком ободочной и 20 541 – раком прямой кишки. В 2003 году (10 лет назад) в России выявлено 50 689 новых случаев заболевания, на данный момент имеется тенденция роста данной нозологической единицы [1, 5].
В 2003 году в России от данной патологии умерло 36 036 человек [1, 5]. Прирост стандартизированных показателей смертности за последнее десятилетие наиболее выражен при раке ободочной кишки за счет осложнений в послеоперационном периоде – 13,3 % [5, 6]. Основной причиной летальности при данной патологии является отсутствие раннего выявления злокачественных заболеваний толстой кишки и развившихся осложнений [4, 7].
Цель исследования: анализ осложнений в периоперационном периоде хирургического лечения больных раком толстого кишечника.
Материал и методы исследования
С 2010 по 2012 годы в клинике кафедры госпитальной хирургии медицинского факультета им. Т.З. Биктимирова Ульяновского государственного университета г. Ульяновска пролечено 196 больных по поводу осложненных форм рака толстой кишки. Мужчин было 101 человек (51,5 %), женщин – 95 (48,5 %) в возрасте от 36 до 86 лет. Анализ возрастного состава больных показал, что 138 (70,4 %) пациентов были пожилого и старческого возраста, опухолевый процесс у которых был отягощен сопутствующими заболеваниями сердечно-сосудистой системы, органов дыхания и мочевыделительной системы, а также нарушениями обменных процессов. И 58 (29,6 %) пациентов были молодого и среднего возраста. Диагностика распространенности рака ободочной кишки, выявление осложнений опухолевого процесса, а также сопутствующих заболеваний основывались на комплексе клинико-инструментальных обследований, который включал лабораторные, рентгенологические, ультразвуковые, эндоскопические и морфологические методы диагностики.
В зависимости от осложнений злокачественных опухолей толстой кишки было выделено четыре группы пациентов, представленные в таблице, в клинической картине которых преобладали основные симптомы: первая группа – острая толстокишечная непроходимость – 98 (50,0 %), вторая группа – воспалительные параканкрозные осложенения с элементами абсцедирования – 45 (23,0 %), третья группа – перфорация опухоли с развитием перитонита различной распространенности – 28 (14,3 %), четвертая группа – профузное кишечное кровотечение – 25 (12,7 %).
Группы пациентов, распределённые по клиническим проявлениям
Симптомы рака толстого кишечника
Острая толстокишечная непроходимость
Воспалительные параканкрозные осложенения с элементами абсцедирования
Перфорация опухоли с развитием перитонита
Профузное кишечное кровотечение
Большая часть выявленных осложнений отмечена у пациентов с раком сигмовидной и слепой кишок – 78 %. Осложненные опухоли в 36 % случаев (n = 70) локализовались в правой половине ободочной кишки, в 59 % (n = 116) – в левой, в поперечной ободочной кишке у 5 % (n = 10) больных.
Наибольшее количество больных с вновь диагностированным колоректальным раком приходится на 3–4 стадию заболевания [1, 2]. По нашим данным, у большинства оперированных пациентов – 123 (62,7 %) – выявлена III стадия, у 54 (27,5 %) – IV стадия рака ободочной кишки и лишь у 19 (9,8 %) – II стадия.
При анализе данных обследования и клинической картины, изучении операционных находок и морфологического материала не было обнаружено зависимости распространения процесса от пола и возраста больных. Во всех группах больных по данным гистологического исследования основное место занимали аденокарциномы различной степени дифференциации – 80,8 %, гораздо реже встречались перстневидно-клеточные и недифференцированные формы рака (7,1 и 12,1 % соответственно).
В 45 % наблюдений во время оперативного вмешательства было обнаружено метастатическое поражение регионарных лимфатических узлов, отдаленные метастазы выявлены у 27 % обследованных с наиболее частой локализацией в печени (62 %), легких (12 %), канцероматоз брюшины выявлен в 18 % наблюдений.
Результаты исследования и их обсуждение
Острая обтурационная толстокишечная непроходимость (n = 98 (50 %)) являлась самой частой формой осложнений рака ободочной кишки. Причем в 75 % это были больные старше 60 лет. Преобладающее число пациентов с этим осложнением составили больные с опухолями сигмовидной (n = 54 (53,3 %)) и слепой (n = 29 (31 %)) кишок. В эту группу вошли больные с декомпенсированным нарушением проходимости ободочной кишки и при отсутствии эффекта от консервативных мероприятий, направленных на разрешение непроходимости кишечника. Клинически у всех были отмечены анемия, интоксикация, гипопротеинемия и нарушение водно-электролитного баланса. В 59 % наблюдений отмечены проявления токсико-анемичного синдрома преимущественно у пациентов с локализацией опухоли в правых отделах ободочной кишки. Неблагоприятным явился тот факт, что у 21 (22 %) больного обтурационная непроходимость сочеталась с опухолевым перифокальным воспалением, у 12 (11 %) – имела место перфорация опухоли в свободную брюшную полость с развитием разлитого перитонита, у 4 (4 %) – с пенетрацией опухоли в брыжейку тонкой кишки с развитием абсцесса. Предоперационная подготовка заключалась в проведении лечебных мероприятий, направленных на коррекцию водного и белково-электролитного баланса, кислотно-щелочного состояния, купирования интоксикации.
Объем операции при обтурационной непроходимости ободочной кишки зависел от локализации опухоли, степени непроходимости, состояния толстой кишки, характера метастазирования, тяжести общего состояния и наличия сопутствующих заболеваний. Из 70 оперированных пациентов с локализацией опухоли в правых отделах ободочной кишки в 21,2 % (n = 15) случаев выполнили правостороннюю гемиколэктомию с наложением илеотрансверзанастомоза и интраоперационную декомпрессию тонкой кишки. Восьми (11,4 %) пациентам с локализацией нерезектабельной опухоли в печеночном изгибе и восходящем отделе ободочной кишки были выполнены паллиативные симптоматические операции – наложение илеотрансверзанастомоза с обязательной зондовой назоинтестинальной декомпрессией, пятерым пациентам (7,1 %) этой группы при наличии тяжелой сопутствующей патологии наложена разгрузочная цекостома. При IV стадии онкологического процесса с наличием отдаленных метастазов, но при технически возможной резектабельности опухоли считали правомочным выполнение паллиативной санационной правосторонней гемиколэктомии с первичным наложением анастамоза.
При раке левой половины и поперечно-ободочной кишок, осложненных кишечной непроходимостью, у 71 (61,2 %) пациента выполнены резекции сегмента кишки со стенозирующей опухолью с последующим ушиванием дистального отрезка кишки и выведением проксимального конца в виде одноствольной колостомы на переднюю брюшную стенку по типу операции Гартмана. При неоперабильности опухоли 45 (38,7 %) пациентам были наложены разгрузочные трансверзо- и сигмостомы.
Умерли после операции 12 (12,2 %) пациентов от прогрессирующей раковой интоксикации и декомпенсации сопутствующей патологии.
Параканкрозные воспалительные процессы осложняют клиническое течение рака ободочной кишки. По нашим данным, воспалительные изменения в опухоли, выходящие за пределы кишечной стенки, составили 22,9 % (n = 45). У большинства пациентов (n = 38 (84 %)) опухоль с перифокальным воспалением локализовалась в правой половине ободочной кишки, что клинически проявлялось токсико-анемичным синдромом. И только у 7 (16 %) пациентов воспалительный процесс локализовался при опухолях селезеночного изгиба и сигмовидной кишки.
Клинические проявления в этой группе зависели от степени выраженности и характера воспалительной реакции тканей вокруг опухоли (стадии развития опухолевого процесса, локализации опухоли, реактивности организма больного). В 87 % случаев эти больные поступали по неотложным показаниям с симптоматикой острых хирургических заболеваний органов брюшной полости или забрюшинного пространства. Сложность дифференцировки перифокального воспаления, обусловленного опухолью или доброкачественной воспалительной инфильтрацией стенки ободочной кишки (при дивертикулите, болезни Крона, неспецифическом язвенном колите), позволяла разрешить эндоскопическое исследование. При ирригоскопии определялся суженный участок ободочной кишки, неровность рельефа слизистой, выход контрастного вещества за пределы кишечной стенки, что не позволяло отдифференцировать опухолевое поражение от доброкачественного воспалительного процесса. В сомнительных случаях при наличии положительных симптомов раздражения брюшины, а также в связи с дифференциальной диагностикой острой хирургической патологии органов брюшной полости у 8 (17,7 %) пациентов была выполнена диагностическая лапароскопия, которая позволила определить характер воспалительного процесса и его распространенность. У 22 больных (51,1 %) этой группы при отсутствии симптомов перитонита и прогрессирования воспалительного процесса предпринята выжидательная тактика, позволяющая выполнить операцию в плановом порядке после купирования воспалительного процесса путем проведения курса антибактериальной и детоксикационной терапии. Однако у 15 (33,3 %) из 45 больных с клиникой прогрессирования перитонита и кишечной непроходимости пришлось выполнить экстренные оперативные вмешательства.
При локализации опухоли в правых отделах, печеночном изгибе, правой трети поперечной ободочной кишки с распространением воспалительной инфильтрации на брыжейку у 25 (55,5 %) больных была выполнена расширенная правосторонняя гемиколэктомия с адекватным дренированием забрюшинной клетчатки и брюшной полости в зоне оперативного пособия. При левосторонней локализации (n = 8 (16 %)) выполняли операцию типа Гартмана, так как наличие даже умеренного перифокального воспаления тканей в зоне оперативного вмешательства не создают условия для безопасного наложения первичного толстокишечного анастомоза, тем более при наличии параканкрозных абсцессов.
Тяжелым осложнением при раке ободочной кишки является перфорация кишечной стенки. Перфорацию кишечной стенки в зоне опухоли и диастатическую перфорацию проксимальнее опухоли мы наблюдали у 28 (14,2 %) больных. Значительно чаще это осложнение развивалось при поражении левых отделов ободочной кишки (n = 26 (92,8 %)) с перфорацией опухоли вследствие ее распада. Перфорация вне зоны опухоли от пролежня каловым камнем или перерастяжения кишечной стенки при обтурационной непроходимости выявлена у 2 (7,2 %) больных. Обнаруженные осложнения позволяют предполагать, что ведущим этиологическим фактором при диастатической перфорации кишки являются сосудистые расстройства и дистрофические изменения стенки кишки, тогда как основной причиной перфорации самой опухоли явились нарушения кровоснабжения с последующей ишемией и некрозом. Во всех случаях перфорации обнаружены при III и IV стадии заболевания преимущественно у пациентов пожилого и старческого возраста.
Исходы лечения в этой группе пациентов характеризовались наибольшим количеством осложнений и летальных исходов (n = 12, что составило 42,8 %).
Кишечные кровотечения являются нередким осложнением рака ободочной кишки. Мы наблюдали 25 (12,7 %) больных с профузными (n = 7, то есть 28 %) и рецидивирующими (n = 18 соответственно 72 %) кровотечениями из опухолей толстой кишки. Локализация опухолей, явившихся источником профузного кровотечения, по нашим данным была преимущественно в левой половине ободочной кишки (92 %), тогда как для рецидивирующих кровотечений более характерна правосторонняя локализация опухоли (8 %). Как правило, возникновение обильных кровотечений связано с аррозией сосудов при распаде опухолевой ткани.
Клиническая картина кишечного кровотечения проявляется значительной слабостью пациентов, анемией и кровянистыми выделениями или кратковременными периодическими кровотечениями из прямой кишки. Длительность существования этих признаков у 20 пациентов (80 %) превышала несколько месяцев. Эти больные длительно лечились и обследовались по поводу анемии, которая в определенной степени была связана не только с кровотечением, но и с раковой интоксикацией. Половина пациентов этой группы (n = 13, что составило 52 %) поступила в стационар с анемией тяжелой степени и требовала заместительных гемотрансфузий.
В диагностический алгоритм этой группы пациентов нами включены эндоскопия и ультразвуковая диагностика, которые в 72 % случаев помогли поставить правильный диагноз. Проведение экстренной диагностической фиброколоноскопии у 5 (20 %) больных было затруднительным вследствие невозможности адекватной подготовки кишечника к исследованию из-за наличия сгустков крови и поступления её из проксимальных отделов кишки, затрудняющих визуализацию и идентификацию источника кровотечения.
В связи с отсутствием эффекта от гемостатической терапии и невозможностью выполнения эндоскопического гемостаза 2 пациента с профузным кишечным кровотечением опухолевого генеза были оперированы по жизненным показаниям в ургетном порядке, выполнена правосторонняя гемиколэктомия. Крайне тяжелое состояние двух пациентов старческого возраста с анемией тяжелой степени позволило выполнить только паллиативные резекции сигмовидной кишки с кровоточащей опухолью по типу операции Гартмана. Эта группа пациентов с геморрагическими осложнениями опухолей ободочной кишки характеризовалась наименьшим количеством послеоперационных осложнений и двумя летальными исходами.
У 166 (84,7 %) пациентов удалось выполнить радикальную операцию. Умерло 26 пациентов, следовательно, послеоперационная летальность составила 13,3 %. Наибольшее количество осложнений в послеоперационном периоде выявлено у больных с перфорацией опухоли и развитием перитонита.
Таким образом, непосредственные результаты хирургического лечения больных осложненным течением рака ободочной кишки находятся в прямой зависимости от своевременной диагностики основного заболевания и его осложнения, обоснованной хирургической тактики, выбора способа и техники выполнения оперативного вмешательства, а также от полноценной профилактики и терапии послеоперационных осложнений.
Несмотря на современный уровень организации и оснащенность медицинской помощи, ранняя диагностика рака толстого кишечника остается на низком уровне, и выявление данной патологии происходит на поздних стадиях, что способствует увеличению периоперационных осложнений.
Рецензенты:
Содержание:
Получить бесплатную консультацию
Ведущие специалисты Центра ответят на ваши вопросы.
Рак ректосигмоидного соединения лечение 1, 2, 3 стадии. Симптомы, признаки, метастазы, прогноз.
Ректосигмоидное соединение представляет собой переходную зону между сигмовидной и прямой кишкой на расстоянии от 13 до 17 см от кожноанальной линии при жесткой ректоскопии.
В цивилизованных, экономически развитых странах колоректальный рак является одной из наиболее распространенных злокачественных опухолей.
В структуре онкологической заболеваемости в мире колоректальный рак в настоящее время занимает четвертое место. Ежегодно в мире регистрируется около 800 тысяч вновь заболевших больных колоректальным раком, из них более половины (440 тысяч) умирает. Рак ободочной и прямой кишок является причиной смерти около 3,4 % лиц общей популяции и второй по частоте причиной смерти в США.
В европейской популяции риск развития колоректального рака составляет 4–5 %. Это означает, что в течение жизни один из 20 человек заболевает раком этой локализации.
Хотя во всех экономически развитых странах отмечается неуклонный рост заболеваемости колоректальным раком, тем не менее, этот показатель не является фатальным спутником цивилизации. Так, в некоторых штатах США среди белого населения за последнее десятилетие отмечается некоторое снижение заболеваемости колоректальным раком, в то время как среди цветного населения этот показатель неуклонно растет.
Это объясняется рядом предпринятых профилактических мер:
- изменение характера питания в результате усиленной санитарной пропаганды (уменьшение потребления животных жиров, увеличение потребления свежих фруктов и овощей, борьба с избыточным весом);
- ранней диагностики колоректального рака.
Факторы риска в развитии колоректального рака.
Диетические факторами повышающие риск возникновения рака ободочной кишки являются:
- избыточное употребление животных жиров;
- употребление пищи с недостаточным содержанием растительной клетчатки;
- избыточное питание;
- употребление алкоголя (особенно пива).
- Пищевой рацион с избытком продуктов, содержащих красное мясо и животные жиры, бедный клетчаткой, является важным причинным фактором в возникновении рака прямой кишки.
Рацион с большим содержанием фруктов, овощей и богатых клетчаткой продуктов с низким содержанием насыщенных жиров призван обеспечить защиту слизистой толстой кишки от агрессивного воздействия желчных кислот и пищевых канцерогенов.
Понижают риск возникновения колоректального рака:
- употребление пищи с высоким содержанием растительной клетчатки;
- витамины D и C;
- кальций.
Большинство случаев рака прямой и ободочной кишки (колоректального рака) являются спорадическими, то есть не связанными с какими-либо выявляемыми на настоящий момент наследственными факторами.
Роль наследственно обусловленной мутации доказана в рамках двух синдромов: тотального (семейного) аденоматозного полипоза (САП) и наследственного неполипозного рака толстой кишки (синдром Линча).
Семейный аденоматозный полипоз - это менее частый, чем наследственный колоректальный рак, патологический процесс. Риск развития колоректального рака у пациентов с семейным аденоматозным полипозом составляет почти 100 %.
Семейный аденоматозный полипоз обычно характеризуется:
- сотнями колоректальных аденоматозных полипов в молодом возрасте (20—30 лет);
- аденоматозными полипами двенадцатиперстной кишки;
- множественными внекишечными проявлениями (блок 2-6);
- мутацией в опухолевом гене-супрессоре аденоматозного полипоза толстой кишки (АПТК) в хромосоме 5д;
- наследованием по аутосомно-доминантному типу (потомки пораженных болезнью имеют один из двух шансов унаследовать САП).
Вторым (после семейного аденоматозного полипоза) синдромом со значительным вкладом наследственной предрасположенности является наследственный неполипозный рак толстой кишки (ННРТК).
Для данного синдрома характерны следующие критерии:
- три случая рака толстой кишки (один из которых возник в возрасте до 50 лет) в 2-3 разных поколениях;
- два морфологически верифицированных рака толстой кишки в 2-3 разных поколениях и один или более случаев рака желудка, эндометрия, тонкого кишечника, яичников, уретры, почечной лоханки (один из случаев любого рака должен быть в возрасте до 50 лет);
- молодой возраст возникновения рака толстой кишки (до 50 лет) у обоих родственников в двух разных поколениях;
- наличие синхронных, метахронных опухолей толстой кишки у одного родственника и случай рака толстой кишки у второго родственника (один из случаев любого рака должен быть в возрасте до 50 лет).
Молекулярно-генетической причиной ННРТК являются наследственные мутации в ряде генов, но 95 % этих мутаций сосредоточенно в 2 генах - MLH1и MSH2. При выявлении мутации в указанных генах у пациента рекомендуется поиск данной мутации у его родственников.
Также рекомендуется динамическое наблюдение тех родственников, которые являются носителями мутаций для выявления возможного возникновения рака толстой кишки на ранней стадии, что несомненно приведет к более эффективному лечению.
- единичные и множественные аденомы (полипы) толстой кишки;
- неспецифический язвенный колит;
- болезнь Крона;
- рак женских гениталий или молочной железы в анамнезе;
- иммунодефициты.
Выявление полипов играет исключительно важную роль в предупреждении возникновения рака, так как рак толстой кишки чаще всего развивается из полипов, а не de novo. Риск перерождения полипа толстой кишки в рак велик: при полипе размером менее 1 см – 1,1 %, 1–2 см – 7,7 %, более 2 см – 42 %, в среднем – 8,7 %.
Хотя большинство полипов так и остаются доброкачественными, некоторые, если их не удалить, могут переродиться или трансформироваться в злокачественные (раковые) опухоли. Процесс трансформации полипов скорее всего обусловлен генетическими мутациями в клетках.
Бывают разные виды полипов, но считается, что только один вид способен превратиться в раковую опухоль. Этот тип полипов называется аденоматозные полипы. Пока Вы не сделаете специальное обследование (колоноскопию), Вы не можете быть уверены в том, что в Вашем кишечнике нет полипов, потому что полипы не вызывают никаких симптомов. Большие полипы или опухоли могут приводить к возникновению симптомов – кровотечение, кровь в стуле, анемия или нарушение проходимости кишечника. Эти симптомы достаточно редки и начинают появляться только тогда, когда полипы становятся очень большими или злокачественными.
Своевременное выявление колоректального рака предполагает диагностику его на ранних, доклинических стадиях, когда отсутствуют всякие клинические проявления этого заболевания. Скрининг, или раннее выявление колоректального рака, проводится с помощью пальцевого обследования, гемоккультного теста и эндоскопического метода. При пальцевом исследовании прямой кишки возможно выявление до 70 % ректальных карцином.
Основанием для проведения гемоккульт-теста является то, что колоректальные аденомы и карциномы в той или иной степени кровоточат.
При проведении скрининга среди формально здорового населения от 2 до 6 % обследованных имеют положительный гемоккульт-тест. При дальнейшем обследовании пациентов, имеющих положительный гемоккульт-тест, колоректальный рак выявляется в 5–10 %, а железистые аденомы – в 20–40 % случаев.
В 50–70 % случаев тест бывает ложноположительным.
Сигмоидоскопия и тотальная колоноскопия являются важными составляющими скрининга колоректального рака. При использовании современных гибких сигмоидоскопов длиной 60 см удается выявить 55 % аденом и карцином сигмовидной и прямой кишки, развивающихся de novo. Чувствительность этого метода составляет 85 %. (в настоящее время Американская ассоциация врачей рекомендует проведение сигмоидоскопии каждые 3–5 лет, начиная с 50–летнего возраста, у лиц, не предъявляющих каких–либо жалоб на дисфункцию кишечника).
На ранних стадиях развития (отсутствие прорастания в мышечный слой кишки, отсутствие регионарных и отдалённых метастазов) рак прямой и ободочной кишки излечим практически в 100 %.
Рак прямой кишки может проявляться выделением крови, слизи из заднего прохода, нарушением привычного характера стула. Возможно появление вздутий и болей в животе. Развитие рака может привести к похуданию, анемии, появлению болей в заднем проходе, болезненных позывов на дефекацию.
Большинству людей неудобно обсуждать функционирование своего кишечника, тем не менее, если Вы сами не скажете доктору о необычных симптомах, например, изменение формы стула, он никогда об этом не узнает и скорее всего даже не спросит!

Вот краткое перечисление того, на что нужно обращать внимание (большинство из этих симптомов встречаются у многих людей и не связаны с раком, тем не менее, позвольте это решить доктору):
- изменение режима и характера опорожнения кишки – единовременные или хронические поносы или запоры, неприятные ощущения при опорожнении кишки, изменение формы стула (тонкий, как карандаш, или тоньше, чем обычно), ощущение неполного опорожнения кишки;
- необычные ощущение, связанные с кишечником, такие как – повышенное газообразование, боль, тошнота, вздутие живота, ощущение переполнения кишечника;
- кровотечение (светло-красная или очень темная кровь в стуле);
- постоянная усталость;
- необъяснимая потеря веса;
- необъяснимый дефицит железа;
- необъяснимая анемия.
Однако на ранних стадиях рак может развиваться бессимптомно. Единственной возможностью выявить в таких случаях рак или предраковое заболевание (аденоматозный полип), является профилактические колноскопии.
Выполнить всем без исключения жителям страны колоноскопию не по силам даже очень развитым системам здравоохранения, кроме того, инструментальное исследование носит инвазивный характер, а значит, и минимальный риск развития осложнений. Поэтому в Беларуси, как и в большинстве социально ориентированных стран, проводятся так называемые скрининг-исследования кала на скрытую кровь. При выявлении положительной реакции такому пациенту показано выполнение колоноскопии.
Основным методом установления диагноза является морфологический: так называемая биопсия, когда фрагмент ткани опухоли извлекается для микроскопического исследования.
Достичь опухоли в просвете кишки возможно с помощью эндоскопических исследований:
- ректороманоскопии (введение в задний проход негнущейся трубки на глубину до 28 см);
- колоноскопии (эластичнкая оптика на всю длину кишечника).
Для определения распространённости опухоли используются методики медицинской визуализации:
- УЗИ (в том числе и через просвет прямой кишки – трансректальное УЗИ);
- компьютерную томографию;
- магнитно-резонансную томографию.
Основным методом лечения рака ректосигмоидного соединения является хирургический – резекция ректосигмоидного соединения.
При резекции ректосигмоидногосоединения толстой кишки дистальный и проксимальный края отсечения кишки должны быть на достаточном расстоянии от опухоли: минимум 5 см на нефиксированном препарате. В едином блоке с опухолью удаляются все регионарные лимфатические узлы от устьев нижних брыжеечных сосудов.
Резекция ректосигмоидного соединения по Гартману (с формирование концевой колостомы) выполняется при осложнениях опухолевого процесса (кишечная непроходимость, перфорация опухоли) и декомпенсированным по сопутствующим заболеваниям состоянием больного.
В случаях распространения опухоли на прилежащие органы и ткани, выполняются комбинированные операции с удалением препарата в едином блоке, а при наличии отдаленных синхронных метастазов (в печени, легких, яичниках и т.д.) – одномоментное или поэтапное их удаление (что определяется консилиумом врачей).
Целесообразность проведения других методов лечения (лучевой и химиотерапии) определяется после стадирования заболевания, на основании получения окончательного морфологического заключения патоморфолога (примерно через 7-10 дней после операции).
Хирургическое удаление опухоли – это самое эффективное лечение рака прямой кишки. Даже после удаления всей раковой опухоли, в других органах и частях тела могут остаться раковые клетки. Эти скопления раковых клеток во время первой операции могут быть настолько маленькими, что их невозможно определить. Однако, спустя какое-то время они могут начать расти.
Возможность развития рецидива рака прямой кишок (возврата заболевания) зависит от стадии и особенностей течения заболевания. Появление рецидива опухоли может усложнить последующее лечение с помощью химиотерапии и/или лучевой терапии.
При ранней диагностике рецидива рака толстой и прямой кишок пациенты имеют большие шансы на проведение успешного лечения, в том числе хирургического.
Периодическое наблюдение за пациентами позволяет выявить образование новых полипов в толстой кишке у пациентов, которые ранее уже перенесли рак толстой кишки (после операции новые полипы образуются приблизительно у каждого пятого пациента, у которого ранее был обнаружен и пролечен рак толстой кишки).
Большинство рецидивов раковых образований обнаруживается в течение первых двух лет после хирургии, поэтому интенсивность мониторинга максимальна именно в этот промежуток времени и целью обследования является в первую очередь исключение развития возврата заболевания.
При контрольном осмотре оценивается состояние вашего здоровья и назначается обследование: один раз в каждые шесть месяцев в течение первых двух лет после операции и 1 раз в год в последующие 3-5 лет и включает:
- физикальный осмотр;
- анализ крови на опухолевый маркер CEA или РЭА (аббревиатура названия карциноэмбрионального антигена или ракового эмбрионального антигена) – это особый белок, который обнаруживают в крови. При активном опухолевом процессе уровень этого белка в крови больных раком толстой и прямой кишок иногда может повыситься);
- колоноскопия (осмотр просвета толстой и прямой кишок);
- рентгенография органов грудной клетки;
- компьютерная томография;
- осмотр органов брюшной полости и таза с помощью ультразвука.
Прейскурант цен
Резекция ректосигмоидного соединения толстой кишки
Удаление рецидивной опухоли малого таза с тазовой перитонэктомией, ректосигмоидной колэктомией
Читайте также:


