Кандидоз полости рта журнал

В последние годы во всем мире, и особенно в развитых странах, наблюдается значительный рост грибковых заболеваний, вызываемых дрожжеподобными грибами рода Candida.
Известно, что грибковые инфекции занимают одну из ключевых позиций среди заболеваний слизистой оболочки полости рта по распространенности среди населения и тяжести возможных осложнений для организма пациента.
Кандиданосительство статистически определяется у 5% младенцев, у лиц же пожилого возраста этот показатель увеличивается до 60% [1]. Однако истинное проявление патогенных свойств грибов рода Candida зависит главным образом от состояния макроорганизма. Главную роль в развитии кандидоза играет ослабление иммунной системы. Именно уровень состояния функциональной системы ротовой полости у каждого индивидуума с учетом его возраста, гигиенических навыков и других факторов характеризует экосистему в целом. Кандидоз возникает, как правило, на фоне более или менее выраженного иммунодефицита или дисбаланса иммунной системы [2].
Развитию кандидоза могут способствовать тяжелые сопутствующие заболевания: злокачественные новообразования, ВИЧ - инфекция, туберкулез, эндокринопатии (сахарный диабет, гипотиреоз, гипопаратиреоз, гипо и гиперфункция надпочечников). Заболевания желудочнокишечного тракта, особенно пониженная кислотность желудочного сока и ахилия, часто обусловливают развитие кандидоза слизистой оболочки рта. Развитию кандидоза полости рта способствует длительное лечение кортикостероидными препаратами, цитостатиками, которые подавляют иммунную систему организма и усиливают вирулентность дрожжеподобных грибов [3].
Вследствие широкого применения антибиотиков за последние годы значительно увеличилось количество больных кандидозом слизистой оболочки рта. Длительный прием антибиотиков нарушает состав резидентной микрофлоры полости рта, в результате чего формируется дисбактериоз. Происходят угнетение резидентной микрофлоры полости рта и резкий рост вирулентности условнопатогенных грибов Candida, вызывающих заболевание слизистой оболочки рта (суперинфекция, аутоинфекция). Прием антибиотиков может вызвать также дисбактериоз кишечника, следствием чего являются гипо- и авитаминозы В, В2, В6, С, РР, что в свою очередь отрицательно сказывается на функциональном состоянии слизистой оболочки рта (она становится подверженной влиянию кандидозной инфекции).
В настоящее время, с учетом всего вышеперечисленного, кандидоз рассматривается как иммуннодефицитное состояние, возникшее в результате глубокой разбалансировки экосистемы в целом. Такое представление о заболевании обуславливает принципиальную необходимость комплексного лечения кандидоза, в состав которого будут непременно включаться:
- мероприятия, направленные на устранение местных проявлений заболевания;
- мероприятия для системного лечения проявлений кандидоза;
- мероприятия, направленные на восстановление и нормализацию иммунной системы.
Целью данного исследования явилось определение эффективности комплексного лечения кандидоза полости рта.
Материалы и методы исследования
Изучение данного вопроса осуществлялось на кафедре стоматологии ФУВ ВолгГМУ, на базе терапевтического отделения ГСП №1 г. Волгограда. В исследовании участвовали 50 человек, диагноз "кандидоз" которым ставили на основании ряда критериев – жалоб пациента, клинической картины заболевания и данных бактериологического посева материала, забранного с поверхности дорзальной части языка. Для реализации исследования были сформированы 2 группы пациентов – основная и контрольная. Основную группу составили 28 человек в возрасте 31 – 55 лет, страдающие кандидозом полости рта. По форме клинических проявлений больные распределялись следующим образом: острая псевдомембранозная форма – 13 пациентов, хроническая псевдомембранозная – 8, хроническая атрофическая – 7 человек. В контрольную группу были включены пациенты с тождественной возрастной категорией, в количестве 22 - х человек. В данной группе острая псевдомембранозная форма определялась у 7 пациентов, хроническая псевдомембранозная – у 10, хроническая атрофическая форма регистрировалась у 5 человек.
Пациентам обеих групп назначалось лечение, направленное на ликвидацию возбудителя заболевания. Оно включало в себя антимикотическую терапию, системную и местную.
Для применения системной антимикотической терапии необходимо наличие ряда показаний, в первую очередь определенной клинической формы поражения (острый псевдомембранозный кандидоз, клинические признаки диссеминации, хронические формы заболевания, резистентные к ранее проводимой местной терапии и т.д.), поэтому отбор пациентов в группы осуществлялся с учетом данных показаний. Фунгицидные средства назначались по данным результатов бактериологического посева на чувствительность к препаратам. При этом у 83% пациентов выявлялась высокая чувствительность к флуконазолу, у 17% - к итраконазолу. Данные препараты принимались больными внутрь в таблетированной форме по общепринятой схеме.
Местная противогрибковая терапия осуществлялась 0,5% мирамистином в виде мази, аппликации препарата проводились 3 раза в сутки. Мирамистин – антисептик с выраженным антимикробным, фунгицидным и противовирусным действием, усиливающий местные иммунные реакции и регенераторные процессы. Кроме этого, всем пациентам 4 раза в день назначались полоскания ротовой полости 2% бикарбоната натрия.
Всем пациентам назначалась также десенсебилизирующая терапия, этой целью рекомендовался эриус (5 мг 1 раз в сутки).
Помимо данной схемы, пациенты основной группы получали лечение, направленное на повышение иммунологической резистентности организма. Известно, что при кандидозе резко снижается усвояемость таких жизненно важных элементов как витамины и минералы (особенно железо). Учитывая этот факт, оптимальным в данном случае представляется препарат ферроглобин В12 – комплекс, содержащий железо, витамины группы В и С, фолиевая и пантеноновая кислоты, а также экстракт корня солодки. Корень солодки оказывает стимулирующее действие на неспецифическую резистентность организма. Препарат назначали пациентам внутрь, после еды по 1 ч.л. 3 раза в сутки.
Высокой эффективностью в борьбе с кандидозной инфекцией обладают конкурентные пробиотики. Их использование обусловлено антагонистическими свойствами относительно грибов рода Candida, которые реализуются путем конкуренции за питательные субстраты и синтеза антикандидозных метаболитов. Наш клинический опыт подтверждает высокую эффективность самоэлиминирующего пробиотика Бактистатин. Препарат назначался пациентам основной группы по 1 капсуле 3 раза в день во время еды.
Таким образом, пациенты основной группы помимо антимикотической и десенсебилизирующей терапии получали дополнительное лечение, направленное на коррекцию иммунных механизмов организма в виде двух препаратов – Ферроглобин В12 и Бактистатин.
Курс лечения кандидоза в обеих группах составил 21 день.
Далее состояние пациентов оценивали с учетом наличия или отсутствия жалоб и динамики клинической картины заболевания, а также данных повторного бактериологического посева материала спустя 21 день (3 недели) и шести месяцев после окончания лечения и отдаленной реколонизации экосистемы.
и их обсуждение
Оценка эффективности лечения складывалась из совокупности субъективных и объективных данных, полученных в процессе исследования. В качестве субъективных данных рассматривались наличие или отсутствие жалоб у пациента, а также оценка врачом клинической картины заболевания. При анализе полученных фактов выяснилось, что в краткие сроки после проведенного лечения (через 3 недели) отсутствие признаков заболевания было зарегистрировано в основной группе в 92, 8% случаев, в контрольной – у 68,2% пациентов. В отдаленные сроки, через 6 месяцев после лечения, в основной группе ситуация принципиально не изменилась, и в 89,3% случаев не было зафиксировано случаев рецидива заболевания. В контрольной группе пациентов с отсутствием рецидива было зарегистрировано значительно меньше – в 36,4% случаев (табл. 1).
Исчезновение признаков заболевания у пациентов в динамике
Отсутствие признаков заболевания через 3 недели после лечения
Отсутствие признаков заболевания через 6 месяцев после лечения
Известно, что грибковые инфекции занимают одну из ключевых позиций среди заболеваний слизистой оболочки полости рта по распространенности среди населения и тяжести возможных осложнений для организма пациента.
В последние годы во всем мире, и особенно в развитых странах, наблюдается значительное увеличение числа грибковых заболеваний, вызываемых дрожжеподобными грибами рода Candida.
Согласно последним исследованиям, кандидоз слизистой оболочки рта относится к наиболее распространенным заболеваниям, что подтверждается увеличением его распространенности среди других заболеваний слизистой оболочки рта до 63% [30].
Основываясь на данных современных литературных источников, лечение кандидоза должно быть комплексным, с повторными курсами и индивидуальным подходом. При проведении лечебных мероприятий учитывают этиологию, характер и продолжительность заболевания 16.
Кандидоносительство статистически определяется у 5% младенцев, у лиц же пожилого возраста этот показатель увеличивается до 60% [6]. Однако истинное проявление патогенных свойств грибов рода Candida зависит главным образом от состояния макроорганизма. Главную роль в развитии кандидоза играет ослабление иммунной системы. Именно состояние функциональной системы ротовой полости у каждого индивидуума с учетом его возраста, гигиенических навыков и других факторов характеризует экосистему в целом. Кандидоз возникает, как правило, на фоне более или менее выраженного иммунодефицита или дисбаланса иммунной системы [14].
Развитию кандидоза могут способствовать тяжелые сопутствующие заболевания: злокачественные новообразования, ВИЧ-инфекция, туберкулез, эндокринопатии (сахарный диабет, гипотиреоз, гипопаратиреоз, гипо- и гиперфункция надпочечников). Заболевания желудочно-кишечного тракта, особенно пониженная кислотность желудочного сока и ахилия, часто обусловливают развитие кандидоза слизистой оболочки рта.
Возникновению кандидоза слизистой оболочки полости рта способствует длительное лечение кортикостероидными препаратами, цитостатиками, которые подавляют иммунную систему организма и усиливают вирулентность дрожжеподобных грибов [15].
Однако следует отметить, что используемые большинством пародонтологов антисептики при их разведении ротовой жидкостью явно снижают свою активность, а некоторые антисептики, например, хлоргексидин, оказывают побочное действие [6,13,23 и др.]. Что касается применяемых в настоящее время иммунотерапевтических препаратов, то иммуномодулятор левамизол обладает пирогенными свойствами [24], а имудон эффективен лишь при легких формах заболеваний пародонта [3].
Вследствие широкого применения антибиотиков за последние годы значительно увеличилось количество больных кандидозом слизистой оболочки рта. Длительный прием антибиотиков нарушает состав резидентной микрофлоры полости рта, в результате чего формируется дисбактериоз. Происходят угнетение резидентной микрофлоры полости рта и резкий рост вирулентности условно патогенных грибов рода Candida, вызывающих заболевание слизистой оболочки рта (суперинфекция, аутоинфекция). Прием антибиотиков может вызвать также дисбактериоз кишечника, следствием чего являются гипо- и авитаминозы В, В2, В6, С, РР, что в свою очередь отрицательно сказывается на функциональном состоянии слизистой оболочки рта (она становится подверженной влиянию кандидозной инфекции).
В настоящее время, с учетом всего вышеперечисленного, кандидоз рассматривается как иммуннодефицитное состояние, возникшее в результате существенной разбалансировки экосистемы в целом. Такое представление о заболевании обуславливает принципиальную необходимость комплексного лечения кандидоза, в состав которого будут непременно включаться:
- мероприятия, направленные на устранение местных проявлений заболевания;
- мероприятия для системного лечения проявлений кандидоза;
- мероприятия, направленные на восстановление и нормализацию функций иммунной системы.
Материалы и методы исследования
Таблица 1. Общее количество пациентов
| Возраст | Количество пациентов | ||
| муж. | жен. | Всего | |
| 20-30 | 5 | 7 | 12 |
| 31-40 | 10 | 8 | 18 |
| 41-50 | 9 | 11 | 20 |
| Общее число | 24 | 26 | 50 |
По мнению Шумского А.В. (2009), системная терапия кандидоза слизистой оболочки рта назначается при определенных показаниях: хронический гиперпластический кандидоз, эрозивно-язвенная форма кандидоза, кандидоз рта на фоне сахарного диабета, иммунодефицитного состояния, при неэффективной местной терапии [32].
В схему местного лечения входит комплекс мероприятий, включающих профессиональную гигиену полости рта, санацию рта, ортопедическое лечение, коррекцию протезов и др. [7].
По данным современных литературных источников, используемые в лечении кандидоза противогрибковые средства подразделяются на полиеновые антибиотики (нистатин), азольные соединения (флуконазол), аллиламиновые средства (нафтифин и тербинафин), смешанные вещества (антисептики, щелочные полоскания и анилиновые красители) [31].
Антисептическим препаратом из группы четвертичных аммониевых соединений является Мирамистин ® , который обладает широким спектром антимикробного действия, включая госпитальные штаммы, резистентные к антибиотикам.
Рис. 1. Бензилдиметил[3-(миристоиламино)пропил] аммоний хлорид, моногидрат
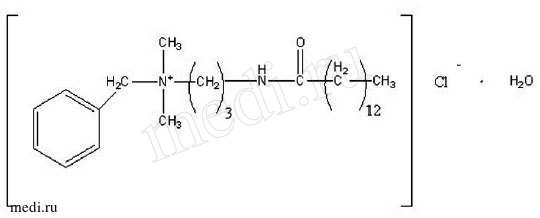
Активное вещество препарата -бензилдиметил[3-(миристоиламино) пропил]аммоний хлорид, моногидрат - относится к классу поверхностно-активных веществ (см. рис. 1).
Проведенные экспериментальные исследования показали, что препарат оказывает выраженное бактерицидное действие в отношении грамположительных (Staphylococcus spp., Streptococcus spp., Streptococcus pneumoniae и др.), грамотрицательных (Pseudomonas aeruginosa, Escherichia coli, Klebsiella spp. и др.), аэробных и анаэробных бактерий, определяемых в виде монокультур и микробных ассоциаций, включая госпитальные штаммы с полирезистентностью к антибиотикам. Оказывает противогрибковое действие на аскомицеты рода Aspergillus и рода Penicillium, дрожжевые (Rhodotorula rubra, Torulopsis glabrata и т.д.) и дрожжеподобные грибы (Candida albicans, Candida tropicalis, Candida krusei, Pityrosporum orbiculare (Malassezia furfur) и т.д.), дерматофиты (Trichophyton rubrum, Trichophyton mentagrophytes, Trichophyton verrucosum, Trichophyton schoenleini, Trichophyton violacent, Epidermophyton Kaufman-Wolf, Epidermophyton floccosum, Microsporum gypseum, Microsporum canis и т.д.), атакже на др. патогенные грибы в виде монокультур и микробных ассоциаций, включая грибковую микрофлору с резистентностью кхимиотерапевтическим препаратам (см. рис. 2) [1, 9].
Рис. 2. Преобладающий механизм действия мирамистина
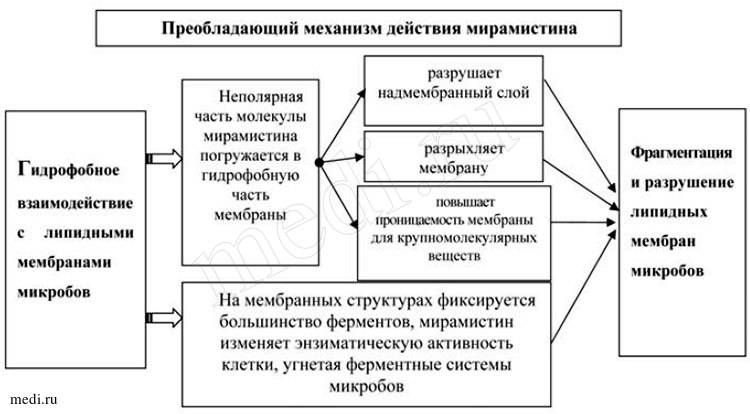
Кроме того, мирамистин характеризуется низкой токсичностью, отсутствием аллергизирующего и раздражающего действия. Мирамистин ускоряет репаративную активность, а также усиливает действие антибиотиков, снижая устойчивость бактерий и грибов к ним; обладает противовоспалительным действием; эффективно действует на патогенные микроорганизмы, не оказывая при этом отрицательного действия на ткани организма человека; повышает местный иммунитет - стимулирует защитные реакции в месте применения за счет активации поглотительной и переваривающей функции фагоцитов; потенцирует активность моноцитарно-макрофагальной системы (см. рис. 2) [25].
В ходе исследования мирамистин применялся для лечения кандидоза слизистой оболочки полости рта в виде бактерицидной повязки. Курс лечения кандидоза составил 21 день.
Спектр антимикробного действия мирамистина довольно широк и включает грамположительные (стрептококки, стафиллококки), грамотрицательные (гонококки, эшерихии, вибрионы, спирохеты, шигеллы, сальмонеллы), а также вирусы гриппа, герпеса, грибы рода Candida и простейшие [9, 11, 12, 20, 33].
Изучение фармакодинамических свойств мирамистина показало, что наряду с антимикробным действием препарат стимулирует репаративные процессы и функциональную активность иммунокомпетентных клеток, оказывая иммуномодулирующее действие в патологическом очаге [18]. При комбинированном применении мирамистина с антибиотиками он замедляет развитие резистентности микрофлоры к антибиотикам [21]. Мирамистин устойчив во внешней среде. Действие мирамистина представлено на рис. 3.
Рис. 3. Действие мирамистина
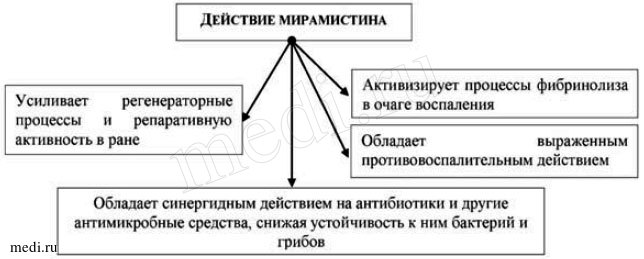
Конечно, нельзя исключать и возможность общего воздействия на обменные процессы. Поэтому автор статьи рекомендует включать в комплекс терапии расшлаковку (детоксикацию) ЖКТ (полисорб, лактофильтрум, активированный уголь), лечение дисбактериоза (нормофлорин-Л и нормофлорин-Б, биовестин-лакто) [2].
Таблица 2. Количественное определение состояния индексов индивидуальной гигиены полости рта до лечения
| Возраст | Индексы индивидуальной гигиены полости рта | |||
| Silness-Loe | РМА | Kotzschke | SBI | |
| 20-30 | 0,95 | 30% | II степень | 4 |
| 31-40 | 1,5 | 45% | II степень | 4 |
| 41-50 | 2,6 | 60% | II степень | 4 |
| Средний показатель | 1,68 | от 30% до 60% (средняя степень тяжести гингивита) | II степень | 4 |
Таблица 3. Количественное определение состояния индексов индивидуальной гигиены полости рта при лечении кандидоза в динамике
| Возраст | Индексы индивидуальной гигиены полости рта | |||||||
| Silness-Loe | РМА | Kotzschke | SBI | |||||
| 3 нед. | 3 мес. | 3 нед. | 3 мес. | 3 нед. | 3 мес. | 3 нед. | 3 мес. | |
| 20-30 | 0,3 | 0,2 | 6% | 5% | I степень | I степень | 1 | 1 |
| 31-40 | 0,8 | 0,7 | 16% | 14% | I степень | I степень | 1 | 1 |
| 41-50 | 1,6 | 1,4 | 22% | 20% | I степень | I степень | 1 | 1 |
| Средний показатель | 0,9 | 0,77 | от 6% до 22% | от 5% до 30% | I степень | I степень | 1 | 1 |
| легкая степень тяжести гингивита | ||||||||
Таблица 4. Количественные данные исследования применения мирамистина в комплексе с медикаментозной терапией при лечении пациентов с диагнозом кандидоз слизистой оболочки полости рта*
| Кол-во пациентов** | Отсутствие признаков заболевания | ||
| Через 3 нед.*** | Через 3 мес.*** | ||
| Число пациентов | 50 человек | 84% (43 человек) | 90% (45 человек) |
Таблица 5. Данные бактериологического исследования материала при применении мирамистина в комплексе с медикаментозной терапией при лечении пациентов с диагнозом кандидоз слизистой оболочки полости рта*
| Динамика изменения количества пациентов с наличием грибов рода Candida | |||
| До начала лечения | Через 3 нед.** | Через 3 мес.** | |
| Число пациентов | 50 | 7 | 5 |
| % | 100 | 14 | 10 |
Результаты исследования и их обсуждение
Оценка эффективности лечения складывалась из совокупности субъективных и объективных данных, полученных в процессе исследования. В качестве субъективных данных рассматривались наличие или отсутствие жалоб у пациента, а также оценка врачом клинической картины заболевания.
Оценка основных показателей пародонтологического статуса включала: количественное определение уровня гигиены полости рта с использованием индекса РМА, индекса Silness-Loe (Silness I., Loe H.), индекса Kotzschke (1975), индекса кровоточивости десневой борозды (SBI) (Muehlemann, Son, 1971) [28].
Оценка гигиенического состояния полости рта проводилась по количеству зубного налёта. Индекс гигиены Silness-Loe основан на определении количества мягкого зубного налёта в придесневой борозде. Папиллярно-маргинально-альвеолярный индекс предназначен для оценки тяжести гингивита. Наличие воспалительных заболеваний пародонта является одним из показателей кандидоза. Индекс Kotzschke (1975) фиксирует кровоточивость по данным анамнеза. Индекс кровоточивости десневой борозды (SBI) (Muehlemann, Son, 1971) учитывает кровотечение из десневой борозды, возникающее при зондировании, а также гиперемию, припухлость и отек десны (см. табл. 2-3 и рис. 4-5).
Рис. 4. Количественное определение индекса Silness-Loe
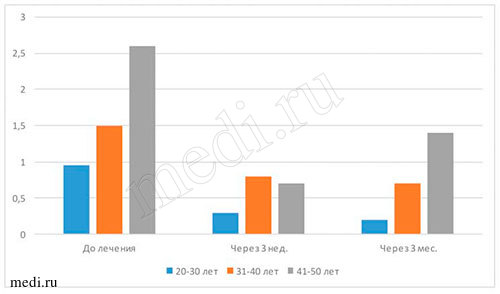
Рис. 5. Количественное определение индекса РМА
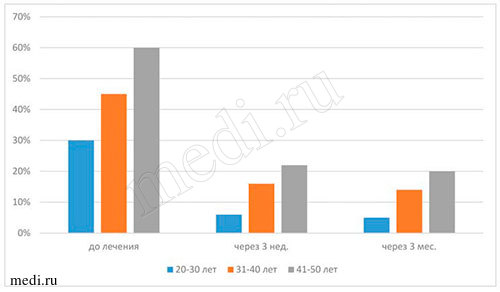
Рис. 6. Данные бактериального посева на определение содержания грибов рода Candida и отсутствие почкующегося мицелия на дорсальной поверхности языка во всех возрастных группах исследуемых при применении мирамистина в комплексе с медикаментозной терапией пациентов с диагнозом кандидоз слизистой оболочки полости рта
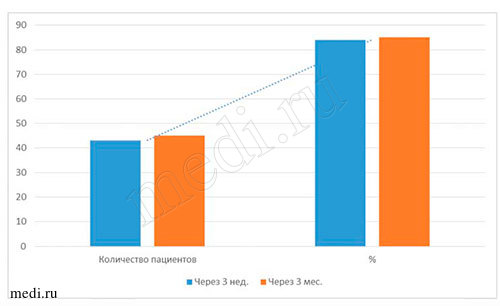
Рис. 7. Данные бактериологического исследования материала при применении мирамистина в комплексе с медикаментозной терапией пациентов с диагнозом кандидоз слизистой оболочки полости рта
Изучение динамики воспалительного процесса на фоне лечения в различных возрастных группах пациентов свидетельствует о следующем:
- кровоточивость десен при чистке зубов(индекс Kotzschke) - до начала лечения II степень, после лечения - снизилась до I степени; припухлость и отек десен отсутствовали, отмечались незначительная гиперемия десен и кровотечение из десневой борозды при зондировании (индекс SBI до начала лечения соответствовал 4, а после лечения равен 1); снизилось количество мягкого зубного налета в придесневой борозде (индекс Silness-Loe - до начале лечения - 1,68, а в конце лечения - 0,9); индекс РМАдо начала лечения находился в интервале от 30% до 60%, в конце лечения - от 6% до 22% (до начала лечения отмечалась средняя степень гингивита, а в конце лечения - легкая степень гингивита).
Следует отметить, что числовые значения вышеуказанных показателей через 3 месяца после лечения незначительно снизились.
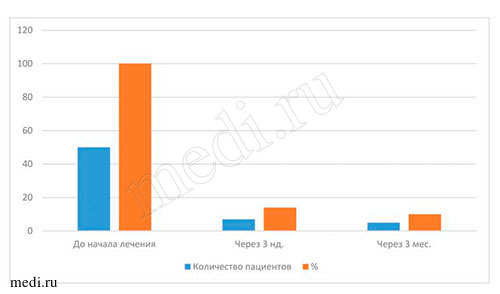
Наиболее объективными показателями эффективности лечения пациентов всех возрастных групп с диагнозом кандидоз слизистой оболочки полости рта являются результаты, полученные при бактериологических исследованиях материала на определение содержания грибов рода Candida на дорсальной поверхности языка. По полученным данным, во всех исследуемых возрастных группах пациентов до начала лечения мирамистином грибы рода Candida были выявлены у 100% (50 человек), через 3 нед. - приближались к норме (14% - у 7 чел.), через 3 мес. - отмечены единичные проявления (10% - 5 человек). Данные, полученные через 3 нед. и 3 мес. после курса лечения, свидетельствуют о прогрессирующей динамике лечения мирамистином в комплексе с другими препаратами (см. выше) пациентов с диагнозом кандидоз слизистой оболочки полости рта во всех возрастных группах. По моему мнению, незначительное количество грибов рода Candida на дорсальной поверхности языка у пациентов всех возрастных групп могло быть обусловлено многими факторами, например, ремиссией заболевания, возрастными изменениями организма, особенностями иммунитета, географией проживания,экологией местности и т.д. (см. табл. 4-5 и рис. 6-7).
Заключение
Применение мирамистина в комплексе с медикаментозной терапией кандидоза полости рта в течение 3 мес. уменьшает тяжесть воспалительного процесса и образование зубного налета и обеспечивает стойкий положительный клинический эффект, что подтверждается длительной нормализацией цитологических и микробиологических показателей.
Данные, полученные при проведенном исследовании, ярко свидетельствуют о том, что при лечении кандидоза слизистой оболочки полости рта необходимо воздействовать не только на возбудителя инфекционного процесса, но и на все предрасполагающие факторы заболевания. Терапия, направленная на все звенья патологического процесса, позволяет повысить эффективность лечения и, кроме того, способствует достижению длительного периода ремиссии заболевания.

Дата публикации: 13.03.2020 2020-03-13
Статья просмотрена: 23 раза
Большинство популяций населения Европы колонизировано дрожжеподобной флорой, в основном грибами Candida, однако в последние в одиночку не способны быть необходимой и достаточной причиной болезни, поэтому их нельзя расценить как истинных паразитов [4,5].
Вместе с тем, считается, что при нарушении иммунной защиты, в том числе под действием персистирующей вирусной инфекции, обретение Candida агрессивных свойств в полостях, выстланных слизистыми оболочками, становится реальностью. Когда в просвете полостей и трубчатых структурах устанавливаются различные сочетания Candida с бактериями, вирусами и подобная интеграция не сопровождается инвазией гриба в слизистые оболочки, она оценивается как кандидоносительство. Дрожжеподобные резиденты долгое время стабильны по качеству и количеству, они не опасны для людей без нарушения местных защитных барьеров слизистых оболочек, иммунодефицитов и нейтропении [2].
При непосредственном микроскопическом изучении нативного материала или посеве на питательные среды грибы рода Candida могут быть выделены из ротовой полости и слюны, однако даже количественная оценка высевов свидетельствует лишь о вероятности развития кандидоза, поскольку известно, что увеличение популяции грибов рода Candida у отдельных индивидуумов может не сопровождаться возникновением инвазивного процесса. Иммунологические критерии также могут служить надёжной основой дифференциальной диагностики носительства и кандидоза [1].
Отсутствие или наличие инвазии Candida стало для цитоморфологов определяющим в дифференциации кандидоносительства и кандидоза как инвазивного инфекционного заболевания (2). Однако всё оказалось значительно сложнее. Прежде всего морфологический метод (цитологический) не мог стать универсальным в прижизненной диагностики, потому что, основанный на поиске псевомицелия- активной тканевой формы Candida, он имеет ограничения по чувствительности. Нужно всегда помнить о миниатюрности биоптата. Следует учитывать, что если исследуемый фрагмент биоматериала (соскоб со слизистых оболочек, биопсия) не содержит псевдомицелия, нет гарантии отсутствия кандидозной инвазии в соседних участках ткани. По самым оптимистическим данным, частота обнаружения в биоптате псевдомицелия составляет менее 10–15 % [3,4].
Поэтому исследователи стали говорить о косвенных признаках возможной инвазии, которым часто относят часто встречающиеся почкующиеся формы дрожжеподобных клеток и ростковых трубок, свидетельствующие об активном состоянии грибов [4,5]. Однако это предположение всегда требует дополнительного подтверждения. Вышеизложенное, с одной стороны, определило возврат к оценке дополнительных возможностей методов иммунодиагностики, а с другой, — к разработке молекулярных методов, в частности, полимеразной цепной реакции (ПЦР).
Поломка в системе многоуровневого антифунгального барьера, количественные и качественные нарушения со стороны нейтрофилов в просветах и на поверхности слизистых оболочек, а также изменения в T-клеточной системе и экспрессии маркеров клеточной кооперации обусловливают возможность агрессии в виде адгезии, колонизации и инвазии резидентных условно патогенных грибов.
При прижизненной диагностики кандидоносительства, просветочного прединвазивного и инвазивного кандидоза, основанной на комплексном подходе, должна быть предусмотрена возможность своевременного выявления отличающихся друг от друга форм взаимодействия Candida и макроорганизма, что определяет их более адекватное этиологическое и патогенетическое лечение.
Всего было обследовано 12 больных разными формами кандидоза слизистой оболочки полости рта (СОПР) и пародонтита, в том числе 5 мужчин и 8 женщина в возрасте от 23 до 69 лет. Для подтверждения диагноза были использованы клинические и лабораторные-цитоморфологический, культуральный, иммуноферментный и молекулярный методы.
По результатам комплексного клинико-лабораторного и иммуномикробиологического исследования выявлены следующие формы кандидоза:
- острый гиперпластический кандидоз у 1 пациентов.
- хронический гипертрофический кандидоз у 6 пациентов.
- хронический атрофический кандидоз у 3 пациентов.
- кандида-ассоциированный пародонтит у 2 пациентов.
Анализ клинической картины кандидоза СОПР показал, что частота выявления кандида-ассоциированного пародонтита при отсутствии явных клинических проявлений кандидоза СОПР оказалось довольно значительной-у четверти пациентов. Диагноз кандидоз у всех пациентов подтвержден цитоморфологически.
При микроскопическом исследовании (окраска по Граму) у обследованных пациентов обнаружен псевдомицелий гриба в материале пародонтального кармана, взятого при завершении процедуры кюретажа пародонтальных карманов.
При идентификации выделенных чистых культур грибов установлено, что у 8 больных из 12 выделялся вид Candida albicans (у 80 % больных), причем у восьми пациентов в ассоциации с другими видами: C.krusei у четырех,C.guilliermondii у двух, С.glabrata у двух.
Читайте также:


