Эритематозная гастропатия кандидоз пищевода
Оппортунистические инфекции, включая микозы органов пищеварения, представляют собой актуальную проблему современной гастроэнтерологии.
Оппортунистические инфекции, включая микозы органов пищеварения, представляют собой актуальную проблему современной гастроэнтерологии. Диагностика и лечение кандидоза пищевода в ряде случаев сопряжены с определенными трудностями.
Дрожжеподобные грибы рода Candida — одноклеточные микроорганизмы размерами 6–10 мкм. Эти дрожжи диморфны: в различных условиях они образуют бластоспоры (клетки-почки) и псевдомицелий (нити удлиненных клеток). Эта морфологическая особенность имеет, как будет показано ниже, важное клиническое значение.
Исход контакта с дрожжеподобными грибами рода Candida обусловлен состоянием системы антифунгальной резистентности индивида. В большинстве случаев такой контакт формирует транзиторное кандидоносительство, когда структуры и механизмы антифунгальной резистентности обеспечивают деконтаминацию макроорганизма. В то же время у лиц с нарушениями в системе антифунгальной резистентности контакт может сформировать как персистирующее носительство, так и кандидоз. Таким образом, кандидоз пищеварительного тракта имеет типичные черты оппортунистический инфекции.
Однако решающее значение в системе антифунгальной резистентности имеет функция клеток фагоцитарного ряда — полиморфноядерных лейкоцитов, в первую очередь, и, в меньшей степени, мононуклеарных фагоцитов и естественных киллеров. Специфический антифунгальный гуморальный ответ реализуется за счет синтеза В-клетками специфических противокандидозных антител классов IgA, IgM, IgG и в определенной степени IgE. Наконец, сложная кооперация дендритных клеток, Т-хелперов 1 и 2 типа, а также Т-регуляторных клеток обеспечивает адекватный специфический клеточный иммунный ответ.
Дефекты в описанной выше системе антифунгальной резистентности являются факторами, способствующими возникновению кандидоза, или так называемыми факторами риска. Группы риска по развитию кандидоза пищеварительного тракта представлены ниже.
В указанных группах кандидоз выявляют чаще обычного. Отметим, что иногда причину нарушения антифунгальной резистентности определить не удается.
Патогенез кандидоза пищеварительного тракта характеризуется последовательным прохождением грибами следующих этапов — адгезии, инвазии, кандидемии и висцеральных поражений. На первом этапе дрожжи адгезируются к эпителиоцитам какого-либо участка слизистой оболочки. В дальнейшем дефекты в системе резистентности позволяют дрожжам через трансформацию в псевдомицелий внедряться (инвазироваться) в слизистую оболочку и подлежащие ткани. Цитопения — решающий фактор, который позволяет инвазирующим грибам достигать стенки сосудов, разрушать ее и циркулировать в сосудистом русле. Такой этап называют кандидемией. В отсутствие адекватной терапии кандидемия приводит к образованию очагов инвазивного кандидоза в висцеральных органах, например, печени, легких, центральной нервной системе и др.
Парадоксально, но внедрение грибов рода Candida чаще наблюдается в участках, представленных многослойным эпителием (полость рта, пищевод) и значительно реже в однослойный эпителий (желудок, кишечник).
На практике клиницисту приходится сталкиваться преимущественно с кандидоносительством, частота которого у здоровых лиц достигает в полости рта 25%, а в кишечнике — до 65–80%.
Объем обследования при кандидозе органов пищеварения включает изучение анамнеза и клинической картины, оценку рутинных клинических тестов, эндоскопические исследования, микологические (культуральные, морфологические и серологические) и иммунологические тесты.
Кандидоз пищевода встречается у больных общего профиля в 1–2% случаев, у больных сахарным диабетом 1 типа — в 5–10% случаев, у больных СПИДом — в 15–30% случаев. В то же время, по сообщению Yoo S.S. и соавт., при эндоскопическом исследовании 6683 практически здоровых лиц у 0,25% выявлен кандидоз пищевода. Среди местных факторов риска называют ожог, ахалазию, дивертикулез, полипоз пищевода. Характерными жалобами являются дисфагия, одинофагия, ретростернальный дискомфорт, однако встречается и латентное течение. Симптомы кандидоза пищевода могут нарушить акт глотания, что в свою очередь приводит к нарушению питания и значительному снижению качества жизни.
Показаниями для эндоскопического исследования с целью исключения кандидоза пищевода является: группа риска, клинические признаки эзофагита и верифицированный кандидоз других локализаций (например, орофарингеальный, кандидоз урогенитальной системы, диссеминированный кандидоз).
Эндоскопические признаки кандидоза пищевода — гиперемия и контактная ранимость слизистой оболочки, а также фибринозные налеты различной локализации, конфигурации и размеров. Среди всего разнообразия визуальных признаков кандидоза пищевода можно выделить три группы типичных изменений:
Напомним, что схожие эндоскопические изменения могут наблюдаться при рефлюкс-эзофагите, пищеводе Барретта, герпес-эзофагите, плоских лейкоплакиях, красном плоском лишае, ожоге или опухоли пищевода. Поэтому диагностика кандидоза пищевода основана на эндоскопическом исследовании и лабораторном изучении биопсийных материалов из пораженных участков. Необходимо учитывать, что при однократной биопсии чувствительность лабораторных методов недостаточна.
С целью обнаружения псевдомицелия используют морфологические микологические методы: цитологический — с окраской мазков по Романовскому–Гимза, и гистологический — с окраской биоптатов ШИК-реакцией. Таким образом, учет диморфности Candida spp. является ключом к дифференциальному диагнозу между кандидозом и кандидоносительством. В современных условиях клиницист должен требовать от морфолога точного описания морфологических структур гриба, ведь обнаружение отдельных дрожжевых клеток, как правило, свидетельствует о кандидоносительстве, а обнаружение псевдомицелия позволяет подтвердить диагноз кандидоза.
К недостатку морфологических методов можно отнести их ограниченную чувствительность при эндоскопической биопсии. Известно, что биопсионные щипцы позволяют получить для изучения миниатюрный фрагмент ткани, и вероятность обнаружения информативного признака при однократной биопсии недостаточна.
Культуральное исследование биоматериалов слизистых оболочек с определением вида возбудителя становится строго необходимым при рецидивирующем течении кандидоза или резистентности к стандартной антимикотической терапии.
Чувствительность и специфичность серологических тестов диагностики кандидоза пищевода (иммуноферментный анализ с антигеном Candida, уровень специфического IgE, тест латекс-агглютинации Platelia) пока не достигли требуемой точности и в практике применяются редко.
Кандидоз пищевода, даже протекающий субклинически, опасен своими осложнениями — стриктурой, кровотечением, перфорацией и диссеминацией микотического поражения.
Рентгенографический метод при кандидозе органов пищеварения малоинформативен, так как не уточняет этиологии процесса, но при развитии осложнений (например, стриктура, язва, перфорация) приобретает решающее значение.
Развитие стриктуры пищевода отмечают у 8–9% пациентов с кандидозным эзофагитом. Чаще они локализованы в верхней или средней трети грудного отдела пищевода и вызывают перманентную дисфагию. Другим частым осложнением кандидоза верхних отделов органов пищеварения является кровотечение, вызванное контактной ранимостью слизистой оболочки. Такое хроническое малоинтенсивное кровотечение приводит к анемии, а у пациентов с цитопенией кровотечение может развиваться стремительно (нередко наблюдается рвота алой кровью и псевдомембранозными массами) и приводить к серьезной потери крови. Клиническая картина перфорации пищевода характеризуется, кроме интенсивного болевого синдрома, развитием пневмомедиастинума и подкожной эмфиземы в области шеи.
Лечение кандидоза пищевода основано на применении антифунгальных препаратов. Общий принцип действия всех антифунгальных средств — угнетение биосинтеза эргостерина клеточной стенки дрожжей. Антифунгальные средства, используемые для лечения кандидоза в целом, можно разделить на три группы. Первая группа — полиеновые антимикотики, практически нерезорбируемые при приеме per os. К ним относят амфотерицин В, нистатин и натамицин. Вторая группа — азольные антимикотики, относительно хорошо резорбируемые при приеме per os. К ним относятся: кетоконазол, флуконазол, итраконазол, вориконазол, позаконазол. Третья группа — эхинокандины: каспофунгин, анидулафунгин, микафунгин.
Цель лечения кандидоза слизистых оболочек верхних отделов пищеварительного тракта — устранение симптомов и клинико-лабораторных признаков заболевания, а также предотвращение рецидивов.
Нужно подчеркнуть, что при кандидозе пищевода местная терапия неэффективна. У больных с выраженной одинодисфагией, которые не способны глотать, должна использоваться парентеральная терапия.
Препаратом выбора для лечения кандидоза пищевода является флуконазол 100–200 мг/сут, назначаемый перорально или внутривенно в течение 2–4 нед. Подчеркнем, что как средство лечения кандидоза пищевода флуконазол превосходит по эффективности и кетоконазол, и итраконазол в капсулах из-за непостоянной абсорбции последних.
Лишь в случаях непереносимости флуконазола или резистентности возбудителя (чаще это C. krusei, C. glabrata, C. pseudotropicalis) показаны препараты второй линии (также в течение 2–4 недель ). Препаратами второй линии при кандидозе пищевода являются:
Необходимо добавить, что применение нерезорбируемых антимикотиков (нистатин, натамицин) неэффективно.
Несмотря на высокую эффективность флуконазола у пациентов с сохраняющимся иммунодефицитным состоянием высока вероятность рецидивов кандидоза пищевода. Необходимо помнить, что безрецидивного течения кандидоза можно достичь только у больных с полной коррекцией фонового состояния. Так, например, при СПИДе рецидивы кандидоза прекращаются только при успешной антиретровирусной терапии, обеспечивающей снижение вирусной нагрузки и увеличение числа CD4-лимфоцитов.
Для предотвращении рецидивов может быть эффективна длительная поддерживающая терапия флуконазолом (100мг/день) или назначение дозы флуконазола 200 мг еженедельно.
Литература
М.А. Шевяков, доктор медицинских наук, профессор СПбМАПО, Санкт-Петербург
Оппортунистические инфекции, включая микозы органов пищеварения, представляют собой актуальную проблему современной гастроэнтерологии. Диагностика и лечение кандидоза пищевода в ряде случаев сопряжены с определенными трудностями.
Патогенез
Дрожжеподобные грибы рода Candida — одноклеточные микроорганизмы размерами 6-10 мкм. В различных условиях они образуют бластоспоры (клетки-почки) и псевдомицелий (нити удлиненных клеток). Дрожжи рода Candida широко распространены в окружающей среде: в почве, питьевой воде, пищевых продуктах, на коже и слизистых оболочках человека и животных. Исход контакта с дрожжеподобными грибами рода Candida обусловлен состоянием системы антифунгальной резистентности индивида. В большинстве случаев такой контакт формирует транзиторное кандидоносительство. В то же время у лиц с нарушениями в системе антифунгальной резистентности контакт может сформировать как персистирующее носительство и как кандидоз.
Перечисленным факторам патогенности естественным образом противостоят многочисленные факторы:
- целостность слизистой оболочки и мукополисахариды слизи;
- антагонизм дрожжеподобных грибов и бактерий пищеварительного тракта;
- активность пищеварительных ферментов и фунгистатического действия неспецифических гуморальных факторов, таких как лизоцим;
- функция клеток фагоцитарного ряда — полиморфноядерных лейкоцитов;
- специфический антифунгальный гуморальный ответ (реализуется за счет синтеза В-клетками специфических противокандидозных антител).
Дефекты в описанной выше системе антифунгальной резистентности являются факторами, способствующими возникновению кандидоза.
1. Физиологические иммунодефициты (детский, старческий возраст, беременность).
2. Генетически детерминированные (первичные) иммунодефициты.
4. Онкологические заболевания, особенно на фоне лучевой и химиотерапии.
5. Аллергические и аутоиммунные болезни, особенно на фоне лечения глюкокортикостероидами.
6. Заболевания эндокринной системы, в первую очередь, сахарный диабет, аутоиммунный полиэндокринный синдром, гипотиреоз, ожирение и др.
7. Дисбиоз на фоне антибиотикотерапии.
9. Трансплантация органов и тканей.
Внедрение грибов рода Candida чаще наблюдается в участках, представленных многослойным эпителием (полость рта, пищевод) и значительно реже - в однослойный эпителий (желудок, кишечник).
На практике клиницисту приходится сталкиваться, преимущественно, с кандидоносительством, частота которого у здоровых лиц достигает в полости рта 25%, а в кишечнике — до 65–80%.
Диагностика
Объем обследования органов пищеварения при кандидозе включает изучение анамнеза и клинической картины, оценку рутинных клинических тестов, эндоскопические исследования, микологические (культуральные, морфологические и серологические) и иммунологические тесты.
Кандидоз пищевода встречается у больных общего профиля в 1–2% случаев, у больных сахарным диабетом 1 типа — в 5–10% случаев, у больных СПИДом — в 15–30% случаев.
Среди местных факторов риска называют ожог, ахалазию, дивертикулез, полипоз пищевода.
Характерными жалобами являются дисфагия, одинофагия, ретростернальный дискомфорт, однако встречается и латентное течение.
Симптомы кандидоза пищевода могут нарушить акт глотания, что в свою очередь, приводит к нарушению питания и значительному снижению качества жизни.
Показаниями для эндоскопического исследования с целью исключения кандидоза пищевода является: группа риска, клинические признаки эзофагита и верифицированный кандидоз других локализаций.
Среди всего разнообразия визуальных признаков кандидоза пищевода можно выделить три группы типичных изменений:
2. Фибринозный (псевдомембранозный) эзофагит. Наблюдают бело-серые или бело-желтые рыхлые налеты в виде округлых бляшек диаметром от 1 до 5 мм, выступающие над ярко гиперемированной и отечной слизистой оболочкой. Контактная ранимость и гиперемия слизистой оболочки заметно выражены.
Схожие эндоскопические изменения могут наблюдаться при рефлюкс-эзофагите, пищеводе Барретта, герпес-эзофагите, плоских лейкоплакиях, красном плоском лишае, ожоге или опухоли пищевода, поэтому диагностика кандидоза пищевода основана на эндоскопическом исследовании и лабораторном изучении биопсийных материалов из пораженных участков.
Культуральный микологический метод основан на посеве биоматериалов слизистых оболочек на среду Сабуро. Преимущество данного метода — в возможности видовой идентификации грибов рода Candida и тестировании культуры на чувствительность к антимикотикам. Культуральное исследование биоматериалов слизистых оболочек с определением вида возбудителя становится строго необходимым при рецидивирующем течении кандидоза или резистентности к стандартной антимикотической терапии.
Осложнения
Кандидоз пищевода опасен своими осложнениями: стриктурой, кровотечением, перфорацией и диссеминацией микотического поражения.
Развитие стриктуры пищевода отмечают у 8–9% пациентов с кандидозным эзофагитом. Чаще они локализованы в верхней или средней трети грудного отдела пищевода и вызывают перманентную дисфагию.
Хроническое кровотечение вызвано контактной ранимостью слизистой оболочки, оно малоинтенсивное, приводит к анемии.
Клиническая картина перфорации пищевода характеризуется, кроме интенсивного болевого синдрома, развитием пневмомедиастинума и подкожной эмфиземы в области шеи.
Лечение
В план ведения пациентов с кандидозом пищевода необходимо включить диагностику и коррекцию фоновых заболеваний, других очагов кандидозной инфекции, рациональную антифунгальную терапию и иммунокоррекцию. Также необходимо исключение злокачественных опухолей, рентгенография легких, фиброколоноскопия, дополнительно для мужчин — УЗИ предстательной железы, дополнительно для женщин — УЗИ молочных желез и малого таза с консультацией гинеколога.
Лечение кандидоза пищевода основано на применении антифунгальных препаратов:
- полиеновые антимикотики (амфотерицин В, нистатин и натамицин);
- азольные антимикотики (кетоконазол, флуконазол, итраконазол, вориконазол, позаконазол);\
- эхинокандины (каспофунгин, анидулафунгин, микафунгин).
Цель лечения кандидоза слизистых оболочек верхних отделов пищеварительного тракта — устранение симптомов и клинико-лабораторных признаков заболевания, а также предотвращение рецидивов.
Нужно подчеркнуть, что при кандидозе пищевода местная терапия неэффективна. У больных с выраженной одинодисфагией, которые не способны глотать, должна использоваться парентеральная терапия.
Несмотря на высокую эффективность флуконазола у пациентов с сохраняющимся иммунодефицитным состоянием высока вероятность рецидивов кандидоза пищевода. Необходимо помнить, что безрецидивного течения кандидоза можно достичь только у больных с полной коррекцией фонового состояния. Так, например, при СПИДе рецидивы кандидоза прекращаются только при успешной антиретровирусной терапии, обеспечивающей снижение вирусной нагрузки и увеличение числа CD4-лимфоцитов.
Зав. эндоскопическим отделением
Новополоцкой городской больницы
Кожушкевич А.Ю.
Приемная главного врача
(+375 214) 50-62-70
(+375 214) 50-62-11 (факс)
Канцелярия
(+375 214) 50-15-39 (факс)
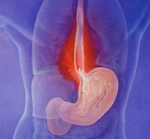
Эзофагит - это поражение слизистой оболочки пищевода воспалительного характера. Проявлениями эзофагита могут служить жгучая боль за грудиной, нарушения глотания, изжога, повышенная саливация. Осложнением эзофагита могут явиться пептическая язва, стеноз, перфорация пищевода, болезнь Барретта. Диагностический минимум состоит из проведения эзофагоскопии, эндоскопической биопсии и рентгенографии пищевода. Лечение назначается с учетом этиологии эзофагита; включает диету, медикаментозную терапию, физиотерапию; при необходимости – хирургическое лечение сужения пищевода (бужирование, рассечение рубцовых стриктур и др.).
МКБ-10



Общие сведения
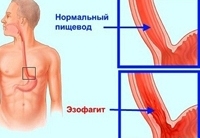
Эзофагит – воспалительное заболевание стенки пищевода острого или хронического течения. При эзофагите воспалительный процесс развивается во внутренней, слизистой оболочке пищевода и при прогрессировании может поражать более глубокие слои. Среди заболеваний пищевода эзофагит является наиболее частым, в 30-40% случаев заболевание может протекать без выраженной симптоматики.
Эзофагиты могут быть следствием различного рода повреждений слизистой пищевода или развиться вследствие инфекционного поражения, гастрита, заброса желудочного сока (иногда с желчью) из желудка. Эзофагит вследствие рефлюкса (заброса) желудочного содержимого выделяется как отдельное заболевание – гастроэзофагеальная рефлюксная болезнь.

Причины эзофагита

Острый эзофагит развивается вследствие повреждающего фактора кратковременного действия:
- острые инфекционные процессы (грипп, грибковое поражение, дифтерия и др.);
- физическое повреждение (ожог, травмирование при введении зонда, повреждение инородными телами);
- химический ожог (повреждение едкими химическими веществами);
- аллергическая реакция на пищевые продукты (как правило, сочетается с другими признаками аллергии).
Наиболее тяжелыми бывают повреждения пищевода после ожогов. В патогенезе инфекционного эзофагита основным фактором развития воспаления считается снижение иммунных свойств организма.
Причины развития хронических эзофагитов также разнообразны:
- алиментарный эзофагит (употребление очень горячей, острой пищи, крепкого алкоголя);
- профессиональный эзофагит (работа, связанная с вдыханием паров едких химических веществ);
- застойный эзофагит (раздражение слизистой остатками скопившейся пищи при разного рода затруднениях эвакуационной функции пищевода);
- аллергический эзофагит (развивается в связи с пищевой аллергией);
- дисметаболический эзофагит (связан с нарушениями обмена – гиповитаминозами, недостаточностью микроэлементов и тканевой гипоксией, продолжительной интоксикацией организма и т. п.);
- идиопатический ульцерозный эзофагит (особая форма хронического воспаления пищевода неясной этиологии, морфологически подобная язвенным колитам и гранулематозу пищевода (неспецифический регионарный стенозирующий эзофагит).
В качестве отдельного заболевания выделяют пептический, или рефлюкс-эзофагит. Он развивается вследствие гастроэзофагеального рефлюкса (заброса желудочного содержимого в пищевод). Иногда сочетается с дуодено-гастральным рефлюксом. Рефлюкс из желудка в пищевод может возникать по следующим причинам: недостаточность кардии (нижнего пищеводного сфинктера); хиатальная грыжа (грыжа пищеводного отверстия диафрагмы); недостаточная длина пищевода.
Классификация
Эзофагит по течению может быть острым, подострым и хроническим. По характеру воспалительного процесса и его выраженности в гастроэнтерологии различают катаральный, отечный, эрозивный, псевдомембранозный, геморрагический, эксфолиативный, некротический и флегмонозный эзофагиты.
Катаральный и отечный эзофагит (наиболее часто встречающиеся формы) ограничиваются гиперемией слизистой и ее отеком. При остром инфекционном процессе, а также химических и тепловых ожогах пищевода возможно развитие эрозий слизистой оболочки (эрозивный эзофагит). При тяжелом течении инфекции нередко происходит развитие некротической формы. Геморрагический эзофагит сопровождается кровоизлияниями в стенку пищевода. При псевдомембранозной форме фиброзный экссудат не сращен с подслизистой тканью в отличие от эксфолиативного эзофагита. Флегмона пищевода, как правило, развивается при повреждении стенки пищевода инородным телом.
По локализации и распространенности воспалительного процесса различают дистальный, проксимальный и тотальный эзофагит. Классификация эзофагита по степени поражения имеет различия для острого и хронического течения заболевания. Острые эзофагиты и ожоги пищевода делят на три степени:
- поверхностное поражение без эрозивных и язвенных дефектов;
- поражение всей толщи слизистой с язвенными дефектами и некрозом;
- поражение распространяется на подслизистые слои, образуются глубокие дефекты с возможностью перфорации стенки пищевода, кровотечения. После залечивания возможно образование рубцовых стриктур.
Хронический эзофагит по выраженности поражения стенки делят на 4 степени согласно классификации Савари и Миллера (классификация эндоскопических признаков хронического эзофагита):
- гиперемия без эрозивных дефектов в дистальных отделах;
- разрозненные мелкие эрозивные дефекты слизистой;
- эрозии слизистой сливаются друг с другом;
- язвенное поражение слизистой, стеноз.
Симптомы острого эзофагита
Выраженность симптоматики при остром эзофагите имеет прямую зависимость от выраженности воспалительного процесса в слизистой пищевода. При катаральной форме эзофагит может протекать без клинических симптомов, только иногда проявляясь повышенной чувствительностью пищевода к горячей или холодной пище. Тяжелые формы эзофагита проявляются выраженным болевым симптомом (острая, сильная, жгучая боль за грудиной, отдающая в шею и спину), расстройством глотания (дисфагия) из за сильной боли, изжогой, повышенным слюноотделением.
В крайне тяжелых случаях – кровавая рвота вплоть до шокового состояния. Тяжело протекающий эзофагит спустя неделю может смениться периодом мнимого благополучия (резкое стухание симптомов, возможно даже употребление твердой пищи), но без адекватного лечения спустя несколько недель (до 3-х месяцев) заживления тяжелых дефектов пищеводной стенки может привести к образованию грубых рубцов и стеноза, что приведет к прогрессированию дисфагии и регургитации пищи.
Симптомы хронического эзофагита
При рефлюкс-эзофагите основным клиническим проявлением является изжога (жжение в области эпигастрия и за грудиной). Как правило, изжога усиливается после приема жирной, острой пищи, кофе, газированных напитков. Переедание также способствует развитию симптоматики. Другими вероятными симптомами могут быть: отрыжка (воздухом, кислым, горьким с примесью желчи); ночью может проявляться регургитация. Нередки присоединения расстройств дыхания, ларингоспазм, бронхиальная астма, частые пневмонии. Симптомы нарушения дыхания проявляются, как правило, ночью, в горизонтальном положении тела.
Хронический эзофагит может протекать с болями за грудиной в районе мечевидного отростка, иррадиирующими в спину и шею. Для хронического эзофагита характерна умеренная выраженность болевого симптома.
У детей первого года жизни недостаточность сфинктера пищевода можно диагностировать по многократным умеренным срыгиваниям сразу после кормления в горизонтальном положении. При упорных срыгиваниях могут развиться симптомы гипотрофии.
Осложнения

Осложнениями эзофагитов могут стать следующие заболевания и состояния:
- пептическая язва пищевода (часто развивается при болезни Баррета), характеризуется образованием глубокого дефекта стенки пищевода, может вести к грубому рубцеванию и укорочению пищевода;
- сужение (стеноз) просвета пищевода (ведет к нарушению прохождения пищи в желудок, снижению массы тела);
- прободение стенки пищевода (перфорация) – осложнение, опасное для жизни, требует срочного хирургического вмешательства;
- гнойные осложнения эзофагита – абсцесс, флегмона (как правило, являются следствием повреждения пищевода инородным телом);
- болезнь Барретта (при продолжительном рефлюкс-эзофагите без адекватного лечения развивается перерождение эпителия пищевода – метаплазия). Пищевод Баррета – предраковое состояние.
Диагностика

Если острый эзофагит проявляется клинической симптоматикой, то диагностика этого заболевания, как правило, не составляет проблем – локализация болевого симптома весьма специфична и характерна. Опрос позволяет выявить вероятную причину развития эзофагита. Для подтверждения диагноза используется:
- Эзофагоскопия. Показывает изменения в слизистой, их выраженность. Проведение эндоскопического обследования пищевода проводят не ранее чем на шестой день после проявления выраженной клинической картины. Показания для эндоскопического обследования выявляются индивидуально. При необходимости берут эндоскопическую биопсию слизистой и исследуют гистологически.
- Манометрия. Нарушения моторной функции пищевода выявляются с помощью эзофагоманометрии.
- Рентген.Рентгенография пищевода позволяет выявить изменения контуров пищевода, изъязвления, отек стенки и скопление слизи.
Лечение эзофагита
Эзофагит вследствие химического ожога требует срочного промывания желудка для удаления химического агента. Для лечения легких форм острых эзофагитов больным рекомендовано воздерживаться от приемов пищи 1-2 дня, медикаментозное лечение заключается в приеме антацидов и препаратов группы фамотидина. После начала питания исключают продукты, способные повредить слизистую (алкоголь, кофе, горячая, острая, грубая пища) и пища, активизирующая выработку желудочного сока (шоколад, жирные продукты). Всем больным эзофагитом рекомендован отказ от курения.
При тяжелом протекании болезни - бережное питание вплоть до отказа от энтерального питания, обволакивающие и гелевые антацидные препараты. При выраженной интоксикации проводится инфузионная терапия с помощью дезинтоксикационных растворов. Для подавления инфекционного процесса показана антибиотикотерапия.
При язвенном эзофагите с выраженным болевым симптомом прописано обезболивание и противопоказано промывание желудка. При безуспешности массированного лечения антибиотиками очагов гнойного воспаления (флегмона, абсцесс) – хирургическая санация. Также показанием к хирургическому лечению эзофагита является развитие тяжелой стриктуры пищевода, не поддающейся дилатации.
В терапии хронического эзофагита основное значение играет устранение фактора его возникновения. Важнейшей составляющей лечения является строгое соблюдение диеты и режима питания и образа жизни. Рекомендации по диете в период острых клинический проявлений: употребление умеренного количества мягкой протертой пищи комнатной температуры. Исключение из рациона продуктов, оказывающих раздражающее действие на слизистую – острые, жирные, жареные, газированные, алкоголесодержащие продукты. Также исключают пищу, содержащую большое количество клетчатки.
Больным эзофагитом необходимо отказаться от курения и приема лекарственных препаратов, влияющих на тонус сфинктера пищевода (седативные препараты, транквилизаторы, теофиллин, простагландины и т. п.). Также следует отказаться от приемов пищи не менее чем за полтора-два часа до сна, не принимать горизонтальное положение после еды, не проводить много времени наклонясь. Спать рекомендуется на приподнятом изголовье. Терапия хронического эзофагита:
- препараты, снижающие кислотность желудочного сока (антациды – оптимальным выбором являются гелевые антациды с анестетиками, ингибиторы протоновой помпы, блокаторы Н2-гистаминовых рецепторов);
- препараты, усиливающие тонус кардии (нижнего сфинктера пищевода и ускоряющие продвижение пищевого комка из желудка в двенадцатиперстную кишку (блокаторы дофа-рецепторов и холиномиметики).
- при рефлюкс-эзофагите хороший результат дает амплипульстерапия;
- снижение болевого синдрома достигается сеансами электрофореза ганглиоблокаторов;
- грязелечение и бальнеотерапия.
При тяжелом течении рефлюкс-эзофагита со стриктурами, язвами и стенозом физиотерапия противопоказана. Операции при стенозе пищевода заключаются в эндоскопическом рассечении стриктур, расширении или бужировании пищевода. По показаниям проводится резекция и пластика пищевода.
Прогноз и профилактика
При отсутствии осложнений (стеноз, перфорации, кровотечение, воспаление средостения и т. п.) прогноз благоприятен. Важным фактором в перспективе излечения эзофагита является строгое соблюдение режима питания, образа жизни и рекомендаций по диете.
Профилактика эзофагитов подразумевает избегание причин его развития – ожогов горячей пищей, химическими веществами, повреждений инородными телами и т. п. Профилактика хронического эзофагита – регулярное диспансерное обследование у гастроэнтеролога и при необходимости – лечение. Больным хроническим эзофагитом в качестве профилактики обострений показано санаторно-курортное лечение.
Читайте также:


