Увеличен твп плода из-за герпеса
Самые часто встречающиеся ультразвуковые маркеры хромосомной аномалии:
Оценка этого параметра проводится в первое скрининговое УЗИ (11-14 недель)
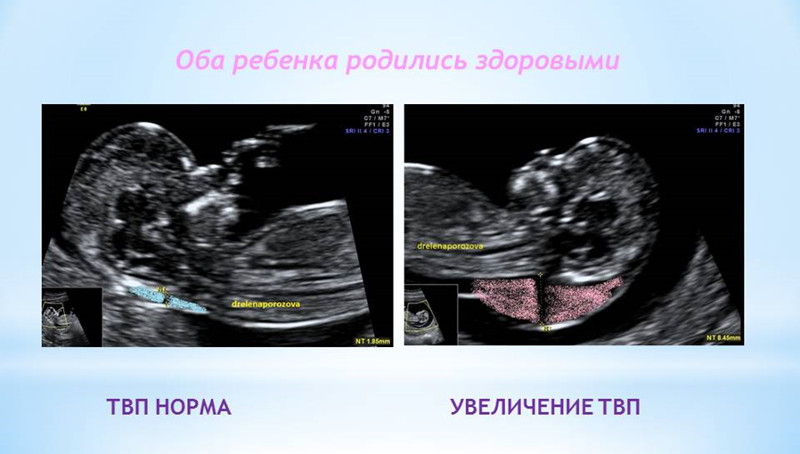
ТВП (толщина воротникового пространства) может оказаться больше нормы по нескольким причинам.
Почему у плода может выявляться увеличение ТВП?
Родители бывают крайне взволнованы и хотят сразу же получить ответы на все, возникающие у них вопросы – с чем связано, что делать и многие другие. Вопросы, на которые невозможно ответить сразу. Ведь причин увеличения ТВП множество. Данная находка может встречаться у абсолютно здоровых плодов, это не порок развития, это лишь сигнал к более глубокому обследованию, потому что такая особенность может иметь место у плодов с хромосомной патологией, аномалиями сердца либо другими врожденными или наследственными заболеваниями. При увеличении максимального порога ТВП ВАЖНО, чтобы врач оценил все остальные ультразвуковые маркеры (признаки), а также провел детальную оценку анатомии плода. Возможно, причина увеличения ТВП кроется в нарушении развития плода (например, аномалии строения сердца).
Что делать при выявлении увеличения ТВП у плода?
Если у вашего плода обнаружили расширение ТВП, Вас обязательно направят на консультацию к врачу генетику, который собрав анамнез, оценив все риски, даст рекомендации по дополнительным методам исследования (инвазивная диагностика). Далее потребуется экспертное УЗИ плода на сроке 20 недель для детальной оценки анатомии. Если по всем этим исследованиям отклонений не выявлено, то шансы родить здорового ребенка велики даже при значительной величине ТВП.
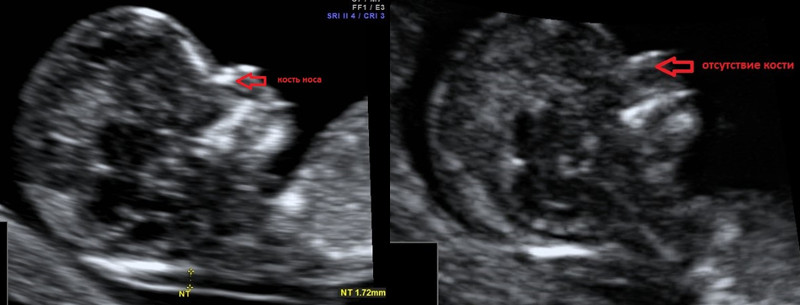
Гипоплазия костей носа – уменьшение размеров косточки носа в зависимости от КТР вашего малыша.
Аплазия костей носа – отсутствие визуализации косточки носа у вашего малыша.
Отсутствие видимости костной части спинки носа у плода или ее недоразвитие (недостаточно яркая) на первом скрининге связана с задержкой отложения кальция. Такая ситуация несколько чаще может встречаться у плодов с синдромом Дауна, однако важно, что:
- само по себе отсутствие костей носа на УЗИ не является аномалией развития; может встречаться у абсолютно здоровых плодов (в 3% случаев);
- для оценки степени индивидуального риска необходима оценка остальных ультразвуковых маркеров (толщина воротникового пространства плода, показатели кровотока на сердечном клапане, показатели кровотока в венозном протоке, ЧСС плода) и биохимического анализа материнской сыворотки (РАРР-А, ХГЧ);
- Если результат комбинированного скрининга (оценка в специальной программе данных УЗИ и анализа крови) показывает НИЗКИЙ риск хромосомной патологии – беспокоиться не стоит. Обязательно пройдите контрольное УЗИ в 19-20 недель беременности, где будет проведена тщательная оценка анатомии плода и исследованы определенные ультразвуковые маркеры второго триместра беременности.
- Что делать если результат комбинированного скрининга оказался ВЫСОКИМ? – Переживать не стоит. Вас обязательно направят на консультацию к врачу генетику, который собрав анамнез, оценив все риски, даст рекомендации по дополнительным методам исследования (инвазивная диагностика).
Это термин, говорящий о повышенной эхогенности (яркости) кишечника на ультразвуковом изображении. Выявление гиперэхогенного кишечника НЕ является пороком развития кишечника, а просто отражает характер его ультразвукового изображения. Необходимо помнить, что эхогенность нормального кишечника выше, чем эхогенность соседних с ним органов (печени, почек, легких), но такой кишечник не считается гиперэхогенным. Гиперэхогенным называется только такой кишечник, эхогенность которого сравнима с эхогенностью костей плода.
Почему кишечник у плода может быть гиперэхогенным?
Иногда гиперэхогенный кишечник выявляется у абсолютно нормальных плодов, и при УЗИ в динамике этот признак может исчезать. Повышенная эхогенность кишечника может быть проявлением хромосомных болезней плода, в частности, синдрома Дауна. В связи с этим при обнаружении гиперэхогенного кишечника проводится тщательная оценка анатомии плода. Однако при выявлении гиперэхогенного кишечника можно говорить лишь о повышенном риске синдрома Дауна, так как подобные изменения могут встречаться и у совершенно здоровых плодов. Иногда гиперэхогенный кишечник может быть признаком внутриутробной инфекции плода. Гиперэхогенный кишечник часто обнаруживается у плодов с задержкой внутриутробного развития. Однако при этом будут обязательно выявляться отставание размеров плода от срока беременности, маловодие и нарушение кровотока в сосудах плода и матки. Если ничего из вышеперечисленного не выявлено, то диагноз задержки развития плода исключен.
Что делать при выявлении гиперэхогенного кишечника у плода?
Вам следует обратиться к специалисту генетику, который еще раз оценит результаты биохимического скрининга и даст необходимые рекомендации по дальнейшему ведению беременности.
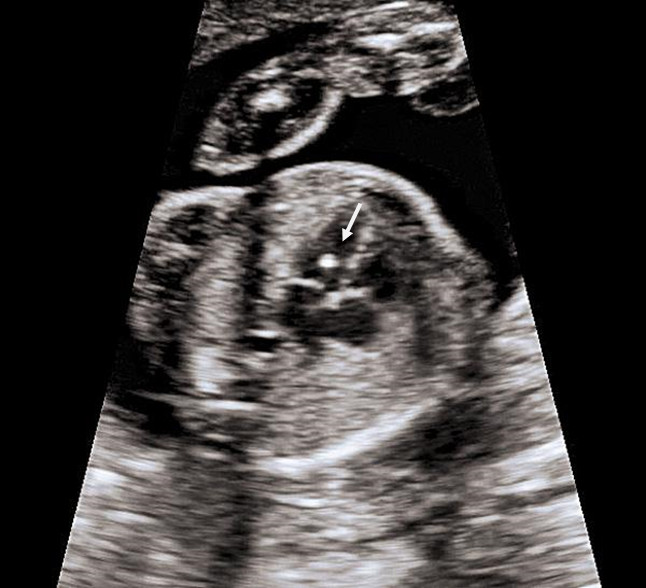
Это термин, говорящий о повышенной эхогенности (яркости) небольшого участка сердечной мышцы на ультразвуковом изображении. Выявление гиперэхогенного фокуса в сердце НЕ является пороком развития сердца, а просто отражает характер его ультразвукового изображения. Гиперэхогенный фокус возникает в месте повышенного отложения солей кальция на одной из мышц сердца, что не мешает нормальной работе сердца плода и не требует никакого лечения.
Почему у плода может выявляться гиперэхогенный фокус в сердце?
Что делать при выявлении гиперэхогенного фокуса в сердце плода?
Если у плода выявлен ТОЛЬКО гиперэхогенный фокус в сердце, то никаких дополнительных обследований не требуется; риск болезни Дауна не увеличивается. На плановом УЗИ в 32-34 недели еще раз будет осмотрено сердце плода. В большинстве случаев гиперэхогенный фокус в сердце исчезает к этому сроку беременности, но даже если он продолжает оставаться в сердце, это никак не влияет на здоровье плода и тактику ведения беременности.
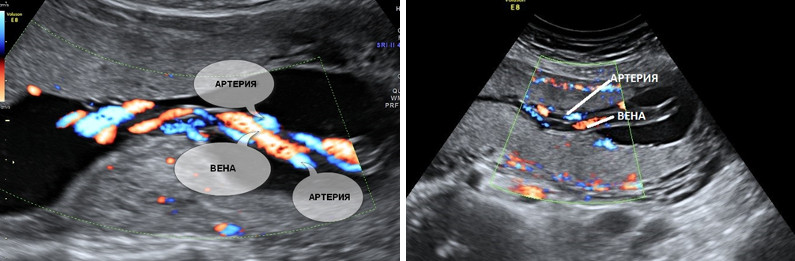
Нормальная пуповина состоит из трех сосудов – две артерии и одна вена. Иногда вместо двух артерий в пуповине формируется только одна артерия и одна вена, таким образом, в пуповине определяется всего два сосуда. Данное состояние считается пороком развития пуповины, однако этот порок не оказывает никакого влияния на послеродовое состояние ребенка и его дальнейшее развитие.
Почему у плода может определяться единственная артерия пуповины?
Что делать при выявлении единственной артерии пуповины у плода?
Выявление только единственной артерии пуповины не повышает риск наличия синдрома Дауна и не является показанием к консультации генетика и проведению других диагностических процедур. Необходимо контрольное УЗИ в 26-28 и 32 недели беременности для оценки темпов роста плода и оценки его функционального состояния.
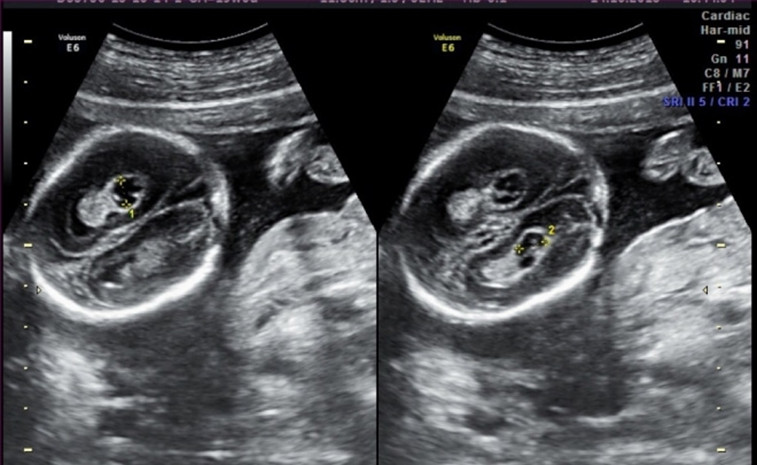
Сосудистые сплетения - одна из первых структур, которая появляется в головном мозге плода. Это сложная структура, и присутствие обоих сосудистых сплетений подтверждает, что в мозге развиваются обе половины. Сосудистое сплетение производит жидкость, питающую головной и спинной мозг. Иногда жидкость образует скопления внутри сосудистых сплетений, которые при УЗИ имеют вид "кисты". Кисты сосудистых сплетений иногда могут быть найдены при ультразвуковом исследовании в сроках 18-22 недели беременности. Наличие кист не оказывает влияния на развитие и функцию головного мозга. Большинство кист самопроизвольно исчезает к 24-28 неделям беременности.
Часто ли встречаются кисты сосудистых сплетений?
В 1-2 % всех нормальных беременностей плоды имеет КСС, в 50 % случаев обнаруживаются двусторонние кисты сосудистых сплетений, в 90 % случаев кисты самопроизвольно исчезают к 26-ой неделе беременности, число, размер, и форма кист могут варьировать, кисты также найдены у здоровых детей и взрослых. Несколько чаще кисты сосудистых сплетений выявляются у плодов с хромосомными болезнями, в частности, с синдромом Эдвардса (трисомия 18, лишняя 18 хромосома). Однако, при данном заболевании у плода всегда будут обнаруживаться множественные пороки развития, поэтому выявление только кист сосудистого сплетения не повышает риск наличия трисомии 18 и не является показанием к проведению других диагностических процедур. При болезни Дауна кисты сосудистых сплетений, как правило, не выявляются. Риск синдрома Эдвардса при обнаружении КСС не зависит от размеров кист и их одностороннего или двустороннего расположения. Большинство кист рассасывается к 24-28 неделям, поэтому в 28 недель проводится контрольное УЗИ. Однако, если кисты сосудистых сплетений не исчезают к 28-30 неделям, это никак не влияет на дальнейшее развитие ребенка.
Почечные лоханки это полости, где собирается моча из почек. Из лоханок моча перемещается в мочеточники, по которым она поступает в мочевой пузырь.
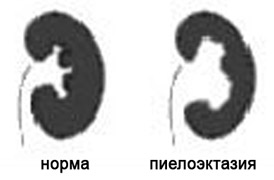
Пиелоэктазия представляет собой расширение почечных лоханок. Пиелоэктазия в 3-5 раз чаще встречается у мальчиков, чем у девочек. Встречается как односторонняя, так и двухсторонняя пиелоэктазия. Легкие формы пиелоэктазии проходят чаще самостоятельно, а тяжелые иногда требуют хирургического лечения.
Причина расширения почечных лоханок у плода.
Если на пути естественного оттока мочи встречается препятствие, то моча будет накапливаться выше данного препятствия, что будет приводить к расширению лоханок почек. Пиелоэктазия у плода устанавливается при обычном ультразвуковом исследовании в 18-22 недели беременности.
Опасна ли пиелоэктазия?
Умеренное расширение почечных лоханок, как правило, не влияет на здоровье будущего ребенка. В большинстве случаев при беременности наблюдается самопроизвольное исчезновение умеренной пиелоэктазии. Выраженная пиелоэктазия (более 10 мм) свидетельствует о значительном затруднении оттока мочи из почки. Затруднение оттока мочи из почки может нарастать, вызывая сдавление, атрофию почечной ткани и снижение функции почки.
Нужно ли обследовать ребенка после родов?
У многих детей умеренная пиелоэктазия исчезает самопроизвольно в результате дозревания органов мочевыделительной системы после рождения ребенка. При умеренной пиелоэктазии бывает достаточно проводить регулярные ультразвуковые исследования каждые три месяца после рождения ребенка. При присоединении мочевой инфекции может понадобиться применение антибиотиков. При увеличении степени пиелоэктазии необходимо более детальное урологическое обследование.
В случаях выраженной пиелоэктазии, если расширение лоханок прогрессирует, и происходит снижение функции почки, бывает показано хирургическое лечение. Хирургические операции позволяют устранить препятствие оттоку мочи. Часть оперативных вмешательств может с успехом выполняться эндоскопическими методами – без открытой операции, при помощи миниатюрных инструментов, вводимых через мочеиспускательный канал. В любом случае вопрос об оперативном лечении решается после рождения ребенка и полного его обследования.
Что делать при выявлении ультразвуковых маркеров хромосомной патологии у плода?
Вам следует обратиться к специалисту генетику, который еще раз оценит результаты ультразвукового исследования и биохимического скрининга, рассчитает риск индивидуально для вашего случая и даст необходимые рекомендации по дальнейшему ведению беременности.
Челябинская государственная медицинская академия
Проблема наследственной и врожденной патологии, прежде всего врожденных пороков развития (ВПР), хромосомных и моногенных заболеваний за последнее десятилетие приобрела серьезную социально-медицинскую значимость. Частота врожденной и наследственной патологии в популяции составляет в среднем 5% от числа новорожденных детей. В структуре перинатальной заболеваемости и смертности врожденная и наследственная патология занимает 2-3 место. Широкое внедрение в клиническую практику скринингового ультразвукового исследования в 11-14 недель беременности позволяет провести раннюю пренатальную диагностику ВПР и хромосомных аномалий (ХА) [4]. Среди многочисленных эхографических маркеров ХА наиболее ценным считается толщина воротникового пространства [5]. Использование этого маркера позволяет выявлять до 66,7-92% хромосомных дефектов уже в ранние сроки беременности [6, 7]. Поэтому представляет научный интерес дальшейшее изучение увеличения толщины воротникового пространства (ТВП) плода как пренатального эхографического маркера врожденной и наследственной патологии.
Целью исследования явилась оценка величины толщины воротникового пространства плода в качестве маркера хромосомных аномалий и врожденных пороков развития плода.
Материал и методы. Тип исследования: когортное с проспективной когортой (2008 - 2010 г.).
Метод выборки: сплошной по мере обращения.
1. Беременность в сроке гестации 11–14 недель.
2. Известная дата последней менструации при 26–30 дневном цикле.
3. Согласие женщины на участие в исследовании.
1. Нарушения менструального цикла.
2. Указание на прием гормональных контрацептивов за два месяца до цикла зачатия.
3. Стимулированная беременность.
4. Многоплодная беременность.
В соответствии с критериями включения/исключения за указанный период было отобрано 1310 беременных в сроки гестации от 11 до 14 недель, состоявших на диспансерном учете в женских консультациях г. Челябинска.
После проведения ультразвукового скрининга беременные были распределены на две группы, с учетом размеров толщины воротникового пространства (ТВП) плода: основная группа - 175 женщин с увеличением размеров толщины воротникового пространства у плода (группа 1), группа сравнения – 1135 пациенток с нормальными размерами толщины воротникового пространства у плода, беременность которых завершилась своевременными родами и рождением нормальных здоровых детей (группа 2). В качестве пороговых (разделительных) значений принимался 95‰ ТВП от показателей, разработанных в результате наших исследований, согласно рекомендациям Н.А. Алтынник и М.В. Медведева и К. Николаидеса и соавт. [1,7]. Группы были сопоставимы по возрасту, паритету и сроку гестации.
Эхографические исследования проведены на ультразвуковых сканерах фирмы TOSHIBA (Япония) высокого (XARIO XG) и экспертного (APLIO XG) классов. Для измерения размеров ТВП использовали трансабдоминальный доступ сканирования. В случаях регистрации у плода эхографических маркеров хромосомных дефектов или врожденных пороков развития, исследование завершали трансвагинальным доступом для детального изучения анатомии и проведения расширенной эхокардиографии плода. В ходе пренатального консультирования пациентке сообщали о наличии риска хромосомной патологии и объясняли целесообразность пренатального кариотипирования. В сроке 11-13 недель гестации осуществляли трансабдоминальную аспирацию ворсин хориона. При отказе от пренатального кариотипирования в ранние сроки и выявлении других эхографических маркеров хромосомной патологии или врожденных пороков развития плода во втором триместре беременности, рекомендовалась оценка кариотипа плода методом кордоцентеза в 21-24 недели.
Статистический анализ данных проводился при помощи пакета статистических программ STATISTICA 6.0 (StatSoft, 2001) и программы MedCalc (9.1.0.1) for Windows. При распределении признака в выборке, близком к нормальному, количественные значения представлялись в виде средней арифметической и ее среднеквадратичного отклонения (M±σ).
Для оценки различий между двумя группами в количественных признаках с учетом характера распределения, близкому к нормальному, применяли t-критерий Стьюдента. Оценка межгрупповых различий по качественным признакам проводилась с использованием критерия χ 2 , а при ожидаемых частотах менее 10 – применялась поправка Йетса.
С целью оценки прогностической значимости показателей проводился ROC-анализ с вычислением чувствительности, специфичности, отношения положительного и отрицательного правдоподобия. Для всех видов анализа статистически достоверными считались значения p 0,05).
Согласно полученных нами данным толщина воротникового пространства плода в группе 2 (со своевременными родами и рождением здорового ребенка) постепенно увеличивается на сроках от 11 до 14 недель, составляя в среднем 1,3±0,3 мм в 11–12 недель, 1,4±0,4 мм в 12–13 недель и 1,5±0,3 мм в 13-14 недель, при отсутствии различий между величинами ТВП в эти сроки беременности (р>0,05).
В табл. 1 представлены значения толщины воротникового пространства плода в 11–14 недель беременности в группах сравнения.
Таблица 1. Показатели толщины воротникового пространства плода в 11–14 недель беременности в группах сравнения
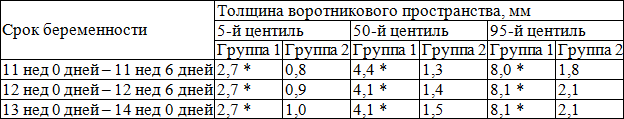
Примечание: * - значимость различий (р 0,05
Таким образом, в соответствии с полученными данными, необходимо выделять пациенток с расширением ТВП у плода в группу высокого риска по врожденным порокам развития даже при отсутствии хромосомной патологии. Особое внимание следует уделять детальному изучению анатомии плода и эхокардиографическому исследованию, так как множественные врожденные пороки развития и пороки сердца регистрируются наиболее часто.
С целью оценки прогностического значения величины ТВП в отношении развития хромосомных аномалий плода в группах сравнения нами использовался ROC-анализ (рис. 4).
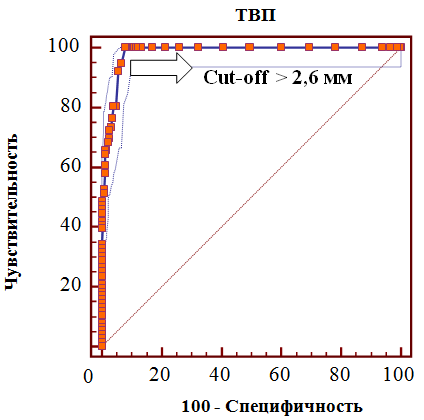
Рис. 4. ROC-кривая прогностического значения толщины воротникового пространства в отношении хромосомных аномалий плода
Проведенный анализ показал, что толщина воротникового пространства выше 2,6 мм ассоциирована с высоким риском развития хромосомных аномалий, причем указанный уровень имеет высокую чувствительность (100%) и специфичность (89,7%), а также отношение правдоподобия положительного результата (9,65), р
Список использованных источников:
1. Нормативные значения копчико-теменного размера и толщины воротникового пространства плода в ранние сроки беременности/ Н.А. Алтынник, М.В. Медведев// Ультразвуковая диагностика. Акуш. Гин. Педиат. - 2001. - Т. 9, №1. - С. 38–40.
2. Диагностическая ценность расширенного воротникового пространства в сочетании с допплеровским исследованием плодово-плацентарного кровотока в I триместре беременности при врожденной и наследственной патологии/ С.Г. Ионова, И.П. Цымбалова, А.В. Сидорова// Пренатальная диагностика. - 2004. - Т. 3, №3. - С. 233.
3. Копытова Е.И. Расширенное воротниковое пространство плода как пренатальный эхографический маркер врожденных и наследственных заболеваний: Автореф. дис. … канд. мед. наук. – М., 2007. – 22 с.
4. Медведев М.В. Основы ультразвукового исследования в акушерстве. - М.: Реал Тайм, 2006. – 96 с.
5. Основы ультразвукового скрининга в 11-14 недель беременности/ М.В. Медведев, Н.А. Алтынник. - М.: Реал Тайм, 2008. – 88 с.
6. Новый подход к расчету риска при проведении скринингового ультразвукового исследования в первом триместре беременности/ Е.С. Некрасова, А.Л. Коротеев, Т.В. Кузнецова, В.С. Баранов// Пренатальная диагностика. - 2005. - Т. 4, №1. - С. 22–28.


Легкость и удобство в новом объеме.
У постели пациента, в операционной или на спортивной площадке - всегда готов к использованию.
Актуальность темы пренатальной диагностики врожденных пороков сердца (ВПС) понятна всем врачам, которые связаны с пренатальной диагностикой, неонатологией, педиатрией, кардиологией, генетикой. ВПС являются одной из ведущих причин перинатальной смертности и регистрируются с частотой 4-13 на 1000 живорожденных [1]. В связи с тем, что профилактические мероприятия по предупреждению ВПС не имеют должного успеха, представляется актуальной и необходимой их пренатальная ультразвуковая диагностика.
В многочисленных исследованиях зарубежных и отечественных коллег неоднократно формулировались и изучались различные группы риска по возникновению ВПС. Это делалось для того, чтобы потенциально сузить группу беременных женщин, которым показана эхокардиография в специализированном центре. Среди этих групп риска выделяли:
- Семьи, имеющие ребенка с ВПС.
- Семьи с ВПС у одного или обоих супругов.
- Женщин, страдающих сахарным диабетом, системными заболеваниями соединительной ткани, гипотиреозом.
- Беременных с тератогенной экспозицией в ранние сроки беременности (герпес ранее 6-7-й недели) [2].
Однако параллельно другими учеными эти группы риска отвергались, потому что большинство ВПС встречались у плодов и детей, матери которых не входили ни в одну из предложенных групп риска. Единственными разумными критериями так называемого селективного отбора были признаны беременные, попавшие в группу риска после проведения скрининга I триместра и беременные с подозрением на ВПС при ультразвуковом исследовании (УЗИ) плода [3].
Неоспоримо, что оптимальными сроками беременности для исследования сердца плода являются 20-22 недели, однако большинство летальных и клинически значимых пороков сердца могут быть диагностированы в конце I триместра беременности. Позволим себе процитировать слова главы Fetal Medicine Foundation Кипраса Николаидеса, высказанные им на страницах сайта FMF (www.fetalmedicine.com): "Специалист ультразвуковой диагностики с 12 недели беременности должен заверить большинство родителей, что у их ребенка нет крупных врожденных пороков сердца. В случае крупных врожденных пороков сердца их раннее выявление может привести к постановке правильного диагноза или хотя бы вызвать подозрение для осуществления ультразвукового мониторинга".
Главная цель пренатальной диагностики сформулирована специалистами пренатальной диагностики всего мира - это обеспечение женщины максимально возможной информацией о пороке как можно раньше. Мы должны дать право женщине и семье в целом решать вопрос о пролонгировании беременности с грубыми пороками развития у плода [4].
С каждым годом все большее количество публикаций посвящается диагностике ВПС в ранние сроки - в I триместре беременности 6. Практически ни один из выпусков журнала ISUOG (Ultrasound In Obstetrics and Gynecology, или "белого" журнала, как его называют специалисты) не обходит своим вниманием тему ранней диагностики врожденных пороков развития.
Цель эхокардиографии в I триместре беременности состоит в выявлении летальных и клинически значимых ВПС. Это исследование не ставит целью выявление стенозов и гипоплазий выносящих трактов, диагностику мелких дефектов перегородок, патологий дуги аорты и артериального протока. Многие из этих пороков не только технически невозможно заподозрить в I триместре, манифестируют они после 30-й недели беременности, т.е. их диагностика является прерогативой исследования III триместра.
Точность пренатальной диагностики ВПС во все сроки беременности варьирует в широком диапазоне. Причинами этого могут быть разный опыт специалистов, ожирение беременной, частота использованных ультразвуковых трансдьюсеров и класс ультразвукового аппарата, перенесенные ранее абдоминальные операции, срок беременности, количество околоплодных вод и положение плода. Однако заметим, что многие из этих факторов теряют свою актуальность именно при проведении трансвагинальной эхокардиографии в I триместре беременности. Своевременная диагностика ВПС позволяет идентифицировать плоды высокого риска по генетическим синдромам, что имеет важное значение при проведении пренатального консультирования и оказывает существенное влияние на акушерскую тактику.
С 2006 по 2011 г. пренатально в I триместре беременности были выявлены 125 ВПС. Из них 68 (55%) ВПС сочетались с различными хромосомными аномалиями (ХА) плода, 30 (24%) входили в состав различных множественных врожденных пороков развития (МВПР), 27 (21%) ВПС были изолированными.
При эхокардиографии изучались четырехкамерный срез сердца плода (рис. 1) и срез через три сосуда (рис. 2). УЗИ проводилось трансабдоминальным датчиком, лишь при необходимости (затрудненная визуализация) использовался внутриполостной датчик. Четырехкамерный срез сердца плода при ультразвуковом сканировании трансабдоминальным датчиком визуализировался в 85% случаев, срез через сосуды - в 73%, при использовании трансвагинального датчика эти цифры существенно возрастали до 100 и 91% соответственно. Оптимизация пренатальной диагностики ВПС может быть достигнута путем строгого соблюдения основных методических правил. При оценке четырехкамерного среза плода необходимо оценить нормальное расположение сердца плода, исключив его эктопию (рис. 3), положение оси сердца плода, что не представляет никаких трудностей, нормальные пропорции и размеры камер сердца, движение створок атриовентрикулярных клапанов должно быть свободным, септальная створка трикуспидального клапана должна располагаться ближе к верхушке сердца (рис. 4). При оценке среза через три сосуда необходимо оценить взаиморасположение сосудов и их диаметр.
Рис. 1. Беременность 12 недель. Четырехкамерный срез сердца плода. Отчетливо видны камеры сердца.
Ультразвуковое исследование, которое позволяет определить вероятность рождения ребенка с синдромом Дауна. Речь идет о скоплении подкожной жидкости на задней поверхности шеи плода, которое измеряют на сроке 11-13 недель. Некоторое количество жидкости присутствует в каждом случае, но у многих детей с синдромом Дауна ее количество сильно превышает норму. Точный диагноз можно поставить только на основании дополнительных исследований: биопсии хориона или амниоцентеза. Однако, их проведение чревато небольшим риском прерывания беременности.
Определение толщины воротникового пространства не дает точного представления о состоянии ребенка, но помогает определить, требуется ли назначение более глубокого диагностического теста. 
Определение толщины должно проводиться на этапе от 11 до 13 недель плюс 6 дней. Раньше этого срока выполнить его будет сложно, ведь ребенок еще слишком мал, а позже излишки жидкости поглощаются его лимфатической системой. Как правило, измерения проводятся обычным способом, лишь иногда требуется сделать вагинальное УЗИ.
Для того, чтобы точно определить срок беременности, врач УЗИ, измеряет плод от макушки до копчика (это называется копчико-теменной размер КТР). Затем доктор устанавливает толщину воротникового пространства. При этом кожа выглядит на мониторе белой линией, а подкожная жидкость — черной.
На 11-й неделе беременности нормой является ширина в 1-2 мм, а на сроке 13 недель и 6 дней – 2,8 мм. Толщина воротникового пространства растет пропорционально росту ребенка. Высокий показатель не всегда указывает на наличие проблемы. У некоторых детей, не предрасположенных к синдрому Дауна, содержание подкожной жидкости иногда бывает выше нормы. Девять из десяти детей с показателем 2,5-3,5 мм рождаются абсолютно нормальными.
Чем выше показатель толщины воротникового пространства, тем выше риск развития синдрома Дауна и других хромосомных нарушений.
Вероятность рождения такого ребенка существует у каждой женщины, и с возрастом она увеличивается. Для определения степени риска учитывается возраст будущей мамы и результат теста на определение толщины воротникового пространства. Специальная программа помогает определить эту вероятность для женщины определенного возраста – ее называют фоновым показателем. Личные показатели используют для определения степени риска в каждом конкретном случае. Эта степень может быть выше или ниже фонового показателя.
Большинство женщин с высокой степенью риска рожают здоровых детей. Ребенок с синдромом Дауна появляется в одном из 150 случаев присутствия высокого риска или даже реже. В ситуации, когда риск настолько высок, что составляет 1 из 5, стоит помнить, что сохраняется шанс четыре против одного, что ребенок родится здоровым. Единственная возможность точной диагностики вероятности появления хромосомных отклонений – диагностический тест, такой как биопсия хориона или амниоцентез.
Одним из преимуществ теста на определение толщины воротникового пространства является то, что его делают на ранних сроках беременности. Поэтому биопсия ворсин хориона (БВХ) также может быть сделана в первом триместре.
У 75% детей, страдающих синдромом Дауна, отклонения были выявлены во время исследования толщины воротникового пространства.
Иногда измерения демонстрируют вероятность наличия порока у здоровых детей. Такой результат называется ложноположительным, это 5% от общего числа. Таким образом, у одной из 20 женщин ошибочно определяется высокая степень риска рождения ребенка с отклонениями. Наиболее точный результат можно получить при совмещении показателей теста на определение толщины воротникового пространства и анализа крови. Последний выявляет уровень свободного бета-ХГЧ и концентрацию протеина PAPP-A (ассоциированного с беременностью плазменного белка А). У детей с синдромом Дауна обычно наблюдается высокий уровень свободных бета-ХГЧ и низкая концентрация протеина PAPP-A. УЗИ для определения толщины воротникового пространства в сочетании с анализом крови в 90% случаев дает точный результат. Это исследование называется двойным тестом.
Вы не указали, какое именно исследование Вам проводили в 16 недель. Если делали амниоцентез и результат выдавали по клеткам культуры амниотической жидкости – там выявляют как численные аномалии плода, так и структурные перестройки. Если делали плацентобиопсию, то в основном выявляют численные аномалии хромосом и крупные аберрации. Мелкие перестройки при таком методе плохо видны.
Отставание длины бедренной кости у плода может быть обусловлено не только трисомией по 21 хромосоме, но и другими генетическими заболеваниями. Кроме того, хорошие результаты скрининга не исключают 100% синдром Дауна у плода. Вам лучше сходить на генетическую консультацию.
Утолщение плаценты может наблюдаться как в норме, так и при внутриутробной инфекции, иммунологических нарушениях, пороках развития плода, аномалиях хромосомного набора и т.д. Для уточнения ситуации необходимо обследование, в том числе, консультация генетиком.
В таком виде, как вы написали, ответы по хромосомному анализу не выдаются. Если врач видит укорочение хромосомы, он должен указать точки разрыва. При частичной делеции (утрате части хромосомы, приводящей к укорочению), могут быть большие проблемы. Хромосома не может быть короче на 0,02 (чего?). Вероятность ошибки зависит от квалификации врача, делавшего анализ.
В вашей семье есть доминантная форма синдактилии (сросшиеся пальцы). Вероятность повторного рождения ребенка с таким заболеванием – 50%. Синдактилия может быть как на руках, так и на ногах. Но это все корректируется хирургическим путем.
Хромосомные аберрации практически всегда дают тяжелые последствия, но так как вы привели результаты хромосомного анализа не полностью, точно сказать нельзя. Возможно также сочетание хромосомной аберрации с родовой травмой.
Судя по тому результату хромосомного анализа Вашей дочери, который вы привели, у нее была так называемая простая трисомная форма. Она обычно бывает следствием случайной мутации, а не унаследованной от родителей. Если анализ кариотипа Ваш и супруга будет без отклонений (а это скорей всего так), то риск повторения равен 0,7%. Кариотип Вам нужен простой.
Специального названия для такого синдрома нет – только то, что указано в приведенном Вами заключении. У Вашего сына присутствует обмен участками между хромосомами 5 и 11. В скобках указаны те точки хромосом, в которых произошли разрывы (только они обозначаются не буквой g, а q) При этом произошла утрата фрагмента хромосомы, (т. е. потеря части наследственного материала), что и стало причиной пороков развития – т. е. транслокация не сбалансированная. Такая же транслокация есть и у Вас, но без потери фрагмента хромосомы, т. е. сбалансированная. Поэтому Вы не имеете аномалий развития.
Зачатие ребенка в этом случае возможно. Мутация (и проблемы) с вероятностью 50% могут передаться сыну. По поводу целесообразности стимуляции сперматогенеза лучше проконсультироваться с урологом-андрологом. Скорее всего Вам надо решать вопрос об ЭКО/ИКСИ.
У плода увеличена ТВП до 3 мм (после 14 недель может уменьшиться, но это не влияет на показания для инвазивной диагностики). Такое ТВП может быть как вариантом нормы, так и признаком хромосомной аномалии плода ( в том числе синдрома Дауна), так и маркеров порока развития плода ( сердце, почки, скелетные аномалии). Такое ТВП является прямым показанием для инвазивной диагностики, хотя синдром Дауна подтверждается и не всегда.
Рекомендую сходить в перинатальный центр и обсудить ситуацию с генетиком и неонатологом. Не исключено, что сразу после рождения малышу потребуется операция (если обструкция или атрезия части кишечника подтвердится).
В Вашей ситуации делать хромосомный анализ необходимо. Причем желательно не тянуть до 20-22 недель, а сделать раньше – плацентоцентез или амниоцентез. Вероятность хромосомной патологии высокая. Вероятность ВПР ЦНС зависит от квалификации врача, который проводил Вам УЗИ. Заочно оценить ее сложно.
Такой результат означает, что у вашего супруга 11 и 22 хромосомы обменялись участками хромосом. Рождение здорового ребенка возможно.
Краниостенозы бывают с разными типами наследования. В зависимости от этого и риск разный. (от 0 до 50%). Вам с супругом надо придти на очную генетическую консультацию с фото супруга до операции и желательно принести рентгеновские снимки до операции для уточнения типа краниостеноза.
Плацентарный мозаицизм бывает примерно в 2% случаев. Плод при этом не имеет хромосомных дефектов, т.е. здоров. Возможна такая ситуация и в вашем случае. Но с учетом увеличенной воротниковой зоны, мозаицизм может быть истинным, т.е. быть и у плода ( т.е. плод имеет мозаичную форму синдрома Дауна). Решить вопрос можно только при проведении амниоцентеза (а еще точнее – при кордоцентезе, когда исследуют именно клетки плода, а не плаценты).
Решать в любом случае только вам. Но по результатам скрининга у вас показатели в норме, риск родить ребенка с трисомией повышен за счет фактора возраста.
Учитывая, что анемия Минковского-Шоффара наследуется по аутосомно-доминантному типу, вероятность того, что ваши дети унаследуют это заболевание составляет 50%.
Однозначно сказать нельзя, но, возможно подозревают аномалию Арнольда-Киари?
Скорее всего, не скажется.
На все вопросы в рамках заочной консультации ответить сложно. Вам лучше придти на прием к генетику.
Ошибки при измерении ТВП зависят от квалификации врача. ТВП к 12 неделе может как уменьшится, так и увеличиться. Но все равно, если ТВП было увеличено – вам показано проведение пренатального кариотипирования плода.
Вам с супругом надо самим сделать хромосомный анализ. Это позволит уточнить шансы.
Дополнительные исследования вам не нужны. Исследование хромосомного набора в сперматозоидах с использованием FISH- метода много информации не даст.
По вашему описанию – была неимунная водянка плода, а не пороки развития. Резус-конфликт может быть причинной неимунной водянки в том числе, но возможна и другая причина. Для назначения точных анализов вам нужна очная консультация генетика с результатами скринингов и УЗИ во время беременности.
Синдром Смита-Лемли–Опитца – это моногенное аутосомно-рецессивное заболевание. Пол ребенка значения не имеет. При каждой беременности риск появления заболевания у плода высокий – 25% (соответственно шанс родить здорового – 75%) Вам с супругом надо обратиться в Медико-генетический центр для обследования вместе с супругом – сделать ДНК-анализ для выявления мутации. В последующем – возможна пренатальная ДНК-диагностика (прокол) на сроке с 10 недель беременности.
Дополнительные анализы не нужны. Беременность можно планировать через 6 месяцев.
Ответить однозначно на ваши вопросы нельзя. Односторонняя эктродактилия может быть как случайным пороком развития, так и проявлением наследственной патологии. Учитывая один случай такой аномалии в семье, сделать однозначный вывод нельзя. Также теоретически возможно, что у вашего брата и дочери разные проявления одного заболевания, которое у вас не проявилось. В целом риск рождения ребенка с патологией у вас можно оценить как средний, так же как и для вашей дочери.
Вам с супругом надо придти на генетическую консультацию с патологоанатомическим заключением, результатами УЗИ и скринингов, сделанных во время данной беременности. Также вам обоим надо сделать хромосомный анализ как минимум.
Судя по всему, у ребенка произошла случайная мутация. Риск повторения низкий – менее 1%.При нормальном хромосомном анализе обоих супругов анализ кариотипа плода не обязателен, но маленький риск в этом случае все равно остается. Вероятность рождения в вашей семье здорового ребенка при последующих беременностях – более 99%.
У вас сложная ситуация. Заочно на нее ответить невозможно. Вам необходима очная консультация и генетика и опытного акушер-гинеколога.
Читайте также:


