При какой температуре убивается герпес
справочника
Инфекционные болезни, фармакотерапия
Простой герпес (лат., herpes simplex) – хроническое инфекционное антропонозное заболевание, вызванное вирусами простого герпеса двух серотипов, характеризующееся локализованным поражением кожи, слизистых, либо развитием генерализованных форм с полиорганной патологией.
Вирус простого герпеса (ВПГ) относится к семейству герпесвирусов (Herpesviridae), подсемейству α-herpesviruses. Диаметр вируса составляет приблизительно 100-160 нм, геном представлен ДНК, нуклеокапсид состоит из 162 капсомеров, липидная оболочка имеет гликопротеиновые шипы. Нуклеокапсид содержит группоспецифические белки, внешняя оболочка – типоспецифические. Выделяют ВПГ-1 (преимущественная локализация поражения – кожа и слизистые головы) и ВПГ-2 (доминируют патологические изменения слизистых гениталий).
ВПГ термолабильный, погибает при температуре 50-52 °С за 30 мин., при 100 °С – за 5 мин., нестабильный при комнатной температуре. До 5 дней сохраняется при замораживании (-70 °С), в среде с рН = 6,5.
Ультрафиолетовое излучение, высушивание, органические жирорастворители, желчь инактивируют ВПГ.
Источник инфекции: человек с манифестной или субклинической формой инфекции.
Механизм передачи: преимущественно контактный прямой (через слизистые или кожу), непрямой (через бытовые предметы, медицинский инструментарий, трансфузии биологических жидкостей), реже – вертикальный (при наличии патологии плаценты). Не исключается возможность воздушно-капельной трансмиссии.
К группам с повышенным риском заражения ВПГ относятся проститутки, люди, часто меняющие половых партнёров, представители социально-неблагополучных прослоек общества (в развивающихся странах практически 100% населения страдает инфекцией, вызванной ВПГ-1), стоматологи, отоларингологи, акушеры-гинекологи, урологи и др.
Географическая распространённость – повсеместная.
Иммунитет: типоспецифический, нестерильный.
Репликация вируса начинается в области входных ворот инфекции, в эпителиальных клетках. Часть вирусов по нервным окончаниям продвигается к нервным ганглиям и реплицирует там. Часть вирусов попадает в кровь, вследствие чего активизируются клеточные и гуморальные факторы защиты.
Местная реакция обусловлена непосредственным действием вируса и морфологически проявляется признаками баллонной дегенерации поражённых клеток, которые гибнут, образуя очаги некроза и формируя местную воспалительную реакцию. Активность Т-лимфоцитов, вируснейтрализующих, комплементсвязывающих антител обусловливает разрешение местных патологических изменений и вирусемии. Последующие рецидивы провоцируются состояниями иммунного дисбаланса различного генеза и вызываются вирусами, которые сохраняются в нервных ганглиях.
К причинам вирусной реактивации и перехода инфекции из латентного состояния в активное относятся: гиперинсоляция, стрессы, переутомление, простудные заболевания, приём иммунодепрессантов, ГКС и др. Особенно тяжело герпетическая инфекция протекает у ВИЧ-инфицированных пациентов с развитием генерализованных форм и клиническими проявлениями менингита, энцефалита, полиорганных поражений.
Инкубационный период: 4-12 дней, зависит от инфицирующей дозы.
15% людей со специфическими антителами никогда не имели клинических проявлений герпетической инфекции. Первичное заражение в большинстве случаев сопровождается клиническими симптомами.
Клинические формы герпетической инфекции:
1. Кожно-слизистый герпес:
• Герпетический гингивостоматит.
• Герпес губ и носа.
• Герпетические поражения кожи.
• Герпетический панариций.
• Герпетическое поражение глаз.
• Генитальный герпес.
• Герпетический проктит.
2. Герпетическое поражение нервной системы:
• Энцефалит.
• Асептический менингит.
• Автономная радикулопатия.
3. Висцеральная герпетическая инфекция:
• Эзофагит.
• Пневмония.
• Гепатит.
4. Генерализованный герпес.
5. Герпес новорождённых.
6. Герпес у ВИЧ-инфицированных и у больных с иммунодефицитом другого генеза.
Каждая из этих форм может проявляться как первичное инфицирование (острый процесс) или рецидив (хроническая форма), типично или атипично.
Гингивостоматит – наиболее частая форма инфекции в случае первичного инфицирования ВПГ. Заболевание начинается с общетоксических явлений: слабость, лихорадка, увеличение подчелюстных лимфоузлов. В первые 2-3 дня на гиперемированной слизистой полости рта появляются небольшие прозрачные пузырьки (от одного до большого количества). Через 1-3 суток пузырьки вскрываются, образуются поверхностные эрозии. При этом больные отмечают выраженные боли и чувство жжения во рту, усиливающиеся во время приёма пищи. Повышение температуры тела может сохраняться до 7-10 дней, эрозии эпителизируются в течение 1-2 недель.
В случае генитального герпеса первичное инфицирование сопровождается симптомами интоксикации (гипертермия, миалгии, артралгии, головная боль). Через 1-2 дня возникает боль внизу живота, появляется отёчность слизистой и/или кожи половых органов, регионарный лимфаденит. На поражённых участках видны везикулы, пустулы, эрозии. В 80% случаев в патологический процесс вовлекаются также мочевые пути с развитием дизурических явлений. У мужчин дизурия на фоне интоксикационного синдрома может быть единственным проявлением инфекции.
Герпес губ и носа характеризуется возникновением локализованного ощущения жжения, зуда с одновременным или более поздним (через 1-2 дня) появлением типичных высыпаний на отёчном и гиперемированном основании кожи. Вначале образуются папулы, от 2-3 до нескольких десятков, которые трансформируются в везикулы. Через несколько дней содержимое везикул мутнеет, они раскрываются, образуются эрозии, которые через 3-5 дней покрываются жёлто-коричневыми корочками. Под корочками происходит образование новой кожи. Через 6-9 дней от начала заболевания корочки отпадают, и на их месте сохраняется постепенно исчезающая пигментация. Обычно весь процесс длится 1-2 недели. В этот период может наблюдаться и регионарный лимфаденит с явлениями общей интоксикации.
Энцефалит (менигоэнцефалит) чаще начинается остро с лихорадки, психоэмоциональных нарушений, судорог, очаговых симптомов, парезов и параличей. Менингеальные знаки выражены слабо либо отсутствуют.
Рецидивы инфекции протекают, как правило, значительно легче или вообще бессимптомно.
Встречаются также атипичные формы простого герпеса с выраженным отёком подкожной клетчатки и гиперемией кожи (чаще – на мошонке, губах, веках), везикулы могут отсутствовать. Зостериформный простой герпес напоминает опоясывающий лишай, однако с менее интенсивным болевым синдромом, имеет локализованные высыпания по ходу нервных стволов (на лице, туловище, конечностях). Геморрагическая форма характеризуется кровянистым содержимым везикул, часто с последующим развитием язвенных дефектов. Язвенно-некротическая форма развивается при выраженном иммунодефиците. На коже образуются язвы различных размеров с некротизированным дном и серрозно-геморрагическим или гнойным отделяемым. Обратное развитие патологического процесса с отторжением корок, эпителизацией и рубцеванием язв происходит очень медленно. Один из вариантов атипичного течения герпетической инфекции – развитие герпетиформной экземы (вариолиформный пустулёз Юлисуберга-Капоши).
В зависимости от формы герпетической инфекции, возможно развитие следующих осложнений: абсцесс, флегмона, сепсис, мозговая кома, ДВС-синдром, дистресс-синдром, преждевременное прерывание беременности, мертворождение, снижение остроты зрения вплоть до полной слепоты.
Прогноз для людей с нормальным иммунным статусом и локализованными формами герпетической инфекции благоприятный. Для больных с иммунодефицитом прогноз неблагоприятный, при развитии генерализованных форм – часто с летальным исходом.
Эпидемиологический анамнез – уточнение особенностей эпидемиологического анамнеза.
Клиническая диагностика – характерные высыпания.
Лабораторные исследования
• Общий анализ крови: нормальный, или незначительная лейкопения с лимфомоноцитозом.
• Специфические лабораторные методы: электронная микроскопия мазков из элементов сыпи, ИФА с определением титров IgM, IgG к ВПГ-1, ВПГ-2 в крови, СМЖ, ПЦР HSV DNA в крови, СМЖ.
Инструментальные исследования
Рентгенологические исследования, УЗИ, КТ, МРТ поражённых органов и систем.
Консультации специалистов
По показаниям: окулист, невропатолог, пульмонолог, кардиолог, гастроэнтеролог.
Дифференциальный диагноз
Дифференциальный диагноз необходимо проводить с ветряной оспой, опоясывающим герпесом, везикулёзным риккетсиозом, герпангиной, экземой, аллергическим дерматитом, полиморфной экссудативной эритемой, менингоэнцефалитами другой этиологии.
На разных этапах заболевания применяется комплексное этиологическое и патогенетическое лечение, направленное на подавление репродукции ВПГ и повышение иммунологической резистентности макроорганизма.
Терапия герпетических инфекций предусматривает уменьшение клинических проявлений – топическое или системное назначение противогерпетических химиопрепаратов: ацикловир, валaцикловир, фамцикловир и др. или применение препаратов лейкоцитарного и рекомбинантного интерферона, а также противорецидивное лечение.
Противорецидивная терапия включает:
1. Длительные беспрерывные курсы ацикловира в поддерживающих дозах (800 мг в сутки).
2. Иммунотерапию противогерпетическими вакцинами.
3. Терапию иммуномодулирующими препаратами, индукторами интерферона.
Общая профилактика: избегать близкого контакта с больными, которые имеют клинические признаки инфекции, соблюдение правил личной гигиены, использование барьерных методов контрацепции, мониторинг серологических маркеров герпетической инфекции у беременных и особенно у серонегативных.
Для слабовидящих
Переводчик
Главное меню
Для сотрудников
Опрос
Анкетирование
Оспа ветряная – высококонтангиозное острое вирусное заболевание с воздушно-капельным путем передачи, возникающее преимущественно в дет-ском возрасте и характеризующееся умеренной интоксикацией, лихорадочным состоянием, везикулезной сыпью на коже и слизистых.
Этиология. Возбудитель ветряной оспы относится к вирусам группы гер-песа, неустойчив во внешней среде. Быстро погибает под действием высоких температур, ультрафиолетового облучения, эфира. Хорошо переносит замора-живание. Вирус отличается летучестью и с потоком воздуха может перено-ситься на значительные расстояния.
Эпидемиология. Вирус вызывает два клинических варианта: ветряную ос-пу, опоясывающий герпес. Считают, что ветряная оспа – это проявление пер-вичной инфекции в восприимчивом организме (чаще у детей), так как опоясы-вающий герпес – это реактивация инфекции в иммунном и ослабленном орга-низме. Пути передачи инфекции – воздушно-капельный, реже – контактно– бытовой. Возможна также передача вируса ветряной оспы и опоясывающего лишая от матери к плоду во время беременности (вертикальный путь передачи инфекции). Однако реализуется эта возможность крайне редко.
Под воздействием каких-либо провоцирующих факторов (или на фо-не иммунодефицитных состояний) вирус может активизироваться вновь, что может выражаться в виде локальных высыпаний на коже – опоясывающего герпеса или опоясывающего лишая. Опоясывающий лишай - это спорадиче-ское заболевание, возникающее в результате активизации латентного вируса ветряной оспы. Характеризуется воспалением задних корешков спинного моз-га и межпозвоночных ганглиев, а также появлением лихорадки, общей инток-сикации и везикулезной экзантемы по ходу вовлеченных в процесс чувстви-тельных нервов.
Основной удельный вес заболевших приходится на возраст 3-6 лет. Заболеть ветряной оспой могут и взрослые, ранее не болевшие данной инфек-цией. Восприимчивость к ветряной оспе уникальна – она составляет 100%. Как и другие вирусы, вирус герпеса отличается низкой устойчивостью в окру-жающей среде, поэтому больной представляет угрозу только при непосредст-венном общении с ним. Вирус быстро гибнет при воздействии на него прямых лучей солнечного света, ультрафиолетового облучения, и при нагревании.
Случаи ветряной оспы регистрируются на протяжении всего го-да. Максимальная заболеваемость ветряной оспой наблюдается в осенне-зимние месяцы, минимальная – летом. Групповая заболеваемость отмечается в осенне-зимний период, главным образом в организованных коллективах среди детей дошкольного возраста. Дети, посещающие детские сады и ясли, болеют этой инфекцией в 7 раз чаще, чем неорганизованные дети.
Клиника ветряной оспы. Инкубационный период может длиться 11—21 день, в среднем около 14 дней. Заболевание начинается остро: повышается температура тела, возникают симптомы интоксикации, понижается аппетит. Одновременно на всем теле появляется сыпь с элементами в виде мелких па-пул, которые быстро превращаются в везикулы. Через 1—3 дня везикулы под-сыхают, и на их месте образуются корочки, отпадающие на 2—3-й неделе бо-лезни. После них на коже остается легкая пигментация. Рубцы не образуются. Зуд кожных покровов наблюдается у детей раннего возраста и лиц, склонных к аллергическим реакциям. Элементы ветряночной сыпи появляются сразу на всех кожных покровах, в том числе на волосистой части головы, а также на слизистой полости рта, конъюнктивах. Кожа ладоней и стоп сыпью не покры-вается. Элементы не сливаются. Могут отмечаться осложнения, которые свя-заны с присоединением вторичной бактериальной инфекции, и проявляются в виде абсцессов, флегмон, пневмоний, энцефалитов, отитов, синуситов, конъ-юнктивитов, рожи, скарлатины, лимфаденитов, стоматитов.
После перенесенного заболевания остается пожизненный иммунитет. Од-нако следует отметить, что у лиц с тяжелым иммунодефицитом различной этиологии (ВИЧ-инфекция, после пересадки органов) возможно повторное возникновение заболеваний. Опоясывающий лишай, напротив, чаще всего встречается среди взрослых.
Лечение. Лечение проводится в амбулаторных условиях, при тяжелом те-чении с осложнениями со стороны ЦНС и гнойными осложнениями или по эпидемиологическим показаниям больные госпитализируются в стационар.
Профилактика. Больной подлежит изоляции на дому до 5-го дня с момента появления последнего элемента сыпи. Дезинфекция не производится. Детей в возрасте до 3 лет, бывших в контакте с больным ветряной оспой и не болев-ших ею ранее, разобщают с 11-го по 21-й день, считая от момента контакта.
Специфическая профилактика. В настоящее время в соответствии с Национальным календарем профилактических прививок и перечнем профилактических прививок по эпидемическим показаниям иммунизация против ветряной оспы осуществляется детям, которым планируется проведение операции по трансплантации органов и (или) тканей человека, при отсутствии антител или через 2 года после окончания иммуносупрессивной терапии после трансплантации.

Герпетическая инфекция – инфекция, вызываемая герпесвирусами 1-го и 2-го типа – хроническое рецидивирующее заболевание, входящее в группу ТОRСН – инфекций, для которого характерно поражение кожи, слизистых, глаз, нервной системы.
Инфекция, вызванная герпесвирусами, распространена повсеместно. Инфицированность населения очень высокая. По данным Всемирной организации здравоохранения (ВОЗ) герпесвирусная инфекция занимает второе место среди вирусных заболеваний человека, уступая лишь гриппу.
Восприимчивость к инфекции всеобщая, независимо от пола и возраста.
Подъемы заболевания регистрируются в осенне-зимний период.
Проведенные за последние 10 лет эпидемиологические исследования показали, что к 15-летнему возрасту инфицировано 80% детей, а к 30 годам 90% населения имеют антитела к вирусам того или иного типа.
Возбудитель инфекции – вирус простого герпеса 1 или 2 типа (ВПГ 1 или ВПГ 2). Попадая в клетку – вирус вызывает ее гибель. В отдельных клетках вирус может сохраняться длительное время, но при последующей активации вируса, клетка погибнет.
Считается, что ВПГ – 1 чаще поражает дыхательные пути, а ВПГ-2 - урогенитальную систему, но, несмотря на это, роль ВПГ-1 в развитии генитального герпеса увеличивается.
Вирусы простого герпеса неустойчивы к действию физических и химических факторов, легко разрушаются под действием ультрафиолетовых и рентгеновских лучей, чувствительны к этиловому спирту, эфиру. При низких температурах (-20-70 о С) вирус сохраняется десятилетиями.
Источники инфекции – вирусоносители и больные с различными формами болезни.
Пути передачи инфекции:
- Половой (наиболее значимый);
- Гематогенный;
- Воздушно-капельный;
- Контактно-бытовой (через игрушки, предметы обихода, одежду).
Факторами передачи вируса являются: слюна, кровь, слезная жидкость, сперма, секрет влагалища и цервикального канала, различные органы и ткани, используемые при трансплантации, моча, медицинский инструментарий.
Попадает вирус в организм через поврежденные участки кожи и слизистой, затем, в месте внедрения вируса происходит размножение вирусных частиц. Первичное инфицирование вызывает латентную (скрытую, вялотекущую) инфекцию.
Клинические проявления герпетической инфекции отличаются значительным разнообразием. Они зависят от локализации поражения, распространенности, состояния иммунной системы, типа вируса, а также от механизма заражения.
По механизму заражения герпетическая инфекция бывает первичная и рецидивирующая.
Первичная форма – остро возникающее заболевание при первом контакте с вирусом простого герпеса.
По локализации поражения:
- Кожа – простой герпес, герпетиформная экзема;
- Слизистые оболочки ротоглотки – стоматит, фарингит, тонзиллит;
- Верхние дыхательные пути – острое респираторное заболевание;
- Глаза – кератоконъюнктивит;
- Урогенитальный тракт – уретрит, цистит, вульвовагинит;
- Нервная система – менингит, энцефалит, менингоэнцефалит;
- Внутренние органы – гепатит, гломерулонефрит, пневмония.
Генитальный герпес развивается у молодых людей после начала половой жизни. Первичный генитальный герпес отличается более тяжелым и продолжительным течением. Высыпания обильные и занимают большую площадь поражения. При первичном генитальном герпесе отмечается повышение температуры, общая слабость, раздражительность. В области гениталий появляются везикулезные высыпания, сохраняющиеся до 8 суток.
Влияние вируса простого герпеса на беременность и роды.
Первичное инфицирование и рецидивы во время беременности могут привести к мертворождению, выкидышам, а также к формированию пороков у плода. Наиболее опасно заражение в третьем триместре.
При первичном инфицировании матери во время беременности инфицирование плода происходит в 5% случаев. Чаще всего инфицирование ребенка происходит во время родов (85%) или после родов (10%).
Инфицирование ребенка ВПГ во время родов может стать причиной последующего развития герпетической инфекции новорожденного.
Основную опасность представляет выделение вируса со слизистой половых органов в момент родов. Выделение вируса может сопровождаться высыпаниями в области половых органов, а может и не сопровождаться никакими симптомами.
Последствия герпесвирусной инфекции для ребенка:
- распространение вируса по всему организму с поражением головного мозга, легких, печени, надпочечников, кожи, глаз, ротовой полости;
- поражение ЦНС (снижение аппетита, судороги, повышенная возбудимость);
- поражение кожных покровов, слизистой оболочки глаз, рта.
Профилактика герпесвирусной инфекции:
Важным принципом профилактики этого заболевания является прекращение близких контактов с больным человеком в период обострения.
не пользоваться чужими предметами личной гигиены;
после контакта с пораженным герпесом участком (после нанесения противовирусного крема) необходимо тщательно вымыть руки;
Больной герпесвирусной инфекцией должен иметь отдельную посуду и пользоваться личным полотенцем;
Профилактика ВПГ-1 сводится к соблюдению общих правил предупреждения респираторных заболеваний. Профилактика ВПГ-2 соответствует профилактике инфекций передающихся половым путем ( использование презервативов во время половых контактов), использование антисептических растворов после полового акта.
Профилактика инфицирования во время беременности:

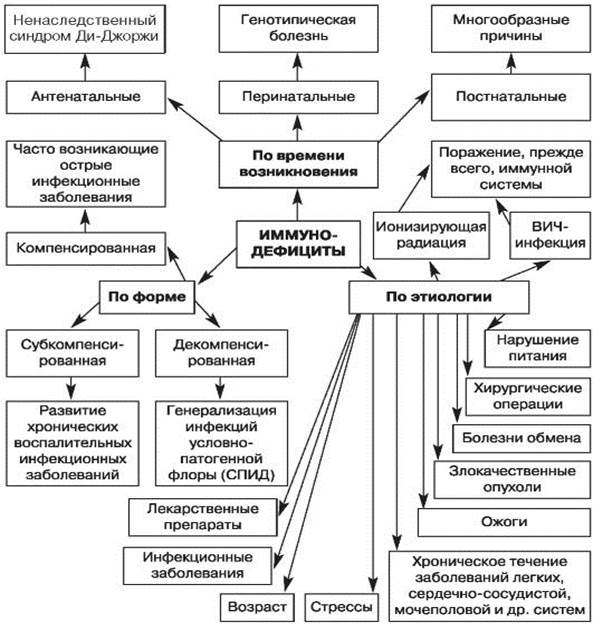
Рис. 1. Классификация вторичных иммунодефицитов по времени возникновения, этиологии, форме (по Белозерову Е.С. и др., 1992) [3]
Подводя итог в теоретической составляющей статьи – актуальности, необходимо обобщить следующее.
В педиатрии (17 лет 11 месяцев и 29 дней) в доминирующем большинстве речь идет об антенатальных и перинатальных иммунодефицитных болезнях, вторичных по отношению к анатомо-морфологическому субстрату иммунной системы – функциональных.
Таким образом, заключение врача-иммунолога должно быть сформулировано следующим образом. Антенатальная (или функциональная) иммунодефицитная болезнь, смешанного типа (или, при возможности, по отдельным звеньям, что мало вероятно), комбинированная индукция (инфекционная, гипоксическая и т.д.) с клиническими проявлениями основных синдромов – инфекционного, аллергического, аутоиммунного, неопластического и/или лимфопролиферативного.
Данные теоретические изыскания легли в основу целого цикла научно-исследовательских работ. Одно из таких исследований представлено в данной статье и посвящено исследованию иммуноиндуцирующей роли герпеса 4 типа - вируса Эпштейна-Барр у детей.
Цель: изучение особенностей клинических проявлений у детей с герпес-индуцированными формами иммунодефицитов (на примере 4 типа герпеса).
Все дети (100%) относились к часто и длительно болеющим, при этом 72 ребенка были неорганизованными (22,5%). У 78 (24,4%) детей были зарегистрированы признаки рецидивирующей герпетической инфекции с локализацией на губах, крыльях носа, слизистой оболочке полости рта. Ежегодно 92 ребенка (28,4%) переносили бактериальные инфекции в виде тонзиллитов, пневмоний, пиелонефритов, фурункулезов, гнойных конъюнктивитов, отитов, рино-синуситов. Признаки лимфоаденопатии (микролимфоаденопатии) регистрировались у 270 детей (84,4%). У 2 детей были диагностированы неопластические процессы (один ребенок умер в 2009 году). Одна девочка с лейкемоидной реакцией наблюдается у гематоонколога в течение 2 лет. Субфебрильные реакции более 12 месяцев были зарегистрированы у 39 детей (12,2%). Грубые неврологические нарушения (преимущественно двигательные) были зафиксированы у 43 детей (13,4%) (рис. 2).
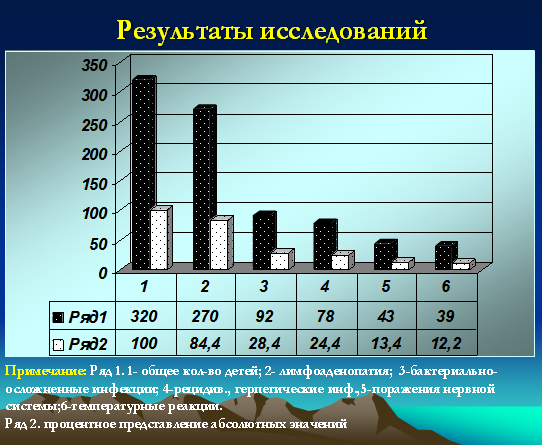
Рис. 2. Частота распределения клинических проявлений у детей с герпесиндуцированными иммунодефицитами
Иммунологические данные (в т.ч. данные лейкограммы), кроме количества лейкоцитов и лимфоцитов (абсолютное и относительное количество), носили неоднозначный характер. Классический супрессорный тип (в т.ч. и со снижением клеток цитолитической направленности) выявлялся у 108 детей (33,7%). Активация в системе клеток естественной цитотоксичности (CD16+) зафиксирована у 52 детей (16,2%). Увеличение В-клеточного пула было зарегистрировано у 38 детей (11,8%). Интересными, на наш взгляд, были полученные данные по CD95 маркеру, у 92 (28,7%) детей данный показатель был резко повышен и достигал значений 20-25%, у 30 (9,3%) детей указанный показатель не превышал 3% (рис. 3).
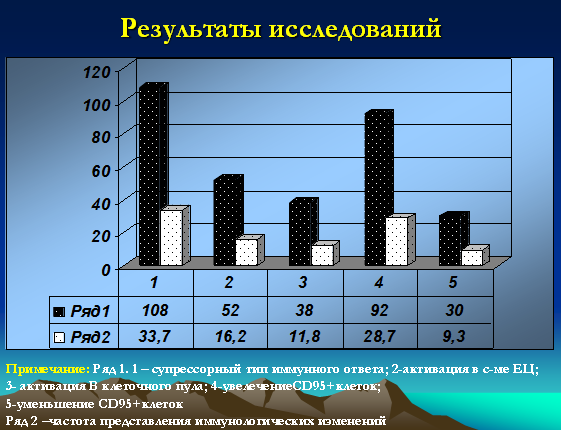
Рис. 3. Иммунологические особенности (типы распределения) у детей с герпесиндуцированными иммунодефицитами
ИФА, проведенный у детей, выявил 100% контаминацию вирусом ЭБ. Определялась следующая совокупность специфических антител:
- IgM к VCA (к капсидному антигену) – выявляются в крови в первые дни и недели болезни, максимально сохраняются до 3-4 недель;
- IgG к VCA (к капсидному антигену) – появляются в крови спустя 1-2 месяца от начала болезни, затем постепенно снижаются и сохраняются на пороговом (низком уровне) пожизненно. Повышение их титра характерно для обострения хронической ЭБВИ;
- IgM к EA (к раннему антигену) – появляются в крови в первую неделю заболевания, сохраняются в течение 2-3 месяцев и исчезают. Могут сохраняться в высоких титрах длительное время (более 3-4 месяцев), тревожно в плане формирования хронической формы ЭБВИ. Появление их при хронической инфекции служит индикатором реактивации;
- IgG к ЕA (к раннему антигену) – появляются к 3-4-й неделе заболевания, становятся максимальными на 4-6-й неделе болезни, исчезают через 3-6 месяцев. Появление высоких титров повторно указывает на активацию хронической инфекции;
- IgG к NA-1 или EBNA (к нуклеарному или ядерному антигену) – являются поздними, поскольку появляются в крови через 1-3 месяца после начала заболевания. При этом острофазные антитела выявлялись (IgM к VCA и IgM к EA) у 42 детей (13,1%), у 268 (83,7%) детей титры антител (IgG VCA + IgG к NA-1 или EBNA) значительно превышали нормативные и достигали значений более 160, у 10 (3,1%) детей диагностически значимых титров выявлено не было [9; 13] (рис. 4).
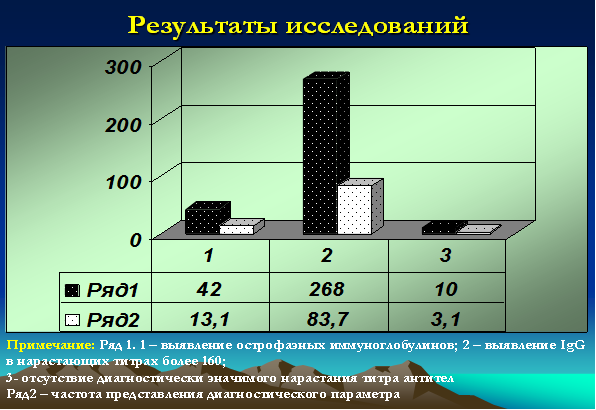
Рис. 4. Серологические исследования у детей с герпесиндуцированными иммунодефицитными болезнями
Клинические, иммунологические и этиологические сопоставления выявили следующие закономерности.
Отдельно хочется остановиться на методах ПЦР-диагностики. В литературе активно обсуждается вопрос об использовании ПЦР для исследований на инфекции семейства герпес в различных биологических субстратах. Здесь необходимо понимать, что данный метод, особенно при использовании его для исследования плазмы, имеет свои особенности – он всегда количественный! Определение качественное не имеет смысла, так как инфекция пожизненно персистирует в организме человека. Как у больных ЭБВИ, так и у носителей может быть положительная ПЦР. Поэтому для их дифференцировки проводится ПЦР-анализ с заданной чувствительностью: для носителей до 10 копий в пробе, а для активной инфекции – 100 копий в пробе. Специфичность данного метода хоть и достигает 100%, при этом не исключает ложноположительные результаты, т.к. ПЦР-анализ информативен только при размножении (репликации) вируса, то существует и определенный процент ложноотрицательных результатов с отсутствием репликации в момент исследования [5; 9].
В результате проведенного нами исследования, ПЦР крови всегда имела отрицательный результат, даже у детей с неопластическими процессами. Распределение ПЦР-положительных результатов у детей со слизистых оболочек (ротоглотка, нос) и мочи имело следующее цифровое распределение.
Положительные реакции с 3 биологических объектов имели 36 детей (11,25%), у 62 положительные ПЦР реакции были с зева и носа – 19,38%, у 43 детей диагностировали положительный результат только с зева (13.44%), и 71 ребенок имели положительные значения ПЦР со слизистой оболочки носа (22,19%). Положительные значения только в моче имели 51 ребенок (15,94%). Остальные дети (в количестве 57) имели отрицательный результат ПЦР-исследований с биологических сред.
Дети с неопластическими процессами, длительным субфебрилитетом, лейкемоидной реакцией, лимфоаденопатией имели признаки активации хронической инфекции, резкое увеличение CD95+ клеток, положительные маркеры наличия и обострения ВЭБ в ИФА и ПЦР-исследованиях.
Таким образом, все дети имели индуцированные формы функциональной иммунодефицитной болезни, доминирующей причиной которой являлся вирус ЭБ. Проведенные предварительные клинико-иммунологические исследования наглядно демонстрируют необходимость комплексного обследования детей с функциональными нарушениями в системе иммуногенеза с обязательной оценкой уровня инфекционной (вирусной) контаминации. Выявление основных причин трактуется необходимостью применения комплексных методов лечения, в т.ч. и с применением противовирусных препаратов.

Герпесвирусная инфекция кошек, или ринотрахеит (FHV)- заболевание, вызванное вирусом герпеса.
Ринотрахеит – широко распространенное респираторное заболевание кошачьих, вызываемое вирусом герпеса кошек тип 1. Заболевание видоспецифичное и не представляет угрозы для других видов животных и человека. Протекает в острой и хронической форме.
- больные животные с острой формой инфекции/
- переболевшие кошки - носители: являются скрытыми (латентными), т.е. без симптомов болезни, носителями вируса в нервных клетках, особенно тройничного нерва, длительность носительства в среднем составляет 6 мес, но может быть пожизненной.
- кошки с хронической формой инфекции в стадии обострения.
Заражение вирусом происходит через выделения из носа, рта, глаз больных животных: при непосредственном контакте с больной кошкой, через инфицированный воздух, предметы ухода, корма, а также через обувь и одежду людей, контактировавших с источником инфекции. Внедрение и размножение вируса (репликация) в организме кошки происходит в основном в слизистых оболочках носоглотки и миндалин, но помимо этого часто в патологический процесс включается конъюнктива глаз, лимфоузлы и пр.; заражение невакцинированных беременных кошек приводит к внутриутробному инфицированию плодов ( и как следствие- аборты, рождение мертвых или нежизнеспособных плодов).
Выделение вируса в окружающую среду начинается через 24 часа после заражения и продолжается до 3 недель. Устойчивость вируса: вирус погибает при 37С в течение 3 часов, при 56С – в течение 5 мин; остается жизнеспособным при 25С в течение 1 мес, при 4С -5 месяцев. Чувствителен к большинству дезинфектантов и антисептиков.
Вирус герпеса кошек приводит, как правило, к острому респираторному заболеванию. Инкубационный (скрытый) период заболевания обычно 2-6 дней.
Клинические признаки заболевания:
- Угнетение и отсутствие аппетита.
- Чихание и выделения из носа и глаз, сначала прозрачные (серозные), а при продолжительном течение болезни становятся слизисто-гнойными.
- Повышение температуры тела.
- Может быть кашель, одышка.
- Иногда появляются язвы языка, что клинически напоминает другую инфекционнную болезнь кошек - кальцивироз. Чаще всего этот симптом наблюдается у кошек с хроническим течением герпеса в стадии обострения.
- Поражение роговицы: язвы и глубокий кератит.
- Может быть слюнотечение (обычно наблюдается при язвах в ротовой полости).
- Очень редко - язвы на носу, коже морды.
- Часто ринотрахеит протекает совместно с другими инфекциями: хламидиоз, кальцивироз, микоплазмоз, бордетелла бронхосептика (Bordetella bronchiseptica).
Несмотря на то, что данная болезнь может приводить к тяжелому состоянию, уровень смертности невысокий, за исключением очень маленьких котят и кошек с сильно ослабленным иммунитетом. Смерть бывает наиболее часто вследствие обезвоживания, вторичной бактериальной инфекции, приводящей к бронхопневмонии. В среднем симптомы болезни наблюдаются в течение 7-10 дней.
- После переболевания острой герпесвирусной инфекцией около 80% кошек остаются вирусоносителями (т.е. внешне выглядят совершенно здоровыми) и примерно 50% из них выделяют вирус в окружающую среду. Выделение вируса может происходить спонтанно, но в основном это случается после стресса: переезд на другое место жительства, посещение выставок, роды, лактация, использование глюкортикостероидов (например, преднизолон, дексаметазон), оперативные вмешательства и др.
- Кошки могут стать вирусоносителями и без проявления каких-либо симптомов, т.е. кошка, заразившись, может оказаться носителем даже несмотря на то, что сама никогда не проявляла признаков болезни или была полностью вакцинирована.
- Также для ринотрахеита характерен переход в хроническую (латентную, или скрытую) форму: в этом случае вирус поступает в окружающую среду только в период обострения, т.е. когда проявляются симптомы заболевания. Хроническая (латентная) герпесвирусная инфекция наиболее часто переходит в острую стадию из-за стресса: переезд, выставки, оперативные вмешательства и др.
Несмотря на то, что у кошек встречаются и другие инфекции, сопровождающиеся респираторными симптомами (такие как кальцивироз, хламидиоз и др.), в большинстве случаев для постановки диагноза достаточно имеющихся клинических признаков.
Для диагностики в России чаще всего используют метод ПЦР, для этого берутся мазки из носа и конъюнктивы глаз. При первичной герперсвирусной инфекции вирус обнаруживается максимум в течение 7 дней от начала клинических проявлений, при повторной инфекции- максимум в течение 4 дней, во время латентной фазы в обычных мазках с конъюнктивы вирус не выявляется, т.к здесь его уже нет, а локализуется он в клетках нервной ткани.
- Многие больные кошки не едят, т.к. теряют обоняние или из-за болезненности, вызванной наличием язв в ротовой полости, поэтому очень важно кошку кормить: для этой цели подойдет любой готовый корм в виде паштета, который предварительно разводят теплой водой, и дают кошке из шприца на 10-20мл без иглы. Если кошку в течение 3 дней не получается кормить насильно, ей показана установка специальных зондов, через которые будет осуществляется кормление.
- Промывание носа раствором натрия хлорида 0,9% (физиологический раствор) для очищения от скопившихся выделений, проводится ежедневно и несколько раз в день. Больная кошка должна содержаться в чистом, хорошо проветриваемом помещении.
- Антибиотики для лечения вторичной бактериальной инфекции
- Системные противовирусные препараты
- Симптоматическое лечение: для кошек с выраженными симптомами обезвоживания необходимы внутривенные капельницы, при повышенной температуре используются жаропонижающие средства и пр.
Читайте также:


