Папиллома во рту при раки

Вирус папилломы человека (ВПЧ) является наиболее распространенным заболеванием, передающимся половым путем. По данным всемирной организации здоровья, существует более 40 типов ВПЧ, но большинство из них не причиняют вреда организму человека, так как защищены иммунной системой, не вызывая никаких проблем со здоровьем.
Тем не менее, некоторые типы ВПЧ негативно влияют на полость рта и горло. У людей с низким уровнем риска могут возникать бородавки в ротовой полости или горле, но штаммы с высоким риском связаны с раком головы и шеи (также известный как рак ротоглотки), которые влияют на рот, горло, миндалины, основание языка. Оральный рак - это всего лишь один тип рака головы и ротоглотки. Данные ВОЗ показывают, что около 7% людей имеют пероральное ВПЧ, но только 1% имеют тип перорального ВПЧ, обнаруженного при раке головы и шеи.
Вирус распространяется в большинстве случаев при половом контакте. Много случаев передачи ВПЧ из рук/рта к половым органам. По статистике у женщин вирус диагностируется в 80% случаев в возрасте 50+ . А у мужчин в 60% случаев. Вирус состоит из двойной спирали ДНК. В котором закодировано 2 поздних и 8 ранних типов белков – L и E, соответственно. Всего описано более 1000 видов ВПЧ. Среди них выделяют типы с высоким риском развития опухоли, и с низким.
High risk: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 73, 82.
Low risk: 6, 11, 40, 42, 43, 44, 54, 61, 70, 72, 81, 89.
Какие симптомы рака головы или ротоглотки от ВПЧ?
Болезненность или раздражение, которые не исчезают.
Красные или белые пятна во рту.
Боль, повышенная чувствительность или онемение во рту или губах.
Шероховатые пятна, сыпь, чувствительные или эродированные участки во рту.
Трудность жевания, глотания, произношения.
Сложность перемещения челюсти или языка.
Отклонения в прикусе.
Некоторые пациенты жалуются на стойкое воспаление горла, чувствуя, что что-то попадает в их горло, охриплость, изменение голоса, боли в ушах, боль при глотании и необъяснимую потерю веса. Если у вас есть какие-либо из этих симптомов, сообщите об этом терапевту, особенно они не проходят более 10 дней.

Определить вирус папилломы у пациента можно путем забора ткани и ее исследования. Также существуют тесты на определение ВПЧ:
Выявление вирусов 16 и 18, которые провоцируют большинство онкологических заболеваний.
Обнаружение вируса папилломы 16 и 18 среди других вирусов с высоким уровнем рисков.
Выявление ВПЧ с высоким уровнем риска без определение конкретного типа.
Определить его можно проведя анализ любых клеток организма, но чаще всего проводят скрининг женщинам при подозрении рака шейки матки.
Для труднодоступных областей горла доктор использует фарингоскоп и ларингоскоп. При подозрении на тонзиллярный ВПЧ-рак проводится биопсия папилломы через полую иглу.
Папилломатоз гортани
Это заболевание, которое спровоцировано ВПЧ. Имеет рецидивирующий характер и проявляется образованием наростов (бородавчатого типа) в районе гортани и голосовых связок больного, подскладочном пространстве и надгортаннике. Наросты создают ощущение постороннего (инородного) тела в гортани, могут вызывать приступы одышки, удушья и кашель. В ряде случаев отмечают расстройства дыхания, хрипоту и даже потерю голоса. Вирус передается половым путем. Многие больные отмечали наличие папиллом на половых органах. После вступления в сексуальный контакт вирус проявлялся у акцептора. Также может передаваться при проходе ребенка родовыми путями или через плаценту. Как правило, инфицирование происходи неонкогенными типами ВПЧ (6-й и 11-й).
Лечение папилломатоза гортани противовирусными препаратами при поддержке иммунотерапией не дают стойких результатов, поэтому в большинстве случаев не рекомендуется к применению. Эффективный метод борьбы – удаление наростов с частичной резекцией поврежденных голосовых связок.

Основная группа признаков: проблемы при глотании, сложности пережевывания пищи, шишкоподобное образование на шее или щеке, кашель с мокротой и кровью, непрходящая долгое время хрипота.
Вторая группа признаков: налет на миндалинах белого или алого цвета, боли и спазмы в горле, онемение языка, спазмы и отек в челюсти.
ВПЧ-положительный рак головы и шеи обычно развивается в горле в задней части языка и вблизи или в складках миндалин, что затрудняет их обнаружение. Хотя у людей с ВПЧ-положительным раком риск смерти или рецидива ниже, чем у тех, у кого отрицательный уровень ВПЧ, ранний диагноз связан с лучшими результатами терапии. Регулярные терапевтические осмотры, которые включают осмотр всей головы и шеи, могут быть жизненно важными для раннего выявления рака. Также вы можете попросить вашего стоматолога внимательно изучать ротоглотку во время лечения или профилактики. Иногда дантист может заметить нехарактерные изменения и направить на консультацию к терапевту.
Онкогенные ВПЧ 16 и 18
Данные два типа вирусов являются наиболее опасными, так как могут спровоцировать развитие онкологического заболевания у человека. По статистике они становятся причиной развития рака шейки матки в 70% случаев. Вероятность возрастает при наличии усугубляющих болезней – сахарный диабет, туберкулез, гепатит B и C, вирус Эпштейн-Барра.
В докладе всемирной организации здоровья, который был представлен в начале 2000-х годов, прозвучала информация, что 5,2% случаев рака вызваны вирусом папилломы человека. К сожалению, новых данных по данному направлению ВОЗ не публиковала.
Специфика заболевания у мужчин и женщин
Мужчины. Проявляются в большинстве случаев развитием бородавок в районе половых органов и заднего прохода. Вызывают внутриклеточную неоплазму клеток полового члена и ануса. В возрасте старше 50 лет могут возникать в гортани.
Женщины. В большинстве случае протекают бессимптомно многие годы. Проявляются после наступления менопаузы. Чаще всего в области половых органов, провоцируя онкологию шейки матки.
Дети. Может проявляется наростами в различных частях тела при снижении общего иммунитета ребенка. При нормализации – уходят. У маленьких детей иногда фиксируют папилломатоз гортани при инфицировании через плаценту или при родах.
Почему ВПЧ вызывает рак
Вирус папилломы человека заражает клетки выстилающие эпителий, который покрывает человеческий организм внутри и снаружи. Среди них – горло, шея, голова, половые органы, анус. Он не опадает в кровоток и не разносится по организму. Однако вырабатывает чрезмерное количество белка. Иммунная система способна его распознать, но не всегда может побороть ВПЧ. Следственно, инфицированные клетки не разрушаются, вирус становится стойким к атакам иммунной системы и возможно проявление мутаций. Таким образом появляются новообразования. Стоит отметить, что несмотря на высокий риск перерастания мутации в рак, далеко не всегда так происходит. Кроме того, более чем в половине случаев фиксируется образование доброкачественной онкологии.
Вирус может стать причиной возникновения:
26 февраля 2014
Опасный поцелуй и его последствия
Что приводит к позднему выявлению рака ротовой полости
– Александр Узбекович, врачебное сообщество Европы и США обеспокоено увеличением числа зарегистрированных случаев заболевания раком слизистой оболочки полости рта. Актуальна ли эта проблема для России?
– Злокачественные новообразования полости рта относятся к онкопатологии области головы и шеи. В Европе рак головы и шеи находится на шестом месте по распространенности. Он встречается приблизительно в 2 раза реже, чем рак легких, но в 2 раза чаще, чем рак шейки матки.
В 2012 г. в Европе выявлено более 150 тыс. новых случаев – это количество эквивалентно дважды целиком заполненному олимпийскому стадиону в Лондоне. Например, в структуре причин смертности населения Архангельской области второе место занимают злокачественные новообразования, а опухоли челюстно-лицевой области составляют 15% от общего числа раковых заболеваний. Причем они, как правило, относятся к разряду высокой степени злокачественности, для которых характерен быстрый рост и раннее метастазирование. Несмотря на увеличение числа заболевших, люди мало знают об этом виде онкопатологии, а потому исход при постановке данного диагноза в основном неблагоприятный: в 60% случаев рака головы и шеи фиксируют позднюю стадию заболевания, и 60% таких пациентов умирают на первом году с момента установления диагноза.
– В принципе, онкологическим заболеванием заразиться нельзя, но можно инфицироваться онкогенным вирусом, который, в свою очередь, индуцирует появление злокачественной опухоли. Что делается для того, чтобы население было более информировано в вопросах ранней симптоматики рака головы и шеи?
– Болезнь начинается с маленькой язвочки или нароста на слизистой оболочке полости рта, которые не беспокоят длительный период времени и постепенно увеличиваются в размерах. 90% людей, страдавших данным видом онкопатологии, могли бы быть живы, если бы обратились за квалифицированной помощью вовремя. В целях повышения осведомленности среди населения о признаках и симптомах этого вида злокачественного новообразования Европейское общество исследователей головы и шеи (EHNS) инициировало проведение Первой общеевропейской недели ранней диагностики рака головы и шеи. В прошлом году Россия присоединилась к странам, в которых прошла неделя ранней диагностики, приняла участие в акции и наша область. Двери Архангельского областного клинического онкологического диспансера и областной клинической больницы были открыты для всех, кто пожелал пройти обследование. В дни открытых дверей приём населения вела мультидисциплинарная команда специалистов, в число которых также входили и сотрудники нашего университета.
– В рамках проведения Первой общеевропейской недели ранней диагностики в Архангельске было осмотрено более 50 человек, у одного из них было выявлено предраковое заболевание (пациент уже прооперирован), у 12 – обнаружены доброкачественные новообразования кожи и мягких тканей. Это хороший результат?
– Это средний результат по стране, учитывая то, что данное мероприятие в нашем городе практически не рекламировалось. Я думаю, что европейская неделя ранней диагностики – хороший повод еще раз напомнить людям о необходимости ответственно относиться к своему здоровью. Тем более что в нашей области есть все возможности получить квалифицированную помощь специалистов при онкологических заболеваниях головы и шеи.
Работа профильных специализированных отделений проводится в тесном контакте и под руководством кафедр онкологии, лучевой диагностики и лучевой терапии, челюстно-лицевой хирургии и хирургической стоматологии Северного государственного медицинского университета. Задача наших кафедр – теоретическая и практическая подготовка кадров по онкологии. Выявление больных с новообразованиями головы и шеи и первичная диагностика проводятся на местах главным образом врачами-стоматологами и лор-врачами, а также офтальмологами, дерматологами, нейрохирургами, невропатологами, эндокринологами, терапевтами и хирургами общей лечебной сети. Именно поэтому ведущие ЛПУ города и области должны оснащаться современным диагностическим оборудованием, которое позволит более эффективно решать проблему ранней диагностики рака данной локализации.
– Кроме плохой осведомленности населения, каковы еще причины поздней постановки диагноза?
– Основные причины онкозапущенности – это бессимптомное течение начальных стадий, дефицит онкологов, большой процент изношенности медицинского оборудования во многих лечебных учреждениях и, что хотелось бы особенно выделить, недостаточная онконастороженность врачей и формальный подход к разбору ошибок в диагностике заболеваний. Опухоли полости рта относятся к визуальным локализациям, и, следовательно, их диагностика на ранних стадиях должна превышать 90% случаев, однако этого не происходит.
По сводным данным различных отделений опухолей головы и шеи, около 40% больных имеют запущенные формы злокачественных новообразований челюстно-лицевой области и шеи по вине врачей. Врач любой специальности любого лечебно-профилактического учреждения должен при осмотре пациента исключить симптомы, наводящие на онкологическую патологию. Ранняя диагностика злокачественной опухоли полости рта зависит от внимательности, в том числе, и врачей-стоматологов, их знаний в области онкологии, дальнейшей тактики в отношении больного.
Основные ошибки, приводящие к позднему выявлению раковых заболеваний, которые допускают врачи, – это игнорирование тщательного осмотра и пальпации подозрительных изменений губ, полости рта и языка у всех больных, обращающихся за медицинской помощью. Отсутствие у врачей онкологической настороженности заставляет больного ходить от специалиста к специалисту для уточнения диагноза, теряя при этом драгоценное время.
– В основном именно стоматологи первыми проводят осмотр полости рта. На что специалисты этого профиля должны обращать особенное внимание?
– При осмотре больного обязательно необходимо использовать бимануальную пальпацию дна полости рта, языка, региональных лимфатических узлов, так как увеличение лимфатических узлов подбородочной, подчелюстной областей может свидетельствовать о наличии злокачественной опухоли. Обращать внимание на такие симптомы, как болезненные или безболезненные уплотнения на красной кайме губ, шероховатая бляшка, слегка возвышающаяся над окружающими тканями, сосочкового вида кровоточащая поверхность, длительно незаживающие язвы с валикообразными краями, постоянная заложенность или сукровичные выделения из полости носа, ограничение открывания рта, онемение кожи подглазничных областей. Широкий охват населения плановой санацией полости рта также открывает перед стоматологами реальные возможности ранней диагностики злокачественных опухолей. В задачи, стоящие перед стоматологами, входит повышение медицинской грамотности населения, разъяснение необходимости неотложно обращаться к специалисту за помощью при первом появлении признаков какого-либо патологического процесса в челюстно-лицевой области. И конечно, устранение предрасполагающих факторов развития злокачественной опухоли и лечение предопухолевых заболеваний, ранняя диагностика злокачественных новообразований и своевременное направление пациентов в специализированные лечебные учреждения – онкологические диспансеры. А также профессиональный рост наших врачей.
В 1974 г. немецкий врач и ученый Харальд цур Хаузен совершил революцию в канцерогенезе, а спустя 34 года получил Нобелевскую премию в области медицины. Изучая вирус-индуцированные опухоли, он доказал взаимосвязь между вирусом папилломы человека и развитием рака шейки матки. В ходе исследований выяснилось, что онкогенный вирус взаимодействует с молекулой ДНК, поэтому в новообразовании могут существовать комплексы ВПЧ-ДНК, которые и были впоследствии обнаружены. Беспорядочные половые связи, оральный секс, отсутствие гигиены полости рта – вот основные пути передачи вируса папилломы человека и, как следствие, увеличение числа случаев появления злокачественных новообразований полости рта в молодом возрасте. Некоторые из серотипов ВПЧ вызывают развитие крайне злокачественных форм заболевания, вирус обусловливает 40-80% всех орофарингеальных раков. Если человеку требуется еще больше мотивации для того, чтобы быть более разборчивым в половых связях и поддерживать должную гигиену полости рта, теперь она точно есть.

Заболеваемость и смертность раком органов полости рта (РОПР) в последние годы имеет тенденцию к росту во всем мире и в структуре онкопатологии, составляя 2,3 %. Ежегодно у 90 тысяч человек в мире впервые диагностируются опухоли данной локализации [9].
Стандартизированный показатель заболеваемости в Европе равен 1,6 на 100 тысяч населения, а в мире этот показатель составляет 1,15 [7, 9].
В России в структуре онкологической заболеваемости населения в 2013 году рак слизистой оболочки полости рта составляет около 5,5 % [4]. Среди опухолей головы и шеи данная патология занимает второе место, после рака гортани [6].
Рост данной патологии связывается с курением, употреблением крепких алкогольных напитков, плохой гигиеной полости рта, неполноценным питанием, неудовлетворительными результатами лечения предраковых заболеваний [5].
Рак орофарингеальной зоны среди причин летальности стоит на 4-м месте, после рака легкого, желудка и колоректальной зоны [6].
Несмотря на появление различных современных методик лечения, смертность от рака органов полости рта в Российской Федерации у мужчин занимает 7 место, у женщин – 16-е и в 2007 году составила 8,1 и 1,1 на 100 тысяч населения [6], эти данные указывают на необходимость продолжения изучения онкогенеза с других сторон.
В последние годы появилось много исследований, посвященных связи онкопатологии и вирусных инфекций, изучающих так называемый вирус-ассоциированный онкогенез. Было доказано, что более чем в 15 % этиологическими агентами новообразований являются вирусы [10].
Из всех вирусов наибольший интерес исследователей вызывают вирус Эпштейна ‒ Барр (ВЭБ) и вирус папилломы человека (ВПЧ), им посвящено большое количество научных работ [3].
По данным зарубежных авторов, доказательствами связи вируса Эпштейна ‒ Барр и развития новообразований являются: моноклональность ДНК ВЭБ в опухолевых клетках, высокий уровень свободной вирусной ДНК в плазме крови пациентов, наличие корреляции между титром антивирусных антител, уровнем свободной вирусной ДНК в плазме пациента и тяжестью заболевания, также повышенный титр антивирусных антител часто предшествует появлению новообразования и остается высоким на момент постановки диагноза [8].
Перерождение же папилломы в злокачественное новообразование прямо пропорционально связи между онкогенным белком и опухолевым супрессорным белком, например Е6 связывается с р53, Е7 с Rb. Папилломавирусы – единственная группа вирусов, для которых доказано, что они индуцируют образование опухолей у человека в естественных условиях. Онкопротеин Е6 экспрессирует телемеразу, ответственную за активацию пролиферации клеток. Онкобелок Е7 в сочетании с метаболизированием эстрадиола и как следствие образования 16а-гидроксистерона (16а-ОНЕ1), активирующего экспрессию гена Е7, является патогенетической основой вирус-индуцированного онкогенеза. Все это обеспечивает пролиферацию опухолевых клеток и подавляет иммунный ответ [2]. Наличие Е7 (Е6) в цервикальных пробах свидетельствует о процессе малигнизации эпителиальных клеток. Так, для выявления онкопротеина Е7 были созданы тест-системы, для ИФА [2].
Оценка локального уровня некоторых цитокинов при данных процессах представляет отдельный интерес, поскольку воспалительный процесс вызывает их гиперпродукцию иммунокомпетентными клетками, и некоторые из них могут быть факторами роста и распространения опухоли [1].
Исследование микрососудистой инвазии опухолевых клеток в эндотелиальный слой сосудов вызывает интерес как предиктор высокой стадии, степени и распространённости опухоли и, как следствие, возможность ее использования с прогностической целью для оценки течения и прогноза заболевания.
Таким образом, с учетом мониторинга совокупности факторов, ассоциированных с онкогенезом, представляется целесообразным уточнение их прогностической значимости для оценки прогрессирования процесса при раке органов полости рта.
Цель исследования – оценить роль вирусов Эпштейна – Барр и папилломы человека, микрососудистой инвазии и локального уровня цитокинов (ИЛ-2, ИЛ-8, ИЛ-6, ИЛ-10, ИЛ-1β, ИЛ1RА, ИНФ-α, ИНФ-γ, ФНО-α) на течение РОПР.
Материалы и методы исследования
Мужчин было 56, женщин – 16. Возраст больных составлял 34–73 года. По распространенности процесса: со II стадией (T2N0M0) было 13 человек, III – 30 (T2N1M0 – 4, T3N0M0 – 18, T3N1M0 – 8), IV – 29 (T3N2M0 – 4, T4N0M0 – 15, T4N1M0 – 10).
У 59 (81,9 %) больных опухолевым процессом был поражен язык, у 13 (18,1 %) – слизистая дна полости рта. На языке опухоль располагалась чаще на боковой поверхности (52,8 %).
У всех больных был плоскоклеточный рак. Высокая степень дифференцировки (G1) имела место у 22 больных, средняя степень (G2) – 35 и низкая степень (G3) – 15.
Материалом для исследования служили фиксированные в формалине и парафине (FFPE ткани) интраоперационно взятые образцы ткани опухоли и перитуморальной зоны.
Из гомогената ткани опухоли, взятой интраоперационно, ДНК вируса выделяли методом сорбции на магнитных частицах в автоматическом режиме на приборе MagNa Pure Compact с использованием набора реагентов MagNa Pure Compact Nucleic Acid Isolation Kit I-Large Volume на приборе MagNa Pure Compact (Roche, Швейцария). Амплификацию с последующей детекцией ДНК осуществляли методом полимеразной цепной реакции (ПЦР) с гибридизационно-флуоресцентной детекцией в режиме реального времени на термоциклере RotorGene 6000 (QIAGEN, Германия).
Методом ELISA определяли локальные уровни интерлейкинов (ИЛ-2, ИЛ-8, ИЛ-6, ИЛ-10, ИЛ-1β, ИЛ1RА, ИНФ-α, ИНФ-γ, ФНО-α) в гомогенатах фрагментов ткани опухоли и пограничной с опухолью макроскопически неизмененной ткани, взятые интраоперационно. Рассчитывали удельное содержание цитокинов (пг/мл на 1 г белка).
Для оценки ангиогенеза в опухолях применяли окрашивание микрососудов антителом CD34. Количество сосудов определяли в каждом поле зрения препарата при использовании объектива х40.
Для оценки пролиферативной активности опухоли подсчитывали количество ki-67-положительных опухолевых клеток, приходящихся на 200–300 опухолевых клеток, использовали антиген ki-67. Также определяли нормальный и мутантный тип p53.
Статистическая обработка осуществлялась программой Statistica 6,0.
Результаты исследования и их обсуждение
Данные молекулярно-биологических исследований показали, что уровень инфицирования ткани опухоли вирусами папилломы человека составил 20,8 %, в том числе низкого онкогенного риска 5,4 %, высокого 15,3 % Чаще других были выявлены 16 тип (11,1 %) и 11 тип ВПЧ (4,2 %). Частота инфицирования пациентов в зависимости от группы представлена на рис. 1.
Установлена зависимость частоты метастазирования и рецидивирования опухоли от группы вируса. ВПЧ низкого и высокого онкогенного риска чаще были обнаружены в образцах без метастазов.
Частота инфицирования ткани опухоли вирусами группы герпеса составила 68,1 %, в т.ч. вируса простого герпеса 1 типа (ВПГ 1 типа) 5,5 %, цитомегаловируса (ЦМВ) 11,1 %, вируса Эпштейна ‒ Барр (ВЭБ) 62,5 %, вируса герпеса человека 6 типа (ВГЧ 6 типа) 16,7 %. На рис. 2 представлено распределение инфицированности вирусами группы герпеса в зависимости от группы больных.
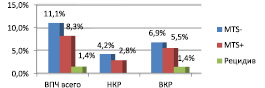
Рис. 1. Частота инфицирования FFPE ткани у пациентов с метастазами, без метастазов, с рецидивами
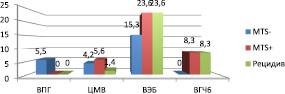
Рис. 2. Частота инфицирования ткани опухоли вирусами группы герпеса у пациентов с метастазами, без метастазов и с рецидивами
С увеличением распространенности опухолевого процесса было отмечено увеличение частоты инфицирования ткани опухоли вирусами группы герпеса. В большей степени это положение характерно для ВЭБ, ВГЧ 6 типа. Так, суммарная частота инфицирования всеми представителями этой группы для стадии Т2 составила 70,6 %, Т3 – 80 %, Т4 – 84 %. Для цитомегаловируса эти показатели составили 5,9; 12,5 и 16 %, для вируса Эпштейна – Барр – 64,7; 80 и 80 %, для вируса герпеса 6 типа 11,7; 16,7 и 20 % соответственно.
При анализе клинических данных в сопоставлении с полученными лабораторными было установлено, что у больных с регионарными метастазами ВЭБ встречался в 17 случаях (70,8 %) от общего числа больных данной группы), в то время как ВПЧ – в одном (25 %). У больных без метастазов ВЭБ был выявлен в 11 случаях (45,8 %), в то время как ВПЧ – у 8 (33,3 %). Для больных с рецидивами ВЭБ составил – 17 случаев (70,8 %), а ВПЧ – 1 (1,4 %). Таким образом, у больных с метастазами и рецидивами выявление ВЭБ-ассоциированного рака было выше (70,8 %), чем у больных без метастазов (45,8 %), в то время как ВПЧ-позитивные больные встречались чаще в группе без метастазов (33,3 %), в отличие от других групп (25 и 1,4 %).
При изучении локальных уровней цитокинов (ИЛ-2, ИЛ-8, ИЛ-6, ИЛ-10, ИЛ-1β, ИЛ1RА, ИНФ-α, ИНФ-γ, ФНО-α) отмечено статистически значимое (р Примечания:
* – отличия показателей статистически достоверны по отношению к группе без метастазов (Р ≤ 0,05);
º – отличия показателей статистически достоверны по отношению к группе с метастазами (Р ≤ 0,05).
1. Инфицированность вирусами папилломы человека ткани опухоли можно рассматривать как благоприятный прогностический признак в отношении развития метастазов у больных с раком органов полости рта (в группе без метастазов (33,3 %), в отличие от других групп (25 и 1,4 %)). Инфицирование вирусами группы герпеса ткани опухоли можно рассматривать как неблагоприятный прогностический признак (выявление ВЭБ-ассоциированного рака – 70,8 % у больных с метастазами и рецидивами, у больных без метастазов 45,8 %).
2. Различия тканевого цитокинового состава между больными раком языка и полости рта без регионарных метастазов, с регионарными метастазами и при рецидивах статистически не значимы. При этом показаны различия их уровня между тканью опухоли и перитуморальной области с преобладанием содержания провоспалительных цитокинов ИЛ-1ß, ИЛ-6, ИЛ-8 в опухолевой ткани. Вероятно, избыток провоспалительных цитокинов, у которых описаны ростостимулирующие свойства, наблюдается за счет их продукции опухолевыми клетками, а также присутствующими в очаге активированными макрофагами, что способствует росту и распространению опухоли.
3. Преобладание сосудов крупного диаметра с утолщенной стенкой может коррелировать с наличием или возможным развитием метастазов и рецидивов, таким образом, иметь неблагоприятный прогностический характер.
ВГЧ – вирус герпеса человека,
ВПГ 1 типа – вирус простого герпеса 1 типа,
ВГЧ 6 типа – вирус герпеса человека 6 типа,
ВПЧ – вирус папилломы человека,
ВПЧ 16 типа – вирус папилломы человека 16 типа,
ВПЧ ВКР – вирус папилломы человека высокого канцерогенного риска,
ВПЧ НКР – вирусы папиллом человека низкого канцерогенного риска,
ВЭБ – вирус Эпштейна ‒ Барр,
ДНК – дезоксирибонуклеиновая кислота,
ИЛ-1β – Интерлейкин – 1β,
ИЛ1RА – Интерлейкин 1RА,
ИФА – Иммуноферментный анализ,
ПЦР – полимеразная цепная реакция,
РОПР – рак органов полости рта,
ФНО-α – Фактор некроза опухоли – α.
Рецензенты:
Каймакчи О.Ю., д.м.н., ассистент кафедры онкологии, Ростовский государственный медицинский университет, г. Ростов-на-Дону;
Шихлярова А.И., д.б.н., профессор, руководитель лаборатории изыскания новых противоопухолевых средств и изучение механизма их действия, ФГБУ РНИОИ МЗ РФ, г. Ростов-на-Дону.
Основные факты
- Вирус папилломы человека (ВПЧ) — это общее название группы вирусов, чрезвычайно широко распространенных во всем мире.
- Известно более 100 типов ВПЧ, из которых не менее 14 являются онкогенными (так называемые вирусы высокого онкогенного риска).
- ВПЧ передается, главным образом, половым путем, и большинство людей заражаются ВПЧ вскоре после начала половой жизни.
- Рак шейки матки развивается в результате передающейся половым путем ВПЧ-инфекции определенных типов.
- В 70% случаев причиной рака шейки матки оказываются ВПЧ двух типов (16 и 18).
- Имеются также доказательства связи ВПЧ с раком заднего прохода, вульвы, влагалища, полового члена и ротоглотки.
- Рак шейки матки — второй по распространенности вид рака среди женщин, проживающих в развивающихся странах. По оценкам, в 2018 г. число новых случаев в этих странах составило 570 000 (84% от всех новых случаев в мире).
- В 2018 г. от рака шейки матки умерло около 311 000 женщин, причем более 85% этих случаев смерти имели место в странах с низким и средним уровнем дохода.
- В комплекс мероприятий по борьбе с раком шейки матки входят первичная профилактика (вакцинация против ВПЧ), вторичная профилактика (скрининг и лечение предраковых поражений), третичная профилактика (диагностика и лечение инвазивного рака шейки матки) и паллиативная помощь.
- Вакцины, формирующие иммунитет к ВПЧ 16-го и 18-го типов, рекомендованы ВОЗ и одобрены к применению во многих странах.
- Одним из экономически эффективных способов профилактики рака шейки матки считается скрининг и лечение предраковых поражений у женщин в возрасте старше 30 лет.
- При выявлении рака шейки матки на ранней стадии возможно полное его излечение.
Общие сведения о ВПЧ
Вирусы папилломы человека (ВПЧ) — возбудители самой распространенной вирусной инфекции половых путей. Большинство ведущих половую жизнь женщин и мужчин рано или поздно приобретают эту инфекцию, а некоторые могут заражаться несколько раз в течение жизни.
Большинство женщин и мужчин заражаются ВПЧ вскоре после начала половой жизни. Инфекция ВПЧ относится к заболеваниям, передающимся половым путем, хотя заражение возможно и при половых контактах без проникновения. Известно, что передача вируса происходит и при простом соприкосновении половых органов.
Среди множества типов ВПЧ многие не представляют опасности для здоровья. ВПЧ-инфекции обычно исчезают за несколько месяцев без какого бы то ни было лечения, и примерно в 90% случаев элиминация инфекции из организма достигается в течение 2 лет. В небольшой доле случаев инфекции ВПЧ определенных типов могут принимать хронический характер и со временем приводить к развитию рака шейки матки.
Рак шейки матки вне всяких сомнений является самым распространенным из заболеваний, связанных с ВПЧ. Почти все случаи рака шейки матки вызваны ВПЧ-инфекцией.
Инфекциями ВПЧ некоторых типов также обусловлена определенная доля случаев рака заднего прохода, вульвы, влагалища, полового члена и ротоглотки, — заболеваний, которые можно предотвратить с помощью тех же методов первичной профилактики, что и рак шейки матки.
Некоторые не онкогенные вирусы папилломы человека, особенно ВПЧ 6-го и 11-го типов, могут приводить к образованию остроконечных кондилом и развитию респираторного папилломатоза (заболевания, при котором опухоли образуются в дыхательных путях, ведущих от носа и полости рта в легкие). Хотя эти патологические состояния очень редко приводят к смерти, распространенность заболевания может быть значительной. Остроконечные кондиломы очень широко распространены, отличаются высокой контагиозностью и отрицательно влияют на половую жизнь.
Каким образом инфекция ВПЧ приводит к развитию рака шейки матки
Несмотря на то, что большинство ВПЧ-инфекций исчезают сами по себе, а предраковые поражения в большинстве случаев самопроизвольно излечиваются, все женщины подвержены риску перехода инфекции в хроническую форму и прогрессирования предраковых поражений в инвазивный рак шейки матки.
У женщин с нормальным иммунитетом рак шейки матки может развиваться в течение 15-20 лет. Однако при нарушениях иммунной системы, например у женщин с нелеченой ВИЧ-инфекцией, этот процесс может занять всего 5–10 лет.
Факторы риска хронической ВПЧ-инфекции и рака шейки матки
- степень онкогенности ВПЧ (способности вируса вызывать рак);
- нарушения иммунитета: люди с ослабленным иммунитетом, в частности, лица, живущие с ВИЧ, подвержены более высокому риску хронической ВПЧ-инфекции и ускоренного развития предраковых поражений и рака;
- наличие сопутствующих инфекций, передающихся половым путем, таких как генитальный герпес, хламидиоз и гонорея;
- количество родов в анамнезе и роды в раннем возрасте;
- курение табака.
Бремя рака шейки матки в мире
Рак шейки матки — четвертый в мире по распространенности вид рака у женщин. Так, в 2018 г. было зарегистрировано около 570 000 новых случаев этого заболевания. Оно является причиной 7,5% всех случаев смерти от онкологических заболеваний среди женщин. Ежегодно от рака шейки матки умирает более 311 000 женщин, причем более 85% этих случаев приходится на развивающиеся страны.
В развитых странах реализуются программы по вакцинации девочек против ВПЧ и ведется регулярный скрининг женщин на ВПЧ-инфекцию. Скрининг позволяет выявлять предраковые поражения на стадиях, на которых они легко поддаются лечению. В этих странах раннее начало лечения позволяет предотвратить развитие рака шейки матки почти в 80% случаев.
В развивающихся странах из-за ограниченного доступа к профилактике рак шейки матки часто остается не выявленным до поздних стадий заболевания и появления клинических симптомов. Кроме того, в этих странах может быть крайне ограничен доступ к лечению поздних стадий рака (например, доступ к онкохирургии, лучевой и химиотерапии), в связи с чем смертность от рака шейки матки там намного выше.
Проведение эффективных лечебно-профилактических мероприятий могло бы позволить снизить высокий показатель смертности от этого заболевания в мире (стандартизированный по возрасту коэффициент смертности в 2018 г.: 6,9 на 100 000).
Комплексный подход к борьбе с раком шейки матки
ВОЗ рекомендует комплексный подход к профилактике и лечению рака шейки матки. В рекомендуемый набор действий входят мероприятия, относящиеся ко всем этапам жизненного цикла. В эту многопрофильную программу должны входить такие компоненты, как просветительская работа в сообществах, мобилизация социальных ресурсов, вакцинация, скрининг, лечение и паллиативная помощь.
Первичная профилактика начинается с вакцинации девочек в возрасте 9–14 лет до начала половой жизни.
В перечень других рекомендуемых профилактических мероприятий для девочек или мальчиков, в зависимости от ситуации, входят:
- информирование о практиках безопасного секса, в том числе о нежелательности раннего начала половой жизни;
- пропаганда использования презервативов и предоставление их тем, кто уже начал половую жизнь;
- предупреждение о вреде употребления табака, к которому многие приобщаются в подростковом возрасте и которое является серьезным фактором риска развития рака шейки матки и других онкологических заболеваний;
- мужское обрезание.
Начиная с 30 лет все женщины, ведущие активную половую жизнь, должны проходить скрининг на атипичные клетки шейки матки и наличие предраковых поражений.
Если для лечения предраковых поражений шейки матки необходимо иссечение участков с атипичными клетками или измененными тканями, рекомендуется применять метод криотерапии, основанный на разрушении патологических тканей путем их замораживания.
При обнаружении признаков рака шейки матки необходимо начинать лечение, вариантами которого могут быть хирургическое вмешательство, лучевая терапия и химиотерапия.
Вакцинация против ВПЧ
В настоящее время существуют три вакцины, которые защищают одновременно от ВПЧ 16-го и 18-го типов, вызывающих не менее 70% случаев рака шейки матки. Одна из этих вакцин обеспечивает дополнительную защиту от трех других онкогенных ВПЧ, ответственных еще за 20% случаев этого заболевания. С учетом того, что вакцины только от ВПЧ 16-го и 18-го типов, обеспечивают также определенный уровень перекрестной защиты от других менее распространенных онкогенных типов ВПЧ, ВОЗ считает, что эти три вакцины являются равноценными средствами профилактики рака шейки матки. Две из этих вакцин защищают также от ВПЧ 6-го и 11-го типов, вызывающих аногенитальные остроконечные кондиломы.
Клинические и пострегистрационные исследования показывают, что вакцины против ВПЧ отличаются высокой безопасностью и высокой эффективностью в предотвращении ВПЧ-инфекций.
Вакцины против ВПЧ дают максимальный эффект, если их вводят до контакта организма с этими вирусами. В связи с этим ВОЗ рекомендует вакцинировать девочек в возрасте от 9 до 14 лет, когда большинство из них еще не начали вести половую жизнь.
Вакцины не лечат ВПЧ-инфекцию и связанные с ВПЧ заболевания, в частности, рак.
В некоторых странах начали вакцинировать и мальчиков, так как вакцинация предотвращает развитие рака половых органов не только у женщин, но и у мужчин, а две из существующих вакцин способны также препятствовать развитию остроконечных кондилом у представителей обоих полов. Рекомендуемая ВОЗ вакцинация девочек в возрасте от 9 до 14 лет представляет собой наиболее эффективное с точки зрения затрат медицинское мероприятие по борьбе с раком шейки матки.
Вакцинация против ВПЧ не отменяет необходимости скрининга на рак шейки матки. В странах, где вакцинация против ВПЧ внедрена в медицинскую практику, может сохраняться необходимость в разработке или усилении программ по скринингу.
Выявление и лечение предраковых поражений
Скрининг на рак шейки матки предусматривает проверку на наличие предраковых и раковых образований у женщин, которые зачастую могут чувствовать себя совершенно здоровыми и у не иметь никаких симптомов заболевания. Если при скрининге обнаруживаются предраковые поражения, их лечение не представляет трудностей и позволяет избежать развития рака. Кроме того, скрининг позволяет обнаруживать рак на ранней стадии, когда высока вероятность полного излечения.
Поскольку предраковые поражения развиваются на протяжении многих лет, скрининг рекомендуется регулярно проходить всем женщинам, начиная с возраста 30 лет (периодичность скрининга зависит от используемого для этого метода). Регулярный скрининг у женщин с ВИЧ-инфекцией, ведущих активную половую жизнь, должен начинаться раньше — с момента, когда они узнают о своем ВИЧ-статусе.
При проведении скрининга необходимо обеспечить возможность последующего лечения и предусмотреть необходимые действия в случае получения положительных результатов теста. Без надлежащей организации таких мероприятий проведение скрининга неэтично.
Существуют три различных типа скрининговых тестов, рекомендуемых ВОЗ в настоящее время:
- тесты на ВПЧ, относящиеся к группе высокого риска;
- визуальная проверка с применением уксусной кислоты;
- традиционный ПАП-тест и метод жидкостной цитологии (ЖЦ).
Для лечения предраковых поражений ВОЗ рекомендует применять методы криотерапии и электрохирургической петлевой эксцизии. При обнаружении более глубоких поражений следует направлять пациенток на дополнительные обследования для принятия обоснованных решений о дальнейших действиях.
Лечение инвазивного рака шейки матки
При наличии у женщины симптомов, позволяющих заподозрить рак шейки матки, ее необходимо направить в специализированное лечебное учреждение для проведения дополнительных исследований, постановки диагноза и лечения.
На ранних стадиях рака шейки матки могут появляться следующие симптомы:
- нерегулярные мажущие кровянистые выделения или слабое кровотечение в период между месячными у женщин детородного возраста;
- мажущие выделения или кровотечение у женщин в постменопаузе;
- кровотечение после полового акта;
- более обильные выделения из влагалища, иногда с неприятным запахом.
По мере прогрессирования рака могут появляться более тяжелые симптомы, в том числе:
- постоянная боль в спине, ногах и (или) в области таза;
- потеря веса, утомляемость, снижение аппетита;
- неприятно пахнущие выделения и дискомфорт во влагалище;
- отек одной или обеих нижних конечностей.
При далеко зашедших формах рака могут развиться и другие тяжелые симптомы, в зависимости от того, на какие органы распространился рак.
Диагноз рака шейки матки должен быть подтвержден результатами гистологического исследования. Стадию заболевания устанавливают на основании размеров опухоли и распространения процесса на область таза и отдаленные органы. Выбор метода лечения зависит от стадии рака, при этом в перечень возможных вариантов входят хирургическая операция, лучевая терапия и химиотерапия. Кроме того, важную роль в ведении пациентов с онкологическими заболеваниями играет паллиативная помощь, позволяющая облегчать боль и страдания, причиняемые болезнью.
Действия ВОЗ
ВОЗ разработала руководство по профилактике рака шейки матки и борьбе с этим заболеванием путем вакцинации, скрининга и лечения инвазивной формы рака. Совместно со странами и партнерами ВОЗ занимается разработкой и осуществлением комплексных программ.
В мае 2018 г. Генеральный директор ВОЗ выступил с призывом к действиям, направленным на ликвидацию рака шейки матки, и предложил странам и партнерам объединить усилия для расширения доступа к мерам профилактики рака шейки матки и увеличения охвата населения. В качестве трех основных мер были названы вакцинация против ВПЧ, скрининг и лечение предраковых поражений, а также ведение пациенток с раком шейки матки.
Читайте также:


