Лучевая терапия при папилломе
Андрей Каприн рассказал, какие виды рака сейчас наиболее опасные, перспективах лечения и ожидаемом уменьшении смертности

Москва. 14 сентября. INTERFAX.RU - Главный внештатный специалист-онколог Минздрава, генеральный директор НМИЦ радиологии Минздрава России, Андрей Каприн рассказал "Интерфаксу" о том, какие виды рака сейчас наиболее опасные, перспективах лечения и ожидаемом уменьшении смертности в результате злокачественных новообразований.
- Андрей Дмитриевич, какие сейчас наиболее опасные виды рака? Как они реагируют на лечение?
- На первом месте по заболеваемости все те же "лидеры": у женщин - рак молочной железы, рак шейки матки. У мужчин - рак легких, желудка и предстательной железы. В пятерку входит также рак кожи, тут нет разницы по половому признаку. Особенно агрессивной была и остается меланома - она поражает практически все возрастные группы, вероятность метастазирования крайне велика, хотя наука нашла эффективные способы ее лечения. В последнее время появилось очень много интересных препаратов и методов лечения, но главное оружие пациентов и врачей - ранняя диагностика. Чем раньше мы диагностируем опухоль, тем больше шансов ее победить.
В лечении некоторых локализаций достигнуты серьезные успехи: при раннем выявлении рака молочной железы процент излечения, например, составляет 95-97%. Хорошие результаты дает лечение методом внутритканевой брахитерапии предстательной и молочной желез, который НМИЦ радиологии Минздрава России ввел в регулярную практику. С другой стороны, очень опасным остается рак поджелудочной железы, который вносит большую долю в статистку смертности, имеет плохой прогноз. Но все-таки удается замедлить развитие этого заболевания, продлить жизнь пациентов на несколько месяцев. Недавно мы провели ряд успешных операций на поджелудочной железе с применением брахитерапии с очень хорошим результатом. Будем продолжать идти в этом направлении, сейчас метод проходит стадию клинических исследований.
- Что влияет на возникновение рака? Некоторые исследователи утверждают, что виной всему ухудшение экологии.
Безусловно, заболеваемость злокачественными новообразованиями растет и в связи со старением населения к этому нужно быть всем готовыми, и предпринимать все меры для усиления онкологической службы, ведь пул наблюдаемых пациентов растет. Сейчас в стране зарегистрировано 3 млн 700 тысяч человек, страдающих онкологическими заболеваниями.
Думаю, борьба с курением и чрезмерным потреблением алкоголя, и, как следствие, уменьшение потребления алкоголя и табака, увеличение количества людей, ведущих здоровый образ жизни, принесет серьёзные положительные результаты.
- Несколько недель назад был опубликован прогноз по экономическим потерям от рака в России, что сейчас он составляет 8 млрд долларов, а к 2030 году снизится до 7,5. Вы согласны с этим прогнозом? У нас же выявление растет, хотя качество лечения и повышается, но все-таки и смертность, мне кажется, пока увеличивается.
- Это вопрос очень сложный. Я не экономист и не могу оценивать эти данные. Но могу сказать, что сейчас растет показатель выявляемости, людей обследуют больше, чаще. Когда выявляется III-IV стадия рака, к сожалению, велик процент потерь таких пациентов, если среди них люди трудоспособного возраста – то это, безусловно, экономические потери. Но стоит отметить, что растет количество пациентов I и II стадии, которым можно назначить эффективное лечение, перевести в группу длительно наблюдаемых больных, существенно продлить жизнь и улучшить ее качество.
Также не стоит забывать и про экономические потери от инвалидизации граждан трудоспособного возраста в результате перенесенного лечения – хирургического или комбинированного, включающего в себя и химиотерапию и лучевую терапию. То есть в результате раннего выявления рака этих последствий тоже, возможно, удастся избежать.
Россия приближается к такому кресту между кривыми заболеваемости и смертности, который развитые страны прошли лет 30 назад. Это означает, что наступает переломный момент, когда свою эффективность покажут скрининги, дающие возможность выявлять заболевание на ранней стадии. Соответственно, тех, кого в свое время "пропустили", не выявили рак вовремя, станет меньше, начнут чаще выявлять рак на ранних стадиях, а это приведет к увеличению благоприятных исходов лечения и, как следствие, уменьшению экономических потерь.
- Сколько человек сейчас умирает от рака?
- Три года назад в течение первого года после выявления умирало 27%. Сейчас удалось снизить показатель до 22%.
- Так насколько удастся снизить этот показатель в результате выявления на начальных стадиях?
- По оценкам наших специалистов мы должны к 2024 году выйти на показатель смертности 185 случаев на 100 тысяч населения. Сейчас он составляет 199,6. Этот индикатор заложен в государственной программе по борьбе с онкологическими заболеваниями. И вырастет выявление ранних стадиях рака до 64% -70%. Сейчас этот показатель составляет 57%.
- А что дальше, какие вы видите перспективы этих усилий?
- Я думаю, что несмотря на рост заболеваемости от злокачественных новообразований, который прогнозирует Всемирная организация здравоохранения, эти тенденции нам удастся удержать. Хотя трудно заглянуть в будущее, тем не менее совокупный эффект и от новых методов диагностики и лечения, и от пропаганды здорового образа жизни должен дать свои результаты. Во всяком случае, мы уже добились того, что называем мультидисциплинарный подход к решению проблемы заболеваемости раком. Общество осознало, что это задача не только одних онкологов. Не случайно на наших профессиональных форумах собираются люди очень многих специальностей – врачи, организаторы здравоохранения, физики, математики, химики, чтобы вместе решать, каким быть будущему борьбы против онкологических заболеваний. В конце сентября в ЦМТ пройдет Второй форум онкологии и радиологии.
- Хватает ли лекарств сейчас, довольны ли вы их качеством?
- На сегодняшний день благодаря поддержке Министерства здравоохранения почти в два раза увеличился объем финансирования регионов на закупку современных препаратов. Наша задача, как референсных национальных центров, – оказать методическую помощь в обучении и переподготовке врачей в местных больницах и онкодиспансерах, в первую очередь в том, как провести своевременную и правильную диагностику, как грамотно выстроить маршрутизацию обследований и схему лечения, как правильно применять все самые современные схемы комбинированного лечения. В настоящее время идет разработка рекомендаций для врачей общей практики, которые направлены на повышение общей онконастороженности докторов первичного звена, учат, как распознать первые признаки онкологического заболевания и направить пациента в специализированное учреждение. Для специалистов – онкологов профессиональным сообществом под эгидой Ассоциации онкологов России разрабатываются клинические рекомендации по диагностике и лечению злокачественных новоообразований, которые необходимо неукоснительно выполнять. Это давняя зарубежная практика, которую нам стоит принять на вооружение.
- Что за лекарства у нас используются, зарубежные, российские, какие в основном?
Выбор терапии зависит от многих факторов – стадии заболевания, генетических особенностей и прочее. Государством гарантированы необходимые для лечения лекарства, зарубежные заказываются в основном по индивидуальной программе по необходимости. Многим зарубежным препаратам уже есть аналоги российского производства, которые не хуже. Есть, конечно, препараты, которые мы закупаем за границей, например, некоторые таргетные препараты, которые не производятся, но уже разрабатываются в России. Принят нормативно-правовой акт, в соответствии с которым при участии в торгах двух и более российских производителей, участие иностранных затрудняется. Несмотря на возникшие вначале опасения, впоследствии это простимулировало иностранцев локализовать производства лекарств в России, на которых будет написано "Сделано в России, по лицензии такой-то компании". Отмечу, это не только российская практика, так делали многие государства при отсутствии своей достаточной базы. Очень надеюсь, что Россия вернет свои былые позиции, особенно в производстве радиофармпрепаратов, ведь все у нас для этого есть.
- А незарегистрированные препараты вы заказываете из-за рубежа?
- Незарегистрированные препараты у нас идут только в рамках клинических испытаний. В нашем центре одновременно проходят испытания до 75 препаратов ежегодно.
- Значит, нехватку лекарств не ощущаете?
- Как я уже сказал, лекарств достаточно - и российских, и зарубежных, и даже незарегистрированные тестируются в большом объеме.
- А вы ведете здоровый образ жизни?
- Я много езжу по стране, из-за этого не могу сказать, что правильно питаюсь, но стараюсь не есть вредные продукты, много ходить. Самое главное, что я делаю, это регулярно прохожу диспансеризацию и, в ее рамках, скрининги в соответствии с возрастом. Я сдаю все анализы, которые необходимы, и того же требую от своих коллег.

Почему так происходит и что мешает обнаружить недуг вовремя и вылечить пациента? Ждут ли онкологи новых случаев после сезона простуд и чем поможет прививка от ВПЧ? Об этом и многом другом мы беседуем с заведующим специализированным отделением Челябинского областного клинического центра онкологии и ядерной медицины, к.м.н. Александром Гузем.
— Почему?
— Загадка! Каждый день мы смотрим сами на себя в зеркало, другие люди на нас смотрят, и мы на них. Во рту расположено огромное количество болевых рецепторов, благодаря которым действуют все органы чувств. Поэтому любой дискомфорт в этой области мы должны замечать очень быстро, но почему-то это не так и в России, и в Америке, и в Европе. Локализация может успешно лечиться при начальных стадиях заболевания, врачу нужно чаще замечать какие-либо изменения, а пациенту — чаще обращаться к врачу.
— На что обратить внимание самому пациенту?
— Рак развивается на фоне хронических воспалительных заболеваний, в том числе кариеса, пародонтита, гайморита, либо из-за неправильно подогнанных зубных протезов. Все начинается с гигиены. Те, кто в конце концов попал к онкологам, о состоянии полости рта, как правило, не заботились совсем. Порой достаточно сменить зубную пасту, щетку, чтобы чистка зубов стала тщательней и воспалительный процесс ушел. Сейчас в сезон простуд и гриппа нужно пролечивать насморк, а не ждать, когда он сам пройдет.

— Тогда возникает закономерный вопрос: есть какие-то особенные симптомы?
— Один из действенных способов предупреждения раковых заболеваний — это своевременное выявление и лечение фоновых, или предраковых, заболеваний, которые могут привести к развитию рака. Например, лейкоплакия — заболевание, которое развивается на слизистых оболочках и характеризуется образованием белых разрастаний на их поверхностях. Она может возникать на фоне хронического травмирования: прикусил щеку, поранил десну щеткой при чистке зубов и т.д. Но рак не развивается в течение дня, это длительный процесс. Трансформация клеток из нормальных в злокачественные происходит постепенно. За это время — месяцы и годы — предрак можно обнаружить и пролечить. К сожалению, лейкоплакию мало кто лечит, потому что это дело долгое и неблагодарное. Лечению она поддается плохо, но делать это нужно.
— Насколько фатально пропустить начальную стадию? Чем это грозит?
— С одной стороны, пациентов немного, с другой — риск фатального исхода очень велик. Самая трагическая ситуация складывается при раке ротоглотки (все, что находится за языком: миндалины, задняя поверхность глотки и т.д.). Сразу 3-4-я стадия встречается в 80 % случаев, и в 40 % они заканчиваются летальным исходом. При раке гортани на 1-2-ю стадию приходится более 50 % всех случаев, но каждый четвертый заболевший попадет под одногодичную летальность. Рак полости рта на поздних стадиях диагностируется у 60 % пациентов, и каждый третий погибает.
— Что поможет снизить риски?
— Причины возникновения банальны: курение, алкоголь и ВПЧ-инфекция. Алкоголь выступает катализатором при курении, увеличивая риски возникновения рака в несколько раз. В современном западном мире среди причин возникновения рака на первый план выходит ВПЧ — до 80 % всех новых случаев. Глобальная защита от ВПЧ не медицинская: это образ жизни и поведения, половое воспитание. Механизм передачи понятен: из половых путей вирус попадает в рот. Чем чаще человек встречается с ВПЧ-инфекцией, чем больше контактов и половых партнеров, тем выше риск, что вирус вызовет развитие рака. Организм человека может сам иллюминировать эти вирусы, специфического лечения нет, но чем выше вирусная нагрузка, тем выше вероятность, что вирус прорвется через оборону, интегрируется в ДНК клетки и начнутся мутации клеток, что и станет причиной развития рака.
Она носит скорее этический характер, чем технический. В лечении онкологических заболеваний, как правило, хирургический метод основной, но что-то удалить на голове и шее без последствий невозможно. Технологии в хирургии позволяют сделать очень многое, но должна быть в этом целесообразность. Может быть, гуманнее и эффективнее назначить химиотерапию. Пусть она не излечит, зато всю оставшуюся жизнь пациент проведет на более значимом уровне ее качества. Мы прекрасно понимаем, что человек смертен. Поэтому вопрос не в том, что можно сделать, а в том, как вовремя остановиться, принять правильное решение в интересах пациента.

— Мне казалось, что в лечении онкологических заболеваний всегда присутствует триада методов в их сочетании. Кроме операции что помогает?
— При разных локализациях и стадиях — разные подходы к лечению. При раке гортани, слизистой оболочки полости рта, шеи, кожи, придаточных пазух носа — преимущественное хирургическое. При распространенных стадиях возможно использование лучевой терапии в сочетании с химиотерапией. Второй по важности метод — лучевая терапия. Самостоятельно применяется при раке носоглотки, ротоглотки, придаточных пазух носа, когда невозможно подобраться к опухоли хирургическим путем либо лечение вызовет худший функциональный результат.
Химиотерапия в самостоятельном варианте не применяется для наших пациентов, поскольку не позволяет излечить опухоль полностью. Метод позволяет бороться с метастазами или с рецидивами, добавляет эффективности для лучевой терапии.
Лечение пациентов с опухолями головы и шеи должно в обязательном порядке проходить в условиях крупного многофункционального онкологического центра, каким мы и являемся, потому что только тогда есть нужные специалисты, есть возможность использовать все три метода, сочетать их и управлять результатом лечения — отслеживать эффективность, менять тактику, последовательность, дозировку и так далее. На распространенных стадиях успех лечения зависит именно от возможности комбинировать разные методы индивидуально для каждого пациента.
Но пациент должен знать о возможных вариантах лечения и их исходах, трудностях, чтобы быть к этому готовым, оценивать трезво риски и свои возможности. Процесс принятия решений сложный и длительный, но важный. Решить судьбу человека — вот что самое сложное.
— Хорошо, но ведь сколько людей — столько и мнений. Как выбрать оптимальный вариант? Как договориться и не навредить?
— В нашем онкоцентре консилиум, или мультидисциплинарная команда, как это называется в мире, обсуждает каждый клинический случай. Это то, что пациенту не видно, но без чего невозможно назначить адекватное лечение. Выбор тактики лечения и риск ошибки минимизируется. Такой подход дает возможность найти пространство для маневра, когда стандартные методики испробованы, а полученный результат не устраивает.
На что обратить внимание:
- односторонняя боль в горле
- незаживающие язвы или белые пятна в горле
- болезненность языка
- постоянная или нарастающая осиплость голоса
- заложенность носа или повторяющиеся кровянистые выделения
- опухоль в области головы и шеи
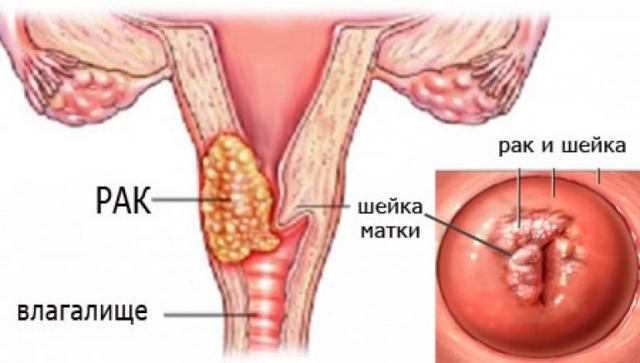
Рак шейки матки является одним из наиболее часто встречаемых злокачественных новообразований у женщин. Он возникает из плоского многослойного эпителия, покрывающего шейку матки. По типу опухоли рак шейки матки делится на:
- плоскоклеточный рак (70-80 % случаев);
- аденокарциному (10-20 % случаев);
- низкодифференцированный рак (примерно 10% случаев).
Факторы риска возникновения рака шейки матки:
- Вирус папилломы человека
- Раннее начало половой жизни (до 16 лет)
- Ранние роды
- Частая смена половых партнеров
- Курение
- Аборты
- Воспалительные заболевания половых органов
- Длительный прием гормональных контрацептивов
- Нарушение иммунитета
- Возраст от 40 до 50 лет (однако, рак шейки матки в мире молодеет и встречается у женщин в возрасте от 25 до 29 лет).
В настоящее время доказана прямая связь между раком шейки матки и вирусом папилломы человека (ВПЧ). Он выявляется более чем у 95% больных. ВПЧ типов 16, 18, 31, 33, 35 или 39, вызывают рак шейки матки. Передается ВПЧ преимущественно половым путем.
Профилактика:
- Предупреждение ранней половой жизни
- Отказ от курения
- Использование презервативов
- Исключение частой смены половых партнеров
- Вакцинация от ВПЧ (желательный возраст 10 – 25 лет, до начала половой жизни)
- Регулярные медосмотры у гинеколога с забором мазка на цитологию, а также кольпоскопия для выявления предраковых заболеваний шейки матки и ранних стадий рака шейки матки, которые могут быть полностью излечены.
Симптомы рака шейки матки. Что должно Вас насторожить?
Ранние стадии рака шейки матки протекают без проявления каких-либо симптомов, но если вы наблюдаете следующие изменения, необходимо обратиться к врачу:
- Выделения из влагалища беловатые с примесью крови
- Кровеносные выделения после полового акта или подъема тяжестей, возможно с неприятным запахом
- Кровотечение между менструациями
- Боли в нижней части живота, области крестца, поясницы
- Нарушение мочеиспускания, дефекации, боли в ногах, отек ног (при прогрессировании опухоли).
Каждый из вышеописанных симптомов может быть вызван другой причиной. Но для исключения возможности возникновения рака шейки матки, нужно пройти обследование у гинеколога.
Диагностика
Диагностика начинается с визита к гинекологу, который проведет осмотр шейки матки на предмет наличия изменений, возьмет мазок на цитологическое исследование (тест Папаниколау) и проведет кольпоскопию с помощью специального оптического прибора (кольпоскопа), увеличивающего в разы исследуемую область, для выявления видимых патологических очагов. При этом может браться небольшой кусочек ткани – биопсия – для гистологического анализа.
В случае подтверждения рака – проведение дополнительных исследований (КТ, МРТ, УЗИ органов малого таза) для определения стадии опухолевого процесса, т.е. уточнение размеров, локализации и распространенности заболевания.
Лечение
Что влияет на выбор типа лечения, подходящий именно ВАМ?
- Стадия опухолевого процесса.
- Наличие или отсутствие других заболеваний. Будьте честны с доктором. Некоторые заболевания являются противопоказанием для проведения того или иного вида лечения.
- Ваш возраст.
- Риск осложнений от того или иного вида лечения.
Хирургический метод лечения
Как правило, хирургическое лечение применяется на ранних стадиях заболевания, когда процесс максимально локализован и не требует дополнительной терапии. Но, в случае наличия сопутствующих заболеваний, являющихся противопоказанием к операции, очень успешно используют лучевую терапию.
Во время операции может быть удалена часть шейки матки вместе с опухолью, а при более распространенных заболеваниях целиком шейка матки и сама матка.
Лучевая терапия
При лечении рака шейки матки используется два вида лучевой терапии: дистанционная и внутриполостная. Часто эти два вида терапии применяются в сочетании. В этом случае, дистанционная лучевая терапия направлена на область тазовых лимфатических узлов, а внутриполостная – а первичный опухолевый очаг.
В 75% случаев рака шейки матки лучевая терапия является основным или единственным методом лечения.
Стандартом дистанционной радиотерапии является конформная лучевая терапия, которая подразумевает облучение опухоли в пределах ее границ. Перед лечением пациент проходит топометрическую подготовку, в ходе которой с помощью КТ, МРТ или ПЭТ определяют конфигурацию и точную локализацию новообразования, вовлечение соседних анатомических структур, метастазирование в лимфатические узлы.
Дистанционно облучают не только первичную опухоль, если она не была удалена хирургически, но и окружающие ее ткани — параметрий, крестцово-маточные связки региональные лимфатические узлы.
Внутриполостное облучение, или брахитерапия рекомендована как обязательный этап лечения. Суть метода заключается в имплантации радиоактивного препарата непосредственно в ткани, например, в культю влагалища. При этом локальный объем облучения, который обеспечивается одной процедурой, практически эквивалентен общей дозе, полученной при дистанционной терапии.
Современные аппараты лучевой терапии позволяют облучить пораженную зону, не затрагивая близ расположенные здоровые органы и ткани. Это дает возможность избежать поздних лучевых реакций и сохранить качество жизни после перенесенного лечения. Во время облучения происходит постепенное воздействие на пораженную область определенной дозы радиации, в результате чего раковые клетки гибнут.
Одним из таких современных аппаратов является аппарат томотерапии TomoTherapy серии TomoHD, который благодаря своим конструктивным особенностям и заложенным в него физическим характеристикам позволяет максимально конформно подвести лечебную дозу радиации и минимизировать лучевое воздействие на мочевой пузырь, прямую кишку, яичники, сохраняя их функции. Отсутствие лучевых повреждений ведет к лучшей переносимости лечения, быстрому восстановлению организма и сохранению качества жизни.
Стоимость лечения рака шейки матки
| Наименование услуги | Цена, руб. | Ед. измерения |
|---|---|---|
| Консультация врача онколога радиотерапевта | 0 | шт. |
| Консультация врача детского онколога | 0 | шт. |
| Повторная консультация специалистов | 500 | шт. |
| Топометрия на специализированном компьютерном томографе первичная | 15 000 | процедура |
| Топометрия на специализированном компьютерном томографе повторная | 7 000 | процедура |
| Дозиметрическое планирование лучевой терапии (томотерапии) первичное | 20 000 | шт. |
| Дозиметрическое планирование лучевой терапии (томотерапии) повторное | 7 000 | шт. |
| Лучевая терапия (томотерапия), включая IMGRT (*) | 223 000 | курс |
| Лучевая терапия (томотерапия) стереотаксическая радиохирургия(*) | 250 000 | курс |
| Лекарственная сопроводительная терапия: внутривенные введение в процедурном кабинете (без учета стоимости лекарственных препаратов) | 1 000 | процедура |
| Лекарственная сопроводительная терапия: внутримышечное введение в процедурном кабинете (без учета стоимости лекарственных препаратов) | 200 | процедура |
| Топометрическая разметка | 750 | процедура |
Вид лучевой терапии и количество сеансов курса определяется врачебной комиссией индивидуально для каждого пациента исходя из локализации, нозологии опухоли и с учетом анамнеза.
Химиотерапия
Химиотерапия для лечения рака шейки матки, как правило, применяется при распространенных метастатических процессах. Чаще она используется в сочетании с лучевой терапией для усиления радиочувствительности опухоли.


Автореферат диссертации по медицине на тему Метод комбинированного видеоэндоларингеального лечения больных ранним раком и папилломатозом гортани
_ .цллвах рукописи
Гладышсв Александр Александрович
МЕТОД КОМБИНИРОВАННОГО ВИДЕОЭНДОЛАРИНГЕАЛЬНОГО ЛЕЧЕНИЯ БОЛЬНЫХ РАННИМ РАКОМ И ПАПИЛЛОМАТОЗОМ
АВТОРЕФЕРАТ диссертации на соискание ученой степени кандидата медицинских наук
доктор медицинских наук, профессор СОКОЛОВ Виктор Викторович Научный консультант:
чл.-корр. РАМН, профессор РЕШЕТОВ Игорь Владимирович Официальные оппоненты:
Учреждение Российской академии медицинских наук Российский онкологический научный центр имени Н.Н.Блохина РАМН.
Защита диссертации состоится 21 декабря 2010 года в_ часов на
Ученый секретарь диссертационного совета
доктор биологических наук Завалишина Лариса Эдуардовна.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ.
Актуальность проблемы: рак гортани (РГ) среди злокачественных опухолей верхних дыхательных путей занимает 1-е место и составляет 65 -70 %. В России в 2007 году показатель заболеваемости РГ у мужчин составил 7,35 на 100 тыс. населения, при этом в возрастной группе 30 - 59 лет вышел на 5-ое место. Лишь у 20 - 35 % больных РГ диагностируется в 1-Н стадии заболевания, когда возможно применение органосохраняющего лечения [А.И. Пачес, 1997; В.О. Ольшанский и соавт., 2004; В.И. Чиссов, В.В. Старинский и соавт., 2009].
В возникновении РГ важную роль играют предраковые заболевания, к которым в первую очередь относят дискератоз и папилломатоз гортани. Частота малигнизации рецидивирующей папилломы колеблется от 8 до 28 %, дискератоза - от 7 до 40 % [В.П. Барсук и соавт., 1989; А.И. Пачес, 2000; Б. ЗсЬгаГ!' е1 а1., 2004]. Своевременное выявление и радикальное лечение предраковых заболеваний являются эффективными методами профилактики развития РГ.
В настоящее время к наиболее распространенным методам лечения РГ 1-Н стадии относятся лучевая терапия (ЛТ), хирургическая операция или комбинированное лечение. Опыт отечественных и зарубежных авторов свидетельствует, что при начальных стадиях рака среднего отдела гортани эффективность лучевого и хирургического способов практически равна, пятилетняя выживаемость достигает 80 - 95 %, частота рецидива колеблется от 6 до 18 % [А.С. Лопатин и соавт., 2005; Р. М. Рзаев, 2006; В.С. Ушаков и соавт., 2003; Ь.Р. Вгоп, й а1., 2001]. Однако среди этой группы больных имеется определенный процент пациентов (до 30 %) преклонного возраста, которым не может быть выполнено традиционное лечение в связи с тяжестью сопутствующей патологии. Дискутабельным остается вопрос о применении ЛТ при раннем РГ у лиц молодого возраста [М. KrengIi, 2004; К. Атепиуа, 2005].
После лучевого или хирургического лечения РГ не редко развиваются побочные реакции и осложнения. Так, после лучевой терапии (СОД = 60-70 Гр.) неизбежны побочные реакции (эпителиит, эпидермит, отек) со стороны гортани и окружающих органов у 83 - 87 % больных, поздние отеки слизистой оболочки, хопдро-перихондрит, фиброз гортани наблюдаются у 7,5 - 35 % пациентов [В.Г. Андреев и соавт., 1998; А.И. Пачес, 2000]. Наиболее частыми осложнениями после органосохраняющих операций при РГ являются: рост грануляций по линии резекции с сужением просвета гортани (14 %); рубцовая деформация (10 %); стеноз гортани с затруднением дыхания (4 %). Нарушение голосовой функции наблюдается у 25 - 37 % оперированных больных [А.И. Пачес, 2000; Б.К. Поддубный и соавт., 2006]. При выполнении хирургических операций по поводу остаточной опухоли или рецидива РГ после радикальной ЛТ частота послеоперационных осложнений увеличивается. От 10 до 25 % больных после операции с наложением трахеостомы остаются хроническими канюленосителями, чт 0,05). Методика комбинации КскУАО-лазера, АПК с последующей ФДТ, проводимой на втором этапе лечения у больных с большей площадью поражения и остаточной опухолью после первого эндохирургического этапа, позволила добиться полной регрессии в 13 (87 %) из 15 наблюдений. Различия всех четырех применяемых методик по результатам лечения оказались статистически не достоверными (р>0,05), т.е. при правильно определенных показаниях эффективность разработанного метода эндоскопического лечения одинаково высока.
После окончания первого курса лечения полного удаления папиллом удалось достичь у 22 (76 %) из 29 больных при сочетанном использовании Ш:УАО-лазера и АПК с последующей ФДТ. Применение Х Гладышев, Александр Александрович :: 2010 :: Москва
Глава 1. Современные методы диагностики и лечения предрака и раннего рака гортани (обзор литературы). 9.
1.1. Этиопатогенез предрака и рака гортани. 9.
1.2. Диагностика предрака и рака гортани. 13.
1.3. Методы лечения предрака и рака гортани. 18.
1.3.1. Лечение дискератоза и папилломатоза гортани. 18.
1.3.2. Лечение рака гортани. 22.
Глава 2. Клинический материал и методы лечения. 34.
2.1 Общие сведения о больных. 34.
2.2. Методы диагностики и лечения больных предраком и раком гортани. 50.
2.2.1. Методики видеоларингоскопии и флуоресцентной диагностики предрака и рака гортани. 51.
2.2.2. Методики эндоларингеальной хирургии и терапии с использованием гибкой эндоскопической техники. 53.
2.2.2.1. Ш: У А С-лазерная термо абляция. 54.
2.2.2.2. Аргоноплазменная коагуляция. 56.
2.2.2.3. Петлевая электрорезекция. 57.
2.2.2.4. Фотодинамическая терапия. 59.
2.3. Подготовка к эндоскопическому лечению, методики анестезии, особенности ведения больных в послеоперационном периоде. 63.
2.4. Методы статистической обработки. 65.
Глава 3. Результаты комбинированного эндоларингеального лечения больных предраком и раком гортани с использованием гибкой видеоэндоскопической техники. 66.
3.1. Методы оценки эффективности лечения больных предраком и раком гортани. 66.
3.2. Показания к выбору методики эндоскопической хирургии и/или фотодинамической терапии больных предраком и раком гортани. 67.
3.3. Непосредственные результаты эндоларингеального лечения больных предраком и раком гортани. 68.
3.3.1. Результаты лечения больных дискератозом с дисплазией среднего отдела гортани. 74.
3.3.2. Результаты лечения больных ранним раком среднего отдела гортани. 76.
3.3.3. Результаты лечения больных резидуальным и рецидивным раком среднего отдела гортани. 82.
3.3.4. Результаты лечения больных рецидивирующим папилломатозом дыхательных путей. 90.
3.4. Ближайшие и отдаленные результаты лечения. 99.
3.5. Рецидив при предраке и раке гортани после эндоскопического 100. лечения.
3.6. Осложнения при эндоскопическом лечении предрака и рака 111. гортани.
Введение диссертации по теме "Онкология", Гладышев, Александр Александрович, автореферат
Рак гортани (РГ) среди злокачественных опухолей верхних дыхательных путей занимает 1-е место (65 - 70 %). В России в 2007 году показатель заболеваемости РГ у мужчин составил 7,35 на 100 тыс. населения, при этом в возрастной группе 30 - 59 лет вышел на 5-ое место. Лишь у 20 - 35 % больных РГ диагностируется в I - II стадии заболевания, когда возможно применение органосохраняющего лечения [29, 32, 68, 69].
Ранняя диагностика и радикальное лечение предраковых заболеваний верхних дыхательных путей являются эффективными методами профилактики РГ. Частота малигнизации таких облигатных форм предрака, как рецидивирующий папилломатоз и дискератоз гортани колеблется от 8 до 28 %, и от 7 до 40 %, соответственно. [4, 32, 125].
В настоящее время традиционными методами лечения РГ стадии 1-Н является лучевая терапия, хирургическая операция или комбинированное лечение. Эффективность лучевого и хирургического методов лечения практически равна: пятилетняя выживаемость, по данным отечественных и зарубежных авторов, достигает 95 %, частота рецидива колеблется от 6 до 18 % [22, 40, 61, 76]. Однако среди пациентов РГ стадии 1-Н до 30 % находятся в преклонном возрасте, имеют тяжелую сопутствующую патологию, которая не позволяет выполнить традиционное лечение.
После лучевого или хирургического лечения не редко развиваются побочные реакции и осложнения. Восстановление всех функций гортани отмечается не во всех наблюдениях. Так, после лучевой терапии (СОД = 60 -70 Гр.) неизбежны побочные реакции со стороны гортани и окружающих органов у 83 - 87 % больных, поздние отеки слизистой оболочки, хондро-перихондрит, фиброз гортани наблюдаются у 7,5 - 35 % пациентов [2, 32]. Наиболее частыми осложнениями после органосохраняющих операций при РГ являются: рост грануляций по линии резекции (14 %); рубцовая деформация (10 %); рубцовый стеноз гортани с нарушением дыхания (4 %). Нарушение голосовой функции наблюдается у 25 — 37 % оперированных больных [32, 38].
При выполнении хирургических операций по поводу остаточной опухоли или рецидива РГ после радикальной лучевой терапии частота послеоперационных осложнений увеличивается. От 10 до 25 % больных остаются хроническими канюленосителями, что значительно снижает качество жизни пациентов [38, 46, 57].
В течение последних двух десятилетий активно развиваются и внедряются в практику органосохраняющие и функционально-щадящие эндоларингеальные методы лечения больных предраком и РГ с использованием ригидных ларингоскопов, микрохирургических инструментов или различных типов лазера. После эндоларингеальных операций по поводу раннего РГ непосредственные и отдаленные результаты аналогичны таковым при открытых хирургических операциях: процент излечения варьирует от 84 до 91 %, 5-ти летняя выживаемость составляет 93 - 97 %, рецидивы выявляются у 5,6 - 21 % больных [76, 91, 108, 132, 136].
Ригидная эндоларингеальная хирургия в условиях общего обезболивания имеет ряд ограничений, к которым относятся тяжелая сопутствующая патология и особенности анатомического строения (остеохондроз шейного отдела позвоночника, короткая толстая шея, массивный корень языка и др.), затрудняющие введение операционного ларингоскопа.
В последние годы наметилась тенденция к применению различных новых способов эндоскопического лечения больных предраком и раком гортани, как с паллиативной так и радикальной целью. Однако в отечественной и зарубежной литературе представлены лишь единичные работы, посвященные использованию эндоларингеальных операций с использованием ЫсЬУАС-лазера или фотодинамической терапии (ФДТ), в качестве самостоятельных методов лечения при предраке или начальных формах рака гортани. Остается мало изученной проблема рационального выбора той или иной методики эндоскопического лечения и возможности их использования в комбинации друг с другом, а также после предшествующей лучевой терапией.
Таким образом, материалы мировой литературы указывают на целесообразность и перспективность дальнейшей разработки функционально-щадящих эндоскопических методов лечения больных предраком и раком гортани ввиду распространенности этих заболеваний у лиц молодого и трудоспособного возраста, а также у пожилых людей с наличием сопутствующей патологии и высокой частотой осложнений при традиционных методах лечения.
Целью настоящего исследования является разработка функционально-щадящего метода комбинированного эндоларингеального лечения с использованием гибкой видеоэндоскопической техники и физических факторов у больных предраком (дискератоз, рецидивирующий папилломатоз), первичным ранним раком гортани, локальным резидуальным и рецидивным раком гортани.
1. Разработка методики гибкой видеоэндоскопической эндоларингеальной электро-, лазерной и аргоноплазменной хирургии при предраке и раке гортани.
2. Разработка методики адьювантной ФДТ, как второго этапа комбинированного эндоларингеального лечения при рецидивирующем папилломатозе и раке гортани.
3. Изучение характера и частоты побочных эффектов и осложнений при видеоэндоларингеальной хирургии и адьювантной ФДТ у больных предраком и раком гортани. Разработка мер профилактики и лечения осложнений.
4. Оценка непосредственных и ближайших результатов комбинированного эндоларингеального лечения больных предраком и раком гортани, а также противовирусной эффективности ФДТ при вирусассоциированном рецидивирующем папилломатозе гортани.
5. Определение показаний и противопоказаний для комбинированного видеоэндоларингеального лечения больных предраком и раком гортани с использованием гибкой эндоскопической техники.
Научная новизна исследования:
В данной работе впервые разработан функционально-щадящий метод комбинированного эндоларингеального лечения больных предраком и раком гортани с использованием гибкой видеоэндоскопической техники, Ис1:УАО-лазера, аргоноплазменной коагуляции (АПК), электрорезекции и ФДТ.
Впервые изучены непосредственные и ближайшие результаты разработанного метода эндоскопического лечения больных предраком и раком гортани, оценен противовирусный эффект ФДТ при рецидивирующем папилломатозе дыхательных путей. Определен характер и частота осложнений и побочных эффектов эндоскопической хирургии и ФДТ.
Разработанные методики комбинированной видеоэндоскопической хирургии и ФДТ больных ранним, резидуальным и рецидивным раком гортани, а также дискератозом и рецидивирующим папилломатозом дыхательных путей позволяют выполнить органосохраняющее и функционально-щадящее лечение, расширяют возможности оказания условно-радикальной и радикальной помощи категории больных с тяжелой сопутствующей патологией, которым отказано в традиционном хирургическом или лучевом лечении.
Объем и структура диссертации
Диссертация изложена на 143 страницах машинописного текста. Состоит из введения, трех глав и заключения. Список литературы включает 72 отечественных и 76 зарубежных источников. Диссертация иллюстрирована 22 рисунками, 23 таблицами, 11 диаграммами и 15 клиническими наблюдениями.
Читайте также:


