Герпес и глицирризиновой кислотой

В сложившейся в настоящее время тенденции изменения структуры инфекционных болезней урогенитальной сферы, всё большее значение приобретают микроорганизмы, патогенные потенции которых слабо учитывались здравоохранением [2,3,10]. К таким заболеваниям относится герпесвирусная инфекция (ГВИ). По данным сероэпидемиологических исследований антитела к вирусам простого герпеса выявляются у 70–100 % населения [4, 6]. Заболеваемость генитальным герпесом в России за период с 1993 по 2013 год выросла с 8,5 до 18,4 случаев на 100000 населения. Установлено, что 20–50 % взрослых, обращающихся в венерологические клиники, имеют антитела к вирусу простого герпеса [1, 3]. 90 % населения земного шара инфицировано герпесвирусами, 2–12 % – страдает рецидивирующими герпесвирусными заболеваниями [2]. Особую опасность представляет заражение ВПГ у беременных, что нередко приводит к инфицированию плодных оболочек и плода. Результатом данного процесса является хроническое невынашивание беременности, раннее отхождение околоплодных вод, внутриутробная инфекция плода [4].
Необычайно широкая распространенность заболевания, разнообразные варианты ВПГ, его устойчивость к терапии традиционными противовирусными препаратами и длительное течение заставляют многих исследователей обращать внимание на причины, приводящие к развитию герпесвирусной инфекции и обусловливающие ее персистирование [7, 8]. Определенные трудности связаны с лечением больных часто рецидивирующим генитальным герпесом (РГГ), что обусловлено большим разнообразием ВПГ и их пантропизмом, сложностью механизмов развития и течения заболевания, формированием резистентных к базовым препаратам штаммов вирусов герпеса. Известно, что классические антивирусные вещества (ацикловир, бромвинилдиоксиуредин и др.), являясь нуклеоаналогами, взаимодействуют с ДНК вируса и блокируют синтез новых вирусных частиц. Однако в последние годы выявлены новые мутантные штаммы вирусов, нечувствительные к нуклеоаналогам. В то же время они оказались чувствительны к дефензинам и глицирризиновой кислоте (ГК), являющейся активным компонентом препарата "Кольпоцид" (UPL). Основными действующими веществами препарата являются пептидогликаны (PTG) и липотейхоевая кислота (LTA), полученные из продуктов ферментации лактобактерий, а также глицирризиновая кислота (ГК). Липотейхоевая кислота в комплексе с протеогликанами стимулирует выработку дефензинов, которые являются естественными защитными пептидами организма человека, стимулируя репаративные процессы, активируя локальный противовирусный иммунитет. Катионные антимикробные играют ключевую роль в обеспечении первой линии защиты макроорганизма от инфекции. Дефензины составляют большое семейство низкомолекулярных катионных пептидов, которые способны к киллингу широкого спектра патогенов. Они эффективны в отношении ДНК- и РНК-вирусов, ингибируя их репликацию [2, 10]. Антивирусная активность ГК была обнаружена в последние годы. Было показано, что ГК способна ингибировать ДНК и РНК вирусы. В исследованиях на культуре клеток, зараженных различными вирусами, выявлено, что ГК в концентрациях, хорошо переносимых неинфицированными клетками, ингибирует рост и цитопатическую активность указанных вирусов [7]. Как было показано в последних исследованиях, молекулярный механизм противовирусного действия ГК заключается в ингибировании киназы Р, что приводит к подавлению фосфорилирования клеточных и кодируемых вирусом белков в инфицированных клетках. Таким образом, ГК относится к классу киназных ингибиторов, развитие толерантности вирусов к которым затруднено [7]. Кроме того, активированная глицирризиновая кислота является выраженным иммуностимулятором, влияя как на гуморальные, так и клеточные факторы иммунитета. Иммуностимулирующий эффект проявляется индукцией выработки собственных интерферонов, повышением активности Т-лимфоцитов, уменьшением концентрации иммуноглобулинов класса Gи увеличением концентрации иммуноглобулинов класса AиM [4].
Материалы и методы
В период нашей работы наблюдалось 150 женщин в возрасте от 17 до 34 лет – 120 больных рецидивирующим генитальным герпесом, у которых, после окончания курса предложенной терапии, в течение 12 месяцев произошло оплодотворение с последующим успешным вынашиванием плода и рождением ребенка. Исследования проводились на базе кафедр акушерства, гинекологии и перинатологии Кубанского государственного медицинского университета, в ООО "ВИП КлиникГрупп", г. Краснодар. Всем женщинам проведено клинико-лабораторное, общесоматическое, гинекологическое обследование, ультразвуковое исследование органов малого таза, по показаниям мазки на онкоцитологию, кольпоскопия. Для оценки эффективности современного традиционного и предлагаемого способа терапии методом случайной выборки все больные с обострением РГГ (120 пациенток) были разделены на две репрезентативные группы:
I группа (60 пациенток) – получавших традиционную противовирусную терапию ацикловиром в дозе 200 мг 5 раз в сутки в течение 5 дней;
Диагноз РГГ устанавливался на основании клинико-микробиологического обследования. Диагностику инфицированности различными вирусами простого герпеса проводили комплексно: 1) прямая микроскопия; 2) реакция прямой иммунофлуоресценции; 3) метод полимеразной цепной реакции (ПЦР), который обладает 95 % чувствительностью, 100 % специфичностью; 4) серологическая диагностика с определением иммуноглобулинов (Ig) класса M, Aи G. Концентрацию цитокинов (IL-1β, IL-8, TNFα, IFNγ, IL-4 и IL-10) в сыворотке крови и в цервикальной слизи определяли твердофазным иммуноферментным методом с использованием наборов по прилагаемым методикам (CaltagLaboratories, USA).
Обследование беременных проводилось согласно приказу № 572н от 12. 11. 2012 г. Министерства здравоохранения Российской Федерации.
Ввиду того, что группы по всем исследованным параметрам были однородными, нами без определения достоверной массовой доли каждого исследуемого признака, для суждения о клиническом состоянии больной была предложена интегральная субъективно-объективная балльная оценка (0 баллов – отсутствие симптома, 1 балл – средняя степень выраженности симптома, 2 балла – выраженная симптоматика). Это позволяет в динамике оценивать, как интенсивность каждого симптома, так и суммарную интегральную балльную оценку клинической картины. Результаты исследований были обработаны методом вариационной статистики с определением критерия Фишера (F) для оценки непараметрических показателей групп малых выборок и критерием Стьюдента (t) для независимых групп [М.Б. Славин, 1989; В.М. Зайцев и соавт., 2003]. Анализ проводился с использованием программы "STATISTICA" 6,0.
Результаты и обсуждение
Клиническая эффективность. До лечения суммарная балльная оценка клинических проявлений ВПГ инфекции в обеих клинических группах была одинаковой, что еще раз подтверждает репрезентативность выборки (рис. 1).
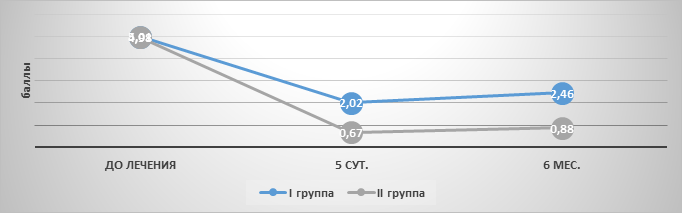
Рис. 1. Динамика клинической эффективности у больных сравниваемых групп
Через 5 дней после окончания проводимой терапии в обеих группах отмечено достоверное (P
- КЛЮЧЕВЫЕ СЛОВА: вирусы, инфекции, гистамин, фосфолипаза, герпес, Эпиген интим
Исследования последних лет показали, что вирусы способны поддерживать воспалительный процесс в зоне поражения с изменением структурно-функциональных характеристик ткани, вызывать изменения антигенной структуры инфицированных клеток, индуцируя появление аутоантител, могут быть индукторами неопластических трансформаций. Локальные изменения слизистых оболочек и кожи при вирусной инвазии проявляются появлением в ткани воспалительных инфильтратов, активацией клеток иммунной системы, изменением уровня цитокинов, факторов роста и протеолитических ферментов, активацией ангиогенеза, изменением экспрессии генов.
Препараты солодки обладают многосторонней биологической активностью и оказывают противовоспалительное, противовирусное и иммуномодулирующее действие. Противовоспалительное действие заключается в купировании воспалительных реакций, вызываемых гистамином, серотонином и брадикинином. Кислота ингибирует активность фосфолипазы А и образование простагландина Е2 в активированных макрофагах, ускоряет миграцию лейкоцитов в зону воспаления. При этом угнетается как экссудативная, так и пролиферативная фаза воспалительного процесса. Как показали исследования, глицирризиновая кислота обладает также выраженным противовирусным действием. Первое исследование антивирусных свойств глицирризиновой кислоты было проведено в 1979 году, а в 90-е годы было установлено, что она прерывает репликацию вирусов на ранних стадиях за счет ингибирования киназы Р.
В ряде исследований было показано, что мутантные штаммы вирусов, резистентные к ацикловиру, сохраняют чувствительность к глицирризиновой кислоте. При взаимодействии кислоты с вирионами изменяются различные фазы вирусного цикла, что сопровождается необратимой инактивацией вирусных частиц, находящихся в свободном состоянии вне клеток; блокируется внедрение активных вирусных частиц внутрь клетки, нарушается способность вируса к индукции синтеза новых вирусных частиц.
Глицирризиновая кислота обладает также выраженным иммуномодулирующим действием. Показана способность глицирризиновой кислоты индуцировать образование ИФН и активировать неспецифические факторы клеточного иммунитета.
Все пациентки были разделены на группы:
- I группа – 30 женщин с папилломавирусной инфекцией половых органов;
- II группа – 30 женщин с типичной формой генитального герпеса (легкой и средней степени тяжести);
- III группа – 30 женщин с цитомегаловирусной инфекцией половых органов;
- контрольная группа – 10 здоровых женщин репродуктивного возраста.
В исследовании с целью оценки механизма действия исследуемого препарата использовалась модель моноинфекции и монотерапии. В каждой группе пациенткам проводили местную терапию глицирризиновой кислотой (n = 20) или препаратом плацебо (n = 10) в течение 1 мес., препарат наносили ежедневно по 2-3 раза на слизистые оболочки половых органов путем распыления, при локализации поражений на шейке матки препарат применяли интравагинально с помощью специальной насадки. Назначение препарата или плацебо в группах проводили слепым методом. Во время исследования лечение другими противовирусными препаратами не проводилось. Клиническую эффективность терапии оценивали в ходе лечения, период последующего наблюдения составил 6 мес.
С целью оценки локального действия глицирризиновой кислоты (до лечения и сразу после его окончания) исследовали слизь цервикального канала на содержание провоспалительных Th1-цитокинов – IL-1b, IL-6, TNF-α и IFN-γ, противовоспалительных Th2-цитокинов – IL-4, IL-10, а также матриксных металлопротеиназ ММР-1 и тканевых ингибиторов матриксных металлопротеиназ ТIМР-1.
Анализ динамики клинических симптомов инфекции после применения глицирризиновой кислоты свидетельствует о высокой клинической эффективности препарата. При типичной форме генитального герпеса на фоне лечения длительность и клиническая выраженность рецидивов герпеса по субъективной оценке больных значительно уменьшилась, что позитивно повлияло на качество жизни пациенток. По сравнению с плацебо на фоне применения глицирризиновой кислоты отмечалось быстрое купирование симптомов вульводинии (зуда, жжения, дискомфорта в области герпетических высыпаний вульвы и влагалища); более быстрое заживление поражений (в среднем на 2 ± 0,78 дня по сравнению с плацебо); ускорение процессов эпителизации зон поражения; значительное сокращение зоны гиперемии вокруг герпетических элементов и реакции регионарных лимфатических узлов. Значительное снижение на фоне лечения местной воспалительной реакции, окружающей герпетические элементы, и ускорение процессов репарации ткани способствовало снижению риска присоединения вторичной бактериальной инфекции и развитию осложнений.
На фоне терапии глицирризиновой кислотой у пациенток с экзофитными формами папилломавирусной инфекции гениталий отмечалось купирование симптомов стойкого дискомфорта, зуда и жжения в области наружных половых органов через 4-6 дней от начала применения препарата. При наличии небольших и множественных кондилом вульвы и влагалища отмечено значительное уменьшение экзофитных образований в размере и общей площади поражения. При цитомегаловирусной инфекции исходно только у 6 пациенток отмечались симптомы вульводинии, которые были быстро купированы на фоне терапии глицирризиновой кислотой.
Основной задачей исследования была оценка влияния глицирризиновой кислоты на локальные молекулярно-биологические процессы в половом тракте при вирусных инфекциях. При анализе содержания провоспалительных цитокинов IL-1b, IL-6, TNF-α и IFN-γ в цервикальном канале до лечения во всех группах было выявлено, что персистенция вирусной инфекции сопровождалась значительным увеличением уровня Th1-цитокинов, что отражало интенсивность воспалительных реакций в ткани и являлось важным маркером фазы активации вирусной инфекции. При всех типах вирусной инфекции локальные уровни Th1-цитокинов достоверно превышали контрольные значения:
- при генитальном герпесе в I группе уровень IL-1b был повышен в 33,2 раза, IL-6 – в 3,5 раза, TNF-α – в 4,6 раза и IFN-γ – в 3,6 раза;
- при папилломавирусной инфекции во II группе уровень IL-1b был повышен в 62,4 раза, IL-6 – в 2,4 раза, TNF-α – в 13,6 раза и IFN-γ – в 3 раза;
- при цитомегаловирусной инфекции в III группе уровень IL-1b был повышен в 18,6 раза, IL-6 – в 1,3 раза, TNF-α – в 3,7 раза и IFN-γ – в 2,8 раз (во всех случаях p 0,05 (рисунки: 1, 3, 5).
При анализе системы тканевых протеолитических ферментов матриксных металлопротеиназ и их ингибиторов как ключевых эффекторов тканевого ремоделирования и важных маркеров воспалительного процесса во всех группах выявлено повышение локальной активности ММР-1 (рисунки: 2, 4, 6).
После курса терапии глицирризиновой кислотой локальные уровни Th1-цитокинов IL-1b, IL-6, TNF-α и IFN-γ в цервикальном канале достоверно снизились до контрольных значений, при этом динамика изменений была особенно показательна в I группе пациенток с генитальным герпесом, где исходная интенсивность воспалительных реакций была максимальной (рисунки 1, 3 и 5).
Терапия глицирризиновой кислотой привела к усилению защитного потенциала слизистой оболочки – к активации противовоспалительных Th2-цитокинов, при этом уровни IL-4 и IL-10 повысились, в ряде случаев превысив контрольные значения. При применении плацебо уровни провоспалительных Th1-цитокинов и регуляторных Th2-цитокинов незначительно колебались за счет волнообразности самого вирусного инфекционного процесса, но достоверно не изменились (p > 0,05 во всех группах по сравнению с исходными значениями и контролем).
При анализе действия глицирризиновой кислоты на уровень тканевых матриксных металлопротеиназ выявлено достоверное снижение после лечения активности протеолитических ферментов до контрольных значений:
- в I группе уровень ММР-1 снизился в 2,25 раза (p 0,05).
Терапия препаратом привела к повышению протективных свойств слизистой оболочки – выявлено повышение до контрольных значений уровня тканевых ингибиторов металлопротеиназ: уровень ТIМР-1 достоверно повысился в I и II группах (p
Изобретение относится к области фармацевтики и касается фармацевтической композиции для лечения герпес-вирусной инфекции. Изобретение заключается в том, что в композиции в качестве антигерпетического средства используют состав, содержащий глицирризиновую кислоту, эфтидерм, мефенамовую кислоту, протеолитические ферменты, наполнитель в виде смеси вазелина и ланолина, а также спирт этиловый и воду очищенную в заданном соотношении. Изобретение позволяет полностью купировать инфекционный процесс на стадии латентных признаков заболевания, снижает сроки лечения болезни до 1-2 дней и увеличивает срок ремиссии до одного года и более. 2 з.п. ф-лы.
Изобретение относится к области медицины, а именно к фармакологии, и может быть использовано для лечения герпес-вирусных инфекций.
Герпес - инфекционное заболевание, вызываемое одним из нескольких родственных вирусов, в том числе вирусами 1 и 2 типа простого герпеса (ВПГ) и вирусом варицелла зостер (ВВЗ). Данная инфекция может передаваться внутриутробно, воздушно-капельным и половым путем, вовлекая при этом в патологический процесс любой орган и систему организма, вызывая иммунодефицитные состояния, тяжелые формы экземы и стоматита. Особенно опасен он, когда добирается до центральной нервной системы: возникают энцефалиты, менингоэнцефалиты. Каждый третий из заболевших погибает, другая треть становится инвалидами. В последнее время есть серьезные основания полагать, что герпес вызывает и некоторые виды онкологических заболеваний. Герпетическое заболевание довольно широко распространено среди населения (по данным ВОЗ около 35% населения планеты заражены им) и по смертельным исходам среди вирусных заболеваний стоит на втором месте после гриппа (не считая СПИД).
Вирус простого герпеса первого типа (ВПГ-1) обычно вызывает появление пузырьков “простуды” на губах, вокруг ноздрей и в полости рта. Вирус простого герпеса второго типа (ВПГ-2) является главной причиной генитального герпеса (герпеса генитальных органов). Вирус варицелла зостер (ВВЗ) ответственен за развитие ветряной оспы и опоясывающего герпеса.
Для лечения герпеса разработано множество препаратов как симптоматического характера, так и этиотропного действия, направленного непосредственно на вирусы - возбудителя болезни.
Препараты симптоматического действия направлены на купирование болевого синдрома (болеутоляющие средства), снятие воспалительного процесса (противовоспалительные препараты), повышение репаративных процессов (стимуляторы клеточного роста) и коррекцию иммунологических реакций (иммунокорректоры) организма.
Действие этиотропных препаратов направлено непосредственно на возбудителя болезни, а именно на возбудителя простого или опоясывающего герпеса.
Анализ уровня известных технических решений показывает, что тяжесть заболеваний, вызванных вирусами 1 и 2 типа простого герпеса и вирусом варицелла зостер, их широкое распространение и большой процент летальных исходов явились причиной появления в медицинской практике достаточно большого количества разнообразных по компоновке и действующему началу антигерпетических средств, которые, не влияя существенно на частоту новых вспышек заболеваний, способны на определенное время купировать герпетический процесс. Последнее во многом предопределяет актуальность поставленной задачи по поиску новых, более эффективных средств защиты от герпетического вирусного поражения организма.
Для лечения простого герпеса используют, например, экстракт чеснока, который принимают внутрь ежедневно в течение 1-3 недель, каждую неделю, снижая дозу, либо используют аппликацию экстракта чеснока на пораженную зону (патент США №4795636, oп. 03.01.1989).
Известен препарат Протефлазид (Регистрационное удостоверение №Р.02.01/02777), представляющий собой водно-этанольный экстракт флавоноидных гликозидов, выделенных из диких злаков Deschampsia caespitosa L. и Calamagrostis epigeios L., которые способны неспецифически подавлять фермент ДНК-полимеразу в клетках, инфицированных вирусами простого герпеса 1-го и 2-го типов, герпеса зостер и СПИД. Это приводит к снижению способности или к полному блокированию репликации вирусной ДНК и, как следствие, препятствует размножению вирусов. Препарат применяют для лечения, профилактики и предупреждения вирусных инфекций, которые вызваны вирусом простого герпеса 1-го и 2-го типов.
Препарат принимают внутрь каплями, нанесенными на кусочек сахара (или пищевой крахмал). Для лечения инфекций простого герпеса, включая первичный и рецидивирующий генитальный герпес и герпес губ, препарат наносят в виде примочки на пораженный участок кожи или слизистой оболочки 3-5 раз в сутки. Для приготовления примочек с Протефлазидом® 1,5 мл (36-38 капель) препарата разводят в 10 мл физиологического раствора. Смоченную в растворе марлю наносят на пораженный участок кожи до 3 раз в сутки. Для приготовления вагинальных тампонов с Протефлазидом® 3 мл (72-75 капель) препарата разводят в 20 мл физиологического раствора.
Лечение продолжают до исчезновения признаков поражения кожи или слизистой оболочки. Максимальный курс лечения не менее 14 дней.
Наиболее часто применяемым в настоящее время является антивирусный химико-терапевтический препарат, действующим началом которого является синтетический аналог одного из наиболее часто встречающихся нуклеозидов в триплетах ДНК - ацикловир (9-[(2-гидроксиэтокси)метил]гуанин), созданный в 70-е годы и выпущенный в практику под названием "Зовиракс" (Великобритания).
Известны также производные ацикловира - валацикловир (ВАЛТРЕКС), фамцикловир (ФАМВИР) (WO 9725989), которые применяют для больных с герпес-вирусными инфекциями с нарушениями кишечного всасывания: пожилых людей, онкологических больных, ВИЧ-инфицированных (Матяш В.И., Шевчук В.Б., Толкунова Т.Л., Василенко Л.Г. "Этиопатогенетическая терапия тяжелых форм герпетической инфекции". Институт эпидемиологии и инфекционных болезней им. Л.В.Громашевского АМН Украины (Киев)).
Как правило, мази и кремы с использованием этих соединений готовят на основе парафина либо пропиленгликоля, с содержанием действующего вещества не менее 5 мас.%.
Известна композиция, которая в качестве действующего начала, предназначенного для подавления и уничтожения вируса, включает в себя мочевину, гиалуроновую кислоту или ее соль (патент сша №5550112). Для усиления лечебных и потребительских свойств композиции в нее вводят добавки: антисептические, противовоспалительные, анестезирующие и смазочные вещества (патент сша №5550112).
Известно введение в композицию, содержащую в качестве действующего вещества рибофлавин, добавок, содержащих каротиноиды, флавоноиды, ацетил СоА, витамины А, Е, С, В6, В9, а также лизоцим, глутатион и др. (патент США №6020333).
Известен противовирусный препарат HERPIGEN фирмы Sananavita Enterprises, выпускаемый в виде мази, содержащий в качестве действующего вещества 0,1 г глицирризиновой кислоты и наполнитель. Мазь наносят три раза в день на пораженные участки обычно в течение недели. Для более быстрого выздоровления возможна аппликация на 6-8 часов ежедневно.
Наиболее близким к заявляемому является препарат Эпиген (EPIGEN) фирмы Хеминова Интернасьональ С.А., Испания, в состав которого входит 0,1 мас.% глицирризиновой кислоты, набор органических кислот, обладающих консервирующим, смягчающим и антисептическим действием, эмульсионный воск в качестве наполнителя, а также отдушка и вода очищенная. Препарат выпускается в виде крема, мази или аэрозоля. Мазь наносят тонким слоем без втирания на пораженную кожу и слизистую 3-5 раз в сутки в течение как минимум 3 дней.
Технической задачей изобретения является расширение арсенала отечественных лечебных средств, используемых для антигерпетической терапии, обладающих высокой терапевтической активностью и ускоренным репаративным действием.
Поставленная задача решается фармацевтической композицией для лечения герпес-вирусной инфекции, содержащей глицирризиновую кислоту, наполнитель в виде смеси вазелина и ланолина в соотношении 1:6, воду очищенную и дополнительно водно-глицериновый комплекс (2,3-диоксипропил)-ортотитаната гидрохлорида, мефенамовую кислоту (Acidum mephenamicum), протеолитические ферменты и спирт этиловый при следующем соотношении компонентов, мас.%:
Глицирризиновая кислота 0,1-1,0
Вазелин желтый медицинский 10,0-50,0
Ланолин безводный 1,0-10,0
Мефенамовая кислота 0,4-1,0
Спирт этиловый 3,0-10,0
Протеолитические ферменты 0,01-0,40
Вода очищенная Остальное
Состав фармацевтической композиции подобран эксперементально на основании максимальной эффективности ее действия и ускорения репаративного действия при лечении герпес-вирусной инфекции.
Используемая в заявляемой композиции глицирризиновая кислота представляет собой тритерпеновый гликозид, молекулярная формула С42Н62O16, молекулярный вес 822,94 (М.Д.Машковский. "Лекарственные средства", М., Медицина, 1978, с.325). Обладает противовирусным, противовоспалительным действием.
Водно-глицериновый комплекс (2,3-диоксипропил)-ортотитаната гидрохлорида выпускается промышленностью под наименованием ЭФТИДЕРМ (рег. номер 94/34/12). Представляет собой полупрозрачную, студнеобразную массу светло-желтого цвета, хорошо растворимую в воде, глицерине и спирте.
Мефенамовая кислота - кристаллический порошок серовато-белого цвета. Практически нерастворим в воде, мало растворим в спирте, обладает противовоспалительной, анальгезирующей и жаропонижающей активностью (М.Д.Машковский. "Лекарственные средства", т.1, M., Медицина, 1994, с.219). Введение кислоты в заявляемый состав осуществляют либо непосредственно, либо используют ее спиртовой раствор.
Протеолитические ферменты, входящие в состав композиции, например, такие, как лидаза, панкреатин, липаза и др., увеличивают степень репаративных механизмов и восстановление целостности поврежденных кожных и слизистых покровов.
В качестве наполнителя используют смесь вазелина желтого медицинского (ФС 42-2456-57) и ланолина безводного (ФС 373, изд. десятое) в соотношении 1:6, позволяющую повысить потребительские свойства композиции и обеспечивающую возможность легкого нанесения и равномерного распределения состава по поверхности кожи.
Приготовление заявляемой композиции осуществляют стандартным способом приготовления мазей и кремов, путем смешивания всех входящих в состав композиции компонентов. Обычно к эфтидерму добавляют глицирризиновую кислоту, растворяют в спирте или добавляют непосредственно мефенамовую кислоту, ферменты, спирт и воду, а затем полученную смесь вводят в наполнитель - смесь вазелина с ланолином - и тщательно перемешивают до получения однородной массы.
Композиция дополнительно может содержать отдушку, в качестве которой можно использовать любые пригодные для этой цели спиртовые экстракты или эфирные масла, например, эвкалипта, мяты и т. д. Их количество подбирают экспериментально, традиционными способами, но, как правило, содержание их в композиции не превышает 0,01-1,00 мас.%.
Для придания композиции противоаллергических свойств в ее состав дополнительно вводят любые пригодные для этой цели противоаллергические препараты, такие как, например, димедрол, пипольфен, супрастин и т.д., в количестве 0,02-0,05 мас.%.
Как показали проведенные исследования, использование заявляемой композиции позволяет полностью купировать начальную стадию инфекционного процесса, усилить противогерпетический и репаративный эффекты действия композиции. Указанный результат достигается за счет иммуномодулирующего эффекта, возникающего при нанесении данной композиции на поврежденную поверхность кожи или слизистой оболочки, усилением действия местного клеточного специфического и неспецифического звеньев иммунной системы, что подтвердили проведенные цитологические исследования.
Методы поверхностной и глубокой биопсии и непрямой мембранной иммунофлюоресценции (МИФ) ("Иммунологические методы", М., Медицина, 1987, с. 136) показали, что заявляемая композиция оказывает стимулирующее действие на иммунокомпетентные клетки, обладающие противовирусной активностью: NK-клетки (CD-16), Т-цитологические лимфоциты (CD-8), моноциты и макрофаги (CD-23), о чем свидетельствует сравнение их содержания до начала лечения и через 12 часов после нанесения композиции, а именно до начала лечения содержание СД-16, СД-8 и СД-23 составляло соответственно 1,9±0,14; 1,5±0,24 и 0,4±0,43, а через 12 часов соответственно 3,8±0,26; 5,8±0,3 и 4,6±0,26.
На усиление репаративных процессов в очаге поражения указывает повышенное количество фибробластов и полибластов. Так, до применения композиции фибробласты не были обнаружены, а уже через 12 часов после применения их количество составило 3,4±0,3. То же относится и к полибластам, которые не были найдены до начала лечения, а через 12 час после применения композиции их число составило 6,7±0,8.
Заявляемая композиция позволяет быстро снять болевой синдром, сопровождающий герпетическую инфекцию, полностью купировать инфекционный процесс на стадии латентных признаков заболевания (пощипывание, чувство онемения) при одновременном увеличением срока ремиссии до одного года и более, а также снизить сроки лечения клинической стадии заболевания до 1-2 дней.
Действие заявляемой фармацевтической композиции было проверено в клинике кожно-венерических болезней ВГМУ (Владивостокский государственный медицинский университет).
Под наблюдением находились 22 больных с различными формами простого герпеса (у 11 - генитальный герпес, у 10 - лабиальный герпес и у 1 - опоясывающий), из них 16 женщин, 6 мужчин в возрасте от 18 до 36 лет. У 10 наблюдавшихся больных процесс носил рецидивирующий характер (не более 3 рецидивов в год) и у 12 поражения развились впервые. При клиническом обследовании больных с локализацией высыпаний в области половых органов у 7 из 11 процесс носил ограниченный характер, представлен был мелкими сгруппированными пузырьками, наполненными светлым содержимым, без признаков воспаления на периферии очага поражения. У 5 из 11 отмечалась эритема, отечность в очаге поражения, сопровождающиеся интенсивньм жжением и зудом. У 6 из 10 больных с локализацией высыпаний в области красной каймы губ процесс представлен сгруппированными мелкими пузырьками, с серозным содержимым, а у остальных 4 - эрозиями, с серозно-геморрагическими корочками, слизистая отечная, гиперемированная. У больного с опоясывающим герпесом отмечались пузырьки с серозным содержимым в области поясницы, жжение и зуд. Контрольную группу составляли 5 больных генитальным герпесом и 5-лабиальным, которые получали наружную терапию кремом ЭПИГЕН.
В группе наблюдавшихся больных использовалась для наружной терапии заявляемая композиция, содержащая 45 г эфтидерма, 0,1 г глицирризиновой кислоты, 0,5 г мефенамовой кислоты, растворенной в 10 мл 50% этилового спирта, 0,02 г лидазы, 9,38 г воды очищенной. Данные компоненты тщательно перемешивали и затем добавляли в предварительно приготовленный наполнитель, состоящий из 30 г вазелина и 5 г ланолина. Все тщательно перемешивали до образования однородной кремообразной массы светло-желтого цвета.
Препарат наносили на очаг поражения три раза в день. Сразу после нанесения препарата отмечается купирование болевого синдрома, через 1-2 часа значительно снижаются эритема, отечность. Через 12 часов наблюдается подсыхание высыпаний, что расценивается как клиническое разрешение заболевания. У лиц контрольной группы высыпания разрешались на 4-6 день. Побочного эффекта в виде менингиальных явлений, поражения коньюктивы глаз после применения заявляемой композиции у наблюдавшихся больных не обнаружилось.
Таким образом, заявляемая фармацевтическая композиция может найти широкое применение в практическом здравоохранении. Она позволяет полностью купировать инфекционный процесс на стадии латентных признаков заболевания, увеличивает срок ремиссии до одного года и более, снижает сроки лечения клинической стадии болезни до 1-2 дней и может служить в качестве профилактического средства герпес-вирусных инфекций.
1. Фармацевтическая композиция для лечения герпес вирусной инфекции, содержащая глицирризиновую кислоту, наполнитель и воду очищенную, отличающаяся тем, что композиция дополнительно содержит водно-глицериновый комплекс (2,3-диоксипропил)-орто-титанат гидрохлорида, (эфтидерм) мефенамовую кислоту (Acidum mephenamicum), протолитические ферменты и спирт этиловый, а в качестве наполнителя - смесь вазелина и ланолина в соотношении 1: 6, при следующем соотношении компонентов, мас.%:
Глицирризиновая кислота 0,1-1,0
Вазелин желтый медицинский 10,0-50
Ланолин безводный 1,0-10,0
Мефенамовая кислота 0,4-1,0
Спирт этиловый 3-10
Протолитические ферменты 0,01-0,4
Вода очищенная Остальное
2. Фармацевтическая композиция по п.1, отличающаяся тем, что дополнительно содержит антиаллергические вещества димедрол или пипольфен или супрастин в количестве 0,02-0,05 мас.%.
3. Фармацевтическая композиция по любому из пп.1 и 2, отличающаяся тем, что дополнительно содержит отдушку в виде спиртовых экстрактов или эфирных масел эвкалипта и/или мяты в количестве 0,01-1,00 мас.%.
NF4A Восстановление действия патента СССР или патента Российской Федерации на изобретение
Дата, с которой действие патента восстановлено: 10.09.2008
Читайте также:


