Гентамицин грудничку при стафилококке отзывы

Наиболее трудными для лечения являются инфекции, вызванные метициллинорезистентными штаммами S. aureus (MRSA) и S. epidermidis (MRSE), в частности инфекции области хирургического вмешательства после больших ортопедических операций. Распространенность штаммов MRSA в России высока. Несмотря на то, что по данным многоцентрового исследования в структуре бактериальных возбудителей нозокомиальных инфекций за 2011–2012 гг. доля S. aureus составила 16,7 %, что сопоставимо с данными 2006–2008 гг. (19,5 %), существенно увеличилась значимость метициллинорезистентных штаммов данного возбудителя. Доля MRSA составляла 33,4 % в 2001–2002 гг. и 55,4 % в 2006–2008 гг., возросла до 66,9 % к 2011–2012 гг. [5]. Выделение метициллинорезистентных штаммов S. aureus и S. epidermidis из гнойного очага при перипротезной инфекции является неблагоприятным прогностическим признаком для эффективности антибактериальной терапии и лечения в целом. В РФ до настоящего времени препаратом выбора при MRSA- и MRSE-ассоциированных инфекциях остаётся гликопептидный антибиотик ванкомицин. Однако в настоящее время в научной медицинской литературе многие авторы отмечают снижение эффективности ванкомицина при антибактериальной терапии инфекций, вызванных метициллинорезистентными стафилококками, in vitro демонстрирующими чувствительность к ванкомицину [9]. Это определяет необходимость применения эффективных комбинаций уже известных лекарственных средств разных классов, обладающих синергидным действием в отношении лекарственноустойчивых микробных возбудителей. К примеру, сохранившие активность рифампицин и фузидиевую кислоту для достижения хорошего антистафилококкового эффекта необходимо сочетать c β-лактамами или фторхинолонами [8]. Многие зарубежные исследователи предлагают широко использовать комбинированную антибактериальную терапию при лечении инфекции протезированного сустава стафилококковой этиологии для усиления бактерицидного эффекта, воздействия на микробные биопленки и на клетки бактерий, расположенные внутриклеточно [8].
Целью настоящего исследования было оценить in vitro активность комбинации гентамицина и диоксидина, обладающих принципиально различным механизмом антимикробного действия, в отношении штаммов метициллинорезистентных стафилококков.
Материалы и методы исследования
FIX = FIC (одного антибиотика) + + FIC (второго антибиотика),
где FIC (fractional inhibitory concentrations) – фракционная ингибирующая концентрация исследуемого антибиотика, определяемая как отношение величины минимальной подавляющей концентрации (МПК) этого антибиотика в комбинации с МПК второго антибиотика. Характера взаимодействия препаратов определяли по величине коэффициента FIX согласно шкале: 4 антагонизм.
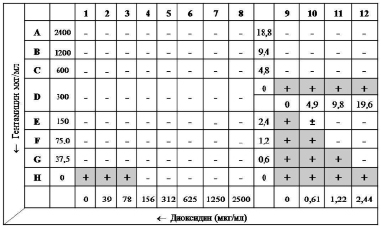
Технически метод осуществляли следующим образом: в каждую лунку 96-луночного планшета вносили по 50 мкл питательного бульона Мюллера-Хинтон (МХБ). Антимикробные препараты титровали серийно двукратно: гентамицин с концентрации 2400 до 0 мкг/мл (ряды A-H), диоксидин – с 2500 до 0 мкг/мл (колонки 1–12) (рис. 1).
Инокулюм каждой тест-культуры (0,5 McFarland) готовили в стерильном изотоническом растворе. В каждую лунку вносили по 100 мкл инокулюма и инкубировали планшет 18 ч при 37 °C. За МПК (в мкг/мл) принимали наименьшую концентрацию антимикробного средства, при которой не наблюдалось видимого роста микроорганизма. Далее для тестируемых штаммов S. aureus рассчитывали коэффициенты FIX. На основе значений фракционных коэффициентов FIC строили изоболограмму и оценивали ее характер.
Количественные результаты представлены в виде медиан, в качестве меры рассеивания использовали межквартильный интервал 25–75 % (МКИ 25–75 %).
Результаты исследования и их обсуждение
Установленные по результатам 3-х экспериментов медианы МПК (табл. 1) показали крайне невысокую активность диоксидина при воздействии как на штаммы устойчивые к метициллину (156 мкг/мл), так и чувствительные (39 мкг/мл). Кроме того, МПК гентамицина в отношении тестируемых изолятов MRSA также в 4 раза превысила МПК для чувствительных к метициллину референс-штаммов. Однако применение антимикробных препаратов в комбинации потребовало существенно меньших их концентраций для эффективного подавления возбудителей.
Медианы коэффициентов FIC и FIX взаимодействия гентамицина и диоксидина свидетельствуют (табл. 2) об эффективном действии изучаемой комбинации в отношении всех тестируемых культур стафилококков. Величина итоговых коэффициентов FIX во всех случаях не превысила 0,5 и составила для всех штаммов 0,09–0,26, что характерно для синергидного действия препаратов. Установлено, что, несмотря на выявленное синергидное действие в отношении метициллинорезистентных изолятов стафилококков устойчивых к гентамицину, коэффициент FIX для них был выше, чем для референс-штаммов, чувствительных к метициллину и гентамицину.
Действующее вещество


Фармакологические группы
Нозологическая классификация (МКБ-10)
Состав
| Мазь глазная | 1 г |
| активные вещества: | |
| дексаметазон | 0,3 мг |
| гентамицина сульфат | 5 мг |
| (в пересчете на гентамицин — 3 мг) | |
| вспомогательные вещества: вазелин белый — 775,98 мг; парафин жидкий — 149,13 мг; ланолин — 69,9 мг |
Описание лекарственной формы
Белая с желтоватым оттенком полупрозрачная мазь.
Фармакологическое действие
Фармакодинамика
Комбинированное средство, действие которого обусловлено входящими в его состав компонентами. Оказывает противоаллергическое, противовоспалительное и антибактериальное действие.
Дексаметазон — ГКС — оказывает выраженное противовоспалительное действие, индекс его относительной противовоспалительной активности составляет 30.
Гентамицина сульфат — антибиотик группы аминогликозидов — характеризуется широким спектром действия, активен в отношении большинства грамотрицательных и грамположительных микроорганизмов (Pseudomonas aeruginosa, Escherichia coli, Proteus spp., Klebsiella spp., Serratia spp., Salmonella spp.). Умеренно активен в отношении штаммов Staphylococcus spp.
Фармакокинетика
При местном применении дексаметазон хорошо проникает в эпителий роговицы и конъюнктиву; при этом в водянистой влаге глаза достигаются терапевтические концентрации; при воспалении или повреждении слизистой оболочки скорость пенетрации увеличивается.
Гентамицина сульфат при местном применении обнаруживается в терапевтической концентрации в строме роговицы, во влаге передней камеры, стекловидном теле в течение 6 ч. Гентамицина сульфат не проникает в системный кровоток через неповрежденный эпителий роговицы.
Показания препарата Декса-Гентамицин
инфекции переднего отрезка глаза, вызванные чувствительной к гентамицину микрофлорой (конъюнктивит, кератит, блефарит, ячмень);
аллергические процессы в переднем отрезке глаза, сопровождающиеся бактериальным инфицированием;
профилактика и лечение воспалительных явлений в послеоперационном периоде (удаление катаракты, антиглаукоматозные операции).
Противопоказания
повышенная чувствительность к любому из компонентов препарата;
кератит, вызванный Herpes zoster (древовидный кератит), ветряная оспа и прочие вирусные заболевания роговицы и конъюнктивы;
микобактериальные инфекции глаз;
грибковые заболевания глаз;
острые гнойные заболевания глаз с поражением роговичного эпителия;
травмы и язвенные поражения роговицы;
ношение контактных линз;
I триместр беременности;
детский возраст до 18 лет (в связи с отсутствием данных по эффективности и безопасности).
Применение при беременности и кормлении грудью
В настоящее время данные клинических испытаний относительно применения препарата Декса-Гентамицин во время беременности, лактации, а также у детей отсутствуют. Однако препарат может применяться во II–III триместре беременности в том случае, если предполагаемая польза для матери превышает возможный риск для плода.
Побочные действия
В редких случаях после закладывания мази возможна аллергическая реакция и ощущение жжения.
Длительное применение препарата может стать причиной возникновения вторичной глаукомы и стероидной катаракты, поэтому при применении препарата более 2 нед , а также у пациентов, имеющих в анамнезе глаукому, рекомендуется регулярно контролировать ВГД .
Возможно возникновение контактного дерматита, герпетического кератита, перфорации роговицы при наличии кератита, грибковой инфекции, усиление выраженности бактериальной инфекции роговицы, птоза, мидриаза. При применении после травм роговицы может приводить к замедлению ее заживления.
В случае возникновения побочных эффектов следует прекратить пользоваться препаратом и как можно скорее обратиться к офтальмологу.
Взаимодействие
При совместном применении с атропином, другими холинолитическими или мидриатическими препаратами возможно увеличение уровня ВГД .
При местном применении гентамицин несовместим с амфотерицином В, гепарином, сульфадиазином, цефалотином и клоксациллином. Местное применение этих препаратов вместе с гентамицином может привести к отложению преципитатов в конъюнктивальной полости.
Способ применения и дозы
Конъюнктивально. Полоска мази длиной 1 см закладывается 2–3 раза в день.
Во время аппликации глазной мази Декса-Гентамицин следует избегать контакта тюбика с поверхностью кожи или конъюнктивы.
При одновременном применении нескольких глазных ЛС рекомендуется закладывать глазную мазь Декса-Гентамицин не ранее чем через 15 мин после использования глазных капель.
Длительность лечения препаратом Декса-Гентамицин обычно не превышает 2–3 нед .
Передозировка
При местном применении препарата Декса-Гентамицин глазная мазь передозировка маловероятна.
Особые указания
Влияние на способность управлять транспортными средствами и работать с механизмами. Сразу после закладывания глазной мази Декса-Гентамицин может возникнуть кратковременное нарушение остроты зрения, приводящее к замедлению психических и физических реакций. Поэтому не рекомендуется применять препарат непосредственно перед работой с механизмами и вождением автотранспорта. В течение 30 мин после аппликации необходимо воздерживаться от занятий, требующих повышенного внимания.
Форма выпуска
Мазь глазная. По 2,5 г в тубе алюминиевой с ПЭ-наконечником и навинчивающейся крышкой. 1 туба в картонной пачке.
Производитель
Урсафарм Арцнаймиттель ГмбХ. Индустриштрассе 35, 66129 Саарбрюкен, Германия.
Тел.: +49 (0) 6805-92 92-0.
Претензии по качеству препарата направлять по адресу представительства: 107996, Москва, ул. Гиляровского, 57, стр. 4.
Тел./факс: (495) 684-34-43.
Условия отпуска из аптек
Условия хранения препарата Декса-Гентамицин
Хранить в недоступном для детей месте.
Срок годности препарата Декса-Гентамицин
Не применять по истечении срока годности, указанного на упаковке.
Аннотация научной статьи по клинической медицине, автор научной работы — Кудрявцева А.В., Катосова Л.К., Балаболкин И.П., Асеева В.Г.
Авторы наблюдали 70 больных атопическим дерматитом (АД) в возрасте от 4 месяцев до 16 лет. В комплекс обследования больных включено определение общего IgE в сыворотке крови, постановка кожных скарификационных проб, бактериологические посевы с кожи и фекалий; у 5 больных исследовали специфический IgE к эндотоксинам А и В золотистого стафилококка (ЗС). ЗС выявлен на коже у 73% больных АД. Отмечена зависимость между тяжестью и характером поражения кожных покровов и степенью колонизации ЗС, а также между выраженностью обсеменения кожи ЗС и уровнем эозинофилов в периферической крови. У больных с тяжелым течением АД выявлены специфические IgE к стафилококковым эндотоксинам А и В.
Похожие темы научных работ по клинической медицине , автор научной работы — Кудрявцева А.В., Катосова Л.К., Балаболкин И.П., Асеева В.Г.
Role of Staphylococcus aureus in pediatric atopic dermatitis
Authors observed 70 patients with atopic dermatitis (AD) in the ade 4 months 16 years old. Complex examination included determination of total serum IgE, skin tests, skin and stool culture. Specific IgE-antibodies to Staphylococcus aureus (SA) A and В endotoxins were studied in 5 cases. SA skin culture was positive in 73% of patients with AD. Authors noted the dependence between skin lesion character and severity and degree of skin contamination by SA and between degree of skin contamination by SA and number of peripheral blood eosinophiles. Patients with severe AD had high level of specific IgE antibodies to staphylococcal A and В endotoxins.
А. В. Кудрявцева, Л. К. Катосова, И. И. Балаболкин, В. Г. Асеева
РОЛЬ ЗОЛОТИСТОГО СТАФИЛОКОККА ПРИ АТОПИЧЕСКОМ ДЕРМАТИТЕ У ДЕТЕЙ
НИИ педиатрии Научного центра здоровья детей РАМН (дир. акад. А. А. Баранов), Москва
Авторы наблюдали 70 больных атопическим дерматитом (АД) в возрасте от 4 месяцев до 16 лет. В комплекс обследования больных включено определение общего в сыворотке крови, постановка кожных скарификационных проб, бактериологические посевы с кожи и фекалий; у 5 больных исследовали специфический к эндотоксинам А и В золотистого стафилококка (ЗС). ЗС выявлен на коже у 73% больных АД. Отмечена зависимость между тяжестью и характером поражения кожных покровов и степенью колонизации ЗС, а также между выраженностью обсеменения кожи ЗС и уровнем эозинофилов в периферической крови. У больных с тяжелым течением АД выявлены специфические к стафилококковым эндотоксинам А и В.
2А В. Кудрявцева, Л. К. Катосова, И. И. Балаболкин, В. Г. Асеева
ПЕДИАТРИЯ № 6, 2003 г.
Authors observed 70 patients with atopic dermatitis (AD) in the ade 4 months —16 years old. Complex examination included determination of total serum IgE, skin tests, skin and stool culture. Specific IgE-antibodies to Staphylococcus aureus (SA) A and B endotoxins were studied in 5 cases. SA skin culture was positive in 73% of patients with AD. Authors noted the dependence between skin lesion character and severity and degree of skin contamination by SA and between degree of skin contamination by SA and number of peripheral blood eosinophiles. Patients with severe AD had high level of specific IgE antibodies to staphylococcal A and B endotoxins.
Атопический дерматит (АД) относится к числу хронических аллергических заболеваний кожи, характеризующихся упорным течением, часто торпид-ным к проведению традиционной терапии. Несмотря на большое количество научных исследований, проводящихся как в нашей стране, так и за рубежом, больших успехов в лечении этого заболевания достигнуть до настоящего времени не удалось.
Одной из причин, способствующих рецидивирующему, упорному течению АД, является колонизация на поверхности кожи золотистого стафилококка (ЗС), способного поддерживать воспаление и приводить к сенсибилизации организма. Как известно, этот микроорганизм относится к условно патогенной микрофлоре, однако при определенных условиях он способен не только образовывать очаги нагноения, но и поддерживать бактериальную сенсибилизацию и гиперпродукцию [1, 7]. По данным литерату-
ры, у 80—95% больных АД золотистый стафилококк является доминирующим микроорганизмом среди определяемых на пораженных участках кожи. Плотность его на непораженной коже у больных АД может достигать 107 КОЕ/см2 [4 — 6]. Продуцируя ряд токсинов (энтеротоксин А, энтеротоксин В, экс-фолиативный токсин и токсин стафилококкового шокового синдрома), обладающих достаточной молекулярной массой, чтобы выступать в качестве аллергенов, ЗС способен приводить к продукции специфических ]^Е. В научных исследованиях более чем у 50% больных этим заболеванием выявлены антитела к энтеротоксинам [5—7]. Наличие прямой корреляционной связи между тяжестью течения заболевания и численностью колоний ЗС, выделенных с кожи больных, а также выявление специфических 1§Е к энтеротоксинам А и В доказывают наличие влияния этого микроорганизма на течение АД.
Целый ряд научных работ как отечественных, так и зарубежных ученых посвящен изучению влияния ЗС на течение АД у детей и взрослых. Однако, несмотря на большое количество исследований, до настоящего времени не выработано определенного подхода к терапии АД с учетом роли золотистого стафилококка. Одни врачи склоняются в сторону применения наружных и системных антибиотиков, другие ограничиваются использованием антисептиков.
Цель нашей работы состояла в изучении роли ЗС в развитии, поддержании ободрения и утяжелении течения АД у детей и предложении некоторые подходов к терапии этого заболевания с учетом выявленных изменений.
Материалы и методы исследования
Было обследовано 70 детей, страдающих АД, возраст которых составил от 4 мес до 16 лет (средний возраст около 6,5 лет). В основном это были дети со среднетяжелым течением заболевания (62%), легкое течение отмечено в 14% случаев, тяжелое — в 24%. Только АД страдали 57 детей (81%), АД и бронхиальной астмой (БА) — 13 (19%). АД, осложненный пиодермией, отмечался у 3 больных. Еще у 6 пациентов в анамнезе были отмечены неоднократные эпизоды пиодермии неизвестной этиологии. При анализе тяжести течения БА выяснено, что чаще встречались случаи тяжелого течения болезни — 50% детей, реже среднетяжелого — 40% и в 10% случаев — легкого течения. Средняя продолжительность АД приблизительно совпадала со средним возрастом больных в связи с ранним дебютом болезни и составила 5,5 лет. Все дети поступали в отделение в период обострения АД и БА.
В контрольную группу вошли 10 детей с БА, не имеющие в анамнезе и во время исследования заболеваний кожи.
При изучении анамнеза болезни была выявлена наследственная отягощенность по аллергическим заболеваниям в 63% случаев, чаще по материнской линии (75%). Экссудативные изменения со стороны кожных покровов отмечались редко (10%) и только у детей младшей возрастной группы, у остальных изменения носили эритематозно-сквамозный характер, иногда, в основном у подростков, имелись очаги лихенификации. Средний показатель 8СОКАБ составлял 58,76 баллов.
Анализируя данные обследования детей с АД, было выявлено значительное увеличение абсолютного количества эозинофилов в периферической крови, при этом у детей с тяжелым и среднетяжелым течением заболевания отмечался достоверно более высо-
кий уровень эозинофилов, чем при легком течении (р Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Количество эозинофилов в периферической крови у больных атопическим дерматитом в зависимости от тяжести заболевания. 1 — легкий АД, 2 — среднетяжелый АД, 3 — АД.
Чувствительность к антибиотикам ЗС, выделенного с кожи
Атопический дерматит из-за своей высокой распространенности у детей, раннего начала и быстрого формирования хронических форм представляет собой одну из актуальнейших проблем педиатрии. Кожа больных атопическим дерматитом обсеменена различными микроорган
Атопический дерматит из-за своей высокой распространенности у детей, раннего начала и быстрого формирования хронических форм представляет собой одну из актуальнейших проблем педиатрии.
Кожа больных атопическим дерматитом обсеменена различными микроорганизмами (табл.1), количество которых значительно выше, чем на коже здоровых детей. Так, например, золотистый стафилококк (Staphylococcos aureus) высевается с кожи больных атопическим дерматитом в 80—100% случаев.
| Таблица 1. Основные представители микрофлоры кожи (по W. S. Noble, 1981) | |
| Грамположительные бактерии | Стафалококки, стрептококки, микрококки, дермобактер, пропионибактерии, коринеформные бактерии |
| Грамотрицательные бактерии | Протей, клебсиелла, эшерихия, псевдомонас |
| Дрожжеподобные грибы | Кандида, мalasseria furfur, родоторула |
| Вирусы | Герпес, паповавирусы, папалломавирусы |
| Микоплазмы | При ослабление организма |
В последние годы золотистому стафилококку отводят ключевую роль в механизмах развития атопического дерматита. Согласно распространенной в настоящее время гипотезе, возникновение этого заболевания объясняется колонизацией кожи золотистым стафилококком, секретирующим токсины-суперантигены, которые вызывают поликлональную активацию Т-лимфоцитов и макрофагов, продуцирующих провоспалительные цитокины и модулирующих развитие иммунного ответа при атопическом дерматите.
Суперантигены золотистого стафилококка, а также стрептококков, вирусов, микоплазм активируют Т-лимфоциты путем прямого взаимодействия с TCR-Vb-цепью и молекулами МНС II класса. Золотистый стафилококк вырабатывает суперантигены, представленные энтеротоксинами SEA-D и токсинами токсического шокового синдрома TSST-1. Они действуют не только как антигены, но и как аллергены, вызывая образование IgE-антител.
В сыворотке у 57% больных атопическим дерматитом были обнаружены специфические IgE-антитела к SEA, SEB, ТSSТ-1. Большинство из этих пациентов были носителями токсигенных штаммов S. аuereus. Обнаружено, что пациенты, страдающие атопическим дерматитом, сенсибилизированные к SEB, имели более высокую активность заболевания.
Присутствие экзотоксинов в коже провоцирует высвобождение биологически активных веществ (медиаторов) из тучных клеток и возникновение зуда, экскориаций. Токсины могут связывать специфические IgE-антитела на поверхности клеток Лангерганса, что ведет к дальнейшей активации специфических Т-клеток.
Штаммы S.auereus высвобождают не только токсины с активностью суперантигенов, но и термолабильные токсины, такие как a-токсин, известный как цитолизин, а также стимулируют высвобождение из них TNF-α, способных повреждать эпидермальные клетки.
Суперантигены золотистого стафилококка, проникая в эпидермис и дерму, вызывают у больных атопическим дерматитом повреждение поверхностных слоев липидов кожи и нарушение рогового слоя эпидермиса. Как только кожа больных атопическим дерматитом теряет кореальный слой, рецепторы дермального фибронектина открываются, что ведет к повышению адгезии золотистого стафилококка и плотности колонизации кожи, которая коррелирует с воспалением на коже. В итоге снижается антибактериальная активность кожных покровов, нарастает недостаточность местного иммунитета, что является одной из причин развития инфекции на коже. С другой стороны, стафилококковый энтеротоксин В, стимулируя Т-лимфоциты у больных атопическим дерматитом, усиливает экспрессию Fas-рецепторов, вызывает их апоптоз. Все это может индуцировать недостаточность клеточного иммунитета.
Недостаточность системного и местного иммунитета, наличие входных ворот из-за расчесывания вследствие кожного зуда и развития экскориаций, особенности состояния водно-липидной пленки и рогового слоя эпидермиса — это наиболее частая причина инфекционных осложнений атопического дерматита. Развитие инфекционных осложнений, имеющих бактериальную, вирусную и грибковую этиологию, является одной из особенностей атопического дерматита (табл. 2).
| Таблица 2. Бактериальные осложнения атопического дерматита (пиодермии) | |
| Стафилококковая инфекция кожи | Импетиго (остеофолликулит, фолликулит, фурункул, карбункул, везикулопустулез, абсцессы |
| Стрептококковая инфекция кожи | Импетиго (фликтена, вульгарная эктима, рожистое воспаление), "заеда" |
При осложнении кожи бактериальной инфекцией (пиодермией) процесс может иметь как локальный, так и распространенный характер.
Клинические особенности стафилококковых пиодермий определяются тем, что стафилококк обычно располагается в устье потовых, сальных, апокриновых желез и волосяных фолликулов. Первичным высыпным элементом стафилококковой инфекции является остеофолликулярная пустула. При распространении воспалительного процесса в глубину волосяного фолликула с захватом глубоко лежащих тканей развивается фолликулит — острое гнойное воспаление воронки сально-волосяного фолликула. Когда в процесс вовлекаются сальная железа и окружающая подкожно-жировая клетчатка, возникает фурункул. Наличие нескольких фурункулов расценивается как фурункулез. Примерами локальной инфекции, вызываемой золотистым стафилококком у детей старшего возраста, могут служить стафилогенное импетиго (остеофолликулит), фолликулит, фурункул, карбункул, гидроаденит. У новорожденных в силу анатомо-физиологических особенностей строения кожи и желез стафилококки вызывают развитие везикулопустулеза, множественные абсцессы.
Стафилококковое импетиго (остеофолликулит) проявляется на любом участке кожного покрова, где имеются пушковые, щетинистые или длинные волосы.
Фурункулы, карбункулы, гидроаденит — достаточно редко встречающиеся стафилококковые осложнения атопического дерматита, которые легко диагностируются по характерным клиническим признакам, течению процесса и своеобразной локализации.
Стафилококковый везикулопустулез у детей раннего возраста характеризуется возникновением диссеминированных поверхностных везикулопустул, наполненных серозным и серозно-гнойным содержимым. Высыпания располагаются на коже туловища, верхних и нижних конечностях, в области волосистой части головы, крупных складок. В течение нескольких дней появляются свежие гнойнички, постепенно подсыхающие в корочки. Процесс сопровождается субфебрильной температурой, недомоганием. У ослабленных детей инфекция легко распространяется по поверхности и в глубину, возможна трансформация в множественные абсцессы, флегмону.
Стрептококковые инфекции кожи — различные виды стрептококкового импетиго (фликтена, вульгарная эктима и рожистое воспаление).
Стрептококковое импетиго (фликтена) — самая распространенная форма стрептодермии у детей, отличается высокой контагиозностью. Первичным элементом являются пузырьки (фликтены) с прозрачным содержимым и дряблой покрышкой, имеется тенденция к их периферическому росту и слиянию. Размеры пузырьков варьируют от просяного зерна до горошины. В процессе эволюции фликтены подсыхают в тонкую серозную или серозно-гнойную корочку, расположенную на отечно-гиперемированном основании. Стрептококковое импетиго часто сопровождается зудом. Наиболее часто стрептококковое импетиго локализуется на открытых частях тела — лице, верхних конечностях, реже на туловище. При распространенном и выраженном процессе стрептодермия может скрывать кожные высыпания атопического дерматита.
Анулярный стоматит, заеда стрептококковой этиологии диагностируются при расположении в углах рта фликтен, которые быстро вскрываются, образуя розовые, слегка влажные эрозии или трещины с обрывками эпидермиса на периферии.
Стрептококковая инфекция кожи в основном имеет поверхностный характер. Однако могут развиться и более глубокие инфильтративные поражения. К ним относятся вульгарная эктима и рожистое воспаление, которые, однако, при атопическом дерматите наблюдаются достаточно редко.
Чаще всего при атопическом дерматите встречаются пиодермии смешанной стрептостафилококковой этиологии, среди них наиболее распространено вульгарное стрептостафилококковое импетиго.
Вульгарное стрептостафилококковое импетиго развивается после короткого продромального периода с легким повышением температуры и появлением чувства жжения в местах будущих высыпаний. На покрасневшей, слегка отечной коже возникает фликтена, содержимое которой быстро мутнеет. Через несколько часов содержимое пузырька становится гнойным. Покрышка пузырька вскрывается, образуя эрозию, а отделяемое пузырька ссыхается в желтоватые корки.
В ряде случаев при атопическом дерматите вторичная инфекция может быть связана с грамотрицательными палочками — Pseudomonas aeruginosa, реже Proteus. Они вызывают язвы, паронихии, инфекции межпальцевых промежутков.
При хронических паронихиях почти всегда отмечается сопутствующая инфекция Candida albicans, при которой поражается ногтевое ложе. Инфекция в межпальцевых промежутках, вызванная грамотрицательными бактериями, может оказаться довольно тяжелой. Характеризуется она сильным шелушением, мацерацией и гиперкератозом.
Наиболее частая разновидность вирусных осложнений атопического дерматита — герпес простой. Клиническая картина заболевания характеризуется появлением отечной эритемы различной степени интенсивности на любом участке кожных покровов и слизистых оболочек. На фоне эритемы быстро возникают сгруппированные пузырьки размером от 1 мм до 3—4 мм с напряженной покрышкой и серозными прозрачным содержимым. Количество элементов варьирует от единичных до нескольких десятков. При слиянии пузырьков образуются плоские, напряженные, многокамерные пузыри. Через несколько дней содержимое пузырьков мутнеет, они вскрываются с образованием эрозий. Через 3—5 дней на месте спавшихся пузырьков и эрозий образуются медово-желтые рыхлые корочки. Обычно герпес локализуется на коже лица (окружность рта, красная кайма губ, крылья носа, реже — кожа щек, ушных раковин, лба, век). Нередко высыпания герпеса наблюдаются на коже гениталий, ягодиц, бедер, поясницы, пальцев рук, на слизистой оболочке рта, глотки, небе, миндалинах, конъюнктиве. Характерным поражением слизистой оболочки полости рта является афта. Заболевание протекает по типу острого инфекционного процесса с повышением температуры и выраженным нарушением общего состояния. Отмечается увеличение региональных лимфатических узлов.
Среди герпетических осложнений АД следует выделить герпетиформную экзему Капоши — одну из наиболее тяжелых форм простого герпеса, которая часто развивается у детей с АД через 1—2 недели после контакта с больным герпесом. Проявляется она наличием сгруппированных, диссеминированных, эритематозно-пустулезных, булезных, папуловезикулезных или везикуло-пустулезных элементов с западением в центре. На слизистых оболочках образуются многочисленные афты. Болезнь протекает тяжело, с лихорадкой, явлениями интоксикации. У отдельных больных могут наблюдаться менингиальные явления, желудочно-кишечные расстройства, пневмонии, абсцессы на коже.
Наиболее частыми возбудителями грибковых инфекций кожи у детей с АД являются дерматофиты и дрожжеподобные грибы рода Candida. Они вызывают различные проявления кандидоза, среди которых выделяют поверхностный (интертригинозный) кандидоз кожи, кандидоз гладкой кожи, кандидоз углов рта, кандидозные онихии и паронихии, кандидозные поражения слизистых оболочек (молочница).
Поверхностный кандидоз характеризуется наличием эритематозно-отечных участков с везикулами, серопапулами и пустулами. Экссудативные элементы быстро вскрываются с образованием эрозий, имеющих белесоватый налет. В глубине складки имеются небольшие трещины и наблюдается скопление белесоватой кашицеобразной массы.
Кандидоз углов рта характеризуется появлением в углах рта шелушения, поперечных трещин, покрытых серозно-гнойными корочками, участков мацерации с серовато-белым.
Патогенез осложненных форм атопического дерматита тесно связан с состоянием иммунной системы организма ребенка. Многочисленные исследования показали, что иммунная недостаточность, нарушение рогового слоя и водно-липидной мантии эпидермиса, наличие входных ворот для инфекции, дисбаланс аутофлоры кожи с преобладанием золотистого стафилококка и кандида являются причинами развития инфекционных осложнений атопического дерматита.
Терапия атопического дерматита у детей является многокомпонентной. Она включает в себя этиотропную и патогенетическую терапию. Носит индивидуальный характер и зависит от возраста ребенка, тяжести и стадии заболевания, а также наличия сопутствующих системных и местных проявлений.
Этиотропная терапия АД заключается в элиминации причинно-значимых факторов или уменьшении контакта с ними. Неотъемлемой частью этиотропной терапии АД является организация рационального диетического питания. Хорошо продуманные фармакотерапия и наружная терапия являются залогом успешного лечения атопического дерматита у детей.
Терапия осложненных инфекцией форм атопического дерматита предусматривает использование системных и местных антимикробных средств.
Все поверхностные и ограниченные формы стрептостафилококковой инфекции требуют наружной терапии. Пиогенные элементы вскрываются, эрозии обрабатываются 1—2%-ным раствором анилиновых красителей, а затем применяются местные антибактериальные средства. Для этого используют наружно мази, содержащие эритромицин, линкомицин, гарамицин. Высокую терапевтическую эффективность при стрептостафилококковой инфекции оказывает мазь бактробан, предназначенная для местного применения. Бактробан воздействует также на грамотрицательные микроорганизмы. Мазь наносят на пораженный участок до 3 раз в сутки. Продолжительность курса лечения составляет до 10 дней.
Антибиотики местного действия при атопическом дерматите следует назначать в комбинации с топическими кортикостероидами. Это обусловлено тем, что монотерапия местными антибиотиками часто приводит к обострению воспалительного процесса и способствует развитию на поверхности кожи кандидозной флоры. Применение же комбинированных местных препаратов, содержащих антибиотики и кортикостероидные средства, обеспечивает более выраженный терапевтический эффект при осложненных инфекцией формах атопического дерматита (в зарубежной литературе это явление получило название стероидсберегающего эффекта. К таким комбинированным препаратам относят целестодерм с гарамицином, оксикорт, полькортолон ТС, дипрогент.
Как показали клинические исследования, S.aureus может быть элиминирован с кожи больных атопическим дерматитом только при использовании сильных топических кортикостероидов. Стимуляция Т-клеток может быть снижена антибиотиками со стероидсберегающим эффектом. В то же время лечение детей оральным цефтином в ходе двойного слепого плацебо-контролируемого исследования показало определенное снижение колонизации S.aureus, что, однако, не облегчало течения атопического дерматита.
При распространенных и глубоких пиодермиях назначается общее лечение. Если нет возможности определения чувствительности микрофлоры, назначаются антибиотики широкого спектра действия.
Препаратами первого выбора в отношении золотистого стафилококка являются оксациллин и цефалоспорины I поколения. При устойчивости этих антибиотиков к штаммам стафилококка используют амоксициллин/клавуланат. Однако у детей с атопическим дерматитом и при наличии у ребенка аллергии на препараты из группы пенициллинов они не применяются. В таких случаях назначают линкомицин или его синтетический аналог — кландомицин. При наличии метициллинрезистентных штаммов золотистого стафилококка применяют ванкомицин или рифампицин.
При стрептококковых инфекциях кожи назначают эритромицин, кландамицин или линкомицин. В легких случаях препараты назначают внутрь, при тяжелых — парентерально.
При инфекциях кожи, вызванных грамотрицательными бактериями, назначают пенициллины (амоксициллин/клавуланат), цефалоспорины III поколения. При необходимости их комбинируют с аминогликозидами II (гентамицин, тобрамицин) и III поколений (амикацин).
При назначении системных антибактериальных препаратов следует помнить о риске обострения кожного процесса и возможном развитии побочных реакций.
При кандидозной инфекции кожи местно назначается нистатиновая мазь или пимафуцин в виде 2%-ного крема 1—2 раза в день. Возможно применение и других местных препаратов — микозолон, микосептин, микоспор, тридерм. При распространенных формах используют противогрибковые препараты общего действия — нистатин, амфотерицин В, дифлюкан.
При сочетанном поражении кожи больных атопическим дерматитом S. aureus и Candida высокоэффективен многокомпонентный препарат тридерм, содержащий кортикостероид — бетаметазона дипропионат, антибиотик — гентамицин сульфат и фунгицид азольного ряда — клотримазол. Применение комбинированного препарата тридерма позволяет всегда быть уверенным в высокой эффективности лечения, учитывая тот факт, что использование при лечении больных с осложненным АД препаратов, в состав которых не входит антимикотик, часто ведет к активизации Candida, использование же только противогрибковых препаратов при кандидозной инфекции не исключает возможности развития пиококковых осложнений. Состав тридерма позволяет воздействовать и на бактериальную, и на грибковую инфекцию одновременно. Тридерм выпускается в форме мази и крема, назначается 2 раза в сутки, разрешен к применению у детей начиная с двухлетнего возраста.
Выбор препаратов с антимикробной активностью у детей с атопическим дерматитом должен осуществляться с учетом индивидуальной чувствительности и характера кожного процесса.
В. А. Ревякина, доктор медицинских наук, профессор
Научный центр здоровья детей РАМН
Читайте также:


