Чем отличается обычный стафилококк от золотистого стафилококка
Антибиотики прямо под нашим носом
Немецкие ученые обнаружили новое оружие для борьбы с больничным монстром – мультирезистентным золотистым стафилококком. Долгие годы оно скрывалось не в вечной мерзлоте или Марианской впадине, а прямо под нашим носом. Вернее – в нём.
В последние годы во всем мире увеличилось количество инфекционных заболеваний, вызванных устойчивыми к антибиотикам бактериями. Организмы с множественной лекарственной резистентностью (multidrug-resistant organisms, MDRO), такие как метициллин-резистентный золотистый стафилококк, нечувствительные к ванкомицину энтерококки или резистентные к цефалоспоринам третьего поколения грамотрицательные бактерии, в ближайшие десятилетия могут стать более частыми причинами смерти, чем рак [1].
Несколько лет назад удалось обнаружить, что представители человеческой микробиоты способны производить бактериоцины, поражающие близкородственных бактерий [2]. Например, в 2014 году из человеческого комменсала Lactobacillus gasseri выделили и описали новый синтезируемый рибосомами тиопептидный антибиотик – лактоциллин [3].
Немецкий исследователь Александр Ципперер со своими сотрудниками в июле 2016 года сообщил о том, что обнаружил в человеческом носу бактерию Staphylococcus lugdunensis IVK28, которая подавляет рост метициллин-резистентного золотистого стафилококка (methicillin-resistant Staphylococcus aureus, MRSA) [1].
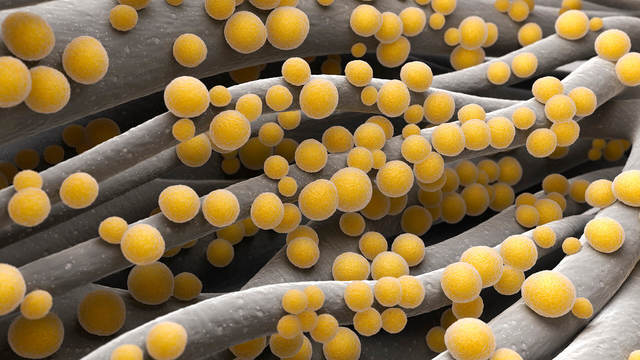
Стафилококки относятся к типичным бактериям-комменсалам, колонизирующим кожу и поверхности слизистых оболочек. Staphylococcus aureus – шаровидные грамположительные бактерии, вырабатывающие каротиноидный пигмент, который придает их клеткам золотистый цвет (рис. 1). Эти микроорганизмы чрезвычайно устойчивы к внешним воздействиям и выживают в воздухе, пыли, почве, продуктах питания, на оборудовании пищевых производств и предметах быта [6, 7].

Рисунок 1. Staphylococcus aureus и лейкоциты. Рисунок с сайта relatedscience.blogspot.ru.
Staphylococcus aureus – бактерия условно-патогенная, проявляющая свои патологические свойства только в благоприятных условиях, а создает их, как правило, ослабление иммунитета носителя. Активная жизнедеятельность стафилококка может привести к разнообразным заболеваниям [5, 7, 8]:
- кожи (прыщи, фурункулы, синдром ошпаренной кожи);
- органов дыхания (плеврит, пневмония);
- костной и соединительной тканей (артрит, остеомиелит);
- нервной системы и органов чувств (отит, менингит);
- сердечно-сосудистой системы (эндокардит, флебит, стафилококковая бактериемия).
Факторы патогенности S.aureus – это микрокапсула, компоненты клеточной стенки, ферменты агрессии и токсины. Микрокапсулы защищают клетки бактерий от фагоцитоза, способствуют их адгезии и распространению по организму хозяина. Составляющие клеточной стенки (например пептидогликан, тейхоевые кислоты и белок А) вызывают развитие воспаления, обездвиживают фагоциты и нейтрализуют иммуноглобулины. Коагулаза, главный фермент агрессии, вызывает свертывание плазмы крови [7, 9].
Наиболее опасны метициллин-резистентные стафилококки (methicillin-resistant S.aureus, MRSA) (рис. 2). Метициллин – это модифицированный пенициллин, с помощью которого еще недавно успешно боролись со стафилококковой инфекцией. MRSA устойчивы не только к метициллину, но и к другим антибиотикам пенициллиновой группы (диклоксациллину, оксациллину, нафциллину и др.), а также к цефалоспоринам.

Рисунок 2 (с сайта thinglink.com). Метициллин-резистентные золотистые стафилококки.
В последнее время выявлены штаммы и с более широким спектром устойчивости: ванкомицин-резистентные (VRSA) и гликопептид-резистентные (GISA) [6, 9, 10].
Штамм S.lugdunensis IVK28 эффективно боролся со своим вредоносным родственником лишь в условиях недостатка железа и только на твердых агаризованных средах (рис. 3, слева). Механизм противостояния был неясен, а потому Ципперер провел транспозонный мутагенез клеток выделенного штамма – чтобы выявить ген, ответственный за синтез смертельного для S.aureus вещества.

В итоге удалось получить мутанта IVK28, который не мог подавлять рост MRSA. Анализ места встройки транспозона показал, что тот нарушил структуру гена предполагаемой нерибосомной пептидсинтетазы (НРПС). Оказалось, что этот ген вместе с другими последовательностями, связанными с биосинтезом антибиотиков, входит в состав оперона размером 30 т.п.н. Это указывало на то, что предполагаемая молекула ингибитора может быть комплексом нерибосомных пептидов.
Оперон методом ПЦР обнаружили во всех культурах S.lugdunensis, а значит, он характерен для всего вида, а не только для штамма IVK28. Однако GC-состав оперона (26,9%) отличался от GC-состава остального генома S.lugdunensis (33,8%), что свидетельствовало о возможном заимствовании этого полезного генетического кластера у других видов бактерий – путем горизонтального переноса.
Оперон состоит из генов lugA, B, C и D, кодирующих пептидсинтетазные белки (см. врезку ниже), а также из других генов, чьи продукты необходимы для синтеза и транспорта нерибосомного пептида.
Чтобы окончательно вменить оперону участие в антибактериальной деятельности S.lugdunensis, наименьший ген (lugD) удалили. Мутант ΔlugD, как и ожидалось, не мог подавлять рост золотистого стафилококка, но когда в него ввели плазмиду с работающим геном lugD, агрессивный фенотип восстановился (рис. 3, в центре и справа).
Выделенный Ципперером продукт lug-оперона оказался нерибосомным циклическим пептидом, состоящим из пяти аминокислот (двух D-валинов, L-валина, D-лейцина и L-триптофана) и тиазолидинового гетероцикла (рис. 4). Назвали антибиотик лугдунином.

Химическим синтезом удалось получить продукт с идентичными природному лугдунину химическими свойствами и антибактериальным эффектом. Ученые предположили, что этот антибиотик ингибирует синтез бактериальных биополимеров – белков, ДНК и пептидогликанов [5].
Этот класс пептидов синтезируется в клетках низших грибов и бактерий без участия рибосом. Нерибосомные пептиды (НРП) также встречаются и у высших организмов, которые имеют бактерий-комменсалов [12].
НРП подразделяются на несколько функциональных групп [13]:
- антибиотики (ванкомицин);
- предшественники антибиотиков (ACV-трипептид – предшественник пенициллина и цефалоспорина);
- иммуносупрессоры (циклоспорин);
- противоопухолевые пептиды (блеомицин);
- сидерофоры (пиовердин);
- токсины (HC-токсин);
- сурфактанты (сурфактин).
Каждый модуль состоит как минимум из трех доменов:
- конденсирующего (принимающего пептидную цепь из предыдущего модуля);
- аденилирующего (выбирающего нужную аминокислоту);
- пептидильного (образующего пептидную связь).
Нередко модули включают и другие домены, в том числе эпимеризующий, который преобразует L-аминокислоты в D-формы [14].
По аналогии с триплетным рибосомным кодом для синтеза белка существует и нерибосомный, код НРПС, определяемый 10 остатками аминокислот в субстрат-связывающем кармане аденилирующего домена. От комбинации этих остатков зависит то, какая аминокислота будет встроена в пептид конкретным модулем НРПС. Зная этот код, можно предсказывать субстратную специфичность аденилирующих доменов и даже произвольно изменять ее посредством замены аминокислот в домене [14].
В экспериментах немецких ученых лугдунин действовал не только на метициллин-резистентных стафилококков, но и на гликопротеин-резистентных, и даже на других грамположительных бактерий типа листерии и ванкомицин-резистентного энтерококка (табл. 1). Минимальная ингибирующая концентрация (МИК) нового бактериоцина – 1,5–12 мкг × мл −1 , что говорит о высокой активности вещества. При этом такие концентрации никак не влияли на человеческую сыворотку, не вызывали лизис нейтрофилов или эритроцитов и не ингибировали метаболическую активность моноцитов. Бактериальные же клетки под действием лугдунина в концентрации даже ниже МИК прекращали синтезировать ДНК, РНК, белки и компоненты клеточной стенки. В этом отношении лугдунин напоминает даптомицин, дающий такой же эффект, но способ действия которого пока не изучен. Не было отмечено возникновения резистентности клеток S.aureus к лугдунину даже после их месячного выращивания на малых концентрациях.
| Виды и штаммы | Резистентность | МИК лугдунина (мкг × мл −1 ) | |||||
| Staphylococcus aureus USA300 (LAC) | MRSA | 1,5 | |||||
| + 50% человеческой сыворотки крови | 1,5 | ||||||
| Staphylococcus aureus USA300 (NRS384) | MRSA | 1,5 | |||||
| Staphylococcus aureus Mu50 | GISA | 3 | |||||
| Staphylococcus aureus SA113 | 3 | ||||||
| Staphylococcus aureus RN4220 | 3 | ||||||
| Enterococcus faecium BK463 | VRE | 3 | |||||
| Enterococcus faecalis VRE366 | VRE | 12 | |||||
| Listeria monocytogenes ATCC19118 | 6 | ||||||
| Streptococcus pneumoniae ATCC49619 | 1,5 | ||||||
| Bacillus subtilis 168 (trpC2) | 4 | ||||||
| Pseudomonas aeruginosa PAO1 | >50 | ||||||
| Escherichia coli DH5α | >50 | ||||||
| Условные обозначения: MRSA — метициллин-резистентные S. aureus; GISA — устойчивые к гликопротеинам S. aureus; VRE — ванкомицин-резистентные Enterococcus. Таблица из [1]. | |||||||
Испытания в боевых условиях
Как и полагается, способность лугдунина лечить стафилококковые инфекции продемонстрировали in vivo на мышиной модели (рис. 5). У шести мышей сбрили шерсть на спине и, повредив кожу многократным приклеиванием/отклеиванием пластыря, нанесли на это место золотистого стафилококка. Затем кожу обработали мазью, содержащей 1,5 мкг лугдунина, и спустя шесть часов оценили результат. Обработка новым антибиотиком сильно сокращала или даже полностью уничтожала популяцию S.aureus. Причем не только на поверхности кожи, но и в более глубоких ее слоях.

Рисунок 5. Общая схема подхода к идентификации природного антибиотика. Из бактериальных популяций человеческого тела отбирают представителей, которые не могут сосуществовать с интересующими патогенными бактериями. Этих возможных конкурентов тестируют по отдельности на средах с инфекционным агентом. Из культуры, успешно подавляющей рост патогенов, выделяют антибиотик, действие которого проверяют на животных моделях. Рисунок из [5], модифицирован и адаптирован.
Чтобы понять, может ли S.lugdunensis помешать колонизации носовой полости позвоночных животных золотистым стафилококком в естественных условиях, ученые провели следующий эксперимент. В носы хлопковых хомяков ввели два вида смешанных культур (S.aureus + S.lugdunensis IVK28 и S.aureus + S.lugdunensis IVK28ΔlugD) и каждую по отдельности. В контрольных случаях, когда вводили по одному штамму, все три культуры стабильно колонизировали носовую полость. Однако при введении смеси S.aureus + S.lugdunensis IVK28 количество золотистого стафилококка через 5 дней значительно уменьшилось по сравнению со смесью S.aureus + S.lugdunensis IVK28ΔlugD. Этот эксперимент показал, что продукция лугдунина позволяет штамму IVK28 эффективно конкурировать с золотистым стафилококком in vivo.
Оставалось разобраться, предотвращает ли присутствие S.lugdunensis в носу человека колонизацию бактериями S.aureus. Ципперер и его коллеги исследовали мазки из носовых ходов 187 госпитализированных больных. Из них у 60 человек (32,1%) обнаружили золотистого стафилококка и у 17 человек (9,1%) – S.lugdunensis. И только у одного пациента с S.lugdunensis в носу обитал S.aureus. У всех выделенных штаммов S.lugdunensis ПЦР-анализ продемонстрировал наличие lug-оперона, а все обнаруженные штаммы S.aureus оказались восприимчивы к лугдунину.
Лугдунин оказался первым обнаруженным бактериоцином нового класса – макроциклических тиазолидиновых пептидных антибиотиков. Все проверенные штаммы S.aureus (как природные, так и лабораторные) не смогли выработать резистентности к нему. Это дает надежду на то, что лугдунин в будущем станет коммерческим препаратом для борьбы с золотистым стафилококком.
И наконец, сам факт обнаружения нового антибиотика у представителя человеческой микробиоты должен послужить стимулом для активизации поиска других продуцентов бактериоцинов в составе именно таких сообществ. В дальнейшем это поможет медикам успешнее сдерживать наступление мультирезистентных патогенов.

Хотя новые антибиотики разрабатываются постоянно, пессимистично настроенные эксперты полагают, что выработка устойчивости к ним — это только вопрос времени.
Если верить официальной статистике, количество смертельных случаев от одной из наиболее опасных больничной инфекций — MRSA (метициллин-резистентного золотистого стафилококка) в последние годы значительно увеличилось, а число случаев заражения постоянно растет.
Что такое золотистый стафилококк (MRSA)?
Стафилококки – распространенное семейство бактерий. Они присутствуют у большинства людей и являются частью нормальной микрофлоры кожных покровов, слизистых оболочек и нижнего отдела кишечника. Носительство стафилококка часто встречается и у медицинского персонала.
Заражение стафилококком в больницах и роддомах происходит воздушно-капельным путем и через загрязненные руки медиков. Заразиться можно через открытые раны, ожоги, глаза, кожу, кровь. Возможна передача инфекции с инструментами, катетерами, перевязочным материалом, предметами ухода, а также пищей.
Для лечения MRSA необходимо применение более высокой дозы препаратов, увеличение длительности лечения или использование альтернативного антибактериального средства, к которому данный вид MRSA все еще чувствителен.
Инфицированность MRSA может вызывать широкий спектр симптомов в зависимости от органа, подвергшегося заражению. Признаками заражения являются краснота, отечность и болезненность инфицированного участка. Клинические проявления стафилококковых болезней многообразны – от заболеваний кожи и пневмонии до менингита и сепсиса.
Почему MRSA существует?
Естественный отбор до сих пор является основным принципом развития всего живого. А бактерии живут в этом мире намного дольше, чем мы, поэтому они особенно преуспели в этом. Кроме этого, гены бактерий постоянно видоизменяются, чтобы противостоять основному своему врагу — антибиотику.
Более слабые виды бактерий, столкнувшись с антибиотиком, погибают, в то время как более стойкие просто игнорируют лекарство. Это означает, что в следующий раз вы можете столкнуться уже со стафилококком, который удачно пережил встречу с антибиотиком, а, следовательно, приобрел устойчивость к нему.
Именно поэтому врачи всегда советуют пациентам пропивать весь курс антибиотиков до конца. Если пациент не заканчивает курс лечения, то большинство бактерий умирает, но не все. Выжившие приобретают резистентность (то есть устойчивость) к антибиотикам. А каждая последующая мутация только увеличивает способность бактерий к выживанию.
Применение огромного числа антибиотиков в больницах и роддомах вызывает огромное число мутаций стафилококка, тем самым увеличивая его устойчивость к лекарственным препаратам.
Почему это настолько опасно?
Тот факт, что в больницах стафилококком заражаются чаще, чем вне лечебных учреждений, можно объяснить.
- Во-первых, обитатели больниц обычно более слабы, чем остальное население, что делает их более уязвимыми для инфекции.
- Во-вторых, условия в больницах, где находится большое количество людей на небольших площадях, являются прекрасной средой для передачи инфекций. Инфицированность MRSA может быть очень опасна для ослабленных пациентов и новорожденных, особенно если ее вовремя не распознать и не вылечить правильными антибиотиками.
Каковы перспективы?
Сильную обеспокоенность у врачей вызывают сообщения об увеличении количества инфекций и смертельных случаев из-за MRSA. Может случиться так, что сформируется вид стафилококка, устойчивый ко всем антибиотикам. Уже существует VRSA или ванкомицин-резистентный Staphylococcus Aureus, устойчивый к ванкомицину. А в Великобритании зафиксирован GISA или гликопептид-резистентный Staphylococcus aureus, соответственно устойчивый к гликопептидам.
Хотя новые антибиотики разрабатываются постоянно, пессимистично настроенные эксперты полагают, что выработка устойчивости к ним — это только вопрос времени.
Одна из главных причин появления устойчивых к лекарствам микробов — злоупотребление антибиотиками. Сплошь и рядом встречается назначение врачом антибиотиков пациентам с вирусной инфекцией. При этом антибиотики не оказывают никакого эффекта на вирусы. Зато бактерии в организме от применения антибиотиков прекрасно себя чувствуют — мутируют и размножаются. Поэтому сейчас врачам рекомендовано сократить назначение антибиотиков.
Важным фактором в защите пациентов от MRSA является улучшение гигиенических условий больниц. Ручные осмотры в больницах в настоящее время приносят больше вреда, чем пользы, так как благодаря им разносится инфекция. Решением этой проблемы видится тщательная обработка рук после каждого пациента. Есть также предложение ввести в штат больниц специальную должность медсестры, ответственной за чистоту (в российских ЛПУ обычно эти обязанности возлагаются на старшую медсестру отделения).
Пока врачи ищут способ борьбы с MRSA, число инфицированных неуклонно растет. А многие эксперты сходятся во мнении, что может потребоваться очень крупное научное достижение, родственное открытию пенициллина, для того, чтобы люди получили возможность эффективно противостоять устойчивым бактериям.
МРЗС передается при непосредственном физическом контакте с бактериями. МРЗС также передается через предметы, зараженные человеком, являющимся носителем бактерий, такие как повязки, полотенца, постельное белье или спортивный инвентарь. Обычно бактерии не передаются через воздух. Однако они могут передаваться при непосредственном контакте с жидкостью, выделяемой при кашле или чихании. Если у вас кожная инфекция МРЗС, существует риск рецидива в будущем.
При подозрении на инфекцию МРЗС врач может сделать посев выделений из раны (wound culture) для подтверждения диагноза. При наличии абсцесса он может быть дренирован. Вероятно, вам будет назначен один или несколько антибиотиков, которые действуют на МРЗС.
Уход в домашних условиях
Принимайте антибиотики в точном соответствии с назначением. Даже если вы почувствовали себя лучше, не прекращайте принимать их, пока они не закончатся, или до тех пор, пока не получите указание прекратить их прием от своего лечащего врача.
Если вам была назначена мазь с антибиотиком, применяйте ее в соответствии с полученными указаниями.
В течение 5 дней ежедневно мойте все тело (от волосистой части головы до пальцев ног) специальным мылом. Два раза в день чистите ногти пальцев рук в течение 1 минуты щеткой со специальным мылом.
Раны должны быть закрыты чистыми и сухими повязками. Если повязки загрязнились, их необходимо заменить. Каждый раз, когда вы меняете повязку или касаетесь раны, тщательно мойте руки.
Если у вас наращенные ногти или лак на ногтях, их необходимо снять.
Если у вас диагностировано возможное заражение инфекцией МЗРМ, ваши близкие, живущие вместе с вами, подвержены более высокому риску наличия бактерий на коже или в носу, даже при отсутствии признаков инфекции. Бактерии необходимо удалить с кожи всех членов семьи одновременно, чтобы они не передавались от одного к другому. Проинструктируйте их, как следует удалить бактерии:
Члены семьи должны использовать специальное мыло, как описано выше.
Если у кого-либо из членов семьи имеется кожная инфекция, ее должен лечить врач. Чтобы вылечить инфекцию МРЗС, мытья не достаточно.
Очистите столешницы и детские игрушки.
Каждый член семьи должен пользоваться только своими предметами личного обихода, такими как зубные щетки или бритвенные станки. При этом пользоваться общими очками, тарелками и столовыми приборами разрешается.
Часто мойте руки простым мылом и теплой водой. Обязательно очищайте зоны под ногтями, между пальцами и запястья. Вытирайте руки одноразовыми полотенцами (например, бумажными). Если нет возможности воспользоваться мылом и водой, можно использовать антисептик для рук на основе спирта. Втирайте антисептик по всей поверхности рук, пальцев и запястий до полного высыхания.
Не пользуйтесь чужими предметами личного обихода, такими как полотенца, бритвенные станки, одежда или униформа. Стирайте постельное белье, полотенца и одежду в горячей воде со стиральным порошком. Устанавливайте для сушилки режим высокой температуры, чтобы убить оставшиеся бактерии.
Если вы посещаете тренажерный зал, до и после каждого применения протирайте инвентарь антисептиком на основе спирта. Также протирайте все ручки и места, за которые беретесь руками.
Если вы занимаетесь спортом, после каждой тренировки принимайте душ с обычным мылом. Каждый раз после душа используйте чистое полотенце.
Последующее наблюдение
Приходите на контрольные приемы, назначенные вашим врачом, или в соответствии с указаниями, полученными от наших сотрудников. Если был сделан посев выделений из раны, получите результаты в указанное время. Если в ваш курс лечения будут внесены какие-либо изменения, вам о них сообщат.
Если у вас был диагностирован МРЗС, в будущем вам необходимо будет сообщать медицинскому персоналу о том, что вы проходили лечение от этой инфекции.
Когда необходимо обратиться за медицинской помощью
В любом из следующих случаев обратитесь в обслуживающее вас медицинское учреждение:
Усиливающееся покраснение, опухание или боль
Красные полосы в коже вокруг раны
Слабость или головокружение
Появление гноя или выделений из раны
Температура выше 100,4 ºF (38,0 ºС) или в соответствии с указаниями вашего лечащего врача
Аннотация научной статьи по ветеринарным наукам, автор научной работы — Алексеева Надежда Борисовна, Челышева Галина Матвеевна
В обзорной работе рассмотрены способы санации стафилококковых бактерионосителей , рекомендуемые как действующими регламентирующими документами, так и другими средствами применяемыми официальной медициной.
Похожие темы научных работ по ветеринарным наукам , автор научной работы — Алексеева Надежда Борисовна, Челышева Галина Матвеевна
TO THE QUESTION OF HOW SANATION STAPHYLOCOCCAL BACILLICARRIERS
In a review paper discusses methods for remediation of staphylococcal bacteria carriers, as recommended by the regulations in force, as well as other means applied by official medicine.
АЛЕКСЕЕВА Н.Б., ЧЕЛЫШЕВА Г.М.
Минздрава России, г. Новокузнецк
К ВОПРОСУ О СПОСОБАХ САНАЦИИ СТАФИЛОКОККОВЫХ
В обзорной работе рассмотрены способы санации стафилококковых бактерионосителей, рекомендуемые как действующими регламентирующими документами, так и другими средствами применяемыми официальной медициной.
Ключевые слова: стафилококки; бактерионосители; факторы персистенции; санация.
ALEKSEEVA N.B., CHELYSHEVA G.M.
Novokuznetsk State Institute of Postgraduate Medicine, Novokuznetsk
TO THE QUESTION OF HOW SANATION STAPHYLOCOCCAL
In a review paper discusses methods for remediation of staphylococcal bacteria carriers, as recommended by the regulations in force, as well as other means applied by official medicine.
Key words: staphylococcus; bacillicarriers; factors of persistence; drainage.
АЛЕКСЕЕВА Надежда Борисовна,
654041, г. Новокузнецк, ул. Кузнецова, д. 35,
Тел: 8 (3843) 71-78-03. E-mail: mgzh@yandex.ru
Сведения об авторах:
ЧЕЛЫШЕВА Галина Матвеевна, канд. мед. наук, врач-бактериолог, ГБОУ ДПО НГИУВ Минздрава России, г. Новокузнецк, Россия.
Information about authors:
ALEKSEEVA Nadezhda Borisovna, doctor-bacteriologist, bacteriological laboratory, City Hospital N 2 of St. George the Victorious, Novokuznetsk, Russia.
CHELYSHEVA Galina Matveevna, candidate of medical sciences, doctor-bacteriologist, Novokuznetsk State Institute of Postgraduate Medicine, Novokuznetsk, Russia.
Стафилококки при нарушении функций нормофлоры или попадании в больших количествах заселяют кожу и слизистые на длительное время, при этом иммунная система не реагирует на их бессимптомное присутствие,
что приводит к хроническому носительству [2].
Бактерионосители являются основным источником гнойных стафилококковых инфекций, возникающих в акушерских и хирургических стационарах. Длительное переживание стафилококков и создание основы резидентного бактерионосительства обеспечивается факторами их перси-стенции (антилизоцимная, антиинтерфероновая, антикомплементарная активности).
Люди, которые работают в детских и медицинских учреждениях, обязаны два раза в год сдавать посев слизи или клеток эпителия из переднего отдела носа. При положительных результатах
АКТУАЛЬНЫЕ ВОПРОСЫ МЕДИЦИНЫ
(т.е. обнаружении стафилококка) должна быть проведена санация носоглотки, чтобы работник не являлся постоянным источником инфекции в коллективе. После санации посев на носительство стафилококка повторяют, стремясь добиться отрицательного результата. Поскольку возможны рецидивы носительства, плановые посевы проводятся каждые полгода. Как правило, санация приводит к хорошим ближайшим результатам, но со временем носительство возобновляется, поэтому лечение необходимо регулярно повторять [3].
По данным бактериологической лаборатории МЛПУ ГКБ № 2 среди обследованных на стафилококковое бактерионосительство в течение 2012-2013 годов (n = 3626 человек) выявлено 208 бактерионосителей (5,7 %).
Цель данного обзора — рассмотреть способы санации стафилококковых бактерионосителей, рекомендуемые как официальными материалами, так и другими антисептическими средствами, применяемыми официальной медициной.
Для эрадикации назофарингеального носи-тельства Staphylococcus aureus использовать антибиотики нежелательно по нескольким причинам: а) большое количество штаммов (до 80 %) образует различные р-лактамазы, которые разрушают пенициллины и цефалоспорины, эффективные в отношении стафилококков. Лишь несколько антибиотиков способны помочь в случае инфекции MRSA (метициллинрезистентных стафилококков), например, ванкомицин, тейкопланин, линезолид, фузидиевая кислота; б) кроме того, антибактериальные средства вызывают дисбактериоз — нарушение микробного равновесия на коже и слизистых. Это само по себе способствует распространению патогенных и условно-патогенных бактерий и росту грибов (молочница и др.).
В Методических рекомендациях [2] рекомендуются способы санации, основанные на снижении персистентного потенциала стафилококка. Предлагаемые средства отличаются от существующих [1] тем, что подавляя персистентные (патогенные) свойства возбудителя, затрудняют его паразитирование внутри клеток и, тем самым, повышают эффективность санации. К таким препаратам относятся следующие:
1) Санация масляным раствором витамина А, который является активным антиоксидантом, снижает патогенные свойства стафилококка (но не убивает его) и способствует заживлению слизистой. Эффективность 78 %.
2) Санация электролизным водным раствором гипохлорита натрия. Раствор получают путем электролиза обычного физиологического раствора. Образуется антисептик, обладающий антимикробным, детоксицирующим, иммуномодулирующим свойствами. Не вызывает дисбактериоза в носу. Противопоказаний нет. Эффективность 87 %.
3) Санация микроклиматом спелеошахты. Нахождение в естественной или искусственной пещере со стенами из определенных типов минералов. Снижает патогенные свойства стафилококка, укрепляет иммунитет. Рекомендуется для санации бактерионосителей, страдающих аллергическими заболеваниями. Противопоказаний нет. Эффективность 91 %.
4) Санация раствором фурацилина + отвар травы зверобоя + натрий-карбоксиметилцеллюло-зы (КМЦ). Фурацилин является антибактериальным компонентом, отвар травы зверобоя обладает высокой противостафилококковой активностью, уменьшает воспаление и усиливаете регенерацию тканей. Натрий-карбок-симетилцеллюлоза стабилизирует раствор. Метод высокоэффективен и безопасен для слизистой оболочки носа.
В вышеуказанном приказе Минздрава СССР № 720 от 31.07.1978 г. вместо антибиотиков для санации носителей золотистого стафилококка рекомендуется ряд антисептических средств:
1. Хлорофиллипт — является экстрактом из листьев эвкалипта. Оказывает антибактериальное действие в отношении антибиотикоустойчивых стафилококков, широко применяется и в настоящее время, однако способен вызывать аллергические реакции. Для санации но-сительства стафилококка в носу используют 2 %-ный масляный раствор хлорофиллипта, для санации зева его полощут 1 %-спиртовым раствором хлорофиллипта.
2. Риванол — используется в виде свежеприготовленного раствора (из таблеток) 1 : 5000. Малотоксичен, не вызывает раздражения.
3. Фурацилин — широко применяемый в хирургических отделениях антисептик. Не раздражает ткани. В последние годы появились сообщения о распространении устойчивых к нему стафилококков.
4. Лизоцим — эффективен только бактериальный лизоцим золотистого стафилококка в отношении коагулазоотрицательных видов. В России производство бактериальных лизоцимов не налажено.
5. Стафилококковый бактериофаг — обладает незначительной эффективностью в связи с циркуляцией во внутрибольничной среде устойчивых к нему штаммов стафилококков. Существуют также методы санации носителей
госпитальных штаммов стафилококка с помощью молочнокислых бактерий лактобактерий).
Современная фармацевтическая промышленность предлагает следующие средства для санации и лечения стафилококковых инфекций:
высокие химиотерапевтические концентрации.
4. Фузидерм — 2 %-ный крем (мазь), содержащий фузидиевую кислоту, которая подавляет стафилококк.
6. Улучшающие обмен веществ: линимент алоэ (мазь), является биогенным стимулятором. Обладает некоторой противомикробной активностью в отношении стафилококков и стрептококков.
Представленный перечень лекарственных препаратов, обладающих персистирующими, антибактериальными и иммуномодулирующими свойствами, для санации стафилококковых бактерионосителей, позволяет применять их отдельно и в комплексе друг с другом, а также при повторной санации заменять одни средства другими во избежание появления устойчивых штаммов стафилококка, что приводит к снижению или даже потере эффективности химиотерапии.
1. Инструкция по бактериологическому обследованию на выявление носителей патогенного стафилококка и проведению санации //Приложение к Приказу Минздрава СССР от 31.07. 1978 № 720.
2. Диагностика и санация стафилококковых бактерионосителей: метод. реком. //МЗ Российской Федерации. -6.04.2001.
3. Павлов, И.А. Современные лекарственные средства /Павлов И.А. - М., 2010. - 640 с.
2. Октенисепт — современный антисептик, применяется для обработки кожи и слизистых, в том числе и для санации носителей стафилококков. Содержит октенидиндигидрохлорид и 2-феноксиэтанол. Обычно не раздражает ткани и не мешает их заживлению. Воздействие достигается через 1 мин. и длится около 1 часа. Используется лишь для наружного применения. Не рекомендуется одновременное применение с йодсодержащими антисептиками. Разрешен беременным и детям.
3. Банеоцин — мазь для наружного применения, в которую входят 2 антибиотика — бацитра-цин и неомицин. Оба антибиотика обладают бактерицидным действием по отношению к стафилококку, усиливая друг друга. Антибиотики мази почти не всасываются из кожи и потому не оказывают системных побочных эффектов, но создают в коже и слизистых
Читайте также:


