Кардиомиопатия при вич инфекции





ВИЧ и СПИД
- ноль новых ВИЧ – инфекций;
- ноль смертей вследствие СПИДа

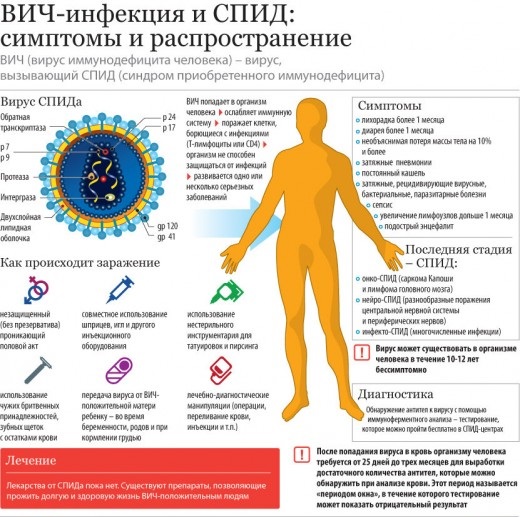
СПИД развивается в результате заражения людей вирусом иммунодефицита человека (ВИЧ). От момента инфицирования ВИЧ до развития заболевания с проявлениями СПИДа может пройти в среднем 5-15 лет. Во многом это время связано с исходным состоянием иммунной системы человека. Человек – вирусоноситель может продолжительное время неплохо себя чувствовать. Продолжительность жизни ВИЧ – инфицированных людей в последнее десятилетие возрастает в связи с применением новых действенных противовирусных и иммуномодулирующих препаратов.
Важно отметить, чтобы выявить ВИЧ, необходимо провести диагностику по анализу крови неоднократно, это связано с особенностями развития вируса.
ВИЧ и заболевания сердечно – сосудистой системы
В результате накопленного опыта по исследованию течения данной инфекции на значительном количестве пациентов были выявлены особенности воздействия ВИЧ на сердечно - сосудистую систему. Данное воздействие может быть прямым, непосредственным на клетки эндотелия. Из-за прогрессирующего снижения иммунитета возможно развитие аутоиммунных изменений тканей сердца и сосудов. В связи с увеличением продолжительности жизни и роста количества ВИЧ – инфицированных пациентов в средних и старших возрастных группах, развитию у них атеросклеротических изменений сердца и сосудов, возрастает необходимость профилактики и лечения сердечно – сосудистых заболеваний, присущих данной возрастной категории.
Болезни сердца у ВИЧ – инфицированных пациентов были сгруппированы Германской сетью по сердечной недостаточности в рабочую классификацию по морфологическому принципу:
- перикардит (вирусный, бактериальный, грибковый);
- опухоли (саркома Капоши, лимфома).
- ВИЧ – ассоциированная дилятационная кардиомиопатия;
- миокардит (острый, хронический);
- опухоли (саркома Капоши, лимфома);
- побочное действие лекарственных средств (особенно при противо – вирусной терапии).
- инфекционный эндокардит (бактериальный, грибковый);
- неинфекционный тромботический (марантический) эндокардит.
Профилактика поражений сердца при ВИЧ
Вопросы первичной профилактики общеизвестны и заключаются в исключении прямого контакта между кровью и поврежденными слизистыми оболочками каждого человека с ВИЧ - инфицированным человеком или материалом.
Своевременная постановка диагноза и раннее назначение действенной антиретровирусной терапии позволит длительно удержать разрушение иммунной системы ВИЧ – инфекцией.
При наличии сердечно – сосудистого заболевания важно проводить регулярные профилактические осмотры у кардиолога, т.к. в большинстве своем болезни системы кровообращения протекают преимущественно бессимптомно и начинают активно проявляться только в период развития осложнений. Иногда такие фатальные осложнения как инфаркт миокарда, инсульт, тяжелые нарушения ритма, тромбоэмболии становятся первым и последним проявлением заболевания.
Берегите себя и своих близких от заболеваний и их осложнений!
Производится перенаправление с сайта
Всероссийской акции по тестированию на ВИЧ-инфекцию

- Главная
- Образ жизни
- Сердечно-сосудистые заболевания у людей с ВИЧ. Способы профилактики

Какие заболевания относятся к сердечно-сосудистым?
Название этой группы заболеваний говорит само за себя. К ней относят болезни сердца и кровеносных сосудов, наиболее распространенными из которых являются:
· Ишемическая (коронарная) болезнь сердца – вследствие которой страдают кровеносные сосуды снабжающие кровь сердечную мышцу;
· Атеросклероз – поражает коронарную артерию, аорту и наиболее крупные ее ветви, включая почечные артерии.
· Гипертоническая болезнь – в результате которо, страдают сосуды, отвечающие за снабжение кровью головной мозг;
· Варикозное расширение вен – болезнь периферических артерий отвечающих за кровоснабжение сосудов рук и ног;
· Тромбоэмболия легких – закупорка сосудов легкого оторвавшимся тромбом;
· Ревмокардит – болезнь поражающая сердечные мышцы и клапаны;
· Врожденный порок сердца – деформации в строении сердца, существующие с рождения.
Причины развития ССЗ самые разные: неправильное питание, недостаточная физическая активность человека, наличие вредных привычек (курение, алкоголизм). Это относится и к ВИЧ-инфицированным, однако имеются данные о том, что ВИЧ-инфекция непосредственно связна с повышением риска развития ССЗ. Следовательно, при наличии ВИЧ-инфекции они развиваются чаще, но их достаточно просто предотвратить, придерживаясь здорового образа жизни, правильного питания и проходя регулярные клинические обследования.
Первые научные данные относительно связи болезней сердца и сосудов с ВИЧ были получены еще в середине 1990-х годов, когда начали появляться сообщения о проявлении инфаркта миокарда у молодых людей, инфицированных вирусом иммунодефицита человека.
Ранее уже было доказано негативное влияние ВИЧ-инфекции на работу сердечнососудистой системы, в частности, были изучены некоторые механизмы поражения сердечной мышцы:
- Осуществляется проникновение вируса в миокард через внутреннюю оболочку сосудов.
- В сердечной мышце происходит инфицирование ВИЧ находящихся там макрофагов и лимфоцитов. В результате этого начинаетcя воспалительная реакция за счет вовлечения в процесс других макрофагов и Т-лимфоцитов.
- Вирус быстро распространяется по миокарду и запускает процесс самоуничтожения – апоптоз – в результате чего кардиомиоциты начинают гибнуть.
Не так давно проводилось интересное исследование, результаты которого были опубликованы в Archives of Internal Medicine за апрель 2011 года. Основная цель его проведения заключалась в определении зависимости между ВИЧ-инфекцией и развитием первично диагностированной ишемической болезни сердца, которая нередко приводит к сердечной недостаточности. В исследовании участвовало 8486 человек, из которых 28,2% были ВИЧ-инфицированные. Полученные данные свидетельствовали о том, что при поражении вирусом иммунодефицита человека возрастает и риск развития сердечной недостаточности.
Сердечная недостаточность при ВИЧ чаще всего развивается по типу дилатационной кардиомиопатии. При данной патологии наблюдается снижение сократительной функции миокарда, а также его растяжение. Вследствие этого развиваются такие симптомы, как одышка, отеки при различной степени физической нагрузки. Тактика лечения и диагностики сердечной недостаточности у ВИЧ-инфицированных людей такая же, как у ВИЧ-негативных пациентов.
Перикардит у людей, живущих с ВИЧ
Данное заболевание относится к возможным осложнениям протекания ВИЧ-инфекции. В одних случаях развивается с выпотом, а в других с тампонадой сердца, то есть с полной остановкой его работы. Пока не была разработана эффективная антиретровирусная терапия (АРТ).
Перикардит может протекать с минимальным количеством клинических признаков. Для проведения диагностики используется эхокардиография, а если необходимо подтвердить диагноз, назначается магнитно-резонансная томография (МРТ) или компьютерная томография (КТ).
Различают тромботический и инфекционный эндокардит. Последний вид заболевания часто развивается у тех ВИЧ-инфицированных, которые употребляют наркотики, причем чаще всего затрагивается правосторонний клапан. Воспаление внутренней оболочки сердца приводит к изменениям внутренних структур органа, в результате чего развивается недостаточность одного или нескольких клапанов.
Эндокардит в 75% случаев вызывается золотистым стафилококком, хотя нередко участвуют пневмококки и гемофильная инфекция. Диагноз эндокардита чаще всего устанавливается на основе обследования пациента и результатов проведенных лабораторных и инструментальных исследований. С началом использования высокоактивной антиретровирусной терапии (ВААРТ) количество эндокардитов значительно уменьшилось.
Ишемическая болезнь сердца (ИБС)
Является болезнью кровеносных сосудов, которые снабжают кровью сердечную мышцу. Развитие данного заболевания при ВИЧ-инфекции связано с ранним атеросклерозом (Morgello, 2002). Стенки сосудов заметно ослабляются, а в сердечной мышце появляются участки ишемии, которые влияют на сократительную способность миокарда. В тяжелых случаях ИБС становится причиной развития инфаркта миокарда и внезапной остановки сердца.
Для постановки диагноза ИБС проводят физикальное обследование больного, электрокардиографию, экографию и исследуют лабораторные показатели. При необходимости делают функциональные пробы, когда используют различные нагрузочные тесты (беговую дорожку, велотренажер, степ тест).
Профилактика развития сердечно-сосудистых заболеваний у ВИЧ-инфицированных
В основном, профилактика ССЗ при ВИЧ-инфекции такая же, как и при ее отсутствии:
1. Правильное рациональное питание – следует обратить внимание на фрукты и овощи, рыбу и бобовые, блюда из нежирного мяса и цельного зерна. В небольших количествах можно употреблять соль, сахар.
2. Регулярные физические упражнения – для поддержания сердечнососудистой системы в оптимальном состоянии: следует регулярно хотя бы по полчаса делать физзарядку.
3. Отказ от вредных привычек – курение и алкоголь так же, как и сама ВИЧ-инфекция, значительно повышают риск развития ССЗ, в частности, инсульта и инфаркта. Поэтому если на протяжении года не употреблять табачные изделия, тогда риск развития ССЗ сразу снижается на 50%.
ВИЧ-инфицированным людям настоятельно рекомендуется знать свое артериальное давление, уровень сахара и липидов в крови, а также отслеживать вирусную нагрузку в организме. Тогда станет возможным значительно снизить риск развития сердечно-сосудистых заболеваний и жить активной, полноценной жизнью.

Количество людей на Земле, живущих с инфекцией, вызванной вирусом иммунодефицита (ВИЧ), превышает 40 млн. В России — 350 тыс. человек. К сожалению, распространенность алкоголизма среди ВИЧ-инфицированных лиц очень высока, что порождает ряд дополнительных медицинских и социальных проблем. Отдельно следует отметить тот факт, что действие алкоголя на сердце на фоне ВИЧ-инфекции продолжает оставаться неизученным.
Однако более значительными являются болезни сердца. Среди мужчин 35 — 74 лет смертность от сердечно-сосудистых заболеваний приближается к 1 200 на 100 тыс, что в 6 раз больше чем, например, в Австралии, Франции, Японии. За год из-за болезней сердца наша страна теряет около миллиона человек. Демографические потери, обусловленные болезнями сердца, сопоставимы с человеческими потерями военного времени.
Как ни странно, болезни сердца постепенно становятся значительной проблемой и при лечении ВИЧ-инфицированных пациентов. Дело в том, что внедрение агрессивных схем антиретровирусной терапии в клиническую практику ведет к столь значительному продлению их жизни, что примерно у половины таких пациентов успевает развиться обусловленное ВИЧ-инфекцией поражение сердца.
В свете эпидемиологических данных о пользе потребления алкоголя в малых количествах для сердечно-сосудистого здоровья, эти проблемы видятся еще более сложными.
Наше исследование было направлено на то, чтобы размотать тугой клубок, состоящий из трех смежных проблем:
• Какие конкретные молекулярные механизмы запускают развитие алкогольной и ВИЧ-ассоциированной болезней сердца?
• К каким последствиям приводит употребление алкоголя на фоне хронической ВИЧ-инфекции?
• Каким образом можно ограничить повреждение миокарда, вызванное алкоголем?
Алкоголь и сердце
Однако зависимость между уровнем потребления алкоголя и смертностью является J-образной. Это значит, что уже при незначительном превышении суточной дозы в 1-2 дринка даже несколько раз в месяц смертность, в том числе и сердечно-сосудистая, начинает прогрессивно возрастать. Именно поэтому мы не можем в условиях отсутствия культуры пития в России широко рекомендовать употребление алкоголя в качестве профилактической меры.
В токсических дозах алкоголь оказывает депрессивное действие на миокард. Самые ранние стадии дебюта алкогольной болезни сердца сегодня продолжают оставаться малоизученными.
Как показывают последние исследования, ключевое значение здесь принадлежит упоминавшемуся выше оксидативному стрессу.
Интересно, что сердечная недостаточность в данном случае оказывается полностью обратимой при прекращении приема алкоголя.
ВИЧ и сердце
Несмотря на то, что болезни сердца не являются превалирующей проблемой среди пациентов с ВИЧ-инфекцией, в молодом возрасте, по данным аутопсии, более 50% таких пациентов демонстрируют повреждение миокарда той или иной степени. С одной стороны, высокоэффективная артиретровирусная терапия снижает риск развития ВИЧ-ассоциированной патологии сердечно-сосудистой системы. С другой стороны, в случае развития болезни сердца уже на фоне антиретровирусного лечения хороший эффект наблюдается при отмене ретровирусной терапии и начале лечения сердечной недостаточности.
Точные механизмы дебюта болезни сердца, вызванной ВИЧ, остаются малоизученными. На сегодняшний день известны лишь основные звенья этого процесса:
2. Оказавшись в миокарде, ВИЧ инфицирует расположенные вокруг сосудов макрофаги и лимфоциты, что вызывает выброс из них сигнальных молекул цитокинов, которые усиливают миграцию дополнительного количества воспалительных клеток, макрофагов и Т-лимфоцитов.
3. Инфицированные макрофаги и лимфоциты являются источниками новых частиц вируса, а также фактора некроза опухоли, который запускает программу самоуничтожения — апоптоза — клеток сердца кардиомиоцитов и дебюту сердечной недостаточности.
ВИЧ-трансгенные животные как новая биологическая модель
Одним из самых сложных этапов представлялся поиск модели, на которой можно подобный эксперимент поставить, так как изучение патогенеза вызванного ВИЧ повреждения органов у людей во многом ограничивается этическими обстоятельствами. Длительное время наиболее приемлемой моделью изучения такого рода поражения была лентивирусная инфекция у приматов, которая очень похожа на ВИЧ-инфекцию у людей. Однако определенные различия в физиологии, течении инфекции и высокая дороговизна методики делали ее не удобной в широком практическом использовании.
Многие аспекты ВИЧ-инфекции оказались бы раскрытыми значительно позже, однако не так давно были получены трансгенные животные, несущие гены вируса иммунодефицита человека. В геном мышей и крыс были искусственно встроены все гены ВИЧ-1, кроме критически необходимых для развития реального инфекционного процесса генов gag и pol. Это исключает возможность заражения при работа с такими ВИЧ-трансгенными животными.
Новая уникальная модель ВИЧ-трансгенных крыс Sprague-Dawley оказалась одной из самых удачных для изучения ВИЧ-ассоциированной патологии. У данных животных наблюдается высокий уровень продукции вирусных белков, включая gp 120, в миокарде и других тканях. Исследования, посвященные изучению патологии сердечных и скелетных мышц ВИЧ-трансгенных крыс, показали сходство их повреждений с таковыми выявляемыми у ВИЧ-инфицированных людей.
Атрогин-1 и путь деградации белков
И в случае алкогольной, и в случае ВИЧ-обусловленной болезней сердца одним из наиболее важных моментов является атрофия сердечной мышцы. Стенки сердца истончаются, при этом размеры полости напротив увеличиваются. Первостепенное значение здесь имеет дисбаланс между синтезом и деградацией сердечных белков. Что же приводит к тому, что распад белков сердца начинает преобладать над их синтезом? Рассмотрим здесь судьбу белков в клетке сердца подробнее (рис 1.).
Рисунок 1. Жизненный путь белков в клетке (подробнее — в тескте).
Таким образом получается, что необратимо поврежденные белки, структуру которых уже невозможно восстановить, за счет специальных сшивающих молекул помечаются убиквитином и затем отправляются в протеасому для разрушения. Одной из таких метящих молекул является атрогин-1, который был открыт в 2001 году в скелетных мышцах. Было показано, что атрогин-1 участвует в развитии мышечных дистрофий, так как увеличение синтеза атрогина-1 ведет к более быстрому разрушению белков клетки.
В последствии оказалось, что и в сердце атрогин-1 играет сходную роль и соответственно является важным фактором регуляции баланса между сердечной гипертрофией и атрофией.
Однако до последнего времени не было получено экспериментальных свидетельств о росте уровня атрогина-1 в условиях хронической алкогольной интоксикации и ВИЧ-инфекции. Заметим, что на сегодняшний день отсутствуют и фармакологические агенты, способные влиять на систему деградации сердечных протеинов.
ВИЧ и алкоголь: что общего? Эксперимент первый
Наша гипотеза состояла в том, что массивное разрушение белков миокарда и, в итоге, атрофия сердечной мышцы в случае избыточного приема алкоголя и/или ВИЧ-инфекции обусловливается активацией каскада деградации белков, связанного с атрогином-1.
Но, в первую очередь, предстояло узнать, развилось ли у наших трансгенных и алкоголизированных крыс повреждение миокарда?
После анализа специально окрашенных полутонких срезов у ВИЧ-трансгенных крыс выявлялся значимое замещение сердечных мышечных клеток элементами соединительной ткани, признаки атрофии отдельных кардиомиоцитов и хаотичность их расположения, особенно выраженные в группе ВИЧ+алкоголь. В одном из образцов из последней группы выявлялась инфильтрация миокарда лимфоцитами. Эти изменения являются характерными и для ВИЧ-ассоциированной болезни сердца у человека. Сердца экспериментальных животных, после поправки на массу тела, весили больше контрольных, что также может свидетельствовать о развившемся повреждении миокарда. Таким образом, нашу модель можно было признать вполне адекватной.
Для того чтобы определить различия в экспрессии гена атрогина-1 в сердцах забитых экспериментальных животных, мы использовали метод полимеразной цепной реакции в режиме реального времени (RT-ПЦР). Этот высокотехнологическое и довольно непростое в практическом воплощении исследование позволяет количественно оценить активность работы — степень экспрессии — интересующих генов в любой ткани, в том числе и в сердечной мышце.
После проведения сравнительного анализа уровней экспрессии гена атрогина-1 с использованием RT-ПЦР выяснилось, что статистически достоверно экспрессия атрогина-1 была в 5 раз выше в группе алкоголя, в ≈14 раз выше — в группе ВИЧ и в ≈32 раза выше в группе ВИЧ + алкоголь, в сравнении с группой контроля (р
Но только ли рост концентрации необратимо поврежденных алкоголем и продуктами его метаболизма белков взывает столь значительное увеличение атрогина-1?
TGF β и миокард. Эксперимент второй
Как мы уже указывали, важным компонентом миокардиопатий является замещение клеток сердечной мышечной ткани клетками соединительной с нарушением структуры миокарда, другими словами миокардиальный фиброз, который и наблюдался у наших животных, получавших алкоголь, и несущих гены ВИЧ-1.
Существует множество концепций, объясняющих возникновение фиброза миокарда при избытке в крови алкоголя. Однако вклад в данный процесс такого мощного вызывающего фиброз фактора, как трансформирующий фактор роста β (TGF β) в случае индуцированной алкоголем болезни сердца, до сих пор не был оценен. Интересно, что, будто двуликий Янус, TGF β с одной стороны вызывает фиброз миокарда, а с другой — защищает сосуды сердца от атеросклероза.
Недавно выяснилось, что продукция атрогина-1 в сердце регулируется именно TGF β, на котором мы и сфокусировали свое внимание во втором эксперименте. Применение метода ПЦР в режиме реального времени показало, что, в действительности, экспрессия мРНК TGF β1 была статистически достоверно в ≈ 5 раз выше в группе животных, получавших алкоголь (p
Можно ли предотвратить повреждение миокарда? Эксперимент третий
Сам по себе глутатион не очень удобен в использовании, но у него есть аминокислота-предшественник процистеин. После всасывания в кишечнике он легко превращается в тканях в мощный антиоксидант глутатион. Примечательно, что процистеин обладает очень хорошим профилем переносимости и безопасности. Введение его в рацион питания способно значимо снижать уровень оксидативного стресса. Мы предположили, что добавление процистеина в диету экспериментальных животных может способствовать ограничению вызывемого алкоголем повреждения сердца.
Как выяснилось после постановки дополнительного эксперимента, добавление процистеина в диету крыс, получавших алкоголь в течение 6-ти недель, снижало в 6 раз уровень экспрессии атрогина-1 (p
Что дальше?
Открытые изменения уровня мРНК атрогина и TGF β, по всей видимости, представляют собой маленький фрагмент сложной мозаики патогенеза кардиомиопатий. Важность атрогин-1-зависимого пути деградации белков скелетных и сердечных мышц была определена совсем недавно. Атрогин-1, очевидно, является ключевым фактором, определяющим в миокарде баланс между атрофией и гипертрофией. Возросшие уровни атрогина-1 могут вести к увеличению скорости маркировки белков убиквитином белков, эндоцитозу β-адренорецепторов и потере белка, что может являть собой начало прогрессирования атрофии сердца. Возможно, и сам феномен дилатации камер сердца (при отсутствии утолщения его стенок) при алкогольной кардиомиопатии может объясняться именно возросшими уровнями атрогина-1. В то же время, фиброз миокарда может быть обусловлен возросшими уровнями TGF β, одновременно имеющего как антиатеросклеротическую, так и профибротическую активность (рис. 2).
Рис. 2. Возможный механизм ВИЧ/алкоголь-ассоциированного поражения миокарда и скелетных мышц. Алкоголь и экспрессия белков ВИЧ могут вести к индукции генов атрогина-1, что, в свою очередь, запускает каскад TGF β. Увеличение продукции TGF β (а возможно, и атрогина-1) может обусловливать миокардиальный фиброз и повреждение кардиомиоцитов).
Клинически, у лиц, употребляющих алкоголь, коронарное русло зачастую оказывается минимально пораженным атеросклерозом, в то время как частота развития нарушения ритма сердца и алкогольной болезни сердца заметно выше.
Тут мы вплотную подходим к необходимости разграничения действия алкоголя на защитное в отношении сосудов сердца и губительное для сердечной мышцы. Именно активация каскада атрогин-1/TGF β при хроническом употреблении алкоголя может защищать коронарные сосуды и, в то же время, вести к развитию кардиомиопатии.
Оксидативный стресс принимает прямое участие в реализации пагубных эффектов алкоголя. Как было показано в нашей работе, добавление в диету крыс, получающих алкоголь, процистеина может статистически достоверно снижать уровень экспрессии атрогина-1, возможно, за счет ограничения свободнорадикального повреждения.
Мы постарались комплексно исследовать один из фрагментов сложной мозаики ВИЧ/алкоголь-ассоциированных поражений миокарда. По результатам работы удалось найти новый значимый путь патогенеза ВИЧ/алкоголь-ассоциированного поражения миокарда и затормозить его развитие посредством процистеина, мощного агента, ограничивающего уровень оксидативного стресса.
Мы впервые, по нашим сведениям, продемонстрировали, что молекулярный каскад атрогин-1/TGF β, ассоциированный с миокардиальным фиброзом и деградацией пула протеинов, играет одну из ключевых ролей на ранних стадиях развития алкогольной кардиомиопатии и ВИЧ-кардиомиопатии. Определяемая с помощью ПЦР реального времени экспрессия атрогина I и TGF β оказывается выше в экспериментальных группах животных с ВИЧ и получавших алкоголь крыс в сравнении с группами контроля.
Мы показали, что поражение миокарда наиболее выражено при сочетании ВИЧ и алкоголя. Эта группа характеризуется наиболее высокими уровнями экспрессии мРНК атрогина I и TGF β, а также высокой фракцией фиброза, при окрашивании по три-хром.
Введение в рацион питания грызунов процистеина снижает уровень экспрессии атрогина-1, что потенциально может противостоять развитию и прогрессированию алкогольной кардиомиопатии, в особенности в условиях хронической ВИЧ-инфекции. Дальнейшие клинические испытания агентов, способных снижать уровень оксидативного стресса, могут стать ключом к решению проблемы поиска эффективного специфического лечения вторичных кардиомиопатий.
Примечание
Результаты исследования носят сугубо научный характер и не могут быть использованы при принятии каких-либо решений в сфере медицины и при консультировании. В настоящее время отсутствуют доказательные клинические исследования, в которых бы было показано положительное влияние антиоксидантов на прогноз. Также автор предостерегает пациентов от применения БАД, в том числе и содержащих антиоксиданты, равно как и алкоголя.
Литература:
Ashikhmin Y.I. ; J.S. Otis; D.M. Guidot Alcohol Induces The Expression Of Atrogin-1, An E3 Ligase Implicated In Muscle Atrophy, In The Myocardium Of Hiv-1 Transgenic And Wild Type Rats RSoA Meeting, Chikago, 2007 (accepted for poster presentation)
Bdolah Y. et al The atrophy-related ubiquitin ligases atrogin-1 and MuRF-1 are associated with uterine smooth muscle involution in the post partum period Am J Physiol Regul Integr Comp Physiol (September 28, 2006).
Cotter Bruno R. Epidemiology of HIV Cardiac Disease Progress in Cardiovascular Diseases, Vol. 45, No. 4, (January/February) 2003: pp 319-326
Dakin C. et al. HAART to Heart HIV-related Cardiomyopathy and Other Cardiovascular Complications AACN Clinical Issues Volume 17, Number 1, pp. 18–29 °C 2006
Fleming M. F., Krupitsky E. Alcohol and drug use disorders, HIV status and drug resistance in a sample of Russian TB patients Int J Tuberc Lung Dis. 2006 May; 10(5): 565–570. mortality in Novosibirsk, Russia: a prospective cohort study. Lancet 2002; 360: 1448-1454.
Pearson T.A., Terry P. What to advice patients about drinking alcohol: the clinician’s conundrum. JAMA.1994; 272:967-968. Editorial.
Pearson T.A. Alcohol and Heart Disease Circulation. 94:3023-3025, 1996
Reid W. et al. HIV-1 transgenic rat that develops HIV-related pathology and immunologic dyfunction. Proc Natl Acad Sci USA 2001; 98:9271–9276.
Thomas D. Stamos
, MD, University of Illinois at Chicago
Last full review/revision December 2018 by Thomas D. Stamos, MD


Кардиомиопатия является первичным заболеванием сердечной мышцы (см. также Обзор кардиомиопатий [Overview of Cardiomyopathies]).
Патофизиология
Как первичное заболевание миокарда, дисфункция сердечной мышцы при дилатационной кардиомиопатии возникает при отсутствии других расстройств, которые могут вызвать расширение миокарда, таких как тяжелая ишемическая болезнь сердца, или патологий, включающих перегрузку желудочка вследствие изменения давления или объема (например, гипертония, заболевания клапанов сердца). Предполагают, что у некоторых пациентов дилатационная кардиомиопатия начинается с острого миокардита (вероятно, вирусного в большинстве случаев), сопровождающегося вариабельной латентной фазой, фазой диффузного некроза кардиомиоцитов (вследствие аутоиммунной реакции на поврежденные вирусом миоциты) и хроническим фиброзом. Независимо от причины миокард дилатируется, истончается и компенсаторно гипертрофируется (см. рисунок Типы кардиомиопатии [Forms of cardiomyopathy]), что часто приводит к функциональной митральной регургитации или трикуспидальной регургитации, а также расширению предсердий.
У большинства пациентов поражается оба желудочка, в ряде случаев только левый желудочек (ЛЖ) (не ишемического происхождения) и намного реже - правый желудочек (ПЖ).
Формирование пристеночных тромбов может начаться сразу, как только дилатация камер сердца достигает значительного размера, особенно во время острой фазы миокардита. Сердечные тахиаритмии нередко осложняют течение острого миокардита и позднюю фазу хронической дилатации, возможно развитие атриовентрикулярной блокады. Вследствие дилатации левого предсердия часто возникает фибрилляция предсердий.
Этиология
Дилатационная кардиомиопатия имеет много известных и, вероятно, много неизученных причин (см. таблицу Причины дилатационной кардиомиопатии [Causes of Dilated Cardiomyopathy]). Более 20 вирусов могут вызвать дилатационную кардиомиопатию. В зонах умеренного климата вирус Коксаки группы В наиболее распространен. В Центральной и Южной Америке наиболее частой причиной инфекционного происхождения является болезнь Шагаса, вызываемая Trypanosoma cruzi, хотя она обуславливает только 10% случаев сердечной недостаточности в последнее время. Дилатационная кардиомиопатия все чаще встречается среди больных с активной ВИЧ-инфекцией.
Другие причины включают длительную тахикардию, токсоплазмоз, тиреотоксикоз и болезнь бери-бери. Многие токсичные вещества, особенно алкоголь, различные органические растворители, железо или ионы тяжелых металлов и определенные химиотерапевтические препараты (например, доксорубицин, трастузумаб), вызывают поражение сердца. Частый эктопический желудочковый ритм (> 10000 желудочковых экстрасистол в день) связан с левожелудочковой систолической дисфункцией.
Внезапный эмоциональный стресс и другие гиперадренергические состояния могут приводить к острой дилатационной кардиомиопатии, которая обычно обратима (как например та, что вызвана длительной тахикардией). Примером является острая верхушечная баллонная кардиомиопатия (кардиомиопатия такоцубо). При этом заболевании поражается верхушка, а иногда и другие отделы ЛЖ, вызывая регионарную дисфункцию стенки и в некоторых случаях фокальную дилатацию (баллонирование).
Генетические факторы имеют значение в 20–35% случаях; известны более 60 генов и локусов, связанных с развитием заболевания.
Частая вентрикулярная эктопия
Неконтролируемая фибрилляция предсердий или другая стойкая тахиаритмия
Заболевания соединительной ткани
Лекарственные препараты и токсины
Психофармакологические препараты (трициклические и квадрициклические антидепрессанты, фенотиазин)
Наследственные заболевания у 20-30% пациентов: аутосомно-доминантный, X-сцепленный, аутосомно-рецессивный или митохондриальный тип наследования
Гранулематозный или гигантоклеточный миокардит
Врожденные нервномышечные или неврологические заболевания
Мышечная дистрофия Дюшенна
Врожденная миотония Эмери
Лице-лопаточно-плечевая мышечная дистрофия
Инфекции (острые или хронические)
Вирусная (включая ВИЧ-инфекцию)
Нарушения обмена веществ
Наследственные болезни накопления
Нарушения питания (например, бери-бери, дефицит селена , дефицит карнитина, квашиоркор)
Беременность (перипартальный период)
Некоторые гормонально-активные опухоли (например, феохромоцитома, опухоли надпочечников, опухоли щитовидной железы)
Клинические проявления
Начало дилатационной кардиомиопатии обычно постепенное, за исключением случаев острого миокардита, острой апикальной баллонной дилатации и тахизависимой кардиомиопатии. Приблизительно 25% всех пациентов с дилатационной кардиомиопатией отмечают нетипичную боль в груди. Другие симптомы зависят от того, какой желудочек поражен.
Дисфункция левого желудочка вызывает одышку при физической нагрузке, а также усталость вследствие повышенного диастолического давления в ЛЖ и низкого сердечного выброса.
Недостаточность правого желудочка приводит к периферическим отекам и набуханию вен шеи. Иногда у молодых людей преимущественно поражается ПЖ с типичным развитием предсердных аритмий и внезапной смерти из-за злокачественных желудочковых тахиаритмий.
Диагностика
Рентгенография грудной клетки
Эндомиокардиальная биопсия (отдельные случаи)
Выяснение причины, если необходимо
Диагноз дилатационной кардиомиопатии ставится на основании анамнеза, данных объективного обследования, при исключении других частых причин желудочковой недостаточности (к примеру, системной гипертензии, первичного поражения клапанов, инфаркта миокарда—см. таблицу Диагностика и лечение кардиомиопатии [Diagnosis and Treatment of Cardiomyopathies]). Требуется проведение рентгенографии грудной клетки, ЭКГ, эхокардиографии и, с некоторых пор, МРТ сердца. В отдельных случаях проводится биопсия эндокарда.
При наличии острых симптомов или болей в грудной клетке необходимо определение сывороточных сердечных маркеров. Несмотря на то, что обычно повышение уровня тропонина свидетельствует о коронарной ишемии, повышение его уровня может также наблюдаться при сердечной недостаточности, особенно если функция почек снижена. При сердечной недостаточности также повышен уровень сывороточного натрийуретического пептида.
Проводят выявление возможных специфических причин (см. в других разделах Р у к оводства ). Если специфическая, клинически выраженная причина отсутствует, необходимо измерить ферритин и железосвязывающую способность сыворотки и уровень тиреотропного гормона.
В некоторых случвях могут быть проведены серологические тесты на Toxoplasma, T. cruzi, вирус Коксаки, ВИЧ и эховирус.
При рентгенологическом исследовании выявляется кардиомегалия, обычно с увеличением всех камер сердца. Плевральный выпот, особенно справа, часто сопровождает увеличение венозного давления в легких и интерстициальный отек.

При ЭКГ можно выявить синусовую тахикардию и неспецифичную депрессию сегмента ST с низковольтным или инвертированным зубцом Т. Иногда в грудных отведениях могут присутствовать патологические зубцы О, симулируя перенесенный ИМ. Часто отмечается блокада левой ножки пучка Гиса и фибрилляция предсердий.
Эхокардиография демонстрирует расширение, гипокинезию камер сердца и исключает первичные клапанные нарушения. Локальные нарушения сократимости стенок могут также возникать при дилатационной кардиомиопатии, поскольку процесс может быть очаговым. Эхокардиография может также продемонстрировать наличие тромба в камерах.
Все чаще выполняется МРТ сердца, она является полезной для подробной визуализации структуры и функции миокарда. МРТ с контрастом гадолиния может идентифицировать аномальную структуру миокарда или рубцовые изменения (то есть, отсроченное контрастирование гадолинием, или LGE). Паттерны LGE могут играть диагностическую роль при активном миокардите, саркоидозе, мышечной дистрофии, или болезни Шагаса).

Доказано, что позитронно-эмиссионная томография (ПЭТ) является чувствительным методом диагностики саркоидоза сердца.
Может потребоваться коронарная ангиография, чтобы исключить ишемическую болезнь сердца, как причину дисфункции ЛЖ, когда диагноз ставится под сомнение после неинвазивных исследований. У пациентов с болью в грудной клетке или несколькими факторами сердечно-сосудистого риска и у пациентов пожилого возраста, более вероятна ишемическая болезнь сердца. Во время катетеризации можно выполнить биопсию стенки любого желудочка в тех случаях, когда результаты могут повлиять на лечение.
Эндомиокардиальная биопсия назначается, если есть подозрение на гигантоклеточный миокардит, эозинофильный миокардит или саркоидоз, так как результаты будут влиять на ведение.
Прогноз
В целом прогноз при дилатационной кардиомиопатии неблагоприятный, однако он может улучшаться на фоне проводимой терапии (например, использования бета-блокаторов, ингибиторов ангиотензин-превращающего фермента [АПФ], антагонистов рецепторов минералкортикоидов, имплантируемых кардиовертер-дефибрилляторов или сердечной ресинхронизирующей терапии). Около 20% пациентов умирают в течение первого года, в последующем около 10% в год; от 40 до 50% всех случаев смерти – внезапные, в результате злокачественной аритмии или эмболии. Прогноз лучше, если вследствие компенсаторной гипертрофии толщина стенки желудочков сохранена, и хуже, если стенки истончены, что приводит к расширению желудочков. У пациентов, имеющих хорошо компенсированную, благодаря лечению, дилатационную кардиомиопатию, может наступить стабилизация процесса на многие годы.
Лечение
Лечение причины, если она выявлена
При фибрилляции предсердий назначают антикоагулянты и другие препараты
Иногда ИКД, сердечная ресинхронизирующая терапия (СРТ) или трансплантация
Иммуносупрессия у больных гигантоклеточным миокардитом, эозинофильным миокардитом или саркоидозом
Необходимо устранить поддающиеся лечению причины (например, токсоплазмоз, болезнь Шагаса в острой форме, гемохроматоз, тиреотоксикоз, бери-бери). Пациентам с ВИЧ-инфекцией, должна быть назначена оптимизированная антиретровирусная терапия (АРТ), лечение с иммуносупрессией должно быть ограничено у пациентов с подтвержденным биопсией гигантоклеточным миокардитом, эозинофильным миокардитом или саркоидозом.
Во всем остальном, лечение такое же как при сердечной недостаточности с ограниченной фракцией выброса: ингибиторы АПФ, бета-блокаторы, блокаторы рецепторов альдостерона, блокаторы рецепторов ангиотензина II, валсартан/сакубитрил, гидралазин/нитраты, диуретики и дигоксин. Недавние исследования показали, что пациенты с идиопатической дилатационной кардиомиопатией гораздо лучше отвечают на стандартное лечение СН и, в целом, чувствуют себя лучше пациентов с ишемической болезнью сердца.
При лечении перипартальной кардиомиопатии необходимы особые меры предосторожности. Во время беременности из-за риска повреждения плода следует избегать применения многих лекарств (например, ингибиторов АПФ и блокаторов рецепторов ангиотензина II). Кроме того, эти лекарственные препараты не рекомендуются кормящим женщинам.
Профилактическая оральная антикоагулянтная терапия использовалась в прошлом для предотвращения образования париетальных тромбов при других формах кардиомиопатии. Использование антикоагулянтов у пациентов со сниженной функцией ЛЖ и синусным ритмом остается спорным, а рекомендации относительно использования антикоагулянтов в этой ситуации ожидают результатов текущих клинических испытаний. Варфарин или новый пероральный антикоагулянт (НОАК) рекомендуются, когда присутствуют специфические симптомы (например, предшествующая цереброваскулярная эмболия, выявленный сердечный тромб, фибрилляция предсердий и/или трепетание).
Как Американская ассоциация кардиологов (American Heart Association), так и Европейское общество кардиологов (European Society of Cardiology) рекомендуют применение антикоагулянтной терапии для пациентов с перипартальной кардиомиопатией, у которых фракции выброса очень низкие, учитывая риск развития гиперкоагуляции во время беременности (1, 2). Варфарин, однако, нельзя использовать во время беременности из-за риска для плода.
Лечение сердечной недостаточности снижает риск аритмии, а имплантируемый кардиовертер-дефибриллятор может быть использован для предотвращения смерти из-за внезапной аритмии у пациентов, которые имеют пониженную фракция выброса, несмотря на оптимальную медикаментозную терапию. Поскольку атриовентрикулярная (AV) блокада, возникшая в фазу острого миокардита, часто разрешается, неотложная установка постоянного кардиостимулятора обычно не требуется. Тем не менее, при сохранении АВ-блокады или ее развитии во время хронической дилатационной фазы может потребоваться постановка постоянного кардиостимулятора. У больных с расширенным комплексом QRS, сниженной фракцией выброса ЛЖ и тяжелыми клиническими проявлениями, несмотря на оптимальную медикаментозную терапию, необходимо рассматривать проведение сердечной ресинхронизирующей терапии.
Пациенты с рефрактерной сердечной недостаточностью, несмотря на лечение, могут стать кандидатами на трансплантацию сердца. Критерии отбора включают отсутствие связанных с патологией системных заболеваний, психических нарушений и необратимой легочной гипертензии. Поскольку существует дефицит доноров, приоритет отдают более молодым больным (обычно 60 лет). Аппараты для поддержки функции левого желудочка (LVAD) могут назначаться в качестве конечной целевой терапии (например, пациентам, которые не могут быть кандидатами на трансплантацию сердца). В конечной целевой терапии аппарат для поддержки функции левого желудочка LVAD используется в качестве постоянной терапии для пациентов с рефрактерной сердечной недостаточностью (а не как временная мера перед пересадкой сердца).
1. Bozkurt B, Colvin M, Cook J, et al: Current diagnostic and treatment strategies for specific dilated cardiomyopathies: A Scientific Statement From the American Heart Association. Circulation 134(23):e579–e646.2, 2016.
2. Regitz-Zagrosek V, Roos-Hesselink JW, Bauersachs J, et al: 2018 ESC Guidelines for the management of cardiovascular diseases during pregnancy: The Task Force for the Management of Cardiovascular Diseases during Pregnancy of the European Society of Cardiology (ESC). European Heart Journal 39: 3165–3241, 2018.
Основные положения
При дилатационной кардиомиопатии отмечается дилатация, истончение и гипертрофия миокарда.
Причины включают инфекцию (обычно вирусную), токсины и нарушения обмена веществ, генетические или заболевания соединительной ткани.
Необходимо выполнить рентгенографию грудной клетки, ЭКГ, эхокардиографию и МРТ сердца для оценки степени заболевания; у некоторых пациентов проводят эндомиокардиальную биопсию.
Нужно искать и другие причины сердечной недостаточности в случае необходимости.
Необходимо лечить первопричину, если это возможно, и использовать стандартные методы лечения сердечной недостаточности (например, ингибиторы АПФ, бета-блокаторы, блокаторы рецепторов альдостерона, блокаторы рецепторов ангиотензина II, сакубитрил/валсартан, гидралазин/нитраты, диуретики, дигоксин, имплантируемый кардиовертер-дефибриллятор и/или сердечную ресинхронизирующую терапию).
Использовать пероральные антикоагулянты и иммунодепрессанты у некоторых пациентов.
Читайте также:



