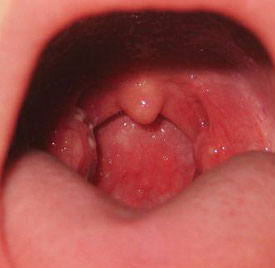
Стрептококк д энтерококк в зеве что это

Энтероккоки играют неодназначную роль в жизни человека. Энтероккоки широко распространены в природе. Они являются представителями нормальной микрофлоры человека и животных, встречаются в пищевых продуктах, в воде, растениях, у животных, птиц и насекомых. У людей, как у животных, они обитают в кишечнике, женском генитальном тракте, реже в уретре мужчин и в условиях стационара. Некоторые штаммы данных микроорганизмов, приобретя ряд признаков патогенности, могут вызывать серьезные инфекционные заболевания, а другие штаммы служат необходимым компонентом нормального микробиоценоза. Ключевым критерием для энтероккока является наличие или отсутствие у штамма генов патогенности.
В последние годы изучение энтерококков как биологических объектов и оценка их роли в физиологии и патологии человека чаще всего рассматриваются сквозь призму участия энтерококков в возникновении инфекционных заболеваний, количество которых постоянно нарастает. Однако односторонняя оценка микроорганизмов зачастую не позволяет объективно оценить их значение, так как многие из них являются составной частью нормальной микрофлоры. Обнаружение у больного энтерококков часто ставит неразрешимые вопросы перед клиницистами в плане определения врачебной тактики [4].
Род Enterococcus включает 16 основных видов, из которых наиболее распространены Е. faecalis и Е. faecium. В клиническом материале от человека чаще других видов встречаются Е. faecalis, Е. faecium, Е. gilvus и E. pallens. Длительное время данные микроорганизмы рассматривали как представителей сапрофитной флоры, не способной вызывать патологический процесс. Они входят в состав микрофлоры ротовой полости, кишечника и мочеполовой системы. E. faecium выделяется при исследованиях микрофлоры влагалища 25,3 % здоровых женщин. Большинство инфекций, вызываемых энтерококками, носит эндогенный характер и обусловлено инвазией микроорганизмов при избыточной колонизации данными бактериями сайтов прикрепления. Исследованиями убедительно показана возможность возникновения нозокомиальной инфекции, особенно при высокой частоте применения цефалоспоринов широкого спектра действия [8, 6].
Особую опасность представляет пролиферация мультирезистентных видов Enterococcus faecium и Enterococcus faecalis. Эти микроорганизмы являются постоянными обитателями различных экосистем организма, в том числе и вагинального биотопа, и, кроме того, обладают способностью быстро приобретать устойчивость ко многим антибактериальным препаратам и передавать ее другим бактериям. Энтерококки являются одним из наиболее распространенных участников развития анаэробно-аэробных микст-инфекций. Являясь факультативными аэробами, они способны эффективно стимулировать рост облигатно-анаэробных патогенов, усиливая их вирулентный потенциал [1]
Наиболее частые проявления энтерококкковых поражений мочеполовой системы наблюдаются при длительном использовании катетеров, у клинически здоровых лиц подобные поражения наблюдаются значительно реже. Генерализованные формы энтерококковых инфекций могут развиваться как следствия поражений мочеполовой системы, однако более чем в 40% случаев путь попадания энтерококков в кровоток остается невыясненным [3].
В последнее десятилетие возросла роль двух видов энтерококков - E. faecalis и E. faeсium - как нозокомиальных патогенов в различных клиниках [17, 20]. Принимая во внимание увеличение числа лиц с иммунодефицитными состояниями, нельзя исключить возможное увеличение спектра видов энтерококков, причастных к патологии у человека [16].
Показано значение энтерококков как возбудителей инфекционных осложнений после операций аортокоронарного шунтирования, реконструктивных операций на сердце и трансплантации почек. Было изолировано 465 штаммов энтерококков из крови, операционного материала (клапанов сердца), мочи, отделяемого трахеи, ран, плевральной жидкости, внутрисосудистых катетеров. Энтерококки были обнаружены при воспалительных процессах у 39,8% пациентов отделений трансплантации почек, у 34,6% больных реанимационного отделения, 20,4т - сердечно-сосудистой хирургии и в 4,2% материала из операционного блока. Наибольшее количество этих микробов было изолировано из мочи (47,7%) и из трахеи (24,3%). Из крови пациентов различных отделений выделено 45 штаммов (E. faecalis - 0,7%, E. faecium - 14,6%). У выделенных энтерококков отмечена высокая степень резистентности к антибиотикам [5].
По данным B.E.Murray, в 1990 году 80-90% выделенных у человека энтерококков приходилось на долю E. faecalis и 5-10% - на E. faecium [19]. Энтерококки, изолированные при бактериемиях, составили 38,5% от грампозитивной микрофлоры и 9,7% - от всех изолятов энтерококков. По этиологической значимости энтерококки заняли второе место после коагулазоотрицательных стафилококков. Показано, что в 7-10% случаев бактериемии имеют энтерококковую этиологию. Свыше 60% тяжелых энтерококковых инфекций зарегистрированы в отделениях интенсивной терапии [11].
Исследования последних лет показали, что энтерококки синтезируют существенное количество веществ, так называемых факторов вирулентности, способствующих развитию инфекционного процесса.
Энтерококки продуцируют факторы вирулентности, которые могут объяснить их патогенетическую значимость в инфекционном процессе. К таким факторам можно отнести поверхностные белки, участвующие в процессе адгезии и инвазии еsp, аsal, еfaA, поверностные белки участвующие в процессе адгезии и инвазии сyl A, сylM - цитолизины, gel E - желотиназа, Spr E - сериновая протеиназа. Некоторые штаммы энтероккока обладают гиалуронидазной активностью. У клинических изолятов Е. faecalis обнаружена плазмида, кодирующая синтез поверхностного белка, сообщающего способность энтероккокам к интеграции с клетками кишечного эпителия. К факторам вирулентности относят также белки и токсины, обеспечивающие повреждение тканей хозяина, белки, обусловливающие устойчивость к антибиотикам, а также факторы, индуцирующие воспаление [14].
Следует указать, что энтерококки редко являются причиной инфицирования здоровых лиц. Только при значительном снижении резистентности макроорганизма, особенно при травмах кишечника или мочеполового тракта в результате инструментальных исследований они могут проникать в стерильные в нормальных условиях органы и ткани организма хозяина, вызывая оппортунистические инфекции мочевыводящих путей, бактериемию, сепсис, подострый септический эндокардит, инфекции желчных путей или абсцессы в брюшной. Нельзя не отметить, что многие из так называемых факторов патогенности энтерококков являются необходимыми компонентами их функционирования, обеспечивающими их существование в свойственной им экосистеме, и не связаны напрямую с повреждением тканей хозяина или подавлением системы иммунитета. Так адгезины жизненно необходимы для нормальной колонизации в желудочно-кишечном тракте, а гидролаза желчных кислот повышает их шансы выжить в двенадцатиперстной кишке [15].
Известно, что факторы вирулентности энтерококков (цитолизин, желатиназа, агрегационная субстанция) могут быть вовлечены в патогенез инфекционного процесса по-разному, то есть экспрессия вирулентности может меняться от одного типа инфекции к другому и от одного вида макроорганизма к другому (таблица).

Автохтонная микрофлора ротоглотки человека, адгезируясь на эпителии, образует биопленку. Различные факторы, включая инструментальное, хирургическое или лекарственное воздействие, могут изменить целостность имеющейся биопленки, что приводит к утрате автохтонной микрофлоры. В результате биопленка из нормальной микрофлоры может замениться биопленкой, состоящей из других микроорганизмов. Следствием подобной трансформации может явиться инфекционный процесс. Преобладание представителей условно-патогенной флоры и/или появление патогенных микроорганизмов в микробном пейзаже глотки имеют место при развитии тонзиллита [12].
Ранее считалось, что в природных условиях бактерии существуют как свободно плавающие (планктонные) клетки. В настоящее время известно, что более 99% бактерий существуют в природе не в виде свободно плавающих клеток, а в виде прикрепленных к субстрату биопленок. Автохтонная микрофлора ротоглотки человека, прикрепляясь к эпителию, также образует биопленку. Результаты экспериментов показывают, что бактерии, входящие в состав биопленки, намного более устойчивы к факторам иммунной системы и резистентны к антимикробным препаратам. Связано это с тем, что в составе биопленок бактерии приобретают качественно новые свойства по сравнению с микроорганизмами в планктонной форме [15].
Лечение хронического тонзиллита часто осложняется тем, что антибиотикотерапия нередко оказывается малоэффективной. Одной из возможных причин низкой эффективности антибиотикотерапии хронического тонзиллита как раз и является то обстоятельство, что колонизирующие нёбные миндалины микроорганизмы существуют там в виде биопленки [5].
Возбудителями тонзиллита, помимо бактерий, могут быть вирусы (аденовирус, риновирус, коронавирус, вирус простого герпеса, вирус Эпштейн-Барра, цитомегаловирус и др.), простейшие (например, амебы ротовой полости), грибы (кандида и др.) [6, 8, 12, 14].
Наиболее распространенными бактериальными возбудителями тонзиллита и фарингита являются стрептококки. Из стрептококков наиболее значимым является β-гемолитический стрептококк группы A - Streptococcus pyogenes (обычно пишется сокращенно - БГСА). Реже тонзиллит вызывают стрептококки группы C и G, пневмококк (Streptococcus pneumoniaе), стафилококк (Staphilococcus aureus), гемофильная палочка (Haemophilus influenzae), Arcanobacterium haemolyticum, Neisseria gonorrhoeae, Corynebacterium diphtheriae. В последнее время увеличилось число тонзиллитов, возбудителями которых являются моракселлы, листерии, иерсинии (Yersinia enterocolitica). Возбудителями ангины Симановского-Плаута-Венсана является не один микроорганизм, а симбиоз спирохет и фузобактерий; здесь проявляется синергизм патогенного действия бактерий. Очень редко тонзиллит вызывают микоплазмы и хламидии [2, 3, 6, 7, 8, 14, 17, 19]. Некоторые авторы считают, что актиномицеты, в частности Actinomyces sp., также могут являться возбудителями тонзиллита [20, 21].
При хронической форме тонзиллита в качестве сопутствующей микрофлоры выявляются различные виды сапрофитных и условно-патогенных микроорганизмов - Str. viridans, Staph. aureus, Staph. epidermidis, Klebsiella sp., Enterobacter sp. В зависимости от стадии и выраженности воспалительного процесса в лимфаденоидном аппарате глотки состав микрофлоры в нёбных миндалинах также может заметно меняться. Так, в стадии ремиссии (т.е. при ослаблении симптомов) хронического тонзиллита при стихании воспалительного процесса доля БГСА снижается, и начинают преобладать микоплазмы, энтеробактерии и стафилококки. При катаральной, фолликулярной и лакунарной ангине удельный вес БГСА, напротив, заметно повышается, особенно при формировании паратонзиллярного абсцесса. Энтерококки и различные виды энтеробактерий, как правило, выявляются только у пациентов с сопутствующей патологией желудочно-кишечного тракта (гастроэзофагеальной рефлюксной болезнью, язвенной болезнью). Заметную роль в формировании воспалительного процесса, по-видимому, играет Mycoplasma pneumoniae. Тем не менее основными возбудителями обострений при хроническом тонзиллите остаются БГСА, которые выявляются у большинства пациентов, причем с увеличением тяжести процесса доля стрептококков только увеличивается [1, 4, 12].
Из-за большой значимости стрептококков в этиологии тонзиллита рассмотрим их более подробно. Род Streptococcus (семейство Streptococcaceae, класс Bacilli) объединяет грамположительные, неспорообразующие, неподвижные микроорганизмы со сферическими или овальными клетками диаметром 0,5-2,0 мкм. В мазках они расположены парами и короткими цепочками, особенно при выращивании на жидких питательных средах. На поверхности клеточной стенки расположены фимбрии; у некоторых видов, особенно у патогенных, клетка окружена капсулой. При неблагоприятных воздействиях стрептококки способны образовывать L-формы. Характерная особенность стрептококков - отсутствие каталазной активности. Являются факультативными анаэробами, метаболизм бродильного типа, образуется в основном лактат, но не газ. В роде Streptococcus в настоящее время выделяют около 40 видов. Рост большинства стрептококков усиливается при повышенном содержании углекислого газа в атмосфере инкубации до 5-7%. Микроорганизмы прихотливы, для их выращивания обычно используются питательные среды с добавлением крови; многие виды лизируют эритроциты. Большая часть стрептококков является паразитами ротовой полости и верхних дыхательных путей позвоночных; часть видов патогенны для человека [9, 10, 13, 16].
По типу определяемого на кровяных средах лизиса эритроцитов все стрептококки подразделяются на 3 группы: I - β-гемолитические, вызывающие гемолиз эритроцитов с формированием вокруг колоний прозрачной обесцвеченной зоны; II - α-гемолитические (зеленящие) стрептококки, образующие вокруг колоний ореол серовато-зеленого цвета за счет разрушения эритроцитов; III - γ-гемолитические (негемолитические), не образующие гемолиз вокруг колоний.
Р. Ленсфильд (1933 г.) предложила серологическую классификацию β-гемолитических стрептококков. В основу ее классификации положены антигенные свойства полисахарида клеточной стенки (группового полисахарида), экстрагируемого с помощью кислоты. Различие антигенов определило существование 20 серогрупп. Групповой полисахарид не является фактором патогенности стрептококков.
В пределах серогруппы по типоспецифическому агенту можно выделить серотипы. В роли типоспецифического агента может выступать М-белок (классификация предложена Р. Ленсфильд) или Т-белок (классификация предложена Ф. Гриффитом). Например, в серогруппе А на основании антигенных свойств М-белка выделяют более 100 серотипов, а по антигенным свойствам Т-белка - более 20 серотипов. Типирование БГСА (по М- и Т-белку проводится в научных целях в рамках эпидемиологических исследований.
Ферментативная активность положена в основу видовой классификации. Среди β-гемолитических стрептококков выделяют 11 видов. Видовая идентификация обычно в повседневной практике не используется из-за ее трудоемкости и низкого клинического значения. В клинической практике для идентификации ограничиваются определением типа гемолиза и определением антигенных свойств (т.е. определение серогруппы). Между этими двумя классификациями существует сложная взаимосвязь. Принадлежность того или иного стрептококка к определенной серогруппе не обязательно совпадает с его видовой принадлежностью. Некоторые из групповых антигенов у БГСА могут определяться и у зеленящих стрептококков. Микроорганизмы различных видов могут иметь одинаковые групповые антигены, а штаммы одного вида - разные групповые антигены. Например, зеленящие стрептококки Str. anginosus (раньше назывался Str. milleri), Str. constelatus, Str. Intermedius могут содержать любой из групповых антигенов - А, C, G или F. Серогруппа B, наоборот, представлена только одним видом Str. agalactiae.
БГСА в основном представлены видом Str. pyogenes. Но к БГСА могут быть также отнесены некоторые штаммы Str. dysgalactiae subsp. equisimilis, штаммы последнего могут продуцировать групповой антиген A, C, G или L, причем представители серогруппы A этого вида чрезвычайно редки.
Главным фенотипическим отличием Str. pyogenes является образование относительно крупных (более 0,5 мм в диаметре) колоний на кровяном агаре. Другие виды БГСА образуют очень мелкие колонии с зоной гемолиза, в 10 раз и более превышающей размер колоний [11, 13, 16].
Стрептококки группы А - БГСА (β-гемолитический стрептококк серогруппы А) в основном представлены видом Streptococcus pyogenes, поэтому эти два понятия часто рассматриваются как синонимы. Str. pyogenes - один из наиболее распространенных возбудителей бактериальных заболеваний человека. Считается доказанным, что БГСА является наиболее важным и доказанным этиологическим фактором тонзиллита, а также наиболее опасным в плане развития осложнений [12]. Помимо тонзиллита, он вызывает такие заболевания, как скарлатина, импетиго, рожистое воспаление, флегмоны, некротизирующий фасцит, миозит, артрит, синдром токсического шока [16]. В последние десятилетия ХХ в. появились сообщения (большей частью из США) о вспышках острой ревматической лихорадки среди детей и взрослых, которая во многих случаях являлась последствием перенесенного БГСА-тонзиллита, протекающего со стертыми клиническими симптомами; были выделены так называемые ревматогенные БГСА-штаммы, одним из признаков которых было образование мукоидных колоний на кровяном агаре. В начале 1990-х гг. в США и некоторых странах Западной Европы были описаны случаи крайне тяжелой БГСА-инфекции, та называемый синдром стрептококкового токсического шока. Входными воротами этой инфекции являются кожа и мягкие ткани, но в некоторых случаях заболевание было связано с первичным очагом, локализованным в лимфоидных структурах носоглотки [17].
Str. pyogenes вызывает заболевания только у человека. Кожа и слизистые оболочки человека служат естественным резервуаром данного микроорганизма, а больные или носители являются единственным источником инфекции. Передача происходит воздушно-капельным путем или при непосредственном контакте (с заносом в рот грязными руками), а также через инфицированные пищевые продукты, хранящиеся при комнатной температуре (например, молоко). Наиболее высокая заболеваемость фарингитами/тонзиллитами, вызываемыми Str. pyogenes, отмечается у детей младше 10 лет в осенне-весенний период. Бессимптомное носительство возбудителя также более распространено среди детей (15-20%) по сравнению со взрослыми (5%) [8, 10, 16].
Строение клеточной стенки Str. pyogenes типично для грамположительных бактерий; ее основой являются пептидогликан и тейхоевые кислоты со встроенными белками. Тейхоевые кислоты, расположенные между клеточной стенкой и цитоплазматической мембраной (периплазматические тейхоевые кислоты), представляют собой групповой полисахарид, антигенное разнообразие которого положено в основу серологической классификации β-гемолитических стрептококков; этот антиген не является поверхностной структурой, поэтому требуется проводить его экстракцию. Фактором патогенности групповой полисахарид не является. Имеется капсула из гиалуроновой кислоты, играющая важную роль в патогенезе инфекций.
Факторы патогенности (вирулентности) БГСА
В патогенезе инфекций, вызываемых Str. pyogenes, имеют значение капсула, элементы клеточной стенки микроорганизма и секретируемые факторы. Благодаря перечисленным факторам вирулентности обеспечиваются адгезия к клеткам человеческого организма, устойчивость к фагоцитозу, проникновение и распространение в тканях, их повреждение [16].
Первый этап инфекционного процесса - адгезия микроорганизма к эпителию слизистых оболочек. Основные адгезины - липотейхоевые кислоты, покрывающие поверхностные фимбрии. Важную роль в адгезии также играют гиалуронидаза, стрептокиназа и стрептодорназа (ДНКаза).
Белок М (анг. mucoid, слизистый, так как колонии штаммов-продуцентов имеют слизистую консистенцию) по структуре похож на фимбрии грамотрицательных бактерий. Белок М - основной фактор вирулентности и типоспецифический антиген; он ингибирует фагоцитарные реакции, а также проявляет свойства суперантигена. Существует множество вариантов строения М-белка - это используется для типирования БГСА. В настоящее время выделяют более 90 серотипов БГСА по антигенным свойствам М-белка.
Капсула - второй по значимости фактор вирулентности. Она защищает бактерии от фагоцитов и обеспечивает адгезию к эпителию. Капсула образована гиалуроновой кислотой, аналогичной входящей в состав соединительной ткани, поэтому капсула проявляет минимальную иммуногенную активность и не распознается как чужеродный агент. Штаммы Str. pyogenes, лишенные капсулы, значительно менее устойчивы к фагоцитозу и менее вирулентны. Штаммы, имеющие толстую капсулу, образуют слизистые колонии на кровяном агаре, хотя слизистый вид колоний может быть обусловлен обильной продукцией М-белка.
F-белок (фибронектин-связывающий белок) играет важную роль в адгезии микроорганизма к эпителиальной клетке, связываясь с фибронектином на ее поверхности.
Т-белок имеет сходство в строении с М-белком, однако не имеет антифагоцитарных свойств и не является фактором патогенности. Антигенные свойства Т-белка используются для типирования штаммов БГСА.
OF (opacity factor) представляет собой фермент липопротеиназу, расщепляющий липопротеины сыворотки крови. Роль его в патогенезе инфекций не ясна.
С5а-пептидаза - подавляет активность фагоцитов; фермент расщепляет и инактивирует С5а компонент комплемента.
Стрептолизин О - проявляет свойства гемолизина, разрушая эритроциты в анаэробных условиях; проявляет также иммуногенные свойства. Стрептолизин S - резистентен к кислороду, вызывает поверхностный гемолиз на кровяных средах, не проявляет иммуногенных свойств. Оба фермента разрушают не только эритроциты, но и некоторые другие клетки, например кардиомиоциты.
Пирогенные (эритрогенные) токсины (А, B и C) - проявляют свойства суперантигенов: оказывают митогенное действие на Т-лимфоциты, которые вследствие этого продуцируют избыточное количество цитокинов, что обусловливает развитие лихорадки. Способность к образованию токсинов детерминирована заражением бактериальной клетки умеренным фагом, несущим ген токсинообразования.
Стрептокиназа (фибринолизин) - активирует антисвертывающую систему крови, а именно - плазминоген, что приводит к образованию плазмина и растворению тромбов. Фермент не проявляет прямой фибринолитической активности. Вероятно, этот фермент имеет значение в распространении возбудителя по организму.
Гиалуронидаза - вызывает разрушение гиалуроновой кислоты, которая составляет основное вещество соединительной ткани человека, что способствует распространению возбудителя в тканях.
Никотин-аденин-динуклеотидаза (НАДаза) - непосредственно влияет на лейкоциты, ослабляя их способность к таксису и фагоцитозу. НАДаза продуцируется многими, но не всеми штаммами Str. pyogenes.
К продуктам, секретируемым в окружающую среду, относятся стрептолизин О, гиалуронидаза, НАДаза, пирогенные экзотоксины. К поверхностным белкам относятся М-белок, F-белок, фактор опалесценции, стрептолизин S, стрептокиназа, С5а-пептидаза [10, 11, 16].
Доказана способность БГСА к формированию биопленки in vitro на поверхности абиогенных носителей, что, возможно, отражает способность БГСА переходить в хроническую форму и образовывать рецидивы в естественных условиях [5].
К β-гемолитическим стрептококкам также относятся Streptococcus equi (группа С по Лансфилд) и Streptococcus canis (группа G по Лансфилд). Помимо ангины, они вызывают у человека пневмонию, рожу, различные инфекции мягких тканей, гнойный артрит, инфекционный эндокардит, сепсис, хотя их регистрируют сравнительно редко. Патогенез поражений аналогичен прочим стрептококковым инфекциям; основные факторы патогенности - гиалуронидаза, фибринолизины, стрептокиназа, стрептолизин О и эритрогенные токсины [8, 12].
Среди возбудителей тонзиллита следует также отметить Streptococcus pneumoniae (пневмококк), который может в небольшом количестве встречаться среди представителей нормальной микрофлоры. Этот микроорганизм не содержит группового антигена и не включен в какую-либо серологическую группу. В зависимости от антигенов капсульных полисахаридов выделяют более 90 серотипов и не менее 40 серогрупп пневмококка. При росте на кровяном агаре колонии пневмококка окружает зона α-гемолиза. Кроме тонзиллита, пневмококк является одним из основных возбудителей бактериальных пневмоний, регистрируемых вне стационаров. Основной фактор патогенности - капсула, защищающая бактерии от действия фагоцитов. Некапсулированные штаммы авирулентны. Резервуар инфекции - больные и носители. Основной путь передачи - контактный, а в период вспышек также воздушно-капельный. В подавляющем большинстве случаев клинические формы инфекции развиваются при нарушениях резистентности организма (в том числе вследствие холодовых стрессов), а также на фоне сопутствующей патологии [10, 11, 12].
Staphylococcus aureus, как установлено, также может играть определенную роль в этиологии тонзиллита. Staph. aureus не является представителем нормальной микрофлоры человека, может выделяться у 15-30% клинически здоровых лиц. Носительство в большинстве случаев ограничено несколькими неделями или месяцами, а подавляющее число инфекций носит эндогенный характер. Известны случаи внутриклеточной персистенции Staph. aureus, что может свидетельствовать о возможности данного микроорганизма поддерживать хронический очаг инфекции в нёбных миндалинах [12, 23, 18, 22].
Выводы
Возбудителями тонзиллита могут быть вирусы, бактерии, грибы или простейшие. Наиболее распространенным бактериальным возбудителем тонзиллита является β-гемолитический стрептококк группы А. Реже тонзиллит вызывают стрептококки других серологических групп, пневмококки, стафилококки, гемофильная палочка, листерии, иерсинии, моракселлы или другие бактерии. Лечение тонзиллита может осложняться тем, что колонизирующие нёбные миндалины бактерии - возбудители тонзиллита существуют там в виде биопленки. Бактерии, входящие в состав биопленки, намного более устойчивы к факторам иммунной системы и к антимикробным препаратам; по этой причине антибиотикотерапия часто оказывается малоэффективной. Изучение свойств биопленок верхних дыхательных путей и ротовой полости может привести к появлению новых эффективных способов терапии и профилактики тонзиллита или других инфекционных патологий.
Рецензенты:
Кузнецова Т.А., д.м.н., зав. лабораторией иммунологии ФГБУ НИИ эпидемиологии и микробиологии имени Г.П. Сомова, г. Владивосток;
Стрептококк ( лат. Streptococcus) – это бактерия шарообразной или яйцеподобной формы, принадлежащая к семейству Стрептококковые (Streptococcaceae).
Стрептококки являются анаэробными паразитами не только человека, но и животных. Местом обитания и размножения стрептококковой инфекции являются органы дыхания, желудочно-кишечного тракта и мочеполовой системы мужчин и женщин, может находиться на коже. Преобладающее же количество бактерий стрептококк обычно оседает в носу, ротовой полости, горле и толстом кишечнике, иногда встречается в уретре мужского органа и влагалище женщины.
В природе, данный вид бактерий также существует в земле, на поверхности растений, грибов.
Стрептококковая инфекция является условно-патогенной микрофлорой, — она практически всегда присутствует в организме человека и не несет в себе какую-либо опасность, поскольку ее количество и пребывание в человеке контролирует иммунная система. Однако, как только человеку стоит ослабеть (стрессы, переохлаждение организма, гиповитаминоз и т.д.), бактерии сразу же начинают активно размножаться, выделять в организм большое количество продуктов своей жизнедеятельности, отравляя его, и провоцировать развитие различных заболеваний, как написано выше, преимущественно – дыхательной, пищеварительной и мочеполовойсистем. И потому, основным превентивным действием против развития стрептококковой инфекции в организме, и связанных с ней заболеваний, является укрепление и поддержание нормального функционирования иммунитета. Однако не следует считать все виды стрептококков патогенными, — некоторые из них являются полезными бактериями, например — Streptococcus thermophilus, которые применяются при производстве кисло-молочной продукции – йогуртов, сметаны, моцареллы и других.
Основные способы заражения стрептококковой инфекцией – воздушно-капельный и контактно-бытовой путь.
Заболевания, которые способны вызвать стрептококки
- Абсцесс;
![]()
- Бронхит;
- Васкулит;
- Гломерулонефрит;
- Импетиго;
- Лимфаденит;
- Менингит;
- Остеомиелит;
- Острый тонзиллит (ангина);
- Пародонтит;
- Пневмония;
- Ревматизм;
- Рожистое воспаление (рожа);
- Сепсис;
- Скарлатина;
- Стрептодермия;
- Фарингит;
- Хейлит, заеды;
- Эндокардит;
- Заболевания мочеполовой системы.
Кроме того, стрептококковая инфекция может стать вторичной инфекцией, присоединяясь, например к стафилококковой, энтерококковой и другим видам инфекции.
Наиболее часто, заболеваниями стрептококковой этиологии болеют дети, люди преклонного возраста, а также офисные работники.
Давайте немного рассмотрим краткую характеристику бактерий – стрептококк.
Стрептококк представляет собой типичные клетки, диаметр которых составляет менее 1 мкм, располагающиеся попарно или цепочками, образуя вытянутую палочку с утолщениями и утончениями, по форме напоминающую бусинки, нанизанные на цепочку. Из-за этой формы они и получили свое название. Стрептококковые клетки образуют капсулу, и способны легко превратиться в L-форму. Бактерии неподвижны, за исключением штаммов группы D. Активное размножение происходит при контакте с частичками крови, асцитической жидкости или углеводами. Благоприятная температура для нормальной жизнедеятельности инфекции +37°С, кислотно-щелочный баланс (рН) – 7,2-7,4. Живут стрептококки преимущественно колониями, образуя как бы сероватый налет. Перерабатывают (ферментируют) углеводы, образовывая кислоту, расщепляют аргинин и серин (аминокислоты), в питательной среде синтезируют внеклеточно такие вещества, как — стрептокиназа, стрептодорназа, стрептолизины, бактериоцины и лейкоцидин. Некоторые представители стрептококковой инфекции – группы В и D образовывают красные и желтые пигменты.

Стрептококковая инфекция включает в себя около 100 видов бактерий, наиболее популярными из которых являются – пневмококки и гемолитические стрептококки.
Как инактивировать стрептококк?
Бактерии стрептококки погибают при:
— их обработке растворами антисептиков и дезинфектантов;
— пастеризации;
— воздействии антибактериальных средств – тетрациклинов, аминогликозидов, пенициллинов (не применяется при инвазивной стрептококковой инфекции).
Как передается стрептококк? Рассмотрим наиболее популярные пути заражения стрептококковой инфекцией.
Условия, при которых человек начинает заболевать стрептококковыми болезнями, обычно состоят из двух частей – контакт с данной инфекцией и ослабленный иммунитет. Однако, человек может серьезно заболеть и при обычном контакте с данным видом бактерий.
Как стрептококк может попасть в организм?
Воздушно-капельный путь. Риск заражения стрептококковой инфекцией обычно возрастает в период простудных заболеваний, когда концентрация различной инфекции (вирусы, бактерии, грибок и другие) в воздухе, преимущественно в закрытых помещениях существенно возрастает. Пребывание в офисах, общественном транспорте, выступлениях и других местах с большим скоплением людей, особенно в период ОРЗ-болезней, является основным способом заражения данными бактериями. Чиханье и кашель – это основные сигналы, которые предупреждают, что из этого помещения лучше удалиться, или хотя бы тщательно его проветривать.
Воздушно-пылевой путь. Пыль обычно состоит из мелких частичек тканей, бумаги, слущенной кожи, шерсти животных, пыльцы растений и различных представителей инфекции – вирусов, грибков, бактерий. Пребывание в запыленных помещениях, еще один фактор, повышающий риск попадание в организм стрептококковой инфекции.
Контактно-бытовой путь. Заражение происходит при совместном, вместе с болеющим человеком, использовании посуды, предметов личной гигиены, полотенца, постельного белья, кухонных принадлежностей. Риск заболевания повышается при травмировании слизистой оболочки носовой или ротовой полости, а также поверхности кожи. Очень часто, на работе, люде заражаются через использование одной чашки на несколько человек, или же питье воды из горла, из одной бутылки.
Половой путь. Инфицирование происходит при интимной близости с человеком, который болеет стрептококками, или же просто является их носителем. Данный вид бактерий имеет свойство жить и активно размножаться в органах мочеполовой системы мужчин (в уретре) и женщин (во влагалище).
Фекально-оральный (алиментарный) путь. Инфицирование стрептококками происходит при несоблюдении правил личной гигиены, например, при употреблении пищи немытыми руками.
Медицинский путь. Заражение человека происходит, в основном при его осмотре, хирургическом или стоматологическом вмешательстве не продезинфицированными медицинскими инструментами.
Как стрептококк может серьезно навредить здоровью человека, или что ослабляет иммунную систему?
Наличие хронических болезней. Если у человека присутствуют хронические заболевания, это обычно свидетельствует об ослабленном иммунитете. Чтобы не усложнять течение болезней, и стрептококковая инфекция не присоединилась к уже имеющимся болезням, обратите должное внимание и сделайте акцент на их лечение.
Наиболее распространенными заболеваниями и патологическими состояниями, при которых стрептококк часто атакует больного, являются: переохлаждение организма, ОРВИ, грипп, ОРЗ, тонзиллит, туберкулез, сахарный диабет, ВИЧ-инфекция, заболевания эндокринной и других систем организма, травмирование слизистых оболочек ротовой и носовой полости, горла, органов мочеполовой системы.
Кроме того, риск заражения стрептококком повышают:
- Вредные привычки: употребление алкоголя, курение, наркотики;
- Отсутствие здорового сна, стрессы, хроническая усталость;
- Употребление пищи, преимущественно малополезного характера;
- Малоподвижный образ жизни;
- Недостаточность в организме витаминов и микроэлементов (гиповитаминозы);
- Злоупотребление некоторыми лекарственными препаратами, например – антибиотиками, сосудосуживающими препаратами;
- Посещение салонов красоты сомнительного характера, особенно процедур маникюра, педикюра, пирсинга, набивке татуировки;
- Работа в загрязненных помещениях, например, на предприятиях химической или строительной промышленностей, особенно без средств защиты дыхательных путей.
Клиническая картина (симптомы) стрептококка весьма разнообразна, и зависит от локализации (органа), который поражает данный род бактерий, штамма инфекции, состояния здоровья и иммунной системы, возраста человека.
Общими симптомами стрептококка могут быть:
- Боль в горле, изменение тембра голоса;
- Образование налета, часто гнойного характера на миндалинах больного;
- Увеличение лимфатических узлов;
- Общая слабость, недомогание, боль в мышцах и суставах;
- Повышенная и высокая температура тела, от 37,5 до 39 °С;
- Озноб;
- Покраснение кожи, а также зуд и появление на ней пузырьков или бляшек;
- Боль в животе, отсутствие аппетита, тошнота, рвота, диарея, холецистит;
- Чувство болезненности и зуда в органах мочеполовой системы, выделения из них;
- Синуситы – ринит (насморк), этмоидит, гайморит, сфеноидит и фронтит;
- Затрудненное дыхание, кашель, чиханье, одышка;
- Нарушение чувства обоняния;
- Болезни дыхательных путей: ангина, ларингит, фарингит, трахеит, бронхит и пневмония (воспаление легких);
- Головные боли, головокружения, нарушение сознания;
- Бессонница;
- Обезвоживание организма;
- Нарушение нормального функционирования некоторых органов и тканей, которые стали очагом оседания бактерии.
- Гломерулонефрит;
- Менингит;
- Воспаление сердечной мышцы — миокардит, эндокардит, перикардит;
- Васкулит;
- Гнойный отит;
- Потеря голоса;
- Абсцесс легких;
- Ревматизм;
- Ревматоидный артрит;
- Пульпит;
- Тяжелые формы аллергии;
- Хронический лимфаденит;
- Рожа;
- Сепсис.

Всего известно около 100 видов стрептококков, каждый из которых характеризуется своей патогенностью.
Для удобства, данный род бактерий, в зависимости от типа гемолиза эритроцитов, выделили в 3 основные группы (классификация Брауна):
- Альфа-стрептококки (α) , или зеленящие стрептококки — вызывают неполный гемолиз;
- Бета-стрептококки (β) — вызывают полный гемолиз, и являются наиболее патогенными бактериями;
- Гамма-стрептококки (γ) – являются негемолитическими бактериями, т.е. они не вызывают гемолиза.
Классификация Лансфилда (Lancefield), в зависимости от строения карбогидрата C клеточной стенки бактерии, также выделяет 12 серотипов β-стрептококков: А, В, С… до U .
Streptococcus pneumoniae (Пневмококк). Является основным возбудителем таких болезней, как – пневмония (воспаление легких), менингит, бронхит, ларингит, средний отит, ринит, остеомилит, септический артрит, перитонит, эндокардит, сепсис и другие. Место оседания – дыхательные пути человека.
Streptococcus thermophilus (Стрептококк термофильный). Синонимы: Streptococcus salivarius thermophilus, Streptococcus salivarius subsp. thermophilus. Является полезной бактерией. Используется для приготовления полезных молочных продуктов – йогуртов, сметаны, ряженки, различных сыров (например – моцареллы), используется в БАДах.
Streptococcus mutans (Стрептококк мутанс). Способствует развитию таких заболеваний, как – кариес зубов. Развитие кариеса из-за данной вида бактерии происходит из-за ее свойства переводить сахарозу, глюкозу, фруктозу и лактозу в молочную кислоту, благодаря которой происходит постепенной разрушение зубной эмали. Streptococcus mutans имеет также свойство прилипать к зубной эмали, поэтому тщательная чистка зубов и полоскание ротовой полости специальными средствами являются профилактической мерой против данного вида инфекции.
Streptococcus salivarius (Слюнной стрептококк). Обычно обитает в ротовой полости и верхних дыхательных путях человека – в носу, в горле. Как и предыдущий тип, Streptococcus salivarius способен ферментировать сахарозу в молочную кислоту, однако не имеет такой же патогенности, как первый. В современном мире, некоторые штаммы слюнного стрептококка используют в качестве пробиотика. Его используют для производства специальных сосательных леденцов, способных предохранять полость рта с более опасными типами стрептококков. Замечено, что присутствие в полости рта слюнного стрептококка способствует снижению риска заразиться ангиной, фарингитом и другими инфекционными болезнями верхних дыхательных путей.
Streptococcus sanguis (ранее — Streptococcus sanguis). Является обычным обитателем зубного налета, однако имеет интересное свойство – он предотвращает прилипание к зубам streptococcus mutans, косвенно способствующего развитию кариеса.
Streptococcus mitis (ранее — Streptococcus mitior). Обычно оседают в верхних дыхательных путях – носовой и ротовой полости, горле. Этот вид бактерии является одним из возбудителей такого заболевания сердца, как — инфекционный эндокардит.
Бета-гемолитические стрептококки обычно несут в себе наибольшую опасность для здоровья человека. Это связано с их способность разрушать эритроциты (красные кровяные тельца). При этом во время своей жизнедеятельности, бета-стрептококки выделяют большое количество различных токсинов (ядов), распространение по организму которых приводит к различным сложным, а иногда и смертельно-опасным болезням и патологическим состояниям. Рассмотрим их более подробно.
Яды, вырабатываемые жизнедеятельностью бета-стрептококков в организме:
Стрептолизин – нарушает целостность клеток крови и сердца;
Лейкоцидин – фермент, разрушающий лейкоциты (иммунные клетки крови);
Скарлатинозный эритрогенин – способствует расширению капилляров, что приводит к кожной сыпи при болезни скарлатина;
Стрептокиназа, гиалуронидаза, протеиназа и амилаза – ферменты, которые способствуют распространению стрептококковой инфекции по всему организму, а также пожиранию здоровых тканей;
Некротоксин и летальный токсин – яды, которые способствуют омертвлению тканей.
Все вышеприведенные вещества, разносятся по организму через кровь.
Кроме того, попадая бактерий в организм, иммунитет начинает вырабатывать по отношению к ним антитела. Опасным положением является, когда антитела не могут признать измененные клетки и ткани организма, тогда они начинают их атаковать, поражая, фактически свой же организм. Таким образом, развиваются аутоиммунные заболевания.
Читайте также: