Отличия дифтерии от мононуклеоза у
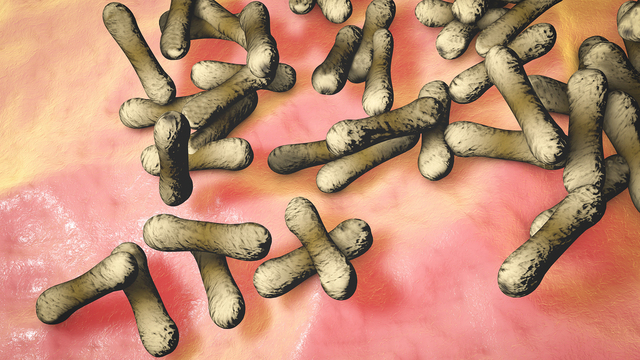

Дифтерия - это острое инфекционное заболевание, опасное для жизни. Наиболее восприимчивы к нему дети в возрасте 3–7 лет, в последние годы увеличилась заболеваемость подростков и взрослых.
Дифтерия – это острое инфекционное заболевание, опасное для жизни. Оно протекает в виде острого воспаления верхних дыхательных путей, преимущественно глотки (примерно 90% случаев), носа, кожи в местах ее повреждения, глаз или половых органов.
Основную угрозу, однако, представляет не воспаление, а отравление токсином, который вырабатывает бактерия – возбудитель заболевания, при этом преимущественно поражаются сердечно-сосудистая и нервная системы.
Возбудитель дифтерии и пути заражения
Возбудителем дифтерии являются Corynebacterium diphteriae – грамположительные бактерии в виде палочек с характерными колбовидными утолщениями на концах, которые в мазках располагаются попарно, под углом в виде римской цифры V по отношению друг к другу. Дифтерийные палочки в процессе жизнедеятельности выделяют дифтерийный токсин, фермент нейраминидазу и другие биохимически активные соединения.
Синтез дифтерийного токсина микробными клетками контролируется специальным геном tox. Бактерии могут терять его в процессе жизнедеятельности, утрачивая вместе с ним и свою способность вырабатывать токсин (токсигенность). И, наоборот, изначально нетоксигенные штаммы могут приобретать патогенные свойства, к счастью, это случается крайне редко.
Заболевание передается воздушно-капельным путем от больных дифтерией или от здоровых носителей инфекции, значительно реже – через предметы обихода.
Группа риска
Наиболее восприимчивы к заражению дифтерией дети в возрасте 3–7 лет, но в последние годы увеличилась заболеваемость подростков и взрослых.
Источником инфекции являются больные люди или здоровые носители токсигенных бактерий. Наиболее заразны страдающие дифтерией зева, носа и гортани, так как они активно выделяют возбудителей заболевания с выдыхаемым воздухом. Больные дифтерией глаз, кожи могут распространять инфекцию контактным путем (руки, предметы быта). Здоровые носители бактерий гораздо менее заразны, но отсутствие у них каких-либо внешних признаков их состояния не позволяет контролировать распространение ими инфекции, ведь выявить их можно только случайно в ходе массовых диспансерных обследований. В результате большинство случаев заражения дифтерией обусловлено контактом со здоровыми носителями дифтерийной палочки.
Инкубационный период (время от момента заражения до появления первых признаков заболевания) составляет 2–10 дней.
Дифтерийный токсин
Токсин, вырабатываемый дифтерийной палочкой, состоит из нескольких компонентов. Один из них – фермент гиалуронидаза разрушает гиалуроновую кислоту капилляров и увеличивает их проницаемость, что приводит к выходу из сосудов и пропитыванию окружающих тканей плазмой крови с отложением белка фибриногена. Второй компонент – некротоксин разрушает клетки эпителия с выделением из них фермента тромбокиназы. Тромбокиназа способствует превращению фибриногена в фибрин и образованию на поверхности тканей фибринной пленки. При действии дифтерийного токсина на небные миндалины, которые покрыты несколькими слоями эпителиальных клеток, формируется фибиринная пленка, проникающая вглубь эпителия миндалин и плотно спаянная с ним.
Третий (основной) компонент – собственно токсин способен блокировать процессы клеточного дыхания и синтеза белковых молекул. Наиболее чувствительными к его действию являются капилляры, клетки миокарда и нервные клетки. В результате развивается дистрофия миокарда и инфекционно-токсический миокардит, повреждение капилляров приводит к инфекционно-токсическому шоку, повреждение шванновских клеток (вспомогательные клетки нервной ткани) приводит к демиелинизации нервных волокон (разрушение электроизолирующего слоя миелина с нарушением проведения нервных импульсов по нервным волокнам). Кроме того, дифтерийный токсин вызывает общую интоксикацию организма.
Симптомы и течение
Дифтерия зева обычно начинается с небольшого повышения температуры, незначительной болезненности при глотании, покраснения и отечности миндалин, формированию на них специфического пленчатого налета, увеличения передних верхних шейных лимфатических узлов. Цвет пленок – обычно белый в первые 2–3 дня заболевания, но потом приобретает серый или желтовато-серый цвет. Примерно через неделю заболевание, или заканчивается выздоровлением (легкая форма, как правило, у привитых от дифтерии), или переходит в более тяжелую токсическую форму, обусловленную системным действием дифтерийного токсина.
Токсическая форма дифтерии всегда протекает очень тяжело. Она характеризуется очень высокой температурой тела (39,5-41,0°С), сильными головными болями, сонливостью, апатией. Кожа становится бледной, во рту отмечается сухость, у детей возможна многократная рвота и боль в животе. Отек миндалин становится резко выраженным, может приводить к полному закрытию входа в глотку, распространяется на мягкое и твердое небо, часто также на носоглотку, дыхание затрудняется, голос часто становится гнусавым. Налет распространяется на все ткани ротоглотки. Классическим признаком токсической формы дифтерии зева является отек подкожной клетчатки в области шеи, а иногда и грудной клетки, в результате чего кожа приобретает студнеобразную консистенцию. Передние верхние шейные лимфатические узлы значительно увеличены и болезненны.
Дифтерия носа протекает на фоне нормальной или слегка повышенной температуры тела, интоксикация отсутствует. Из носовых ходов видно серозно-гнойное или кровянисто-гнойное отделяемое. На крыльях носа, щеках, лбу и подбородке появляются участки мокнутия, а затем сухие корочки. Внутри носа видны пленчатые налеты. Патологический процесс может также поражать придаточные пазухи носа. При токсической форме наблюдается отек подкожной клетчатки щек и шеи.
Дифтерия глаза протекает как банальный конъюнктивит и характеризуется умеренной гиперемией и отеком конъюнктивы века, небольшим количеством серозно-гнойного отделяемого из конъюнктивального мешка (катаральная форма). Пленчатая форма проявляется выраженным отеком век, наличием на их конъюнктиве трудно снимаемых пленок серовато-белого цвета. Токсическая форма также сопровождается отеком клетчатки вокруг глазницы.
Дифтерия кожи приводитк длительному не заживлению любых повреждений кожи, гиперемии, на коже присутствует грязно-серый налет, отмечается плотная инфильтрация окружающей кожи.
Диагностика
Диагностику дифтерии проводят на основании данных осмотра больного и результатов анализов. При осмотре за диагноз дифтерия говорят следующие признаки: наличие характерных пленок, а также затруднение дыхания и свистящий шум на вдохе, не характерные для ангины, лающий кашель. Диагноз дифтерии по характерным клиническим признакам при заболевании, протекающем в легкой форме, поставить сложнее.
Общий анализ крови – признаки острого воспалительного процесса.
Исследования мазка под микроскопом (бактериоскопия) – выявление имеющих характерный вид бактерий Corynebacterium diphteriae.
Бактериологическое исследование – посев биологического материала на специальную питательную среду и культивирование колоний микроорганизмов.
Определение уровня (титра) антитоксических антител (высокий титр – 0,05 МЕ/мл и выше позволяет исключить дифтерию).
Серологическое исследование – определение специфических антител в сыворотке крови с помощью методов РПГА, ИФА и др.
Дифтерию зева нужно дифференцировать от острого тонзиллита (фолликулярная и лакунарная формы), ангины Симановского-Венсана (грибковое поражение), сифилитической ангины, ложнопленочной ангины при инфекционном мононуклеозе, паратонзиллярным абсцессом, эпидемическим паротитом, лейкозом. У детей необходимо отвести диагноз ложного крупа.
Лечение
Всех заболевших дифтерией, вне зависимости от тяжести состояния, необходимо госпитализировать в инфекционную больницу.
Лечение состоит в следующем:
Диета – витаминизированная, калорийная, прошедшая тщательную кулинарную обработку еда.
Этиотропная терапия (то есть направленная на устранение причины заболевания) – введение противодифтерийной сыворотки (ПДС), доза и количество раз введения зависят от тяжести и формы заболевания. При легкой форме ПДС вводится однократно внутримышечно в дозе 20–40 тыс. МЕ, при среднетяжелой форме – 50–80 тыс. МЕ однократно или, при необходимости, повторно в той же дозе через 24 часа. При лечении тяжелой формы заболевания суммарная доза увеличивается до 90–120 тыс. МЕ или даже до 150 тыс. МЕ (инфекционно-токсический шок, ДВС-синдром). При этом 2/3 дозы вводится сразу, и в течение первых суток госпитализации должно быть введено 3/4 суммарной дозы.
Антибиотики: при легких формах – эритромицин, рифампицин внутрь, при среднетяжелых и тяжелых формах – инъекционное введение пенициллинов или цефалоспоринов. Продолжительность курса – 10–14 дней. Антибиотики не влияют на дифтерийный токсин, но уменьшают количество бактерий, его вырабатывающих.
Местное лечение – полоскания и орошения дезинфицирующими растворами.
Дезинтоксикационная терапия – глюкозо-солевыми растворами с учетом суточной потребности в жидкости и ее потерь (среднетяжелая и тяжелая форма).
Глюкокортикостероиды – при среднетяжелой и тяжелой формах.
Лечение бактерионосителей проводят антибиотиками: тетрациклины (дети старше 9 лет), эритромицин, цефалоспорины на фоне общеукрепляющей терапии и устранения хронических очагов инфекции.
Осложнения
Среди наиболее серьезных осложненийдифтерии на сердечно-сосудистую систему можно выделить миокардиты, нарушения сердечного ритма.
Неврологические осложнения дифтерии обусловлены поражением различных черепных и периферических нервов и проявляются параличом аккомодации, косоглазием, парезами конечностей, а в более тяжелых случаях параличом дыхательных мышц и мышц диафрагмы.
Вторичными осложнениями дифтерии являются такие тяжелые патологические состояния как острые нарушения мозгового кровообращения (тромбозы, эмболия), метаболическая энцефалопатия, отек головного мозга, токсические поражения почек, дифтерийный гепатит, а также инфекционно-токсический шок и ДВС-синдром (синдром дессиминированного внутрисосудистого свертывания – тяжелое нарушение системы свертывания крови). Токсическая форма дифтерии может приводить к острой почечной, сердечно-сосудистой, дыхательной или полиорганнной недостаточности.
Неспецифическими осложнениями дифтерии являются паратонзиллярный абсцесс, отит, пневмония.
Вакцинация
Вакцинация от дифтерии проводится анатоксином, то есть инактивированным токсином. В ответ на его введение в организме образуются антитела не к Corynebacterium diphteriae, а к дифтерийному токсину.
Согласно российскому прививочному календарю, вакцинация детей в возрасте до года проводится в 3, 4–5 и 6 месяцев. Первая ревакцинация проводится в 18 месяцев, вторая – в 7 лет, третья – в 14. Взрослые должны ревакцинироваться от столбняка и дифтерии каждые 10 лет.
Проявления инфекционного мононуклеоза могут быть похожи на обычное ОРЗ. Поэтому мононуклеоз часто остается нераспознанным, и родители начинают бить тревогу лишь тогда, когда сталкиваются с последствиями болезни. Что нужно сделать для своевременной диагностики заболевания?
Самая высокая заболеваемость мононуклеозом отмечается среди детей 3-9 лет, но чаще всего болезнь у них протекает в легких формах, которые наиболее сложны для диагностики и часто остаются нераспознанными. Основная опасность этой инфекции в том, что после перенесенного заболевания у ребенка длительно сохраняются нарушения в иммунной системе, и он становится восприимчивым к самым разнообразным микроорганизмам - бактериям, вирусам, грибам, которые могут стать причиной многочисленных инфекционных осложнений.
Инфекционный мононуклеоз - это вирусная инфекция, для которой характерны поражение лимфатических узлов, печени и селезенки, ангина и повышение температуры.
Дети первого года жизни, как правило, не болеют: они защищены антителами, полученными от матери во время внутриутробного периода развития (при условии, что мать в свое время перенесла эту инфекцию).
Возбудитель заболевания
Вызывает заболевание вирус Эпштейна-Барр, являющийся близким "родственником" вируса герпеса. Свое название этот вирус получил в честь двух канадских исследователей, которые открыли его в 1964 г. Вирус распространен во всем мире, и его можно обнаружить у большей части взрослого населения планеты. Подобно вирусу простого герпеса, однажды проникнув в организм, вирус Эпштейна-Барр навсегда остается в нем. Заболеваемость отмечается круглый год, подъемы ее случаются весной и осенью.
Вирус мало устойчив к внешним воздействиям и быстро погибает вне организма человека. Заразность его не очень велика, поэтому инфекционный мононуклеоз никогда не протекает в виде эпидемий - отмечаются только отдельные (спорадические) случаи или небольшие локальные вспышки. Передается вирус воздушно-капельным путем, но для заражения требуется длительный контакт с больным. Еще вирусные частицы можно обнаружить в слюне больного или вирусоносителя, и вторым путем передачи возбудителя может быть контактный: болезнь передается через игрушки или другие предметы, на которые попала инфицированная слюна.
После заражения вирус проникает в слизистую оболочку верхних дыхательных путей, размножается там, проникает в миндалины и лимфатические узлы. Он поражает практически все лимфоузлы, печень, селезенку. Взамен В-лимфоцитов, зараженных и поврежденных вирусом, организм начинает вырабатывать новые клетки, получившие название "атипичные мононуклеары". Они отсутствуют у здоровых людей, а их название определило современное название болезни - "мононуклеоз".
Симптомы
Первые признаки заболевания можно обнаружить через неделю-две после заражения. Иногда инкубационный период более длительный (может увеличиваться до 1-1,5 месяцев).
Заболевание начинается остро, с быстрым подъемом температуры до высоких цифр (38-39°С). У больного увеличиваются все лимфатические узлы, особенно заднешейные, затылочные и подчелюстные. Их увеличение заметно на глаз, при надавливании они безболезненны.
Практически всегда при инфекционном мононуклеозе поражается носоглотка и миндалины. У больных отмечается заложенность носа и затруднение носового дыхания, осиплость голоса. Дети часто храпят во сне. Небные миндалины (гланды) увеличены и воспалены, часто на них появляются налеты (сплошные или в виде отдельных островков), которые могут быть похожими на налеты при дифтерии. Их появление обычно сопровождается еще большим (до 39-39,5°С) повышением температуры и ухудшением самочувствия. Несмотря на воспалительные изменения, боли в горле у больных, как правило, нет (или она незначительна), выделения из носа тоже отсутствуют.
У всех больных обнаруживается увеличение печени и селезенки. Иногда появляется желтуха. Но тяжелых гепатитов при инфекционном мононуклеозе не бывает. Увеличение печени может сохраняться длительно, ее размеры обычно нормализуются только через 1-2 месяца от начала заболевания.
В разгар заболевания только у некоторых больных появляются высыпания на коже. Но сыпь возникает практически всегда в том случае, если больного лечили ампициллином - широко распространенным антибиотиком. Эта сыпь пятнистая, ярко-красная, очень похожая на аллергическую, держится 6-14 дней и проходит самостоятельно без какого-либо лечения. Ее появление не означает, что у больного аллергия на ампициллин и другие пенициллиновые антибиотики. Просто вирус Эпштейна-Барр непонятным образом "извращает" реакцию организма на их введение.
Течение инфекционного мононуклеоза обычно заканчивается за 2-4 недели, но иногда может затянуться до полутора месяцев.
В-лимфоциты, которые поражает вирус Эпштейна-Барр, - это одни из главных клеток иммунной системы. Поэтому заболевание сопровождается ослаблением иммунитета и повышенной восприимчивостью ребенка к другим инфекциям. Эти инфекции вызываются уже не вирусами, а, как правило, бактериями и расцениваются как осложнения инфекционного мононуклеоза. Например, каждый десятый ребенок после ангины, вызванной самим вирусом, переносит еще одну ангину, вызванную стрептококком. Также возможны гнойные отиты (воспаления среднего уха), бронхиты и воспаление легких.
Диагностика
Симптомы инфекционного мононуклеоза достаточно характерны - увеличение лимфоузлов, ангина, увеличение печени и селезенки, повышение температуры. Но не всегда каждый из этих признаков достаточно выражен, поэтому правильно поставить диагноз может только врач. В обязательном порядке назначается лабораторное исследование: диагноз выставляют в случае обнаружения в общем анализе крови характерных для инфекционного мононуклеоза клеток - атипичных мононуклеаров. Чем больше их количество, тем тяжелее протекает заболевание. Кроме того, современные лабораторные методы позволяют обнаружить в крови и сам вирус (точнее, его генетический материал), с этой целью широко используется ПЦР - полимеразная цепная реакция.
Всех больных инфекционным мононуклеозом обследуют на ВИЧ-инфекцию (дело в том, что ее ранние стадии тоже могут сопровождаться мононуклеозо-подобными симптомами). Консультация врача нужна и для того, чтобы исключить другие грозные болезни - злокачественные заболевания крови и дифтерию. Отличить инфекционный мононуклеоз от дифтерии или обычной ангины помогает бактериологическое исследование (больным делают мазок с небных миндалин, а затем посев на дифтерийную палочку и стрептококки, если эти бактерии не обнаружены - вероятность диагноза "инфекционный мононуклеоз" значительно возрастает).
Опасный вирус
Помимо инфекционного мононуклеоза, вирус Эпштейна-Барр считают виновником еще ряда более серьезных недугов: рассеянного склероза - хронического заболевания, при котором вследствие нарушений работы иммунной системы повреждаются нервные волокна, что ведет к постепенной утрате различных функций нервной системы (нарушениям зрения, потере координации, двигательным расстройствам и т.д.); онкологических заболеваний системы кроветворения; синдрома хронической усталости, который имеет разные причины и характеризуется повышенной утомляемостью, постоянным чувством сильной усталости, болями в мышцах, сонливостью и депрессией, которые длятся месяцами, а иногда и годами.
Лечение
До настоящего времени нет доступного и эффективного лекарства, которое могло бы быстро уничтожить вирус в организме. Поэтому лечение направлено в первую очередь на облегчение симптомов заболевания и предупреждение развития осложнений. Больных с легкими формами лечат на дому. Детей госпитализируют в инфекционный стационар только при тяжелых формах инфекции, выраженном увеличении печени и селезенки, появлении желтухи, а также в случае необходимости подтверждения диагноза и исключения других заболеваний.
Очень важен постельный режим в остром периоде заболевания (в среднем от 1 до 3 недель): есть вероятность травмирования увеличенной селезенки и даже ее разрывов. По этой же причине детям ограничивают физическую нагрузку в течение полугода после перенесенного заболевания.
Для снижения температуры при инфекционном мононуклеозе используют парацетамол или препараты на его основе. Аспирин категорически не рекомендуется, поскольку его применение, особенно при этом заболевании, может спровоцировать развитие синдрома Рея (тяжелого поражения печени и головного мозга). Для облегчения носового дыхания назначают сосудосуживающие капли в нос, для профилактики бактериальной ангины и фарингита - полоскание зева и глотки растворами антисептиков (раствором фурациллина, настойками календулы, ромашки или шалфея). Для уменьшения интоксикации необходимо обильное теплое питье.
В некоторых случаях (тяжелое течение заболевания, значительное увеличение селезенки и лимфатических узлов) приходится назначать кортикостероидные гормоны (преднизолон), которые оказывают противовоспалительное действие.
Как бы тяжело ни протекало заболевание, оно заканчивается выздоровлением. Но нарушения в иммунной системе могут сохраняться достаточно продолжительное время (до 6 месяцев). В течение этого времени ребенок имеет повышенную восприимчивость к различным инфекциям, поэтому необходимо ограничивать его контакты с другими людьми. Организм еще долго восстанавливается после болезни: ребенок быстро утомляется, капризничает, жалуется на плохой аппетит еще несколько месяцев после выздоровления. На это время нежелательно планировать дальние поездки, в том числе и "на оздоровление", при необходимости выполнения плановых прививок их переносят на более поздний срок.
Перенесенное заболевание оставляет после себя стойкий иммунитет: несмотря на то, что вирус навсегда сохраняется в организме, рецидивов инфекционного мононуклеоза практически не бывает. Повторные заражения тем более невозможны.
Вирус Эпштейна-Барр имеет онкогенную активность (может вызывать онкологические заболевания крови), поэтому детей, у которых после клинического выздоровления длительно не восстанавливается нормальный состав клеток крови, обязательно направляют на консультацию к врачу-гематологу, у которого они в последующем длительно могут находиться на диспансерном учете.
Профилактика инфекционного мононуклеоза сводится к ограничению контактов с больными. Поскольку вирус малозаразен, то при появлении случая заболевания в организованном детском коллективе (в яслях, детском саду) никаких карантинных мероприятий не проводится - достаточно обычной влажной уборки. Детей, которые были в контакте с заболевшим, наблюдают 20 дней. Это максимальный инкубационный период заболевания, и если дети не заболели в течение этого времени - значит, заражения не было.
Специфической профилактики инфекционного мононуклеоза (например, прививок) до настоящего времени нет.
По медицинским вопросам обязательно предварительно проконсультируйтесь с врачом


Слово – нашему эксперту, старшему научному сотруднику Центрального научно-исследовательского института эпидемиологии, врачу-инфекционисту высшей категории, кандидату медицинских наук Василию Шахгильдяну.
Мнение. Распознать инфекционный мононуклеоз очень сложно.
На самом деле. Это не совсем так. Хотя стертых форм этой болезни, возбудитель которой вирус Эпштейна–Барр (ВЭБ) относится к семейству герпесвирусов, действительно значительно больше, особенно в детском возрасте. У детей инфицирование ВЭБ часто не проявляется клинически.
Заражение вирусом в юношеском возрасте в 75% случаев приводит к развитию инфекционного мононуклеоза. Наиболее тяжелое течение острой ВЭБ-инфекции наблюдается у лиц старше 25 лет. Для болезни характерны повышение температуры до 38–39 °C, общее недомогание, боль в горле, выраженное увеличение передних и боковых шейных, реже заднешейных и затылочных лимфоузлов, признаки тонзиллита или фарингита с яркой гиперемией (покраснением) слизистой оболочки мягкого неба, отеком небных и глоточных миндалин, при котором возникают характерное затруднение дыхания, гнусавость голоса. Возможно также наличие длительно сохраняющегося налета на миндалинах, увеличение печени и селезенки, развитие отечности мягких тканей вокруг шейных лимфоузлов, что приводит к одутловатости лица.
Однако столь острые проявления бывают лишь у 20–30% заболевших мононуклеозом, который врачи нередко ошибочно принимают за фолликулярную ангину и начинают лечить антибиотиками.
Мнение. Инфекционный мононуклеоз – заразное заболевание.
Инфицирование ВЭБ может произойти с первых месяцев жизни, но инфекционный мононуклеоз наиболее часто регистрируется у детей 3 –14 лет, подростков и взрослых до 30 лет. Пик частоты инфекционного мононуклеоза приходится на возраст 14–18 лет.
Совет. Запретить подросткам целоваться, конечно, невозможно. И оградить малышей от заражения вирусом через игрушки в детском саду сложно. Но ограничить тесный контакт с болеющим взрослым или ребенком необходимо. Специалисты не перестают повторять: соблюдайте бытовую культуру!
Мнение. Инфекционный мононуклеоз опасен.
На самом деле. Инфекционный мононуклеоз – доброкачественное заболевание, которое чаще всего проходит и без лечения. Но иногда мононуклеоз может привести к выраженной ангине, напоминающей стрептококковую, клинически выраженному гепатиту, значительному увеличению размеров селезенки. Иные осложнения мононуклеоза редки, но возможны. Среди них: пневмония, миокардит, поражение нервной системы (энцефалит, менингит, миелит).
И, наконец, очень важно отличить мононуклеоз от так называемого мононуклеозоподобного синдрома, который возможен при других, более серьезных и опасных заболеваниях: острой ВИЧ-инфекции, острой цитомегаловирусной инфекции, фолликулярной ангине, дифтерии, дебюте острого лейкоза.
Совет. При подозрении на наличие у вас или вашего ребенка мононуклеоза необходимо пройти всестороннее обследование, которое, помимо упомянутых анализов крови, должно в себя включать обязательный осмотр лор-врачом, повторные клинический и биохимический анализы крови, УЗИ органов брюшной полости.
Мнение. При лечении мононуклеоза без антибиотиков не обойтись.
На самом деле. Как и при других вирусных заболеваниях, применение антибиотиков при инфекционном мононуклеозе не показано (за исключением тех случаев, когда у пациента развилось бактериальное осложнение). Антибиотики снижают иммунитет, тем самым лишь утяжеляя течение заболевания.
При мононуклеозе нет смысла и в приеме иммуномодуляторов и индукторов интерферона, которые сплошь и рядом назначают больным инфекционным мононуклеозом педиатры и терапевты. Эффективность этих небезобидных (особенно для детей) средств не доказана.
Совет. В большинстве случаев инфекционный мононуклеоз не требует лечения. Однако при тяжелом течении заболевания есть смысл начать прием противогерпетических препаратов (ацикловира и его аналогов) в максимально возможных высоких дозах. Лечение следует продолжать не менее двух недель.
Мнение. После мононуклеоза полгода нельзя делать операции и прививки.
На самом деле. Из-за астенического синдрома (слабости. – Ред.), который нередко возникает после перенесенной болезни, а также возможного поражения печени, нарушений в иммунной системе целесообразно в течение трех месяцев после перенесенного инфекционного мононуклеоза ограничить физические нагрузки, по возможности перенести на более поздний срок плановые операции и прививки.
справочника
Инфекционные болезни, фармакотерапия
Инфекционный мононуклеоз (лат., mononucleosis infectiosa) – вирусное антропонозное заболевание с преимущественно воздушно-капельным механизмом передачи, вызывается в большинстве случаев Эпштейна-Барр вирусом и характеризуется лихорадкой, поражением ротоглотки, лимфатических узлов, печени, селезёнки и специфическими изменениями гемограммы.
Долгое время развитие инфекционного мононуклеоза (ИМ) связывали только с вирусом Эпштейна-Барр (EBV). Сегодня в возникновении ИМ доказана роль других возбудителей, преимущественно группы герпесвирусов. Актуальность проблемы обусловлена высокой степенью инфицированности населения во всём мире, лёгкостью заражения, часто латентным течением заболевания и пожизненной персистенцией вируса в организме человека.
Наиболее изученным среди герпесвирусов является ЕВV. В последнее время ЕВV-инфекция стала наиболее распространённой в Украине (антитела к ЕВV выявляют у 15% детей до 1 года и у 90% взрослых).
Доказана этиологическая роль вируса Эпштейна-Барр для таких заболеваний, как лимфома Беркитта, лимфогранулематоз, назофарингеальная карцинома, других злокачественных опухолей. Вирус может поражать центральную и периферическую нервную систему, с развитием серозного менингита, энцефалита, арахноидита, полирадикулоневрита, является оппортунистической инфекцией при СПИДе. Появляется всё больше свидетельств того, что вирус Эпштейна-Барр может вызывать патологические изменения в печени, почках, соединительной ткани, провоцировать возникновение болезни Альцгеймера, синдрома хронической усталости, аутоиммунных процессов.
Клинические проявления болезни впервые описал Н.Ф. Филатов (1885) и
Е. Пфайффер (1889). В соответствии с характерными изменениями гемограммы, американские учёные Т. Спрэнт и Ф. Эдванс назвали заболевание инфекционным мононуклеозом. Возбудитель был выделен из клеток лимфомы Бёркитта в 1964 году М.А. Эпштейном и И. Барр.
Эпштейн-Барр вирус – ДНК геномный вирус, принадлежит к семейству герпесвирусов (Herpesviridae) подсемейству g-herpesviruses, тропный к В-лимфоцитам. Размеры вируса – 180-200 нм. Выделяют А и В штаммы. В отличие от других герпесвирусов, не вызывает гибели клеток, а активирует их пролиферацию.
EBV имеет четыре основные антигена: ранний антиген (EA), капсидный антиген (VCA), мембранный антиген (МА), ядерный антиген (ЕВNA).
Культивируют EBV в культуре клеток (В-лимфоцитов) человека и приматов.
Вирус нестойкий в условиях внешней среды, быстро гибнет при высушивании, при действии высоких температур и дезинфектантов.
Источник инфекции: человек с манифестной или субклинической формой инфекции.
Механизм передачи: воздушно-капельный, контактный прямой (через слизистые или кожу), непрямой (через бытовые предметы, медицинский инструментарий, трансфузии биологических жидкостей), реже – вертикальный.
Обычно заболеваемость носит спорадический характер, иногда регистрируются случаи в виде семейных вспышек. Восприимчивость к данной инфекции высокая. Географическая распространённость: штамма А – повсеместная, штамма В – преимущественно в странах Азии и Африки.
Иммунитет: типоспецифический, нестерильный.
Входными воротами инфекции является слизистая оболочка носоглотки и верхних дыхательных путей. Лимфогенно возбудитель попадает в регионарные лимфатические узлы, где развивается первичный лимфаденит. В случае преодоления лимфатического барьера через 30-50 дней возникает вирусемия и происходит генерализация процесса. Следующая фаза патогенеза – инфекционно-аллергическая, которая предопределяет волнообразное течение болезни. Последняя фаза – формирование иммунитета и выздоровление. Поражение лимфоидной и ретикулярной ткани приводит к увеличению в крови количества лимфоцитов, моноцитов и наличия моноцитоподобных лимфоцитов. Вирус не разрушает инфицированные клетки, а стимулирует их размножение, может долго персистировать в лимфоцитах, стимулируя их пролиферацию и дифференцировку в плазмоциты. Одновременно в острый период возрастает количество Т-лимфоцитов. Т-супрессоры сдерживают пролиферацию В-лимфоцитов, цитотоксические Т-лимфоциты уничтожают пораженные вирусом клетки. Вирус остается в организме человека и персистирует всю жизнь, обуславливая хроническое течение инфекции. Реактивация процесса наступает при снижении иммунитета. Во время интенсивного разрушения инфицированных клеток в лимфо- и кровоток попадает значительное количество антигенов вируса, вызывающих общую аллергическую реакцию. Патогенез последней изучен плохо. Появляются разнообразные антитела, в том числе против собственных нейтрофилов, лимфоцитов, ампициллина. Антитела против VCA та ЕВNA сохраняются всю жизнь.
Инфекционный мононуклеоз относится к ВИЧ-ассоциированным заболеваниям.
Гистологически обнаруживают генерализованную гиперплазию лимфатической и ретикулярной ткани всех органов и систем, а также инфильтрацию мононуклеарного характера, иногда – неглубокий очаговый некроз в печени, селезенке, почках, центральной нервной системе.
Инкубационный период составляет 20-50 дней. ИМ может протекать бессимптомно или проявляться умеренными катаральными явлениями со стороны верхних дыхательных путей. В случае поступления большого количества инфекта и/или ослабления иммунной системы у пациента может развиваться клиническая картина заболевания.
Клинические формы ИМ:
• типичная;
• атипичная – мезаденит, псевдоаппендицит, гепатит, нефрит, пневмония, респираторная;
• инфекционный мононуклеоз неуточнённый.
Течение: острое, затяжное, хроническое.
Степень тяжести: легкая, средней тяжести, тяжёлая.
Типичная форма ИМ характеризуется триадой клинических симптомов – лихорадкой, ангиной, гепатоспленомегалией. В первые 3-5 дней могут наблюдаться продромальные явления в виде умеренной головной боли и вялости, затем появляются основные клинические проявления: лихорадка, боль в горле, фарингит, лимфаденопатия, гепатоспленомегалия, гепатит, кожные высыпания. Лихорадка, как правило, длится в течение 5-10 дней, но может сохраняться свыше 2 недель. Обычно температура повышается до 39-40 °С. При осмотре миндалины увеличены, отёчны, иногда смыкаются между собой. Поражение носоглоточной миндалины приводит к затруднению носового дыхания, пациент дышит полуоткрытым ртом. Задняя стенка глотки также отечна, гиперемирована, с увеличенными фолликулами (гранулезный фарингит), покрыта густой слизью. На 5-17-й день болезни у 25% больных на мягком небе появляются петехии. В первые дни болезни, а иногда и через 3-4 дня, на миндалинах могут возникать налёты разной величины и характера, преимущественно вызванные активацией сопутствующей бактериальной флоры. Важным признаком ИМ является лимфаденопатия, с преимущественным увеличением шейных, особенно заднешейных, лимфоузлов, расположенных цепочкой по заднему краю m. sternoсleidomastoideus (они плотные, чувствительные при пальпации, размером от 1 до 4 см в диаметре). Иногда наблюдается массивное увеличение медиастинальных лимфатических узлов, что приводит к затруднению дыхания. При увеличении мезентериальных лимфоузлов появляется острая боль в животе. Лимфаденопатия занимает от нескольких дней до нескольких недель и даже месяцев. Спленомегалия отмечается примерно у 50% больных ИМ. Увеличение селезенки обычно наблюдается на 2-3-й неделе заболевания и может быть умеренным или значительным, но протекать бессимптомно. У подавляющего большинства больных наблюдается гепатомегалия. Максимальных размеров печень достигает на 4-10-й день заболевания. При ее пальпации отмечается умеренная болезненность. Иногда появляется незначительная желтушность кожи и склер, гипербилирубинемия. У 70-80% больных ИМ выявляется минимальное повышение активности трансаминаз в сыворотке крови. У 3-19% больных ИМ в разгаре заболевания возникает сыпь на коже (чаще на туловище и руках), которая держится несколько дней и по характеру может быть пятнисто-папулезной (кореподобная), точечной (скарлатиноподобная), эритематозной, уртикарной, геморрагической. На слизистой оболочке ротовой полости появляется энантема. При ИМ поражаются практически все органы. В литературе описаны висцеральные формы ИМ с поражением отдельных органов (нервные, легочные, сердечные, желудочно-кишечные, печеночные, почечные).
После первичной EBV-инфекции в организме наблюдается персистенция вируса, которая может клинически никак не проявляться (бессимптомное вирусоносительство или латентная форма инфекции). Однако возможна реактивация процесса в виде хронической рецидивирующей EBV-инфекции, по типу хронического ИМ, генерализованной формы хронической активной инфекции с поражением ЦНС, миокарда, почек и др., EBV-ассоциированного гемофагоцитарного синдрома, стертой или атипичной формы с длительным субфебрилитетом и клиникой вторичного иммунодефицита, онкологического лимфопролиферативного процесса, аутоиммунных заболеваний (СКВ, ревматоидный артрит, синдром Шегрена и др.), синдрома хронической усталости.
Осложнения
Присоединение вторичной бактериальной микрофлоры (стафилококк, стрептококк и проч.) с развитием бактериального воспаления верхних дыхательных путей. Неврологические осложнения: асептический менингит, энцефалит, менингоэнцефалит, синдром Гийена-Барре, паралич Белла, поперечный миелит. Гематологические осложнения: лейкопения, тромбоцитопения, тромбоцитопеническая пурпура, аутоиммунная анемия. Сердечно-сосудистые осложнения: миокардит, перикардит. Тяжёлым и очень редким осложнением может быть разрыв селезенки. В период реконвалесценции возможно развитие интерстициального нефрита аутоиммунного генеза.
В 90-95% случаев при отсутствии осложнений заболевание после манифестного периода переходит в латентную форму. У больных с иммунодефицитом, особенно у ВИЧ-инфицированных, часто развиваются тяжелые формы с поражением ЦНС и летальным исходом.
Эпидемиологический анамнез – учет особенностей эпиданамнеза.
Клинический – наличие характерной триады симптомов.
Лабораторные исследования
• Общий анализ крови: лейкоцитоз (до 15-30х10 9 /л), реже – нормальное количество лейкоцитов или лейкопения, лимфоцитоз, моноцитоз, незначительное увеличение СОЭ. В начале болезни у большинства больных снижается количество сегментоядерных и увеличивается содержание палочкоядерных нейтрофилов. Характерный признак – наличие атипичных мононуклеаров (вироцитов). Они появляются в крови в разгар заболевания и сохраняются в течение 2-3 недель, а иногда и нескольких месяцев. Количество вироцитов колеблется от 5-10 до 50% и выше. Существует прямая связь между количеством вироцитов и тяжестью болезни.
• Биохимический анализ крови: повышение уровня трансаминаз, билирубина.
• Специфические лабораторные методы: EBV вызывает все случаи серопозитивного ИМ.
ИФА:
1. Определение NA, ЕА антигенов – показатели острого процесса.
2. Определение VCA, МА антигенов – показатели хронического процесса.
3. Анти-VCA EBV IgM могут определяться уже в инкубационный период и сохраняются еще 2-3 месяца после клинико-лабораторного выздоровления.
4. Анти-VCA EBV IgG появляются после анти-VCA EBV IgM и сохраняются пожизненно.
5. Анти-ЕА EBV (маркеры тяжелого течения) появляются через несколько недель после начала заболевания и исчезают через несколько месяцев после выздоровления.
6. Анти-NA EBV появляются через 3-4 недели после начала заболевания и могут сохраняться пожизненно.
7. ПЦР ДНК EBV в сыворотке крови, слюне и других биологических средах.
Возбудителями серонегативных ИМ могут быть цитомегаловирус, токсоплазма, вирусы краснухи, гепатита А, герпеса человека 6 типа (HHV-6), иммунодефицита человека (HIV), аденовирусы.
Инструментальные исследования
Рентгенологические исследования, ЭКГ, УЗИ, КТ, МРТ.
Консультации специалистов
При наличии показаний: окулист, невропатолог, пульмонолог, кардиолог, гастроэнтеролог.
Дифференциальный диагноз
Дифференциальный диагноз необходимо проводить с бактериальной ангиной, дифтерией миндалин, краснухой, скарлатиной, листериозом, аденовирусной инфекцией, бруцеллёзом, СПИДом, туберкулёзом лимфатических узлов, вирусными гепатитами, лимфогранулематозом, лимфосаркомой, лимфолейкозом.
Острый ИМ не требует противовирусного лечения. В тяжелых случаях показано применение короткого курса глюкокортикостероидных гормонов. Иммуностимулирующую терапию при ИМ проводят только в период ремиссии. В острый период ИМ рекомендуются полоскания горла растворами антисептиков, приём гипосенсибилизирующих и симптоматических средств. В случае присоединения вторичной бактериальной инфекции, назначают антибактериальные препараты, за исключением ампициллина и его аналогов. В стадии реактивации ИМ применяют ганцикловир и фоскарнет. Противовирусный эффект ганцикловира после окончания его приема длительный. В лечении хронической активной EBV-инфекции используют также a-интерферон, специфический иммуноглобулин человека против вируса Эпштейна-Барр. В тяжелых случаях применяют иммуноглобулин человека нормальный. Другие методы лечения имеют второстепенное значение. Хирургическое лечение при опухолях челюстей противопоказано из-за значительной васкуляризации опухоли и опасности кровотечения. Лучевая терапия оказывает местный противоопухолевый и обезболивающий эффекты.
Общие меры профилактики аналогичны таковым при ОРВИ. Неспецифическую профилактику осуществляют повышением общей и иммунологической резистентности организма.
Больные EBV-инфекцией не требуют строгой изоляции. Взрослые, перенесшие ИМ, не могут быть донорами. После выписки из стационара больные подлежат диспансерному наблюдению.
Меры специфической профилактики не разработаны.
Читайте также:


