Железодефицитная анемия при воспалении и инфекциях
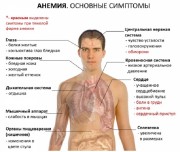
Железодефицитная анемия (малокровие) – патологический синдром, характеризующийся уменьшением количества эритроцитов и гемоглобина крови. Она является основной гипоксии тканей и органов, так как к клеткам доставляется мало кислорода. Особо опасно данное состояние для головного мозга. Нервные клетки при гипоксии погибают, что приводит к постепенной деградации личности. На начальных этапах заболевания человек чувствует постоянную усталость и снижение работоспособности. Если при этих симптомах выполнить лабораторный анализ крови, в нем определяется снижение уровня гемоглобина и эритроцитов. Анемия железодефицитная — очень распространенный недуг, который встречается как у взрослых людей, так и у детей. Она может развиваться по ряду некоторых причин и представляет собой серьезное заболевание, которое необходимо лечить. В противном случае анемия может нанести существенный ущерб здоровью.
Почему недостаток железа вызывает заболевание
Для взрослого человека нормой является наличие в организме до 5 г железа. Установлено, что механизм заболевания связан с дефицитом минерала железа в крови. Его роль трудно преувеличить. Ведь из всего количества 70% непосредственно заняты в построении гемоглобина. Это значит, что железо — незаменимый материал для удержания эритроцитами молекул кислорода и последующего процесса переноса от легочных пузырьков в ткани. Любой вариант недостатка железа приводит к снижению синтеза гемоглобина и кислородному голоданию всего организма.
Важно не только поступление минерала с пищей (в организме железо не вырабатывается), но и правильный процесс его усвоения и переноса. За всасывание молекул железа из 12-перстной кишки отвечает специальный белок (трансферрин). Он доставляет железо в костный мозг, где синтезируются эритроциты. Организм образует "склад" в печеночных клетках для быстрого восполнения в случае острого недостатка. Запасы хранятся в виде гемосидерина.
Выведение излишков минерала происходит с мочой, калом, через потовые железы. У женщин с подросткового возраста до климактерического периода есть еще путь менструальных кровотечений. В сутки выводится около 2 г железа, значит поступать с пищей должно не меньшее количество. От правильного функционирования этого механизма зависит поддержание нужного баланса для обеспечения тканевого дыхания.
Причины возникновения
Необходимым условием развития недостаточности является превышение потребления тканями железа над его поступлением. Железодефицит провоцируют следующие состояния (перечислены по степени распространенности):
- Кровопотеря хроническая (суточная потеря крови 5-10 мл) - частые носовые кровотечения; желудочные и кишечные кровотечения; обильная менструация; патология почек с характерной гематурией.
- Острая (массивная кровопотеря) - травмы, обширные ожоги; неконтролируемое донорство; патологические кровотечения (например, маточное при онкопатологии и др.).
- Недостаточное поступление железа - изнуряющие диеты и голодание; несбалансированное питание; вегетарианство.
- Снижение уровня усвоенного железа - заболевания ЖКТ, глистная инвазия; старческий и младенческий возраст.
- Повышение уровня необходимого железа - активный рост (1-2 год и подростковый период); беременность, лактация (необходимость в железе повышается вдвое до 30 мг/сут.); становление менструального цикла; физические нагрузки, спорт; частые воспаления (ОРВИ и др.).
- Врожденная анемия у детей - недоношенная беременность; анемия у беременной.
В зависимости от глубины дефицита железа различают 3 степени тяжести ЖДА:
- Легкая – значения гемоглобина находятся в пределах 110 – 90 г/л;
- Средняя – содержание Hb колеблется от 90 до 70 г/л;
- Тяжелая – уровень гемоглобина падает ниже 70 г/л.
Симптомы заболевания
Симптоматика зависит от степени развития болезни. О начале заболевания свидетельствуют следующие признаки: снижение концентрации внимания; утомляемость; ухудшение памяти; снижение аппетита; головокружение; снижение работоспособности; вялость; раздражительность; расслоение ногтей; кожа становится сухой. По мере усугубления анемического состояния эти симптомы становятся более выраженными. Уже на латентной стадии больные указывают на такие субъективные симптомы как: сухая слизистая языка; пощипывание языка; изменение вкуса — больные отдают предпочтение соленым, кислым и острым блюдам; затруднение глотания; ощущение инородного тела в горле при глотании; учащенное сердцебиение. При осмотре врач отмечает и объективные первые признаки анемии: атрофированные сосочки языка; ощущение зуда и жжения в области вульвы при железодефицитной анемии у женщин; хейлит (заболевание, которое проявляется поражением губ в виде их побледнения, мацерации с поперечными трещинами и ярко-красной каймой на линии смыкания губ).
Врачи отмечают, что выраженность симптоматики зависит не только от степени анемии, но и от возраста больного и продолжительности болезни. С течением времени симптоматика расширяется. Отмечаются следующие изменения:
Ø Со стороны кожных покровов. Кожа приобретает характерный зеленоватый оттенок, становится бледной. На щеках быстро возникает румянец, кожа теряет упругость, становится морщинистой, трескается.
Ø Со стороны волос. Волосы тоже становятся сухими, ломкими, приобретают сероватый оттенок и теряют блеск, становятся более редкими, быстро седеют.
Ø Со стороны ногтей. Ногтевые пластины истончаются, теряют блеск, становятся плоскими, а при более тяжелых формах анемии отмечается койлонихия, когда ногти принимают вогнутую форму.
Ø Со стороны мышечной системы. Мышечная слабость — признак, который характерен только для анемии, вызванной дефицитом железа.
Ø Со стороны слизистых оболочек. Оболочки пищеварительного тракта, дыхательных и половых органов атрофируются.
Ø Со стороны органов чувств. При тяжелых формах болезни изменяется обоняние, больной приобретает извращенные вкусовые привычки, например начинает есть мел, лед, известку, сырые крупы и пр.
При адекватном лечении, в частности при помощи препаратов железа, такая симптоматика быстро исчезает.
Диагностика железодефицитной анемии
В первую очередь очень важно правильно определить тип анемии, поскольку существуют признаки, общие для всех типов анемий. Для этого необходима полная лабораторная диагностика пациента. Она включает в себя следующие мероприятия: анализ крови (общий и биохимический), пункцию костного мозга, консультацию узкого специалиста. Для этого женщин направляют к гинекологу, поскольку нередко причина анемии кроется в заболеваниях матки или ее придатков. Мужчин направляют к урологу и проктологу, поскольку анемия у мужчин может развиваться на фоне геморроя или заболеваний предстательной железы. Только после постановки окончательного диагноза и выявления причин анемии врач составляет индивидуальную схему лечения.
Лечение железодефицитной анемии
Проводится лечение железодефицитной анемии только длительным приёмом препаратов железа внутрь в умеренных дозах, причём существенный прирост гемоглобина, в отличие от улучшения самочувствия, будет не скорым — через 4—6 недель. Перечень железосодержащих препаратов, который легко выяснить, не является руководством к действию, назначать и рассчитывать дозу – дело лечащего врача. Лечебные дозы назначаются до нормализации уровня гемоглобина, затем пациента переводят на профилактические дозы.
Диета
Международная ассоциация гематологов утверждает, что при нормализации пищевого поведения пациента с признаками легкой степени железодефицитной анемии, можно в значительной степени нормализовать показатели крови и не прибегать к применению препаратов железа для устранения железодефицитного состояния. Больным тяжелой формой анемии показано применение специализированной диеты в качестве дополнения к основному лечению. Основополагающими принципами лечебного питания при железодефицитной анемии является резкое ограничение употребления жиров как растительного, так и животного происхождения, а также обогащение продуктами, содержащими большое количество белка. Доказано, что на усвоение организмом железа никаким способом не влияют углеводы, поэтому их потребление не стоит ограничивать.
Для того чтобы восполнить необходимый для нормального кроветворения уровень железа, необходимо включить в рацион питания пациента большое количество продуктов, содержащих железо (печень, говяжий язык, постное мясо индейки, красные виды морской рыбы, гречневая и пшенная крупы, черника и персик). Большой процент железа также содержится во всех видах зелени, говядине и яйцах. Среди фруктов следует отдавать предпочтение хурме, айве и яблокам в сыром или запеченном виде. Из рациона питания больным с железодефицитной анемией рекомендовано полностью исключить продукты молочного ряда и черный чай, так они содержат в своем составе вещества, препятствующие всасыванию железа. И, напротив, продуктами-синергистами, которые следует в большом количестве употреблять совместно с железосодержащими продуктами, являются те, которые содержат большой процент витамина С (щавель, смородина, квашеная капуста, свежевыжатые фруктовые и цитрусовые соки с мякотью).
Профилактика
Экспертами ВОЗ были сформулированы основные догмы профилактических мер, направленных на снижение уровня распространения железодефицитных анемий среди населения. Главными путями достижения этой цели считаются: употребление в рационе пищи, обогащенной легко усваиваемой формой железа; применение средств, способствующих улучшению всасывания железа; лечение хронических очагов инфекций. Кроме того, профилактика железодефицитной анемии делится на первичную, вторичною и соответственно третичную. Цель первичной – устранить основной фактор, способствующий анемизации организма, вторичной – своевременно выявить признаки, вовремя грамотно диагностировать и пролечить заболевание. Цель же третичной профилактики – сведение к минимуму возможных осложнений.
В подавляющем числе случаев железодефицитная анемия успешно поддается коррекции, признаки и симптомы анемии отступают. Однако при отсутствии лечения развиваются осложнения и болезнь прогрессирует. Если у человека выявлен пониженный уровень гемоглобина, то необходимо пройти полное клинико-лабораторное обследование и выявить причину анемии. Правильно поставленный диагноз – залог успешного лечения.
Анемии являются довольно частым вторичным синдромом при гастроэнтерологических заболеваниях. Основными видами анемий, выявляемых у гастроэнтерологических больных, являются: железодефицитная анемия (ЖДА), анемия хронических заболеваний (АХЗ), гемолитическа
Анемии являются довольно частым вторичным синдромом при гастроэнтерологических заболеваниях. Основными видами анемий, выявляемых у гастроэнтерологических больных, являются: железодефицитная анемия (ЖДА), анемия хронических заболеваний (АХЗ), гемолитическая анемия, В12- и фолиеводефицитная анемия, гипо-, апластические анемии.
ЖДА — наиболее частая форма анемий в гастроэнтерологии, и причиной ее развития являются кровотечения, нарушения всасывания железа, диетические ограничения. Второй по распространенности после ЖДА в детской гастроэнтерологии является АХЗ, которая отличается достаточными запасами железа в организме, но снижением насыщения им трансферрина, сниженным или нормальным уровнем сывороточного железа. Причина развития АХЗ заключается в действии провоспалительных цитокинов (интерлейкина 1-альфа и интерлейкина 1-бета, фактора некроза опухоли альфа, гамма-интерферона и др.).
Воспалительные заболевания кишечника
Воспалительные заболевания кишечника (ВЗК), прежде всего, неспецифический язвенный колит (НЯК) и болезнь Крона (БК), часто сопровождаются развитием анемии. Частота анемии при ВЗК, по данным литературы, достаточно вариабельна и колеблется от 6% до 74% [17]. В большинстве исследований это значение составляет 35–50% [9, 12, 13, 19, 25, 27]. С несколько большей частотой анемия выявляется у больных НЯК. Так, S.?Schreiber и соавт. [26] сообщили о наличии анемии у 25% больных с БК и 37% больных с НЯК.
В развитии анемии при ВЗК всегда играют роль несколько механизмов. Условно можно выделить следующие группы причин возникновения анемии при ВЗК [2, 4, 7, 13, 17, 18, 20]:
Наиболее часто у больных ВЗК комбинируются АХЗ и железодефицитная анемия [1, 4, 17, 18], однако роль других факторов тоже велика и выраженность анемии может усиливаться вследствие повторных эпизодов кровотечения, дефицита витаминов и нутриентов, влияния лекарственных препаратов.
Анемия хронических заболеваний была впервые описана Maxwell Wintrobe и George Cartwright в 1949 году. Основными критериями ее диагностики являются снижение уровня сывороточного железа и насыщения трансферрина железом при сохранных запасах железа в ретикулоэндотелиальной ткани (нормальный уровень ферритина).
Успехи в расшифровке основных механизмов АХЗ привели к повышенному вниманию к этому виду анемии, в том числе и в педиатрии. Установлено, что на долю АХЗ приходится около 10–20% всех анемий.
На сегодняшний день главным звеном в патогенезе АХЗ считается гиперпродукция провоспалительных цитокинов. Они приводят к угнетению синтеза эритропоэтина и значительно снижают его эффекты, направленные на усиление пролиферации и созревания эритроидных предшественников [1–4, 13].
Нарушение метаболизма железа при АХЗ во многом опосредовано экспрессией гепсидина. Гепсидин — это белок острой фазы воспаления, который синтезируется печенью в ответ на воздействие липополисахаридов бактерий и интерлейкина 6. Гепсидин снижает всасывание железа в двенадцатиперстной кишке, блокирует высвобождение железа из макрофагов и снижает способность красного костного мозга его усваивать. Недостаточное поступление железа в эритроидные клетки приводит к нарушению их созревания и снижению синтеза гема [3, 14].
Участие провоспалительных цитокинов в генезе АХЗ при ВЗК обусловлено как прямым их ингибирующим действием (в первую очередь, гамма-интерферона) на созревание эритроидных клеток и усилением процессов апоптоза, так и опосредованными эффектами: подавлением синтеза эритропоэтина, снижением чувствительности к нему эритроидных клеток, активацией синтеза гепсидина и нарушением утилизации железа, а также усилением свободно-радикальных реакций [5, 10, 14].
В течение последних двадцати лет в отделении гастроэнтерологии Российской детской клинической больницы (РДКБ) наблюдалось 155 пациентов с НЯК и 61 пациент с БК. Анемия выявлялась у 35% детей с НЯК и имела железодефицитный характер, обусловленный преимущественно хронической кровопотерей. В 69% случаев анемия была легкой степени, в 27% — среднетяжелой, а в 4% — тяжелой. Тяжесть анемии в значительной степени зависела от обширности поражения толстой кишки и выраженности язвенного процесса.
Снижение уровня гемоглобина (110 г/л ≤ Hb
А. В. Малкоч*, кандидат медицинских наук
С. В. Бельмер*, доктор медицинских наук, профессор
Н. А. Анастасевич*
Е. В. Семенова*
Л. М. Карпина**
Н. Е. Щиголева**
И. А. Матина**
А. П. Пономарева**
*РГМУ, **Российская детская клиническая больница, Москва
НИИ детской гематологии Минздрава России
Кровь, будучи внутренней средой организма, несет в себе стигматы жизнедеятельности различных органов и систем, изучение которых имеет несомненное клиническое значение, необходимо для диагноза, прогноза течения и контроля за терапией практически всех внутренних болезней человека.
- подавляющее большинство автоматических счетчиков не определяет молодые формы лейкоцитов, нормобласты и ретикулоциты - эти данные можно получить только "вручную";
- нормативные значения никогда не выражаются одной цифрой, существует предел допустимых колебаний (он представлен в таблице для всех показателей), в который укладывается 99,9% нормы.
Показатели красной крови.
- Анемия при хронической почечной недостаточности
- Анемия при эндокринной патологии.
- Анемия при раке.
- Гемолитические анемии, иммунные и неиммунные.
- Апластическая анемия.
- Миелодиспластический синдром.
- Мегалобластная В-12 – дефицитная (пернициозная) анемия.
- Мегалобластная фолиеводефицитная анемия.
- Аутоиммунная гемолитическая анемия.
Остановимся подробнее на железодефицитной анемии и анемии при хроническом воспалении, диагностика и лечение которых являются прерогативой врачей-терапевтов и не требуют специальных гематологических исследований.
Клиническая картина ЖДА складывается из следующих клинических синдромов:
- сывороточное железо ниже 12,5 мкмоль/л
- общая железосвязывающая способность (ОЖСС) выше 64,4 мкмоль/л
- ферритин сыворотки ниже 12 мкг/л.
Нормобластоз в периферической крови бывает редко и всегда свидетельствует о серьезной патологии. Его появление закономерно наблюдается при тяжелых формах гемолитической анемии и у пациентов, перенесших спленэктомию. Обнаружение нормобластов в крови пациентов, не страдающих этой патологией, должно явиться поводом для поиска онкологической патологии.
Об эритроцитозе можно говорить при следующих показателях крови: эритроциты выше 5,7х10*12/л у мужчин и 5,2х10*12/л у женщин, гемоглобин выше 177 г/л и 172 г/л соответственно, гематокрит выше 52% и 48% соответственно.
Значительно чаще встречаются вторичные эритроцитозы, обусловленные повышенным образованием эритропоэтина в ответ на артериальную гипоксию или при некоторых опухолях.
Вторичные эритроцитозы могут быть разделены на следующие группы:
- Опухоли почек, гипернефрома
- Опухоль надпочечников
- Гемангиома мозжечка
- Рак яичников
- Киста
- Гидронефроз
- Стеноз почечной артерии
- Кобальтовое отравление
Нейтрофилезом называется увеличение числа нейтрофилов более 6х10*9/л.
Нейтропения – снижение числа нейтрофилов менее 1,8 х 10*9/л.
Агранулоцитоз - снижение числа нейтрофилов менее 0,5 х 10*9/л.
Эозинофилия – увеличение числа эозинофилов выше 0,4 х 10*9/л.
Моноцитоз – число моноцитов выше 0,8 х 10*9/л.
- Инфекции (особенно туберкулез, эндокардит, сифилис).
- Лихорадка неясного происхождения
- Различные формы неоплазий и миелопролиферативных болезней.
- Хронические воспаления (особенно холецистит и ревматоидный полиартрит)
- Состояние после спленэктомии.
Гипертромбоцитозом считается увеличение числа тромбоцитов более 400,0 х 10*9/л.
- После оперативных вмешательств ( около 2-х недель).
- После спленэктомии (до 1 года).
- При злокачественных опухолях
- При острой постгеморрагической и гемолитической анемиях.
- При некоторых воспалениях (туберкулез, острый ревматизм, язвенный колит, остеомиелит).
СОЭ - скорость оседания эритроцитов представляет собою неспецифическую реакцию. В норме она составляет у мужчин до 50 лет - 2-15 мм в час, а у женщин до 50 лет - 2-20 мм в час. После 50 лет у мужчин до 20 мм в час, а у женщин - до 30 мм в час.
Д.Т. Абдурахманов
Кафедра терапии и профболезней ГБОУ ВПО "Первый МГМУ им. И.М. Сеченова" Минздравсоцразвития РФ, Москва
Обсуждается проблема железодефицитной анемии (ЖДА), развивающейся в т. ч. при заболеваниях желудочно-кишечного тракта. Представлены сведения, касающиеся причин возникновения ЖДА, патогенеза, симптоматики, диагностики и лечения данной патологии. Особое внимание уделено препарату Феринжект (железа карбоксимальтозат), который применяется в комплексной терапии пациентов с ЖДА, обусловленной воспалительными заболеваниями кишечника.
Ключевые слова: железодефицитная анемия, дефицит железа, ферротерапия, железа карбоксимальтозат
The article discusses the problem of iron deficiency anemia (IDA), which develops against the background of many diseases, including gastrointestinal diseases. The data on the causes of IDA, pathogenesis, symptoms, diagnosis and treatment of this disease are presented. Particular attention is paid to the drug Ferinject (ferric carboxymaltosate) used for the treatment of IDA in patients with inflammatory bowel diseases.
Key words: iron deficiency anemia, iron deficiency, ferrotherapy, ferric carboxymaltosate
Наиболее частая в популяции причина анемии — дефицит железа в организме. По данным отчета Всемирной организации здравоохранения (ВОЗ) о состоянии здоровья за 2002 г., железодефицитная анемия (ЖДА) входит в десятку глобальных факторов риска развития нетрудоспособности. Так, показано, что ЖДА встречается среди 30 % населения планеты [1]. В США ЖДА наблюдается среди 5-12 % небеременных женщин и 1-5 % мужчин [2].
Метаболизм железа в организме
Общее количество железа в организме взрослого человека составляет около 3,5-4,0 г, в среднем 50 и 40 мг/кг у мужчин и женщин соответственно. Основная часть железа входит в состав гемоглобина эритроцитов (около 2,5 г), значительная часть железа (около 0,5—1,0 г) депонируется в составе ферритина или входит в состав гемсодержащих и других ферментов (миоглобина, каталазы, цитохромов) организма (около 0,4 г) и небольшая часть железа (0,003—0,007 г) находится в связанном с трансферрином состоянии в крови.
Баланс железа в организме поддерживается соответствием количества поступающего железа его потерям. В пище железо присутствует в составе гема или как негемовое железо. Ежедневно с пищей (стандартный пищевой рацион) в организм человека поступает 10—20 мг железа, из которого в норме в кишечнике всасывается около 10 % (от 3 до 15 %), что компенсирует суточные потери железа, главным образом при слущивании эпителиальных клеток. Организм обеспечивает баланс железа в организме, регулируя процесс его всасывания в кишечнике. В случае развития дефицита железа организм увеличивает процент всасываемого железа (может достигать 25 %), при избытке — уменьшает [3]. В этом процессе ключевое значение придают гепсидину — белку, который синтезируется в печени. Поступление с пищей или выведение железа, как правило, вне контроля организма.
Около 25—30 мг железа ежедневно реутилизируется после разрушения (вследствие старения) эритроцитов в селезенке и поступает снова в костный мозг для синтеза новых эритроцитов. Железо, которое всасывается в кишечнике, предварительно на поверхности энтероцита восстанавливается с участием ферроредуктаз из трехвалентного (Fe 3+ ) в двухвалентнтное (Fe 2+ ), затем с помощью специфического переносчика — транспортера двухвалентных металлов (DMT1) поступает в цитоплазму [4]. Железо в составе гема (содержится в мясе, рыбе) всасывается напрямую. В дальнейшем двухвалентное железо с помощью другого переносчика, ферропортина (также мобилизует железо из ферритина), секретируется в кровь, где снова окисляется до трехвалентного (при участии белка гефестина) и связывается с плазменным белком трансферрином [5]. Трансферрин осуществляет транспорт железа в костный мозг, где оно утилизируется для синтеза эритроцитов, или преимущественно в печень, где железо депонируется в составе ферритина (рис. 1) [6].
При снижении запасов железа, гипоксии, анемии, усиленном эритропоэзе в печени снижается синтез гепсидина, что усиливает всасывание железа в кишечнике, при хроническом воспалении синтез гепсидина в печени увеличивается и, соответственно, всасывание железа в кишечнике снижается.
Ферритин — ключевой белок, отражающий запасы железа в организме. Он депонирует железо в нетоксической форме, которое при необходимости мобилизуется. В среднем одна молекула ферритина содержит до 4500 атомов железа. Главным образом железо депонируется в печени, костном мозге и селезенке. Снижение уровня ферритина в сыворотке крови является достаточно надежным показателем дефицита железа в организме, его увеличение, как правило, указывает на перегрузку организма железом. В то же время необходимо помнить, что ферритин относится к белкам острой фазы воспаления, поэтому увеличение его содержания в крови может быть следствием активного воспалительного процесса, а не телько избытка железа. В ряде случаев некоторые злокачественные опухоли обладают способностью синтезировать и секретировать в кровь большое количество ферритина (в рамках паранеопластического синдрома). В норме содержание ферритина в сыворотке крови составляет 30-300 нг/мл.
Причины железодефицитной анемии
Выделяют три глобальные причины развития дефицита железа в организме (рис. 2):
1. Недостаточное поступление с пищей или повышенная потребность.
2. Нарушение всасывания железа в кишечнике.
3. Хронические потери крови.
В популяции наиболее частой причиной ЖДА является недостаточное поступление с пищей: по данным ВОЗ, от четверти до трети населения в мире хронически голодают из-за нехватки продуктов питания, особенно мясной пищи. Однако в клинической практике среди основных причин ЖДА выделяют хронические потери крови, прежде всего из желудочно-кишечного тракта.
Клиническая картина
При ЖДА наблюдаются общие для всех анемий проявления циркуляторно-гипоксического синдрома:
Кроме того могут встречаться специфические признаки тканевого дефицита железа:
Диагностика
Лабораторная диагностика ЖДА основана на изучении обмена железа и выявлении его дефицита. Выделяют ряд признаков, указывающих на железодефицитный характер анемии (табл. 1).
Таблица 1
Лабораторные признаки дефицита железа и ЖДА
| Параметры | Значения при ЖДА | Норма | |
| Железо сыворотки, мкг/дл | 3 | 5 | Примечание. НПВС - нестероидные противовоспалительные средства.
Среди причин ЖДА (почти 30-50 % всех случаев) прежде всего рассматривают острые или хронические кровопотери из ЖКТ. Основной причиной ЖДА у женщин до менопаузы являются беременность и менструации, у женщин после менопаузы и у мужчин — хронические (латентные) потери крови из ЖКТ. Анализ кала на скрытую кровь — основной скрининговый метод выявления скрытого желудочно-кишечного кровотечения (тест положительный при выделении не менее 10 мл крови в сутки). При потере не менее 30 мл крови в сутки тест на скрытую кровь бывает положительным в 93 % случаев [8]. Наиболее часто при хронической ЖДА и особенно в случаях положительного результата кала на скрытую кровь выполняют эзофагогастродуодено- (ЭФГДС) и колоноскопию. В 5-10 % случаев анемий, связанных с заболеваниями ЖКТ, при ЭФГДС и колоноскопии не удается выявить очага поражения [9]. В 25 % случаев это обусловлено небольшим размером пораженного участка, который обнаруживается при повторном осмотре, в остальных случаях необходимо обследование тонкой кишки. В последние годы наиболее часто для выявления источника кровотечения из тонкой кишки используется беспроводная капсульная эндоскопия. В 10-17 % случаев причиной ЖДА у мужчин и женщин старше 40 лет являются онкологические заболевания ЖКТ; прежде всего колоректальный рак. ЖДА в течение длительного времени может быть единственным проявлением рака толстой кишки правосторонней локализации, при этом размер опухоли обычно превышает 3 см. Другая наиболее частая причина ЖДА -язвенная болезнь желудка и двенадцатиперстной кишки. При скрытых кровопотерях, обусловленных поражением тонкой кишки, наиболее часто в возрасте до 40 лет выявляют опухоли (лимфому, карциноид, аденокарциному, полипоз), ангиоэктазию артерий (Dieulafoy’s поражение), целиакию и болезнь Крона, в возрасте старше 40 лет -патологию сосудов различной природы и прием НПВС. У трети больных воспалительными заболеваниями кишечника (болезнь Крона, язвенный колит) выявляется анемия, имеющая сложный генез (сочетание ЖДА и анемии хронических заболеваний). При этом дефицит железа становится следствием нескольких причин:
Лечение Суточная терапевтическая доза элементарного железа при лечении ЖДА для взрослых составляет в среднем 100— 200 мг в 2—3 приема. Поливитаминные комплексы, содержащие железо, не рекомендуют в качестве лечения ЖДА, т. к. они содержат недостаточное количество железа либо оно плохо всасывается в кишечнике. При адекватном лечении уже в течение первых 3 суток наблюдается увеличение числа ретикулоцитов в крови, на 7—10-й день отмечается ретикулоцитарный криз (пик ретикулоцитоза). К 3—4-й неделе лечения имеет место увеличение уровня гемоглобина на 20 г/л. Прием препаратов железа необходимо продолжать еще в течение 3—6 месяцев после нормализации уровня гемоглобина — пока насыщение трансферрина железом не превысит 30 % и концентрация ферритина не достигнет 50 нг/мл (показатель восстановления тканевых запасов железа). Среди 20—30 % пациентов в результате приема препаратов железа отмечаются различные диспептические расстройства (тошнота, дискомфорт в эпигастрии, диарея или запор). Риск развития желудочно-кишечных расстройств можно снизить, принимая препарат во время еды или на ночь, а также при постепенном увеличении дозы. Среди причин неэффективности пероральных форм железа рассматривают целый ряд факторов [10]: недостаточное поступление железа; Нарушение всасывания железа: Продолжающиеся потери крови или повышенная потребность в железе: Сопутствующие заболевания или состояния: Неправильный диагноз или наличие других причин анемии: Выделяют следующие показания к парентеральному введению, преимущественно внутривенному, препаратов железа: Основная опасность при парентеральном введении железа — развитие тяжелых аллергических реакций, включая анафилактических шок с летальным исходом, которые наблюдаются в 0,6—1,0 % случаев. Данные реакции, в основном, характерны для препаратов железа, содержащих декстран. Среди парентеральных препаратов железа широкое распространение, особенно в комплексной терапии воспалительных заболеваний кишечника, получили сахарат железа и железа карбоксимальтозат (Феринжект), которые в отличие от декстрана железа ассоциируются с минимальным риском развития анафилактических и других аллергических реакций [11—13]. Так, в 2011 г. были опубликованы результаты рандомизированного контролируемого исследования применения железа карбоксимальтозата пациентами с железодефицитной анемией, обусловленной воспалительными заболеваниями кишечника (FERGIcor — a Randomized Controlled Trial on Ferric Carboxymaltose for Iron Deficiency Anemia in Inflammatory Bowel Disease) [14]. В исследовании сравнивали эффективность и безопасность нового режима фиксированной дозы железа карбоксимальтозата (Феринжекта) и индивидуально рассчитываемых доз сахарата железа (СЖ) для пациентов с воспалительными заболеваниями кишечника и ЖДА. В исследование были включены 485 пациентов с ЖДА (уровень ферритина ЛИТЕРАТУРА Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу. Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции
|

