Заложенность носа при инфекционном мононуклеозе

Герпесвирусные инфекции широко распространены среди детей и взрослых. По данным ВОЗ до 90 % взрослого и детского населения планеты инфицировано герпесвирусами, причем у 50 % из них отмечают манифестное, рецидивирующее течение вызываемых ими заболеваний. Инфекционный мононуклеоз является наиболее характерным типичным клиническим проявлением герпесвирусных инфекций. В мире инфекционным мононуклеозом ежегодно заболевают от 16 до 800 лиц на 100 тыс. населения. В России ежегодно регистрируют 40–80 случаев инфекционного мононуклеоза на 100 тыс. населения [1, 2, 3, 5]. Большинство клиницистов связывают инфекционный мононуклеоз с вирусом Эпштейна – Барр, хотя в настоящее время доказана роль цитомегаловируса (5-й тип) и вируса герпеса человека 6-го типа, а также вирусов простого герпеса 1-го, 2-го типов в этиологии заболевания [5]. Установлена роль вируса Эпштейна – Барр в развитии злокачественных новообразований, аутоиммунных, неврологических заболеваний и синдрома хронической усталости [3, 8, 9, 10]. Показано, что после перенесённой инфекции новое поколение В-клеток содержит несколько генокопий вируса Эпштейна – Барр в латентной форме, в результате чего вирус может длительно персистировать в организме, вызывая иммунодефицитное состояние и повышая риск развития онкогематологических заболеваний [8, 9]. В крови у часто болеющих детей выявлена определённая концентрация цитомегаловируса и вируса Эпштейна – Барр. Вероятно, персистенция инфекции приводит к возникновению иммунной недостаточности, на фоне которой формируется частая заболеваемость [1, 4]. В последние годы доказана гепатотропность герпетических вирусов, которые могут вызывать различные поражения печени – от бессимптомного гепатита до гепатоцеллюлярной карциномы [2].
Инфекционным мононуклеозом преимущественно болеют дети: их доля в суммарной заболеваемости достигает 65–80 %. Исключение составляют дети первых 6–7 месяцев жизни, защищенные материнскими антителами [6].
Целью исследования является анализ особенностей клинического течения инфекционного мононуклеоза у детей в современных условиях.
Материал и методы исследования
Для проведения исследования была проведена экспертная оценка 32 историй болезни больных с инфекционным мононуклеозом. Под наблюдением находились дети, госпитализированные в инфекционный стационар г. Чебоксары. Лабораторная диагностика проводилась методом качественного иммунохроматографического экспресс-теста для определения специфических IgМ-антител к вирусному капсидному антигену (VCA) вируса Эпштейна–Барр в сыворотке крови, методом иммуноферментного анализа с определением в крови маркеров Эпштейн–Барр вирусной инфекции (IgM VCA), определялась ДНК-EBV методом полимеразной цепной реакции.
Для статистической обработки данных исследования использован параметрический метод с определением доверительных границ средних величин и относительных показателей генеральной совокупности. Заданная степень вероятности безошибочного прогноза Р=95 %, при этом t=2. Проводился корреляционный анализ с определением коэффициента корреляции Пирсона.
Из 32 наблюдаемых пациентов мальчики составляли 69 %, девочки – 31 % (22 и 10 детей соответственно).
Максимальная заболеваемость инфекционного мононуклеоза приходится на 4–8-летний возраст, дети первого года жизни болеют редко. В нашем исследовании большинство заболевших (44 %) составили дети дошкольного возраста, самой малочисленной группой (3 %) оказались дети грудного возраста, детей от 1 до 3 лет было 22 %, 7–12 лет – 22 %, старше 12 лет – 9 %.
Согласно данным некоторых исследований, этиология инфекционного мононуклеоза зависит от возраста [2]. Так, у детей первых 4 лет жизни чаще (37,2 %) определяется цитомегаловирусная этиология; у детей в возрасте от 4 до 7 лет чаще наблюдается Эпштейн – Барр вирусная инфекция (76,2 %) с манифестными формами заболевания с характерными клиническими симптомами и гематологическими изменениями (атипичные мононуклеары выявлены у 94,6 % пациентов); в старших возрастных группах достоверно чаще развивается микст-инфекция, тяжелая степень болезни, чаще встречается поражение печени. Риск хронизации инфекции возникает с 4-летнего возраста и более характерен для подростков и взрослых [2].
Наблюдаемые нами пациенты с инфекционным мононуклеозом были обследованы с целью выяснения этиологии заболевания. У всех больных подтверждена причастность к заболеванию вируса Эпштейна – Барр: у 19 % детей методом полимеразной цепной реакции в пробе крови, у 31 % – методом иммуноферментного анализа, у 50 % – с помощью экспресс-теста для определения специфических IgМ VCA.
У 56 % детей диагностировано заболевание средней степени тяжести, у 44 % – тяжёлой.
По данным литературы наиболее часто больными предъявляются жалобы на затруднение носового дыхания (52,3 %), боль в горле (68,5 %), недомогание (59 %), головную боль (44,5 %), боль в животе, тошноту, рвоту (15 %), озноб (10 %) [2].
У большинства обследуемых детей (47 %) наблюдались жалобы на заложенность носа, на боль в горле жаловались 19 %, недомогание – 35 %, головную боль – 10 %, боль в животе, рвоту – 7 %, кашель – 13 % детей.
Температура у больных мононуклеозом в течение первых 2–5 дней чаще бывает субфебрильной, а в период разгара поднимается выше 38 ºС в 83 % случаев и держится на протяжении первых двух недель болезни, иногда – месяц. Увеличение лимфоузлов и ангина наиболее выражены в первые две недели, наблюдаются в 98–99,3 % и 80,7–96 % соответственно, гепатоспленомегалия – на второй-третьей неделе (41–100 %) [2, 3, 5, 6]. Лимфоузлы увеличиваются симметрично, они болезненны, но подвижны, размеры их варьируются от мелкой горошины до грецкого ореха или куриного яйца. Чаще всего страдают заднешейные и затылочные лимфоузлы, но встречается и генерализованное увеличение. В клинической картине часто лидирует ангина, при этом в 85 % случаев на миндалинах появляются различные наложения. Небные миндалины отечны, налеты могут быть беловато-желтоватого или грязно-серого цвета, легко снимаются, ткань миндалины после снятия налёта обычно не кровоточит. Гиперемия ротоглотки обычно умеренно выражена, боль в горле незначительная. У 5 % больных появляется пятнисто-папулезная или папулезная сыпь, обычно на туловище и руках. Инфекционный мононуклеоз в большинстве случаев длится 2–4 нед. [3, 6, 7].
В нашем исследовании у всех детей наблюдалось повышение температуры, причём у большинства (75 %) её значение превышало 38 ºС. Увеличение лимфоузлов обнаруживалось у всех пациентов, преимущественно шейных групп. Изменения в ротоглотке характеризовались лёгкой гиперемией в 50 %, умеренной – в 22 %, яркой – в 28 % случаев. Увеличение миндалин зарегистрировано у 72 % детей, в 6 % случаев – III степени, при этом у 6 % больных наблюдался отёк нёбных дужек и миндалин. Наложения на миндалинах обнаружены у 81 % пациентов, по форме они были сплошными у 22 %, островчатыми – у 37 %, точечными – у 22 % детей, цвет их был в 19 % случаев жёлтым, в 66 % – белым. Гепатоспленомегалия выражена во всех возрастных группах, за исключением детей старшего школьного возраста, что подтверждено данными ультразвукового исследования. При проведении корреляционного анализа гепатоспленомегалии выявлена прямая высокая положительная корреляционная связь – коэффициент корреляции Пирсона 0,87 (рисунок). У 6 % детей наблюдалась экзантема. При проведении лабораторного исследования периферической крови выявлены атипичные мононуклеары у всех пациентов (таблица).
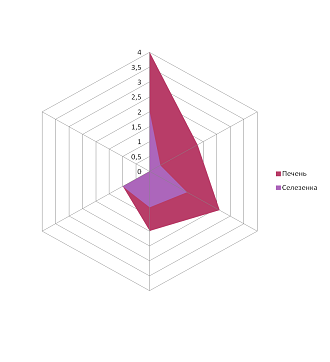
Гепатоспленомегалия при инфекционном мононуклеозе, прямая корреляционная связь
Клинические признаки и лабораторные показатели инфекционного мононуклеоза
Роспотребнадзор (стенд)
Об инфекционном мононуклеозе и профилактике
Инфекционный мононуклеоз вызывается вирусом Эпштейна-Барр (ВЭБ).
Естественная восприимчивость человека к ВЭБ высока.
До 60% заболевших инфекционным мононуклеозом - это лица в возрасте 2–20 лет.
В социально неблагополучных и густонаселенных регионах большинство детей заражается уже в раннем и младшем возрасте.
Около 50% взрослого населения переносят инфекцию в подростковом возрасте. Максимальная заболеваемость у девочек отмечается в возрасте 14-16 лет, у мальчиков - в 16-18 лет. К 30-35 годам у большинства людей в крови выявляют антитела к вирусу инфекционного мононуклеоза.
Контагиозностьзаболевания невысокая.
Большое значение в распространении инфекционного мононуклеоза имеют не столько больные с развернутой клинической картиной, сколько со стертыми и нетипичными формами.
Классификация заболевания
Выделяют стертую, абортивную, субклиническую формы, форму инфекционного мононуклеоза с развернутой клинико-гематологической картиной заболевания.
Клиническая картина инфекционного мононуклеоза
Инкубационный период при инфекционном мононуклеозе, чаще всего, составляет от 7 до 12 дней (может достигать 21 дня).
Типичная форма заболевания, как правило, начинается остро, с повышения температуры до 38-40 0 С и появления синдрома интоксикации. Высокая температура тела сохраняется обычно 4-10 дней, однако иногда повышение температуры может затягиваться до 2-4 нед. (как правило, в этом случае имеет место субфебрилитет). У некоторых детей температурная реакция может отсутствовать.
Синдром интоксикации проявляется выраженными в разной степени слабостью, вялостью, снижением аппетита, миалгиями и артралгиями, нарушением сна и т.д.
Из других групп лимфатических узлов могут быть резко увеличены (до 2-4 см) подчелюстные лимфоузлы. Пораженные лимфоузлы не спаяны между собой, мягкие или слегка уплотненные на ощупь, обычно безболезненные. Кожа над ними не изменена. Выраженное увеличение лимфоузлов сохраняется около 7-14 дней, однако незначительная полиаденопатия может сохраняться на протяжении 2-3 месяцев и более.
Обычно, одновременно с поражением лимфоузлов развивается аденоидит. Клинически это проявляется заложенностью носа без насморка или с небольшим отделяемым из носа, чаще серозного или слизистого характера. Больным с аденоидитом не помогают сосудосуживающие капли.
Поражение небных миндалин проявляется с первых дней болезни или спустя 3-5 дней. Тонзиллит может носить катаральный характер или выглядеть как лакунарная, реже - фолликулярная или некротическая ангина.
Частый признак инфекционного мононуклеоза - гепатолиенальный синдром (увеличение печение и селезенки), который может проявляться как с начала заболевания, так и спустя 3-5 дней.
Экзантема (высыпания на кожных покровах) при естественном течении заболевания встречается редко (у 5-7% заболевших). Экзантема может появиться в первые дни применения антибиотиков, на 6-8-й день или спустя 2-3 дня после их отмены. Сыпь сохраняется в течение 7-10 дней и обычно оставляет после себя пигментацию.
У 0,5-1% больных инфекционным мононуклеозом развиваются различные варианты поражения нервной системы: энцефалит или менингоэнцефалит, парезы черепных нервов (чаще VII пары), полирадикулоневриты, острый мозжечковый синдром. Обычно они исчезают без последствий.
Из прочих возможных осложнений следует отметить отиты, паратонзиллиты, синуситы, пневмония.
Дифференциальную диагностикуинфекционного мононуклеоза проводят с дифтерией, острыми стрептококковыми поражением зева, лимфомами, острыми лейкозами, эпидемическим паротитом, туляремией, сальмонеллезом, бруцеллезом, при экзантемах – с краснухой и корью.
Лечение заболевания
Специфического лечения не существует. Эффективным средством терапии является системное применение интерферона. При тяжелом течении, выраженной лимфопролиферативной реакции показано назначение глюкокортикостероидов.
В последнее время считается необходимым назначения иммунокорригирующего лечения.
Профилактика инфекционного мононуклеоза
Так как путь заражения – воздушно-капельный, то все меры профилактики сходны с профилактическими мерами относительно острых респираторных заболеваний.
Индивидуальные меры профилактики направлены на предотвращение заражения и распространения заболевания за пределы очага инфекции; для этого нужно:
• находиться в маске в одном помещении с больным;
• в комнате проводить влажную уборку не менее двух раз в день;
• все предметы обрабатывать слабым деизифицирующим раствором;
• изолировать больного в отдельное помещение.
Больных госпитализируют по клиническим показаниям.
Общая профилактика включает соблюдение правил личной гигиены, укрепление иммунитета, ограничение контактов с больными людьми и носителями инфекции.


Инфекционный мононуклеоз
Патогенез заболевания связан с внедрением вируса в В-лимфоциты с последующей их пролиферацией, гиперплазией лимфоидной и ретикулярной ткани.
Клиническими проявлениями болезни являются: повышение температуры тела, интоксикация, ангина, увеличение лимфатических узлов преимущественно шейной группы, гепато- и спленомегалия.
Редкими, но тяжелыми осложнениями инфекционного мононуклеоза являются разрыв селезенки и неврологическая симптоматика.
Диагностируется инфекционный мононуклеоз на основании клинических симптомов, изменений в клиническом анализе крови и выявлении специфических антител в крови.
Лечение заболевания симптоматическое.
-
Эпидемиология Источником вируса являются больные с клинически выраженными или стертыми формами болезни, а также здоровые вирусоносители. От больных вирус выделяется в инкубационном периоде, весь период клинических проявлений и с 4-й по 24-ю неделю в периоде реконвалесценции.
Механизм передачи инфекции аэрозольный. Путь передачи - воздушно-капельный. Реализуется при непосредственном контакте (при поцелуе, через руки, игрушки и предметы обихода). Возможен половой и трансплацентарный пути передачи.
Естественная восприимчивость к вирусу инфекционного мононуклеоза высокая.
Распространено заболевание повсеместно.
Большинство заболевших - дети, подростки, молодые люди от 14 до 29 лет. Чаще болеют лица мужского пола. При заражении в раннем детском возрасте первичная инфекция протекает в виде респираторного заболевания, в более старшем возрасте - бессимптомно. К 30-35 годам у большинства людей в крови выявляют антитела к вирусу инфекционного мононуклеоза, поэтому клинически выраженные формы среди взрослых встречаются редко.
Заболеваемость спорадическая в течение всего года с двумя умеренно выраженными подъемами весной и осенью.
- Классификация Общепринятой классификации не существует. По степени тяжести различают инфекционный мононуклеоз:
- Легкой степени тяжести.
- Средней степени тяжести.
- Тяжелое течение.
- Код МКБ 10 В27 - Инфекционный мононуклеоз.
- Этиология Возбудителем заболевания является ДНК-геномный В-лимфотропный вирус человека (вирус Эпштейна-Барр), относящийся к семейству Herpesviridae, подсемейству Gammaherpesviridae, роду Lymphocryptovirus.
Вирус малоустойчив во внешней среде. Быстро погибает при высыхании, под действием высокой температуры, при обработке всеми дезинфицирующими средствами.
- Патогенез
Проникновение вируса в верхние отделы дыхательных путей приводит к поражению эпителия и лимфоидной ткани рото- и носоглотки. При последующей вирусемии возбудитель внедряется в В-лимфоциты, вызывает их пролиферацию и диссеминирует по всему организму. Распространение вируса вызывает гиперплазию лимфоидной и ретикулярной ткани, вызывая отечность носовых раковин и слизистой оболочки ротоглотки, увеличение миндалин, полиаденопатию, увеличение печени и селезенки.
Репродукция вируса происходит в основном в В-лимфоцитах периферической крови, которые активно размножаются и секретируют иммуноглобулины различных классов, в первую очередь IgM. Пролиферация инфицированных В-лимфоцитов ограничивается Т-лимфоцитами, количество которых, как и В-лимфоцитов, значительно возрастает в остром периоде инфекции, что обуславливает появление в периферической крови атипичных мононуклеаров (огромные клетки округлой формы с большим ядром и резко базофильной протоплазмой).
У лиц с нормальной иммунной системой вирусный антиген на поверхности В-лимфоцитов распознается и уничтожается Т-киллерами; увеличивается активность Т-супрессоров, которые тормозят пролиферацию и дифференциацию В-лимфоцитов; образуются специфические цитотоксические клетки, распознающие инфицированные лимфоциты и уничтожающие их. В результате наступает клиническое выздоровление, но сам вирус персистирует в лимфоцитах пожизненно.
- Основные симптомы инфекционного мононуклеоза
- Чаще подострое начало заболевания.
- Повышения температуры тела.
- Отечность и одутловатость верхней половины лица. век.
- Увеличенные лимфатические узлы шейной группы четко контурируются при повороте головы, в некоторых случаях увеличение лимфоузлов измененяет конфигурацию шеи - "бычья шея".
- Заложенность носа, гнусавый оттенок голоса.
- Острый тонзиллит (катаральный, фолликулярный или лакунарный).
- Гепатомегалия, спленомегалия со 2-й недели болезни.
- Изменения в клиническом анализе крови: лимфомоноцитоз более 60 %, появление атипичных мононуклеаров (более 15%).
В течении заболевания выделяют инкубационный период, начальный период, период разгара и период реконвалесценции.
- Инкубационный период. Продолжительность периода составляет в среднем 33-49 дней.
- Начальный период.
Возможно острое начало болезни с повышения температуры тела до 38-39°С, головной боли, тошноты, ломоты в теле.
У части больных начало заболевания постепенное: недомогание, слабость, заложенность носа, отечность век, пастозность верхней половины лица, субфебрильная температура.
В единичных случаях болезнь начинается с одновременного появления всех трех основных симптомов инфекционного мононуклеоза: лихорадки, острого тонзиллита, лимфаденопатии.
Продолжительность начального периода составляет 4-5 дней.Наступает к концу 1-й недели. Самочувствие больного ухудшается. Проявления: высокая температура, ангина, лимфоаденопатия, гепатоспленомегалия. Одним из основных симптомов периода разгара является ангина, с развитием которой появляется боль в горле. Сопровождается ангина симптомами интоксикации (озноб, головная боль, тошнота, ломота в теле), резким подъемом температуры тела (иногда выше 39°С).
Шейный лимфаденит при инфекционном мононуклеозе.
Периферические лимфатические узлы (в первую очередь шейная группа) в периоде разгара достигают максимальных размеров, слегка болезненны при пальпации, плотноваты на ощупь, подвижны, размеры их колеблются от горошины до грецкого ореха или куриного яйца. Особенностью лимфоаденопатии является симметричность поражения, а также появление отечности подкожной клетчатки вокруг лимфатических узлов, что может привести к изменению конфигурации шеи - "бычья" шея.
В начале 2-й недели инфекционного мононуклеоза в 50-80% случаев наблюдается спленомегалия, на 3-й неделе размеры органа нормализуются. Гепатомегалия наблюдается несколько позже, на 9-11-й день, у части больных размеры печени увеличиваются значительно. Увеличение печени сохраняется дольше увеличения селезенки. Иногда возможна незначительная желтушность склер и кожи.Температура тела нормализуется, исчезают наложения на миндалинах, признаки поражения носоглоточной миндалины, уменьшаются в размерах и становятся безболезненными при пальпации лимфатические узлы, нормализуются размеры селезенки, улучшается самочувствие больного.
Длительность периода различна у разных больных и в среднем составляет 3-4 недели. - Основные симптомы инфекционного мононуклеоза
- Особенности течения инфекционного мононуклеоза у взрослых Начинается заболевание постепенно с продромальных явлений, лихорадка сохраняется больше 2-х недель. Лимфаденопатия и гиперплазия миндалин выражены меньше, чем у детей, но чаще в процесс вовлекается печень с развитием желтушного синдрома.
Преобладают атипичные формы, особенно среди больных старше 35 лет: формы, протекающие без развития фарингита, лимфоаденопатии, без появления атипичных мононуклеаров в периферической крови. Диагностика в этих случаях проводится только с учетом результатов серологических исследований.
- Осложнения
- Разрыв селезенки. Редкое осложнение, встречается в 0,1-0,5% случаев. Как правило, без своевременного оперативного вмешательства приводит к летальному исходу.
- Гемолитическая анемия, иммунная тромбоцитопения как следствие гиперспленизма.
- Неврологические осложнения: менингит, энцефалит, острый психоз, острый мозжечковый синдром, парезы черепных нервов, радикуло- и полиневриты (синдром Гийена-Барре).
- Нарушения ритма сердца (блокада, аритмия), перикардит.
- Пневмония.
- Печеночная энцефалопатия, массивный некроз печеночных клеток.
- Острая почечная недостаточность.
- Асфиксия.
- Когда можно заподозрить инфекционный мононуклеоз?
- Подострое начало заболевания с повышения температуры.
- Выраженное увеличение лимфатических узлов шейной группы, в некоторых случаях это приводит к изменению конфигурации шеи - "бычья шея".
- Отечность, одутловатость верхней половины лица, век.
- Заложенность носа, "гнусавость" голоса.
- Острый тонзиллит.
- Несоответствие между степенью увеличения лимфоузлов и выраженностью изменений в ротоглотке: при значительном увеличении и отечности миндалин размеры лимфоузлов могут увеличиваться незначительно; и наоборот, при катаральном тонзиллите шейные лимфоузлы могут образовывать сплошной конгломерат.
- Гепато- и спленомегалия со 2-й недели болезни. Возможна желтуха.
- Сбор анамнеза
При сборе анамнеза уточняют остроту развития болезни, цикличность течения, определенный порядок появления симптомов, длительность их сохранения. Характерно постепенное начало заболевания с формированием полной клинической картины заболевания на 2-й неделе болезни.
На фоне нерезко выраженных симптомов интоксикации, отечности век и лица, затрудненного носового дыхания и увеличения шейных лимфатических узлов появляется боль в горле при глотании, развивается тонзиллит, что сопровождается повышением температуры тела до 38 °С и более. Общая продолжительность болезни может достигать 1, 5 мес. Лихорадка и симптомы острого тонзиллита сохраняются более 2 недель.При сборе эпидемиологического анамнеза выявляют возможные контакты с больными инфекционным мононуклеозом. Уточняют совместное проживание (общежитие, гостиница, квартира, казарма) и близкие контакты (пользование общей постелью, поцелуи) с больным ангиной или ОРЗ в течение последних 2 месяцев.
-
Физикальное исследование
Кожа и слизистые оболочки. На 1-й и 2-й неделях болезни выявляется отечность век, пастозность верхней половины лица, изменение тембра голоса ("гнусавость"). На 8-11-й день болезни возможна эфемерная сыпь, при тяжелом течении сыпь геморрагического характера.
При развитии гепатита выявляется желтушность кожных покровов и слизистых оболочек.
Задняя стенка глотки резко гиперемирована, слегка отечна, зернистая, с гиперплазированными фолликулами, покрыта густой слизью, на слизистой оболочке мягкого неба - геморрагические элементы.
Периферические лимфатические узлы. Увеличение лимфоузлов симметричное. В период разгара лимфоузлы достигают максимальных размеров, слегка болезненны при пальпации, плотноваты на ощупь, не спаяны между собой и с окружающей клетчаткой, окраска кожи над ними не изменена. Размеры лимфоузлов колеблются от горошины до грецкого ореха или куриного яйца.
Для инфекционного мононуклеоза характерно несоответствие между степенью увеличения лимфоузлов и выраженностью изменений в ротоглотке: миндалины могут быть значительно увеличены, отечны, покрыты сплошным плотным налетом, выходящим за их границы, а размеры лимфоулов при этом незначительно превышают обычные; и наоборот, при катаральном характере тонзиллита, шейные лимфоузлы больших размеров, иногда образуют сплошной конгломерат. Как правило, шейные лимфоузлы четко контурируются и хорошо видны при повороте головы.
Подкожная клетчатка вокруг лимфатических узлов отечна, что вместе с увеличенными лимфоузлами шеи может привести к изменению конфигурации шеи - "бычья" шея.
Органы дыхания. Носовое дыхание затруднено за счет значительного увеличения носоглоточной миндалины с первых дней болезни.
Органы кровообращения. Специфических изменений не наблюдается.
Органы пищеварения. Гепатомегалия. При пальпации край печени плотноэластической консистенции, слегка болезненный.
Органы мочевыделения. Изменений обычно не наблюдается.
Нервная система. Признаков нейротоксикоза даже при высокой лихорадке обычно не наблюдается. Но возможны симптомы мононеврита, радикулита, менингита, энцефалита.
-
Лабораторная диагностика
- Биохимический анализ крови . Умеренное увеличение активности АсАТ и АлАТ, повышение количества связанной фракции билирубина, тимоловой пробы. Функциональные пробы печени нормализуются к 15-20-му дню болезни, но могут оставаться измененными в течение 3-6 мес.
- Серологические методы.
- Определение сывороточных антител различных классов к капсидным (VCA) антигенам. Сывороточные антитела к капсидному белку вируса Эпштейн-Барр (анти-VCA IgM) обнаруживаются в инкубационном периоде; в дальнейшем их выявляют у всех больных (достоверное подтверждение диагноза). Снижение IgM к VCA-антигенам наблюдается через 2-3 мес после выздоровления, снижение содержания антител наблюдается через 3 недели, исчезновение происходит через 1-1,5 месяца.
После перенесенного заболевания пожизненно сохраняются антитела к ядерному антигену вирус Эпштейна-Барр IgG (Анти-EBNA IgG) . Антитела к ядерному антигену вирус Эпштейна-Барр IgG (Анти-EBNA IgG) чаще всего выявляются в крови через 3-12 месяцев ( в среднем через 4-6 месяцев) после инфицирования могут долгое время (несколько лет) обнаруживаться после заболевания. Концентрация антител нарастает в период выздоровления. Отсутствие антител к данному антигену при выявлении антител к капсидному белку вируса Эпштейна-Барр (анти-VCA IgM) скорее всего говорит о текущей инфекции. - Серологические методы обнаружения гетерофильных антител.
Реакция Пауля-Буннеля с эритроцитами барана (диагностический титр 1:32) и реакция Гоффа-Бауэра с эритроцитами лошади (более чувствительная). Применяются при отсутствии возможности определения анти-VCA-IgM (образуются в результате поликлональной активации В-лимфоцитов). Недостаточная специфичность реакций снижает их диагностическую ценность.
- Определение сывороточных антител различных классов к капсидным (VCA) антигенам. Сывороточные антитела к капсидному белку вируса Эпштейн-Барр (анти-VCA IgM) обнаруживаются в инкубационном периоде; в дальнейшем их выявляют у всех больных (достоверное подтверждение диагноза). Снижение IgM к VCA-антигенам наблюдается через 2-3 мес после выздоровления, снижение содержания антител наблюдается через 3 недели, исчезновение происходит через 1-1,5 месяца.
- Молекулярно-биологические исследования. Обнаружение вируса Эпштейн-Барр в крови (EBV) . Исследование крови проводится методом обнаружения ДНК вируса в полимеразной цепной реакции (ПЦР).
- Кровь на антитела к ВИЧ . Всем больным с инфекционным мононуклеозом или при подозрении на него нужно проводить 3-кратное (в острый период, затем через 3 и 6 месяцев) лабораторное обследование на антитела к ВИЧ , поскольку в стадию первичных проявлений ВИЧ-инфекции также возможен мононуклеозоподобный синдром.
- Для исключения стрептококковой ангины и других бактериальных инфекций делается посев из зева на микрофлору .
-
Клинический анализ крови. Умеренный лейкоцитоз, относительная нейтропения со сдвигом лейкоцитарной формулы влево, значительное увеличение количества лимфоцитов и моноцитов (суммарно более 60%).
Атипичные мононуклеары - клетки с широкой базофильной цитоплазмой, имеющие различную форму.
Характерно наличие атипичных мононуклеаров - клеток с широкой базофильной цитоплазмой, имеющих различную форму. Диагностическое значение имеет увеличение количества атипичных мононуклеаров с широкой цитоплазмой не менее чем до 10-12%, хотя число этих клеток может достигать 80-90%. Их появление в периферической крови может задерживаться до конца 2-3-й недели болезни, поэтому отсутствие атипичных мононуклеаров при характерных клинических проявлениях заболевания не противоречит предполагаемому диагнозу.
В период реконвалесценции количество нейтрофилов, лимфоцитов и моноцитов постепенно нормализуется, но атипичные мононуклеары могут сохраняться длительно. Метод ПЦР - позволяет выявлять вирусную ДНК в цельной крови и сыворотке.
- Инструментальные методы исследования
- УЗИ брюшной полости. Выявляется гепато-спленомегалия, увеличение мезентериальных лимфатических узлов.
- Рентгенография органов грудной клетки. Выявляется увеличение лимфоузлов средостения.
- Электрокардиографическое исследование (ЭКГ). При развитии миокардита выявляются нарушения ритма сердца.
- Дифференциальный диагноз Дифференциальный диагноз проводится со стрепококковым тонзиллитом, токсической формой дифтерии, аденовирусной инфекцией, корью, краснухой, токсоплазмозом, туберкулезом, генерализованной формой листериоза, псевдотуберкулезом, заболеваниями крови (острые лейкозы, агранулоцитоз, лимфогранулематоз), лейкемоидными реакциям, цитомегаловирусной инфекцией, хламидиозом, листериозом, ВИЧ-инфекцией.
К. И. ЧУЙКОВА, Л. А. ЖУРАВЛЕВА
СИБИРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ, Томск
Обследовано 60 детей, больных инфекционным мононуклеозом. Основную группу составили 30 пациентов, которые получили лечение Анафероном детским. Другие 30 больных составили контрольную группу и получали плацебо. Как в основной, так в контрольной группе детям проводилась антибактериальная и симптоматическая терапия. У больных, получавших Анаферон детский, укорачивалась продолжительность клинических симптомов, улучшались некоторые параклинические показатели. Это позволяет рекомендовать Анаферон детский в комплексной терапии для больных инфекционным мононуклеозом по установленной схеме. Ключевые слова: инфекционный мононуклеоз, дети, Анаферон детский, схема лечения, эффективность терапии
Инфекционный мононуклеоз (ИМ) — аэрозольная инфекция. Возбудитель ИМ — вирус герпеса человека 4 типа (ВПН-4) или вирус Эпштейна-Барр (ВЭБ) — относится к подсемейству Gammaherpesviri-dae рода Gymphocryptovirus. ВЭБ распространен повсеместно и поражает до 80—100% населения Земного шара [1—3]. Большинство детей инфицируются к трем годам жизни, до 85% взрослых серопозитивны в отношении ВЭБ и переносят стертые атипичные формы ИМ [4]. ВЭБ поражает, в основном, два типа клеток: эпителий верхних дыхательных путей и пищеварительного тракта, а также В-лимфоциты.
Тяжесть ИМ и затяжное рецидивирующее течение заболевания обусловлены, помимо нарушений в Т- и В-клеточном звене иммунитета, угнетением функционирования факторов неспецифической иммунорезистентности и, в частности, системы интерферона [4, 5,8].
Поэтому важным направлением в терапии вирусных инфекций ИМ, в частности, является коррекция нарушений иммунного статуса. Этому способствует применение иммуномодуляторов, в том числе индукторов эндогенных ИфН. Из потенциальных индукторов ИфН лишь единичные оказались пригодными для клинического применения [4, 5]. Несомненный интерес представляет новый иммуномодулятор с противовирусной активностью Анаферон детский, широко применяемый в настоящее время при гриппе и ОРЗ и представляющий собой сверхмалые дозы антител к ИфН-у человека [6—8].
С учетом изложенного выше представляется перспективным исследование применения Анаферона детского в качестве лечебного средства при ИМ у детей. Действующим веществом Анаферона детского являются сверхмалые дозы антител к у-интерферону человека в разведениях С12, С30 и С50.
Цель исследования состояла в оценке лечебной эффективности препарата Анаферона детского по установленной схеме на фоне антибактериальной и симптоматической терапии.
Материалы и методы исследования
Под наблюдением находилось 60 больных ИМ среднетяжелой формы в возрасте от 3 до 12 лет. Путем рандомизации пациенты были разделены на 2 группы. Дети I группы в составе комплексной терапии получали Анаферон детский (Аф) (30 человек), дети II группы получали плацебо (30 человек). В качестве плацебо использовались таблетки идентичного вида, содержащие только индифферентный наполнитель и не содержащие действующее вещество.
Было проведено рандомизированное двойное слепое плацебоконтролируемое исследование. Рандомизация пациентов проводилась во время первого визита после прохождения скрининга и соответствия критериям включения. Распределение на группы проводилось по мере включения пациентов в исследование.
Больные ИМ поступали в стационар на 2—6 день болезни. В ходе исследования осуществлялось 15 визитов (первые 14 ежедневно). В первый визит проводился отбор пациентов по критериям включения в исследование. Больному и родителям предоставлялась информация об исследовании и составлялось информированное согласие с родителями или с ответственным за ребенка лицом о включении пациента в исследование. Проводились следующие исследования: осмотр больного, забор крови и слюны на ПЦР к ВЭБ, ИфА (IgM VCA, IgG EBNA) для определения специфических антител к ВЭБ. Оценивались OAK, OAM и биохимический анализ крови. Всем больным, включенным в исследование, назначались Анаферон детский или плацебо. Во 2—13 визиты осуществлялось заполнение ИРК больного по соответствующим разделам. В 14 визит (после окончания терапии Анафероном детским или плацебо) проводились повторные лабораторные исследования на специфические антитела (Ig-EA к раннему белку ВЭБ), оценивались или проводились OAK, OAM, 6/x исследование крови. 15 визит осуществлялся через 2 недели после окончания лечения Анафероном детским или плацебо. В этот визит проводилась оценка общего состояния больного, определение титра антител IgM VCA, IgG EBNA к ВЭБ, оценка эффективности и переносимости препарата.
В статистический анализ были включены все пациенты, соответствовавшие критериям включения и получившие лечение (30 пациентов группы Анаферона детского, 30 — группы плацебо). Произведено сравнение средних показателей длительности симптомов заболевания по сравнению с группой плацебо (t критерий Стьюдента для независимых выборок). Доли пациентов с определенным использованием критерия χ 2 для однородности пропорций (доверительный интервал 95%).
Лечение получали 34 мальчика и 26 девочек, при этом преобладали дети в возрасте от 3 до 7 лет (70%). Диагноз направления ИМ был зарегистрирован у 40% больных, остальные 60% детей направлялись на госпитализацию с диагнозами: ангина, ОРЗ, фарингит, паротит (табл. 1).
Таблица 1. Направляющий диагноз у наблюдаемых больных
| Группа, n | ИМ | Ангина | ОРЗ, фарингит | Паротит |
| АФ (30) | 14 | 15 | 1 | - |
| Плацебо (30) | 10 | 16 | 2 | 2 |
| Всего | 24 | 31 | 3 | 2 |
Хронические очаги инфекции регистрировались у 18 пациентов основной группы (Анаферон детский) и у 24 — контрольной (плацебо). До поступления в стационар антибиотики получили 17 (56%) детей основной группы и 11 (37%) — в группе плацебо. Диагноз ИМ был верифицирован у 60 детей (100%).
В стационаре антибактериальная терапия проводилась всем больным обеих групп.
Таким образом, исследуемые группы были однородны по полу, возрасту, исходной тяжести состояния и преморбидному фону, клинико-лабораторной картине заболевания, а также срокам обращения к врачу и проводимому лечению.
Анаферон детский назначался по следующей схеме. В первые 2 часа лечения первого дня по 1 таблетке через каждые 30 минут, затем в этот же день в оставшееся время по 1 таблетке 3 раза. Со 2 дня лечения — по 1 таблетке 3 раза в день до еды в течение двух недель. Таблетка держалась во рту до полного растворения, а детям младшего возраста — растворялась в небольшом количестве кипяченой воды. Курс лечения Анафероном детским составил 14 дней.
Результаты и их обсуждение
У больных, получавших Анаферон детский, отмечалось достоверное уменьшение продолжительности основных симптомов ИМ (табл. 2).
Таблица 2. Продолжительность клинических симптомов при инфекционном мононуклеозе у детей (М + m)
| Симптомы | Группа, дни | |
| Анаферон | Плацебо | |
| Головная боль | 0—4; 2,3 ± 0,37 | 0—6; 2,48 ± 0,21 |
| Боль в горле | 1—4; 2,7 ± 0,33 | 1—7; 3,2 ± 0,29 |
| Недомогание | 1—7; 2,9 ± 0,34 | 1—7; 3,2 ± 0,21 |
| Адинамия | 1—7; 2,9 ± 0,32 | 1—7; 3,1 ± 0,22 |
| * Снижение аппетита | 2—6; 3,9 ± 0,40 | 2—14; 4,3 ± 0,46 |
| * Бледность кожи | 0—14; 5,3 ± 0,90 | 0—14; 6,3 ± 0,94 |
| * Ангина | 0—8; 2,7 ± 0,32 | 0—10; 3,7 ± 0,36 |
| Мезаденит | 1—6; 2,27 ± 0,17 | 1—7; 3,3 ± 0,30 |
| Отечный синдром | 1—4; 3,1 ± 0,37 | 1—9; 3,6 ± 0,30 |
| * Заложенность носа | 2—9; 5,1 ± 0,53 | 2—14; 5,8 ± 0,60 |
| * Увеличение шейных лимфоузлов | 1—14; 8,1 ± 0,65 | 4—14; 12,5 ± 0,56 |
| * Приглушение тонов сердца | 0—6; 0,63 ± 0,50 | 1—14; 1,73 ± 0,69 |
| Систолический шум | 2—14; 9,5 ± 2,61 | 0—14; 11,5 ± 2,60 |
| * Увеличение печени | 2—14; 7,1 ± 0,83 | 2—14; 11,4 ± 0,78 |
| Увеличение селезенки | 0—14; 5,9 ± 0,73 | 0—14; 5,6 ± 0,6 |
* — достоверно различимы р
Температурная реакция в обеих группах больных ИМ сохранялась до 5 дней от начала лечения, но характер ее изменялся у детей, получавших Анаферон детский (рис. 1).
Рисунок 1. Характер температурной реакции у больных инфекционным мононуклеозом
Симптомы интоксикации (бледность кожных покровов, приглушенность тонов сердца) и основные клинические показатели ИМ (ангина, заложенность носа, отечный синдром, мезаденит, увеличение лимфатических узлов и печени) исчезали быстрее у больных, получавших Анаферон детский, чем в контрольной группе (табл. 2, рис. 2).
Рисунок 2. Продолжительность основных симптомов инфекционного мононуклеоза у детей: * — р
У пациентов, получавших Анаферон детский, аппетит восстанавливался в течение 2—6 дней, а в контрольной группе — 2—14 дней. Боли в горле сохранялись от 1 до 4 дней в основной группе и от 1 до 7 дней — в контрольной группе. К 14 визиту в группе детей, получавших Анаферон детский, увеличение лимфатических узлов сохранялось только у двух пациентов, которые в анамнезе имели хронический тонзиллит, против 18 детей в группе больных, получавших плацебо. В процессе наблюдения до 15 визита в основной группе увеличение лимфатических узлов сохранялась только у 2 детей (6,6%), при этом увеличения печени и селезенки не отмечалось, а в группе детей, получавших плацебо, у 18 пациентов (60%) доминировало увеличение лимфатических узлов, а у 2 из них оставалась увеличенной печень и сохранялась заложенность носа.
Рисунок 3. Увеличение лимфоузлов, печени, селезенки при инфекционном мононуклеозе у детей: * — р
Показатели OAK до лечения Анафероном детским или плацебо достоверно не различались. Уменьшение количества атипичных мононуклеаров в группе Анаферона детского было достоверным через 2 недели от начала наблюдения и лечения, в дальнейшем также отмечалось его снижение. В группе плацебо достоверное снижение числа мононуклеаров по сравнению с таковым в начале отмечалось только к 4 неделе наблюдения. К 15 визиту в обеих группах показатели OAK нормализовались (табл. 3).
Таблица 3. Показатели крови у больных инфекционным мононуклеозом (М ± m)
| Показатели OAK (60 чел.) | 1 визит | 14 визит | 15 визит | |||
| Анаферон | Плацебо | Анаферон | Плацебо | Анаферон | Плацебо | |
| Эритроциты | 3,9 ± 0,06 | 4,03 ± 0,1 | 3,9 ± 0,07 | 3,78 ± 3,8 | 3,8 ± 0,1 | 4,04 ± 0,07 |
| Гемоглобин | 113,85 ±10,59 | 119 ± 2,5 | 114,1 ± 2,0 | 113 ± 2,3 | 112, 16 ± 2,0 | 117 ± 1,8 |
| Лейкоциты | 9,4 ± 0,9 | 9,9 ± 0,7 | 6,5 ± 0,3* | 6,9 ± 0,3* | 5,8 ± 0,4* | 6,3 ± 0,2* |
| Эозинофилы | 3,24 ± 0,6 | 4,28 ± 0,1 | 3,17 ± 0,46 | 4,08 ± 1,7 | 3,4 ± 0,6 | 2,12 ± 0,2 |
| Нейтрофилы п/я | 7,9 ± 1,2 | 10,5 ±1,6 | 4,1 ± 0,7* | 4,2 ± 0,7* | 3,9 ±1,6* | 2,8 ± 0,4* |
| Нейтрофилы с/я | 41,7 ± 3,5 | 44,9 ± 3,3 | 31,5 ± 2,3* | 30,3 ± 2,6* | 35,1 ± 2,3 | 36,9 ± 1,8* |
| Лимфоциты | 32,7 ± 2,9 | 33,1 ± 2,9 | 52,6 ± 2,3* | 49,8 ± 2,8* | 54,1 ± 2,9* | 53,1 ± 1,8* |
| Моноциты | 5,4 ± 0,9 | 5,7 ± 0,9 | 3,5 ± 0,4* | 7,7 ± 1,5 | 3,5 ± 0,3* | 4,9 ± 0,6 |
| Ат. мононуклеары | 15,7 ± 2,6 | 11,2 ± 0,37 | 9,6 ± 1,2* | 8,6 ±1,2 | 6,7 ± 2,5* | 4,1 ± 1,0* |
| СОЭ | 18,7 ± 2,3 | 20,4 ± 2,8 | 12,1 ± 1,3* | 10,5 ± 1,3* | 7,1 ± 0,6* | 7,5 ± 0,7* |
Результаты б/х исследования крови до и после лечения (к 14 визиту) достоверно не различались, (табл. 4).
Таблица 4. Показатели биохимических исследований крови у больных инфекционным мононуклеозом (М + m)
| Показатели б/х крови (60 чел.) | Анаферон (30) | Плацебо (30) | Анаферон (30) | Плацебо (30) |
| Глюкоза | 4,5 ± 0,1 | 4,4 ±0,1 | 4,1 ± 0,1 | 4,3 ± 0,1 |
| Билирубин общий | 9,8 ±2,3 | 7 ±0,6 | 7,3 ±0,5 | 7,3 ±0,5 |
| Общий белок | 72,5 ±1,2 | 74,7 ±1,1 | 71,2 ±1,3 | 74,3 ±1,0 |
| Тимоловая проба | 3,1 ±0,5 | 3,6 ±0,8 | 3,5 ±0,5 | 3,7 ±0,4 |
| АЛТ | 0,7 ±0,1 | 0,6 ± 0,1 | 0,5 ± 0,1 | 0,5 ±0,1 |
| ACT | 0,4 ± 0,1 | 0,3 ± 0,1 | 0,4 ± 0,1 | 2,4 ± 2,1 |
Клинические критерии лечебной эффективности Анаферона детского позволили отметить отличный и хороший эффект в основной группе у 22 из 30 (73,4%) больных, удовлетворительный — у 7 (23,3%) детей, неудовлетворительный — у 1 (3,3%) больной, у которой в анамнезе рецидивировал хронический бронхит. В группе детей, получавших плацебо, отличного эффекта не наблюдалось, хороший эффект отмечался у 5 (17%) детей, удовлетворительный — у 15 (50%) пациентов, неудовлетворительный — у 10 (33%) больных.
Таблица 5. Оценка эффективности Анаферона детского при инфекционном мононуклеозе
| n=60 | Отлично абс/% | Хорошо абс/% | Удовл. абс/% | Неуд. абс/% |
| Анаферон n=30 | 12/40,4 | 10/33 | 7/23,3 | 1/3,3 |
| Плацебо n=30 | 0 | 5/17,0 | 15/50,0 | 10/33 |
Из 60 исследуемых больных ИМ ни у кого не наблюдалось отрицательных реакций, побочных эффектов, осложнений, препарат обладал хорошей переносимостью.
Результаты рандомизированного слепого плацебо-контролируемого исследования 60 больных ИМ среднетяжелой формы в возрасте 3—12 лет показали, что клинико-лабораторные показатели восстанавливались быстрее у больных, получивших лечение с применением Анаферона детского. Доказана эффективность, безопасность и хорошая переносимость препарата Анаферона детского в лечении больных ИМ. Предлагается схема лечения Анафероном детским.
Выводы
1. Анаферон детский — препарат нового класса иммуномодуляторов с противовирусной активностью — эффективен в лечении больных ИМ.
2. Анаферон детский обладает хорошей переносимостью, не имеет побочных эффектов во время лечения.
Читайте также:


