Стафилококковая инфекция в коленном суставе
В прошлом роли инфекции в ревматических заболеваниях придавалось гораздо большее значение, чем сегодня. В начале нашего века причиной ревматоидного артрита считалась туберкулезная инфекция, и своего рода результатом подобных выводов стало лечение солями золота, которые в отдельных случаях успешно нейтрализуют туберкулезные бактерии. Позднее оказалось, что туберкулез не имеет никакого отношения к ревматоидному артриту, и причиной ревматических заболеваний стали считать инфекционные очаги в зубах, миндалинах или слепой кишке. Излюбленным методом лечения всех ревматических болезней было удаление инфицированных зубов. В настоящее время лечение очагов инфекции в зубах и миндалинах считается скорее общегигиеническим требованием, чем имеющим лечебное значение.
Инфекция может вести себя по отношению к суставам по-разному:
1. Инфекция проникает непосредственно в суставные ткани и полости, бактерии там размножаются и часто наносят огромный вред.
2. Инфекция проникает в места, удаленные от сустава - мочеточники, органы пищеварения, носоглотку и миндалины. После излечения указанных органов через некоторое время в качестве реакции на эту инфекцию возникают артрит и другие внесуставные симптомы заболевания. В самом суставе не удается выявить бактерий, и в данном случае их заболевание является своего рода вторичной защитной реакцией на наличие микроорганизмов в очагах вне суставов.
3. После перенесенного гриппа, в начальных стадиях вирусного гепатита (инфекционного воспаления печени) или инфекционного мононуклеоза, могут проявляться неопасные боли в суставах или быстропроходящие артриты.
Излечиваемость инфекционных артритов, как гнойных, так и туберкулезных, сегодня, при наличии большого выбора антибактериальных средств, довольно высокая, но лечение следует начинать вовремя. Оно должно быть интенсивным, с введением лекарств непосредственно в сустав.
Чаще, чем эти непосредственно инфекционные артриты, возникают так называемые реактивные артриты - реактивные потому, что они представляют собой реакцию на внесуставную инфекцию и возникают только через некоторое время после погашения очага инфекции. К ним относятся ревматическая лихорадка, так называемый синдром Рейтера, лаймский боррелиоз и т. д.
Самой неизученной болезнью из ряда реактивных артритов является ревматическая лихорадка. В прошлом она встречалась довольно часто, особенно в районах со слабым социально-экономическим развитием, где бедность соседствовала с перенаселенностью. В 1925-1950 гг. ревматическая лихорадка была одной из наиболее частых причин смертности детей и подростков, а также главной причиной заболеваний сердца у людей до 40 лет. Постепенно число заболеваний ревматической лихорадкой снижалось, вместе с этим уменьшалась смертность. Число людей, у которых отмечались поражения сердечной мышцы, тоже сокращалось. Снижение заболеваемости ревматической лихорадкой было вызвано целым рядом причин - улучшением качества жизни, широким применением антибиотиков для лечения и профилактики стрептококковых инфекций, а возможно изменился и сам стрептококк, который стал менее агрессивным и утратил способность вызывать ревматическую лихорадку. В ряде стран Азии и Африки проблема ревматической лихорадки существует и в настоящее время. Причиной этого заболевания является инфицирование носоглотки b-гемолитическим стрептококком группы А (слово гемолитический означает, что он может разрушать эритроциты - красные кровяные тельца). Этот стрептококк содержит ряд белковых и небелковых соединений, вызывающих образование специфических защитных антител, которые нейтрализуют его действие. Стрептококк вырабатывает ряд ядовитых веществ, повреждающих ткани организма -к ним относится так называемый стрептолизин О (стрептолизин и является причиной разрушения эритроцитов). Для противодействия этого стрептолизина также образуются специфические антитела, называемые антистрептолизином О - сокращенно АСЛО (эти антитела используются при диагностике, так как их наличие в крови свидетельствует о стрептококковой инфекции).
Стрептококк попадает в ткань лимфоидного кольца глотки (миндалины), вызывает ангину и выделяет ядовитые продукты - токсины. Организм защищается и образует для борьбы защитные антитела. После этого начинает происходить нечто интересное. Из-за определенного биологического и химического сходства некоторых составных элементов тела стрептококка и соединительной ткани сердца и суставов происходит своего рода перекрестная реакция, и антитела, предназначенные для борьбы со стрептококком, начинают атаковать ткань, в которой поселился этот микроб. Здесь мы можем наблюдать пример аутоиммунного заболевания. Определенную загадку представляет собой тот факт, что у большей части населения стрептококковая инфекция носоглотки проходит в виде неосложненного заболевания, а у меньшей части через некоторое время развиваются признаки ревматической лихорадки. Очевидно, что здесь мы имеем пример определенной предрасположенности, которая, к счастью, характерна лишь для небольшой части нашего населения. Таким образом, при ревматической лихорадке события происходят в следующей последовательности: ангина, которая быстро проходит, после чего через несколько дней или недель возникает заболевание с высокой температурой, потливостью, воспалением одного или нескольких, как правило крупных (коленный, голеностопный, локтевой, лучезапястный) суставов. Артрит имеет блуждающий характер и перемещается с одного сустава на другой. Боль в суставах иногда бывает очень острой. Эти боли могут достаточно успешно сниматься рядом противоревматических средств, в связи с чем никогда не считались серьезным заболеванием. Другое дело -осложнения на сердце. Ревматическое воспаление поражает сердечную мышцу, внутреннюю оболочку сердца и сердечную сумку (перикард). Признаки поражения сердца иногда могут быть выражены слабо, и лишь опытный врач может распознать их вовремя. Воспалительный процесс в тканях сердца реагирует на введение лекарственных препаратов не так хорошо, как в суставах, кроме того, он может повторяться и возникать заново. Результатом могут стать дефекты сердечных клапанов. Клапаны могут сращиваться между собой, таким образом возникает их сужение (стеноз), или из-за разрастания соединительной ткани клапан перестает полностью закрываться (недостаточность). Оба этих типа поражений клапанов сердца через несколько лет могут существенно повлиять на работу сердечно-сосудистой системы.
Кроме сердца и суставов при этом заболевании бывает затронута и кожа (появление красноватой сыпи), иногда поражается.центральная нервная система, что проявляется так называемой пляской святого Вита (хорея). В этом случае мышцы сокращаются бесконтрольно и некоорди-нировано, иногда же хорея проявляется лишь в виде непоседливости и нервозности ребенка в школе или неконтролируемыми гримасами.
В диагностике ревматической лихорадки важное место занимают лабораторные анализы. Прежде всего речь идет о седиментации эритроцитов, число которых в начальных стадиях существенно увеличивается. Анализы проводятся таким образом, что венозная кровь больного смешивается с антикоагуляционным раствором для предотвращения ее свертывания, после чего кровь заливается в вертикально установленную стеклянную трубочку. Через час и через два часа высчитывается седиментация эритроцитов в несвернувшейся плазме крови. В норме на верху темного столбца из кровяных телец образуется несколько миллиметров чистой плазмы. Из-за изменений белков крови при наличии воспалительного процесса этот показатель увеличивается до нескольких десятков миллиметров (максимально - 100-120 мм за 1 час). Седиментация эритроцитов говорит нам, насколько интенсивен воспалительный процесс в организме. В дальнейшем проводится анализ уже упоминавшихся антистрептолизиновых антител.
Лечение ревматической лихорадки должно проводиться незамедлительно и энергично. Основой программы лечения является постельный режим, особенно в том случае, если было затронуто сердце. Постельный режим может быть не таким строгим при улучшении показателей анализов (седиментации эритроцитов) и в зависимости от степени пораженно-сти сердца. При ревматической лихорадке, не сопровождаемой осложнениями, процесс выздоровления проходит быстро, хотя до полного исчезновения проявлений этого заболевания может потребоваться до двух месяцев. Осложнения на сердце вызывают и более длительную нетрудоспособность.
Больным, у которых болезнь оставила следы поражения сердца, в течение нескольких лет применяется профилактическое лечение пенициллином. В этом случае речь идет либо о ежедневном приеме небольших доз, либо приема длительно действующей дозировки пенициллина один раз в несколько недель. Важным при этом является тщательное лечение антибиотиками каждой ангины.
В заключение следует указать на важное обстоятельство. Хотя благодаря всем указанным выше факторам к 70-м годам удалось практически покончить с ревматической лихорадкой и врачи понемногу начали о ней забывать, с 1986 г. появляются сообщения о начинающемся росте заболеваемости в Соединенных Штатах. Речь идет о болезнях детей, живущих в семьях с хорошим уровнем качества жизни и в здоровых сельских районах. Кроме этого, как уже было во время второй мировой войны, заболевают молодые новобранцы. При этом оказывается, что социальный фактор не является решающим для победы над ревматической лихорадкой. Ученые, сразу предпринявшие исследования стрептококков из носоглотки и миндалин больных, обнаружили, что этот стрептококк изменился, теперь болезнь вызывает новый, модифицированный тип этого микроорганизма.
Ч Следующим реактивным артритом, но несколько иного рода, является болезнь Рейтера (или синдром). О ее открытии мы говорили в вводном разделе. Она развивается после некоторых острых инфекций мочеполовых органов или кишечника. В первом случае речь идет как об инфекции, занесенной при случайной половой связи, так и о банальном заболевании мочеполовых органов, а также обострении хронической инфекции. В клетках мочеиспускательных каналов был обнаружен специфический паразит, названный хламидией (Chlamidia trachomatis). Но это не тот микроорганизм, который вызывает гонорею. Так же, как и при болезни Бехтерева, большой процент больных (около 70) предрасположен к этой болезни в связи с присутствием у них на поверхности клеток трансплантационного антигена В27 (см. раздел о болезни Бехтерева). Учитывая то, что при болезни Рейтера часто наблюдается и воспаление тазобедренных суставов, это заболевание иногда относят к заболеваниям позвоночника - спондилоартритам.
Первыми симптомами заболевания бывают артриты чаще всего голеностопных или коленных суставов. Они появляются через 1-3 недели после инфицирования мочеиспускательных каналов. Иногда больной может лишь смутно вспомнить о жжении во время мочеиспускания или о частом мочеиспускании, которое некоторое время назад его немного беспокоило. Часто у больного наряду с суставами болит крестцовый отдел позвоночника или возникают боли в области пятки (место соединения сухожилия и пяточной кости). Реже воспаляется слизистая оболочка глаза (конъюнктивит), на коже стоп может появиться шелушащаяся сыпь. Эта болезнь длится недолго, лишь в исключительных случаях она может тянуться несколько месяцев. В начальном периоде она хорошо поддается лечению антибиотиками, позднее для снятия болей необходимы нестероидные противоревматические средства и лечение сульфасалазином (см. раздел о фармакотерапии ревматических заболеваний).
Свое влияние на суставы может оказывать и синдром приобретенного иммунодефицита (СПИД). Вирус, вызывающий это заболевание, поражает человеческие лимфоциты, участвующие в защите организма от инфекции, и ослабляет их нормальную работу. Тем самым у зараженных им лиц облегчается доступ в организм инфекции и увеличивается вероятность развития опухолевых заболеваний. В суставах и костях больных могут возникать инфекционные артриты, вторично вызываемые бактериями. Иногда могут развиваться и симптомы, характерные для синдрома Рейтера и повреждений позвоночника.
Особым типом артрита, имеющим много общего с инфекционными и реактивными артритами, является лаймский боррелиоз. Это сложная болезнь, поражающая, кроме суставов, кожу, сердце и нервную систему. Что касается суставных ее проявлений, то она напоминает симптомы инфекционного артрита, поскольку ткани поражаются бактериями. С другой стороны, это заболевание носит характер и реактивного артрита, поскольку болезнь, особенно в суставах, появляется лишь через несколько месяцев после инфицирования.
Первые признаки заболевания появляются на коже, в месте проникновения инфекции (после укуса клеща) появляются красные пятна, которые увеличиваются в размерах и постепенно бледнеют в центре. Кожа может поражаться и на более поздних стадиях лаймского боррелиоза в виде воспалительных процессов и одновременного истончения (атрофии).
Заболевание это проходит три стадии. На начальной стадии оно проявляется (примерно через месяц после укуса клеща) в виде кожных высыпаний, неопределенных гриппоподобных состояний, быстрой утомляемости, потери аппетита, несильной боли в мышцах и суставах. Еще через 2-3 мес могут появиться симптомы нервных заболеваний в виде раздражения оболочки мозга, полиомиелита и расстройств нервной системы -от лабильности до невроза. Сюда добавляются поражения сердца и воспаления суставов. Суставное воспаление может проявиться в течение нескольких лет после инфицирования. Воспаление в большинстве случаев проходит, но иногда оно приобретает хронический характер. В заключительной стадии проявляются хронические, атрофические кожные изменения, чаще всего - на нижних конечностях. Диагностика этого заболевания заключается в выявлении специфических антител, действие которых в начальной стадии часто оказывается не очень надежным. Позднее без доказательства присутствия антител диагноз лаймского боррелиоза подтвердить уже нельзя.
Открытие лаймского боррелиоза привлекло большое внимание врачей, а высокая заболеваемость им в Чехии (до нескольких тысяч больных) вызвала и определенные опасения. Поскольку лаймский боррелиоз имеет очень изменчивый и разнообразный характер, то целый ряд расстройств начали объяснять наличием именно этого заболевания. Ситуация усложняется и относительно высоким у жителей Чехии наличием антител против боррелии, что обусловлено относительно частыми их контактами с переносчиком этого заболевания. Заболевает из них лишь небольшой процент.
Раннее лечение антибиотиками позволяет излечить эту болезнь и предотвратить ее переход на следующие стадии. Используются при этом антибиотики пенициллиновой и тетрациклиновой группы, иногда в значительных дозах. Более поздние стадии хуже поддаются лечению, и поэтому большие дозы антибиотиков вводятся непосредственно в вену, а иногда применяются самые современные цефалоспориновые антибиотики.
До сих пор не очень ясно, каким образом боррелии вызывают такое сложное заболевание. В начальных стадиях в тканях они присутствуют живыми, а позже погибают под воздействием антибиотиков. Мертвые боррелии вызывают иммунные реакции перекрестного типа. Это означает, что антитела атакуют не только боррелии, но и ткани самого организма. Таким образом, лаймский боррелиоз действительно является частично инфекционным, а частично - реактивным заболеванием.
Профилактика боррелиоза состоит в недопущении попадания переносчика этой болезни на тело. Во время пребывания в лиственном лесу следует выбирать подходящую одежду, прикрывающую все части тела, и соответствующую обувь. Нужно также использовать средства для отпугивания мошкары и насекомых (репелленты). Снимать клещей следует осторожно, при помощи пинцета, после промазывания спиртом, растительным маслом или лаком для ногтей. Ранку нужно сразу же продезинфицировать раствором йода.

Увеличение средней продолжительности жизни, несомненно, положительная тенденция настоящего времени, но обратной стороной медали является не всегда высокое качество жизни, особенно в старшем возрасте. Одним из факторов, снижающих это качество, всё чаще становятся заболевания суставов. Боль и ограничение способности к движению при этих заболеваниях со временем значительно осложняют жизнь пациентам. Наиболее эффективным способом лечения в этих случаях считается хирургическое вмешательство. Для лечения пациентов с тяжелыми посттравматическими осложнениями и дегенеративными заболеваниями суставов оптимальным методом считается эндопротезирование. Однако, несмотря на то что после тотального эндопротезирования коленного сустава наблюдается значительное улучшение состояния пациента, существует риск осложнения в виде парапротезной инфекции, при котором увеличиваются сроки и стоимость лечения. Кроме того, инфекционное осложнение может привести к неблагоприятному исходу хирургического лечения. Согласно исследованиям, проведенным в ряде разных центров, после тотального эндопротезирования коленного сустава инфицирование происходило в 0,5-5% случаев 1.
I. Uçkay с соавт. выполнили ретроспективный анализ 6101 случая реэндопротезирования крупных суставов с 1996 по 2008 г. Из них 2099 случаев – после эндопротезирования коленного сустава. Всего было удалено 234 (11,15%) протеза коленного сустава, из них по поводу инфекции удалено 24 (1,14%) протеза. Полученные результаты позволили авторам сделать вывод, что парапротезная инфекция – редкое осложнение [4; 5].
Внедрение эндопротезирования в клиническую практику в России происходило постепенно, и первоначальные результаты не внушали оптимизма. По данным H.Н. Корнилова с соавт., частота инфекционных осложнений в некоторых лечебных учреждениях, где выполнялось лишь несколько эндопротезирований в год, достигала 17% [5; 6].
Волошин В.П. с соавт. проанализировали опыт лечения 66 пациентов с тотальным эндопротезированием крупных суставов. В 87,9% случаев (58 пациентов), в сроки от 1,5 до 3 лет после эндопротезирования, отмечалось развитие гнойной инфекции. Глубокое нагноение отмечено у 6 пациентов (9,1%). В итоге 10 пациентам было выполнено артродезирование коленного сустава аппаратом Илизарова [5; 7].
Т.А. Куляба с соавторами проанализировали результаты лечения 44 пациентов, у которых после первичного и ревизионного эндопротезирования коленного сустава развилось инфекционное воспаление. Происходило это в разные сроки, у 18 пациентов (40,1%) в раннем послеоперационном периоде, а у 26 (59,1%) в отдаленном, но так или иначе, купировать воспаление и сохранить эндопротез удалось только у 10 (22,7%) больных. В подавляющем большинстве случаев потребовалось провести двухэтапное хирургическое лечение, которое позволило купировать гнойный процесс в 89,3% случаев. Артродез был выполнен у 4 (9,1%) больных [5; 8].
Инфицирование может происходить через прямую или гематогенную передачу бактериальной флоры. Некоторыми примерами прямой передачи являются: несоблюдение условий стерильности в операционных, передача от инфицированного пациента, небрежность хирургов и обслуживающего персонала. Гематогенное инфицирование наблюдается после эпизода бактериемии. Например, стрептококковая инфекция может развиться после стоматологического вмешательства, стафилококковая – как следствие кожного инфекционного заболевания, энтерококковая и анаэробные инфекции – в результате желудочно-кишечных инфекционных заболеваний и инфекций мочеполовой системы [9].
Отек, боль и дисфункция коленного сустава возникают после эндопротезирования коленного сустава и усиливаются по мере прогрессирования инфекции. На фоне инфекции происходит перипротезный остеолиз, приводящий к нестабильности эндопротеза. У пациентов, не получающих своевременного лечения, может развиться сепсис и опасный для жизни септический шок [10].
На основе метаанализа, проведенного Cancienne J.M. с соавт., описаны исходы лечения 18 533 пациентов с ранними инфекционными осложнениями (в течение 1 года) после тотального эндопротезирования коленного сустава [11]. Среди них:
- 691 пациент (3,7%) умер в стационаре;
- 574 пациентам (3,1%) потребовалась ампутация конечности;
- 852 пациента (4,5%) перенесли артродез коленного сустава;
- 2683 пациентам (14,5%) проведена вторичная хирургическая обработка, без реимплантации;
- 13743 (74,1%) пациента прошли через двухэтапное реэндопротезирование коленного сустава, из них 11420 пациентам (61,6%) в течение 1 года проведено удаление спейсера и реимплантация, а 2323 пациентам (12,5%) оставлен спейсер.
Nodzo S.R. и соавторы, при проведении двухэтапного реэндопротезирования, разделили пациентов на три группы в зависимости от типа используемого спейсера [12]. В первой группе использовались преформованные артикулирующие спейсеры, во второй – спейсеры из цемента изготавливались интраоперационно. В третьей группе – в качестве спейсера использовали автоклавированный бедренный компонент удаленного эндопротеза. Признаки санации инфекционного процесса отметили в первой группе пациентов в 82,7% случаях, во второй группе – в 88,4%. Наименьшее количество положительных результатов отмечено в третьей группе – 79,4%. Таким образом, использование цементных спейсеров, изготовленных интраоперационно с использованием антибиотика по чувствительности флоры, приносит максимально положительный результат.
Цель исследования: провести анализ частоты, структуры и причин возникновения инфекционных осложнений при тотальном эндопротезировании и реэндопротезировании коленного сустава и определить оптимальную тактику лечения при этих осложнениях.
Материал и методы. В Новосибирском НИИТО за период с 2007 по 2016 год было проведено 12 245 операций первичного эндопротезирования коленного сустава. Инфекционные осложнения возникли у 470 (3,84%) человек. При этом эпифасциальная (поверхностная) инфекция была зафиксирована у 252 (2,06%) пациентов. В эту группу включены пациенты с некрозом послеоперационного шва и подкожной клетчатки, лигатурными свищами. В случае распространения процесса в пределах 5-6 см по ходу операционного шва, пациентам проводилась одномоментная санация и ушивание кожного дефекта. В случаях распространения процесса на весь шов, пациентам проводились этапные санационные перевязки до очищения стенок раны с последующим вторичным швом раны. Как результат применения такой методики лечения, у всех пациентов отмечался положительный результат.
Группу пациентов с субфасциальной (глубокой) инфекцией, развившейся в разные сроки, составили 218 пациентов (1,8%), что соответствует мировым тенденциям. По нашим убеждениям, в случае глубокой парапротезной инфекции, на фоне сформированной биопленки, эндопротез сохранять бесполезно, и он подлежит удалению. Однако дальнейшая тактика зависит от патологической флоры и других факторов. После удаления выполняется либо одномоментная имплантация нового эндопротеза, либо проведение этапного лечения с целью санации и последующего реэндопротезирования. В случае невозможности выполнения последующего этапа реэндопротезирования, в рассматриваемых случаях выполнялся артродез коленного сустава.
Бактериальное исследование пациентов с глубокой парапротезной инфекцией дало следующие результаты:
· у 172 (78,9%) пациентов была выделена грамположительная кокковая флора: у 113 пациентов – MSSA, у 33 – MSSE, у 8 пациентов – MRSA, и у 18 пациентов – MRSE;
· грамотрицательные палочки (Klebsiella, Pseudomonas, E.coli) были выделены у 33 пациентов (15,1%);
· грамположительные палочки (Korinebacterium, Propionobacter) – у 2 пациентов (0,9%);
· у 11 пациентов (5,0%) была выявлена смешанная флора.
При выборе тактики хирургического лечения больных с глубокой парапротезной инфекцией анализировались сроки возникновения инфекции, степень стабильности компонентов эндопротеза и степень вирулентности возбудителя. Также немаловажную роль в выборе тактики оперативного лечения играли сопутствующая патология и желания самого пациента.
Одномоментное реэндопротезирование после удаления эндопротеза выполнялось пациентам без выраженной сопутствующей патологии, в раннем послеоперационном периоде (до 6 мес.), при отсутствии признаков нестабильности эндопротеза и в случае чувствительности флоры к возможному проведению антибиотикотерапии. В ходе данного вида оперативного лечения выполняли удаление эндопротеза, патологических грануляций мягких тканей и имплантировали новый эндопротез с добавлением в цемент антибактериальных препаратов, подобранных по чувствительности к флоре. В последующем проводили адресную антибиотикотерапию в течение 6 недель.
Этим способом были пролечены 28 пациентов. В 26 случаях инфекция была купирована. У двух пациентов наблюдался рецидив, потребовавший проведения двухэтапного ревизионного вмешательства. Таким образом, выживаемость имплантата составила 93%.
Клинический пример 1. Больная К., 62 года. Выполнено первичное эндопротезирование КС по поводу левостороннего гонартроза III ст.
Через 3 месяца после проведения оперативного лечения развилось осложнение в виде глубокой парапротезной инфекции. По результатам бактериологического исследования выявлен патогенный микроорганизм – MSSA. Больной выполнено удаление эндопротеза и одномоментное реэндопротезирование коленного сустава.
На контрольных осмотрах через 1 год, 3 и 5 лет признаков рецидива инфекции не было.
В зависимости от степени сохранности связочного аппарата устанавливался артикулирующий либо неартикулирующий спейсер с добавлением антибиотика по чувствительности бактериальной флоры. После первого этапа пациенты получали антибиотикотерапию в течение 6-8 недель. Второй этап лечения – удаление цементного спейсера и реэндопротезирование коленного сустава, проводился по истечении 3-8 месяцев при условии нормализации клинических анализов и отсутствии положительных бактериологических исследований пунктата синовиальной жидкости.
Клинический пример 2. Больная Г., 62 года. Первичное эндопротезирование коленного сустава было проведено по поводу гонартроза III ст. Через 3 года после проведенной операции перенесла рожистое воспаление голени, осложнившееся глубокой парапротезной инфекцией. По результатам бактериологического исследования был выявлен патогенный микроорганизм – MRSA. Больной было выполнено удаление эндопротеза, санация и имплантация цементного артикулирующего спейсера (рис. 1).
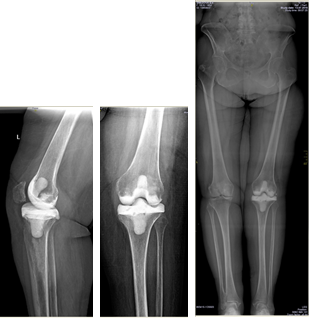
Рис. 1. Клинический пример 2. Рентгенограмма коленного сустава после
имплантации артикулирующего спейсера коленного сустава
Антибиотикотерапия поводилась в течение 6 недель. Через 6 месяцев, когда признаки инфекции были полностью купированы, больной выполнен второй этап оперативного лечения – удаление цементного спейсера и реэндопротезирование коленного сустава (рис. 2). На контрольных осмотрах через 1 и 3 года признаков рецидива инфекции не обнаружено.
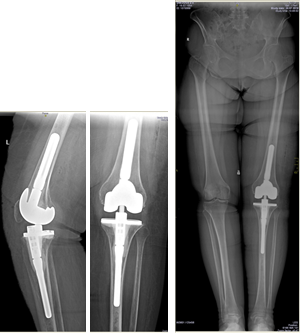
Рис. 2. Клинический пример 2. Рентгенограмма коленного сустава
после удаления спейсера и реэндопротезирования коленного сустава
За период наблюдения двухэтапное оперативное лечение было проведено 146 пациентам. У 124 пациентов признаки инфекции были купированы. Процедив отмечен у 22 пациентов. С целью купирования инфекционного процесса этим больным выполнялся артродез коленного сустава в аппарате внешней фиксации.
Первично артродез коленного сустава выполнялся пациентам с вирулентной флорой, на поддающейся антибиотикотерапии, с выраженной сопутствующей патологией, позволяющей оперировать пациента только по жизненным показаниям, и в случае желания пациента.
Клинический пример 3. Больная Л., 52 года. Первичное эндопротезирование коленного сустава было проведено по поводу вторичного артрозо-артрита коленного сустава III ст. на фоне ревматоидного полиартрита.
Через 6 месяцев после проведенного оперативного вмешательства у больной развилась глубокая парапротезная инфекция. Учитывая высокую активность основного заболевания, пациентка предпочла отказаться от дальнейших оперативных вмешательств, в связи с чем было выполнено удаление и артродез коленного сустава в аппарате внешней фиксации (рис. 3).
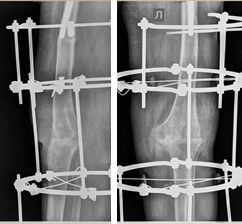
Рис. 3. Рентгенограмма коленного сустава после удаления эндопротеза и артродеза коленного сустава в аппарате внешней фиксации
По различным причинам артродез коленного сустава выполнялся в 66 случаях. В 54 случаях у пациентов сформировался костный анкилоз, и только в 12 случаях отмечалось формирование фиброзного анкилоза или неоартроза. Рецидива инфекции при выполнении артродеза коленного сустава зафиксировано не было.
Результаты. Таким образом, за 10 лет через отделение эндопротезирования коленного сустава Новосибирского НИИТО прошли 470 пациентов с парапротезной инфекцией. Эти пациенты получили следующее лечение:
- 252 (53,6%) пациентам с поверхностной инфекцией проведена вторичная хирургическая обработка, реимплантация эндопротеза не требовалась;
- 26 (5,5%) пациентам проведено одномоментное реэндопротезирование коленного сустава;
- 126 (26,8%) пациентов перенесли двухэтапное оперативное лечение;
- 66 (14,0%) пациентам по различным причинам выполнен артродез коленного сустава.
Ампутаций конечности и летальных исходов, вызванных инфекционным процессом, в отделении не отмечено.
Заключение. Инфекционные осложнения при первичном протезировании коленного сустава, невзирая на улучшение техники хирургического лечения и проводимой профилактики, остаются достаточно частыми и наиболее тяжелыми осложнениями. Как правило, они приводят к повторным оперативным вмешательствам, а зачастую и к инвалидизации пациентов. Обоснованный выбор хирургической тактики позволяет благополучно справиться с инфекционным осложнением и обеспечить пациенту приемлемое качество жизни.
(Септический артрит)
, MD, Cleveland Clinic Lerner College of Medicine at Case Western Reserve University
Бактерии, вирусы или грибки могут распространяться с кровотоком или проникать в сустав из близлежащей инфицированной ткани, вызывая развитие инфекции.
В течение нескольких часов или пары дней появляется боль, отек и повышенная температура.
С помощью иглы извлекается синовиальная жидкость для анализа.
Немедленно назначают антибиотики.
Различают два типа инфекционного артрита:
Острый инфекционный артрит
Острый инфекционный артрит, который вызывают бактерии, развивается быстро. В большинстве случаев инфекционный артрит характеризуется острым началом. Острый инфекционный артрит может возникать у здоровых людей, а также у лиц с факторами риска. В течение нескольких часов или дней хрящевая ткань в суставе, необходимая для его нормальной работы, может быть повреждена или разрушена.
Иногда артрит развивается у людей с инфекциями, не затрагивающими костей или суставов, например, инфекциями половых органов или органов пищеварительного тракта. Такой тип артрита является реакцией на инфекцию и называется реактивным артритом. При реактивном артрите наблюдается воспаление сустава без его фактического заражения.
Хронический инфекционный артрит
Хронический инфекционный артрит развивается постепенно в течение нескольких недель. Инфекционный артрит очень редко принимает хроническое течение. Хронический инфекционный артрит чаще всего возникает у лиц с факторами риска.
Чаще всего отмечается поражение колена, плеча, запястья, тазобедренного сустава, локтя, а также суставов пальцев рук. Большинство бактериальных, грибковых и микобактериальных инфекций поражают только один сустав, в редких случаях несколько суставов. Например, бактерия-возбудитель болезни Лайма чаще всего поражает коленный сустав. Гонококковые бактерии (гонококки), которые вызывают гонорею, вирусы (например, вирус гепатита) и изредка некоторые другие бактерии могут поражать несколько или много суставов одновременно.
Причины
Микроорганизмы, которые вызывают инфекцию (преимущественно бактерии), обычно распространяются из близлежащего источника инфекции (например, очага остеомиелита либо инфицированной раны) или с током крови. Сустав может быть инфицирован напрямую при загрязнении в ходе хирургического вмешательства либо при инъекции или травме (например, ране от укуса человеком или от укуса собаки, кошки или крысы).
Острый инфекционный артрит
Острый инфекционный артрит обычно вызывается бактериями и вирусами.
Сустав может быть инфицирован различными бактериями, но вид бактерий, который с наибольшей вероятностью вызовет острый инфекционный артрит, зависит от возраста больного.
Младенцы и дети младшего возраста: Staphylococcus aureus, стрептококки, грамотрицательные бациллы и Kingella kingae
Дети старшего возраста и взрослые: Staphylococcus aureus, стрептококки и гонококки
Суставы могут инфицироваться спирохетами (вид бактерии), например теми, что вызывают болезнь Лайма и сифилис.
Вирусы, например ВИЧ, парвовирусы и возбудители краснухи, паротита, гепатита В и гепатита C, способны поражать суставы у больных любого возраста.
Существует много факторов риска развития инфекционного артрита. У большинства детей с инфекционным артритом факторы риска не выявлены.
К факторам риска острого инфекционного артрита относятся:
наличие в прошлом инфекции суставов;
искусственный сустав и хирургическое вмешательство на суставе;
использование игл для введения лекарственных препаратов;
хронические заболевания (например, сахарный диабет, волчанка и хронические заболевания легких или печени);
поведение, которое увеличивает риск заболеваний, передающихся половым путём (например, секс со многими партнерами и без использования презервативов);
заболевания, которые вызывают продолжающееся повреждение суставов (включая ревматоидный артрит, остеоартрит и артрит вследствие травмы);
инфекция, которая попадает в кровоток (бактериемия);
Например, бактерии могут скапливаться в одном или нескольких суставах у пациента с пневмонией (инфекцией легких) или сепсисом (инфекция крови), приводящими к инфекционному артриту.
Острый инфекционный артрит может развиваться у детей, не входящих в группы риска. Около 50 % детей с инфекциями суставов младше 3 лет. Однако стандартная вакцинация в детском возрасте для защиты от Haemophilus influenzae и Streptococcus pneumoniae позволяет снизить заболеваемость в этой возрастной группе.
Хронический инфекционный артрит
Возбудителем хронического инфекционного артрита обычно является Mycobacterium tuberculosis (основной возбудитель туберкулеза), грибки или бактерии.
К факторам риска хронического инфекционного артрита относятся:
угнетение иммунной системы (например, при злокачественном новообразовании или применении лекарственных препаратов, которые угнетают иммунную систему);
Люди с хроническим артритом, например, c ревматоидным артритом, при внезапном возникновении боли и отека в одном суставе должны немедленно обратиться к врачу, поскольку у них возможна инфекция даже при отсутствии повышенной температуры.
Симптомы
При остром инфекционном артрите симптомы обычно развиваются в течение от нескольких часов до нескольких дней. В инфицированном суставе возникает сильная боль, иногда он краснеет и становится горячим на ощупь. Боль резко усиливается при движении или прикосновении. В инфицированном суставе скапливается жидкость, приводя к его отеку и уменьшению подвижности. К симптомам иногда относится также жар и озноб.
Гонококковый артрит обычно сопровождается незначительными симптомами. У человека обычно развивается лихорадка, которая продолжается в течение 5-7 дней. У больных возможны волдыри на коже, бугорки, язвы, сыпь или язвы слизистой оболочки ротовой полости или половых органов, а также язвы на туловище, кистях или ногах. Боль может распространяться на другой сустав до того, как он станет отекшим и болезненным. Возможно воспаление сухожилий.
Новорожденные и дети, еще не начавшие говорить, стараются избегать движений в пораженном суставе, раздражительны, могут отказываться от еды; также у них может наблюдаться лихорадка, однако лихорадка может отсутствовать. Маленькие дети с инфекцией коленного или тазобедренного сустава могут отказываться ходить.
При хроническом инфекционном артрите к симптомам обычно относится постепенный отёк, теплота на ощупь, минимальное покраснение области сустава или отсутствие покраснения и ноющая боль, которая может быть незначительной и не такой сильной, как при остром инфекционном артрите. Обычно поражен один сустав.
У больных могут наблюдаться другие симптомы, в зависимости от причины инфекционного артрита, например, симптомы болезни Лайма или увеличенные лимфатические узлы, если причиной является инфицированная рана от укуса.
Диагностика
Анализ и бактериологический посев синовиальной жидкости
Иногда анализы мокроты, спинномозговой жидкости и мочи
Иногда рентгенологическое исследование, магнитно-резонансная томография (МРТ) или ультразвуковое исследование
Врачи обычно подозревают инфекционный артрит у людей с тяжелым или необъяснимым артритом, а также у людей с другими сочетаниями симптомов, которые могут отмечаться у больных с инфекционным артритом.
Обычно при первой возможности у них берут образец синовиальной жидкости с помощью иглы (процедура носит название аспирации сустава, или артроцентеза). Образец изучают на предмет повышенного числа лейкоцитов, наличия бактерий и других микроорганизмов. В лаборатории обычно есть возможность вырастить культуру бактерий-возбудителей из синовиальной жидкости и определить их (так называемый посев), за исключением случаев, когда больной недавно принимал антибиотики. Однако бактерии, которые вызывают гонорею, болезнь Лайма и сифилис, сложно выделить из синовиальной жидкости. Если бактерии способны расти при посеве, лаборатория определяет, какие антибиотики будут эффективны.
Врач обычно проводит анализ крови, так как бактерии, вызывающие инфекции суставов, часто попадают в кровоток. Мокрота, спинномозговая жидкость и моча также могут подвергаться бактериологическому анализу для определения источника инфекции и выявления инфекции в других местах.
Если врач подозревает, что возбудителем инфекционного артрита является гонококк, у пациента возьмут также образцы из уретры, шейки матки, прямой кишки и горла. Кроме того, проводятся анализы на хламидийную инфекцию гениталий (другое заболевание, передающееся половым путём), поскольку многие люди с гонореей также имеют хламидийную инфекцию.
Чтобы облегчить обнаружение и идентификацию бактерий, врач может назначить анализ суставной жидкости с использованием метода полимеразной цепной реакции (тип теста амплификации нуклеиновой кислоты [ТАНК]) для выявления ДНК гонококков и микобактерий.
Врачи могут назначить рентгенологическое исследование пораженного сустава для исключения других заболеваний. При невозможности обследования сустава или его пункции врачи могут проводить магнитно-резонансную томографию (МРТ). МРТ и ультразвуковое исследование также проводятся для обнаружения скоплений жидкости или гноя (абсцессов).
Прогноз
Инфекционный артрит, вызванный негонококковыми бактериями, может в течение нескольких часов или дней привести к необратимому разрушению хрящевой ткани сустава.
Вызванный гонококковыми бактериями инфекционный артрит обычно не приводит к необратимому поражению суставов.
У больных с ревматоидным артритом обычно не наблюдается полного восстановления инфицированного сустава, и частота смертельных исходов увеличена.
Лечение
Антибиотики или противогрибковые препараты
Шинирование суставов с последующей лечебной физкультурой
Нестероидные противовоспалительные препараты (НПВП) позволяют ослабить боль, воспаление и лихорадку.
При подозрении на наличие инфекции важно начать лечение антибиотиками как можно раньше, даже до того, как с помощью лабораторных анализов будет определен микроорганизм, вызвавший инфекцию. До того, как возбудитель будет установлен (продолжительность анализа синовиальной жидкости обычно составляет 48 часов), больному назначают антибиотики, активные в отношении бактерий, которые, скорее всего, вызвали инфекцию. Антибиотики сначала вводят в вену (внутривенно), чтобы гарантировать поступление в инфицированный сустав достаточного количества лекарственного препарата.
Если антибиотики эффективны в отношении бактерии-возбудителя, улучшение обычно возникает в течение 48 часов. Как только врач получит результаты лабораторного исследования, может быть проведена замена антибиотика, в зависимости от чувствительности определенной бактерии к конкретному антибиотику. Лечение антибиотиками с внутривенным введением продолжается в течение 2-4 недель. Затем проводится переход на пероральные антибиотики в больших дозах на срок от 2 до 6 недель.
Инфекция, которая держится продолжительное время и не излечивается в результате применения традиционных антибиотиков, может быть вызвана микобактериями или грибками. Инфекции, вызванные грибками, лечат с помощью противогрибковых препаратов. Инфекции, вызванные микобактериями, лечат с помощью комбинации антибиотиков. Инфекции, вызванные грибками и микобактериями, требуют продолжительного лечения.
Инфекции, вызванные вирусами, обычно проходят без применения антибиотиков.
Врач часто дренирует гной с помощью иглы (аспирация) для предотвращения его скапливания, поскольку скопления гноя могут повредить сустав и затруднить лечение антибиотиками. Если дренаж с помощью иглы сопряжен со сложностями (например, в случае тазобедренного сустава) или неэффективен, для очистки сустава могут применять артроскопию (процедура с использованием небольшого эндоскопа для прямого осмотра внутренней части сустава) или хирургическое вмешательство. Часто проводят несколько сеансов аспирации. Изредка для оттока гноя оставляют дренажную трубку.
Шина на сустав (для предотвращения его движений) накладывается на первые несколько дней после развития инфекции для облегчения боли, а для укрепления мышц и профилактики скованности и необратимой потери функции сустава назначают лечебную физкультуру.
Читайте также:


