Системная красная волчанка лечение стволовыми клетками
Красная волчанка, лечение стволовыми клетками
КРАСНАЯ ВОЛЧАНКА , незаразное хроническое воспалительное заболевание, названное так по характерному покраснению кожи, напоминающему, как говорили когда-то, полосы красноты на коже после волчьих укусов или красноватые волчьи щеки (лат. Lupus erythematosus, от lupus — волк, erythema - покраснение). Красная волчанка не имеет ничего общего с волчанкой обыкновенной (туберкулезной) — редкой формы туберкулеза, приводящей к образованию типичных рыжевато-бурых узлов на коже.
Красная волчанка проявляется разнообразными симптомами и протекает либо в форме кожной дискоидной красной волчанки (ДКВ), либо с поражением внутренних органов в форме системной красной волчанки (СКВ). При ДКВ на коже (в большинстве случаев на лице и других открытых частях тела, доступных солнечному свету) образуются характерные округлые приподнятые бляшки с покраснением и шелушением, в центре которых часто наблюдается рубцевание; внутренние органы, как правило, не поражаются.
СКВ — заболевание ревматической природы, т. е. относится к той же группе болезней, что и ревматоидный артрит. При СКВ возможны тяжелые поражения суставов, кожи, нервной системы, почек и других внутренних органов. Кожные изменения могут быть такими же, как при ДКВ, либо проявляться покраснением и сыпью на скулах в характерной форме бабочки на лице; однако нередко кожа остается нормальной.
Распространение. Красной волчанкой в основном страдают молодые женщины. Среди больных ДКВ семеро из десяти — женщины в возрасте ок. 30 лет и старше, среди больных СКВ девять из десяти - женщины, у половины из них первые симптомы заболевания появляются между 15 × 25 годами.
Причина ДКВ неизвестна, как и причина 90% случаев СКВ; в 10% это, по-видимому, побочный эффект лекарственной терапии, например прокаинамидом (новокаинамидом), который назначают при сердечной аритмии.
Предполагают, что красная волчанка имеет аутоиммунное происхождение, т. е. вызвана аллергическими реакциями особого типа, при которых в организме больного вырабатываются антитела (аутоантитела) к собственным тканям, как будто он вакцинирован против самого себя. Причины таких аллергических реакций остаются неясными.
Диагноз. При СКВ происходит повреждение части лейкоцитов и из них высвобождаются ядерные компоненты (нуклеопротеины), претерпевающие в плазме крови определенные изменения. Этот ядерный материал, поглощенный другими лейкоцитами, изменяет их свойства, превращая в т.н. LE-клетки (LE — от lupus erythematosus). По-видимому, сходным образом действуют аутоантитела, направленные против ядерного материала собственных тканей и называемые поэтому антинуклеарными (антиядерными). В связи с этим при диагностике СКВ выявляют LE-клетки и антинуклеарные аутоантитела, а также определяют количество определенных сывороточных белков, содержание которых падает в активной фазе аутоиммунного заболевания.
Прогноз. Многие заболевшие СКВ в слабо выраженной или волнообразно текущей форме способны вести нормальный образ жизни. Продолжительность заболевания зависит от его тяжести и от того, какие органы преимущественно поражены. Чаще всего причиной смерти служат необратимое повреждение почек и инфекция.
При лечении красной волчанки удается поддержать органы-мишени и приостановить ухудшение.
Внимание!
Мы разработали уникальные процедуры восстановления суставов - это применение специально разработанных нами гелей, содержащих Ваши клетки!
| Лаборатория : Вот так выращивают стволовые клетки. | |
 |  |
| Ваши клетки в надёжных руках | Подготовка клеток к процедуре. |
 |  |
| Специальный инкубатор для выращивания клеток | Клетки готовы к замораживанию. |
 |  |
| В таких флаконах растут клетки. | Контроль за ходом выращивания. |
 |  |
| Проведение лабораторных работ. | Работа в специальной стерильной зоне. |
детский церебральный паралич. Подробнее.
Лечение и профилактика. Подробнее.
Лечение всех стадий заболевания. Подробнее.
инфаркт миокарда, стенокардия и др. Подробнее.
Лечение всех стадий заболевания. Подробнее.
Лечение всех стадий заболевания. Подробнее.
Лечение всех стадий заболевания. Подробнее.
1 и 2 типа, оздоровление. Подробнее.
Неизлечимая болезнь: что нашли у Юлии Началовой
16 марта умерла певица Юлия Началова. По данным СМИ, одной из болезней, ставших причиной ее смерти, стала системная красная волчанка.
Системная красная волчанка — это хроническое аутоиммунное заболевание соединительной ткани и сосудов. При нем антитела, вырабатываемые иммунной системой, повреждают здоровые клетки. Название болезнь получила из-за своего характерного признака — сыпи на переносице и щеках, которая, как считали в Средневековье, напоминает места волчьих укусов.
Впрочем, сыпь появляется лишь у 30-50% пациентов, а дерматологические проявления в целом — примерно в 65% случаев. На руках и туловище могут появиться толстые красные чешуйчатые пятна, в последующем способные привести к атрофии кожи, также среди возможных проявлений болезни — язвы на слизистой рта и влагалища, трофические язвы.
Многие пациенты жалуются на боли в суставах, в основном запястий и мелких суставов рук.
Болезнь способна приводить к деформации суставов, в 20% случаев изменения носят необратимый характер.
Болезнь поражает легкие, вызывая пневмонию и плеврит, сердечно-сосудистая система страдает от перикардита, миокардита, эндокардита Либмана-Сакса (воспалительных заболеваний различных частей сердца). Также у больных волчанкой чаще и быстрее развивается атеросклероз. При поражении желудочно-кишечного тракта выявляются стоматит, расширение пищевода, поражение печени, ишемия стенки желудка. Также при волчанке нередко встречается нефрит — воспалительное заболевание почек.
Возможны поражения нервной системы — двигательные расстройства, головные боли, менингит, судорожные расстройства. Одно из самых опасных неврологических проявлений волчанки — демиелинизирующий синдром, при котором разрушается оболочка нервных клеток. Это приводит к ухудшению проводимости сигналов в пострадавших нервах. В зависимости от локализации, синдром способен вызвать целый спектр осложнений, от дрожи и нарушения координации движений до слепоты и паралича.
Из неспецифических симптомов больных беспокоят необоснованные подъемы температуры, слабость, головные боли, боли в мышцах, быстрая утомляемость.
Волчанка влияет на продолжительность жизни.
Выживаемость через 10 лет после постановки диагноза — 80%, через 20 лет — 60%.
Основные причины смерти — нефрит и неврологические проявления болезни, а также инфекции, развившиеся на фоне основного заболевания. Есть случаи выживаемости 25—30 лет.
Вылечить волчанку нельзя, однако возможно облегчить ее симптомы. Для этого используются глюкокортикостероиды, терапия стволовыми клетками, иммуннодепресанты. При осложнениях применяется симптоматическое лечение.
Отметим, что врач Юлии Началовой опровергает наличие у нее красной волчанки.
Тем не менее, от этого заболевания страдают и за рубежом — в частности, певицы Леди Гага, Тони Брэкстон, Селена Гомес. Последняя из-за болезни пережила пересадку почки, орган ей пожертвовала подруга, актриса Франсия Райса.
Болеющие волчанкой матери рожают детей, страдающих аутизмом, в два раза чаще, чем остальные женщины,
выяснили американские ученые из нью-йоркского госпиталя Маунт-Синай.
К подобным выводам они пришли по итогам исследования, участницами которого стали 509 женщин с волчанкой и их 719 детей, а также 5900 женщин без волчанки и их 8500 детей.
В то же время развитие аутизма у ребенка ученые связывают со временем зачатия. По их мнению, оно не должно происходить в моменты активного проявления болезни.
Ранее был идентифицирован ген, влияющий на осложнения при заболевании волчанкой. Оказалось, что неактивный белок ABIN1 не просто делает организм человек беззащитным перед болезнью, но и способствует деактивации путей, препятствующих воспалительному процессу.
Кроме того, ученым удалось связать функционирование этого белка с последующим влиянием на транскрипционный фактор NF-?B, что в будущем позволит эффективно бороться с заболеванием.
Российские же ученые разработали прототип принципиально нового лекарства для лечения аутоиммунных заболеваний, в том числе и волчанки.
- 18332
- 14,3
- 4
- 4
Системная красная волчанка — это мультифакторное заболевание, развивающееся на основе генетического несовершенства иммунной системы и характеризующееся выработкой широкого спектра аутоантител к компонентам клеточного ядра. Молекулярно-генетические основы болезни изучены довольно плохо, в связи с чем специфического лечения до сих пор не создано, а в основе проводимой в клинике патогенетической терапии лежат иммунодепрессанты — глюкокортикостероиды и цитостатики. И вот, после более чем 50 лет попыток разработать специфическое лечение волчанки, произошел сдвиг: Управление по контролю за качеством пищевых продуктов и лекарств США официально утвердило в качестве лекарства от волчанки препарат Бенлиста (Benlysta) на основе моноклональных антител, специфически блокирующих B-лимфоцит-стимулирующий белок (BLyS).
Системная красная волчанка (СКВ) — одно из самых распространённых аутоиммуных заболеваний, в основе которого лежит генетически обусловленное комплексное нарушение иммунорегуляторных механизмов. При заболевании происходит образование широкого спектра аутоантител к различным компонентам ядра клеток и формирование иммунных комплексов. Развивающееся в различных органах и тканях иммунное воспаление приводит к обширным поражениям микроциркуляторного кровяного русла и системной дезорганизации соединительной ткани [1], [2].
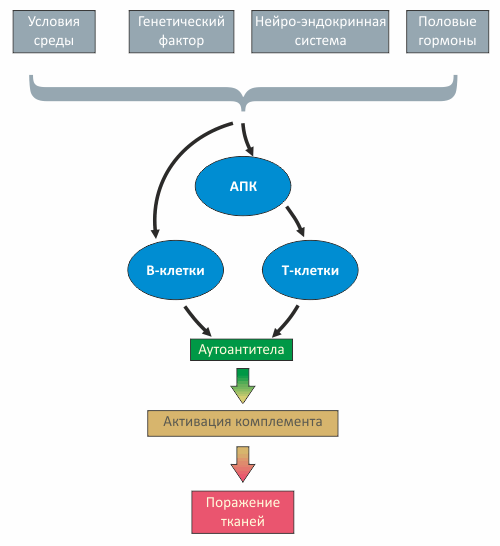
Рисунок 1. Патогенез СКВ
Волчанка во многом связана с нарушениями на уровне пролиферации различных клонов В-клеток, активируемых многочисленными антигенами, в роли которых могут выступать медицинские препараты, бактериальная или вирусная ДНК и даже фосфолипиды мембраны митохондрий. Взаимодействие антигенов с лейкоцитами связано либо с поглощением антигенов антиген-презентирующими клетками (АПК), либо с взаимодействием антигена с антителом на поверхности В-клетки.
В результате поочередной активации то T-, то B-клеток увеличивается продукция антител (в том числе, аутоантител), наступает гипергаммаглобулинемия, образуются иммунные комплексы, чрезмерно и неконтролируемо дифференцируются Т-хелперы. Разнообразные дефекты иммунорегуляции, свойственные СКВ, связаны также с гиперпродукцией цитокинов Th2-типа (IL-2, IL-6, IL-4, IL-10 IL-12).
Одним из ключевых моментов в нарушении иммунной регуляции при СКВ является затрудненное расщепление (клиренс) иммунных комплексов, — возможно, вследствие их недостаточного фагоцитоза, связанного, в частности, с уменьшением экспрессии CR1-рецепторов комплемента на фагоцитах и с функциональными рецепторными дефектами.
Распространённость СКВ колеблется в пределах 4–250 случаев на 100 000 населения; пик заболеваемости приходится на возраст 15–25 лет при соотношении заболевших женщин к мужчинам 18:1. Наиболее часто заболевание развивается у женщин репродуктивного возраста с увеличением риска обострения во время беременности, в послеродовом периоде, а также после инсоляции и вакцинации.
СКВ часто становится причиной инвалидности. В развитых странах в среднем через 3,5 года после постановки диагноза 40% больных СКВ полностью прекращают работать, — в основном, в связи с нейрокогнитивными дисфункциями и повышенной утомляемостью. К потере трудоспособности чаще всего приводят дискоидная волчанка и волчаночный нефрит.
Клинические проявления СКВ чрезвычайно разнообразны: поражение кожи, суставов, мышц, слизистых оболочек, лёгких, сердца, нервной системы и т.д. У одного пациента можно наблюдать различные, сменяющие друг друга варианты течения и активности заболевания; у большинства больных периоды обострения заболевания чередуются с ремиссией. Более чем у половины больных есть признаки поражения почек, сопровождающиеся ухудшением реологических свойств крови [4].
Поскольку молекулярные и генетические механизмы, лежащие в основе заболевания, до сих пор как следует не изучены, специфического лечения волчанки до недавнего времени не существовало. Базисная терапия основана на приёме противовоспалительных препаратов, действие которых направлено на подавление иммунокомплексного воспаления, как в период обострения, так и во время ремиссии. Основными препаратами для лечения СКВ являются:
Для лечения СКВ применяют также препарат моноклональных антител, селективно действующий на CD20 + В-лимфоциты, — ритуксимаб, зарегистрированный FDA для лечения неходжкинской лимфомы. Впрочем, высокая цена этого препарата не позволила ему получить широкого применения при лечении СКВ в нашей стране.
Исследователи, желая специфически блокировать BLyS, сделали ставку на человеческое моноклональное антитело, разработанное совместно с английской биотехнологической фирмой Cambridge Antibody Technology, и названное белимумаб (belimumab). В начале марта 2011 года американское Управление по контролю за качеством пищевых продуктов и лекарственных препаратов (FDA) впервые за 56 лет одобрило препарат, предназначенный для специфического лечения системной красной волчанки. Эти препаратом стал Бенлиста — коммерческое название антитела белимумаба, производством которого уже занимается компания GlaxoSmithKline. До того FDA одобряла для терапии СКВ гидроксихлорохин — лекарство от малярии; было это в 1956 году.
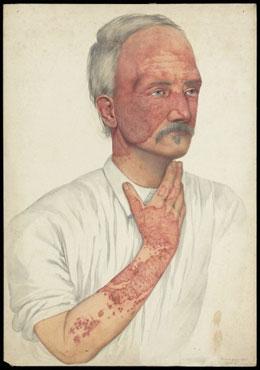
Рисунок 2. Человек, больной системной красной волчанкой (акварель 1902 года кисти Мэйбл Грин). Свое название заболевание получило ещё в средневековье, когда людям казалось, что характерная волчаночная сыпь на переносице напоминает волчьи укусы.
Целенаправленная терапия
Следующие на очереди
О заболевании
Красная волчанка (болезнь Либмана-Сакса, эритематоз, СКВ) – на сегодняшний день является одним из неизлечимых заболеваний человека. Несмотря на то, что болезнь описана еще в средневековых медицинских трактатах и человечество давно пытается найти средства лечения этого аутоиммунного заболевания, СКВ до сих пор неизлечима, так как доподлинно неизвестны причины возникновения этого недуга.
Красная волчанка развивается достаточно медленно, но при отсутствии эффективного лечения большинство больных не доживают до преклонного возраста. При лечении системной красной волчанки в Израиле удается добиться стойких длительных ремиссий без проявления симптомов. Очень много людей успешно справляется с этим заболеванием и его осложнениями на протяжении 25-30 лет, и окружающие даже не подозревают у них эту болезнь.
СКВ может поражать не только кожу, зафиксированы случаи поражения суставов, внутренних органов, мышц, в зависимости от типа заболевания. Существует несколько форм системной красной волчанки:
- лекарственно индуцированная волчанка – возникает вследствие приема определенных препаратов, симптоматика прекращается после отмены этих лекарственных средств. Преимущественно проявляется высыпаниями на коже.
- дискоидная красная волчанка также проявляется характерными высыпаниями на коже, в некоторых случаях может перейти в системное заболевание.
- неонатальная красная волчанка проявляется у новорожденных характерными высыпаниями на коже, поражениями печени и сердца. Этот тип волчанки встречается довольно редко.
Точные причины СКВ еще не установлены, но существует определенная связь между заболеваниями и генетическим фактором. Кроме этого, появлению заболевания могут способствовать и определенные вирусы, в частности – наличие в крови пациентов антител к ретровирусам. Кроме этого, установлена также гендерная предрасположенность – системная красная волчанка преимущественно поражает женщин детородного возраста.
Лечение красной волчанки в Израиле проводится с учетом индивидуальных особенностей организма пациента, степени тяжести болезни и результатов диагностики, на основании которых и разрабатывается оптимальная программа терапии.
получить бесплатную консультацию
Комплекс диагностических мероприятий:
- развернутые лабораторные исследования крови и мочи;
- определение панели коллагенозов
- КТ, МРТ органов-мишеней – почек, сердца, легких, головного мозга,
- биопсия кожи, пораженных лимфоузлов, почек
- консультация дерматолога
- УЗИ печени, почек, мочевого пузыря и др. органов брюшной полости
- ЭКГ сердца в состоянии нагрузки
- консультация кардиолога
- допплерография сосудов почек
- рентгенография суставов для оценки степени артрита
- осмотр и консультация офтальмолога
- консультация специалиста по аутоиммунным заболеваниям.
Данный перечень диагностических мероприятий не является общим для всех больных, в каждом конкретном случае методы диагностики могут присутствовать как опции.
Профессиональная диагностика позволяет выявить очаги наибольшего поражения. Иногда болезнь ограничивается поражением кожных покровов и слизистой (дискоидная красная волчанка, эритематоз), а специфический рисунок красной сыпи на лице и дал название этому заболеванию, но в большинстве случаев с течением времени заболевание вовлекает практически все органы – суставы, почки, сердце, легкие, нервную систему.
Методы лечения красной волчанки в Израиле
Терапия СКВ – это трудный, непрерывный, многолетний процесс, но немедленное лечение в Израиле начинается непосредственно с получения первых результатов диагностики.
Лечение красной волчанки в Израиле очень индивидуально, именно этим и объясняется его эффективность. Основным методом является медикаментозное лечение, которое включает использование гормональных противовоспалительных препаратов, а также иммунодепрессантов. В базовом варианте применяются глюкокортикостероиды в виде инъекций, таблеток или мазей, а также цитостатические иммунодепрессанты; при поражении суставов назначаются нестероидные препараты, которые даже при монотерапии позволяют снизить температуру, снять отечность, уменьшить боль. При лечении СКВ нередко используются противомалярийные средства, подавляющие иммунную реакцию организма.
записаться на лечение
Больные тяжелыми формами аутоиммунных заболеваний нуждаются в периодической очистке крови от иммунных комплексов, антител, поврежденных клеток. Для этого используется плазмаферез, гемосорбция или криоплазмосорбция. Эти методы приносят быстрое облегчение состояния больного, снимают критические проявления болезни, такие как гемморагический шок, молниеносный васкулит, церебральную кому. Применение современных иммунносорбентов позволяют удалять из плазмы крови даже элементы поврежденной ДНК клеток.
Новым методом лечения красной волчанки в Израиле является пересадка костного мозга. Этот метод показывает впечатляющие результаты. Подготовка к трансплантации включает забор костного мозга у самого больного и максимальное уничтожение аутоиммунных клеток в организме больного высокодозной иммунносупрессивной терапией цитостатиками. Пациент в это время должен находиться практически в стерильных условиях, этот режим достигается благодаря специальному оборудованию в больничных палатах. После инфузии стволовых клеток в течение нескольких недель происходит приживление клеток и нормализация кроветворения, после чего больной выписывается домой.
Posted September 20th, 2011 by renat & filed under Вестник КазНМУ, Русский, Фармакология.
Статья посвящена анализу исследований по изучению роли трансплантации стволовых кроветворных клеток при аутоиммунных заболеваниях. Рассмотрены роль, показания, виды трансплантации стволовых кроветворных клеток при аутоиммунных заболеваниях. Сделан вывод, что данный метод лечения может рассматриваться дополнение к обычной иммуносупрессивной терапии.
Совершенствование методов обследования, способствующее более ранней диагностике, и расширение терапевтических подходов с использованием различных режимов приемов глюкокортикоидов, антималярийных, цитостатических, генно-инженерных биологических препаратов позволили значительно улучшить прогноз заболевания. Так, в одном из первых исследований, посвященных продолжительности жизни при СКВ, сообщается о 51% выживаемости в течение 4 лет от начала заболевания [6], то в современных работах 5- и 10-летняя выживаемость составляет 96 и 85% соответственно [7].
Однако, несмотря на достигнутые успехи, лечение больных аутоиммунными заболеваниями сопровождается определенными сложностями. Течение заболеваний носят часто непредсказуемый характер. Кроме того, у некоторой части больных при наличии высокой активности заболевания отмечаются неэффективность стандартной терапии или ее осложнения, что существенно лимитирует ее дальнейшее применение. В этих случаях прогрессирующее течение заболевания неуклонно ведет к неблагоприятному исходу. Таким образом, несмотря на улучшение прогноза, смертность больных по прежнему выше в 3-5 раз выше, чем в общей популяции, что и определяет необходимость поиска новых терапевтических подходов при аутоиммунных заболеваниях.
По утверждению ряда авторов [8,9] аутоиммунные заболевания объединяются в одну группу на основании общих особенностей патогенеза, и подходов к лечению, основой которой является иммуносупрессивная терапия. Общим звеном в патогенезе АИЗ являются нарушения в иммунной системе, приводящие к развитию поликлонального иммунного ответа на собственные антигены (в этом ответе участвуют В-, Т- лимфоциты и макрофаги) [10, 11]. В связи с тем, что все клетки иммунной системы происходят из единой стволовой клетки, высказана гипотеза о развитии АИЗ вследствие дефектов стволовых клеток или их ближайших потомков [12]. Это предположение подтверждают результаты экспериментальных и клинических исследований.
Результаты многочисленных клинических наблюдений свидетельствуют о том, что при сочетании различных АИЗ (рассеянный склероз, системная красная волчанка, ревматоидный артрит, васкулиты, неспецифический язвенный колит, болезнь Крона, псориаз и др.), по поводу которых была проведена аллогенная или аутологичная трансплантация, практически во всех случаях после миелотрансплантации отмечали стойкую и длительную ремиссию в течение АИЗ [17, 18, 19, 20].
Использование иммуносупрессивной терапии без трансплантации СКК вызывало лишь кратковременное улучшение. Был сделан вывод о важной роли самой трансплантации СКК в достижении ремиссии АИЗ [21].
Так, после трансплантации СКК у больной СКВ было отмечено снижение индекса активности SLEDAI с 40 до 2 баллов [22]. В исследованиях у половины из 50 пациентов СКВ после ВИСТ с ТСКК достигнута клиническая и серологическая ремиссия на протяжении 5 лет, общая 5-летняя выживаемость составила 84% [23]. После проведения ТСКК у больных системной склеродермией установлен частичный или полный ответ у 92% случаев, в виде уменьшения кожного счета, улучшения микроциркуляции. Изменений со стороны легких не отмечено, что возможно связано с уже изначально необратимыми изменениями в легких [24]. У больных СКВ с антифосфолипидным синдромом отмечается после ВИСТ с ТССК положительная серологическая картина – достоверное снижение титра антифосфолипидных антител, антикардиолопина Ig M и Ig G [25]. Отмечалось стабилизация почечной функции, снижение индекса SLEDAI, титра ANA, антител в двухцепочной ДНК у пациентов СКВ после ТССК [26]. В исследованиях, проведенных в Европе, все пациенты с хроническим и прогрессирующим течением аутоиммунного заболевания, прошедшие неоднократно иммуносупрессивную терапию без эффекта. В связи с чем, трансплантация стволовых клеток является единственным методом для пациентов с наихудшим прогнозом и отсутствием эффекта от проводимой терапии. Несмотря на положительный ответ на трансплантацию стволовых клеток, механизм действия клеточной терапии пока не объясним до конца.
До настоящего времени в международном сообществе нет единой точки зрения по многим вопросам трансплантации СКК при аутоиммунных заболеваниях. Тем не менее, большинство авторов считают, что в ближайшие годы этот метод будут все шире использовать для лечения АИЗ. К перспективным направлениям относят применение ТСКК при аутоиммунных гематологических (гемолитическая анемия, тромбоцитопения, нейтропения), ревматических (системная красная волчанка, системная склеродермия, ревматоидный артрит, системный васкулит) и неврологических (рассеянный склероз, миастения и др.) заболеваниях [27, 28].
Окончательный ответ на вопрос об абсолютных и относительных показаниях к проведению ВИСТ с ТСКК при АИЗ будет дан после завершения многоцентровых рандомизированных исследований, посвященных данной проблеме. Тем не менее, общие показания к применению метода могут быть сформулированы. Очевидно, что ВИСТ с ТСКК предназначена в первую очередь для лечения больных с органонеспецифическими аутоиммунными заболеваниями, характеризующимися агрессивным течением и первичной или вторичной резистентностью к традиционным методам противовоспалительной и иммуносупрессивной терапии. Для этой группы АИЗ ВИСТ с ТСКК является единственным видом лечения, позволяющим добиться ремиссии в течение заболевания. ВИСТ с ТСКК также можно рассматривать как метод выбора при заболеваниях, неизбежно приводящих к тяжелой инвалидизации больного, таких, например, как рассеянный склероз.
Это один из важнейших и широко обсуждаемых в международном медицинском сообществе вопросов – когда проводить трансплантацию стволовых кроветворных клеток при аутоиммунных заболеваниях? Определены показания для трансплантации — быстротекущее течение заболевания, первичная резистентность к стандартным методам лечения, выход заболевания из-под контроля традиционных методов лечения, высокая вероятность ранней инвалидизации больного.
A. Fassas et al. [29], охарактеризовали показания к проведению данной терапии при СКВ, РА. В частности при СКВ показанием к проведению подобного вида лечения являются люпус-нефрит (Ш-IV морфологический класс, цереброваскулит, вторичный антифосфолипидный синдром, васкулит легких с легочной гипертензией, ECLAM > 6, гемолитическая анемия 4, и тромбоцитопения. Показаниями к проведению ВИСТ с AT СКК при РА критериями включения в протокол являются высокая активность процесса, серопозитивность, вовлечение более 30 суставов и отсутствие ответа на преднизолон и два препарата второй линии иммуносупрессивной терапии.
Выделено 4 вида трансплантаций в зависимости от целей операции, времени ее проведения, характера патологического процесса и степени инвалидизации больного в момент проведения трансплантации.
Ранняя трансплантация Цели А. Патогенетическая – предотвратить развитие необратимых изменений в органах и тканях на этапе иммуновоспалительного процесса. Б. Конечная – сохранить качество жизни больного, предупредить его инвалидизацию. Время выполнения операции – в дебюте заболевания при наличии неблагоприятных прогностических факторов или тяжелой инвалидизации больного.
Трансплантация отчаяния. Цели А. Патогенетическая – остановить прогрессирование заболевания на фоне большого количества очагов необратимых изменений и существенно нару шенных функций, предотвратить появление новых очагов поражения. Б. Конечная – сохранить качество жизни больного на максимально возможном уровне, предотвратить формирование критической инвалидизации пациента. Время выполнения операции – в далеко зашедшей стадии заболевания при высокой активности иммуновоспалительного процесса и быстром прогрессировании инвалидизации больного. Примечание. Вопрос о проведении трансплантации отчаяния является сложной профессиональной и этической проблемой, для его решения требуются глубокий анализ клинических, психологических и юридических аспектов, взвешенное и обоснованное обсуждение с участием врачей, больного и членов его семьи.
Необходим гибкий подход, ориентированный на индивидуальные особенности течения патологического процесса у конкретного больного. Для группы АИЗ, неизбежно приводящих к тяжелой инвалидизации больных (рассеянный склероз,системная склеродермия и др.), одной из многообещающих стратегий является проведение ранней ТСКК с целью обеспечения контроля за иммуновоспалительным процессом на этапе, когда отсутствуют необратимые изменения в тканях и органах. Такой подход перспективен в отношении предотвращения инвалидизации больного. Большой интерес вызывает отсроченная трансплантация, позволяющая в дебюте заболевания заготовить СКК и таким образом обеспечить возможность применить эффективный резервный метод терапии в случае выхода заболевания из/под контроля традиционных способов лечения или при решении интенсифицировать терапию по иным показаниям.
В настоящее время в ряде стран Европы и Северной Америки проводят клинические исследования с целью изучения эффективности ВИСТ с ТСКК при АИЗ: рассеянном склерозе, системной склеродермии, ревматоидном артрите, системной красной волчанке и др. Большинство рандомизированных исследований, посвященных изучению этой проблемы, еще не завершены. Тем не менее полученные предварительные данные и результаты экспериментальных исследований позволяют наметить план ряда будущих исследований. В ближайшем будущем в терапии АИЗ, возможно, будут использованы комбинации ВИСТ+ТСКК с моноклональными антителами, антицитокиновыми препаратами, интерфероном (рассеянный склероз) и др.
Все вышеизложенное обосновывает актуальность изучения механизмов воздействия стволовых клеток при аутоиммунном процессе. Появление в арсенале ревматолога ВДТ с ТСКК увеличивает терапевтические возмрожности в лечении рефрактерных аутоиммунных заболеваний и позволяет надеяться на успешность лечения и прогноза этих заболеваний в будущем. Таким образом, трансплантация стволовых клеток может служить дополнением к обычной иммуносупрессивной терапии.
Литература
- Crow M.K. Developments in the clinical understanding of lupus. Arthr Res Ther 2009; 11(5):245.
- Davidson A., Diamond B.Autoimmune diseases. New Engl J Med 2001; 345:340-50,
- Rioux J.D., Abbas A.K. Paths to understanding the genetic basis of autoimmune disease. Nature 2005; 435:584-9,
- Bizzaro N., Tozzoli R., Shoenfeld Y. Are we at stage to predict autoimmune rheumatic diseases? Arthr Rheum 2007; 56: 1736-44,
- Насонов Е.Л., Александрова Е.Н. современные технологии и перспективы лабораторной диагностики ревматических болезней. Тер. Архив 2010; 5:5-9,
- Merrel M., Shulman L.E. Determination of prognosis in chronic disease. Illustrated by SLE. J Chron dis 1955; 1:12-32,
- Ippolito A., Petry M. An update on mortality in systemic lupus erythematosus. Clin Exp Rheumatol 2008; 26 (Suppl.51):72-9.
- Kolb H. J., Schattenberg A., Goldman J. M. et al. Graft-versus-leukemia effect of donor lymphocyte transfusion in marrow grafted patients: European Group for Blood and Marrow Transplantation Working Party Chronic Leukemia //Blood.-1995.-Vol. 86. -№ 5.-P. 2041-2050.
- McGuire W. P., Hoskins W. J., Brady M. F. et al. Cyclopho-sphamkte and cisplatin compared with paclitaxel and cisplatin in patients with stage III and stage IV ovarian cancer // N. Engl. J. Med. — 1996. — Vol. 334. — № 1. — P. 1-6.
- Насонов Е. Л. Современные направления иммунологических исследований при хронических воспалительных и аутоиммунных заболеваниях человека // Тер. архив. — 2001. — Т. 73. — № 8. — С. 43— 46.
- Назаренко Г. И., Кишкун А. А. Клиническая оценка результатов лабораторных исследований. — М.: Медицина, 2002. — 544 с.
- Шевченко Ю. Л., Бойцов С. А., Новик А. А., Лядов К. В. Концепция клеточной терапии аутоиммунных заболеваний // Вестн. Рос. АМН. -2004. — № 9. — С. 40-4.
- Brunner M.s Knobl P., Kalhs P., Machold K. et al. Autologous peripheral blood stem cell transplantation for the treatment of systemic lupus erythematosus — acase report // Bone Marrow Transplantation. — 2001. — Vol. 27. — P. 117.
- Вермель А. Е. Стволовые клетки: общая характеристика и перспективы применения в клинической практике // Клинич. медицина. — 2004. — № 1. —С. 5-11.
- 15. McSweeney P., Furst D. High-dose immunosuppressive therapy for rheumatoid- arthritis: some answers, more questions // Ibid. — 1997. — Vol. 42. —P. 2269-2274.
- 16. Tyndall A., Gratwohl A. Blood and marrow stem cell transplants in autoimmune disease: a consensus report written on behalf of the European League Against Rheumatism (EULAR) and the European Group for Blood and Marrow Transplantation (EBMT) // B. J. Rheumatol. — 1997. — Vol. 36. — P. 390-392.
- 17. Новик А.А., Богданов А.Н. Принципы трансплантации костного мозга и стволовых клеток периферической крови. – СПб: Военно/медицинская академия, 2001.
- 18. Connors J.M., Reece D., Diehl V. et al. Hodgkin’s lymphoma: New approaches to treatment // Hematology. –1998. – P. 274–295.
- 19. Hematology: Basic principles and practice. – 3nd ed. / Ed.Hoffman. – New York: Churcill Livingston, 2000. –2584 p.
- 20. Sulivan K.M. Long term follow/up and quality of life after hematopoetic stem cell transplantation // J. Rheumatol.– 1997. – Vol. 48, Suppl. – P. 46–52.
- 21. Knaan-Shanzer S., Houben P., Van Bekkun D. W. Remission induction of adjuvant arthritis in rats by total body irradiation and autologous bone marrow transplantation // Ibid. — 1992. — Vol. 8. — P. 333-338.
- 22.Talaulikar D. Tymms KE. Prosser I. Smith R. Autologus peripheral blood stem cell transplantation with in vivo T-cell depletion for life threatening refractory systemic lupus erythematosus. Lupus.2005;10 (2):159-163.
- 23.Burt R.K. et al. Nonmyeloablative hematopoietic stem cell transplantation for systewmic lupus erythematosus. JAMA. 2006 Feb1;295(5):527-35.
- 24. Dominique Farge, Myriam Labopin, Alan Tyndall, Athanasios Fassas. Autologous hematopoietic stem cell transplantation for autoimmune diseases: an observational study on 12 years’ experience from the European Group for Blood and Marrow Transplantation Working Party on Autoimmune Diseases. Haematologica 2010 95(2)-284-292.
- 25. Laisvyde Statkute. Ann Traynor et al. Аntiphospholipid syndrome in patients with systemic lupus erythematosus treated by autologous hematopoietic stem cell transplantation. Blood.2005.106.8-2700-2709.
- 26. Burt R. et al., Nonmyeloablative Hematopoietic stem cell transplantation for systemic lupus erythematosus. Jama. 2006. 295 (5).527-535.
- 27. Новик А.А. Трансплантация стволовых кроветворных клеток при аутоиммунных заболеваниях // Вестн. Рос. военно/мед. акад. – 2002.– Т. 7,№1. – С.98–102.
- 28. Zhao X., Fu Y., Peng X. Autologous hematopoietic stem cell transplantation in the treatment of systemic lupus erithematosus// Bone Marrow Transplantation. – 2002. – Vol. 29, Suppl. 2. – P.
- 29. Fassas A., Anagnostopoulos A., Kazis A. et al.Peripheral blood stem cell transplantation in the treatment of progressive multiple sclerosis: first results of pilot study // Ibit. — 1997. — Vol. 20. — P. 631-638.
Аутоиммундық аурулары бар науқастарды емдеуде бағаналық қантүзу жасушаларын көшіріп қондырудың келешегі
Жүсүпова А.А., М.Б.Аскаров
Мақала аутоиммундық аурулар кезінде бағаналық қантүзу жасушаларын көшіріп қондырудың рөлін анықтауға арналған. Аутоиммундық аурулар кезінде бағаналық жасушалардың түрі, көшіріп қондыруға көрсеткіштері және атқаратын рөлі қарастырылды. Бұл әдіс қалыпты иммуносупрессиялық емге қосымша ретінде қолдануға болатындылығы көрсетілді.
Prospects of transplantation of hemopoietic stem cells in treating patients with autoimmune diseases
Zhusupova AA, M.B. Askarov
This article analyzes studies on the role of transplantation of hemopoietic stem cells in autoimmune diseases. The role, indications, types of transplantation of hemopoietic stem cells in autoimmune diseases. Concluded that this treatment may be considered addition to the usual immunosuppressive therapy.
Национальный научный медицинский центр, г. Астана
Читайте также:


