Селезенка при инфекционном эндокардите
Аннотация научной статьи по клинической медицине, автор научной работы — Шестакова Анна Васильевна, Кадыралиев Бакытбек Кайыбекович, Литвинов Валерий Викторович
Проблема инфекционного эндокардита по прежнему остается значимой, особенно в связи с отсутствием ранней диагностики самого заболевания и его осложнений, корректной тактики ведения пациентов и своевременного установления показаний к оперативному лечению. Экстракардиальные осложнения ИЭ в большинстве случаев развиваются при длительной неэффективной консервативной терапии и чаще всего проявляются патологией со стороны селезенки . В результате системной септической реакции первой поражается пульпа селезенки , что в дальнейшем приводит к ее гиперплазии и некрозу. Ультразвуковое исследование селезенки , а также эхокардиография относится к скрининговым методам диагностики, использование и анализ которых, помогает подобрать необходимую тактику лечения, выявить показания к оперативному вмешательству и оценить эффективность проводимой терапии с прогнозом течения заболевания. Отсутствие своевременной диагностики осложнений инфекционного эндокардита со стороны селезенки , которая может быть очагом дополнительной инфекции в дальнейшем, способствует как прогрессированию заболевания, так и формированию рецидива эндокардита.
Похожие темы научных работ по клинической медицине , автор научной работы — Шестакова Анна Васильевна, Кадыралиев Бакытбек Кайыбекович, Литвинов Валерий Викторович
Clinical and morphological evaluation of spleen condition in the case of infectious endocarditis
The problem of infectious endocarditis is still significant, especially in the absence of early diagnosis of the disease and its complications, the correct management of patients and timely assessment of indications for surgical treatment. Extracardiac complications of infectious endocarditis in most of the cases develop long-term ineffective conservative therapy and often manifest pathology from the spleen . In the result of a systemic septic reaction is first affected pulp of the spleen , which further leads to its hyperplasia and necrosis. Ultrasound examination of the spleen , as well as echocardiography relates to screening methods for diagnosis, the use and analysis which helps to select the right tactics of treatment, to determine indications for surgical intervention and to evaluate the effectiveness of the therapy with the prognosis of the disease. The lack of timely diagnosis of complications of infective endocarditis from the spleen , which can be a hotbed of further infections in the future, promotes both the progression of the disease, and the formation of recurrent endocarditis.
УДК: 616.411-092:616.127-002-022.6 Код специальности ВАК: 14.01.26
КЛИНИКО-МОРФОЛОГИЧЕСКАЯ ОЦЕНКА СОСТОЯНИЯ СЕЛЕЗЕНКИ ПРИ ИНФЕКЦИОННОМ ЭНДОКАРДИТЕ
А.В. Шестакова, Б.К. Кадыралиев, В.В. Литвинов,
Шестакова Анна Васильевна - e-mail: annashestakova1994@mail.ru
Дата поступления 24.04.2017
Проблема инфекционного эндокардита по прежнему остается значимой, особенно в связи с отсутствием ранней диагностики самого заболевания и его осложнений, корректной тактики ведения пациентов и своевременного установления показаний к оперативному лечению. Экстракардиальные осложнения ИЭ в большинстве случаев развиваются при длительной неэффективной консервативной терапии и чаше всего проявляются патологией со стороны селезенки. В результате системной септической реакции первой поражается пульпа селезенки, что в дальнейшем приводит к ее гиперплазии и некрозу. Ультразвуковое исследование селезенки, а также эхокардиография относятся к скрининговым методам диагностики, использование и анализ которых помогает подобрать необходимую тактику лечения, выявить показания к оперативному вмешательству и оценить эффективность проводимой терапии с прогнозом течения заболевания. Отсутствие своевременной диагностики осложнений инфекционного эндокардита со стороны селезенки, которая может быть очагом дополнительной инфекции в дальнейшем, способствует как прогрессированию заболевания, так и формированию рецидива эндокардита.
Ключевые слова: инфекционный эндокардит, селезенка, морфология, абсцесс.
The problem of infectious endocarditis is still significant, especially in the absence of early diagnosis of the disease and its complications, the correct management of patients and timely assessment of indications for surgical treatment. Extracardiac complications of infectious endocarditis in most of the cases develop long-term ineffective conservative therapy and often manifest pathology from the spleen. In the result of a systemic septic reaction is first affected pulp of the spleen, which further leads to its hyperplasia and necrosis. Ultrasound examination of the spleen, as well as echocardiography relates to screening methods for diagnosis, the use and analysis which helps to select the right tactics of treatment, to determine indications for surgical intervention and to evaluate the effectiveness of the therapy with the prognosis of the disease. The lack of timely diagnosis of complications of infective endocarditis from the spleen, which can be a hotbed of further infections in the future, promotes both the progression of the disease, and the formation of recurrent endocarditis.
Key words: infective endocarditis, the spleen, morphology, abscess.
В настоящее время заболеваемость инфекционным эндокардитом (ИЭ) характеризуется неуклонным ростом, несмотря на широкое применение антибиотиков и хирургическое лечение этого заболевания. Летальность при ИЭ также остается на высоком уровне и составляет от 18 до 36% по данным литературы [1]. За последние несколько лет в изучении патогенеза ИЭ отсутствует существенный прогресс, и, как следствие, предлагаемая патогенетическая терапия в основном находится на стадии дискуссии, а ее практическое применение является клиническим экспериментом [2]. С другой стороны, при диагностике и лечении ИЭ часто не уделяется должного внимания экс-тракардиальным осложнениям [3]. Известно, что одним из наиболее частых экстракардиальных осложнений ИЭ является поражение селезенки. Так, частота спленомега-лии колеблется от 14,8 до 40,7% [4]. Увеличение селезенки связано с гиперплазией ее пульпы в результате системной септической реакции на инфекционно-токсический процесс [5]. Наличие спленомегалии позволяет подтвердить диагноз ИЭ, а также отличить ИЭ от старого ревмати-
ческого порока сердца в сочетании с интеркуррентной инфекцией или повторной ревматической лихорадкой у больных с пороками сердца [6]. При ультразвуковом исследовании (УЗИ) селезенки, кроме оценки размеров органа, выявляются также инфаркты и абсцессы [7]. По данным литературы инфаркт селезенки диагностируется на УЗИ у 16-18% пациентов с размерами от 2,0x1,5 до 9,0x4,0 см [8]. Абсцесс селезенки диагностируют реже - у 1,7-1,9% больных ИЭ, но его наличие оказывает неблагоприятное прогностическое влияние в случае несвоевременной диагностики [9]. Недиагностированный абсцесс селезенки, как очаг хронической инфекции, перед операцией протезирования клапана приводит в последующем к ИЭ искусственного клапана [10].
Цель исследования: оценить клинико-морфологичес-кие изменения селезенки у пациентов с инфекционным эндокардитом.
Материал и методы
возраст пациентов составил 39,3±4,0 года (от 28 до 58 лет). Трое из обследованных пациентов страдали хронической наркотической зависимостью. Всем пациентам были проведены эхокардиография, электрокардиография, а также УЗИ и компьютерная томография органов брюшной полости. Ультразвуковая оценка состояния селезенки учитывала следующие критерии: размеры самого органа, выявление гипоэхогенных, жидкостных или эхогенных образований, оценка их расположения и размеров. Дополнительно были проанализированы результаты патологоанатомиче-ского вскрытия у трех умерших пациентов с ИЭ.
Изменения селезенки при ИЭ, выявленные с помощью УЗИ и КТ
Изменения со стороны селезенки Собственные наблюдения Данные литературы [1]
Спленомегалия 63,6% 53,7%
Инфаркт 36,3% 16,9%
Сочетание инфаркта и абсцесса 18,2% -
Обширный инфаркт селезенки, удаленной во время операции.
Множественные инфаркты селезенки умершей пациентки с инфекционным эндокардитом.
Результаты и их обсуждение
В ходе проведенного исследования было установлено, что при ИЭ практически всегда выявляется не только изменение самого сердца, но и селезенки, проявляющееся ее увеличением, а также инфарктами или абсцессами. По данным УЗИ и компьютерной томографии в предоперационный период изменения селезенки у больных ИЭ были представлены увеличением ее размеров от 12,0x5,0 до 19,0x12,1 см у 63,6% пациентов и наличием инфарктов у 36,3% пациентов (рис. 1). Инфаркт селезенки чаще визуализировался как образование средней/высокой эхоген-ности, неправильной/треугольной формы с основанием, обращенным к капсуле органа. Инфаркты располагались в нижнем сегменте органа, а их размеры варьировали в пределах от 3,0x1,5 до 10,0x4,0 см. При этом следует отметить, что наличия инфарктов в среднем и верхнем отделах органа зафиксировано не было.
Абсцессы селезенки по данным УЗИ и компьютерной томографии были установлены у 72,2% пациентов. Все абсцессы являлись единичными и визуализировались как образование неправильной формы, неоднородной структуры, с прерывистыми/четкими неровными контурами или как жидкостное образование с четкими границами. У 18,2% пациентов отмечалось сочетанное поражение в виде наличия в селезенке и инфаркта, и абсцесса. Все полученные на предоперационном этапе данные были подтверждены во время операции на этапе спленэктомии.
При патологоанатомическом исследовании умерших пациентов во всех случаях было выявлено, что консистенция селезенки была дряблая, с соскобом пульпы на разрезе, а ее масса составляла от 249 до 528 г, что превышало нормальные показатели. В одном случае отмечалось наличие множественных инфарктов селезенки (рис. 2). Данные изменения характеризовали выраженное септическое состояние умерших больных.
При микроскопическом исследовании ткани селезенки во всех случаях отмечалось выраженное полнокровие гемокапилляров красной пульпы, умеренный концентрический фиброз центральных артерий, а также истощение лимфоидной ткани с очагами некроза различных размеров.
Таким образом, при ИЭ с помощью УЗИ, компьютерной томографии, интраоперационного исследования, а также на основании данных патологоанатомического вскрытия выявляются такие патологические процессы в селезенке, как абсцессы, инфаркты, и формирование спленомега-лии. Ультразвуковое исследование селезенки, так же, как и эхокардиография в выявлении вегетаций на клапанах сердца, относится к скрининговым методам диагностики, использование и анализ которых помогает подобрать необходимую тактику лечения, выявить показания к оперативному вмешательству и оценить эффективность проводимой терапии с прогнозом течения заболевания.
1. Виноградова Т.Л. Инфекционный эндокардит: современное течение, вопросы и проблемы. Сердце. 2003. Т. 2. № 5. С. 212-225.
Vinogradova Т±. Infekcionnyj jendokardit■ sovremennoe techenie, voprosy I рюЫету. Зе^се. 2003. Т. 2. № 5. 5. 212-225.
2. Delgado V., Anguita M., Castillo J.C. et al. Early and late outcome of patients with infective endocarditis (1987-2004). Eur. Heart J. 2005. Vol. 26. P. 286
3. Тюрин В.П. Инфекционные эндокардиты: руководство, 2-е издание, доп. и перераб. М.: ГЭОТАР-Медиа, 2013. Сс.110-116, 210-215.
Tjurin V.P. Infekcionnye jendokardity: rukovodstvo, 2-e izdanie, dop. i pererab. M.: GJeOTAR-Media, 2013. Ss.110-116,210-215.
4. Лебединская Е.А., Лебединская О.В., Годовалов А.П., Ахматова Н.К., Мелехин С.В. Морфологические характеристики индуцированной иммуносупрессии // Новые задачи современной медицины: мат-лы Междунар. науч. конф. 2012. С. 63-67.
Lebedinskaja E.A., Lebedinskaja O.V, GodovalovA.P, AhmatovaN.K., Melehin S.V. Morfologicheskie harakteristiki inducirovannoj immunosupressii // Novye zadachi sovremennoj mediciny: Mat-ly Mezhdunar. nauch. konf. 2012. S. 63-67.
5. Шевченко Ю.Л. Хирургическое лечение инфекционного эндокардита. СПб.: Наука, 1995. 230 с.
Shevchenko Ju.L. Hirurgicheskoe lechenie infekcionnogo jendokardita. SPb.: Nauka, 1995. 230 s.
6. Категория: руководство и клинические рекомендации // Европейское общество кардиологов-2015. Рекомендации ESC по ведению больных с инфекционным эндокардитом. Сс. 98, 107.
Kategorija: rukovodstvo i klinicheskie rekomendacii // Evropejskoe obshhestvo Kardiologov-2015. Rekomendacii ESC po vedeniju bol'nyh s infekcionnym jendokarditom. Ss. 98, 107.
7. Бадыков И.И., Шестакова А.В., Годовалов А.П., Кадыралиев Б.К. Оценка интегральных показателей эндогенной интоксикации и фагоцитарной активности лейкоцитов периферической крови пациентов с инфекционным эндокардитом. Медицинский академический журнал. 2016. Т. 16. № 4. С. 146-147.
Badykov I.I., Shestakova A.V., Godovalov A.P., Kadyraliev B.K. Ocenka integral'nyh pokazatelej jendogennoj intoksikacii i fagocitarnoj aktivnosti lejkocitov perifericheskoj krovi pacientov s infekcionnym jendokarditom. Medicinskij akademicheskij zhurnal. 2016. T. 16. № 4. S. 146-147.
8. Habib G., Hoen B., Tornos P. et al. Guedelines on the prevention. Diagnosis, and treatment of infective endocarditis, The Task Forsce of the European Society of Cardiology. Eur. Heart J. 2009. Vol. 30. P. 2375-2409.
9. Heiro M. Nikoskelainen J. Engblom E. et al. Neurologic manifestations of infective endocarditis: A 17-year experience in a teaching hospital in Finland. Arch. Intern. Med. 2000. Vol. 160. P. 2781-2787.
10. Шестакова А.В., Кадыралиев Б.К., Годовалов А.П., Быкова Л.П. Опсонизация Сandida albicans иммуноглобулином для внутривенного введения. Медицинская иммунология. 2015. Т. 17. № 5. С. 434.
Shestakova A.V., Kadyraliev B.K., Godovalov A.P., Bykova L.P. Opsonizacija Sandida albicans immunoglobulinom dlja vnutrivennogo vvedenija. Medicinskaja immunologija. 2015. T. 17. № 5. S. 434. гулн
УДК: 616.126.3-002-089:616.9 Код специальности ВАК: 14.01.26
СОВРЕМЕННЫЙ ПОДХОД К ХИРУРГИЧЕСКОМУ ЛЕЧЕНИЮ ИНФЕКЦИОННОГО ЭНДОКАРДИТА ТРИКУСПИДАЛЬНОГО КЛАПАНА
С.А. Журко1, С.А. Федоров2, В.А. Чигинев12, А.П. Медведев2, В.В. Пичугин2, Д.И. Лашманов1, О.Р. Широкова1, Д.Д. Жильцов2, Л.М. Целоусова2,
Федоров Сергей Андреевич - e-mail: SergFedorov1991@yandex.ru
Дата поступления 27.06.2017
Заболеваемость инфекционным эндокардитом (ИЭ) по данным различных авторов колеблется в пределах 3-10 случаев на 100 000 человек в год, при этом в 10-15% поражаются правые отделы сердца. Основным методом лечения стал хирургический, основными принципами которого являются: удаление очага инфекции и нормализация внутрисердечной гемодинамики. С октября 2003 по май 2017 года на базе II кардиохирургического отделения Специализированной кардиохирургической больницы Нижнего Новгорода изолированная коррекция трикуспидального клапана (ТК) выполнена 75 пациентам. В зависимости от выбранного метода коррекции порока было выделено три группы пациентов. В I группу вошли пять человек, которым порок ТК был коррегирован путем имлантации механических клапанов сердца (МКС). 45 пациентам lI группы для коррекции порока использовались различные модели биологических клапанов сердца (БКС). 13 пациентам, несмотря на значительное разрушение створок, удалось выполнить клапаносохраняюшую операцию. Пластические операции на ТК в сравнении с протезированием ТК различными моделями искусственного клапана сердца (ИКС) имеют существенное преимушество, при невозможности реконструктивных вмешательств методом выбора является имплантация БКС.
Ключевые слова: инфекционный эндокардит, протезирование трикуспидального клапана, пластические операции на трикуспидальном клапане, биологические протезы, параллельная перфузия.
Key words: infective endocarditis, prosthetic tricuspid valve, plastic operations on the tricuspid valve, biological valve, parallel perfusion.

Инфекционный эндокардит (ИЭ) – грозное заболевание, характеризующееся крайне неблагоприятным прогнозом при естественном его течении. Анализируя литературные данные, можно отметить, что частота ИЭ в Российской Федерации имеет сравнительно высокие показатели распространенности по отношению к другим странам; так, в расчете на 1 млн населения заболеваемость ИЭ составляет: в США 38-92,9 человека, в Канаде – 20-25, в Швеции – 59, Англии – 23-25, Франции – 18-23, Германии и Италии – 16. В России заболеваемость ИЭ достигает 46,3 человека на 1 млн населения [1]. Особую активность проблема данного заболевания приобретает в связи с неуклонным ростом ИЭ интактных клапанов в течение последних десятилетий на фоне общего роста заболеваемости инфекционным эндокардитом в 3-4 раза 3.
Диагностика ИЭ представляет значительные затруднения в связи с ярко выраженным полиморфизмом клиники, широким спектром возбудителей и ростом доли полимикробной инфекции в генезе ИЭ [5]. На ранних этапах заболевание не имеет специфических диагностических признаков. Так, клиническая картина подострого ИЭ характеризуется преобладанием и нарастанием общей астеновегетативной симптоматики на фоне лихорадки и в некоторых случаях миалгии, а острая форма инфекционного эндокардита может манифестировать уже с осложнений в виде отрыва вегетаций и эмболии органов. Результаты лабораторной диагностики также не позволяют врачу-клиницисту заподозрить данное заболевание, так как у пациента будут отмечаться анемия, лейкоцитоз и ускорение скорости оседания эритроцитов (СОЭ), в общем анализе мочи может быть микрогематурия и протеинурия [6; 7]. Доказана чувствительность С-реактивного белка (СРБ) при диагностике ИЭ, но данный воспалительный маркер специфичен для целого ряда воспалительных заболеваний [8].
Даже несмотря на технические достижения современной медицины, постановка диагноза ИЭ во многих случаях значительно растягивается во времени, что, вероятно, связано с небольшим числом работ, описывающих клинико-эпидемиологические характеристики инфекционного эндокардита на современном этапе [9].
Целью нашей работы явилось изучение структуры заболеваемости, основных особенностей клинической и лабораторно-инструментальной картины, вариантов поражения клапанного аппарата, а также осложнений ИЭ.
Результаты и их обсуждение. За исследуемый период времени наблюдается увеличение числа пациентов с ИЭ (рис. 1), что хорошо согласуется с данными общемировой статистики [1].
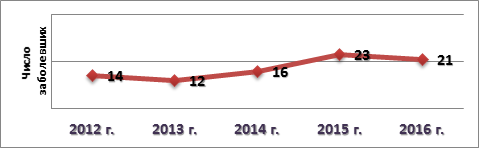
Рис. 1. Случаи выявления ИЭ в период за 2012-2016 гг.
Анализ половой структуры заболеваемости показывает, что мужчины болеют в 3 раза чаще, чем женщины (Z=2,137880, p-level=0,032527), составляя при этом 64% от общего числа.
Результаты анализа возрастной структуры ИЭ позволяют утверждать, что большинство страдающих инфекционным эндокардитом пациентов - это больные молодого и среднего возраста, при этом отмечается отчетливая тенденция к увеличению абсолютного числа пациентов молодого и среднего возраста среди всех пациентов с ИЭ (рис. 2, 3).
Далее нами были проанализированы особенности течения ИЭ по клиническим вариантам: острая форма наблюдалась лишь в 7 клинических случаях (8,14%), подострая – у 91,86% пациентов с ИЭ.
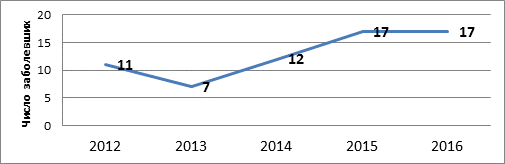
Рис. 2. Динамика заболеваемости ИЭ пациентов молодого и среднего возраста
в период с 2012 по 2016 г.
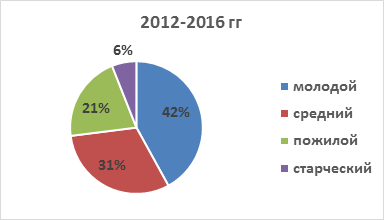
Рис. 3. Возрастная структура пациентов с ИЭ
Анализ поражений клапанного аппарата выявил следующие морфологические варианты инфекционного эндокардита: первичный ИЭ естественных клапанов – 66,27%, вторичный ИЭ естественных клапанов – 15,12%, ранний ИЭ протеза клапанов – 11,63% и поздний ИЭ протеза клапанов в 6,98% случаев.
Среди случаев ИЭ естественных клапанов преобладает эндокардит левых отделов – 65,11%. Сочетанное поражение трикуспидального клапана (ТК) и митрального клапана (МК) наблюдалось в 4,65% случаев в результате сообщения правой и левой полостей сердца вследствие образования абсцессов. Эндокардит правых отделов сердца был выявлен у 33,24% пациентов.
Анализируя случаи эндокардита правых отделов сердца, можно отметить неуклонный рост числа больных с данным видом поражения клапанного аппарата в период с 2013 по 2016 год (рис. 4).
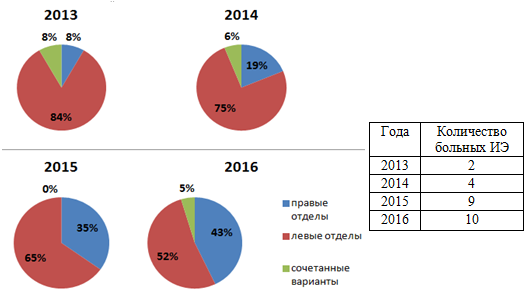
Рис. 4. Рост абсолютного числа больных с эндокардитом правых отделов сердца
Среди наиболее распространенных осложнений ИЭ у пациентов с эндокардитом правых отделов сердца можно отметить: пневмонию, экссудативный перикардит, абсцесс легкого, асцит, гидроторакс, нефритический синдром с явлениями почечной недостаточности.
При этом тяжелая почечная недостаточность с максимальным повышением креатинина до 671 мкмоль/л отмечалась лишь у пациентов с поражением митрального и аортального клапанов.
Среди эндокардита левых отделов характерны осложнения в виде левожелудочковой сердечной недостаточности, нефритического синдрома с развитием почечной недостаточности, экссудативного перикардита, гидроторакса.
Анемия была типичным осложнением как при поражении правых, так и левых отделов, встречаясь в 16,3% случаев.
Эмболические осложнения наблюдались у 8 пациентов, что составило 9% от общего числа. При ИЭ левых отделов сердца у больных развился эмболический инфаркт селезенки в одном случае, а в другом – эмболизация сосудов головного мозга, почек и сердца. При поражении трикуспидального и легочного клапанов в 6 случаях (7% от общего количества больных ИЭ) закономерно развилась тромбоэмболия мелких ветвей легочной артерии.
Проанализировав клиническую симптоматику, можно выявить следующие ведущие симптомы инфекционного эндокардита: одышка в 73% случаев, лихорадка – 72%, астения – 64%, отеки нижних конечностей – 31%, кардиалгия – 30%, миалгия – 10%.
Изучив результаты диагностических методов выявления ИЭ, можно отметить низкую выявляемость положительной гемокультуры среди всех пациентов вне зависимости от формы, сроков возникновения, половозрастной группы (таблица). Положительная гемокультура встречалась только у 23% больных от общего числа, что, вероятно, свидетельствует как о необходимости совершенствования лабораторной диагностики сепсиса, так и о высокой распространенности назначения антибактериальной терапии до проведения бактериологического посева крови.
Структура бактериологически подтвержденных возбудителей ИЭ
*Enterococcus faecium, Klebsiella pneumoniae, Stenotrophomonas maltophilia
Варианты положительной гемокультуры
Анализируя данные лабораторной диагностики, отмечаем повышение СОЭ свыше 20 мм/ч у 57 больных – 67% от общего количества больных, и свыше 40 мм/ч в 27% случаев. Вместе с тем 21% больных имели уровень СОЭ в пределах нормальных значений. В работе [5] Тюрина В.П. и Гогина Е.Е. в качестве одного из патогномоничных симптомов отмечено ускорение СОЭ в 97% случаев у пациентов с ИЭ, что противоречит полученным нами данным. Таким образом, ИЭ не всегда сопровождается увеличением СОЭ (рис. 5).
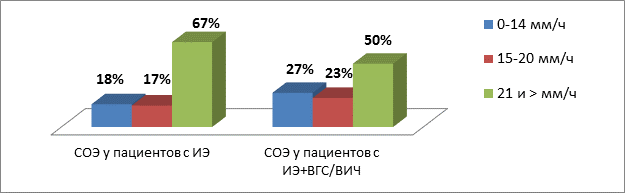
Рис. 5. Показатели СОЭ у пациентов с ИЭ
Примечание к рисунку: СОЭ – скорость оседания эритроцитов, ИЭ – инфекционный эндокардит, ВГС – вирус гепатита С, ВИЧ – вирус иммунодефицита человека
Среднее значение СРБ среди всех пациентов составило 47,99 ±10,49 мг/л. СРБ оставался в пределах нормальных значений (за норму принимали диапазон от 0 до 5 мг/л) у 17,65% пациентов, для большинства пациентов характерно повышение СРБ свыше 10 и более мг/л (76,47%). Подавляющее большинство больных имели значение СРБ свыше 30 мг/л.
Наличие нормальных значений СРБ при ИЭ, очевидно, свидетельствует о крайне низкой реактивности организма. Среди всех пациентов с нормальными значениями СРБ нам встретился лишь 1 пациент в возрасте 46 лет с ИЭ левых отделов сердца. При этом нормальные значения СРБ наблюдались у двух пациентов старческого возраста и 3 больных с ИЭ правых отделов сердца. В первом случае низкая реактивность обусловлена снижением иммунного ответа, связанным с возрастом. Во втором случае – нормальные значения СРБ обусловлены угнетением иммунитета, вероятнее всего, вследствие внутривенной наркомании, определенный вклад в снижение реактивности иммунитета, несомненно, вносит вирусный гепатит С (ВГС). Два из трех пациентов с эндокардитом правых отделов сердца, имевших нормальный уровень СРБ, страдали вирусным гепатитом С.
В целом проанализировать вклад вирусного гепатита С и ВИЧ в ареактивность пациентов с ИЭ практически невозможно, так как значения СРБ у таких больных варьируют в крайне широком диапазоне: от нормальных до крайне экстремальных значений (166, 177 и даже 298 мг/л). Однако при анализе значения СОЭ у пациентов с ИЭ выявляется отчетливая тенденция к более низким значениям СОЭ (рис. 5) у пациентов, страдающих ВГС/ВИЧ, приближающаяся к статистической достоверности (Z=1,676; P=0,09). Вышеописанные изменения СОЭ, вероятно, подтверждают мысль о роли ВГС и ВИЧ в снижении иммунной реактивности организма пациентов с ИЭ.
Необходимо отметить, что в исследовании ряда авторов под руководством Hogevik H., Olaison L. было также установлено, что СОЭ является менее чувствительным показателем по отношению к СРБ, так как нормальные значения СОЭ наблюдались в 28% случаев, в то время когда уровень СРБ был в норме лишь у 4%. В работе также отмечено, что ИЭ стафилококкового происхождения с коротким периодом клинической симптоматики коррелируют с более высокими уровнями СРБ [8].
Таким образом, полученные результаты позволяют отметить, что наблюдающийся рост заболеваемости ИЭ в период за 2012-2016 годы связан с увеличением поражения числа лиц молодого и среднего возраста.
Значительная доля и увеличение числа больных с поражением правых отделов сердца свидетельствуют о том, что вышеуказанные изменения заболеваемости связаны с вероятным распространением внутривенной наркомании.
Таким образом, к 2015-2016 году сформировалось характерное клиническое лицо пациента с ИЭ: молодой больной, чаще мужского пола, с длительным лихорадочным синдромом, проявлениями общей интоксикации, симптомами правожелудочковой сердечной недостаточности в сочетании с инфаркт-пневмонией легкого или деструктивными поражениями легочной ткани.
Согласно анамнестическим данным, проведение посевов крови в большинстве случаев предшествовало проведению антибиотикотерапии, что закономерно привело к значительному снижению лиц с положительной гемокультурой. Выявлен крайне низкий процент высевания микроорганизмов возбудителей ИЭ. Полученные данные убедительно свидетельствуют о первостепенности клинической и инструментальной диагностики (ЭхоКГ, ЧПЭхоКГ). Методы бактериальной диагностики в большинстве случаев имеют вторичное значение в подтверждении диагноза, но играют определяющую роль при выборе антибиотикотерапии в случае выявления положительной гемокультуры у пациента. Отсутствие воспалительной активности в анализах крови при яркой клинической картине ИЭ и положительного результата посева гемокультуры не должно вводить в заблуждение лечащего врача.
Неврологические осложнения инфекционного эндокардита
Шевченко Ю.Л., Кузнецов А.Н., Тюрин В.П. Национальный медико-хирургический центр имени Н.И.Пирогова, Москва
Ни одно заболевание сердца не может сравниться с инфекционным эндокардитом по частоте, разнообразию и тяжести неврологических осложнений. Не случайно, что более ста лет назад Ослер описал инфекционный эндокардит как триаду, состоящую из лихорадки, сердечного шума и гемиплегии [1]. Инфекционный эндокардит является чрезвычайно тяжелым заболеванием с летальностью, достигающей при консервативном лечении 80% (общая летальность составляет [2, 3]. В настоящее время инфекционный эндокардит вышел на четвертое место по уровню смертности среди инфекционных синдромов после уросепсиса, пневмонии и перитонита и занял нишу социально обусловленных заболеваний [4]. Несмотря на успехи в диагностике и лечении инфекционного эндокардита частота неврологических осложнений заболевания остается в последние три десятилетия на уровне (по нашим данным — около 25%) [5, 6, 7, 8, 9, 10, 11]. Присоединение неврологических осложнений значительно увеличивает летальность. При мозговой эмболии на фоне инфекционного эндокардита она колеблется между 20% и 80% (по нашим данным — около 60%), а в доантибиотическую эру она составляла 100% [5, 11, 12, 13, 14]. Основными этиопатогенетическими факторами при инфекционном эндокардите являются: травма эндокарда, бактериемия и ослабление резистентности организма. Спектр наиболее частых возбудителей и предрасполагающих кардиальных повреждений к настоящему времени претерпел некоторые изменения. Ревматическое заболевание сердца было одним из наиболее распространенных заболеваний сердца, предрасполагающих к эндокардиту (вторичный инфекционный эндокардит), но сейчас чаще развивается первичный инфекционный эндокардит, то есть поражение условно неизмененных клапанов сердца. Вместе с изменениями предрасполагающих условий изменились и возбудители эндокардита. Наиболее частыми остаются стрептококки и стафилококки, однако, частота стрептококковой этиологии снижается, а стафилококковой — растет, кроме того, в последние годы продолжает расти доля энтерококка, а также грамотрицательной флоры, микоплазм, вирусов, грибов, риккетсий, вероятно, вследствие иммуносупрессии, изменения клапанного субстрата и использования антимикробных средств. Неврологические осложнения у больных инфекционным эндокардитом чаще развиваются при поражении золотистым стафилококком [3, 11, 12, 15, 16]. Характерный патологический признак инфекционного эндокардита — это наличие вегетаций на створках клапанов. Вегетации состоят из аморфного фибрина и тромбоцитов вместе с возбудителями и лейкоцитами, являясь, таким образом, инфицированными белыми фибрин-тромбоцитарными тромбами. Возбудители, как правило, локализуются глубоко внутри вегетации и, таким образом, надежно защищены от антибактериальных факторов крови. Для обнаружения вегетаций используют эхокардиографию. Трансэзофагеальная эхокардиография значительно превосходит трансторакальное исследование — чувствительность достигает специфичность — [3]. У обследованных нами пациентов вегетации имели существенные различия: по размеру — от очень мелких до массивных (24 мм); по форме — шаровидные, булавовидные, лентовидные, дольчатые; по характеру прикрепления к клапану — на узком основании, на широком основании; по подвижности — флотирующие, фиксированные; по структуре — рыхлые, организованные. Очень важной является последняя характеристика, поскольку она отражает активность инфекционного процесса в сердце и эмбологенный потенциал вегетаций. Шестидесятиминутный транскраниальный допплеровский мониторинг кровотока по средней мозговой артерии позволяет детектировать микроэмболические сигналы (МЭС) у больных инфекционным эндокардитом. В нашем исследовании все пациенты с МЭС имели свежий инфекционный эндокардит (давность не более 2 месяцев) и рыхлые вегетации по данным эхокардиографии. При давности эндокардита более 2 месяцев МЭС не обнаруживались. Появление МЭС связано с пассажем мелких фрагментов рыхлых клапанный вегетаций, а также агрегатов тромбоцитов, образующихся в турбулентном потоке вблизи пораженного клапана. Неврологические осложнения наиболее часто возникают до начала антибактериальной терапии и в первую неделю ее проведения. В подавляющем большинстве случаев церебральная эмболия развивается в течение первого месяца от момента появления симптомов эндокардита. В этот период вегетации являются рыхлыми и могут легко фрагментироваться, вызывая эмболизацию. Затем в процессе адекватной антибактериальной терапии происходит уплотнение вегетаций. По данным эхокардиографии, выполненной в динамике, вегетации становятся плотными и прочными, они организуются, покрываются эндотелием и уже реже вызывают эмболии. Неврологические осложнения инфекционного эндокардита связаны с количеством, размером, локализацией и инфицированностью эмболов. Пациенты с инфекционным эндокардитом могут переносить инфаркт головного мозга, интрацеребральную и субарахноидальную геморрагию, микотическую аневризму, энцефалопатию, внутримозговой абсцесс, менингит и менингоэнцефалит. Ишемический инсульт является наиболее частой неврологической манифестацией инфекционного эндокардита (по данным литературы — у пациентов с инфекционным эндокардитом, по нашим данным — у 20%). Методы нейровизуализации демонстрируют в большинстве случаев множественные ишемические очаги, из которых примерно половина — корковые, локализующиеся в бассейнах концевых ветвей мозговых артерий, а другая половина представляет собой лакунарные очаги, располагающиеся в глубине полушарий мозга на границе серого и белого вещества. При небольших размерах очагов течение инсульта является достаточно доброкачественным. МРТ является более информативным методом исследования, чем КТ, в выявлении очагового поражения головного мозга у больных инфекционным эндокардитом. Наиболее часто поражается бассейн левой средней мозговой артерии. Церебральная геморрагия имеет место приблизительно у пациентов с инфекционным эндокардитом (по нашим данным — у 5%), чаще при поражении Staphylococcus aureus, и происходит вследствие трех отдельных патофизиологических механизмов. Церебральная септическая эмболия с последующим эрозивным артериитом является причиной и ранней геморрагии, и образования микотических аневризм с их последующим разрывом. Геморрагическая трансформация ишемического инфаркта дополняет данную триаду. Экспериментальные исследования церебральной септической эмболии документируют появление септического артериита в течение 1 дня после эмболии. Считается, что сосудистая деструкция возникает вследствие проникновения микроорганизмов из просвета сосуда в пространства Вирхова-Робена через vasa vasorum окклюзированного сосудистого сегмента. Микроорганизмы затем проникают в адвентицию сосуда, разрушая более медиальные слои до тех пор, пока не достигнут внутренней эластической пластинки. Микотические аневризмы по данным литературы имеют место у 5%-12% пациентов с эндокардитом (по нашим данным — около 1%). Примерно половина микотических аневризм разрывается с развитием интрацеребральной геморрагии или субарахноидального кровоизлияния. Иногда разрыв аневризм происходит спустя месяцы после излечения эндокардита. Летальность при разрыве достигает 80%. У 30% больных при антибиотикотерапии аневризмы подвергаются обратному развитию, а также менее вероятен разрыв аневризмы. Острая энцефалопатия — второе по частоте неврологическое осложнение эндокардита (по данным литературы и нашим данным ее переносят около 20% пациентов с инфекционным эндокардитом). Патофизиологическими механизмами являются мультифокальная септическая микроэмболия с последующим образованием микроинфарктов и микроабсцессов, изменения интракраниальных артерий (периваскулярная пролиферация), мозговая дисциркуляция и интоксикация. Аутопсические исследования пациентов с неврологическими осложнениями эндокардита показывают множественные микроинфаркты у 23%, микроабсцессы — у 26%. Большие абсцессы головного мозга редки. Они имеют место менее чем в 1% случаев при эндокардите. Менингит и менингоэнцефалит развиваются примерно у 4% пациентов с инфекционным эндокардитом, являются, как правило, дебютом заболевания, и поражение клапанов сердца выявляется уже после постановки неврологического диагноза. Таким образом, неврологические осложнения при инфекционном эндокардите представляют собой довольно пеструю картину. Инфекционный эндокардит до сегодняшнего дня остается одним из наиболее трудно диагностируемых заболеваний, несмотря на хорошо известные клинические и лабораторные признаки. Особенно затруднена постановка правильного диагноза в случае дебюта заболевания неврологическими осложнениями. По нашим данным примерно у 10% больных инфекционный эндокардит дебютировал развитием неврологических осложнений в виде ишемического, геморрагического инсультов или субарахноидального кровоизлияния. В этом случае имеются некоторые отличительные особенности течения неврологической патологии, которые позволяют заподозрить инфекционный эндокардит в качестве причинного фактора.
- Начало развития неврологической симптоматики является острым, с захватом нескольких бассейнов кровоснабжения головного мозга. Очаговые симптомы поражения нервной системы часто не достигают выраженной степени. Более часто, чем при инсультах иного генеза, встречается общемозговая симптоматика (головная боль, оглушение и др.).
- При нейровизуализации выявляются множественные инфаркты мозга.
- Часто наблюдается повышение температуры тела еще до развития симптомов поражения нервной системы.
- При лабораторных исследованиях выявляется: снижение уровня гемоглобина, снижение количества эритроцитов, лейкоцитоз, увеличение СОЭ.
- При УЗИ часто обнаруживается увеличение селезенки.
- При эхокардиографии выявляются клапанные вегетации.
Читайте также:


