Профилактика инфекций дыхательных путей у детей
В последнее время отмечается активное включение иммуномодуляторов со свойствами вакцин в лечение детей с патологией ЛОР-органов
В последнее десятилетие устойчиво сохраняется тенденция к росту числа часто и длительно болеющих детей. На сегодня выявлены следующие особенности данной патологии:
- заболеванию подвержены дети младшего возраста (3-5 лет);
- начало связано, как правило, с вирусной инфекцией, течение которой часто осложняется бактериальной инфекцией ЛОР-органов (отитами, синуситами, тонзиллофарингитами);
- характерно длительное рецидивирующее течение;
- недостаточная эффективность традиционных видов консервативной терапии (включая антибактериальную);
- раннее формирование хронических форм заболеваний ЛОР-органов.
С другой стороны, в детских дошкольных учреждениях создаются благоприятные условия для массивного инфицирования верхних дыхательных путей, в первую очередь лимфоглоточного кольца, условно-патогенной флорой, что вызывает чрезмерное напряжение иммунной системы, ведущее к ее истощению.
Дети с иммунологической недостаточностью составляют группу повышенного риска при острых респираторных заболеваниях, так как особенно тяжело болеют, многократно получают самые разнообразные антибиотики, однако заметного снижения заболеваемости, в первую очередь связанной с бактериальными возбудителями, у них не отмечается. Обусловлено это в числе прочего и ростом резистентности основных возбудителей инфекций верхних дыхательных путей даже к относительно новым антибактериальным препаратам, усилением роли условно-патогенной микробной флоры, внутриклеточных возбудителей в этиологии данных заболеваний у детей. При обследовании посещающих детские дошкольные учреждения детей в возрасте 4-6 лет, 24% из которых, по нашим данным, можно отнести к часто болеющим (67% имеют хроническую патологию ЛОР-органов), были выявлены следующие закономерности: в микробиоценозе миндалин и носоглотки преобладали стафилококки (77,9%), из них золотистый стафилококк высевался в 61,7% случаев, стрептококк высевался в 16,2% (Strept. pyogenus — в 8,8%); Corinebacter (flaver, xerosis, renale, minitiss, psevdotuberculosis) — в 10,3%; Candida albicans — в 11,8%. Рост монокультуры обнаружился в 60,3% случаев, в 16,1% высевались две культуры бактерий. В подавляющем большинстве случаев Сandida albicans обнаруживалась в сочетании с бактериальной флорой (чаще в ассоциации со стафилококком). В 86% посевов степень обсемененности высокая. Роста бактерий не обнаружено в 8,7% случаев.
Штаммы стафилококка были чувствительны: к рифампицину в 88,7% случаев, к кефзолу в 73,6%, к азитромицину в 69,8%, к ципрофлоксацину в 64,1%, к доксициклину в 62,3%; обладали устойчивостью: к бисептолу в 83%, к ванкомицину в 75,5%, к пенициллину в 69,8%, к клиндамицину в 56,6%, к цефтазидиму в 52,8%. Штаммы стрептококка обладали чувствительностью: к пенициллину в 63,6%, к рифампицину в 62%, к азитромицину в 45,5% случаев. Стрептококк показал устойчивость к клиндамицину в 63,8%, к ванкомицину, бисептолу, цефтазидиму, ципрофлоксацину, доксициклину в 45-46% случаев.
Данные результаты заставили медиков обратить пристальное внимание на вакцины против ведущих патогенов верхних дыхательных путей — Hemophilis influenza, Str. pneumonia, с которыми связывают и развитие внутричерепных, орбитальных осложнений, септических процессов. Достижения в области иммунологии обусловили активное включение бактериальных иммуномодуляторов со свойствами вакцин в процесс лечения больных с разнообразной патологией ЛОР-органов.
Комплексная иммунотерапия у детей может осуществляться несколькими способами: 1) активная иммунизация, 2) пассивная, заместительная иммунотерапия, 3) иммунотерапия растительными препаратами и др.
Среди средств активной иммунизации в середине 80-х годов использовалось парентеральное введение нативного анатоксина, антифагина, стрептостафилококковой, синегнойной вакцины.
В настоящее время особый интерес представляет возможность введения иммунокорригирующих препаратов более простыми и удобными для пациента и его родителей способами — капли, свечи и пр. Стоит обратить внимание на препарат ИРС 19, выпускаемый в виде спрея для интраназального применения.
Нами проведено исследование, в ходе которого оценивался лечебный и профилактический эффект препарата ИРС 19 (амбулаторно и в условиях стационара).
В амбулаторных условиях препарат ИРС 19 применялся у 20 детей с острыми синуситами (катаральными — 15, гнойными — 5). Все пациенты относились к категории часто болеющих и состояли на учете у ЛОР-врача с патологией лимфоглоточного кольца (гипертрофия аденоидных вегетаций, небных миндалин различной степени выраженности); у 50% их них заболевание, а следовательно, и прием ИРС 19, совпали с началом посещения массовых детских учреждений.
Средний возраст детей — 5 лет 3 мес. (от 1 года до 13 лет). Из них 9 мальчиков (45%) и 11 девочек (55%).
Препарат включали в базовую схему лечения основного заболевания: по одному впрыскиванию в обе ноздри 1-2 раза в день.
Эффективность действия оценивалась по срокам нормализации риноскопической картины, а также по результатам следующих анализов:
- оценка иммунологического статуса (определение иммуноглобулинов слюны, а в ряде случаев и носового секрета);
- посев отделяемого из носа и зева на флору и чувствительность к антибиотикам
- анализ крови клинический
- анализ мочи общий
- рентгеновский снимок придаточных пазух носа (ППН), в ряде случаев — УЗИ ППН.
Средние значения иммуноглобулинов слюны детей до и после приема препарата представлены в табл. 1.
Результаты микробиологического исследования показали, что в 45% случаев патогенной микрофлоры в отделяемом из носа высеяно не было; у 55% определялась патогенная микрофлора (Staph. aureus — 85%, Str. viridens — 15%). После курса лечения непатогенная микрофлора определялась в 55% случаев, в 45% случаев штамм остался тот же, уменьшилась степень обсемененности.
В условиях стационара ИРС 19 применялся у 35 детей с острыми синуситами. Средний возраст больных 10,6 лет (от 7 до 14 лет). Среди них — 20 мальчиков (57%) и 15 девочек (43%). В зависимости от формы воспаления была выделена группа с катаральными синуситами (I группа) — 13 детей (37%) и гнойными синуситами (II группа) — 22 (63%). Оценка эффективности препарата проводилась по динамике общего состояния, риноскопической картине, данным пункции верхнечелюстных пазух, результатам клинических анализов крови, по срокам выздоровления (по сравнению с контрольной группой). По окончании исследования было отмечено, что у детей, получавших препарат ИРС 19, сократилось время болезни по сравнению с контрольной группой: на три-пять дней раньше наступало выздоровление (оценивали по данным ЛОР-осмотра и результатам пункций гайморовых пазух), уменьшилось среднее количество пункций верхнечелюстных пазух, повысился процент выздоровления по отношению к улучшению течения заболевания (рис. 1).
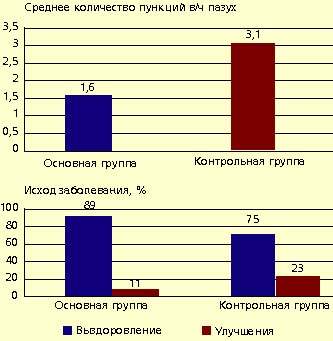 |
| Рисунок 1. Показатели эффективности препарата ИРС 19 у больных с острыми синуситами |
Результаты микробиологического исследования полости носа у больных с острыми синуситами основной и контрольной групп представлены в табл. 2.
Оценивая профилактические возможности препарата ИРС 19 в группе детей с рецидивирующей инфекцией верхних дыхательных путей, мы проанализировали среднюю продолжительность периода обострения, среднюю частоту обострения, интенсивность применения сосудосуживающих и антигистаминных средств после трехнедельного приема препарата, сравнив соответствующие результаты у тех же самых детей за аналогичный период предыдущего (1999) года. В качестве контрольных показателей служили данные о заболеваемости часто болеющих детей, не получавших препарат ИРС 19 за текущий и предыдущий сезоны.
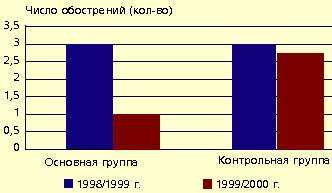 |
| Рисунок 2. Динамика средней частоты обострений инфекций верхних дыхательных путей в основной и контрольной группах |
Рис. 2 и 3 показывают динамику средней частоты и длительности обострений инфекций верхних дыхательных путей. Отмечено также существенное снижение потребности в сосудосуживающих и антигистаминных средствах (соответственно в 5 и 9 раз).
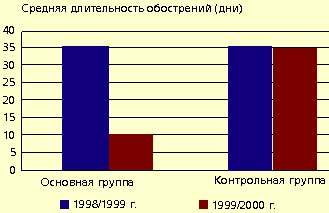 |
| Рисунок 3. Динамика средней длительности обострений инфекций верхних дыхательных путей в основной и контрольной группах |
Говоря о переносимости препарата, хочется отметить практически стопроцентное отсутствие побочных эффектов. Детям младшего возраста рекомендуется индивидуальный подбор дозы, чтобы избежать возможного повышения отделяемого из носовых ходов, приступов чихания после приема препарата. После индивидуального подбора дозы препарата никаких побочных эффектов от приема препарата не отмечено.
Обобщая вышеизложенное, отметим, что ИРС 19 имеет выраженный лечебный и профилактический эффект и очень хорошо переносится. Это позволяет рекомендовать его к более широкому использованию в амбулаторных условиях (детские поликлиники) для профилактики сезонной заболеваемости, а также включать в план лечения острых синуситов, затяжных ринитов для профилактики развития осложнений и для скорейшего выздоровления.
Заболевания органов дыхания традиционно являются одними из наиболее массовых: их доля в общей заболеваемости составляет до 53%.
Дыхание – это жизнь. Когда работа органов дыхания нарушается, жизнь как будто замирает, и начинается борьба с болезнью.

Заболевания органов дыхания традиционно являются одними из наиболее массовых: их доля в общей заболеваемости составляет до 53%. Грозная разновидность злокачественных новообразований – рак легких – в подавляющем большинстве случаев (в 90% в развитых странах) связан с курением; его жертвами в прошлом году в нашей стране стали более 3 тысяч людей. Впрочем, общая заболеваемость этой системы органов в нашей стране впечатляет еще больше: до 60% населения в прошлом году страдали от различных болезней органов дыхания. Кроме того, заболевания дыхания коварны: например, пневмония занимает первое место в списке причин смерти от инфекционных заболеваний и шестое – в списке всех причин летальных исходов. Поэтому так важна и своевременная диагностика, и грамотное лечение, и, конечно, профилактика заболеваний дыхательной системы.
Среди болезней, поражающих органы дыхания, есть инфекционные, аллергические, воспалительные. К инфекционным относятся грипп, туберкулез, дифтерия, пневмония и др.; к аллергическим — бронхиальная астма, к воспалительным — трахеит, бронхит, плеврит, которые могут возникнуть при неблагоприятных условиях: переохлаждении, действии сухого воздуха, дыма, различных химических веществ или, как следствие, после инфекционных заболеваний.
ФАКТОРЫ РИСКА
Факторы риска также можно разделить на две разновидности в соответствии с эффективностью их устранения: неустранимые и устранимые.
Неустранимые факторы риска – это данность, то, с чем нужно считаться, то, что вы не можете изменить.
Устранимые факторы риска – это, напротив, то, что вы можете изменить, приняв соответствующие меры или внеся коррективы в свой образ жизни.
НЕУСТРАНИМЫЕ:
• Наследственность . Некоторые заболевания дыхательной системы обусловлены наследственным фактором. К таким болезням относится, например, бронхиальная астма.
УСТРАНИМЫЕ:
• Курение . Причем как активное, так и пассивное. У курящих людей риск возникновения хронической обструктивной болезни легких превышает 80-90%; все прочие болезни дыхательной системы также провоцируются курением.
• Воздействие аллергенов . Увеличение перечня и фактического присутствия аллергенов в окружающей среде приводит к тому, что каждые 10 лет заболеваемость бронхиальной астмой увеличивается в полтора раза и больше.
• Воздействие профессиональных вредностей (пыль, пары кислот, щелочей и др.). Риск заболеваний дыхательной системы при работе на производствах, связанных с работой с веществами, потенциально вредными для дыхания (угольная, асбестовая, горнорудная, машиностроительная промышленность, деревообрабатывающее и текстильное производство), значительно повышен.
• Загрязнение воздуха . Бытовое загрязнение воздуха (пыль, дым, смог, волокна, чистящие средства, микрочастицы различных материалов) вызывает развитие заболеваний дыхательной системы и способствует более тяжелому их протеканию.
• Избыточный вес и ожирение. Избыточный вес вызывает одышку, требует усиленной работы не только сердца, но и легких, и, кроме того, является одной из основных причин ночного апноэ.
• Неправильное питание. Недостаток или острый дефицит таких полезных элементов, как витамины С и Е, бета-каротин, флавоноиды, магний, селен и омега-3 жирные кислоты, может быть одним из катализаторов заболевания астмой.
• Ослабление иммунитета. Слабый организм, не защищенный мощным иммунитетом, более подвержен воздействию инфекций. Риск заболеть всегда выше у тех, чей иммунитет слаб.
ПРОФИЛАКТИКА
Для сохранения здоровья необходимо поддерживать нормальный состав воздуха в жилых, учебных, общественных и рабочих помещениях, постоянно их проветривать.
Зеленые растения, выращиваемые в помещениях, освобождают воздух от избытка углекислого газа и обогащают его кислородом. На производствах, загрязняющих пылью воздух, используются промышленные фильтры, специализированная вентиляция, люди работают в респираторах — масках с фильтром для воздуха.
Большой вред организму наносит курение, так как в табаке и табачном дыме содержится никотин — сильный растительный яд, действующий отрицательно на центральную нервную систему. Вредное действие никотина на органы дыхания проявляется в уменьшении жизненной емкости легких, в хроническом раздражении слизистых оболочек дыхательных путей, вызывающем хронический бронхит курящего.
Предупредить заболевания органов дыхания можно самому, придерживаясь некоторых гигиенических требований.
1. В период эпидемии инфекционных заболеваний своевременно пройти вакцинацию (противогриппозную, противодифтерийную, противотуберкулезную и др.)
2. В этот период не следует посещать многолюдные места (концертные залы, театры и др.)
3. Придерживаться правил личной гигиены.
4. Проходить диспансеризацию, то есть медицинское обследование.
5. Повышать устойчивость организма к инфекционным заболеваниям путем закаливания, витаминного питания.
ИНФЕКЦИИ ВЕРХНИХ ДЫХАТЕЛЬНЫХ ПУТЕЙ
Инфекции верхних дыхательных путей (ИВДП) представляют собой группу наиболее распространённых острых заболеваний, наблюдаемых в амбулаторных условиях.ИВДП являются самым распространённым инфекционным заболеванием среди населения в целом, являются ведущими причинами непосещения работы или занятий в школе, и самым частым диагнозом, выставляемым больному при посещении врача.
Источник инфекции – больной человек или носитель инфекционного агента. Заразный период при инфекциях дыхательных путей чаще всего начинается с момента появления симптомов заболевания.
Механизм заражения аэрогенный, включающий в себя воздушно-капельный путь (заражение при контакте с больным посредством вдыхания частичек аэрозоля при чихании и кашле), воздушно-пылевой (вдыхание пылевых частиц с содержащимися в ней инфекционными возбудителями).
Верхние дыхательные пути включают полость носа - сами носовые ходы и придаточные пазухи носа , глотку и гортань, являющиеся путями, по которым воздух при дыхании поступает в трахею, бронхи, а далее к лёгочным альвеолам.
Наименования и определение наиболее распространённых ИВДП звучат следующим образом:
· Ринит - воспаление слизистой оболочки носа;
· Риносинуситы или синуситы - воспаление слизистой оболочки носовых ходов и околоносовых пазух, в том числе лобной, решетчатой, верхнечелюстной и клиновидной;
· Назофарингит или ринофарингит (та самая банальная простуда) - воспаление слизистой оболочки носовых ходов, носоглотки, верхней части гортани, нёбного язычка, дужек и миндалин;
· Фарингит - воспаление слизистой глотки, верхней части глотки, нёбных язычка и миндалин;
· Эпиглоттит (supraglottitis) - воспаление слизистой верхней части гортани и области надгортанника;
· Ларингит - воспаление слизистой оболочки гортани;
· Ларинготрахеит - воспаление слизистой гортани, подсвязочной области и трахеи;
Трахеит - воспаление слизистой оболочки трахеи и подсвязочной области;
Хотя ИВДП могут наблюдаться круглогодично, большинство случаев простуды приходятся на осень и зиму. Повышение частоты наблюдается в конце августа или начале сентября, с похолоданием на несколько недель, и остается повышенным до марта – апреля.
Пик заболеваемости приходится на конец зимы и начало весны. Холодная погода заставляет нас больше времени проводить в помещении (например, на работе, дома, в школе), и, естественно, чаще контактировать с лицами, которые могут быть инфицированы. Влажность также может повлиять на распространённость простуды, поскольку большинство возбудителей процветают в условиях низкой влажности, характерной для зимних месяцев. Низкая влажность воздуха в помещениях может увеличить рыхлость слизистой оболочки носа, повысив тем самым восприимчивость к инфекциям.
Осложнения инфекций органов дыхания
Осложнения инфекций дыхательных путей могут развиться при затянувшемся процессе, отсутствии адекватной медикаментозной терапии и позднем обращении к врачу. Это может быть синдром крупа (ложного и истинного), плевриты , отек легких, менингиты , менингоэнцефалиты , миокардиты , полинейропатии .
Диагностика инфекций дыхательных путей
Диагностика строится на сочетанном анализе развития (анамнеза) болезни, эпидемиологического анамнеза (предшествующий контакт с больным инфекциями дыхательных путей), клиническими данными (или данными объективного осмотра), лабораторными подтверждениями.
Профилактика инфекций дыхательных путей
1) Специфическая профилактика включает вакцинацию при ряде инфекций (пневмококковая
инфекция, грипп – сезонная профилактика, детские инфекции – корь, краснуха, менингококковая инфекция).
2) Неспецифическая профилактика – применение профилактических препаратов в сезон простуд
(осень-зима-весна) по рекомендации врача – педиатра .
3) Избегать переохлаждений (одежда по сезону, недлительное пребывание на морозе, держать ноги в тепле).
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Острые респираторные заболевания (ОРЗ) являются серьезной проблемой здравоохранения вследствие их широкой распространенности как у детей, так и у взрослых. ОРЗ составляют около 90% всей инфекционной патологии детского возраста, это самые часто встречающиеся заболевания в амбулаторной практике. Так, согласно данным Роспотребнадзора, в Российской Федерации в 2012 г. зарегистрирован 28332821 случай заболеваний острыми инфекциями верхних дыхательных путей, в т. ч. 20617641 – у детей до 17 лет.
Наиболее высокий уровень заболеваемости респираторными инфекциями отмечается у детей дошкольного и младшего школьного возраста, которые посещают организованные коллективы. Высокая частота инфекций дыхательной системы у детей обусловлена физиологическими особенностями созревания иммунной системы ребенка, неблагоприятными анте- и перинатальными факторами; курением родителей, особенно матерей; типом конституции; высокой контагиозностью вирусных инфекций, нестойким иммунитетом к ряду возбудителей, разнообразием серо- и биотипов пневмотропных бактерий (пневмококков, стафилококков, гемофильной палочки) и многими другими факторами.
Частые повторные эпизоды инфекций респираторного тракта у детей являются значимой социально-экономической проблемой российского здравоохранения, т. к. не только приводят к ухудшению здоровья и качества жизни пациентов, но и наносят существенный экономический ущерб семье и обществу. Значительное число ОРЗ протекает легко и не требует проведения серьезных лечебных мероприятий. Известно, что контакт и взаимодействие с респираторными инфекциями – необходимые условия становления иммунной системы ребенка, приобретения им иммунологического опыта, необходимого для адекватного реагирования на микробную агрессию. Однако частые респираторные заболевания, следующие одно за другим, безусловно, оказывают на ребенка негативное воздействие. Дети с частыми повторными (рекуррентными) заболеваниями органов дыхания требуют особого внимания врача и должны наблюдаться во II диспансерной группе здоровья с соблюдением соответствующих профилактических и терапевтических стандартов. Повторные респираторные инфекции способствуют формированию хронических заболеваний и могут определить на долгие годы неудовлетворительное качество здоровья ребенка [2, 7, 10].
Профилактика респираторных инфекций ЧБД предусматривает ограничение контактов ребенка с больными гриппом и ОРВИ, проведение санитарно-гигиенических мероприятий, сокращение использования городского транспорта и удлинение времени пребывания ребенка на воздухе. Частая респираторная заболеваемость тесно связана с пассивным курением, поэтому его прекращение – важное условие лечения и профилактики [2, 5]. Все дети, склонные к частым респираторным инфекциям, должны быть осмотрены и, при необходимости, пролечены ЛОР-врачом.
Одним из основных методов повышения сопротивляемости ребенка инфекционным агентам служит закаливание. Систематическое контрастное воздушное или водное закаливание сопровождается повышением устойчивости организма к температурным колебаниям окружающей среды и увеличением иммунологической реактивности организма. Использование любых методов закаливания совершенствует работу аппарата терморегуляции и расширяет возможности приспособления организма к изменившимся температурным условиям. Закаливание не требует очень низких температур, важны контрастность воздействия и систематичность проведения процедур. Хорошо закаливает воздействие на подошвы ног и, постепенно, – на всю кожу туловища и конечностей. Максимальная длительность закаливающих процедур не должна превышать 10–20 мин, гораздо важнее их регулярность и постепенность. Было показано, что у ЧБД сочетание местных закаливающих процедур стоп и носоглотки через 3–4 мес. восстанавливало цитологические показатели носового секрета. Закаливание после нетяжелого ОРЗ можно возобновить (или начать) через 7–10 дней, при заболевании с длительностью температурной реакции более 4 дней – через 2 нед., а после 10-дневной лихорадки – через 3–4 нед. [7]. Эффективность закаливания можно оценить не ранее чем через 3–4 мес., а максимальный эффект наблюдается через 1 год от начала регулярных процедур.
Вакцинация ЧБД – одно из самых важных профилактических мероприятий. Поскольку частые ОРВИ у этой группы детей не свидетельствуют о наличии иммунодефицита, они не могут быть поводом для отвода от прививок, противопоказанием к их проведению. По окончании ОРВИ, как и других острых заболеваний, прививки можно проводить через 2–3 нед. после нормализации температуры тела [10].
С учетом ведущей роли дисфункций иммунитета в развитии повышенной восприимчивости детского организма к респираторным инфекциям кроме комплекса общеукрепляющих мероприятий с целью профилактики используется целый ряд иммуномодулирующих лекарственных средств. При этом большинство авторов подчеркивают, что такие препараты с целью предупреждения респираторных инфекций у ЧБД должны применяться с обязательным соблюдением общих принципов профилактики и оздоровления.
Из средств неспецифической профилактики респираторных инфекций в педиатрии часто применяются препараты, полученные из эхинацеи. В современной медицине чаще применяют препараты из эхинацеи пурпурной (Echinacea purpurea). Известно, что эхинацея богата полисахаридами и фитостеринами, оказывающими стимулирующее действие на иммунную систему, содержит макро- и микроэлементы: железо, цинк, селен, калий, кальций, молибден, серебро, кобальт, никель, барий, бериллий, ванадий, марганец. Эхинацея пурпурная содержит активные вещества, укрепляющие естественные защитные силы организма и действующие в качестве неспецифических стимуляторов. При назначении эхинацеи наблюдаются повышение фагоцитоза, иммунорегуляторного индекса, функциональной активности В-лимфоцитов, индукция синтеза интерферона. В эксперименте показано, что перитонеальные макрофаги мышей под влиянием эхинацеи продуцировали фактор некроза опухоли, интерлейкины (ИЛ): ИЛ-1, ИЛ-6, ИЛ-10.
Как в нашей стране, так и за рубежом хорошо известен и наиболее часто применяется препарат из высушенного сока эхинацеи Иммунал®. Повышая количество лейкоцитов (гранулоцитов) и стимулируя фагоцитоз, активные вещества препарата подавляют рост и размножение микроорганизмов в организме человека и способствуют уничтожению болезнетворных бактерий. Многочисленными исследованиями установлено противовирусное действие препаратов из эхинацеи пурпурной в отношении респираторных вирусов, а также возбудителей гриппа и герпеса.
Мы рассмотрели доказательства применения антибиотиков для предотвращения бактериальных инфекций нижних дыхательных путей (ИНДП) у детей в возрасте до 12 лет, которые находятся в группе повышенной вероятности заражения этими инфекциями.
Ежегодно около 1,4 миллиона детей умирают от инфекций дыхательных путей. Каждый пятый случай смерти приходится на детей в возрасте до пяти лет. Использование антибиотиков для предотвращения ИНДП у детей с высоким уровнем риска в возрасте до 12 лет может быть полезным. Однако, в настоящее время не существует обзора, описывающего доказательства по использованию антибиотиков для предотвращения ИНДП в этой группе населения.
В феврале 2015 года, мы провели поиск исследований, посвященных эффективности применения антибиотиков для предотвращения ИНДП у детей в возрасте до 12 лет с повышенным риском заражения этими инфекциями.
Мы включили 10 исследований: три изучали эффективность антибиотиков в группе из 1345 детей с ВИЧ, четыре - в группе из 429 детей с муковисцидозом, одно - в группе из 219 детей с серповидно-клеточной анемией, одно - в группе из 160 детей, проходящих лечение от рака, и одно в группе из 40 детей со сниженной массой тела при рождении и с проблемами дыхательных путей.
Продолжительность исследований была между 18,9 и 24,7 месяцами у детей с ВИЧ, от 6 до 36 месяцев у детей с муковисцидозом, 15 месяцев в одном исследовании у детей с серповидно-клеточной анемией, от 13 до 24 месяцев в одном исследовании у детей, больных раком, и семь дней у новорожденных со сниженной массой тела при рождении и с проблемами дыхательных путей.
Источники финансирования исследований
Из трех исследований, которые включали детей с ВИЧ, на одно средства были выделены Международным Агентством Помощи, на второе — правительством, третье финансировалось за счет благотворительных средств.
Из четырех исследований, которые включали детей с муковисцидозом, три финансировались благотворительными организациями и одно правительством.
Исследование, включающее детей с серповидно-клеточной анемией финансировалось правительством. Исследование, которое включало детей с раком было профинансировано правительством, представителями промышленности, а также за счет благотворительных средств.
Для исследования, которое включало новорожденных с дыхательными расстройствами, источник финансирования указан не был.
У детей с ВИЧ, антибиотики не снизили вероятность заражения туберкулезом. В целом не отмечалось никакого улучшения в показателях смертности, но было заметно снижение частоты госпитализаций при использовании антибиотиков в одном из исследований.
У детей с муковисцидозом, антибиотики не снизили вероятность заражения бактерией Pseudomonas , но в этой группе отмечалось уменьшение частоты обострений, при которых бактериальная инфекция затрудняет дыхание у детей.
В одном исследовании у детей с серповидно-клеточной анемией, антибиотики снизили вероятность заражения сепсисом.
В одном исследовании у детей с раком, антибиотики уменьшили вероятность инфицирования лёгких Pneumocystis .
В группе новорожденных с низкой массой тела при рождении и с расстройствами дыхания антибиотики не снизили вероятность легочных инфекций.
У детей с ВИЧ, мы оценили общее качество доказательств для двух исследований, которые изучали эффект антибиотиков для предотвращения туберкулеза, как среднее из-за различий в путях введения антибиотиков. Мы оценили качество доказательств в отношении использования антибиотиков для снижения смертности как среднее из-за различий в типах используемых антибиотиков. Из-за отсутствия данных, мы не смогли оценить качество доказательств в отношении исхода - госпитализации.
В двух исследованиях у детей с муковисцидозом, которые изучали влияние антибиотиков на снижение вероятности инфицирования Pseudomonas , мы оценили общее качество доказательств как умеренное (среднее) из-за различий в типах используемых антибиотиков. Мы оценили качество доказательств в отношении эффективности антибиотиков в уменьшении числа вспышек (обострений) как высокое.
У детей, больных раком, мы оценили качество доказательств эффективности антибиотиков в отношении снижения вероятности развития инфекции Pneumocystis как умеренное (среднее) из-за вероятности косвенности результатов исследования.
Из-за отсутствия данных, мы не смогли оценить качество доказательств эффективности при использовании антибиотиков для снижения вероятности развития сепсиса у детей с серповидно-клеточной анемией и снижения вероятности легочных инфекций у новорожденных со сниженной массой тела при рождении и с дыхательными расстройствами; оба исследования имели низкую вероятность и высокую вероятность смещения соответственно.
Читайте также:


