Препараты для лечения цитомегаловирусной инфекции у детей
Каков комплекс диагностических процедур при подозрении на ЦМВИ? Какая терапия проводится у беременных с ЦМВИ? Существуют ли профилактические меры для предупреждения заражения плода ЦМВИ? Цитомегаловирусная инфекция (ЦМВИ) у беременных относится

Цитомегаловирусная инфекция (ЦМВИ) у беременных относится к числу самых распространенных заболеваний, определяющих внутриутробное инфицирование и акушерскую патологию. В последние годы отмечена тенденция к увеличению инфицирования беременных цитомегаловирусом (ЦМВ).
Цитомегаловирусная инфекция может протекать атипично, с латентными, инаппарантными формами проявлений и поражением тканей органов, что представляет большие трудности для своевременного распознавания инфекции и является причиной диагностических ошибок.
Комплекс диагностических мероприятий должен включать раннее выявление ЦМВИ, определение степени ее активности, сопутствующей патологии беременности, плода и новорожденного.
Вирусологический мониторинг предусматривает возможность следующих исследований.
- Метод выделения ЦМВ на клеточной культуре - наиболее достоверный и чувствительный, но при этом относительно трудоемкий и занимающий много времени (от 3 до 7 суток) способ; следует учитывать, что время исследования может быть сокращено до 24 - 36 ч - при использовании метода флуоресцирующих антител.
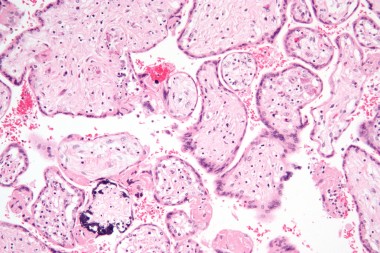
- Цитологическое исследование (световая и электронная микроскопия) позволяет выявить типичные гигантские клетки с внутриядерными включениями.
- Реакция связывания комплемента (РСК) применяется для определения комплементсвязывающих антител к ЦМВ; обычно этот метод используется в сочетании с цитоскопическими исследованиями.
- Метод иммунофлуоресцентного выявления антигенов ЦМВ позволяет получить результат в течение 2 - 3 ч; обнаружение антигенов обеспечивает быстрый ответ, однако данный метод не может считаться достаточно чувствительным.
- Исследование специфических антител к цитомегаловирусу иммуноглобулинов класса М и G с помощью иммуноферментного метода. Серологические методы могут быть использованы как для диагностики ЦМВИ, так и при проведении дифференциального диагноза между первичной и хронической цитомегаловирусной инфекцией. Твердофазный иммуноанализ позволяет производить раздельное исследование субклассов иммуноглобулинов к ЦМВ. Наиболее современным способом исследования специфических антител к ЦМВ следует считать иммуноблот, позволяющий с помощью полиакриламидного гельэлектрофореза определять весь спектр антител к ЦМВ.
- Молекулярно-биологические методы диагностики вирусных инфекций - ДНК-гибридизация, полимеразная цепная реакция (ПЦР) - позволяют определять ДНК цитомегаловируса в любых биологических тканях. ПЦР- метод обладает высокой чувствительностью и специфичностью и может применяться для выявления ДНК ЦМВ в мазках. Применение ПЦР и ДНК-гибридизации позволяет контролировать течение ЦМВИ у беременных и новорожденных.
Клинические и лабораторные исследования, имеющие по большей части вспомогательное значение в диагностике ЦМВИ, тем не менее необходимы для оценки состояния матери и новорожденного. Эти методы включают:
- клинические анализы крови и мочи;
- биохимические исследования крови;
- состояние иммунного статуса.
Диагностика во время беременности асимптоматичной первичной ЦМВИ может быть проведена на основании данных серологических исследований. Присутствие антител IgG к ЦМВ указывает либо на ранее перенесенную, либо на имеющуюся в настоящий момент инфекцию. Высота титра, к сожалению, не помогает установить, идет ли речь о первичной инфекции или ее обострении, которое также может сопровождаться подъемом титра антител.
Присутствие антител IgM позволяет предположить наличие первичной ЦМВИ, однако при интерпретации теста надо иметь в виду, что антитела IgM к ЦМВ могут сохраняться до 12 недель или дольше после перенесенной первичной ЦМВИ.
Выявление культуры вируса в моче, слюне или цервиковагинальных выделениях не позволяет отличить первичную от рецидивирующей формы ЦМВИ, особенно при асимптоматичном течении.
Вирусоносительство, независимо от формы перенесенного заболевания, может наблюдаться у женщин в течение многих лет. Кроме того, присутствие культуры ЦМВ у беременной женщины еще не означает, что имеет место инфицирование или заболевание плода.
ЦМВИ у плода может быть также установлена путем изолирования вируса из амниотической жидкости. Наличие антител IgM в крови плода, полученной с помощью кордоцентеза, служит указанием на возможность инфицирования плода ЦМВ. Отсутствие культуры ЦМВ и отрицательные серологические показатели еще не исключают наличия ЦМВИ. Кроме того, следует отметить, что при двойнях может быть инфицирован только один ребенок.
Лабораторные исследования у новорожденных позволяют выявить анемию, тромбоцитопению, изменение функции печени (АсТ, АлТ ).
У новорожденных диагностика ЦМВИ с использованием крови, слюны, мочи проводится в первые 3 недели жизни.
Инфицирование эмбриона ЦМВИ может быть установлено пренатально с помощью трансабдоминального амниоцентеза с последующим вирусологическим исследованием амниотической жидкости, а также с помощью кордоцентеза — исследования пупочной крови плода.
Методы пренатальной диагностики, включающие УЗИ, допплерометрию, кардиотокографию, позволяют выявить сопутствующую или обусловленную ЦМВИ патологию беременности (маловодие, многоводие, задержку внутриутробного развития), а также патологию внутренних органов плода (гепатоспленомегалия, асцит плода, водянка, кишечная непроходимость, микроцефалия, гидроцефалия, церебральная вентрикуломегалия, внутричерепные или внутрипеченочные кальцификаты).
Важное значение для верификации внутриутробной ЦМВИ имеют морфологические и вирусологические исследования плаценты и плодных оболочек.
Специальные методы определения внутриутробной ЦМВИ становятся ведущими при планировании стратегии родов и служат для педиатра сигналом о возможности возникновения у новорожденного целого ряда проблем.
Первичная ЦМВ-инфекция может быть диагностирована путем определения в крови плода специфических ЦМВ-антител IgM и исследования амниотической жидкости.
В отличие от тех случаев, когда у ребенка пренатально диагностируются генетические заболевания, последствия которых могут быть предсказаны с определенной точностью, у детей с врожденной ЦМВИ нередко наблюдаются патологии, характеризующиеся бессимптомным и атипичным течением. Длительное выделение ЦМВ со слизью из шейки матки и влагалища или со слюной обусловливает большую вероятность инфицирования плода во время и после родов.
Диагностические исследования в полном объеме должны проводиться при малейшем подозрении на наличие цитомегаловирусной инфекции у женщины. Особенно важно проводить эти исследования у первородящих, а также при неблагоприятном исходе предыдущей беременности и при клинической манифестации ЦМВИ во время беременности.
Результаты вирусологического обследования таких беременных имеют важное значение для определения тактики ведения родов.
Вопросы антивирусной химиотерапии остаются до настоящего времени недостаточно разработаны. Наиболее эффективными средствами являются препараты (ганцикловир, фоскарнет и др.), которые оказывают ингибирующий эффект на вирусы герпеса. Однако длительный прием их чаще всего невозможен из-за высокой токсичности. Применение ганцикловира у новорожденных с генерализованной формой ЦМВИ может уменьшить летальность, быстрее купировать проявления пневмонии, гепатоспленомегалию, тромбоцитопению, смягчить неврологическую симптоматику, а также тяжесть поражения зрительного и слухового нервов.
Фоскарнет (препарат дифосфомуравьиной кислоты) эффективен, но и высокотоксичен. Фоскарнет и циклические аналоги гуанозина, ингибирующие ДНК-полимеразу цитомегаловируса и препятствующие его внутриклеточной репликации (ганцикловир, цимевен) пока находят ограниченное применение в перинатологии в связи с их большой токсичностью (гепатотоксичность, депрессия кроветворения) для новорожденного.
Однако эффективность использования различных препаратов в терапии плода, равно как и лечения беременных женщин с первичной ЦМВИ с целью уменьшения перехода вируса к плаценте и плоду, до конца не исследованы.
У беременных женщин с установленной ЦМВИ проводится симптоматическая терапия. Необходимо проводить с ними беседы об опасности, которую представляет для плода ЦМВИ, и методах профилактики этой инфекции.
Методы лечебной терапии у новорожденного с врожденной ЦМВИ нуждаются в дальнейшем совершенствовании.
Специфическая терапия у детей с внутриутробной ЦМВИ должна проводиться только после верификации диагноза, подтвержденного данными клинических, иммунологических, вирусологических исследований.
Терапия ЦМВИ включает в первую очередь применение специфического антицитомегаловирусного иммуноглобулина (цитотект) в разовой дозе 25–50 Е/ кг массы тела — не менее 6 доз препарата с интервалом в 2 — 3 недели.
В остром периоде ЦМВИ у новорожденных и детей раннего возраста показано лечение препаратами рекомбинантного интерферона — виферон, интрон-А, роферон-А (по схеме: 500 тыс — 1 млн. МЕ 1 раз в день в течение 14 дней и далее через день до 1,5 — 3 месяцев; и до 3 — 6 месяцев от начала лечения курсы по 4 недели при хронической инфекции) или индукторами интерферона — ридостин, неовир и др. Эти препараты рекомендуются и для противорецидивной терапии ЦМВИ в тех случаях, если у ребенка появляются признаки реактивации вируса цитомегалии (обнаружение анти-ЦМВ антигена в моче и/или крови или появление анти-ЦМВ IgМ в сыворотке).
При тяжелой генерализованной форме ЦМВИ лечение проводится ганцикловиром (цимевен) (по схеме: 5 — 7,5 мг/кг массы тела в сутки путем двукратных внутривенных инфузий в течение 14 — 21 дней), в комбинации со специфическим ЦМВ-иммуноглобулином (Сytotect) (в дозе 2 мл/ кг капельно через 2 дня — до исчезновения клинических симптомов).
Назначение ганцикловира наиболее обоснованно у детей с врожденной ЦМВИ, поражением центральной нервной системы и пневмонией.
При легкой форме ЦМВИ проводится лечение препаратами интерферона — роферон-А, лейкинферон, виферон (по 500 тыс. МЕ 3 — 5 раз в неделю в течение 4 недель) или стимуляторами интерфероногенеза — ридостин (по 8 мг 1 раз в 3 дня, на курс лечения — 5 — 7 инъекций), неовир (по 1 дозе ежедневно внутримышечно в течение 3 дней, затем по 1 дозе через день в течение последующих 4 дней).
Лечебная терапия у новорожденного должна включать комплекс мероприятий по уменьшению явлений инфекционного токсикоза путем проведения инфузионной терапии: растворов глюкозы, полидеза, реополиглюкина, реополиглюкама, альбумина и др. (по схеме: общим объемом 100–200 мл/кг массы тела в сутки).
При возникновении органной патологии (гепатит, пневмония, панкреатит, энцефалит и др.) дополнительно проводится лечение с учетом тяжести поражения органа.
При присоединении бактериальной инфекции или угрозе возникновения осложнений назначаются антибиотики из групп цефалоспоринов (II — III поколения), аминогликозидов, макролидов, фторхинолонов и др. в дозировках по общепринятым схемам и в соответствии с возрастом ребенка.
Все дети с цитомегаловирусной инфекцией должны получать высококалорийное физиологическое питание, а также поливитаминные препараты (пентовит, витогепат, ревит, глутамевит, мультибонта плюс, мультифит, витанова D, лековит, витамакс и др.).
Выздоровление констатируется на основании отсутствия клинической симптоматики и при стойких отрицательных результатах обследования на ЦМВ-антиген в моче и крови; а также на основании отсутствия анти-ЦМВ IgМ в сыворотке при положительном результате обследования на анти-ЦМВ IgG.
Однако этот контингент детей подлежит динамическому диспансерному наблюдению и контрольному обследованию на активность инфекционного процесса через 1, 3, 6 и 12 месяцев после выписки из стационара.
Что необходимо делать при ЦМВИ во время беременности. Специальных способов профилактики инфицирования плода не существует, в связи с чем беременным с острой ЦМВ-инфекцией следует принимать обычные меры предосторожности. Однако, если женщину сильно беспокоит риск развития заболевания у ребенка, в таких случаях необходим индивидуальный подход. Медикаментозная терапия у беременных лишь уменьшает выраженность симптомов. Противовирусная терапия имеет потенциальный риск для плода. Женщины, которые активно выделяют вирус во время беременности, могут рожать самостоятельно, так как кесарево сечение не обеспечивает в этом случае никаких преимуществ для ребенка.
Цитомегаловирусная инфекция представляет наибольшую опасность для беременных, плода и новорожденного.
Принимая во внимание особенности патогенеза цитомегаловирусной инфекции, а также социальную и медицинскую значимость данной проблемы, необходимо проводить целый комплекс мероприятий, направленных на профилактику материнской, перинатальной заболеваемости и смертности.
В случае неблагоприятного исхода беременности или гибели новорожденного, при подтвержденной лабораторными методами цитомегаловирусной инфекции следующая беременность допустима только на фоне достижения устойчивой ремиссии, после проведения специфического лечения. Для этого в остром периоде наиболее эффективным является использование комплекса антивирусных препаратов, а в период ремиссии, с целью профилактики рецидивов и достижения стойкой ремиссии, — противоцитомегаловирусной вакцины.
Профилактика с помощью иммунизации крайне желательна. Однако отсутствие доступной вакцины для предотвращения ЦМВИ требует особенно тщательного соблюдения принципов личной гигиены, кроме того, необходимо исключить возможность близкого контакта с носителями ЦМВ.
В настоящее время имеются надежные и недорогие серологические методы исследования ЦМВ, которые необходимо рекомендовать женщинам в детородном возрасте. Особенно важно следить за своим серологическим статусом серонегативным к ЦМВ женщинам.
В связи с тем что инфицированные беременные и роженицы могут не только заражать своих детей, но и быть источником внутрибольничной инфекции, необходимо соблюдать эпидемический режим и меры профилактики.
- Проведение санитарно-просветительной работы в женских консультациях.
- Соблюдение санитарно-гигиенических норм во время беременности.
- Соблюдение норм личной гигиены, термическая обработка и мытье продуктов.
- Ранняя диагностика инфекции у матери и ребенка.
- Госпитализация беременных с первичной цитомегаловирусной инфекцией должна проводиться в обсервационное отделение за 2 недели до родов.
- Дети, родившиеся от матерей с первичной цитомегаловирусной инфекцией, должны быть изолированы как от других новорожденных, так и от матерей с клинической манифестацией инфекции.
- Если ребенок получает грудное молоко, его мать должна быть информирована о возможных путях и механизмах передачи ЦМВ и строго соблюдать правила личной гигиены.
- Новорожденный ежедневно должен тщательно обследоваться врачом с целью выявления признаков цитомегаловирусной инфекции. На 2, 5 и 12-е сутки у младенца берутся соскобы тампоном со слизистых оболочек глаз, полости рта и носоглотки для вирусологического обследования.
- Необходимо проводить тщательную дезинфекцию палат, белья, а также стерилизацию медицинского инструментария и средств индивидуального ухода.
- Медицинский персонал, во избежание заражения и передачи инфекции, должен проходить тщательное обследование и соблюдать правила личной гигиены.
- Матери и члены семьи, имеющие цитомегаловирусную инфекцию, должны быть осведомлены о возможных путях ее передачи и соблюдать необходимые профилактические мероприятия.
Предлагаемая диагностическая и лечебная тактика у беременных и у женщин в родах может быть достаточно эффективной и успешно реализоваться в условиях родовспомогательного учреждения.
В. Н. Кузьмин, доктор медицинских наук, профессор МГМСУ, Москва
В статье проанализированы опубликованные данные по вопросам адекватной диагностики антенатальной и постнатальной цитомегаловирусной инфекции (ЦМВИ), а также лечению острых ЦМВИ у беременной, плода и новорожденного. Представлены отечественные клинические р
The article gives analysis of the data on the issues of relevance of diagnostics of antenatal and postnatal cytomegaloviral infection (CMVI), as well as treatment of acute CMVI in the pregnant, fetus and newborns. National clinical guidelines on diagnostics and treatment of congenital CMVI developed by the Russian Association of antenatal medicine in 2016, were presented; as well as the first unofficial international guidelines on the issues of diagnostics and treatment of congenital CMVI.
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R. P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес
И. Я. Извекова 1 , доктор медицинских наук, профессор
М. А. Михайленко
Е. И. Краснова, доктор медицинских наук, профессор
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование
Методы лечения цитомегаловируса у детей и взрослых
Цитомегаловирусная инфекция относится к семейству герпесвирусов. Заболевание протекает латентно у здоровых людей, но весьма опасно для пациентов с иммунодефицитом (ВИЧ-инфицированных, принимающих иммуносупрессоры после трансплантации органов и тканей). Врожденная цитомегаловирусная инфекция может привести к серьезным патологиям и даже смерти. После инфицирования вирус остается в организме на протяжении всей жизни и способен к реактивации в любое время, что может вызвать развитие мукоэпидермоидной карциномы и других злокачественных образований. Вот почему так важно своевременно сдать анализ крови на антитела к цитомегаловирусу во время беременности.
Причины и симптомы заболевания
Заражение происходит при непосредственном контакте с носителем инфекции или больным через различные биологические жидкости: кровь, сперму, слюну, влагалищные выделения, мочу, грудное молоко. Еще один путь передачи инфекции – от матери к плоду во время беременности. При инфицировании плода может развиться врожденная цитомегалия.
У пациентов с нормальным иммунитетом ЦМВ-инфекция через 30-60 суток после заражения часто проявляется мононуклеозоподобным синдромом. Могут отмечаться слабость, лихорадка, боль в мышцах. После выработки антител против вируса симптомы заболевания исчезают, но вирус остается в организме в неактивной форме.
У пациентов с ослабленным иммунитетом цитомегаловирусная инфекция вызывает поражение легких, поджелудочной железы, печени, почек и других органов. Внутриутробное инфицирование плода чревато развитием серьезного заболевания – врожденной цитомегалии.
Симптомы цитомегалии:
- увеличение селезенки, печени;
- хориоретинит;
- пневмония;
- тугоухость;
- аномалии развития зубов.
Вирус Эпштейна-Барр тоже относится к семейству герпесвирусов. Симптомы поражения вирусом Эпштейна-Барр у мужчин:
- повышение температуры тела;
- воспаление миндалин;
- увеличение лимфоузлов на шее, затылке, в паховой области.
Что значит положительный цитомегаловирус IgG
Наличие антител IgM к цитомегаловирусу у женщин при отрицательном IgG говорит о недавнем инфицировании и начале развития болезни. Положительный результат анализа на определение антител IgG и IgM свидетельствует об острой стадии заболевания.
Обнаружен цитомегаловирус при беременности – что делать
Как лечить цитомегаловирус? Вирусоносительство и мононуклеозоподобный синдром у пациентов с нормальным иммунитетом обычно не требуют лечения. Терапию назначают при выявлении генерализованных форм инфекции. Поскольку применяемые для лечения цитомегаловируса препараты достаточно токсичные, их назначают только по жизненным показаниям. Для профилактики цитомегаловирусной инфекции, развивающейся на фоне иммунодепрессивной терапии, назначают иммуноглобулин антицитомегаловирусный (один или в сочетании с противовирусным препаратом). Это позволяет предупредить ухудшение состояния и снизить риск летального исхода.
Если обнаружен цитомегаловирус при беременности, то для профилактики передачи вируса плоду проводят десенсибилизирующую и общеукрепляющую терапию. Назначают иммуномодуляторы, витамины. В качестве специфического средства применяют нормальный человеческий иммуноглобулин. Число мертворождений при такой схеме лечения снижается в пять раз. Препараты с выраженным противовирусным действием токсичны, а потому не применяются для лечения ЦМВ-инфекции у беременных.
Лечение цитомегаловируса у детей проводят с использованием специфических иммуноглобулинов и противовирусных препаратов. Эффективным средством для лечения ЦМВ-инфекции признан ганцикловир – пуриновый ациклический нуклеозид. Однако препарат обладает высокой токсичностью, поэтому его не применяют для лечения цитомегаловируса у новорожденных. В других возрастных группах ганцикловир назначают только при непосредственной угрозе жизни ребенка. Применение препарата оправдано при подтвержденном диагнозе и наличии четких показаний.
Читайте также:
- Живые переносчики возбудителей инфекций
- Гель панавир отзывы от папиломо-вирусной инфекции
- Укажите неправильное утверждение к оппортунистическим инфекциям относят
- Инфекция в море в ялте
- Частные клиники находят инфекции
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции

