Печень при системной красной волчанке
Симптомы
Самые первые симптомы красной волчанки — покраснения и высыпания с четкой локацией на верхней части лица, по форме напоминающие бабочку, они хорошо заметны под глазами, на щеках, на переносице. Часто сыпь сопровождается зудом. Такие симптомы могут время от времени обостряться, а затем снова затихать. Именно поэтому их можно легко спутать с любыми другими проявлениями, например, обыкновенной аллергией, с которой не каждый пациент обратится к доктору. Куда более серьезными симптомами можно считать судороги, повышенную температуру тела, воспаление суставов, которое может причинять невыносимую боль. Нередко при красной волчанке фиксируют увеличение лимфоузлов, сильную головную боль, изъязвления на слизистой ротовой полости, нарушение работы пищеварительной системы.
Диагностика
У больных вырабатываются специфические антинуклеарные антитела – иммуноглобулины, которые свидетельствуют об иммунных нарушениях у пациента. В данном случае маркерами красной волчанки являются LE клетки. Их можно обнаружить в крови у человека на начальной стадии заболевания или в период обострения. Анализ проводится как при первичном обращении для диагностики, так и для контроля эффективности в период лечения.
Несмотря на то что теоретически в медицине различаются несколько видов волчанки, чаще всего в России медики имеют дело с СКВ (системная красная волчанка) – это самая распространенная форма, от которой страдают до 90 % всех больных. Также различают: - неонатальную волчанку – болезнь новорожденных, которые инфицируются через плацентарный кровоток от матери; - кожную – при которой поражаются только кожные покровы, без серьезных системных сбоев в организме - лекарственную – такая форма провоцируется приемом лекарственных препаратов.
Причины возникновения
Красная волчанка - болезнь неизлечимая, ее этиология (причины) медикам до сих пор до конца не понятна, именно поэтому ученые назвали СКВ самым сложным заболеванием в мире. Иммунные нарушения, на основе которых зарождается патология, базируются на аутоиммунной реакции, при которой клетки иммунитета вместо борьбы с патогенными вирусами распознают свои собственные, как чужеродные и атакуют их.
Наследственность – один из решающих факторов, который влияет на развитие заболевания у человека. Но нельзя утверждать, что только при неблагоприятном анамнезе болезнь может развиваться. Образ жизни, стрессовые ситуации, различные приобретенные инфекции и тяжесть их последствий, курение, алкоголь, избыточная масса тела, а также некоторые лекарственные препараты могут быть провокаторами болезни. В свою очередь, обостряться она может при долгом пребывании на солнце: ультрафиолет, жара и высокая влажность – самые благоприятные условия для развития заболевания.
Как известно, 20-й век стал переломным в развитии медицины. В том числе, значительно улучшились показатели по выживаемости пациентов с диагнозом красная волчанка, сократились случаи инвалидизации. Новейшие препараты, методики, поддерживающая медикаментозная терапия помогают купировать тяжелые симптомы, приостанавливать разрушение внутренних органов и тканей человека.
Беременные – в группе риска
Одним из самых опасных по последствиям состояний при красной волчанке была беременность. До середины 20 века женщинам детородного возраста с диагнозом СКВ или имеющим в анамнезе подобную наследственность было фактически противопоказано планировать беременность из-за высоких рисков невынашивания. В худшие времена почти в половине подобных случаев беременность заканчивалась внутриутробной гибелью плода или серьезными угрозами для жизни женщины.
В современной медицине подобные факты также встречаются, но сегодня у врачей гораздо больше инструментов, для того чтобы обеспечить благоприятное течение беременности и родовспоможения. Хотя угрозы могут сохраняться, например, когда женщина узнает о тяжелом диагнозе, только будучи в положении, или уже после родов.
В медицинской практике, например, описан такой случай. Одна из пациенток до момента рождения ребенка в 30 лет не подозревала о том, что больна красной волчанкой. А после родов врачи долгое время не могли поставить ей диагноз. Ребенок родился недоношенным – на 26-й неделе, с небольшим весом и диагнозом ДЦП. Долгое время малыш находился в реанимации, на аппарате ИВЛ. У мамы воспаление брюшины, непрекращающаяся высокая температура тела, невыносимая боль в суставах, периодическая потеря сознания. Все узкие специалисты после обследования не увидели никаких отклонений. Диагноз был поставлен случайно, когда пациентка находилась в реанимации, на волоске от смерти. Последовал курс гормональных препаратов, после которого — алопеция (выпадение волос) и стремительный набор веса. И у малыша, и у мамы — неутешительные прогнозы на жизнь, поддерживать которую помогли многочисленные курсы реабилитации и медикаментозной терапии для обоих.
Аннотация научной статьи по клинической медицине, автор научной работы — Богмат Л.Ф., Шевченко Н.С., Матвиенко Е.В.
Целью исследования явилось изучение состояния печени у подростков с системной красной волчанкой (СКВ). В результате обследования 48 больных СКВ в возрасте 12-18 лет установлены частота поражения печени (22,9 %), взаимосвязь развития цитолиза со степенью активности и клиническими проявлениями заболевания, частота риска развития фиброза (27,3 %) и его вероятное наличие у 9,1 % подростков в дебюте СКВ.
Похожие темы научных работ по клинической медицине , автор научной работы — Богмат Л.Ф., Шевченко Н.С., Матвиенко Е.В.
Liver Damage in Systemic Lupus Erythematosus in Adolescents
The objective of the study was to investigate the state of the liver in adolescents with systemic lupus erythematosus (SLE). As a result of examination of 48 patients with SLE aged 12-18 years, there were established incidence of liver damage (22.9 %), correlation of cytolysis with the degree of activity and clinical manifestations of the disease. Also, the incidence of the risk of fibrosis (27.3 %) and its possible presence in 9.1 % of adolescents in the onset of SLE were detected.
КлУчна пед1атр1я / Clinical Pediatrics
БОГМАТЛ.Ф., ШЕВЧЕНКО Н.С., МАТВИЕНКО Е.В.
ПОРАЖЕНИЕ ПЕЧЕНИ ПРИ СИСТЕМНОЙ КРАСНОЙ ВОЛЧАНКЕ
Резюме. Целью исследования явилось изучение состояния печени у подростков с системной красной волчанкой (СКВ). В результате обследования 48 больных СКВ в возрасте 12—18 лет установлены частота поражения печени (22,9 %), взаимосвязь развития цитолиза со степенью активности и клиническими проявлениями заболевания, частота риска развития фиброза (27,3 %) и его вероятное наличие у 9,1 % подростков в дебюте СКВ.
Ключевые слова: системная красная волчанка, подростки, печень, фиброгенез.
На современном этапе развития клинической педиатрической ревматологии одной из основных ее проблем являются системные болезни соединительной ткани, основным представителем которых остается системная красная волчанка (СКВ) [1, 2]. Благодаря эволюции диагностических возможностей, средств и методов лечения в настоящее время детские ревматологи обладают широким терапевтическим арсеналом для прерывания каскада аутоиммунных реакций и купирования активности болезни. Поэтому на первый план выступает задача сохранения структуры и функции жизненно важных органов и систем, предотвращения их необратимых изменений при развитии заболевания.
Одним из таких органов является печень, выполняющая около 500 различных функций, в связи с чем наши предки считали ее центром души и вместилищем жизни. Печеночные клетки участвуют во всех обменных процессах (углеводном, жировом, белковом, водном, минеральном, пигментном, витаминном, гормональном), синтезе множества веществ (холестерин, жирные и желчные кислоты, белки, факторы свертывания крови), сохранении энергетических ресурсов (гликоген, витамины А, D, E, К, В6 и В12, фолиевая кислота) [2].
Поражение печени, как правило, не является частью диагностического спектра при СКВ, однако выявляется у 60 % больных. Проявления ее патологии могут варьировать от незначительного увеличения до картины довольно тяжелого гепатита. При гистологическом исследовании биоптата печени отмечают полнокровие и застой в сосудах, жировую
инфильтрацию и некрозы в портальной системе [3, 4]. Редко встречается васкулит печени, приводящий к инфарктам и разрывам органа с клиникой острого живота [5]. Примерно у 25 % больных с СКВ отмечается субклиническое повреждение печени, о котором говорит повышенная активность печеночных ферментов. Лишь у 8 % пациентов выявляется повреждение печени, связанное непосредственно с самим заболеванием и возникающее, как правило, на высоте активности болезни, — собственно вол-чаночный гепатит [6]. При этом ряд авторов придерживаются мнения о том, что наиболее частыми причинами повышения уровня трансаминаз и гепа-томегалии у взрослых при СКВ являются ожирение и лекарственная терапия (гепатотоксические препараты) [5].
Адрес для переписки с авторами: Шевченко Н.С.
Определенную роль играет генетическая предрасположенность к возникновению гепатотоксиче-ских эффектов медицинских препаратов, которая определяется полиморфизмом генов, участвующих в метаболизме лекарств, что приводит к особой биотрансформации медицинских препаратов у индивидуально чувствительных лиц [7].
В условиях воздействия неблагоприятных факторов и гибели гепатоцитов (воспаление, лекарственные нагрузки, холестаз) активируется фибро-генез, сопровождающийся повышенным синтезом компонентов экстрацеллюлярного матрикса (ин-терстициальный коллаген, коллаген базальной мембраны, протеогликаны, гликопротеины, такие как ламинин и фибронектин), что в итоге приводит к структурным изменениям и функциональной недостаточности органа [8].
Развитие воспалительной реакции сопровождается гиперпродукцией широкого спектра провоспа-лительных субстанций (цитокинов, эйкозаноидов, оксида азота), которые стимулируют трансформацию звездчатых клеток печени (основные фибро-генные клетки) в миофибробласты [9]. Звездчатые клетки (известные как липоциты, клетки Йю или перисинусоидальные клетки) — это клетки мезен-химального происхождения, в норме выполняющие роль резервуара ретиноидов и регуляторов кровотока. После вовлечения печени в патологический процесс они переходят из состояния покоя (нормы) в активированное (поврежденное) состояние, что приводит к синтезу большого количества нейроэндокринных маркеров, провоспалительных цитокинов, нейтрофильных и моноцитарных хемо-аттрактантов, которые существенно усиливают воспалительную реакцию [10]. Развитие фиброгенеза зависит от длительности воздействия повреждающего фактора, то есть высокой активности аутои-мунного воспаления.
До настоящего времени фиброз печени рассматривался как необратимый процесс, представляющий собой деградацию печеночной паренхимы с замещением ее богатой коллагеном тканью. Однако в последнее время большинство исследователей рассматривают фиброобразование как результат повторяющегося во времени процесса повреждения-восстановления печеночных клеток, а замещение их соединительной тканью — как репаративный процесс, развивающийся в ответ на повреждение гепатоцитов [11]. На обратимость фиброза влияют степень выраженности заболевания, активность макрофагов и тип соединительнотканных образований, расположенных в очагах фиброза. Аутовоспаление является фактором, ускоряющим развитие фиброза, и сроки его формирования при СКВ могут исчисляться в месяцах.
Несмотря на постоянно расширяющийся объем знаний о причинах, механизмах возникновения и прогрессирования заболеваний печени, многие вопросы диагностики данной патологии остаются открытыми. Печень — сложно функционирующий
Вместе с тем анализ литературных данных указывает на недостаточную освещенность вопросов патологии печени при СКВ, особенно в детском и подростковом возрасте. Как в диагностические критерии болезни, так и в индекс повреждения (SLICC/ ACR DAMAGE INDEX, 2010) клинические и лабо-раторно-инструментальные признаки ее повреждения не включены. Однако именно печень, в силу своей компенсаторной способности, является тем скрытым органом-мишенью, где патологические изменения, диагностируемые на стадии биохимических нарушений, сопровождаются и морфологическими, зачастую уже с формированием фиброза. Раннее выявление и оценка характера патологического процесса в печени с выделением ряда лабораторных синдромов, отражающих повреждение гепатоцитов, нарушение поглотительно-экскреторной и синтетической функции печени, степень иммунопатологических расстройств, возможность своевременного адекватного назначения терапевтических мероприятий будут способствовать не только снижению выраженности воспаления, но и уменьшению необратимых изменений в организме больных в целом [12, 13].
Цель исследования: изучение состояния печени у подростков с СКВ на начальных этапах заболевания.
Материалы и методы
Для оценки функционального состояния печени у подростков использовали комплекс клинико-ла-бораторных, биохимических и инструментальных методов исследования (объективный осмотр, ультразвуковое исследование (УЗИ) печени и желчного пузыря, определение уровней билирубина и его фракций, общего холестерина, активности ала-нинтрансферазы, аспартаттрансферазы, щелочной фосфатазы). Рассчитывался коэффициент де Рити-са (отношение АСТ/АЛТ), индекс APRI (Aspartate-aminotransferase-to-Platelet Radio Index) — отношение АСТ к верхней границе ее нормы и к числу тромбоцитов, умноженное на 100.
Статистическая обработка материала проведена с использованием пакета прикладных программ (MS Excel, SPSS). Для оценки достоверности отличий использовался t-критерий Стьюдента (p), наличия взаимосвязей — корреляционный анализ. Критический уровень значимости для проверки статистических гипотез при сравнении групп принимался равным 0,05.
Результаты и их обсуждение
В дебюте СКВ признаки вовлечения печени в патологический процесс отмечены у 11 из 48 больных (22,9 %), что проявлялось увеличением размеров органа и повышением активности трансами-наз. Данную группу составили больные с возрастом дебюта заболевания 14,1 года (169,09 ± 5,91 мес.), средней длительностью СКВ 4,63 ± 1,90 мес., по-дострым вариантом начала (54,5 %) и выраженной активностью патологического процесса (63,6 %).
В клинической симптоматике отмечено наличие кожного (90,9 %) и суставного (81,8 %) синдромов, кардита (54,5 %) с перикардитом (36,4 %), трофических нарушений (45,5 %), гемопатии (36,4 %), люпус-нефрита (27,3 %), поражения центральной нервной системы (18,2 %) и пульмонита (9,1 %). Большинство пациентов (63,6 %) имели высокую степень активности заболевания, у всех больных отмечены повышенные уровни острофазовых показателей. Средние значения скорости оседания эритроцитов составили 38,90 ± 2,27 (25—72) мм/час, С-реактивного белка (СРБ) — 24,9 ± 1,1 (24-96) г/л, серомукоида — 0,216 ± 0,170 (0,245-0,592), сиало-вых кислот — 163,36 ± 0,17 (133-280) и гликопроте-идов — 0,405 ± 0,160 ед. (0,335-0,645). Уровни всех изучаемых маркеров воспаления были достоверно выше (р Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
13. Poynard T., Morra R., Ingiliz P. Biomarkers ofliverfibrosis// Adv. Clin. Chem. — 2008. — Vol. 46, № 1. — P. 131-160.
14. Petri M. et al. Derivation and Validation of the Systemic Lupus International Collaborating Clinics Classification Criteria for Systemic Lupus Erythematosus//Arthr. Rheum. — 2012. — № 64. — P. 2677-2686.
15. Международная классификация функционирования, ограничений жизнедеятельности и здоровья: Пер. Г.Д. Шостка, В.Ю. Ряснянского, А.В. Квашина и др. — ВОЗ: Женева, 2001. — 342 с.
16. Volynets G.V., Potapov A.S., Polyakova S.I. et al. Evaluation of liver failure stage in children // Voprosy sovremennoi pediatrii — Current Pediatrics. — 2013. — № 12. — P. 47-51.
ураження печшки при системному червоному
вовчаку у тдл1тюв
Резюме. Метою дослщження було вивчення стану пе-чшки у тдлггшв 1з системним червоним вовчаком (СЧВ). У результата обстеження 48 хворих на СЧВ вжом 12—18 рошв встановлено частоту ураження печшки (22,9 %), взаемозв'язок розвитку цитсшзу з1 ступеней активносй та клтчними проявами захворювання, частоту ризику розвитку ф1брозу (27,3 %) 1 його ймов1рну наявшсть у 9,1 % шдли-шв у дебюта СЧВ.
Ключовi слова: системний червоний вовчак, п1дл1тки, печшка, ф1брогенез.
liver damage in systemic lupus erythematosus in adolescents
Summary. The objective of the study was to investigate the state of the liver in adolescents with systemic lupus erythematosus (SLE). As a result of examination of 48 patients with SLE aged 12—18 years, there were established incidence of liver damage (22.9 %), correlation of cytolysis with the degree of activity and clinical manifestations of the disease. Also, the incidence of the risk of fibrosis (27.3 %) and its possible presence in 9.1 % of adolescents in the onset of SLE were detected.
Key words: systemic lupus erythematosus, adolescents, liver, fibrogenesis.
Поражения печени при системных заболеваниях соединительной ткани
В статье представлены данные о поражениях печени при системных заболеваниях соединительной ткани, что следует учитывать при назначении лечения таким больным.
Печень, системные заболевания, печеночные ферменты.
Очень часто причиной поражения печени при системных заболеваниях соединительной ткани является сердечная недостаточность. Также нередко первичный билиарный цирроз печени сочетается с системными заболеваниями соединительной ткани.
В биохимическом анализе крови возможно повышение уровней a- и b-глобулинов, снижение уровня альбумина в сыворотке. Уровень билирубина, активность трансаминаз и щелочной фосфатазы (ЩФ) в сыворотке крови обычно в пределах нормы или слегка повышены.
При узелковом периартериите в артериолах печени наблюдаются типичные для этого заболевания изменения, иногда с развитием небольших инфарктов. Диагностическое значение имеет артериография печени, которая может выявить артериальные аневризмы. Заболевание может осложняться узловой регенераторной гиперплазией.
Само по себе носительство HBV может сопровождаться развитием узелкового периартериита, протекающего с мигрирующими артралгиями или полимиозитом. В тканях при этом выявляют иммунные комплексы, содержащие HBsAg.
В литературе описано сочетание гигантоклеточного артериита с гранулематозными заболеваниями печени и печеночным артериитом.
При ревматической полимиалгии в биоптатах печени находят фокальные некрозы гепатоцитов, портальные воспалительные инфильтраты и небольшие рассеянные эпителиоидные гранулемы. У ряда больных обнаруживают повышение ЩФ и/или трансаминаз. Под влиянием терапии стероидами эти изменения обычно подвергаются обратному развитию.
При ревматоидном артрите в печени выявляют неспецифические изменения: умеренную жировую инфильтрацию, очаговые некрозы, расширение синусоидов, иногда амилоидоз. Отмечается гиперплазия клеток Купффера. При биохимическом исследовании крови повышается активность ЩФ при нормальных значениях активности сывороточных трансаминаз и уровня билирубина.
Вследствие инфильтрации синусоидов лимфоцитами и узловой регенераторной гиперплазии возможно развитие портальной гипертензии и кровотечения из варикозно расширенных вен пищевода при синдроме Фелти.
При смешанной криоглобулинемии отмечаются гепатомегалия и повышение активности печеночных ферментов. При гистологическом исследовании биоптатов печени обнаруживаются умеренные неспецифические изменения, иногда выявляется хронический активный гепатит и даже цирроз. У части больных выявляются маркеры вирусов гепатитов В и С. Кроме того, смешанная криоглобулинемия может развиться на фоне острого и хронического гепатита и первичного билиарного цирроза печени.
При болезни Вебера — Крисчена можно выявить значительные жировые изменения и гиалиновые тельца Мэллори. Эти изменения обусловлены снижением синтеза белка в деформированной шероховатой эндоплазматической сети.
Более подробно в литературе описано поражение печени при системной красной волчанке (СКВ).
Примерно у четверти больных с СКВ отмечается субклиническое поражение печени, о чем свидетельствует повышение активности печеночных ферментов в сыворотке, но только у 8 % больных поражение печени не удается объяснить никакой другой причиной, кроме непосредственно СКВ. При биопсии печени значительных изменений не выявляют; имеются редкие описания картины хронического активного гепатита. Желтуха при СКВ обычно обусловлена гемолизом.
В настоящее время доказано, что так называемый люпоидный (аутоиммунный) хронический гепатит, относящийся к хроническим заболеваниям печени, не является проявлением СКВ.
Проявления поражения печени при СКВ варьируют от незначительного увеличения ее размеров до довольно тяжелого гепатита. По данным разных авторов, гепатомегалия выявляется в 23–50 % случаев, при этом желтуха наблюдается лишь в 3–7 % случаев. В то же время нередко повышаются уровни АСТ и АЛТ. При гистологическом исследовании биоптата печени наиболее часто выявляют стеатоз, реже — неспецифическое воспаление портальных трактов, лобулярные инфильтраты, узелковую регенераторную гиперплазию, артериит, цирротическую трансформацию. Иногда выявляют артериит, приводящий к инфарктам печени, спонтанным разрывам, обусловливающим картину острого живота.
Собственно волчаночный гепатит следует дифференцировать от хронического активного гепатита (ХАГ). При сходной симптоматике имеются и различные особенности. Так, при ХАГ диарея встречается в 30 % случаев и лишь в 5 % случаев — при СКВ, гепатомегалия при ХАГ выявляется в 75 % и спленомегалия — в 50 % случаев, при СКВ — в 20 % случаев. Для ХАГ более характерны такие признаки, как желтуха (в 80 % случаев), повышение уровня АСТ, АЛТ (в 90 % случаев) и ЩФ (в 50 % случаев), гипергаммаглобулинемия (в 60 % случаев). В то же время наиболее часто встречающиеся при СКВ LE-клетки (в 75 % случаев), высокий титр антинуклеарного фактора (в 90 % случаев) при ХАГ выявляют в 15 и 40 % случаев соответственно. Антитела к нативной ДНК при СКВ выявляются в 45 % случаев, а при ХАГ они отсутствуют. Антитела к гладкой мускулатуре при ХАГ выявляются в 70 % случаев, а при СКВ они отсутствуют.
Также можно отметить, что при ХАГ редко встречаются полисерозит, гломерулонефрит, поражение ЦНС, а эритематозные высыпания, вульгарные угри, пурпура и витилиго могут наблюдаться достаточно часто. Для обоих заболеваний характерны лейкопения, тромбоцитопения, положительная проба Кумбса. Для уточнения диагноза, особенно если клинически и лабораторно не удается провести дифференциальный диагноз, следует проводить биопсию печени.
Не стоит забывать и о возможности вирусного гепатита. Однако патология печени у больных СКВ на высоте активности болезни, как правило, связана с самим заболеванием.
Поражение печени при системной склеродермии до недавнего времени считалось малоизученным, поскольку относительно незначительные симптомы обычно маскируются более выраженными проявлениями поражения пищевода, дистальных фаланг пальцев рук и ног, часто протекающими с некротическими изменениями кожи и подкожной жировой клетчатки, изменениями кожи лица со склерозированием и натяжением, особенно вокруг рта, что, помимо неприятного, болезненного внешнего вида (нередко очень беспокоящего больных, особенно молодых женщин), порой приводило к значительному ограничению открывания рта, а также многими другими проявлениями этой системной болезни. Такие изменения лабораторных показателей, как увеличение СОЭ, положительные показатели белковоосадочных проб, которые раньше проводились достаточно широко (тимоловая, формоловая, золотоколлоидная и др.), в большей степени свидетельствовали об активности склеродермического процесса, чем о печеночной патологии. У некоторых больных удавалось пропальпировать увеличенную печень и селезенку, но при индуративном отеке кожи живота пальпация значительно затруднена. З.Г. Апросиной и соавт. (1970) при целенаправленном изучении состояния печени те или иные признаки ее вовлечения в патологический процесс были выявлены у 78 из 180 наблюдавшихся больных. Морфологическое исследование (19 патологоанатомических исследований и 11 биопсий), проведенное в данной работе, выявило фиброз портальной стромы, сосудов, перидуктальный и периваскулярный фиброз, признаки жировой дистрофии и некроза гепатоцитов (в ряде случаев отмечался субмассивный некроз, особенно при остром и подостром течении склеродермии). Обнаружены также фиброзные изменения капсулы печени и склеротические изменения стенки желчного пузыря. Таким образом, поражение печени может быть весьма серьезным. Следует иметь в виду, что повреждение печени обычно сопровождается более или менее значительными нарушениями ее участия во всех видах обмена: белкового, жирового и углеводного; страдает детоксикационная функция печени, нарушается синтез протромбина, фибриногена и других факторов свертывания крови и т.п. Эти изменения гомеостаза, в свою очередь, отражаются на функции и других органов. Наиболее часто у больных системной склеродермией повышается активность экскреторных ферментов (g-глютамилтранспептидазы и лейцинаминопептидазы), а также активность глутаматдегидрогеназы, свидетельствующей о нарушении обменных процессов и некрозе гепатоцитов. Это подтверждает имеющиеся в литературе данные, что в основе поражения печени при системной склеродермии лежат разрастание соединительной ткани с утолщением стенок желчных протоков и портальных трактов, а также жировая дистрофия и некроз гепатоцитов. Указанные ферменты должны быть использованы для выявления поражения печени на ранних стадиях и для динамического наблюдения за состоянием печени у больных с любой стадией системной склеродермии.
При синдроме Шегрена поражение печени встречается у 5–10 % пациентов и характеризуется незначительным увеличением ее размеров, повышением уровня печеночных ферментов, щелочной фосфатазы (у 70 % пациентов), выявлением антимитохондриальных антител (у 5 % пациентов). Морфологическую основу поражения печени составляют перидуктально расположенные лимфоплазмоцитарные инфильтраты, сдавливающие протоки. При обнаружении повышенного уровня печеночных ферментов необходимо проведение дифференциальной диагностики с хроническим гепатитом и первичным билиарным циррозом печени. Изменения гепатобилиарной системы, по-видимому, в большой степени отражают участие печени и желчевыделительной системы в аутоиммунных процессах. Частота клинических проявлений поражения печени при синдроме Шегрена, по данным разных авторов, варьирует в широких пределах — от 6 до 72 %. Клинические признаки характеризуются гепатомегалией в 11–42 % случаев, умеренным повышением уровня печеночных ферментов в 5–24 % случаев, билирубина — в 10 % случаев. У 7 % больных обнаруживаются антимитохондриальные антитела. Маркеры вирусного гепатита В и С не выявляются при отсутствии в анамнезе указаний на перенесенный вирусный гепатит. По данным Т.Н. Лопаткиной (1980), при гистологическом исследовании те или иные изменения печени обнаруживаются у всех больных с синдромом Шегрена. Морфологическая картина печени характеризуется тремя типами изменений: 1) картиной хронического гепатита (в 33 % случаев); 2) различными видами дистрофии гепатоцитов и умеренной лимфогистиоцитарной инфильтрацией портальных трактов (в 50 % случаев); 3) только дистрофическими изменениями гепатоцитов (в 17 % случаев). Для всех типов изменений характерны реакция со стороны звездчатых ретикулоэндотелиоцитов и пролиферация холангиол. Морфологические изменения печени у больных с синдромом Шегрена, в сыворотке крови которых обнаруживаются антимитохондриальные антитела, соответствуют картине начальной стадии первичного билиарного цирроза печени. Сочетание синдрома Шегрена и хронических воспалительных заболеваний печени известно давно и хорошо доказано. Наиболее часто, в 69–100 % случаев, синдром сочетается с первичным билиарным циррозом, в 35–51 % случаев — с хроническим активным гепатитом.
Следует также помнить и о том, что поражение печени с повышением активности АСТ и АЛТ может быть обусловлено приемом лекарственных препаратов (в первую очередь ацетилсалициловой кислоты, которая гепатотоксична у 25 % больных, а также циклофосфамида и др.), применяемых для лечения системных заболеваний.
Таким образом, за последние годы получены новые данные о поражениях печени при системных заболеваниях соединительной ткани, что следует учитывать при назначении лечения таким больным.
Поражение селезенки и печени при системной красной волчанке, нередко выступающие в виде гепатолиенального синдрома, представляют важную сторону патологии — участие органов ретикулоэндотелиальной системы в этом сложном заболевании.
В то же время патология печени при системной красной волчанке имеет и другие аспекты: прежде всего это поражение паренхиматозной ткани с развитием дистрофических и воспалительных изменений, особенно жировой печени, воспалительного паренхиматозного, или диффузного, гепатита (паренхиматозной желтухи), и, возможно, даже цирроза.
У больных системной красной волчанкой печень остается при этом увеличенной (большая жирная печень), и непосредственной причиной смерти являются, как правило, поражения других органов — нередко многочисленные.

В качестве примера можно привести следующую историю болезни.
У больного 21 года после инсоляции развилась картина типичной системной красной волчанки с болями в суставах, лихорадкой, увеличением лимфатических узлов (полиадения) и печени. Лечение АКТГ привело к улучшению. Однако с прекращением лечения началось обострение с клинической картиной волчаночного кардита, полисерозита и нефрита. После длительного лечения кортизоном развилась ремиссия, и последующие 3 года, когда применялись поддерживающие дозы кортизона по 25 мг в сутки, больного беспокоил главным образом кожно-суставной синдром. Затем больной без врачебного контроля стал принимать по 200 мг кортизона (в течение 2 месяцев) и был доставлен в клинику в тяжелом состоянии с лихорадкой до 40°, кровавой рвотой, затемненным сознанием, низким артериальным давлением, слабым частым пульсом, увеличенной печенью. В последующие 4 дня отмечалось прогрессивное ухудшение состояния: повторно кровавая рвота, желтуха, возбуждение, высокая лихорадка, в крови повышенный уровень прямого билирубина (1,7 мг %), резкое изменение осадочных глобулиновых проб, азотемия (остаточный азот 156 мг %), далее пневмония и смерть.
Анатомический диагноз: системная красная волчанка, длительно леченная кортизоном; геморрагическая пневмония нижней доли левого легкого; склероз митрального и трехстворчатого клапанов; облитерация плевральных и перикардиальной полостей; спайки в брюшной полости; очаговый нефрит, гиперплазия лимфатических узлов; красная атрофия печени, желтуха; кровоточащие эрозии желудка; резкая дистрофия миокарда.
Гистологически в печени выявлены обширные очаги некроза; клетки печени видны лишь в виде отдельных островков неправильной формы с тяжелыми дистрофическими изменениями в протоплазме; в строме круглоклеточная инфильтрация, стенки артерий с явлениями фибриноидного некроза, местами видны расширенные, полнокровные капилляры.
Собственно волчаночный гепатит с желтухой, увеличенной, обычно нерезко, и чувствительной печенью, нередко с одновременным набуханием селезенки течет циклически, сопутствуя, как правило, одному из обострений системной красной волчанки, протекающих с такими характерными проявлениями, как ускоренная РОЭ, выраженная лейкопения, повышение уровня фибриногена и т. д.
Волчаночный гепатит может привести к циррозу печени. Следует подчеркнуть, что последний констатируют у больных системной красной волчанкой прижизненно (или на секции) и при отсутствии в анамнезе желтухи.
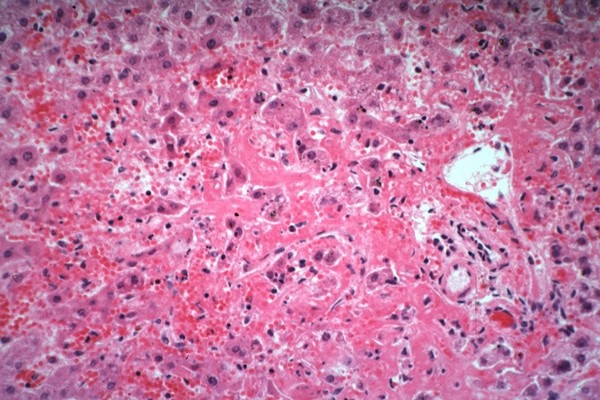
Микропрепарат поражения печени при СКВ
В одном из наблюдений Тареева Е.М. у больной с хроническим течением системной красной волчанки, со стойким кожно-суставным синдромом, периодически рецидивирующим лимфаденитом и энцефалитом при постоянной лейкопении имелась желчнокаменная болезнь, вызвавшая необходимость из-за участившихся обострений холецистэктомии.
Перечисление возможных поражений печени было бы неполным, если не упомянуть также септические заносы в печень, бактериальную инфекцию желчных путей, кандидоз печени и другие инфекционные осложнения.
В наблюдениях Тареева Е.М. ранней серии у 36 из 50 больных печень была умеренно увеличена. Из 29 секционных случаев в 22 наблюдались мелко- или крупнокапельное ожирение печеночных клеток, в 6 — мускатная печень, в одном — амилоидная дистрофия.
При гистологическом исследовании печени в ряде случаев обнаруживались гиалиноз мелких артерий, лимфоидные скопления в межуточной ткани и в строме по ходу воротной вены, утолщение стенок центральной вены, склероз капсулы и перипортальный склероз, некроз печеночных клеток.
Гепатомегалию Тареев Е.М. и его коллеги наблюдали лишь у 3 больных: у одного был волчаночный желтушный гепатит, напоминавший болезнь Боткина, у другого — застойная печень, у третьей больной в одну из волчаночных атак констатировано преходящее увеличение печени, достигавшей пупка.
Klemperer и соавторы (1941) наблюдали хронический фиброзный гепатит и фибринозный периспленит у 12-летней больной системной красной волчанкой.
О начальном циррозе наряду с диффузным ожирением и аденоматозом печени у 16-летней девушки, страдавшей туберкулезом и погибшей от системной красной волчанки, сообщил И.В. Давыдовский (1941); микроскопически было обнаружено крупноклеточное ожирение и многочисленные круглоклеточные инфильтраты с некробиозом в центре.
Harvey наряду с часто наблюдаемой жировой печенью с атрофией и некрозом центральных печеночных клеток отмечал следующую патологию:
- поражение сосудов в портальных пространствах — в 2 случаях,
- портальный цирроз — в 3,
- казеозные бугорки печени — в 2,
- желтуху — в 4 случаях, из них в 2 — гемолитическую желтуху,
- в одном — на почве эпидемического гепатита.
Среди гистологических находок автор называет также своеобразный отек желчных протоков, пузыря, фатерова соска с закупоркой желчных и панкреатических протоков.
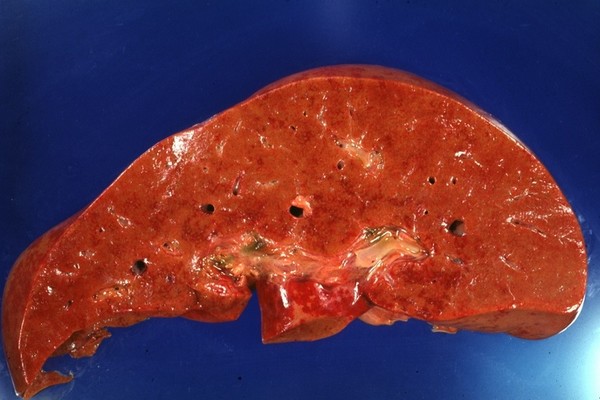
Макропрепарат поражения печени при СКВ
Частота поражения печени и симптоматика этого поражения хорошо иллюстрируются следующими литературными данными.
Из 27 больных Г.А. Раевская нашла увеличение печени у 14; из 9 секционных случаев в 4 обнаружена жировая печень, в 5 — изменения сосудов и склероз их, в 2 — инфильтраты в глиссоновой капсуле.
По наблюдениям Тареева Е.М. (1965) увеличение печени различной степени отмечается не столь редко: у 72 из 100 больных.
Отчетливые изменения функциональной деятельности печени определяются при системной красной волчанке нечасто. Имеет значение билирубинемия за счет прямой фракции пигмента, нарушение выделения желчных кислот, гипопротромбинемия (при гепатите и циррозе), гипоальбуминемия. Harvey отметил задержку бромсульфалеина у 5 из 16 исследованных больных.
Тем не менее именно значительная выраженность глобулиновых сдвигов и аналогичных показателей наряду с более характерными для системной красной волчанки иммунологическими данными привела к попытке сближения волчаночных гепатитов (lupus hepatitis, люпус гепатит, hepatitic lupus — Joske и King, 1955) с хроническим гепатитом (чаще у молодых лиц) иной природы, в частности, вирусной (lupoid hepatitis — МасКау и соавторы, 1956).
Увеличение печени при активной системной красной волчанке не сопровождается какими-либо субъективными жалобами или особенностями пальпаторных данных. Печень остается эластической консистенции, нечувствительной к пальпации, равномерно увеличенной. Такого рода увеличение печени, как и увеличение селезенки, чаще всего оказывается неожиданной находкой при систематическом обследовании больных.
Читайте также:


