Острый гломерулонефрит при стрептококковой инфекции
ТОНЗИЛЛИТ (АНГИНА) И ЧЕМ ОН ОПАСЕН ДЛЯ ПОЧЕК?!
Острый тонзиллит (в повседневной жизни ангина) — инфекционное заболевание с местными проявлениями в виде острого воспаления нёбных миндалин, вызываемое чаще всего стрептококками или стафилококками, реже другими микроорганизмами. Ангиной также называют обострение хронического тонзиллита.
ЧТО ТАКОЕ СТРЕПТОКОКК?
Бета-гемолитический стрептококк из группы А (лат. Streptococcus pyogenes) это весьма распространенный микроб (бактерия), который может быть выявлен в организме многих здоровых людей, однако при неблагоприятных условиях он может провоцировать боли в горле, ангину (острый тонзиллит), скарлатину, инфекции кожи, образование нарывов, заражение крови и осложнения в виде острого ревматизма и ОСТРОГО ГЛОМЕРУЛОНЕФРИТА.
КАК ПРОИСХОДИТ ЗАРАЖЕНИЕ СТРЕПТОКОККАМИ?
В ходе эпидемиологических исследований было установлено, что бета-гемолитический стрептококком заражено до 20% здоровых детей, которые являются носителями этого микроба.
Чаще всего бета-гемолитический стрептококк передается через частички слизи, которые выделяются из горла и носа заболевшего человека (или носителя) во время кашля или чихания.
СТРЕПТОКОКК ПРИЧИНА МНОГИХ ЗАБОЛЕВАНИЙ:
В наши дни стрептококки вызывают интерес преимущественно из-за редких случаев быстро прогрессирующей болезни, а также риска серьезных осложнений при не вылеченных инфекциях.
Острая инфекция стрептококка может проявиться в виде фарингита (острый фарингит), скарлатины (сыпь), импетиго (инфекция поверхностных слоев кожи) или целлюлит (инфекция глубоких слоев кожи). Агрессивная, токсигенная инфекция может привести к некротизирующему фасцииту, миозиту и синдрому стрептококкового токсина шока. У пациентов после острой стрептококковой инфекции могут также развиться иммунно-обусловленные постстрептококковые осложнения, такие как острый ревматизм и острый гломерулонефрит.
ПОЗДНИЕ ОСЛОЖНЕНИЯ СТРЕПТОКОКОККОВОЙ ИНФЕКЦИИ (ИММУННО-ОБУСЛОВЛЕННЫЕ)
РАССМОТРИМ КАК МОЖНО ЗАПОДОЗРИТЬ ОСТРЫЙ ГЛОМЕРУЛОНЕФРИТ:
Если заметите, что через несколько недель после перенесенной ангины (скарлатины, фарингита) у него появились следующие симптомы:
- Появились отеки лица, пастозность век или в другой области тела или ребенок стал редко мочится.
- Моча приобрела темно-красную (бордовую) окраску (цвет мочи мясных помоев)
Другими симптомами могут быть повышение температуры, слабость, озноб, сильная головная боль.
ЕСЛИ ВЫ ЗАМЕТИТЕ ТАКИЕ СИМПТОМЫ, НЕМЕДЛЕННО ОБРАТИТЕСЬ К ВРАЧУ!
В любом случае всем детям и взрослым, заболевшие ангиной, фарингитом или скарлатиной у которых анализы выявили бета-гемолитического стрептококка из группы А должно проводится лечение антибиотиками.
Лечение должно быть начато как можно скорее (это необходимо для предотвращения образования нарывов в горле или распространения инфекции на соседние органы), а также развития поздних осложнения на сердце, почек и суставов.
Если у вас возникли вопросы по данной теме, мы постараемся на них ответить.
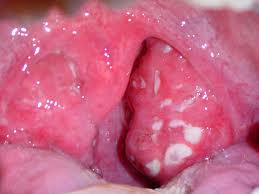
Поражение небных миндалин при остром тонзиллите (гипертрофия (увеличение размера) небных миндалины, налеты)
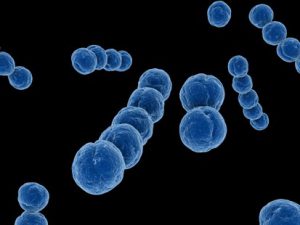
Бета-гемолитический стрептококк из группы А (лат. Streptococcus pyogenes) это весьма распространенный микроб (бактерия), который может быть выявлен в организме многих здоровых людей
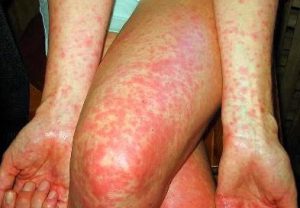
Скарлатина — острое инфекционное заболевание, характеризующееся лихорадкой, интоксикацией, ангиной и обильной точечной сыпью. Болеют чаще всего дети 2-10 лет. Возбудителем скарлатины является стрептококк группы А.


Острый гломерулонефрит - тяжелое поражение структуры почечных клубочков, развивающееся вследствие перенесенной стрептококковой инфекции, вызванной в основном, штаммами М серотипов 1, 2, 4, 12, 18, 25, 49, 55, 57, 60 и некоторых других М-типов стрептококка группы А. Общепринятым является мнение об остроте процесса, однако заболевание может иметь хроническое течение, нередко приводить к дисфункции почек (альбуминурия и снижение скорости клубочковой фильтрации могут сохраняться у перенесших острый гломерулонефрит пожизненно), что позволяет рассматривать его в ряду причинных факторов хронической болезни почек [4]. В настоящее время диагноз острый постстрептококковый гломерулонефрит реже ставится в специализированных нефрологических отделениях, хотя по-прежнему наблюдаются и спорадические случаи, и эпидемические вспышки данного заболевания [2,6,7].
Создание экспериментальных моделей острого гломерулонефрита необходимо не только для дальнейшего изучения механизмов пато- и морфогенеза заболевания, но и для доклинической апробации новых лекарственных препаратов, предлагаемых фармацевтической промышленностью и обладающих нефропротективным действием.
Материалы и методы исследования:
Животные были разделены на 2 экспериментальные группы: I группа - контрольная (интактные животные), n=10; II группа (опытная) - животные, иммунизированные бактериальной суспензией эталонного штамма Streptococcus pyogenes (ГНИИ стандартизации и контроля им. Л. А. Тарасевича), n=16. С целью подтверждения воспроизводимости эксперимента II группа была подразделена на 2 подгруппы, различающиеся сроком забора мочи для лабораторного исследования и органов для аутопсии и гистологического анализа (21 и 31 день иммунизации).
Антигенную суспензию для иммунизации животных получали путем культивирования штамма на мясопептонном бульоне в аэробных условиях при температуре +370С, последующем центрифугировании суточной бульонной культуры Streptococcus pyogenes в течение 10-15 минут при скорости 3000 оборотов в минуту и последующем удаления супернатанта. Полученную взвесь концентрацией 109 КОЕ / мл, определяемой на КФК-3 (оптическая плотность 0,028, длина волны 540 нм, кювета - 1,060 мм), инактивировали при +56 ºС в течение 30 минут. Из расчета 50 мкл взвеси на 1 животное готовили разведение: 9 мл стерильного физиологического раствора и 1 мл взвеси (на 1 животное приходится 500 мкл (0,5 мл) полученной вновь взвеси антигенной суспензии). Иммунизацию животных проводили внутрибрюшинно 1 раз в день по схеме: 3 цикла, каждый из которых состоял из 1, 3, 5 дней иммунизации и 2 дней перерыва между циклами.
Результаты исследования
У животных контрольной группы не было выявлено лабораторных и гистологических признаков развития острого гломерулонефрита. В течение всего эксперимента в моче животных этой группы белок не выявлялся, в микроскопии мочевого осадка патологии не обнаружено.
При проведении аутопсии почки животных контрольной группы имели бобовидную форму, капсула легко снималась, обнажая блестящую, гладкую поверхность светло-коричневого цвета. На разрезе корковое вещество почек было светло-коричневого цвета, мозговое вещество - темно-красное. Лоханка не расширена, ее слизистая оболочка блестящая, гладкая. При проведении гистологического исследования строение ткани почек соответствовало нормальному: четко выявлялась капсула, корковое вещество с почечными тельцами и извитыми канальцами, мозговое вещество, визуализировались сосочки и почечная лоханка, выстланная переходным эпителием. Сосудистые клубочки нефрона не изменены. Проксимальные и дистальные почечные канальцы с типичной структурой.
У иммунизированных животных II группы к 21 дню иммунизации визуально отмечалось снижение аппетита и двигательной активности. У 90 % животных при проведении микроскопии мочевого осадка выявили гематурию - от незначительной до средней степени выраженности, исследование мочи на содержание белка показало положительный результат у 80 % животных.
На секции отмечались макроскопические признаки застойной сердечной недостаточности: общее венозное полнокровие; увеличение печени (печень плотная, тёмная); инъецированность сосудов брыжейки, имелись небольшие кровоизлияния.
С целью подтверждения воспроизводимости модели острого гломерулонефрита забор материала у 8 животных II группы осуществляли на 21 день эксперимента. При проведении аутопсии почки иммунизированных животных имели бобовидную форму, были увеличены в размерах, выглядели набухшими. На разрезе корковое вещество имело серовато-коричневый цвет, мозговое вещество - вишнево-красный; лоханка не изменена. При проведении микроскопии гистологических препаратов в ткани почек выявлялось полнокровие сосудов коркового и мозгового вещества, в корковом веществе визуализировалось большое количество увеличенных гиперцеллюлярных клубочков с резко уменьшенным мочевым пространством, инфильтрированных нейтрофильными гранулоцитами, эозинофилами и лимфоцитами, с аккумуляцией большого числа моноцитов в просветах капилляров. Выявленные изменения характеризовали в этом сроке экссудативную фазу воспаления и были выражены не менее чем в 60 % клубочков, выявляемых в гистологическом срезе. Отмечалось сужение просветов капилляров клубочков вследствие пролиферации эндотелиальных и мезангиальных клеток, появление клубочков с лобулярной структурой. В проксимальных и дистальных канальцах нефронов изменения канальцевого эпителия были выражены умеренно (выявлялись участки белковой дистрофии эпителия, в интерстициальной ткани почек - участки воспалительной инфильтрации лимфоцитами, нейтрофилами и макрофагами) и имели очаговый характер.
У всех животных II группы к 31 дню иммунизации при свободном доступе к пище и воде отмечалось значительное снижение аппетита и потребности в жидкости, а также резкое снижение суточного диуреза по сравнению с контрольной группой. При проведении микроскопии мочевого осадка выявляли гематурию средней степени выраженности, содержание белка показало положительный результат у 100 % животных.
При проведении аутопсии у 8 иммунизированных животных II группы на 31 день эксперимента макроскопически имелись признаки отёка почечной ткани, изменения в лоханках отсутствовали. Гистологическое исследование ткани почек животных этой группы выявило в большинстве клубочков (80 %) преобладание процессов пролиферации, что выражалось в появлении, наряду с мезангиальной и эндотелиальной пролиферацией, отложений нитей фибрина и белковых масс в капсуле Шумлянского-Боумена, сращении капилляров клубочка с капсулой и образовании полулуний в отдельных клубочках. Отмечался также тромбоз капилляров почечных телец. Гломерулярная базальная мембрана визуально выглядела значительно утолщенной. В проксимальных и дистальных извитых канальцах находили белковую дистрофию эпителия, в межуточной ткани почек - воспалительную инфильтрацию нейтрофильными гранулоцитами и лимфоцитами.
Таким образом, в гистологических препаратах почек иммунизированных животных наблюдалась морфологическая картина, соответствующая патоморфологическим изменениям, характерным для
- Бурова Л. А. Способность стрептококков группы А типа М12 связывать иммунные комплексы и их роль в патогенезе постстрептококкового гломерулонефрита / Л. А. Бурова, Е. А. Гаврилова. П. В. Пигаревский, В. Г. Селиверстова, В. А. Нагорнев, К. Шален, Артем А. Тотолян // Медицинская иммунология. - 2006. - Т. 8, № 5-6. - С. 623-630.
- Acute post-streptococcal glomerulonephritis in children of French Polynesia: a 3-year retrospective study / O. Becquet, J. Pasche, H. Gatti, C. Chenel, M. Abély, P. Morville, C. Pietrement// Pediatr. Nephrol. - 2010. - Vol. 25, № 2. - P. 275-280.
- Cunningham, M. W. Pathogenesis of group A streptococcal infections / M. W. Cunningham// Clin. Microbiol. Rev. - 2000. - Vol. 13. - P. 470-511.
- Acute postinfectious crescentic glomerulonephritis: clinicopathologic presentation and risk factors / A. A. El-Husseini, H. A. Sheashaa, A. A. Sabry, F. E. Moustafa, M. A. Sobh // Int. Urol. Nephrol. - 2005. Vol. 37, № 3. - P. 603-609.
- Garnier, A, Postinfectious acute glomerulonephritis / A. Garnier, M. Peuchmaur, G. Deschênes // Nephrol Ther. - 2009. Vol. 5, № 2. - P. 97-101.
- Jankauskiene, A. Postinfectious glomerulonephritis in children in Lithuania during 1995-2004: prevalence and clinical features / A. Jankauskiene, B. Pundziene, R. Vitkevic // Medicina (Kaunas). - 2007. Vol. 43, № l. - P. 16-22.
- Wong, W. Outcome of severe acute post-streptococcal glomerulonephritis in New Zealand children / W. Wong, M. C. Morris, J. Zwi // Pediatr. Nephrol. - 2009. Vol. 24, № 5. - P. 1021-26.
(ПИГН; постстрептококковый гломерулонефрит; нестрептококковый ПИГН)
, MD, MHS, Loma Linda University School of Medicine
Last full review/revision January 2018 by Navin Jaipaul, MD, MHS




Этиология
Постинфекционный гломерулонефрит (ПИГН), нефритический синдром, является самой частой причиной гломерулярных заболеваний у детей в возрасте 5–15 лет; реже встречается у детей 2 лет и у взрослых > 40 лет.
Приблизительно у 5–10% пациентов со стрептококковым фарингитом и примерно у 25% с импетиго развивается ПИГН. Большинство случаев вызвано нефритогенными штаммами бета-гемолитического стрептококка группы А, особенно типом 12 (возбудителем фарингита) и типом 49 (возбудителем импетиго). Латентный период обычно составляет 6–21 день от инфекцирования и до начала ГН, но этот период может продлиться до 6 нед.
Менее распространенные патогены: нестрептококковые бактерии, вирусы, паразиты, риккетсии и грибы ( Причины гломерулонефрита). Септический эндокардит и инфекция предсердно-желудочкового шунта – другие важные причины развития постинфекционного гломерулонефрита; желудочково-перитонеальные шунты более устойчивы к инфекции.
Механизм заболевания неизвестен, но считают, что микробные антигены связываются с гломерулярной базальной мембраной, и в первую очередь активизируют альтернативный путь комплемента как непосредственно, так и опосредованно – через взаимодействие с циркулирующими антителами, вызывая повреждение гломерул, которое может быть очаговым или диффузным. В качестве альтернативы циркулирующий иммунный комплекс может оседать на гломерулярной базальной мембране.
Клинические проявления
Симптомы варьируют от бессимптомной гематурии (около 50% случаев) и умеренной протеинурии до сформированного нефрита с микрогематурией или макрогематурией (бурая моча, цвета кока-колы, дымчатого оттенка или алая кровь в моче), протеинурией (иногда нефротического уровня), олигурией, отеками, артериальной гипертензией и почечной недостаточностью. Лихорадка не характерна и свидетельствует о персистирующей инфекции.
Почечная недостаточность, вызывающая задержку жидкости с сердечной недостаточностью и тяжелой гипертензией, требующей диализа, развивается у 1–2% пациентов и может проявляться легочно-почечным синдромом с гематурией и кровохарканьем.
В редких случаях, нефротический синдром может сохраняться после разрешения тяжелого заболевания.
Клинические проявления нестрептококкового ПИГН могут имитировать другие заболевания (например, узелковый полиартериит, эмболию почечной артерии, антимикробный лекарственно-индуцированный острый интерстициальный нефрит).
Диагностика
Клинические признаки недавней инфекции
Анализ мочи, как правило, демонстрирующий измененные формы эритроцитов, эритроцитарные цилиндры, протеинурию, лейкоциты, а также клетки почечных канальцев
Наличие стрептококкового ПИГН предполагают на основании анамнеза фарингита или импетиго и типичных симптомов ПИГН или случайно выявленных отклонений анализа мочи. Обнаружение гипокомплементемии существенно подтверждает это.
Исследования, необходимые для подтверждения диагноза, зависят от клинической картины. В серологических исследованиях обычно определяется антистрептолизин-О, антигиалуронидаза и антидезоксирибонуклеаза (анти-ДНКаза). Также обычно исследуются уровни сывороточного креатинина и комплемента (С3 и общая гемолитическая активность комплемента); однако у пациентов с типичными клиническими симптомами некоторые исследования можно не проводить. В ряде случаев проводят другие исследования. Биопсия подтверждает диагноз, но необходимость в ней возникает редко.
Антистрептолизин-О – самый распространенный тест недавней стрептококковой инфекции – увеличивается и остается повышенным в течение нескольких месяцев в целом у 75% пациентов с фарингитом и примерно у 50% пациентов с импетиго, но не является специфичным. Стрептозимовая проба, которая дополнительно измеряет антигиалуронидазу, антидеоксирыбонуклеазу и другие титры, обнаруживает 95% недавних стрептококковых фарингитов и 80% кожных инфекций.
Анализ мочивыявляет протеинурию (0,5–2 г/м 2 /день), дисморфные эритроциты, лейкоциты, клетки почечных канальцев, а также, возможно, эритроцитарные, лейкоцитарные и зернистые цилиндры. Соотношение содержания белка к креатинину в моче в случайном образце обычно находится в рамках 0,2-2 (норма 0,2), но иногда может быть в нефротическом диапазоне (≥ 3).
Уровень креатинина сыворотки крови может быстро повышаться, но обычно его пик ниже уровня, требующего диализа.
Концентрации СЗ и общей гемолитической активности комплемента (CH50) падают во время активной фазы болезни и возвращаются к норме в течение 6–8 недель у 80% пациентов с постинфекционным гломерулонефритом. Концентрации уровней C1q, С2 и С4 только незначительно уменьшаются или остаются неизмененными. Криоглобулинемия может появиться и сохраняться на протяжении нескольких месяцев, тогда как циркулирующие иммунные комплексы обнаруживают в течение только нескольких недель.
В биопсийном материале обнаруживают увеличенные и гиперклеточные гломерулы, первоначально с нейтрофильной инфильтрацией, а позже с мононуклеарной инфильтрацией. Гиперплазия эпителиальных клеток – общая ранняя, преходящая черта постинфекционного гломерулонефрита. Также могут развиваться микротромбозы; при тяжелом повреждении гемодинамические изменения, являющиеся результатом клеточной пролиферации и отека гломерул, приводят к олигурии, иногда сопровождаемой деформацией эпителиальных клеток в виде полумесяца (образующихся в пространстве Боумена в результате гиперплазии эпителиальных клеток). Количество эндотелиальных и мезангиальных клеток увеличивается, а мезангиальные пространства часто очень расширяются в результате отека и содержат нейтрофилы, некротизированные клетки, продукты распада клеток и субэпителиальные включения электронно-плотного вещества.

Острый гломерулонефрит - тяжелое поражение структуры почечных клубочков, развивающееся вследствие перенесенной стрептококковой инфекции, вызванной в основном, штаммами М серотипов 1, 2, 4, 12, 18, 25, 49, 55, 57, 60 и некоторых других М-типов стрептококка группы А. Общепринятым является мнение об остроте процесса, однако заболевание может иметь хроническое течение, нередко приводить к дисфункции почек (альбуминурия и снижение скорости клубочковой фильтрации могут сохраняться у перенесших острый гломерулонефрит пожизненно), что позволяет рассматривать его в ряду причинных факторов хронической болезни почек [4]. В настоящее время диагноз острый постстрептококковый гломерулонефрит реже ставится в специализированных нефрологических отделениях, хотя по-прежнему наблюдаются и спорадические случаи, и эпидемические вспышки данного заболевания [2,6,7].
Создание экспериментальных моделей острого гломерулонефрита необходимо не только для дальнейшего изучения механизмов пато- и морфогенеза заболевания, но и для доклинической апробации новых лекарственных препаратов, предлагаемых фармацевтической промышленностью и обладающих нефропротективным действием.
Материалы и методы исследования:
Животные были разделены на 2 экспериментальные группы: I группа - контрольная (интактные животные), n=10; II группа (опытная) - животные, иммунизированные бактериальной суспензией эталонного штамма Streptococcus pyogenes (ГНИИ стандартизации и контроля им. Л. А. Тарасевича), n=16. С целью подтверждения воспроизводимости эксперимента II группа была подразделена на 2 подгруппы, различающиеся сроком забора мочи для лабораторного исследования и органов для аутопсии и гистологического анализа (21 и 31 день иммунизации).
Антигенную суспензию для иммунизации животных получали путем культивирования штамма на мясопептонном бульоне в аэробных условиях при температуре +370С, последующем центрифугировании суточной бульонной культуры Streptococcus pyogenes в течение 10-15 минут при скорости 3000 оборотов в минуту и последующем удаления супернатанта. Полученную взвесь концентрацией 109 КОЕ / мл, определяемой на КФК-3 (оптическая плотность 0,028, длина волны 540 нм, кювета - 1,060 мм), инактивировали при +56 ºС в течение 30 минут. Из расчета 50 мкл взвеси на 1 животное готовили разведение: 9 мл стерильного физиологического раствора и 1 мл взвеси (на 1 животное приходится 500 мкл (0,5 мл) полученной вновь взвеси антигенной суспензии). Иммунизацию животных проводили внутрибрюшинно 1 раз в день по схеме: 3 цикла, каждый из которых состоял из 1, 3, 5 дней иммунизации и 2 дней перерыва между циклами.
Результаты исследования
У животных контрольной группы не было выявлено лабораторных и гистологических признаков развития острого гломерулонефрита. В течение всего эксперимента в моче животных этой группы белок не выявлялся, в микроскопии мочевого осадка патологии не обнаружено.
При проведении аутопсии почки животных контрольной группы имели бобовидную форму, капсула легко снималась, обнажая блестящую, гладкую поверхность светло-коричневого цвета. На разрезе корковое вещество почек было светло-коричневого цвета, мозговое вещество - темно-красное. Лоханка не расширена, ее слизистая оболочка блестящая, гладкая. При проведении гистологического исследования строение ткани почек соответствовало нормальному: четко выявлялась капсула, корковое вещество с почечными тельцами и извитыми канальцами, мозговое вещество, визуализировались сосочки и почечная лоханка, выстланная переходным эпителием. Сосудистые клубочки нефрона не изменены. Проксимальные и дистальные почечные канальцы с типичной структурой.
У иммунизированных животных II группы к 21 дню иммунизации визуально отмечалось снижение аппетита и двигательной активности. У 90 % животных при проведении микроскопии мочевого осадка выявили гематурию - от незначительной до средней степени выраженности, исследование мочи на содержание белка показало положительный результат у 80 % животных.
На секции отмечались макроскопические признаки застойной сердечной недостаточности: общее венозное полнокровие; увеличение печени (печень плотная, тёмная); инъецированность сосудов брыжейки, имелись небольшие кровоизлияния.
С целью подтверждения воспроизводимости модели острого гломерулонефрита забор материала у 8 животных II группы осуществляли на 21 день эксперимента. При проведении аутопсии почки иммунизированных животных имели бобовидную форму, были увеличены в размерах, выглядели набухшими. На разрезе корковое вещество имело серовато-коричневый цвет, мозговое вещество - вишнево-красный; лоханка не изменена. При проведении микроскопии гистологических препаратов в ткани почек выявлялось полнокровие сосудов коркового и мозгового вещества, в корковом веществе визуализировалось большое количество увеличенных гиперцеллюлярных клубочков с резко уменьшенным мочевым пространством, инфильтрированных нейтрофильными гранулоцитами, эозинофилами и лимфоцитами, с аккумуляцией большого числа моноцитов в просветах капилляров. Выявленные изменения характеризовали в этом сроке экссудативную фазу воспаления и были выражены не менее чем в 60 % клубочков, выявляемых в гистологическом срезе. Отмечалось сужение просветов капилляров клубочков вследствие пролиферации эндотелиальных и мезангиальных клеток, появление клубочков с лобулярной структурой. В проксимальных и дистальных канальцах нефронов изменения канальцевого эпителия были выражены умеренно (выявлялись участки белковой дистрофии эпителия, в интерстициальной ткани почек - участки воспалительной инфильтрации лимфоцитами, нейтрофилами и макрофагами) и имели очаговый характер.
У всех животных II группы к 31 дню иммунизации при свободном доступе к пище и воде отмечалось значительное снижение аппетита и потребности в жидкости, а также резкое снижение суточного диуреза по сравнению с контрольной группой. При проведении микроскопии мочевого осадка выявляли гематурию средней степени выраженности, содержание белка показало положительный результат у 100 % животных.
При проведении аутопсии у 8 иммунизированных животных II группы на 31 день эксперимента макроскопически имелись признаки отёка почечной ткани, изменения в лоханках отсутствовали. Гистологическое исследование ткани почек животных этой группы выявило в большинстве клубочков (80 %) преобладание процессов пролиферации, что выражалось в появлении, наряду с мезангиальной и эндотелиальной пролиферацией, отложений нитей фибрина и белковых масс в капсуле Шумлянского-Боумена, сращении капилляров клубочка с капсулой и образовании полулуний в отдельных клубочках. Отмечался также тромбоз капилляров почечных телец. Гломерулярная базальная мембрана визуально выглядела значительно утолщенной. В проксимальных и дистальных извитых канальцах находили белковую дистрофию эпителия, в межуточной ткани почек - воспалительную инфильтрацию нейтрофильными гранулоцитами и лимфоцитами.
Таким образом, в гистологических препаратах почек иммунизированных животных наблюдалась морфологическая картина, соответствующая патоморфологическим изменениям, характерным для
- Бурова Л. А. Способность стрептококков группы А типа М12 связывать иммунные комплексы и их роль в патогенезе постстрептококкового гломерулонефрита / Л. А. Бурова, Е. А. Гаврилова. П. В. Пигаревский, В. Г. Селиверстова, В. А. Нагорнев, К. Шален, Артем А. Тотолян // Медицинская иммунология. - 2006. - Т. 8, № 5-6. - С. 623-630.
- Acute post-streptococcal glomerulonephritis in children of French Polynesia: a 3-year retrospective study / O. Becquet, J. Pasche, H. Gatti, C. Chenel, M. Abély, P. Morville, C. Pietrement// Pediatr. Nephrol. - 2010. - Vol. 25, № 2. - P. 275-280.
- Cunningham, M. W. Pathogenesis of group A streptococcal infections / M. W. Cunningham// Clin. Microbiol. Rev. - 2000. - Vol. 13. - P. 470-511.
- Acute postinfectious crescentic glomerulonephritis: clinicopathologic presentation and risk factors / A. A. El-Husseini, H. A. Sheashaa, A. A. Sabry, F. E. Moustafa, M. A. Sobh // Int. Urol. Nephrol. - 2005. Vol. 37, № 3. - P. 603-609.
- Garnier, A, Postinfectious acute glomerulonephritis / A. Garnier, M. Peuchmaur, G. Deschênes // Nephrol Ther. - 2009. Vol. 5, № 2. - P. 97-101.
- Jankauskiene, A. Postinfectious glomerulonephritis in children in Lithuania during 1995-2004: prevalence and clinical features / A. Jankauskiene, B. Pundziene, R. Vitkevic // Medicina (Kaunas). - 2007. Vol. 43, № l. - P. 16-22.
- Wong, W. Outcome of severe acute post-streptococcal glomerulonephritis in New Zealand children / W. Wong, M. C. Morris, J. Zwi // Pediatr. Nephrol. - 2009. Vol. 24, № 5. - P. 1021-26.
Гломерулонефрит может быть опасным из-за незаметного течения, не менее половины случаев выявляется случайно. Чтобы предупредить серьезное поражение почек, нужно знать признаки болезни отчего она возникает.
Что такое гломерулонефрит
Гломерулонефриты - это группа довольно разнородных почечных заболеваний. Их объединяет поражение клубочков почек (гломерул), которое приводит к нарушению функции почек, отекам, повышению артериального давления. На конечных стадиях болезнь приводит к почечной недостаточности, которая ведет к зависимости от диализа или требует пересадки почки.
С 2003 по 2013 год распространенность неопухолевых болезней почек увеличилась на 2,9% (Каприн А.Д и соавт, 2015). Точные данные по количеству больных гломерулонефритом по России отсутствуют. Однако недавно в Республике Татарстан было подсчитано, что с 2000 по 2010 заболеваемость выросла примерно в полтора раза, хроническим гломерулонефритом – в 2,4 раза (Сигитова О.Н., 2012). Официальный рост заболеваемости в первую очередь говорит об успехах в диагностике.
Медицинские услуги
Диагностические исследования
Как можно заподозрить гломерулонефрит (симптомы и признаки)
Часто гломерулонефрит себя никак не проявляет и его диагностируют, исследуя кровь и мочу по другому поводу. Сочетание симптомов болезни зависит от ее формы и типа течения. Перечислим основные проявления.
- Изменение цвета мочи — от светло-красного до насыщенно-бордового цвета.
- Изменение свойств мочи — становится пенистой из-за присутствия белка.
- Отеки, вплоть до скопления жидкости в брюшной и плевральной полостях, сердечной сумке (перикарде). При болезнях почек наиболее характерны отеки лица.
- Уменьшение количества выделяемой мочи.
- Внезапное стойкое повышение артериального давления.
В 55% случаев диагноз гломерулонефрита устанавливают при обследовании по другим поводам.
Классификация гломерулонефрита
- острый гломерулонефрит
- быстропрогрессирующий гломерулонефрит
- хронический гломерулонефрит с морфологическими вариантами.
Самый тяжелый быстропрогрессирующий вариант встречается достаточно редко (менее 10% всех случаев). Хронические гломерулонефриты разнородны, чаще всего диагностируют иммуноглобулин А-нефропатию. Эта форма составляет до 20% в Европе и США и до 45% в Азии.
- N03.0 - минимальные повреждения
- N03.1 - очаговые и сегментарные гломерулярные повреждения
- N03.2 - мембранозный гломерулонефрит
- N03.3 - мезангио-пролиферативный гломерулонефрит
- N03.4 - эндокапиллярный пролиферативный гломерулонефрит
- N03.5 - мезангиокапиллярный гломерулонефрит
- N03.6 - мембранозно-пролиферативный гломерулонефрит
- N03.7 - экстракапиллярный гломерулонефрит.
Выделяют две большие группы в зависимости от этиологии:
- Первичные гломерулонефриты, изолированно поражающие почечную ткань.
- Вторичные гломерулонефриты, то есть возникшие на фоне какого-то заболевания. В этом случае вовлечены другие органы и системы организма.
Вторичные нефриты могут быть проявлениями:
- системной красной волчанки;
- ревматоидного артрита;
- васкулита, в том числе АНЦА (гранулематозные васкулиты с антинейтрофильными цитоплазматическими антителами);
- антифосфолипидного синдрома;
- вирусного гепатита С;
- ВИЧ-инфекции;
- эндокардита (инфекционного поражения клапанов сердца).
Риск развития гломерулонефрита после стрептококкового фарингита 5-10%, после стрептококкового воспаления кожи – 25% (Stetson C.A. et al, 1955; Anthony B.F et al, 1969)
Острые формы вызываются заражением бета-гемолитическим стрептококком (типы 1, 2, 4, 12, 18, 25, 49, 55, 57, 60). В этом плане стрептококковые ангина, скарлатина и стрептодермия — факторы риска. Иногда гломерулонефрит может быть связан с приемом лекарств (препараты лития, анаболики, интерферон), употреблением героина и вирусными инфекциями (ВИЧ, вирусы Коксаки и Эпштейна-Барр). За хроническими гломерулонефритами, как правило, стоят аутоиммунные нарушения (Национальное руководство по нефрологии под ред. Н.А. Мухина, М., “Гэотар-Медиа”, 2014).
Что происходит с почками при гломерулонефрите?
При развитии стрептококковой инфекции организм вырабатывает антитела для борьбы с возбудителем и иммунные комплексы откладываются в разных структурах почечного клубочка. Следует каскад воспалительных реакций, иммунная система начинает атаковать почечную ткань, повреждая её. Усугубляют ситуацию сужение сосудов в месте воспаления и склонность к тромбообразованию.
Опаснейшая форма — быстропрогрессирующий нефрит: организм вырабатывает антитела, направленные на повреждение базальной мембраны клубочка, или же происходит поражение почек иммунными комплексами. Это нередко сопряжено с АНЦА-васкулитом. При этом заболевании происходят патологические изменения в мелких кровеносных сосудах всего тела, в том числе почек. При хронических гломерулонефритах возможно отложение иммуноглобулинов в самих клубочках.
Существует несколько типов хронических гломерулонефритов:
- Иммуноглобулин А-нефропатия (мезангиопролиферативный нефрит). Почки повреждаются повышенным количеством антител из группы иммуноглобулинов А. Между сосудистыми петлями клубочка усиленно растет соединительная ткань. Эту патологию часто называют гематурическим гломерулонефритом из-за того, что в моче находят эритроциты (красные кровяные тельца).
- Мембранозная нефропатия. Отложение антител вызывает утолщение мембраны клубочков и нарушение ее функции.
- Мембранозно-пролиферативный гломерулонефрит (мезангиокапиллярный нефрит). Считается почечным проявлением других болезней - инфекций, аутоиммунных патологий, злокачественных новообразований, саркоидоза. Клубочки содержат дополнительные клетки и есть неравномерное увеличение толщины стенок капилляров.
- Болезнь минимальных изменений (липоидный нефроз, болезнь малых отростков подоцитов), при которой идет повреждение клубочков за счет расплавления отростков подоцитов. Подоциты - это клетки, которые окружают мелкие сосуды клубочка и не позволяют белку проникать из крови в мочу. Изменения можно определить только при помощи электронного микроскопа. Это самый частый морфологический вариант гломерулонефрита у детей.
- Фокально-сегментарный гломерулосклероз (ФСГС). Воспаление отдельных частей клубочка и замещение сегментов клубочков рубцовой тканью. Вначале часть гломерул никак не повреждается.
- Волчаночный нефрит - это проявление системной красной волчанки.
Диагностика гломерулонефрита
Диагностикой занимается врач-нефролог. Он начинает с опроса пациента, узнает, не было ли ранее инфекционных заболеваний, какие препараты принимает пациент, какими хроническими заболеваниями страдает. Затем проводят дополнительные исследования:
- Анализы мочи:
- клинический анализ;
- проба Зимницкого;
- проба Реберга;
- суточная потеря белка.
- Анализы крови:
- клинический анализ;
- биохимический анализ (креатинин, мочевина);
- протеинограмма;
- липиды крови;
- электролиты крови.
- Экскреторная урография.
- Радионуклидное исследование почек.
- Ультразвуковое исследование почек.
- Пункционная биопсия.

Возможны следующие результаты:
- Белок в моче (протеинурия) — от следового количества до массивной потери, исчисляемой десятками граммов.
- Большое количество красных кровяных клеток в моче (гематурия). Гематурию выявляют общий анализ мочи и анализ по Нечипоренко.
- макрогематурия (если кровь в моче видна невооруженным глазом);
- микрогематурия (если эритроциты обнаруживают только при микроскопии).
- Снижение уровня общего белка и альбумина.
- Повышение холестерина крови.
- Повышение азотистых шлаков крови (креатинина и мочевины).
- Высокий уровень циркулирующих иммунных комплексов, комплемента, IgA.
На УЗИ определяют увеличение в размерах или отечность почек. Самый точный метод диагностики гломерулонефритов — биопсия почек: после обезболивания в почку вводят тонкую иглу и берут фрагмент почечной ткани. Затем этот фрагмент окрашивают и изучают под оптическим и электронным микроскопом.
Биопсия почки – самый точный метод диагностики при гломерулонефрите.
Лечение
Методы терапии зависят от варианта заболевания. В легких случаях, когда нет жалоб и грубых нарушений фильтрационной способности почек, лечение не нужно. Назначают только диету.
Если есть повышение артериального давления, то назначают ингибиторы ангиотензин-превращающего фермента (иАПФ). Они снижают избыточное сосудистое давление в клубочках и защищают их от повреждения, уменьшают потерю белка почками.
При иммунных патологиях назначают иммунодепрессанты: глюкокортикостероиды и циклофосфамид. Из-за множества побочных эффектов такие препараты применяют только в серьезных случаях.
Новые средства, корректирующие иммунный ответ:
- микофенолата мофетил
- ритуксимаб
- циклоспорин
- такролимус.
Если гломерулонефрит вызван вирусной инфекцией, назначают противовирусное лечение. При остром гломерулонефрите применяют антибиотики.
При необходимости проводят симптоматическое лечение. Так, при отеках используют мочегонные средства, при повышенной свертываемости крови - антикоагулянты, при повышении уровня холестерина - статины.
Осложнения гломерулонефрита
Заболевания клубочкового аппарата почек могут протекать с отеками, тромбозами, развитием тяжелой артериальной гипертензии, анемии.
Самое тяжелое осложнение — почечная недостаточность: ткань почек постепенно замещается рубцовой тканью, и орган перестает выполнять свои функции, т.е. регулировать водно-солевой баланс организма, выводить шлаки. В крайних случаях прибегают к гемодиализу или перитонеальному диализу. 
Рекомендации по образу жизни при гломерулонефрите
Диета: ограничение приема поваренной соли, калия и фосфора (если выявлена почечная недостаточность), уменьшение количества белка в рационе. Важен отказ от курения, так как оно негативно влияет на сосуды и может усилить осложнения. При повышенном давлении курение повышает риск инсультов и инфарктов. Также играет роль поддержание здоровой массы тела.
Профилактика
Возможна в отношении острого гломерулонефрита, где есть четкая связь между стрептококковым заболеванием и поражением почек. Важно вовремя излечивать инфекцию полным курсом антибиотиков пенициллинового ряда в адекватной дозе.
Общие рекомендации по снижению риска развития гломерулонефрита:
- Необходимо своевременно обращаться за лечением стрептококковых инфекций горла и кожи.
- Следует контролировать уровень сахара в крови и артериальное давление.
- Предупреждение инфекций, передающихся с кровью (гепатиты, ВИЧ).
Прогноз
При правильном лечении острого гломерулонефрита больные полностью выздоравливают. Острый процесс обычно не переходит в хроническую форму.
Хронические гломерулонефриты тоже могут протекать доброкачественно, так что десятилетиями функция почек остается в норме.
Быстропрогрессирующий нефрит имеет более серьезный прогноз, это всегда экстренная ситуация в нефрологии, но при правильном лечении 80% пациентов достигают ремиссии.
Читайте также:


