Нозологические формы инфекционных заболеваний что это

Здоровье населения является одним из наиболее информативных показателей, отражающих качество среды обитания. Можно выделить множество уже известных внешних факторов, формирующих здоровье популяции, но данный вопрос требует дальнейшего изучения. Увеличение распространенности какой-либо болезни может рассматриваться как показатель действия неблагоприятных факторов окружающей среды [8]. Самара входит в список экологически неблагополучных городов России. Загрязнение воздуха взвешенными веществами над территорией города больше на 43%, чем средний показатель по России. Приоритетными загрязнителями воздуха являются: аммиак, формальдегид, хлор, сероводород [7]. С вдыхаемым воздухом, по пищевым цепям, с водой ксенобиотики поступают в организм человека. Загрязнены также почва и вода. Основными загрязняющими веществами воды являются фенол, нитриты и соединения меди, а почвы – свинец, ртуть, мышьяк, нефтепродукты [7, 11, 12].
По данным литературы за период с 2011 по 2014 гг. в структуре распространенности общей заболеваемости всего населения (расчеты на 100 тыс. человек) по Самарской области преобладали: болезни органов дыхания (24%), органов системы кровообращения (15%), костно-мышечной системы (11%), мочеполовой системы (9%), офтальмологические заболевания (5%), травмы и отравления (5%) [1, 9].
Заболевания, связанные с воздействием неблагоприятных факторов среды, рассматриваются как экологически зависимые [2, 3, 5]. Факторы окружающей среды, которые выступают в качестве основной причины заболевания, расцениваются как детерминирующие; если факторы окружающей среды изменяют клиническую картину, тяжесть и течение заболевания, не являясь их основной причиной, они являются модифицирующими. Ввиду множества причин возникновения хронических заболеваний очень трудно дифференцировать специфические этиологические факторы развития болезни [4, 6, 10].
В связи с этим актуально изучение заболеваемости населения в районах г.о. Самары с разным уровнем антропотехногенной нагрузки и установление взаимосвязи заболеваемости с действием неблагоприятных условий окружающей среды.
Все районы г.о. Самара с точки зрения степени загрязнения окружающей среды можно разделить на 2 группы.
1. Районы с неблагоприятной экологической обстановкой: Кировский, Советский, Куйбышевский, Железнодорожный и Промышленный. На территории этих районов располагаются основные промышленные предприятия города.
2. Районы с относительно благоприятными экологическими условиями: Самарский, Ленинский, Октябрьский, Красноглинский районы. Эти районы расположены вблизи Волги, здесь сосредоточено множество парков, скверов, практически отсутствуют действующие промышленные предприятия.
Цель работы: определить спектр и частоту нозологических форм заболеваний пациентов клиник СамГМУ, проживающих в районах г.о. Самара с различным уровнем антропотехногенной нагрузки.
1. Изучить частоту встречаемости заболеваний по данным отделений гастроэнтерологического, нефрологического и пульмонологического профилей клиник СамГМУ.
2. Выявить патологии, преобладающие у пациентов указанных отделений.
3. Проанализировать взаимосвязь возникновения наиболее распространенных заболеваний с уровнем антропотехногенной нагрузки в различных районах г.о. Самара.
4. На основании полученных результатов создать базу данных для детального изучения влияния неблагоприятных экологических факторов на формирование отдельных мультифакториальных заболеваний.
В ходе выполнения работы проводилось анкетирование и изучение историй болезней пациентов, находившихся на стационарном лечении в гастроэнтерологическом, пульмонологическом и нефрологическом отделениях клиник СамГМУ за период с октября 2015 г. по октябрь 2016 г. Выбор профиля отделений обусловлен тем, что именно органы дыхания, пищеварения и выделения выполняют барьерные функции на границе раздела двух сред – внешней и внутренней — и непосредственно контактируют с экотоксикантами, поступающими в организм человека.
Всего проанализированы истории болезней 908 пациентов в возрасте от 18 до 76 лет (средний возраст обследованных составил 45 лет) мужского и женского пола (433 мужчины и 475 женщин). Среди обследованных пациентов в основном преобладали лица трудоспособного возраста (73%). Все обследованные пациенты проживали в указанных районах г.о. Самара: в районах с неблагоприятной экологической обстановкой 61% и в районах относительного экологического благополучия 39%.
Анализ данных о пациентах гастроэнтерологического отделения показал, что за 9 месяцев (2016 г.) было госпитализировано 210 больных. Спектр нозологических форм заболеваний представлен на рисунке 1.
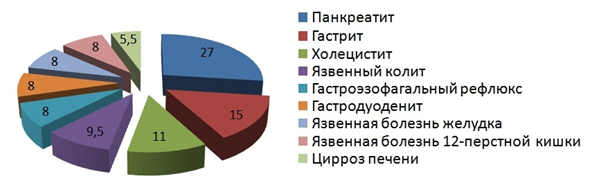
Рис. 1. Нозологические формы заболеваний пациентов отделения гастроэнтерологии
Таким образом, на основании полученных нами данных можно сделать вывод, что за указанный период наиболее часто встречающейся патологией, установленной как основной диагноз у пациентов отделения гастроэнтерологии, является хронический панкреатит.
При выяснении связи развития данных заболеваний с проживанием в определенном районе города или области получены следующие данные. Панкреатит регистрировался практически с одинаковой частотой (14–16%) у лиц, проживающих в Кировском, Промышленном, Железнодорожном, Советском районах, однако большее количество пациентов (19%) проживало в Октябрьском районе г.о. Самара. Наибольшее количество больных холециститом и гастритом проживало в Промышленном районе (22% и 23% соответственно). Далее по количеству больных следует Железнодорожный район. Таким образом, 59% больных острым и хроническим панкреатитом проживали в экологически неблагоприятных районах. 65% из числа больных хроническим холециститом проживают в неблагополучной с точки зрения экологии местности, среди пациентов с гастритом – 81%.
При изучении спектра и частоты встречаемости заболеваний у пациентов, проживающих в экологически неблагополучных районах, получены следующие данные: наиболее часто встречающейся патологией у жителей всех неблагоприятных с точки зрения экологии районов является панкреатит, но регистрируется он с разной частотой. Так, среди больных Советского и Кировского района он преобладает значительно и составляет почти половину от всех других заболеваний желудочно-кишечного тракта. Доля пациентов с панкреатитом, проживающих в Промышленном и Железнодорожном районах, значительно ниже (22% и 17% соответственно). Она практически одинакова по сравнению с другими заболеваниями. Привлекает внимание тот факт, что среди пациентов, проживающих в Промышленном районе, высок процент лиц с язвенным колитом (21%), хотя в общей структуре нозологических форм заболеваний он составляет 9,5%. В Железнодорожном районе по полученным данным самая высокая частота встречаемости цирроза печени – 14% против менее 8% в общей структуре заболеваемости.
В отделении пульмонологии и аллергологии проанализировано 359 историй болезни. Лидирующее место в структуре нозологических форм заболеваний занимают острый и хронический бронхит (23,1%), бронхиальная астма различного генеза (22,3%), хроническая обструктивная болезнь легких (16,1%), внебольничная бактериальная пневмония (13,1%). Далее следуют болезни, частота встречаемости которых не превышает 10%: саркоидоз, бронхоэктатическая болезнь легких, ангионевротический отек, идиопатический фиброзирующий альвеолит и т.д. (рис. 2).
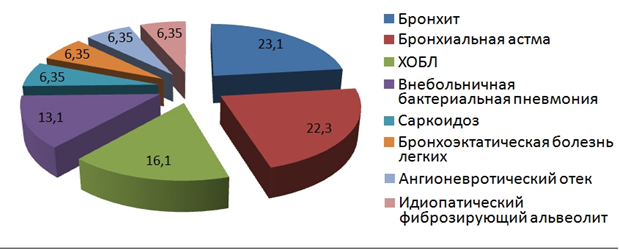
Рис. 2. Нозологические формы заболеваний пациентов отделения пульмонологии и аллергологии
Частота встречаемости острого бронхита наибольшая у пациентов Кировского района (18%), бронхиальной астмы – максимальна у больных, проживающих в Промышленном районе (31%), хронической обструктивной болезни легких – у пациентов Советского района (21%), внебольничной бактериальной пневмонии – Промышленного района (26%). Следовательно, из всех больных с наиболее часто встречающимися заболеваниями органов дыхания более половины проживали в экологически неблагополучных районах: 67% — с острым и хроническим бронхитом, 54% — с бронхиальной астмой, 53% — с ХОБЛ, 70% — с внебольничной бактериальной пневмонией.
При анализе частоты встречаемости бронхолегочных заболеваний у больных, проживающих в экологически неблагополучных регионах, обращает внимание разнородность структуры заболеваемости в разных районах. Так, среди всех пациентов Промышленного района преобладают больные бронхиальной астмой —39%, тогда как в Кировском районе частота встречаемости таких пациентов 16%. В то же время у пациентов Кировского района лидирующей патологией является острый бронхит (36%), а пациенты с данным заболеванием, проживающие в Железнодорожном районе, составляют всего 13%. Среди пациентов, проживающих в Советском районе, распространенность изучаемых болезней пульмонологического профиля практически одинакова.
В отделении нефрологии проанализировано 339 историй болезни. Лидирующее место в структуре заболеваний занимают хронический тубулоинтерстициальный нефрит (30,5%), хроническая болезнь почек (ХБП) (27,6%), хронический пиелонефрит (16%) и хронический гломерулонефрит (14,9%). Далее следуют болезни, которые сравнительно реже регистрировались у пациентов отделения нефрологии (в основном в виде сопутствующей почечной патологии), общая частота их встречаемости не превышала 10%: нефросклероз, кисты почек, цистит, острая почечная недостаточность, мочекаменная болезнь. Отмечались единичные случаи встречаемости системных васкулитов, аномалий развития почек, амилоидоза и др. Всего в совокупности эти виды редко встречающейся патологии составили менее 1% (рис. 3).
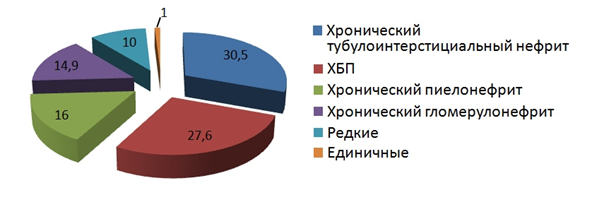
Рис. 3. Нозологические формы заболеваний пациентов отделения нефрологии
Частота встречаемости хронического тубулоинтерстициального нефрита больше всего у жителей экологически неблагополучных районов. Так, у пациентов, проживающих в Советском районе г.о. Самары, этот показатель составлял 43%, в Кировском районе — 38%. Несколько реже у пациентов из этих районов встречается хронический гломерулонефрит (33% и 32% соответственно). Частота встречаемости хронического пиелонефрита у пациентов Кировского района была значительно выше, чем у пациентов, проживающих в других районах г.о. Самары, и составила: в Кировском районе 30%, в Советском районе 19%, в Железнодорожном районе 12,5%.
Спектр заболеваний нефрологического профиля у пациентов, проживающих в относительно экологически благополучных районах, практически не отличался, но заболевания органов мочевыделения у них характеризовались меньшей степенью тяжести и продолжительностью течения.
Как уже было сказано ранее, все пациенты в зависимости от района проживания были условно разделены на 2 группы в соответствии с уровнем антропотехногенной нагрузки. Среди обследованных больных, проживающих в экологически неблагополучных районах г.о. Самара, преобладали пациенты с заболеваниями органов дыхания (38,9%), несколько реже встречались пациенты с заболеваниями органов мочевыделения (37,9%), еще реже – пациенты с заболеваниями желудочно-кишечного тракта (23,2%). Спектр заболеваний у пациентов относительно экологически благополучных районов несколько отличался. Здесь преобладали пациенты с заболеваниями органов мочевыделения (39%). На втором месте – пациенты с заболеваниями органов желудочно-кишечного тракта (37%). Заболевания органов дыхания выявлены у 24% обследованных (рис. 4).
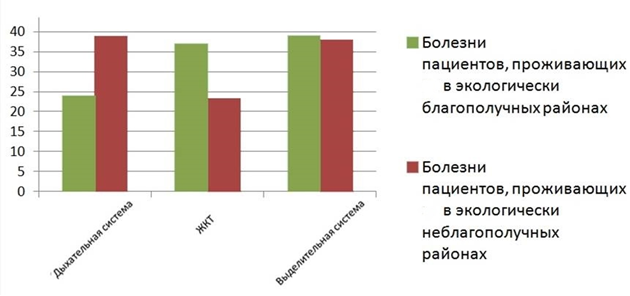
Рис. 4. Сравнительная диаграмма спектра заболеваний населения экологически неблагополучных и благополучных районов
Следует также отметить, что большинство пациентов отделений указанных профилей клиник СамГМУ находились на госпитализации впервые (63%), где и был установлен первичный диагноз. Пациенты с хроническими формами заболеваний и частыми обострениями, требующими госпитализаций до 2–4 раз в год, встречались в 37% случаев. Из них более чем в 50% случаев у пациентов стаж заболевания превышал 3 года, и они находились на амбулаторном наблюдении и лечении.
Таким образом, статистический анализ, проведенный ретроспективно по данным историй болезней, показал зависимость распространенности таких заболеваний, как бронхиальная астма, бронхит, панкреатит и гастрит, от района проживания пациентов, что может быть следствием особенностей окружающей среды и ее влияния на развитие и течение заболеваний органов желудочно-кишечного тракта и дыхания.
Болезни почек и органов мочевыделения, судя по данным нашего исследования, в меньшей степени зависят от района проживания и, как следствие, от влияния экологических и других внешних факторов.
Результаты нашего изучения и анализа историй болезней пациентов клиник СамГМУ в целом подтверждают официальные статистические данные по Самарской области. Разнородность структуры заболеваемости, вероятно, обусловлена воздействием факторов различной природы, разными путями проникновения и механизмами воздействия негативных факторов окружающей среды на организм человека. Однако на данном этапе исследования можно лишь предположить, что антропотехногенная нагрузка вносит определенный вклад в формирование болезни. Для более детального изучения необходимо проанализировать бо?льший временной период, другие районы и нозологии.
1. В настоящее время все большее распространение получают заболевания тех органов и систем организма, которые выполняют барьерные функции на границе раздела двух сред – внешней и внутренней – и тем самым поддерживают и сохраняют постоянство внутренней среды организма: дыхательной, пищеварительной, иммунной и выделительной систем.
2. Среди больных, находящихся на стационарном лечении в клиниках СамГМУ, преобладают пациенты, проживающие в административных районах с высоким уровнем антропотехногенной нагрузки.
3. В отделениях клиник СамГМУ различного профиля отмечается тенденция преобладания определенных нозологических форм заболеваний, как правило, характеризующихся значительной тяжестью и продолжительностью течения.
4. По-видимому, негативные факторы окружающей среды для обследованной группы пациентов являются и детерминирующими, и модифицирующими, так как среди пациентов есть больные как с дебютом заболевания, так и с хроническими, длительно протекающими формами заболеваний.
5. Рекомендуется учитывать факт и длительность проживания населения на территориях с высоким уровнем воздействия негативных факторов среды для формирования групп риска по отельным нозологическим формам заболеваний.
Нозологическую форму (нозологическую единицу) рассматривают как "определенную болезнь, выделенную на основе установленных этиологии и патогенеза и/или характерной клинико-морфологической картины" (Энциклопедический словарь медицинских терминов, 1983). Нозологическая форма — "единица номенклатуры и классификации болезней". Это определение требует некоторых уточнений и дополнений. Прежде всего у большинства из более чем 20 тыс. нозологических форм, которыми "располагает" современная медицина, причина болезни неизвестна. Поэтому этиология не является, к сожалению, ведущим критерием выделения нозологической формы. Этиология явно уступает в этом отношении патогенезу, на основании которого довольно часто объединяют нозологические формы в группы заболеваний. Четкие критерии выделения нозологической формы в настоящее время, как видно, отсутствуют. Наибольшее значение имеет, пожалуй, исторический опыт.
Если исходить в выделении нозологической формы из особенностей клинико-морфологической картины (чем руководствуются наиболее часто), то следует иметь в виду, что этот критерий предусматривает не только своеобразие клинических симптомов и синдромов, присущих данному заболеванию, преимущественную локализацию процесса, но и характер патологического процесса (последнее нужно подчеркнуть особо). К сожалению, последним критерием, т.е. характером патологического процесса, современная медицина (нозология) стала все больше и больше пренебрегать. Примером такого пренебрежения могут служить так называемые патии (нефропатия, энтеропатия, гепатопатия, пневмопатия, кардиопатия и т.д.), в основе которых лежат, пожа-
луй, все, кроме воспалительных и опухолевых, процессы. Неудивительно поэтому, что "патии" стали пристанищем незнания и непонимания.
Отход от классических принципов выделения нозологических форм, выражающийся в отказе от верификации патологического процесса при выделении самих форм, ведет к созданию неверных по существу, а значит, и неприемлемых классификационных схем, чем грешат, к сожалению, и эксперты ВОЗ.
Достаточно привести два примера: современная морфологическая классификация группы гломерулонефрита и клиническая классификация ревматических болезней.
Известно, что в основе выделения гломерулонефрита как нозологии (и группового понятия) лежат два основных критерия: характер патологического процесса — воспаление, и преимущественная его локализация — почечные клубочки. Поэтому-то гломерулонефритом считают "двустороннее диффузное иммуно-воспалительное заболевание почек с преимущественным поражением клубочков" (БМЭ, 1977). Естественно, что дефиницион-ные критерии гломерулонефрита должны быть основополагающими как в выделении различных его форм, так и в построении классификации гломерулонефрита, прежде всего морфологической, которая должна служить целям дифференциальной диагностики форм гломерулонефрита. Но этот принцип современной нефрологией не соблюдается. Мало того, при морфологической верификации гломерулонефрита, выделении его форм современные нефрологи все более и более отходят от определяющих критериев общей патологии. Так, по классификации ВОЗ, к хроническому гломерулонефриту относят пролиферативный гломеру-лонефрит (эндокапиллярный, экстракапиллярный, мезангиопро-лиферативный, мезангиокапиллярный) и склерозирующий (фиб-ропластический), а также минимальные изменения, мембраноз-ную нефропатию и фокальный сегментарный гломерулярный склероз/гиалиноз. Но иммуновоспалительную природу имеют лишь пролиферативный гломерулонефрит и завершающий его эволюцию склерозирующий. В основе же минимальных изменений (болезни малых отростков подоцитов), мембранозной неф-ропатии и фокального сегментарного гломерулярного гиалиноза (ФСГГ) лежат не воспалительные, а диспластические и дистрофические изменения гломерулярной базальной мембраны, ре-цепторные нарушения подоцитов. Как видно, включение в группу хронического гломерулонефрита минимальных изменений, мембранозной нефропатии и ФСГГ не обосновано с чисто обще-патологических позиций. Эти заболевания должны быть исключены из группы хронического гломерулонефрита и включены в группу так называемых невоспалительных гломерулопатий.
Вторым примером формирования групп заболеваний, сущность патологического процесса и морфогенез которых неадекватны данным нозологическим формам, являются ревматические болезни.
Ревматическими болезнями до последнего времени считали болезни системной дезорганизации соединительной ткани иммунопатологического механизма. Морфогенез этой дезорганизации был тщательно изучен, показана смена ее фаз (мукоидное набухание, фибриноидные изменения, фибриноидный некроз, склероз и гиалиноз), изучены особенности иммунного воспаления, сопровождающего эту дезорганизацию, установлена причастность генерализованного васкулита к этим изменениям. На основании особенностей этиологии (роль инфекционного начала и наследственности), патогенеза (иммунопатологический механизм), морфогенеза (системная дезорганизация соединительной ткани, иммунное воспаление) и своеобразия клинико-морфологических проявлений (органопатология) была очерчена группа ревматических заболеваний — болезней системы соединительной ткани с иммунными нарушениями. В нее были включены: ревматизм, ревматоидный артрит, анкилозирующий спондилит (болезнь Бехтерева), системная красная волчанка, склеродермия (прогрессирующий системный склероз), узелковый периартериит, дерма-томиозит и (уже без учета особенностей морфогенеза) сухой синдром Шегрена.
Во что же превратились ревматические болезни в настоящее время? В сборное, хаотичное, полиэтиологическое, полипатогенетическое и полиморфогенетическое понятие. В этом убеждаешься, обратившись к рабочей классификации и номенклатуре ревматических болезней, созданной Всесоюзным научным обществом ревматологов в 1985 г. По этой классификации строится изложение материала в монографиях, посвященных ревматическим болезням, как отечественных, так и зарубежных, да и в учебниках по внутренним болезням.
Среди ревматических болезней в этой классификационной схеме можно найти: рецидивирующий панникулит (болезнь Вебс-ра — Крисчена) рядом с системной красной волчанкой, синдром Шенлейна — Геноха и синдром Гудпасчера рядом со всеми cис темными васкулитами; подагру, амилоидоз и гемохроматоз — бо лезни обменно-дистрофического, а не иммуновоспалительного генеза; миозиты и тендовагиниты, все бактериальные и "микро кристаллические" артриты, остеоартроз, остеопороз, остеомаля цию и даже остеохондропатию бугристости большеберцовой ко сти.
Создание подобной классификации ревматических болезней стало возможным потому, что был отброшен исторический опыт познания ревматических болезней, синдромное взяло верх над
нозологическим, были преданы забвению морфогенетические особенности этих заболеваний, забыто ставшее аксиомой положение: "морфогенез — это основа патогенеза".
Говоря о групповом понятии болезни, т.е. классификационных схемах, нельзя забывать и возможное дробление "устоявшихся" нозологических форм, объединение их в "нозологические группы болезней". Этот процесс обязан успехам прежде всего теоретических дисциплин — молекулярной биологии, генетике, иммунологии, биохимии, целлюлярной патобиологии, которые позволили найти этиологическую, патогенетическую и клинико-морфологическую гетерогенность той или иной нозологической формы. Достаточно сослаться на следующие примеры. Хронический гастрит перестал быть нозологией, это — групповое понятие. Каждая из его бывших форм имеет своеобразие этиологическое (гастрит В — хеликобактерный гастрит), патогенетическое (аутоиммунный гастрит А и рефлюкс-гастрит С). Пилородуоде-нальные язвы и язвы тела желудка претендуют на нозологическую самостоятельность, коль скоро патогенетически это разные заболевания. Формы первичных кардиомиопатий также можно считать самостоятельными заболеваниями — об этом свидетельствуют этиологические, морфогенетические и клинические их различия. Этиологически, пато- и морфогенетически абсолютно различны центральный и периферический рак легкого — это разные заболевания с разной клинико-морфологиче-ской оценкой. Уже известно пять видов вирусных гепатитов (А, В, С, D, F) и каждый вид — самостоятельное заболевание. Наконец, полюбившаяся клиницистам "острая респираторная вирусная инфекция" (ОРВИ), которая как самостоятельное заболевание заполонило поликлиники, да и в клиниках не редкость, хотя представлена по меньшей мере четырьмя болезнями (грипп, парагрипп, аденовирусная инфекция, респираторно-синцитиальная инфекция). Это далеко не полный перечень подмены нозологии групповым понятием болезни.

2. кишечный иерсиниоз.
Заболевания проявляются общей интоксикацией, нередко кожными проявлениями, поражением печени, селезенки, желудочно-кишечного тракта, суставов и других органов, и систем.
Между псевдотуберкулезом и кишечным иерсиниозом много сходства. Однако имеются и различия, что дает основание рассматривать псевдотуберкулез и кишечный иерсиниоз как самостоятельные нозологические формы.
Псевдотуберкулез - острое инфекционное заболевание из группы зоонозов с общей интоксикацией, лихорадкой, скарлатиноподобной сыпью, а также с поражением различных органов и систем.
Этиология. Возбудитель псевдотуберкулеза I. pseudotuberculosis - грамотрицательная палочка. Микроорганизм чувствителен к высыханию, воздействию солнечного света. При нагревании до 60 °С гибнет через 30 мин, при кипячении - через 10 с. Обычная дезинфекция (2% раствор хлорамина, растворы лизола, сулемы и др.) убивает возбудитель в течение 1 мин.
Отличительной особенностью возбудителя псевдотуберкулеза является способность расти при низких температурах (1-4 °С), оптимальная температура роста 22-28 °С.
Эпидемиология. Псевдотуберкулез регистрируется практически на всех административных территориях нашей страны. Болезнь относится к группе зоонозных инфекций. Источником инфекции являются дикие и домашние животные. Возбудитель обнаружен у 60 видов млекопитающих и у 29 видов птиц. Основной резервуар инфекции - мышевидные грызуны. Они инфицируют выделениями пищевые продукты, в которых при хранении в холодильниках и овощехранилищах происходят размножение и массовое накопление возбудителя. Допускается, что его резервуарами могут быть не только грызуны и другие животные, но и почва, где микроорганизм способен размножаться и длительно сохраняться. Его выделяют и из воды, воздуха, фуража, корнеплодов, овощей, молока, молочных продуктов, обнаруживают на таре, предметах кухонного инвентаря и др. Следовательно, возбудитель обитает в организме теплокровных животных и внешней среде.
Это играет важную эпидемиологическую роль, так как позволяет проследить начальные пути заражения овощей и корнеплодов во время их выращивания на полях и огородах. В дальнейшем при хранении обсемененность увеличивается, чему способствует температура овощехранилищ (5-7 °С).
Микроорганизмы сохраняются в воде в течение 2-8 мес, в масле - 5 мес, сахаре - до 3 нед, хлебе - до 150 дней, молоке - 30 дней, в почве при благоприятных условиях - около года.
Заражение происходит алиментарным путем при употреблении инфицированной пищи (салаты, винегреты, фрукты, молочные продукты и др.) или воды, не подвергнутых термической обработке. Эпидемические вспышки различной интенсивности возникают в результате распространения возбудителя пищевым и водным путями, встречаются и спорадические случаи.
К псевдотуберкулезу восприимчивы и дети, и взрослые. Дети до 6 мес практически не болеют, в возрасте от 7 мес до 1 года болеют редко, что можно объяснить особенностями их питания.
Заболевания регистрируются в течение всего года, максимум приходится на февраль - март по причине более широкого употребления в пищу овощей и фруктов, поступающих из овощехранилищ. Заразительность умеренная - 8-20 на 1000 детского населения.
Профилактика. Первое место в системе профилактических мер принадлежит борьбе с грызунами. Большое значение имеет правильное хранение овощей, фруктов и других продуктов питания, исключающее возможность их инфицирования.
Необходим строгий санитарный контроль за технологией приготовления пищи, особенно блюд, которые не подвергаются термической обработке (салаты, винегреты, фрукты и др.), а также за водоснабжением в сельской местности.
Не допускать использование овощей старого урожая, в питании организованных коллективов без термической обработки после 01 марта.
Противоэпидемические мероприятия в очаге инфекции в целом такие же, как и при кишечных инфекциях :
Соблюдать правила личной гигиены: тщательно мыть руки перед приемом и раздачей пищи, после посещения туалета, улицы
Следить за чистотой рук у детей, научить их соблюдать правила личной гигиены
Употреблять для питья кипяченую или бутилированную воду
Выбирать безопасные продукты
Следить за сроками годности продуктов
Тщательно мыть овощи и фрукты перед употреблением под проточной, а для детей – кипяченой водой
Проводить тщательную термическую обработку необходимых продуктов
Употреблять пищу желательно сразу после её приготовления
Готовые продукты хранить на холоде, оберегая их от мух. Не оставлять готовые продукты при комнатной температуре более чем на 2 часа
Правильно хранить продукты в холодильнике: не допускать контакта между сырыми и готовыми продуктами (хранить в разной посуде)
Содержать кухню в чистоте
Не скапливать мусор
Выезжая на отдых, необходимо брать с собой запас чистой питьевой воды. Не употреблять воду из открытых источников
Купаться только в специально отведенных для этой цели местах. При купании в водоемах и бассейнах не допускать попадания воды в рот.
Меры общественной профилактики.
После госпитализации больного проводится заключительная дезинфекция. Специфическая профилактика не разработана.
Кишечный иерсиниоз - острое инфекционное заболевание из группы антропозоонозов с симптомами интоксикации и преимущественным поражением желудочно-кишечного тракта, печени, суставов, реже других органов.
Этиология. Возбудитель кишечного иерсиниоза - короткая грамотрицательная палочка, чувствительная к действию физических и химических факторов.
Она хорошо переносит низкие температуры, сохраняя при этом способность к размножению. Возбудитель кишечного иерсиниоза
Эпидемиология. Возбудитель кишечного иерсиниоза широко распространен в природе. Особенно часто возбудитель обнаруживается у мышевидных грызунов, крупного рогатого скота, свиней, собак, кошек, выделяется из молочных продуктов, мороженого.
Источником инфекции являются человек и животные, больные или носители. Заражение человека происходит в основном через инфицированную пищу, а также контактным путем. Возбудитель передается от человека человеку через руки, посуду, предметы ухода.
В детских организованных коллективах встречаются вспышки заболеваний, обусловленные единым источником питания. Отмечаются семейные и внутригоспитальные вспышки, при которых наиболее вероятным источником инфекции является больной в остром периоде или реконвалесцент. Интервал между отдельными заболеваниями во время таких вспышек составляет от нескольких дней до 3 нед.
Профилактика кишечного иерсиниоза такая же, как и кишечных инфекций другой этиологии. Не меньшее значение имеют и те профилактические мероприятия, которые проводятся при псевдотуберкулезе.
Читайте также:


