Какие выделения при папилломавирусной инфекции
Пятигорский научно-исследовательский институт курортологии
Актуальность. Вирусные инфекции гениталий – одна из актуальных проблем современного акушерства и гинекологии. Нередко именно наличие вирусных инфекций обуславливают развитие многих патологических процессов шейки матки [4,8,12-14]. Так, папилломавирусная инфекция провоцирует формирование йоднегативных очагов, гиперкератозов шейки матки [4,12]. Вирус-индуцированные патологические процессы шейки матки диктуют необходимость коррекции вирусоносительства или остро протекающих вирусных поражений слизистой шейки матки и влагалища, и в то же время не теряет актуальности применение деструктивных методов лечения патологических процессов шейки матки [2,9].
В настоящее время в терапии папилломавирусной инфекции нередко применяют иммуностимулирующий препарат изопринозин. Однако при его длительном применении обращается внимание исследователей на ряд возникающих побочных эффектов, отягощающих состояние больных [6,7,10]. Нередко применяют другие иммуномодуляторы и противовирусные препараты [5,11]. Эти аспекты определяют необходимость поиска других терапевтических подходов к лечению пациенток данной категории.
Цель исследования. Разработать эффективные методы терапии пациенток с выявленной папилломавирусной и другими вирусными инфекциями.
Материалы и методы. Наблюдались 78 пациенток с вирус-индуцированными патологическими процессами шейки матки (ШМ). Больные были разделены в две группы в зависимости от получаемого лечебного комплекса. Лечение проводилось в два этапа. На первом этапе женщины получали противовирусное лечение. Так, в первой группе наблюдения (42 человека) назначался изопринозин курсами по 10 дней в дозировке по 2 таб. 3 раза в день (при массе тела до 80 кг) и по 2 таб. 4 раза в день (при массе тела более 80 кг), перерывы между курсами приема препарата составляли 1 мес. Во второй группе (36 пациенток) назначался изоприназин по 2 таб. 3 раза в день (при массе тела до 80 кг) и по 2 таб. 4 раза в день (при массе тела более 80 кг), курс лечения - 10 дней; всего – 1 курс лечения, в сочетании с приемом препарата лавомакс (тилорон) по 125 мг 2 дня подряд, затем по 125 мг через день, на курс – 20 табл. Количество курсов приема изопринозина и лавомакса определялось нами при обследовании после каждого проведенного курса терапии. Критерием необходимости прекращения или продолжения приема препаратов были показатели полимеразной цепной реакции (ПЦР) и наличие сохраняющейся вирусной инфекции. На втором этапе лечения всем пациенткам проводилось радиоволновое хирургическое воздействие на ШМ.
Всем женщинам оценивались жалобы, проводилось гинекологическое исследование, микроскопия отделяемого из половых органов. Оценивалось состояние вагинального биоценоза по данным ПЦР-диагностики, проводимого для выявления трансмиссивных инфекций (ТСИ). При ПЦР оценивалось наличие хламидиоза, микоплазмоза, уреаплазмоза, вируса папилломы человека (ВПЧ) высокого риска, вируса Эпштейн-Бара (ВЭБ), герпеса, цитомегалловирусную инфекцию (ЦМВ), гарднерелез, трихомониаз, кандидоз до лечения, после каждого курса медикаментозной терапии и после окончания проводимого лечения [1]. До начала курсовой терапии по поводу выявленных при ПЦР-диагностике бактериальных инфекций всем пациенткам было проведено противовоспалительное лечение. Всем женщинам оценивалось состояние ШМ по данным кольпоскопии [3].
Результаты. Возраст женщин составлял в среднем 34,2±6,7 года. Все женщины предъявляли жалобы на выделения из половых путей, которые имели различные оттенки в отношении цветового диапазона – желтоватые, грязно-серые, молочно-белые, прозрачные или беловато-прозрачные. После проведения первого этапа курсового лечения у всех пациенток практически прекратились желтоватые или грязно-серые выделения из половых путей, отмечалось уменьшение слизисто-белых белей, а у части женщин бели подобного характера исчезли после курсового лечения, причем более заметно – во второй группе.
Боли при менструации, определяемые исходно у трети больных в каждой группе наблюдения, после обоих этапов курсового лечения уменьшались незначительно.
У женщин первой группы первый этап медикаментозного лечения был наиболее длительным. В большинстве случаев при приеме изопринозина у женщин наблюдались побочные эффекты: головные боли, боли в правом подреберье и верхних отделах эпигастрия, приступы тахикардии, выраженные боли в суставах и др. Первый курс приема изопринозина сопровождался подобными побочными эффектами только у части больных (табл. 1).
Таблица 1. Симптомы побочного действия курсового применения изопринозина
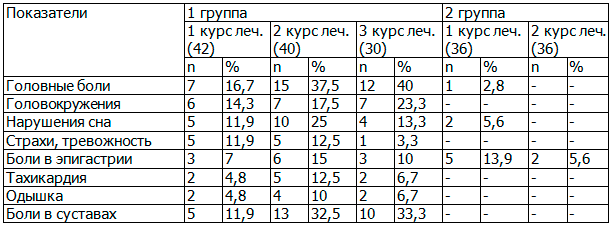
При приеме второго курса изопринозина патологические проявления усугублялись; две пациентки первой группы даже вынуждены были прервать второй курс приема изопринозина из-за нарастающей симптоматики побочных явлений. 10 пациенток первой группы в связи с плохо купируемыми побочными симптомами отказались от третьего курса приема изопринозина.
Во второй группе наблюдения на фоне приема изопринозина назначался лавомакс. При подобном сочетании препаратов у наблюдаемых нами больных побочные эффекты, характерные для приема изопринозина, отсутствовали полностью, что послужило поводом для рассмотрения вопроса о возможном сокращении курсов приема изопринозина.
Всем пациенткам после курсовой терапии проводилось гинекологическое исследование. Ни у одной женщины после первого медикаментозного этапа лечения не определялись воспалительные изменения тканей вульвы и влагалища. В то же время при осмотре ШМ в зеркалах у всех наблюдаемых пациенток во всех группах наблюдения после первого этапа проводимого лечения продолжали определяться патологические процессы ШМ по типу эрозий или белесоватых очагов по поверхности ШМ. После второго этапа лечения с использованием радиохирургического воздействия ни в одном случае наблюдения не было выявлено визуально определяемых признаков эрозий или белесоватых очагов по поверхности ШМ.
При оценке данных бактериоскопического исследования мазков влагалищного секрета IV и III степень чистоты влагалищных мазков после первого же этапа лечения не определялась ни у одной пациентки; II степень была у 9 женщин первой группы (21,5%), 7 – второй (16,7%). У остальных женщин уже после окончания первого этапа лечения определялась I степень чистоты влагалищных мазков. Эти же параметры сохранялись и после второго этапа курсовой терапии.
При ПЦР-диагностике до лечения выявлялся ряд бактериальных инфекций и во всех случаях наблюдения - вирусные инфекции. При обнаружении уреаплазмоза (у 46% женщин), гарднерелеза (у 37%), микоплазмоза (у 2,4% человек), хламидиоза (у 4,8%), кандидоза (у 58%) пациенткам до начала противовирусного лечения назначалось необходимое специфическое лечение. Затем назначалась противовирусная терапия.
После получения медикаментозной терапии и предварительного антибактериального лечения при ПЦР-диагностике случаи хламидиоза и микоплазмоза не были обнаружены. Значительно уменьшилась частота встречаемости уреаплазмоза, кандидоза, гарднерелеза.
После каждого курса медикаментозной терапии на первом этапе лечения оценивались данные ПЦР-диагностики в отношении вирусных инфекций. Обращало на себя внимание, что в первой группе наблюдения после приема первого курса изопринозина значительно уменьшилось содержание герпеса, снизились показатели цитомегалловирусной инфекции, ВПЧ высокого риска; почти не менялись значения данных по вирусу Эпштейн-Бара.
После второго курса приема изоприназина наблюдалось заметное снижение показателей при оценке уровня ВПЧ высокого риска и ЦМВ. После приема третьего курса изопринозина исследуемые вирусные инфекции у пациенток не выявлялись.
Во всех случаях наблюдения значительно снизился уровень показателей вирусных инфекций после всего этапа медикаментозной терапии у женщин первой группы.
Во второй группе наблюдения повторное проведение ПЦР-диагностики было выполнено после первого курса приема изопринозина в сочетании с первым курсом лавомакса. При ПЦР у пациенток второй группы были выявлены единичные случаи сохранившихся повышенных значений ВПЧ высокого риска, ЦМВ и ВЭБ; герпес не определялся ни в одном случае наблюдения (табл.2). В связи с этими изменениями, прием лавомакса был продолжен; все пациентки второй группы дополнительно получили еще 10 табл. лавомакса по 1 табл. через день; при этом повторный курс приема изопринозина не назначался.
Таблица 2. Уровни показателей трансмиссивных инфекций при ПЦР-диагностике
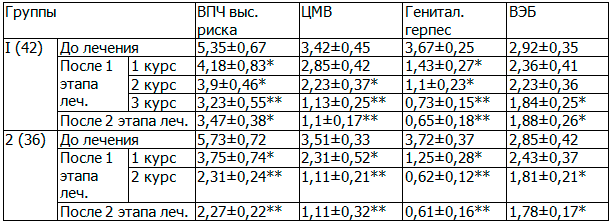
Примечания: показатели в сравнении с данными до лечения * - p
Основные факты
- Вирус папилломы человека (ВПЧ) — это общее название группы вирусов, чрезвычайно широко распространенных во всем мире.
- Известно более 100 типов ВПЧ, из которых не менее 14 являются онкогенными (так называемые вирусы высокого онкогенного риска).
- ВПЧ передается, главным образом, половым путем, и большинство людей заражаются ВПЧ вскоре после начала половой жизни.
- Рак шейки матки развивается в результате передающейся половым путем ВПЧ-инфекции определенных типов.
- В 70% случаев причиной рака шейки матки оказываются ВПЧ двух типов (16 и 18).
- Имеются также доказательства связи ВПЧ с раком заднего прохода, вульвы, влагалища, полового члена и ротоглотки.
- Рак шейки матки — второй по распространенности вид рака среди женщин, проживающих в развивающихся странах. По оценкам, в 2018 г. число новых случаев в этих странах составило 570 000 (84% от всех новых случаев в мире).
- В 2018 г. от рака шейки матки умерло около 311 000 женщин, причем более 85% этих случаев смерти имели место в странах с низким и средним уровнем дохода.
- В комплекс мероприятий по борьбе с раком шейки матки входят первичная профилактика (вакцинация против ВПЧ), вторичная профилактика (скрининг и лечение предраковых поражений), третичная профилактика (диагностика и лечение инвазивного рака шейки матки) и паллиативная помощь.
- Вакцины, формирующие иммунитет к ВПЧ 16-го и 18-го типов, рекомендованы ВОЗ и одобрены к применению во многих странах.
- Одним из экономически эффективных способов профилактики рака шейки матки считается скрининг и лечение предраковых поражений у женщин в возрасте старше 30 лет.
- При выявлении рака шейки матки на ранней стадии возможно полное его излечение.
Общие сведения о ВПЧ
Вирусы папилломы человека (ВПЧ) — возбудители самой распространенной вирусной инфекции половых путей. Большинство ведущих половую жизнь женщин и мужчин рано или поздно приобретают эту инфекцию, а некоторые могут заражаться несколько раз в течение жизни.
Большинство женщин и мужчин заражаются ВПЧ вскоре после начала половой жизни. Инфекция ВПЧ относится к заболеваниям, передающимся половым путем, хотя заражение возможно и при половых контактах без проникновения. Известно, что передача вируса происходит и при простом соприкосновении половых органов.
Среди множества типов ВПЧ многие не представляют опасности для здоровья. ВПЧ-инфекции обычно исчезают за несколько месяцев без какого бы то ни было лечения, и примерно в 90% случаев элиминация инфекции из организма достигается в течение 2 лет. В небольшой доле случаев инфекции ВПЧ определенных типов могут принимать хронический характер и со временем приводить к развитию рака шейки матки.
Рак шейки матки вне всяких сомнений является самым распространенным из заболеваний, связанных с ВПЧ. Почти все случаи рака шейки матки вызваны ВПЧ-инфекцией.
Инфекциями ВПЧ некоторых типов также обусловлена определенная доля случаев рака заднего прохода, вульвы, влагалища, полового члена и ротоглотки, — заболеваний, которые можно предотвратить с помощью тех же методов первичной профилактики, что и рак шейки матки.
Некоторые не онкогенные вирусы папилломы человека, особенно ВПЧ 6-го и 11-го типов, могут приводить к образованию остроконечных кондилом и развитию респираторного папилломатоза (заболевания, при котором опухоли образуются в дыхательных путях, ведущих от носа и полости рта в легкие). Хотя эти патологические состояния очень редко приводят к смерти, распространенность заболевания может быть значительной. Остроконечные кондиломы очень широко распространены, отличаются высокой контагиозностью и отрицательно влияют на половую жизнь.
Каким образом инфекция ВПЧ приводит к развитию рака шейки матки
Несмотря на то, что большинство ВПЧ-инфекций исчезают сами по себе, а предраковые поражения в большинстве случаев самопроизвольно излечиваются, все женщины подвержены риску перехода инфекции в хроническую форму и прогрессирования предраковых поражений в инвазивный рак шейки матки.
У женщин с нормальным иммунитетом рак шейки матки может развиваться в течение 15-20 лет. Однако при нарушениях иммунной системы, например у женщин с нелеченой ВИЧ-инфекцией, этот процесс может занять всего 5–10 лет.
Факторы риска хронической ВПЧ-инфекции и рака шейки матки
- степень онкогенности ВПЧ (способности вируса вызывать рак);
- нарушения иммунитета: люди с ослабленным иммунитетом, в частности, лица, живущие с ВИЧ, подвержены более высокому риску хронической ВПЧ-инфекции и ускоренного развития предраковых поражений и рака;
- наличие сопутствующих инфекций, передающихся половым путем, таких как генитальный герпес, хламидиоз и гонорея;
- количество родов в анамнезе и роды в раннем возрасте;
- курение табака.
Бремя рака шейки матки в мире
Рак шейки матки — четвертый в мире по распространенности вид рака у женщин. Так, в 2018 г. было зарегистрировано около 570 000 новых случаев этого заболевания. Оно является причиной 7,5% всех случаев смерти от онкологических заболеваний среди женщин. Ежегодно от рака шейки матки умирает более 311 000 женщин, причем более 85% этих случаев приходится на развивающиеся страны.
В развитых странах реализуются программы по вакцинации девочек против ВПЧ и ведется регулярный скрининг женщин на ВПЧ-инфекцию. Скрининг позволяет выявлять предраковые поражения на стадиях, на которых они легко поддаются лечению. В этих странах раннее начало лечения позволяет предотвратить развитие рака шейки матки почти в 80% случаев.
В развивающихся странах из-за ограниченного доступа к профилактике рак шейки матки часто остается не выявленным до поздних стадий заболевания и появления клинических симптомов. Кроме того, в этих странах может быть крайне ограничен доступ к лечению поздних стадий рака (например, доступ к онкохирургии, лучевой и химиотерапии), в связи с чем смертность от рака шейки матки там намного выше.
Проведение эффективных лечебно-профилактических мероприятий могло бы позволить снизить высокий показатель смертности от этого заболевания в мире (стандартизированный по возрасту коэффициент смертности в 2018 г.: 6,9 на 100 000).
Комплексный подход к борьбе с раком шейки матки
ВОЗ рекомендует комплексный подход к профилактике и лечению рака шейки матки. В рекомендуемый набор действий входят мероприятия, относящиеся ко всем этапам жизненного цикла. В эту многопрофильную программу должны входить такие компоненты, как просветительская работа в сообществах, мобилизация социальных ресурсов, вакцинация, скрининг, лечение и паллиативная помощь.
Первичная профилактика начинается с вакцинации девочек в возрасте 9–14 лет до начала половой жизни.
В перечень других рекомендуемых профилактических мероприятий для девочек или мальчиков, в зависимости от ситуации, входят:
- информирование о практиках безопасного секса, в том числе о нежелательности раннего начала половой жизни;
- пропаганда использования презервативов и предоставление их тем, кто уже начал половую жизнь;
- предупреждение о вреде употребления табака, к которому многие приобщаются в подростковом возрасте и которое является серьезным фактором риска развития рака шейки матки и других онкологических заболеваний;
- мужское обрезание.
Начиная с 30 лет все женщины, ведущие активную половую жизнь, должны проходить скрининг на атипичные клетки шейки матки и наличие предраковых поражений.
Если для лечения предраковых поражений шейки матки необходимо иссечение участков с атипичными клетками или измененными тканями, рекомендуется применять метод криотерапии, основанный на разрушении патологических тканей путем их замораживания.
При обнаружении признаков рака шейки матки необходимо начинать лечение, вариантами которого могут быть хирургическое вмешательство, лучевая терапия и химиотерапия.
Вакцинация против ВПЧ
В настоящее время существуют три вакцины, которые защищают одновременно от ВПЧ 16-го и 18-го типов, вызывающих не менее 70% случаев рака шейки матки. Одна из этих вакцин обеспечивает дополнительную защиту от трех других онкогенных ВПЧ, ответственных еще за 20% случаев этого заболевания. С учетом того, что вакцины только от ВПЧ 16-го и 18-го типов, обеспечивают также определенный уровень перекрестной защиты от других менее распространенных онкогенных типов ВПЧ, ВОЗ считает, что эти три вакцины являются равноценными средствами профилактики рака шейки матки. Две из этих вакцин защищают также от ВПЧ 6-го и 11-го типов, вызывающих аногенитальные остроконечные кондиломы.
Клинические и пострегистрационные исследования показывают, что вакцины против ВПЧ отличаются высокой безопасностью и высокой эффективностью в предотвращении ВПЧ-инфекций.
Вакцины против ВПЧ дают максимальный эффект, если их вводят до контакта организма с этими вирусами. В связи с этим ВОЗ рекомендует вакцинировать девочек в возрасте от 9 до 14 лет, когда большинство из них еще не начали вести половую жизнь.
Вакцины не лечат ВПЧ-инфекцию и связанные с ВПЧ заболевания, в частности, рак.
В некоторых странах начали вакцинировать и мальчиков, так как вакцинация предотвращает развитие рака половых органов не только у женщин, но и у мужчин, а две из существующих вакцин способны также препятствовать развитию остроконечных кондилом у представителей обоих полов. Рекомендуемая ВОЗ вакцинация девочек в возрасте от 9 до 14 лет представляет собой наиболее эффективное с точки зрения затрат медицинское мероприятие по борьбе с раком шейки матки.
Вакцинация против ВПЧ не отменяет необходимости скрининга на рак шейки матки. В странах, где вакцинация против ВПЧ внедрена в медицинскую практику, может сохраняться необходимость в разработке или усилении программ по скринингу.
Выявление и лечение предраковых поражений
Скрининг на рак шейки матки предусматривает проверку на наличие предраковых и раковых образований у женщин, которые зачастую могут чувствовать себя совершенно здоровыми и у не иметь никаких симптомов заболевания. Если при скрининге обнаруживаются предраковые поражения, их лечение не представляет трудностей и позволяет избежать развития рака. Кроме того, скрининг позволяет обнаруживать рак на ранней стадии, когда высока вероятность полного излечения.
Поскольку предраковые поражения развиваются на протяжении многих лет, скрининг рекомендуется регулярно проходить всем женщинам, начиная с возраста 30 лет (периодичность скрининга зависит от используемого для этого метода). Регулярный скрининг у женщин с ВИЧ-инфекцией, ведущих активную половую жизнь, должен начинаться раньше — с момента, когда они узнают о своем ВИЧ-статусе.
При проведении скрининга необходимо обеспечить возможность последующего лечения и предусмотреть необходимые действия в случае получения положительных результатов теста. Без надлежащей организации таких мероприятий проведение скрининга неэтично.
Существуют три различных типа скрининговых тестов, рекомендуемых ВОЗ в настоящее время:
- тесты на ВПЧ, относящиеся к группе высокого риска;
- визуальная проверка с применением уксусной кислоты;
- традиционный ПАП-тест и метод жидкостной цитологии (ЖЦ).
Для лечения предраковых поражений ВОЗ рекомендует применять методы криотерапии и электрохирургической петлевой эксцизии. При обнаружении более глубоких поражений следует направлять пациенток на дополнительные обследования для принятия обоснованных решений о дальнейших действиях.
Лечение инвазивного рака шейки матки
При наличии у женщины симптомов, позволяющих заподозрить рак шейки матки, ее необходимо направить в специализированное лечебное учреждение для проведения дополнительных исследований, постановки диагноза и лечения.
На ранних стадиях рака шейки матки могут появляться следующие симптомы:
- нерегулярные мажущие кровянистые выделения или слабое кровотечение в период между месячными у женщин детородного возраста;
- мажущие выделения или кровотечение у женщин в постменопаузе;
- кровотечение после полового акта;
- более обильные выделения из влагалища, иногда с неприятным запахом.
По мере прогрессирования рака могут появляться более тяжелые симптомы, в том числе:
- постоянная боль в спине, ногах и (или) в области таза;
- потеря веса, утомляемость, снижение аппетита;
- неприятно пахнущие выделения и дискомфорт во влагалище;
- отек одной или обеих нижних конечностей.
При далеко зашедших формах рака могут развиться и другие тяжелые симптомы, в зависимости от того, на какие органы распространился рак.
Диагноз рака шейки матки должен быть подтвержден результатами гистологического исследования. Стадию заболевания устанавливают на основании размеров опухоли и распространения процесса на область таза и отдаленные органы. Выбор метода лечения зависит от стадии рака, при этом в перечень возможных вариантов входят хирургическая операция, лучевая терапия и химиотерапия. Кроме того, важную роль в ведении пациентов с онкологическими заболеваниями играет паллиативная помощь, позволяющая облегчать боль и страдания, причиняемые болезнью.
Действия ВОЗ
ВОЗ разработала руководство по профилактике рака шейки матки и борьбе с этим заболеванием путем вакцинации, скрининга и лечения инвазивной формы рака. Совместно со странами и партнерами ВОЗ занимается разработкой и осуществлением комплексных программ.
В мае 2018 г. Генеральный директор ВОЗ выступил с призывом к действиям, направленным на ликвидацию рака шейки матки, и предложил странам и партнерам объединить усилия для расширения доступа к мерам профилактики рака шейки матки и увеличения охвата населения. В качестве трех основных мер были названы вакцинация против ВПЧ, скрининг и лечение предраковых поражений, а также ведение пациенток с раком шейки матки.








Существует более 100 типов вируса папилломы человека, из которых, по меньшей мере, 13 приводят к развитию рака шейки матки
Установлено, что рак шейки матки РШМ в 100% случаев обусловлен онкогенными типами вируса папилломы человека(ВПЧ)
Два типа ВПЧ (16 и 18) вызывают 70% всех случаев рака шейки матки (РШМ) и предраковых патологических состояний шейки матки
Рак шейки матки является вторым наиболее распространенным видом рака среди женщин — по оценкам, в 2012 году произошло 530 000 новых случаев заболевания
Ежегодно в России регистрируется порядка 14 000 новых случаев РШМ, что составляет более 30% от всех злокачественных новообразований женских половых органов. Заболеваемость сохраняет тенденцию к росту. На учете по данной патологии состоит в онкологических учреждениях страны более 160 000 женщин. Вероятность заболевания РШМ каждой женщины в России в среднем в течение жизни составляет 0,53%
Высокая глобальную смертность от рака шейки матки (52%), причиной которого является ВПЧ. В 2012 году примерно 270 000 женщин умерли от рака шейки матки, причем более 85% этих случаев смерти произошло в странах с низким и средним уровнем дохода. Ежегодно в Российской Федерации от РШМ умирают около 7 000 женщин
Современные математические модели показывают, что при охвате девочек 12-13 лет полным курсом первичной иммунизации (3 дозы) вакциной против папилломавирусной инфекции, можно прогнозировать снижение рисков развития рака шейки матки на 63%, цервикальной интраэпителиальной неоплазии третьей степени тяжести (предрак) на - 51%, цитологических нарушений в возрастных когортах до 30 лет - на 27%
К концу 2013 года вакцинация против вируса папилломы человека была введена в 55 странах

М. Гомберг.
Причин достаточно
Скачать ( 636.66 Кб ) Чтобы скачать файл, воспользуйтесь встроенными возможнстями вашего браузера
Файл в формате PDF может быть прочитан с помошью бесплатной программы Adobe Reader DC либо встроенными стредствами браузера
Спецпроект "Медицинского вестника": вакцинопрофилактика. Вирус папилломы человека
Общие сведения
Вирус папилломы человека (ВПЧ) — самая распространенная вирусная инфекция половых путей. ВПЧ представляет собой группу вирусов, чрезвычайно широко распространенную во всем мире. Существует более 190 типов данного вируса, из которых по меньшей мере 13 приводят к развитию рака (они известны как типы высокого риска). Вирус папилломы человека передается главным образом при сексуальных контактах, и большинство людей инфицируются им вскоре после того, как начинают вести половую жизнь. Два типа ВПЧ (16 и 18) вызывают 70% всех случаев рака шейки матки (РШМ) и предраковых патологических состояний шейки матки.
Вероятность заболеть
Вирус папилломы человека передается главным образом при сексуальных контактах, и большинство людей инфицируются им вскоре после того, как начинают вести половую жизнь. Но для передачи вируса не обязателен проникающий секс. Телесный генитальный контакт является хорошо установленным путем передачи папилломавирусной инфекции. Группами риска инфицирования ВПЧ являются дети и подростки 15-18 лет.
Рак шейки матки развивается в результате приобретенной половым путем инфекции определенными типами ВПЧ. Факторы риска развития РШМ: первое половое сношение в раннем возрасте; многочисленные сексуальные партнеры; подавление иммунитета (например, ВИЧ-инфицированные люди подвергаются повышенному риску инфицирования ВПЧ и инфицируются более широким спектром типов ВПЧ).
Симптомы и характер протекания заболевания
Большинство инфекций ВПЧ не приводят к появлению симптомов или болезни и проходят сами (около 90% проходят в течение 2-х лет). Однако устойчивая инфекция определенными типами ВПЧ (чаще всего типами 16 и 18) может приводить к развитию предраковых патологических состояний. Без лечения эти состояния могут развиться в рак шейки матки. На сегодняшний день рак шейки матки является самой распространенной болезнью, связанной с вирусом папилломы человека. Рак шейки матки является четвертым среди наиболее распространенных видов рака у женщин, и седьмым в целом: по оценкам, 528 000 новых случаев в мире было в 2012 году.
Симптомы РШМ обычно появляются только на продвинутой стадии рака и могут включать следующие:
- Нерегулярные, межменструальные (в период между месячными) или патологические вагинальные кровотечения после полового акта;
- Боли в спине, ногах или в области таза;
- Усталость, потеря веса, потеря аппетита;
- Неприятные ощущения во влагалище или выделения с неприятным запахом;
- Одна опухшая нога.
На поздних стадиях могут появляться более тяжелые симптомы.
Папилломавирусная инфекция также причастна к 20-90% случаев плоскоклеточного рака ануса, ротоглотки, вульвы, влагалища и полового члена. По оценкам, до 90% всех случаев анального рака обусловлены ВПЧ-16 и ВПЧ-18, а 40% случаев рака вульвы, который встречается в основном у пожилых женщин, ассоциируются с ВПЧ-16.
ВПЧ-инфекции, обусловленные типами низкого риска, вызывают аногенитальные бородавки у мужчин и женщин (остроконечные кондиломы или венерические бородавки). Среднее время между инфицированием типами ВПЧ-6 или 11 и развитием аногенитальных бородавок составляет 11-12 месяцев у мужчин и 5-6 месяцев у молодых женщин16 . Аногенитальные кондиломы с трудом поддаются лечению.
ВПЧ-6 и ВПЧ-11 могут также вызывать редкое состояние, известное как рецидивирующий респираторный папилломатоз (РРП), при котором бородавки формируются в гортани или других частях дыхательных путей. РРП наблюдается в основном у детей в возрасте младше 5 лет (ювенильный РРП) или у лиц на третьем десятке жизни (взрослый РРП). В редких случаях женщины с генитальной ВПЧ-инфекцией могут передать вирус младенцу во время родов. Нелеченный РРП может привести к серьезной проблеме из-за обструкции дыхательных путей.
Установлено, что РШМ в 100% случаев обусловлен онкогенными типами вируса папилломы человека (ВПЧ). У женщин с нормальной иммунной системой рак шейки матки развивается за 15-20 лет. У женщин с ослабленной иммунной системой, например, с ВИЧ-инфекцией при отсутствии лечения, на его развитие может потребоваться лишь 5-10 лет. Несмотря на ограниченные данные об аногенитальных видах рака, отличных от рака шейки матки, все большее число фактических данных свидетельствует о связи вируса папилломы человека с раком ануса, вульвы, влагалища и пениса. И хотя эти виды рака менее распространены, чем РШМ, их связь с ВПЧ делает их потенциально предотвратимыми благодаря использованию таких же стратегий первичной профилактики, как и для рака шейки матки.
Типы ВПЧ, не вызывающие рак (особенно типы 6 и 11), могут вызывать остроконечные кондиломы и респираторный папилломатоз (болезнь, при которой опухоли вырастают в дыхательных путях, ведущих из носа и рта в легкие). И хотя эти состояния очень редко приводят к смерти, они часто могут приводить к заболеванию. Остроконечные кондиломы широко распространены и крайне инфекционны.
Смертность
Наблюдается высокая глобальная смертность от рака шейки матки (52%), причиной которого является вирус папилломы человека. В 2012 году примерно 270 000 женщин умерли от РШМ, причем более 85% этих случаев смерти произошло в странах с низким и средним уровнем дохода. Ежегодно в Российской Федерации от РШМ умирают около 7 000 женщин.
Лечение
Скрининг на РШМ — это тестирование на предраковые состояния и рак среди женщин, не имеющих симптомов и чувствующих себя совершенно здоровыми. Если скрининг выявляет предраковые патологические состояния, их можно легко лечить и тем самым предотвратить развитие рака. Скрининг может также выявить рак на ранней стадии с высокой вероятностью излечения.
С учетом того, что предраковые состояния развиваются на протяжении многих лет, каждой женщине в возрасте 30–49 лет рекомендуется пройти скрининг по меньшей мере один раз в жизни, а лучше – чаще. Скрининг эффективен для снижения смертности от рака шейки матки только в случае участия значительного количества женщин.
В настоящее время доступны 3 разных типа скрининга:
- Обычный тест Папаниколау (Pap) и жидкостная цитология (LBC);
- Визуальная проверка с использованием уксусной кислоты;
- Тестирование на типы ВПЧ высокого риска.
В развитых странах имеются программы, которые предоставляют женщинам возможности для прохождения скрининга, что позволяет выявлять большинство предраковых состояний на стадиях, когда их можно легко лечить. Раннее лечение от вируса папилломы человека позволяет предотвратить до 80% случаев развития РШМ в этих странах.
В развивающихся странах ограниченный доступ к эффективному скринингу означает, что болезнь часто выявляется только на поздних стадиях, когда развиваются симптомы. Кроме того, лечение болезни на таких поздних стадиях малоперспективно, что приводит к высоким уровням смертности от РШМ в этих странах.
Эффективность вакцинации
Результаты клинических испытаний свидетельствуют о том, что существующие сегодня две вакцины безопасны и очень эффективны в профилактике инфекции ВПЧ 16 и 18. Обе вакцины более эффективны, если вакцинация проводится до воздействия вируса папилломы человека. Поэтому предпочтительнее проводить вакцинацию до первого сексуального контакта. Вакцины не лечат инфекцию ВПЧ или связанную с ВПЧ болезнь (такую как рак).
В некоторых странах введена вакцинация мальчиков против вируса папилломы человека с учетом того, что она позволяет предотвращать генитальный рак как у мужчин, так и у женщин, а одна из имеющихся вакцин также позволяет предотвращать развитие генитальных кондилом у мужчин и женщин. Кроме того, вакцинация мальчиков служит для предотвращения циркуляции ВПЧ в популяции подростков и молодых взрослых. ВОЗ рекомендует проводить вакцинацию девочек в возрасте 9-13 лет, так как это является самой эффективной, с точки зрения затрат, мерой общественного здравоохранения против рака шейки матки.
Вакцинация против ВПЧ не заменяет скрининг на рак шейки матки. В странах, где вакцина против ВПЧ введена в действие, может быть также необходимо развитие программ скрининга. К концу 2013 года вакцина против вируса папилломы человека была введена в 55 странах ВОЗ.
Современные математические модели показывают, что при охвате девочек 12-13 лет полным курсом первичной иммунизации (3 дозы) вакциной против папилломавирусной инфекции, можно прогнозировать снижение рисков развития рака шейки матки на 63%, цервикальной интраэпителиальной неоплазии третьей степени тяжести (предрак) – на 51%, цитологических нарушений в возрастных когортах до 30 лет – на 27%.
Вакцины
В настоящее время имеются две вакцины, которые защищают от 16 и 18 типов вируса папилломы человека, вызывающих по меньшей мере 70% раковых заболеваний шейки матки. Эти вакцины могут также обеспечивать некоторую перекрестную защиту от других, менее распространенных типов ВПЧ, вызывающих РШМ. Одна из этих вакцин защищает также от типов ВПЧ 6 и 11, которые вызывают аногенитальные кондиломы.
Последние эпидемии
Рак шейки матки является вторым по распространённости видом рака среди женщин — по оценкам, в 2012 году произошло 530 000 новых случаев заболевания.
Ежегодно в России регистрируется порядка 14 000 новых случаев РШМ, что составляет более 30% от всех злокачественных новообразований женских половых органов. Заболеваемость сохраняет тенденцию к росту. На учете по данной патологии в онкологических учреждениях страны состоит более 160 000 женщин. Вероятность заболевания РШМ каждой женщины в России в среднем в течение жизни составляет 0,53%.
Исторические сведения и интересные факты
В середине семидесятых годов двадцатого века ученый Гарольд цур Хаузен обнаружил, что женщины, страдающие раком шейки матки, неизменно заражены вирусом папилломы человека. В 1983 году он обнаружил ДНК папилломавируса в биопсии рака шейки матки, и это событие можно считать открытием онкогенного вируса ВПЧ-16. В 2008 году Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины Гарольду цур Хаузену за открытие того, что вирус папилломы может вызывать рак шейки матки.
Читайте также:


