Как вылечить герпесвирусную инфекцию
В статье рассматриваются некоторые аспекты этиопатогенеза герпесвирусных заболеваний у детей, современные подходы к лекарственной терапии и профилактике рецидивов.
This article discusses some aspects of the pathogenesis of herpes-associated diseases in children, modern approaches to drug therapy and relapse prevention.
В последние годы среди основных возбудителей вирусных инфекций у детей особое место занимают герпес-вирусы, что связано с их повсеместным распространением, широким разнообразием, полиорганностью поражения, многообразием клинических проявлений, а также высокой частотой хронического течения. Герпес-ассоциированные заболевания входят в число наиболее распространенных и плохо контролируемых инфекций человека. Это связано с тем, что герпес-вирусы могут длительно бессимптомно циркулировать в организме человека с нормальной иммунной системой, а при иммуносупрессии способствовать развитию тяжелых заболеваний, вплоть до угрожающих жизни генерализованных инфекций. Так, по данным Всемирной организации здравоохранения (World Health Organization, WHO), смертность от герпетической инфекции составляет около 16% и находится на втором месте после гепатита среди вирусных заболеваний [1].
.jpg)
Герпес-вирусы (от греч. ?ρπειν (herpein) — ползать) — семейство ДНК-вирусов, объединены в семейство Herpesviridae, которое включает в себя 8 классифицируемых видов вирусов человека: вирусы простого герпеса — вирус простого герпеса (ВПГ-1) и вирус генитального герпеса (ВПГ-2), вирус варицелла зостер, вирус Эпштейна–Барр, цитомегаловирус, вирус герпеса человека 6-го, 7-го, 8-го типов, а также около 80 неклассифицируемых вирусов герпеса человека и животных. К подсемейству α-герпес-вирусов относятся ВПГ-1, ВПГ-2 и вирус варицелла зостер, которые характеризуются быстрой репликацией в различных типах клеток и обладают цитопатическим действием на культуры инфицированных клеток. Бета-герпес-вирусы (цитомегаловирус, вирусы герпеса 6-го и 7-го типов) также поражают различные виды клеток, приводят к увеличению их размеров (цитомегалия), могут способствовать развитию иммуносупрессивных состояний. К подсемейству γ-герпес-вирусов относятся вирус Эпштейна–Барр и вирус герпеса 8-го типа — вирус, ассоциированный с саркомой Капоши (KSHV). Их характеризует тропность к лимфоидным клеткам (Т- и В-лимфоцитам), в которых они могут длительно персистировать. В некоторых случаях способны вызывать развитие лимфомы, саркомы [2].
Вирионы герпес-вирусов термолабильны — они инактивируются в течение 30 мин при температуре 50–52 °C, в течение 20 ч — при температуре 37,5 °C, но хорошо переносят лиофилизацию. На металлических поверхностях (монеты, дверные ручки, водопроводные краны) герпес-вирусы выживают в течение 2 ч, на пластике и дереве — до 3 ч, на влажных медицинских материалах (вата и марля) — до их высыхания при комнатной температуре (до 6 ч). Уникальность герпес-вирусов заключается в том, что они способны непрерывно или циклично размножаться в инфицированных клетках тропных тканей (персистенция), а также пожизненно сохраняться в морфологически и иммунохимически видоизмененной форме в нервных клетках регионарных нервных ганглиев (латенция) и реактивироваться под влиянием различных экзо- и эндогенных провоцирующих факторов. Однако способность к персистенции и латенции у различных штаммов неодинаковая: наиболее активны в этом отношении вирусы простого герпеса, наименее — вирус Эпштейна–Барр.
По данным многочисленных исследований, к 18 годам более 90% жителей городов инфицируются одним или несколькими штаммами вирусов. Основной путь инфицирования — воздушно-капельный, при прямом контакте или через предметы обихода (общие посуда, полотенца, носовые платки и пр.). Отмечается также оральный, генитальный, трансфузионный, трансплантационный и трансплацентарный пути передачи инфекции. ВПГ 1-го и 2-го типов, цитомегаловирус входят в число возбудителей TORCH-инфекций, способствуют развитию серьезных заболеваний новорожденных и детей младшего возраста. Вирусы простого герпеса, цитомегаловирус, вирус Эпштейна–Барр рассматриваются как индикаторы СПИДа в связи с их частым обнаружением при данном заболевании [3, 4]. С герпес-вирусами связывают развитие синдрома хронической усталости (Chronic fatigue syndrome — CFS) [5].
Клинически герпес-инфекция у детей может протекать в виде ветряной оспы (вирус варицелла зостер), инфекционного мононуклеоза (вирус Эпштейна–Барр), внезапной экзантемы (вирус герпеса человека 6-го и 7-го типов), афтозного стоматита (ВПГ 1-го или 2-го типа), мононуклеозоподобного синдрома (цитомегаловирус). У подростков и взрослых людей часто инфекция протекает бессимптомно, что объясняется как биологическими свойствами штаммов, так и индивидуальными особенностями иммунного ответа. Часто при снижении иммунореактивности организма герпес-вирусы выступают в качестве вирусов-оппортунистов, приводя к более тяжелому течению основного заболевания, развитию осложнений. Велика роль герпесвирусных инфекций, особенно цитомегаловирусной, в формировании младенческой смертности. Наибольшую угрозу для жизни и здоровья детей представляют герпетические нейроинфекции — летальность при них достигает 20%, а инвалидизация — 50%. Тяжело протекают офтальмогерпес (развитие катаракты или глаукомы — до 50%), генитальный герпес, генерализованная форма Эпштейна–Барр-вирусной инфекции (инфекционного мононуклеоза) [1, 6].
Герпесвирусная инфекция относится к трудноконтролируемым заболеваниям. Несмотря на разнообразие лекарственных препаратов, использующихся для лечения данной патологии, средств, обеспечивающих полное излечение, не существует. Это обусловлено генотипическими особенностями возбудителя, формированием резистентности герпес-вирусов и молекулярной мимикрией.
Открытые с помощью методов молекулярной биологии механизмов репликации герпес-вирусов, а также изучение взаимодействия вируса с клеткой позволили создать целый ряд эффективных химиотерапевтических средств, обладающих противогерпетической активностью. Однако, эффективно купируя острые проявления инфекции, они не предотвращают рецидивирования, не всегда снижают частоту рецидивов.
Учитывая, что при герпес-ассоциированных инфекциях, как и при других хронических заболеваниях с длительной персистенцией вируса, развиваются иммунодефицитные состояния, для повышения эффективности лечения в схемы терапии наряду с противовирусными препаратами приходится включать препараты, способствующие коррекции иммунного статуса больного. Все это диктует необходимость правильно подбирать лекарственное средство, его дозу и длительность приема, при необходимости использовать комбинацию различных препаратов, избегая при этом полипрагмазии. Определенную сложность терапии в детском возрасте вызывают возрастные ограничения для ряда лекарственных средств, наличие нежелательных лекарстввенных реакций (НЛР) и противопоказаний.
В настоящее время для лечения герпесвирусных заболеваний и профилактики рецидивов используют следующие группы препаратов (табл.).
При лечении герпес-инфекций следует придерживаться комплексного подхода. Длительность и интенсивность терапии определяются возрастом больного, клинической формой заболевания, тяжестью его течения, а также наличием осложнений и сопутствующей патологии. Лечебно-профилактические мероприятия следует разделять на несколько этапов.
- Острый период болезни (рецидив) — охранительный режим, лечебное питание, противовирусные препараты, интерфероны и их индукторы. По показаниям назначаются иммуноглобулины, антибактериальные препараты местного и системного действия, глюкокортикоиды, нейро- и ангиопротекторы, гепатопротекторы, кардиотропные препараты, ингибиторы протеаз. Симптоматическая терапия может включать жаропонижающие, отхаркивающие и муколитические препараты.
- Ремиссия, стихание основных клинических проявлений (иммуномодуляторы, адаптогены растительного происхождения, пре- и пробиотики, витамино-минеральные комплексы).
- Профилактика рецидивов (специфическая профилактика — вакцинация, санация хронических очагов инфекции, восстановление иммунного статуса и пр.).
Следует отметить, что сочетанное применение противовирусных препаратов и иммунобиологических средств имеет ряд преимуществ. Во-первых, комплексная терапия обеспечивает синергидный эффект. Во-вторых, позволяет снизить дозу противовирусного химиопрепарата, уменьшая вероятность развития НЛР, сокращая его токсическое воздействие на организм и снижая вероятность возникновения устойчивых штаммов герпес-вирусов. Кроме того, это значительно сокращает продолжительность острого периода болезни и сроки лечения.
Одним из препаратов, показавшим свою эффективность при лечении герпес-ассоциированных заболеваний у детей, является инозин пранобекс. Инозин пранобекс — это синтетическое комплексное производное пурина, обладающее иммуностимулирующей активностью и неспецифическим противовирусным действием. Препарат восстанавливает функции лимфоцитов в условиях иммунодепрессии, повышает бластогенез в популяции моноцитарных клеток, стимулирует экспрессию мембранных рецепторов на поверхности Т-хелперов, оказывает стимулирующее влияние на активность цитотоксических Т-лимфоцитов и естественных киллеров, функции Т-супрессоров и Т-хелперов, повышает продукцию иммуноглобулина G, интерферонов, интерлейкинов (ИЛ-1 и ИЛ-2), снижает образование провоспалительных цитокинов (ИЛ-4 и ИЛ-10), потенцирует хемотаксис нейтрофилов, моноцитов и макрофагов. Механизм противовирусного действия препарата связан с ингибированием вирусной РНК и фермента дигидроптероатсинтетазы, участвующего в репликации, усилении подавленного вирусами синтеза мРНК лимфоцитов, что сопровождается угнетением биосинтеза вирусной РНК и трансляции вирусных белков.
Инозин пранобекс малотоксичен, хорошо переносится, в России рекомендован в виде таблеток детям с 3-летнего возраста (масса тела более 15 кг). За рубежом он доступен и в форме сиропа и не имеет возрастных ограничений. Препарат назначается по 50–100 мг/кг/сут внутрь в 3–4 приема в течение всего острого периода болезни (5–10 дней в зависимости от длительности вирусемии и выраженности синдрома интоксикации). В качестве поддерживающей терапии для восстановления иммунологических показателей возможно назначение препарата по иммуномодулирующей схеме (50 мг 2 раза в день в течение 14–28 дней). Доказана высокая эффективность курсовой терапии инозином пранобексом (50 мг/кг массы тела в сутки в 3–4 приема внутрь, три курса лечения по 10 дней с интервалом 10 дней) [7], комбинированной курсовой терапии с использованием инозина пранобекса и рекомбинантного интерферона α-2β (3 курса по 10 дней с интервалом 14 дней) у детей с микст-вирусными инфекциями [8].
Применение инозина пранобекса как препарата с иммунотропным и противовирусным действием на различных этапах лечебно-профилактических мероприятий позволяет избежать полипрагмазии, тем самым снизить медикаментозную нагрузку на организм и уменьшить риск нежелательных эффектов.
Литература
- Кускова Т. К., Белова Е. Г. Семейство герпес-вирусов на современном этапе // Лечащий Врач. 2004, № 5, с. 64–69.
- Hjalgrim H., Askling J., Rostgaard K. et al. Characteristics of Hodgkin’s lymphoma after infectious mononucleosis // N. Engl. J. Med. 2003; 349: 1324–1332.
- Никольский И. С., Юрченко В. Д., Никольская К. И. Характеристика активной хронической Эпштейна–Барр вирусной инфекции: клинико-иммунологический синдром // Современные инфекции. 2003, № 3, с. 60–62.
- Katz B. Z., Shiraishi Y., Mears C. J., Binns H. J., Taylor R. Chronic fatigue syndrome after infectious mononucleosis in adolescents // Pediatrics. 2009, Jul; 124 (1): 189–193.
- Lerner A. M., Begar S. N., Deeter R. G. IgM serum antibodies to Epstein-Barr virus are uniquely present in a subset of patients with the chronic fatigue syndrome // In Vivo. 2004, Mar-Apr; 18 (2): 101–106.
- Maakaroun N. R., Moanna A., Jacob J. T., Albrecht H. Viral infections associated with haemophagocytic syndrome // Rev. Med. Virol. 2010, Mar; 20 (2): 93–105.
- Симованьян Э. Н., Денисенко В. Б., Григорян А. В. Эффективность применения инозина пранобекс у часто болеющих детей с хронической Эпштейна-Барр вирусной инфекцией: результаты рандомизированного исследования // Вопросы современной педиатрии. 2011, Т. 10, № 2, С. 16–21.
- Нестерова И. В., Ковалева С. В., Чудилова Г. А., Ломтатидзе Л. В., Клещенко Е. И., Шинкарева О. Н. Динамика изменений фенотипа и функциональной активности нейтрофильных гранулоцитов у иммунокомпрометированных детей с повторными ОРВИ, ассоциированными с герпесвирусными инфекциями, на фоне комбинированной интерфероно- и иммунотерапии // Цитокины и воспаление. 2014, Т. 13, № 1, с. 113.
Т. А. Бокова, доктор медицинских наук, профессор
ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, Москва
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Герпесвирусы широко распространены в человеческой популяции. После первичного инфицирования вирусы герпесгруппы переходят в латентное состояние и пожизненно персистируют в организме. При неблагоприятных условиях и снижении местного или системного иммунитета может происходить реактивация инфекции, что обусловливает развитие воспаления чаще всего на местном уровне. Разнообразие клинических форм герпесвирусных инфекций постоянно поддерживает научный интерес как в области изучения их патофизиологии, так и в области поиска эффективной противовирусной терапии. Особенно актуально это для β- и γ-герпесвирусов, т. к. группа α-герпесвирусов изучена достаточно хорошо.
Цель исследования: определить эффективность валацикловира в отношении репликации вируса Эпштейна – Барр (ВЭБ), вируса герпеса человека 6 типа (ВГЧ-6), цитомегаловируса (ЦМВ) в ротоглотке у часто болеющих взрослых с хроническими воспалительными заболеваниями верхних дыхательных путей (ВДП).
Материал и методы: нами амбулаторно обследованы 80 пациентов с частыми рецидивами хронических воспалительных заболеваний ВДП. Всем пациентам проводились микробиологическое исследование мазков из ротоглотки и оценка вирусной нагрузки в смешанной слюне и цельной крови вне периода обострения. Пациенты получали терапию валацикловиром по схеме 500 мг 3 р./сут в течение 14 дней. Контроль вирусной нагрузки в биоматериале проводился после окончания лечения.
Результаты и обсуждение: микробный пейзаж ротоглотки часто болеющих взрослых вне периода обострения представлен преимущественно нормальной или условно-патогенной микрофлорой. В смешанной слюне обнаруживалась ДНК ВЭБ, ВГЧ-6, но не ЦМВ. При этом в образцах крови указанных пациентов ДНК вирусов герпесгруппы не выявлялась. Применение валацикловира в дозе 500 мг 3 р./сут достоверно снижает репликацию ВЭБ в ротоглотке у часто болеющих взрослых.
Выводы: целесообразно провести дальнейшие исследования по определению режима дозирования и оценке клинической эффективности ациклических нуклеозидов в лечении ВЭБ-инфекции.
Ключевые слова: герпесвирусы, вирус Эпштейна – Барр, вирус герпеса человека, цитомегаловирус, часто болеющие взрослые, вирусная нагрузка, валацикловир.
Для цитирования: Щубелко Р.В., Зуйкова И.Н., Шульженко А.Е. Герпесвирусные инфекции человека: клинические особенности и возможности терапии. РМЖ. 2018;8(I):39-45.
Human herpesviruses infections: clinical features and opportunities of therapy
R.V. Shubelko 1 , I.N. Zuykova 2 , A.E. Shulzhenko 2
1 JSC "K+31", Moscow
2 “National Research Center — Institute of Immunology” Federal Medical-Biological Agency of Russia, Moscow
Herpesviruses are widely spread among the human population. After the primary infection, the herpesviruses become latent and persistent in the human body for life. Adverse conditions and a low local or systemic immunity may reactivate the infection, which causes the inflammation, usually at the local level. The variety of clinical forms of herpesviruses infections constantly supports scientific interest both in the field of studying their pathophysiology and in the search for effective antiviral therapy. This is especially important for β- and γ-herpesviruses, since the α-herpesvirus group has been studied rather well.
Aim: to determine the efficacy of valacyclovir for replication of the Epstein-Barr virus (EBV), human herpesvirus type 6 (HHV-6), cytomegalovirus (CMV) in the oropharynx in frequently ill adults with chronic inflammatory diseases of the upper respiratory tract.
Patients and Methods: 80 patients with frequent recurrences of chronic inflammatory diseases of the upper respiratory tract were examined outpatiently. All patients underwent microbiological examination of swabs from the oropharynx and the viral load in mixed saliva and whole blood not in exacerbation period was assessed. Patients received valacyclovir therapy according to the scheme 500 mg x 3 times a day for 14 days. Control of viral load in the biomaterial was carried out after the end of treatment.
Results and Discussion: out of the period of exacerbation the oropharynx microflora in frequently ill adults is represented mainly by a normal or conditionally pathogenic microflora. EBV DNA, HHV-6, but not CMV DNA, were detected in the mixed saliva. The DNA of the herpesvirus was not detected in the blood samples of these patients. The use of valacyclovir in a dose
of 500 mg 3 times a day significantly reduces the replication of EBV in the oropharynx in frequently ill adults.
Conclusions: it is advisable to conduct further studies to determine the dosage regimen and evaluate the clinical efficacy of acyclic nucleosides in the treatment of EBV infection.
Key words: herpes viruses, Epstein-Barr virus, human herpes virus, cytomegalovirus, frequently ill adults, viral load, valacyclovir.
For citation: Shubelko R.V., Zuykova I.N., Shulzhenko A.E. Human herpesviruses infections: clinical features and opportunities of therapy // RMJ. 2018. № 8(I). P. 39–45.
В статье рассмотрены клинические особенности и возможности терапии герпесвирусных инфекции человека. Определена эффективность валацикловира в отношении репликации вируса Эпштейна – Барр, вируса герпеса человека 6 типа, цитомегаловируса.
Только для зарегистрированных пользователей
Поиск по сайту
Соцсети
По теме
"Простуда" на губах не лечится алоэ, льдом, корвалолом или зеленкой, а генитальный герпес – содовыми ваннами. "Накачка" губ гиалуроновой кислотой может спровоцировать обострение герпеса. Об этом написала и.о. главы Минздрава Ульяна Супрун на своей странице в Facebook.
Она отметила, что герпесвирусов есть целая семья: герпесвирус человека (ГВЛ) 1 и 2 типа, вирусы ветрянки, Эпштейна-Барр, цитомегаловирус и вирусы герпеса человека 6, 7 и 8. Вирус 2-го типа вызывает преимущественно генитально-анальные инфекции, а 1-го – уро-лабиальные (ротовой полости, губ, других частей головы). Впрочем, оба вирусы могут поражать все части тела, то есть во время орального секса "простуда на губах", может передаться на гениталии партнера/партнерши или наоборот.
Что известно о вирусе:
- герпесвирус 2 типа передается во время незащищенного секса, а также во время вагинальных родов, если у матери в этот момент есть обострение герпеса;
- герпесвирус 1 типа может передаваться через общую посуду, когда инфекция проявляется активно;
- большинство людей заражаются ГВЛ-1 в возрасте до 5 лет от родителей или других детей;
- во время бритья лица есть риск распространить свой вирус с участка проявления в волосяных фолликулах кожи. Это повлечет за собой так называемый "герпетический сикоз";
- люди, занимающиеся контактными видами спорта, могут благодаря ударам получать собственный вирус на новых участках тела, например, на челюсти или ухе;
- даже стоматологи, которые работают без перчаток, могут получить инфекцию ногтей и кутикулы после контакта с человеком, у которого гингивостоматит (одно из проявлений герпеса).
Герпесвирусы 1 и 2 типа диагностируют методом ПЦР или серологическими методами, то есть выявляют или ДНК вируса, либо антитела к нему. В случае обнаружения ГВЛ нужно сделать еще анализ на ВИЧ. Рутинный скрининг ГВЛ не нужен.
Возможно ли выздороветь после заражения
После заражения - вирусы уже никогда никуда не деваются, а находятся в нейронах и время от времени активируются. Триггером может быть ультрафиолет, механическое повреждение нерва, временное или постоянное нарушение иммунитета. Во время активации латентного вируса новые вирионы транспортируются по нейронам к слизистым оболочкам, и вызывают язвы и высыпания на коже.
"Впрочем, проявления заболевания не длятся постоянно. Это хорошо, потому что человек не живет в состоянии постоянного дискомфорта. Но плохо то, что в это время вирус может передаваться дальше. Со временем обострения инфекции становятся все реже. Для уменьшения их частоты, продолжительности, или полного предотвращения используют постоянную или периодическую терапию системными противовирусными препаратами", – написала Супрун.
Как лечить герпесвирусную инфекцию
Первичный курс терапии обычно длится 8-10 дней или до исчезновения проявлений. При этом прописывают препараты системного действия, а именно – таблетки на основе измененных нуклеотидов. В случае очень тяжелого течения инфекции возможно внутривенное введение лекарств. Медицинские протоколы не советуют пользоваться лекарствами с местным действием из-за их низкой эффективности. Герпес на лице часто начинается с продрома – периода, когда болезнь можно ощутить как покалывание, зуд, боль, но еще нельзя увидеть. Если начать терапию в период продрома, то это может остановить проявление болезни.
Постоянная супрессивная терапия на 70-80% снижает вероятность проявления генитального герпеса у людей, склонных к частым обострениям (6 или более в течение года). Такой подход (постоянная терапия) улучшает качество жизни пациентов значительно эффективнее, чем эпизодическая (раз в год). Но со временем частота проявлений инфекции уменьшается сама собой, поэтому рано или поздно постоянную терапию можно заменить эпизодической.
Как предотвратить заражение герпесом
- не целуйтесь, если у партнера/партнерши губы или ротовая полость начали чесаться, покалывать, или появились высыпания;
- не пейте вместе из одной чашки или бутылки с человеком, у которого герпес на губах;
- не пользуйтесь общей гигиенической помадой;
- сделайте с партнером/партнершей анализы на ВИЧ, герпес 1 и 2 типов,онкогенные штаммы папилломавируса человека и сифилис. В случае отсутствия инфекций достаточно гормональных контрацептивов. Если у одного из партнеров генитальный герпес, то во время обострений и проявлений от секса нужно воздержаться, даже защищенного. В остальное время нужно пользоваться презервативами.
Как рожать, если у матери герпес
В большинстве случаев герпетическая инфекция новорожденных случается у детей матерей без предварительных данных о заболевания в анамнезе. То есть он был, но никак не проявлялся. Если заражение произошло перед родами, то риск передачи 30-50%. Если мать имела эпизодические проявления генитального герпеса ранее, или заразилась в течение 1-го триместра, то вероятность передачи вируса ребенку меньше 1%.
Здоровым женщинам, чьи партнеры имеют герпесвирусную инфекцию, стоит воздержаться от незащищенного секса в течение 3-го триместра. Если у женщины не было проявлений ГВЛ-1 (на губах), то следует воздержаться во время беременности от орального секса с партнером-носителем вируса. Перед родами женщине необходимо обследоваться по поводу генитального герпеса. Если есть проявления, то рекомендуют делать кесарево сечение.
Что делать, чтобы герпес был постоянно в латентном состоянии
- пользоваться солнцезащитными кремами;
- перед поездкой в горы или на море, где высокий индекс УФ, можно пройти превентивный курс противогерпесными препаратами;
- никакие "иммуностимуляторы" не предотвращают повторного появления герпетической инфекции;
- нет доказательств эффективности мазей с антигерпетическими компонентами;
- если герпес проявляется 1-3 раза в год, то лучше обойтись эпизодической терапией (раз в год или в случае обострения) – иначе есть риск развития устойчивого к терапии штамма вируса;
- люди, чья иммунная система ослаблена противоопухолевой терапией, иммуносупрессией в связи с трансплантацией, или ВИЧ-инфицированным людям следует предотвращать обострения герпеса медикаментозно и постоянно;
- перед введением филеров в лицо или проведением дермабразии надо провести короткий курс терапии противогерпесными препаратами, если есть понимание, что существует риск проявления герпеса.
Герпесвирусные инфекции - группа инфекционных заболеваний, которые вызываются вирусами из семейства Herpesviridae, могут протекать в виде локализованных, генерализованных, рецидивирующих форм болезни, имеют способность к персистированию (постоянному нахождению вируса) в организме человека.
Герпесвирусные инфекции (ГВИ) относятся к наиболее распространенным вирусным болезням человека. Инфицированность и заболеваемость ими каждый год возрастает. Во всех странах мира 60-90% населения инфицированы тем или иным герпесвирусом.
Этиология
Герпесвирусы в своем составе содержат двунитчатую ДНК, имеют глико-липопротеиновую оболочку. Размеры вирусных частиц от 120 до 220 нм.
- два типа вируса простого герпеса (HSV-1, HSV-2),
- вирус ветряной оспы и опоясывающего герпеса (VZV или HHV-3),
- вирус Эпштейн-Барр (ЕBV или HHV-4),
- цитомегаловирус (CMV или HHV-5), HHV-6, HHV-7, HHV-8.
На основе биологических свойств вирусов сформированы 3 подсемейства герпесвирусов: (альфа-герпесвирусы, бетта-герпесвирусы и гамма-герпесвирусы). К a-герпесвирусам относятся HSV-1, HSV-2, VZV.
К бета-герпесвирусам относятся CMV, HHV-6, HHV-7. Они, как правило, медленно размножаются в клетках, вызывают увеличение пораженных клеток (цитомегалия), способны к персистенции, преимущественно в слюнных железах и почках, могут вызывать врожденные инфекции. К гамма-герпесвирусам относятся ЕBV и HHV-8.
Вирус простого герпеса 1 и 2 типов
Термин "герпетическая инфекция" (ГИ) обычно употребляется относительно заболеваний, которые вызываются HSV-1 и HSV-2. Источником HSV-инфекции являются больные люди различными формами заболевания, в том числе и латентной, а также вирусоносители.
HSV-1 передается воздушно-капельным и контактным путем. Попавший на кожу во время кашля, чихания вирус, находящийся в капельках слюны, выживает в течение часа. На влажных поверхностях (умывальник, ванна и прочее) он сохраняет жизнеспособность в течение 3-4 часов, что нередко является причиной вспышек заболеваний в детских дошкольных учреждениях. Заражение может осуществляться при поцелуях, а также через предметы обихода, которые инфицированы слюной больного или вирусоносителя. HSV-2 передается половым или вертикальным путем. При последнем инфицирование происходит во время родов (контакт с родовыми путями матери), трансплацентарно или через цервикальный канал в полости матки. В связи с тем, что при генерализации инфекции имеет место вирусемия, возможен также трансфузионный или парентеральный путь передачи HSV-2 инфекции. HSV-2 вызывает, как правило, генитальный и неонатальный герпес.
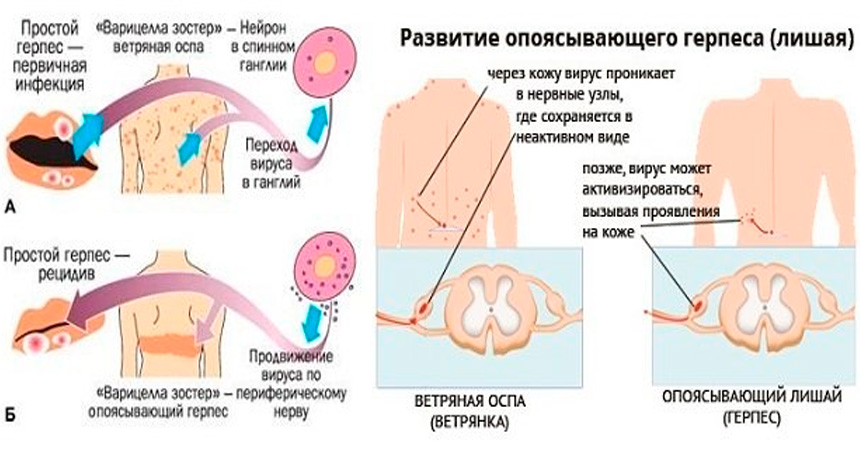
Наибольшая восприимчивость у детей к ГИ в возрасте от 5 месяцев до 3 лет. В зависимости от механизма заражения различают приобретенную и врожденную форму ГИ. Приобретенная ГИ может быть первичной и вторичной (рецидивирующая), локализованной и генерализованной. Также выделяют латентную форму ГИ.
Ни одна инфекция не имеет такого многообразия клинических проявлений, как герпесвирусная. Она может вызывать поражение глаз, нервной системы, внутренних органов, слизистой оболочки желудочно-кишечного тракта, полости рта, гениталий, может являться причиной онкологических заболеваний, имеет определенное значение в неонатальной патологии и возникновении гипертонии. Распространение вируса в организме происходит гематогенным, лимфогенным, нейрогенным путем.
Частота первичной герпесвирусной инфекции возрастает у детей после 6 месяцев жизни, когда полученные от матери антитела исчезают. Пик заболеваемости приходится на возраст 2—3 года. Нередко ГИ встречается и у новорожденных детей, по данным ряда авторов диагностируется у 8% новорожденных с общесоматической патологией и у 11% недоношенных детей.
По данным ВОЗ, заболевания, обусловленные вирусом простого герпеса (HSV), занимают второе место после гриппа среди причин смертности от вирусных инфекций. Решение проблемы диагностики и лечения герпесвирусной инфекции с проявлениями на слизистой оболочке полости рта — одна из важнейших задач практической медицины.
В последнее десятилетие во всем мире значение герпесвирусных заболеваний как проблемы общественного здравоохранения постоянно растет. Представители семейства герпесвирусов человека поражают до 95% населения мира.
К первичным формам ГИ относятся: инфекция новорожденных (генерализованный герпес, энцефалиты, герпес кожи и слизистых), энцефалиты, гингивостоматиты, герпетиформная экзема Капоши, первичный герпес кожи, глаз, герпетический панариций, кератиты. Первичная ГИ возникает вследствие первичного контакта человека с HSV. Как правило, это происходит в раннем детском возрасте (до 5 лет). У взрослых в возрасте 16-25 лет, которые не имеют противовирусного иммунитета, первичная ГИ чаще может быть обусловлена HSV-2. Латентно переносят заболевание 80-90% первично инфицированных детей, и только в 10-20% случаев наблюдаются клинические проявления болезни.
Вторичными, рецидивирующими формами ГИ является герпес кожи и слизистых оболочек, офтальмогерпес, герпес половых органов.
Эпштейн-Барр-вирусная инфекция
Инфекционное заболевание, которое вызывается вирусом Эпштейн-Барр (ЕBV) и характеризуется системным лимфопролиферативным процессом с доброкачественным или злокачественным течением.
ЕBV выделяется из организма больного или вирусоносителя с орофарингеальным секретом. Передача инфекции происходит воздушно-капельным путем через слюну, часто во время поцелуев матерью своего ребенка, поэтому иногда ЕBV-инфекцию называют "болезнью поцелуев". Дети нередко заражаются ЭБВ через игрушки, загрязненные слюной больного ребенка или вирусоносителя, при пользовании общей посудой, бельем. Возможен гемотрансфузионный путь передачи инфекции, а также половой. Описаны случаи вертикальной передачи ЕBV от матери к плоду, предполагают, что вирус может быть причиной внутриутробных аномалий развития. Контагиозность при ЕBV-инфекции умеренная, что, вероятно, связано с низкой концентрацией вируса в слюне. На активацию инфекции влияют факторы, снижающие общий и местный иммунитет. Возбудитель ЕBV-инфекции имеет тропизм к лимфоидно-ретикулярной системе. Вирус проникает в В-лимфоидные ткани ротоглотки, а затем распространяется по всей лимфатической системе организма. Происходит инфицирование циркулирующих В-лимфоцитов. ДНК-вируса проникает в ядра клеток, при этом белки вируса придают инфицированным В-лимфоцитам способность беспрерывно размножаться, вызывая так называемое "бессмертие" В-лимфоцитов. Этот процесс является характерным признаком всех форм ЕBV-инфекции.
ЕBV может вызывать: инфекционный мононуклеоз, лимфому Беркитта, назофарингеальную карциному, хроническую активную ЕBV-инфекцию, лейомиосаркому, лимфоидную интерстициальную пневмонию, "волосатую" лейкоплакию, неходжкинскую лимфому, врожденную ЕBV-инфекцию.
Варицелла-зостер-инфекция
Varicella-zoster вирус вызывает ветряную оспу и опоясывающий герпес. Источником инфекции при ветряной оспе может быть только человек, больной ветряной оспой или опоясывающим герпесом, включая последние 24-48 часов инкубационного периода. Реконвалесценты ветряной оспы остаются заразными на протяжении 3-5 дней после прекращения высыпаний на коже. Через третье лицо заболевание не передается. Возможно внутриутробное заражение ветряной оспой в случае заболевания беременной. Ветряная оспа может встречаться в любом возрасте, но в современных условиях максимальное количество больных приходится на детей в возрасте от 2 до 7 лет. Опоясывающий герпес развивается после первичного инфицирования вирусом Varicella-zoster, после перехода инфекции в латентную форму, при которой вирус локализуется в спинальных, тройничном, сакральном и других нервных ганглиях. Возможна эндогенная реактивация инфекции.
Цитомегаловирусная инфекция
Инфекционное заболевание, которое вызывается цитомегаловирусом (CMV) и характеризуется разнообразными клиническими формами (от бессимптомной до тяжелой генерализованной с поражением многих органов) и течением (острым или хроническим). Факторами передачи CMV могут быть практически все биологические субстраты и выделения человека, в которых содержится вирус: кровь, слюна, моча, ликвор, вагинальный секрет, сперма, амниотическая жидкость, грудное молоко. Потенциальным источником инфекции являются органы и ткани в трансплантологии, а также кровь и ее продукты в трансфузиологии. Пути передачи CMV-инфекции: воздушно-капельный, половой, вертикальный и парентеральный.
Различают врожденную и приобретенную формы CMV-инфекции. Врожденная CMV-инфекция. При антенатальном инфицировании плода заражение происходит преимущественно трансплацентарно. При интранатальном инфицировании CMV поступает в организм при аспирации инфицированных околоплодных вод или секретов родовых путей матери.
У детей более старшего возраста приобретенная CMV-инфекция в 99% случаев протекает в субклинической форме. Наиболее частым проявлением такой формы CMV-инфекции у детей в возрасте старше года является мононуклеозоподобный синдром. Как правило, наблюдается клиника острого респираторного заболевания в виде фарингита, ларингита, бронхита.
Инфекции, вызванные шестым, седьмым и восьмым типами герпесвирусов Герпесвирусы шестого типа (HHV-6) могут явиться причиной эритематозной и розеолезной сыпи (внезапная экзантема), поражений ЦНС и костного мозга у иммуноскомпроментированных детей. Герпесвирусы седьмого типа (HHV-7) вызывают экзантему новорожденных
Для диагностики герпетической инфекции ценным являются цитологический, иммунофлюоресцентный, серологический и ПЦР методы.
Вирусологическое исследование при герпетической инфекции выявляет комплементсвязывающие антитела к ВПГ-1 или -2 в крови матери, пуповинной крови плода и амниотической жидкости.
ПЦР-метод. Материалом для исследования на герпес являются кровь, мазки из глотки, содержимое пузырьков, язв, моча.
Важное значение имеет исследование специфических антител различных подклассов: IgM, IgG1-2, IgG3 и IgG4 к герпес-вирусам. Выявление в сыворотке крови детей специфических иммуноглобулинов М, IgG3, IgG1-2 в титре > 1:20, вирусного антигена и специфических иммунных комплексов с антигеном свидетельствует об остроте инфекционного процесса (активная фаза), а определение только специфических IgG4 расценивается как латентная фаза инфекции или носительство материнских антител.
Лечение
- 1 этап – в активной стадии или при обострении хронического течения заболевания;
- 2 этап – пролонгированное лечение поддерживающими дозами в период ремиссии;
- 3 этап – выявление и санация хронических очагов инфекции, обследование членов семьи для выявления источника инфицирования.
Во всех случаях препараты, их комбинация и длительность подбираются индивидуально с учетом проявлений заболевания, особенности иммунной системы ребенка, возраста, течения заболевания.
Читайте также:


