Интеркуррентные инфекции что это такое
Аннотация научной статьи по клинической медицине, автор научной работы — Сонина О.И., Кикинская Е.Г., Лыскина Г.А., Зиновьева Г.А.
Болезнь Шенлейна-Геноха (БШГ) первичный системный иммунный микротромбоваскулит, наиболее распространенный в детском возрасте. Характеризуется преимущественно поражением сосудов кожи, суставов, брыжейки и слизистой оболочки кишечника, почек. Этиология болезни БШГ до сих пор неизвестна. Предполагают роль бактериальной, в частности, стрептококковой или вирусной инфекции. БШГ заболевание, прогноз и исходы которого полностью зависят от ранней диагностики и правильно проводимого лечения. Целью исследования явилось определение возможной роли инфекционных факторов в развитии и течении БШГ, а также принципов терапии инфекционно_ассоциированных вариантов заболевания. Выявлена высокая частота инфекционных факторов и хронических очагов инфекции при рецидивирующем, торпидном течении БШГ. Убедительно показана необходимость сочетания современной патогенетической терапии с антиинфекционными методами лечения для снижения частоты рецидивирующих форм БШГ и улучшения прогноза.
Похожие темы научных работ по клинической медицине , автор научной работы — Сонина О.И., Кикинская Е.Г., Лыскина Г.А., Зиновьева Г.А.
Role of infection in development and course of Shonlein-Henoch disease
ShÖnlein-Henoch disease (SHD) is primary systemic immune microthrоmbovasculitis, very frequent in childhood. It is characterized by prevalent lesion of skin capillaries and vessels of joint synovial layer, mesenterium and intestinal mucosa. SHD etiology is still unknown. Role of bacterial infection, including streptococcal infection, and viral infections is suspected. SHD is the disease whose prognosis and outcome depends mainly on early diagnosis and proper management. The aim of present study was to study possible role of infectious factors in development and course of SHD, and to review therapeutic approaches in cases of infection_associated SHD. Authors showed important role of acute infections and chronic focuses of infection in cases of torpid and recurrent SHD and proved the necessity of combination of pathogenetic methods and anti_ infection treatment for decreasing of recurrent SHD rate and for improvement of SHD prognosis.
В ПОМОЩЬ ПРАКТИЧЕСКОМУ ВРАЧУ
О.И. Сонина, Е.Г. Кикинская, Г.А. Лыскина, Г.А. Зиновьева
РОЛЬ ИНФЕКЦИИ В РАЗВИТИИ И ТЕЧЕНИИ БОЛЕЗНИ ШЕНЛЕЙНА-ГЕНОХА У ДЕТЕЙ
Кафедра детских болезней ММА им. И.П. Сеченова, Москва
Болезнь Шенлейна—Геноха (БШГ) — первичный системный иммунный микротромбоваскулит, наиболее распространенный в детском возрасте. Характеризуется преимущественно поражением сосудов кожи, суставов, брыжейки и слизистой оболочки кишечника, почек. Этиология болезни БШГ до сих пор неизвестна. Предполагают роль бактериальной, в частности, стрептококковой или вирусной инфекции. БШГ — заболевание, прогноз и исходы которого полностью зависят от ранней диагностики и правильно проводимого лечения. Целью исследования явилось определение возможной роли инфекционных факторов в развитии и течении БШГ, а также принципов терапии инфекционно-ассоциированных вариантов заболевания. Выявлена высокая частота инфекционных факторов и хронических очагов инфекции при рецидивирующем, тор-пидном течении БШГ. Убедительно показана необходимость сочетания современной патогенетической терапии с антиинфекционными методами лечения для снижения частоты рецидивирующих форм БШГ и улучшения прогноза.
Shonlein—Henoch disease (SHD) is primary systemic immune microthrombovasculitis, very frequent in childhood. It is characterized by prevalent lesion of skin capillaries and vessels of joint synovial layer, mesenteri-um and intestinal mucosa. SHD etiology is still unknown. Role of bacterial infection, including streptococcal infection, and viral infections is suspected. SHD is the disease whose prognosis and outcome depends mainly on early diagnosis and proper management. The aim of present study was to study possible role of infectious factors in development and course of SHD, and to review therapeutic approaches in cases of infection-associated SHD. Authors showed important role of acute infections and chronic focuses of infection in cases of torpid and recurrent SHD and proved the necessity of combination of pathogenetic methods and anti- infection treatment for decreasing of recurrent SHD rate and for improvement of SHD prognosis.
Болезнь Шенлейна-Геноха (БШГ) (пурпура Шенлейна-Геноха, геморрагический васкулит) относится к системным иммунокомплексным заболеваниям с преимущественным поражением микроциркуляторного русла и занимает по частоте 1-е место среди системных васкулитов (СВ) [1, 2]. Заболевание может возникнуть в любом возрасте, но чаще страдают дети и подростки [1, 3].
Этиология БШГ до сих пор неизвестна. Предполагают роль бактериальной, в частности, стрептококковой или вирусной инфекции [4, 5]. Провоцирующими факторами могут быть переохлаждение, избыточная инсоляция; пищевая, лекарственная аллергия; профилактические прививки; обострение очагов хронической инфекции и др. [4, 6]. В ряде случаев провоцирующие факторы, приведшие к развитию БШГ, установить не удается. В механизме развития заболевания определяющим является образование циркулирующих иммунных комплексов (ЦИК) [5, 7], избыточное количество которых активирует систему комплемента (С). В результате образуется крупный иммунный комп-
лекс (АГ+АТ+С), который оседает на эндотелии сосудов и повреждает его. В ответ на повреждение вырабатываются фактор некроза опухоли, фактор активации тромбоцитов, протеазы, что приводит к усилению адгезии и агрегации тромбоцитов, образованию тромбоцитарных тромбов, развитию локальной гиперкоагуляции. В сосудистой стенке микроциркуляторного русла происходит иммунное воспаление - васкулит, что способствует повышенной проницаемости сосудов с выходом из них в ткани плазмы и эритроцитов. Считают, что отложение крупных ИК при БШГ вызывает поражение кожи и суставов, а мелкие ИК обусловливают абдоминальный синдром и почечные поражения [2, 8].
В последние годы имеется тенденция к увеличению смешанных форм заболевания [5, 8]. Тяжесть течения БШГ и ее прогноз по-прежнему определяются вовлечением в патологический процесс почек [8, 9]. Проблемой остаются рецидивирующие формы болезни. По данным литературы, у 50-80% таких больных встречаются бактериальные, вирусные, паразитарные инфекции, кото-
О.И. Сонина, Е.Г. Кикинская, Г.А. Лыскина, Г.А. Зиновьева
рые не только провоцируют начало, но и поддерживают рецидивирование заболевания [10]. Поэтому в лечении БШГ используют различные методы подавления инфекционного фактора, прежде всего антибиотикотерапию. Можно полагать, что достигнутый в последние годы прогресс в выявлении бактериальных и вирусных агентов делает возможным поиск более эффективных этиотроп-ных методов лечения очагов инфекции. В связи с этим целью настоящего исследования явилось определение возможной роли инфекционных факторов в развитии и течении БШГ, а также принципов терапии инфекционно-ассоциированных вариантов заболевания.
Материалы и методы исследования
Наблюдали 130 детей в возрасте 5-16 лет с БШГ, из которых у 76 (58,4%) определялась смешанная форма с поражением почек, у 42 (32,3%) -смешанная форма БШГ без поражения почек и только 12 (9,2%) детей имели простую форму болезни. У 92 больных (70,7%) болезнь носила рецидивирующий характер. Анализировали особенности преморбидного фона и клинического статуса больных. Особое внимание уделяли клиническому и лабораторному поиску инфекционных факторов у заболевших. Все больные получали патогенетическую антикоагулянтную и/или антиаг-регантную терапию. При Шенлейна-Геноха-неф-рите (ШГН) в зависимости от варианта назначали глюкокортикоиды (ГК) с цитостатиками; в тяжелых случаях проводили инфузионную терапию.
Результаты и их обсуждение
При клинико-инструментальном и лабораторном обследовании у 121 (93%) из 130 больных выявлены очаги хронической инфекции (или персистирование возбудителей бактериальных и вирусных инфекций), обострение которых провоцировало или поддерживало рецидивирующее течение заболевания.
108 детей (82%) имели от 2 до 5 различных очагов инфекций (см. рисунок). Чаще других встречались хронический тонзиллит (71,5%), туб-инфицированность (26,6%), множественный кариес зубов (13,1%), рецидивирующая гепервирус-ная инфекция 1-го типа (36,7%), паразитарные инвазии (9,2%), хронический гайморит (8,5%). При лабораторном обследовании с высокой частотой определяли повышение титров гемолитичес-
й Е- Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
ких антистрептококковых антител (48,5%), наличие стрептококка в мазках из зева (85,2%), реже - вируса простого герпеса 1-го типа (36,7%). Методом реакции агглютинации с эритроцитарны-ми диагностикумами выявлены диагностические титры антител к шигеллам Флекснера, Зонне, сальмонеллам, иерсиниям (Y. pseudotuberculosis u enterocolitica). Наличие хламидийной инфекции доказано с помощью серологических методов (ИФА) в соскобах из конъюктивы и уретры.
В комплекс лечения помимо патогенетической терапии входила этиотропная терапия сопутствующих инфекционных заболеваний, профилактика обострений хронических очагов инфекции и предупреждение интеркуррентных инфекций. Учитывая высокий процент выявленных очагов инфекции бактериальной природы, антибиотики использовали у подавляющего большинства детей (100). Однократный курс антибактериальной терапии проведен у 42 больных, у остальных - повторный, так как наблюдались частые обострения очагов хронической инфекции или эпизоды острых инфекционных заболеваний. В случаях диагностированной персис-тирующей герпесвирусной инфекции 1-го типа назначали виферон. В результате назначения антибактериальной терапии, воздействующей на сопутствующие инфекционные заболевания, также отмечена явная положительная динамика в купировании клинических симптомов БШГ, особенно макрогематурии, протеинурии, кожных геморрагических высыпаний, транзиторной эритроцитурии.
В комплексе лечения 10 больным с затяжным или хроническим рецидивирующим течением
Эффективность лечения сопутствующей инфекционной патологии
Методы лечения n Исходы БШГ Эффективность, %
Антибактериальная терапия интеркуррентных инфекционных заболеваний 100 79 21 79,0
Тонзиллэктомия/ Аденотомия 27 26 1 96,3
Лечение хронической патологии ЛОР-органов 83 65 18 78,3
Противотуберкулезная терапия 35 25 10 71,4
Санация полости рта 17 14 3 82,4
Лечение хронической, соматической патологии, ассоциированной с инфекцией 50 35 15 70,0
Таким образом, проведенное исследование показало важную роль инфекционных факторов в развитии и характере течения БШГ у детей. Это делает обоснованным использование антибактериальных и антивирусных средств лечения в случае БШГ, ассоциированной с персистирующей инфекцией. Выявлено, что из 105 больных, выздоровевших или имевщих стойкую длительную ремиссию, у 90 (86,7%) рецидивы БШГ прекратились после лечения выявленных инфекций. Среди де-
2. Семенкова Е.Н. Системные васкулиты. М.: Медицина, 1988.
3. Баркаган Л.З. Нарушение гемостаза у детей. М.: Медицина, 1993.
4. Кикинская Е.Г. Лечение, исходы и качество жизни при болезни Шенлейна-Геноха у детей. Автореф. дисс. канд. мед. наук. М., 2000.
5. Davin Jean-Claude, Weening J.J. Henoch-Schonlein purpura nephritis: an update. Eur. J. Pediatr. 2001; 160: 689-695.
6. Кривошеев О.Г. Системные сосудистые пурпуры - кли-нико-этиологический варианты. Автореф. дисс. канд. мед. наук. М., 1999.
тей с рецидивирующим течением БШГ в 100% случаев наступление ремиссии было четко связано с систематическим или радикальным лечением сопутствующих очагов инфекции (см. таблицу). Проведение тонзиллэктомии и/или аденотомии (в 96,3% случаев - у 26 из 27 оперированных), лечение хронической патологии ЛОР-органов (78,3%), специфическая противотуберкулезная химиопро-филактика (71,4%), санация полости рта (82,4%), лечение хронической соматической патологии, ассоциированной с инфекцией (70%), способствовали прекращению рецидивов БШГ развитию кли-нико-лабораторной ремиссии ШГН.
1. Рецидивирующее течение БШГ ассоциируется с сопутствующим хроническим инфекционным процессом и определяет сложность терапевтической тактики.
2. Современная и своевременная патогенетическая терапия в сочетании с антибактериальными и противовирусными средствами при БШГ, протекающей на фоне инфекции, - путь к снижению рецидивирующих и хронических форм БШГ.
3. Использование в комплексном лечении БШГ нового поколения антибиотиков с широким спектром действия, ИГВВ, противовирусных препаратов способствовало снижению частоты трудно купируемых форм заболевания.
9. Лыскина ГА, Кикинская Е.Г., Зиновьева ГА., Фролкова Е.В. Поражение почек при болезни Шенлейна-Геноха у детей. Педиатрия. 2005; 5: 22-28.
10. Ozen S. The spectrum of vasculitis in children. Best Pract. Res. Clin. Reumatol. 2002; 16: 411-425.
1. Данилина ЗА. Клиника и лечение капилляротоксикоза 7. Борисова Е.В. Геморрагический васкулит у детей. Педи-
у детей. М.: Медгиз, 1961. атрия. 2004; 6: 51-56.
И.Е. Шахбазян, Е.И. Алексеева
Протокол лечения ювенильного ревматоидного артрита
Кафедра детских болезней Московской медицинской академии им. И.М. Сеченова
Ювенильный ревматоидный артрит (ЮРА) — хроническое воспалительное заболевание суставов неизвестной этиологии, характеризующееся сложным аутоиммунным патогенезом, неуклонно прогресси рующим течением, возможным вовлечением в процесс внутренних органов и частым развитием инвалидности у детей.
Многие врачи пользуются отечественной классификацией ЮРА, однако наиболее принятой в последнее время является классификация, разработанная Американской коллегией ревматологов.
ЮРА с системными проявлениями (интермитти рующая лихорадка, ревматоидная сыпь, гепатоспленомегалия, лимфаденопатия, полисерозит, миалгии, артралгии, лейкоцитоз и анемия). В зависимости от количества пораженных суставов и преобладания тех или иных системных проявлений выделяют:
А) олигоартрит с преобладанием экссудативных изменений в суставах в сочетании с интермиттирующей лихорадкой, ревматоидной сыпью, гепатоспленомегалией, лимфаденопатией, полисерозитом, гиперлейкоцитозом, анемией (согласно отечествен ной классификации — аллергосептический вариант ЮРА);
В) полиартрит или генерализованный артрит с преобладанием пролиферативных изменений в суставах, быстрым развитием деформации суставов, контрактур и поражением шейного отдела позвоночника в сочетании с лимфаденопатией, гепатоспленомегали ей, анемией, умеренным лейкоцитозом, реже лихорадкой, сыпью и полисерозитом (согласно отечественной классификации — вариант Стилла)
2. Полиартикулярный вариант ЮРА без системных проявлений:
A) серопозитивный подтип (с наличием ревматоидного фактора — РФ);
B) серонегативный подтип (без РФ)
3. Олигоартикулярный вариант ЮРА без системных проявлений:
A) подтип с наличием антинуклеарного фактора, без РФ и с высоким риском развития иридоциклита;
B) подтип с наличием антигена гистосовмести мости HLA B27, без РФ и с повышенным риском развития иридоциклита
Заболевание, в клинической картине которого преобладают лихорадка, сыпь, лимфаденопатия, гепатоспленомегалия, гиперлейкоцитоз в сочетании с артралгиями, но без стойкого артрита, рассматривается в качестве ревматоидоподобного заболевания (псевдосепсис Висслера—Фанкони).
Лечебная тактика в значительной степени определяется формой заболевания. Сначала приведем протокол лечения полиартикулярных и олигоартикулярных вариантов ЮРА.
Полиартикулярный вариант ЮРА
A) серопозитивный подтип (с наличием РФ)
В этой группе больных преобладают девочки школьного возраста. Клинические проявления: симметричный полиартрит с деформацией суставов у 50% больных, со снижением массы тела и отставанием в росте.
Целесообразно следующее лечение: раннее начало базисной терапии, нестероидные противовоспалительные препараты (НПВП), внутрисуставное введение глюкокортикоидов (ГК) при наличии синовита, местная терапия противовоспалительными мазями и гелями, массаж, ЛФК, реабилитационные мероприятия (ввиду частого развития инвалидности, связанной с деформацией суставов).
В) серонегативный подтип (без РФ)
Этот вариант может сопровождаться внесустав ными клиническими проявлениями (субфебрилитет, реакция ретикулогистиоцитарной системы, кардит). Частота развития инвалидности достигает 15%.
Целесообразна та же схема лечения, что и при подтипе "А". В случаях присоединения внесуставных проявлений показаны сеанcы пульс-терапии ГК, при обнаружении вирусной или вирусно-бактериальной инфекции — курсы антибактериальной терапии, включая внутривенное введение человеческого иммуноглобулина.
Олигоартикулярный вариант ЮРА
А) подтип с наличием антинуклеарного фактора, без РФ и с высоким риском развития иридоциклита
Иначе называется "болезнью маленьких девочек" (так как возникает в возрасте от нескольких месяцев до 3 лет). Клинические проявления: в основном поражаются голеностопные и коленные суставы, поражение других суставов наблюдается редко; у 30—50% больных развивается иридоциклит. Артрит протекает доброкачественно, остаточные офтальмоло гические изменения (в том числе слепота) отмечаются у 10—20% больных.
Целесообразно следующее лечение: НПВП в сочетании с базисными препаратами, местное лечение суставов, при наличии синовита — внутрисуставное введение ГК, постоянное наблюдение окулиста.
Местное лечение иридоциклита проводится окулистом и включает раннее назначение мидриатиков в виде инстилляций, субконъюнктивальных инъекций атропина, скополамина, адреналина и ГК (преднизолона и дексаметазона). При наличии осложнений (катаракта) показано хирургическое лечение.
В) подтип с наличием антигена гистосовмести мости HLA B27, без РФ и с повышенным риском развития иридоциклита
В этой группе преобладают мальчики школьного возраста с поражением крупных суставов нижних конечностей — коленных, тазобедренных и крестцово-подвздошных. Острый иридоциклит возникает у 5—10% больных. Необходимо исключить хламидийную инфекцию, псориаз.
Целесообразна та же схема лечения, что и при подтипе "А". При обнаружении хламидийной инфекции показаны антибиотики класса макролидов в сочетании с иммуномодуляторами.
Схемы применения базисных препаратов:
Метотрексат — по 7,5—10 мг/м 2 /нед. Курс лечения не менее 2 лет. Может оказывать гепатотоксическое действие.
Плаквенил — при массе тела >33 кг по 6,5 мг/кг/сут. Курс лечения длительный. Основной побочный эффект — развитие ретинопатии.
Сульфасалазин — по 30—40 мг/кг/сут (дозу следует повышать до расчетной постепенно). Курс лечения длительный. Может оказывать гепатотоксическое действие и вызывать цитопению (преимущест венно лейкопению).
Схемы применения НПВП:
Вольтарен — по 2—3 мг/кг/сут. Основной побочный эффект (как у большинства НПВП) — язвенные поражения слизистой оболочки желудочно-кишечного тракта. Можно принимать в течение многих лет под контролем гастроскопии.
Бруфен (ибупрофен) — по 30—40 мг/кг/сут в течение длительного времени (от нескольких месяцев до нескольких лет). Может оказывать гепатотоксическое действие.
Напроксен (напросин) — по 10—20 мг/кг/сут в течение длительного времени (от нескольких месяцев до нескольких лет). Можно назначать только детям после 10 лет.
Флугалин (флурбипрофен) — по 5 мг/кг/сут в течение 2—3 мес.
Реже применяют аспирин — по 60—80 мг/кг/сут, но не более 2,5—3,0 г/сут. Курс лечения 2—3 мес.
Системные варианты ЮРА
У части больных до появления суставного синдрома в клинической картине преобладают лихорадка, ревматоидная сыпь, гепатоспленомегалия, лимфаденопатия, полисерозит, гиперлейкоцитоз, анемия, миалгия, артралгия. Это состояние расценива ется как ревматоидоподобное заболевание (псевдосепсис Висслера—Фанкони), которое в последующем может трансформироваться в ЮРА.
Цель лечения — купирование системных проявлений, суставного синдрома (при его наличии) и активности интеркуррентной инфекции. Для этого применяются:
1) пульс-терапия метилпреднизолоном в низких дозах (достижение быстрого противовоспалительно го эффекта). Доза препарата — по 5—10 мг/кг на 1 введение; число введений от 1 до 5 каждый день или через день в зависимости от выраженности миоперикардита, пневмонита, васкулита, полисерозита, лихорадки;
2) иммуноглобулин для внутривенного введения (достижение заместительного и "мягкого" иммуносупрессивного эффекта). Доза препарата — по 0,3—1 г/кг на курс; вводится ежедневно или через день в зависимости от тяжести состояния;
3) антибиотики (при системных проявлениях, лейкоцитозе с нейтрофильным сдвигом влево, наличии активной интеркуррентной инфекции). Предпочтение следует отдавать препаратам широкого спектра действия (аминогликозиды — лучше амикацин, цефалоспорины третьего и четвертого поколений и др.), назначая их внутривенно или внутримышечно в течение 7—10 дней; доза препарата зависит от возраста больного;
4) внутрисуставное введение метилпреднизо лона или дипроспана (при наличии экссудата, болевого синдрома и нарушения функции позволяет купировать суставной синдром, пролонгировать противовоспалительный эффект пульс-терапии метилпреднизолоном). Доза препаратов при введении в крупные суставы — 1,0 мл; в средние — 0,5—0,7 мл; в мелкие суставы кистей — 0,1—0,2 мл. В каждый сустав ГК вводятся не чаще 1 раза в 1—3 мес;
5) пероральные ГК (при неэффективности пульс-терапии метилпреднизолоном, внутрисуставного введения ГК, терапии иммуноглобулином для внутривенного введения) в дозе 0,2—0,3 мг/кг/сут, но не более 0,5 мг/кг/сут; длительность приема — не более года. Пероральные ГК нецелесообразно использовать в качестве препаратов первого ряда для длительного лечения ЮРА, учитывая их тяжелые побочные эффекты;
6) НПВП — наиболее безопасен и эффективен вольтарен в дозе 2—3 мг/кг/сут;
7) симптоматическая терапия.
Истинные системные варианты ЮРА
Системный вариант ЮРА с олигоартритом (аллергосептический вариант ЮРА)
Системный вариант ЮРА с генерализованным артритом (вариант Стилла)
Цель терапии — купирование системных проявлений, активности интеркуррентной инфекции и суставного синдрома, предотвращение прогрессирования структурных изменений в суставах и развития инвалидности.
При наличии опасных для жизни системных проявлений тактика лечения аналогична таковой при псевдосепсисе Висслера—Фанкони.
Кроме того, применяются иммуносупрессивные препараты — циклоспорин А и метотрексат. Показания к назначению метотрексата в низких дозах (5—10 мг/м 2 /нед): вариант Стилла у детей дошкольного и школьного возраста, пограничная с суставной полиартикулярной формой ЮРА без опасных для жизни системных проявлений, без развития инвалидно сти и гормональной зависимости. Показания для назначения циклоспорина А: тяжелое течение аллергосептического варианта ЮРА и варианта Стилла — полиартикулярный или генерализованный суставной синдром; функциональная недостаточность суставов с возможным ограничением способности к самообслуживанию; непрерывно рецидивирующее течение заболевания со значительно повышенными СОЭ (>40 мм/ч), содержанием С-реактивного белка и иммуноглобулина G в сыворотке крови; коксит, асептический некроз головок бедренных костей; гормональная зависимость.
Дозы циклоспорина А: при аллергосептическом варианте ЮРА — по 4,0—4,5 мг/кг/сут; при варианте Стилла — по 3,5—4,0 мг/кг/сут; при наличии коксита и асептического некроза головки бедренной кости — по 4,5—5,0 мг/кг/сут.
Сроки назначения иммуносупрессивных препаратов — в течение первого и не позднее второго года болезни; продолжительность лечения — не менее 2 лет. Отменить препараты можно в случае сохранения клинико-лабораторной ремиссии в течение года.
Критерии безопасности — оценку показателей функции печени, почек и общий анализ крови следует повторять каждые 2 нед. Артериальное давление у больных, получающих циклоспорин А, надо измерять ежедневно.
Сопутствующая терапия — для уменьшения вероятности развития побочных эффектов метотрексат и циклоспорин А должны применяться в сочетании не более чем с одним препаратом группы НПВП (вольтарен, бруфен). При этом дозу НПВП следует снизить в 1,5—2 раза, а при лечении циклоспорином А НПВП вообще можно отменить. Допускается сочетанное применение иммуносупрессивных препаратов с пероральными ГК.
Тактика отмены пероральных ГК — категоричес ки противопоказана отмена преднизолона, назначенного в дозе 1,0 мг/кг/сут и выше, в течение 2—4 мес после достижения терапевтического эффекта; не менее 6 мес ребенок должен получать поддержива ющую дозу (как правило, 5—10 мг/сут). Скорость снижения дозы ГК определяется исходной суточной дозой. При исходной дозе 15 мг/сут и более ее снижение должно составлять по 1,25 мг 1 раз в 3—4 дня. При снижении исходной дозы с 15 до 10 мг/сут — по 1,25 мг 1 раз в 5—7 дней. При снижении исходной дозы с 10 до 5 мг/сут — по 1 /8 таблетки через день (в течение 5 дней ребенок находится на интермиттиру ющем режиме лечения, т.е. получает по четным дням исходную дозу препарата, а по нечетным она снижается на 1 /8 таблетки. В отсутствие синдрома отмены в течение следующих 5 дней ребенок постоянно принимает исходную дозу препарата без 1 /8 таблетки). При снижении исходной дозы с 5 мг/сут до полной отмены — по 1 /8 таблетки 1 раз в 1,5 мес (2 нед интермиттирующего приема, а затем 4 нед постоянно го приема в новом дозовом режиме вплоть до полной отмены).
Таким образом, раннее проведение дифференци рованной патогенетической терапии ЮРА позволит купировать системные проявления, предотвратить деструкцию суставов, снизить частоту развития инвалидности и повысить качество жизни детей.
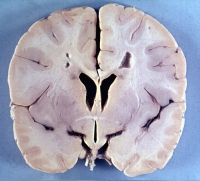
Это прогрессирующее демиелинизирующее заболевание, которое преимущественно поражает младенцев и детей и имеет наследственный характер.
редкое, в основном, генетически обусловленное заболевание. Его развернутая клиническая картина представляет собой двигательные, координаторные нарушения, проблемы с речью и приемом пищи. Почти все взрослые больные живут не более 10 лет с момента развития заболевания. Наиболее точным методом диагностики является генетический. Способы лечения находятся в стадии разработки, больным в настоящее время помогают только симптоматическими средствами.
В 95 % случаев болезнь Александера развивается в результате мутации в гене GFAP (локус 17q21.31). Мутация преимущественно возникает спонтанно.
Тип наследования – аутосомно-доминантный.
У 5 % людей, у которых диагностирована болезнь Александера, подобный или иной генетический дефект не обнаруживается, то есть причина развития остается неизвестной.
- отвечает за продукцию глиального фибриллярного кислого белка GFAP. GFAP – промежуточный филамент ЦНС (астроцитов и эпендимы)
- участвует в астроцит-нейронной связи
- участвует в передаче нервного импульса
- формирует ГЭБ
- репарирует ЦНС после травмы
Патогенез
В случае мутации измененный белок GFAP накапливается нейроглии, что препятствует обеспечению нейронов питательными веществами.
Кроме того, при болезни Александера в самом измененном белке GFAP образуются узелковые образования, которые называют волокнами Розенталя. Последние мешают нормальному проведению нервных импульсов по миелиновым волокнам.
Инфантильная форма
- развивается в раннем детском возрасте, в среднем в 6 месяцев.
- плохой аппетит, частые срыгивания вплоть до рвоты.
- отмечается патологически быстрое увеличение размеров головы, нарастание внутричерепного давления.
- дети плохо прибавляют в весе, поздно начинают держать голову, садиться и ползать.
- по мере роста и развития ребенка развивается мышечная слабость в конечностях (парезы) наряду с повышенным мышечным тонусом (спастичность), что проявляется ограничением объема и силы произвольных движений.
- гиперкинезы, в частности, хореоатетоз.
- возможны судорожные эпилептические припадки.
- страдает интеллект: дети не узнают близких, их не радуют игрушки, они не овладевают навыками
также нарушается координация движений, наблюдаются подергивания глазных яблок. - самостоятельная ходьба практически невозможна.
- заболевание неуклонно прогрессирует и заканчивается смертью в течение 2-3 лет.
Ювенильная форма
- Проявляется в возрасте от 4 до 14 лет, в среднем — около 9 лет.
- голова имеет больший размер по сравнению со сверстниками.
- нарушения речи (смазанность, нечеткость), поперхивание при приеме пищи, а затем и при глотании воды.
- голос приобретает гнусавый оттенок.
- движения языком затрудняются.
- бульбарные и псевдобульбарные расстройства, возникают в результате поражения ствола мозга.
- по утрам больных беспокоят неукротимые рвоты.
- появляется мышечная слабость в конечностях, которая постепенно нарастает.
- мышечный тонус увеличивается, мышцы становятся плотными и твердыми на ощупь, появляются патологические стопные признаки (симптом Бабинского и другие).
- возможны нарушение равновесия, расстройства поведения.
- у больных с ювенильной формой периодически регистрируют рефлекторную остановку дыхания: апноэ.
- в конце концов, прогрессирующее поражение нервной системы заканчивается смертельным исходом, в среднем, через 10 лет от появления начальных клинических признаков заболевания.
Взрослая форма
- развивается в сроки от 20 до 70 лет.
- клинические симптомы довольно разнообразны, поскольку могут быть отражением патологии любого участка головного мозга.
- парезы и параличи с повышенным мышечным тонусом, нарушения координации движений и равновесия, непроизвольные неконтролируемые движения, нарушения речи и глотания.
- снижение интеллекта незначительное.
- часто выявляется нистагм и нарушение содружественных движений глазными яблоками.
- болезнь прогрессирует и неизбежно заканчивается летальным исходом (обычно от присоединения интекуррентных инфекций).
МРТ - диагностика
- выявляется демиелинизация различных отделов мозга (при инфантильной и юношеской формах — преимущественно в лобных с распространением на другие области, при взрослой — более выражена в мозжечке и стволе мозга).
- расширение боковых желудочков.
- преобладание лобной доли.
- снижение плотности белого вещества ГМ.
Другие методы диагностики
Лечение – симптоматическое
- при парезах назначают стимуляторы нервно-мышечной проводимости (Нейромидин);
- при спастичности мышц — миорелаксанты (Баклофен, Сирдалуд, Мидокалм);
- при эпилептических припадках — противосудорожные препараты (Вальпроаты, Сибазон и другие);
- для уменьшения непроизвольных движений могут использоваться нейролептики (Галоперидол, Азалептин и другие).
Прогноз
Неблагоприятный
- неонатальная – продолжительность жизни до 12 месяцев после манифестации симптомов;
- инфантильная – до 2-3 лет;
- ювенильная и взрослая – до 10 лет.
- Основные причины смерти – интеркуррентные инфекции и прогрессирующее поражение нервной системы
Выполнилa:
студентка 2 группы,
5 курса,
І медицинского факультета
Ивахненко Д.А.
Читайте также:


