Инфекционный фактор при воспалении
Глава 2. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ И СОСТОЯНИЯ – ОСНОВА РАЗВИТИЯ ЗАБОЛЕВАНИЙ ИНФЕКЦИОННОЙ ПРИРОДЫ
2.1. ВОСПАЛЕНИЕ – ТИПОВОЙ ПАТОЛОГИЧЕСКИЙ ПРОЦЕСС В РАЗВИТИИ ИНФЕКЦИОННОЙ ПАТОЛОГИИ
2.1.1. Этиологические факторы и общая характеристика воспаления
Воспаление - это типовой патологический процесс, возникающий в ответ на действие разнообразных патогенных факторов экзогенной или эндогенной природы, характеризующийся развитием стандартного комплекса сосуди-стых и тканевых изменений.
Описание внешних признаков воспаления относится к I веку до н.э., когда Цельс обратил внимание на закономерность возникновения при воспалении таких признаков, как краснота (rubor), жар (calor), припухлость (tumor), боль (dolor). Гален указал на неизбежность нарушения функций при воспалении (functio laesa).
Этиологические факторы, вызывающие воспаление, могут иметь инфек-ционную и неинфекционную природу. Индукторами воспаления являются механические, физические, химические альтерирующие агенты.
Развитие воспалительного процесса может быть следствием инфи-цирования организма патогенной микрофлорой, вирусами, простейшими, а также возникать на фоне активации условно патогенной микрофлоры при снижении специфических иммунологических механизмов защиты и рези-стентности организма.
В настоящее время важно учитывать значительные изменения в структуре возбудителей воспалительных гнойных процессов, осложняющих хирургиче-ские вмешательства, в частности, тот факт, что на первое место выдвинулась проблема условно патогенных возбудителей.
В развитии острого и хронического воспалительного процесса большую роль играет группа неклостридиальных анаэробных бактерий (грамотрица-тельные палочки рода Bacteroides, грамположительные кокки рода Peptococcus и Peptostreptococcus, грамположительные палочки), которые не образуют спор и являются представителями нормальной аутофлоры челове-ка. Они обитают в полости рта, в кишечнике, на коже и слизистых. Неклост-ридиальные анаэробы играют важную роль в развитии острой и хронической инфекции.
Частота выделения анаэробов при острых гнойных заболеваниях колеб-лется от 40 до 95% в зависимости от локализации и характера патологическо-го процесса (Кузин М.И., Костюченок Б.М., 1990).
Основные возбудители гнойных хирургических инфекций – стафило-кокки и грамотрицательные бактерии, принадлежащие к семейству Enterobaсteriaceae и к обширной малоизученной группе так называемых не-ферментирующих грамотрицательных бактерий.
Существенная роль в этиологии хирургических инфекций отводится об-лигатным неспорообразующим анаэробным бактериям.
В ряде случаев этиологическими факторами инфекционного воспали-тельного процесса могут быть возбудители, вызывающие развитие особых видов раневой инфекции - клостридиальной (газовая гангрена), неклостриди-альной анаэробной и гнилостной инфекции, сибирской язвы, столбняка, ро-жистого воспаления, актиномикоза, дифтерии, туберкулеза, сифилиса. Ука-занные возбудители резко изменяют течение раневого процесса, придают особую специфику местным и общим проявлениям воспаления.
В хирургической практике следует учитывать возможность первичного и вторичного микробного загрязнения раны. Первичное загрязнение наступает в момент нанесения раны и характерно для травматических и огнестрельных ран. Вторичное загрязнение раны, как правило, связано с нарушением правил асептики во время перевязок и операций и часто бывает следствием внутри-госпитальной инфекции.
Наличие в ране возбудителя является необходимым, но не решающим фактором в развитии заболевания. Так, в 60-70%, а по некоторым данным в 90% случаев, в ранах обнаруживаются анаэробные возбудители, однако ин-фекция развивается примерно у 2% больных (Кузин М.И., Костюченок Б.М., 1990).
Определяющее значение в развитии инфекции имеют реактивность орга-низма и степень местных нарушений в ране. Особенно важное значение имеют повреждение магистральных сосудов (риск развития инфекции воз-растает в15-20 раз), поражение костей и наличие в ране некротизированных тканей и инородных тел.
Для острых гнойных ран характерно то, что на всех этапах обследования основными представителями раневой микрофлоры являются стафилококки, которые выделяются как в монокультурах, так и в различных микробных ас-социациях. Кроме стафилококков с большой частотой высеваются различные грамотрицательные бактерии, особенно синегнойные палочки, а также грам-положительные стрептококки.
У больных, оперированных по поводу хронических гнойных заболеваний, раневая микрофлора носит полимикробный характер и представлена ассо-циациями стафилококков, стрептококков и синегнойных палочек.
Необходимо отметить, что уровень обсемененности операционных ран служит информативным показателем качества хирургической обработки ра-ны и коррелирует с местными и общими признаками воспаления, а также с процессом заживления раны.
В повседневной практике врач может встретиться с таким течением ране-вого процесса, которое резко отличается от описанных вариантов местными изменениями в ране и общим проявлением, обусловленным видом возбуди-теля раневой инфекции.
К таким особым видам раневой инфекции относится клостридиальная ра-невая инфекция (газовая гангрена).
Наибольшее распространение клостридиальная инфекция имеет во время боевых действий, однако и в мирное время она встречается у больных с об-ширными размозженными ранами, сопровождающимися повреждением со-судов и костей, а также в хирургических и гинекологических отделениях у больных, перенесших операции на органах брюшной полости или имеющих пролежни.
Причиной клостридиальной инфекции в мирное время может быть нару-шение правил асептики и антисептики при проведении хирургических мани-пуляций.
Раневой воспалительный процесс может быть вызван неспорообразую-щими анаэробами. При этом инфекция может локализоваться в подкожно-жировой клетчатке, фасциях, мышцах или поражать одновременно все эти образования, что и наблюдается наиболее часто.
Летальность при неклостридиальной инфекции согласно литературным данным составляет 48-60%.
Тяжелое инфекционное поражение раневых поверхностей представляет собой гнилостная инфекция. Чаще всего гнилостной инфекцией осложняются травматические раны с большим количеством размозженных тканей, моче-вые флегмоны, диабетические гангрены, раны с повреждением толстой киш-ки, раны от укусов.
Возбудители гнилостной инфекции: В.coli, petrificum, B.pyocyaneus, B.sporogenes, Str.fecalis, Pr.vulgaris,emphysematicus и др.
Диагностика гнилостной инфекции затруднена ее значительным сходст-вом с анаэробной неклостридиальной инфекцией. Общие клинические при-знаки этих инфекций: поражения кожи и клетчатки, характер экссудата, вы-раженная интоксикация и решающий эффект радикального хирургического вмешательства.
В ряде случаев возможно инфицирование поврежденной ткани возбудите-лем столбняка – Cl. tetani – строго анаэробным, спорообразующим грампо-ложительным подвижным микробом. Особенно высока степень инфициро-ванности ран в условиях военного времени, однако и в мирное время леталь-ность от столбняка составляет 25-50% среди больных молодого возраста и 70-80% - среди лиц пожилого возраста (Беркутов А.Н. и др., 1963; Дубик В.Т.,1971; Цыбуляк Г.Н., 1971).
К особому виду возбудителей инфекции относится -гемолитический стрептококк группы А, вызывающий развитие рожистого воспаления кожи и слизистых, часто принимающего рецидивирующий характер. Хронический специфический воспалительный процесс, сопровождающийся образованием множественных плотных инфильтратов, может быть вызван возбудителем актиномикоза – широко распространенного в природе лучистого грибка Actinomyces bovis. В зависимости от механизма заражения актиномикоз раз-вивается в различных органах и тканях (лицевая область, шея, легкие, ки-шечник и др.).
Спорообразующий микроб B.antracis является возбудителем особого вида инфекции- сибирской язвы. В последнее время заболевание наблюдается, в основном, в сельской местности в виде спорадических случаев.
У человека поражение кожи при сибирской язве встречается в 93-99% случаев, хотя могут быть и другие формы патологии (легочная, кишечная).
Для хирургов наибольший интерес представляет карбункул, так как имен-но его чаще всего приходится дифференцировать от фурункулеза или кар-бункула при банальной инфекции.
При попадании возбудителя Cоrynebacterium diphtheriae на имею-щуюся раневую или язвенную поверхность развивается дифтерия раны. Наиболее часто такое осложнение воспалительного процесса возникает в детском воз-расте. Клинически распознать дифтерию ран трудно, поэтому для уточнения диагноза проводят микроскопическое исследование патологического мате-риала с приготовлением препаратов, окрашенных по Нейссеру, Леффлеру.
Довольно редкой формой поражения раневой поверхности является ту-беркулез ран. Различают экзогенный и эндогенный пути попадания возбуди-теля в рану. Раневой процесс приобретает затяжной, вялотекущий характер, с частыми рецидивами.
В развитии хронического воспалительного процесса инфекционной при-роды нередко важная роль принадлежит сенсибилизации организма, образо-ванию аллергических антител, активации Т-системы лимфоцитов.
Воспалительный процесс может носить первичный характер и возникать в месте действия альтерирующего фактора.
В ряде случаев возможно вторичное развитие воспаления при аутоинток-сикациях (почечная недостаточность, печеночная недостаточность, кетоаци-доз) и при различных экзоинтоксикациях бактериальной и небактериальной природы.
Септические инфекции характеризуются быстрой диссеминацией пато-генных инфекционных факторов и развитием воспалительного процесса да-леко за пределами первичной инокуляции возбудителя.
Вторичные воспалительные процессы различной локализации могут со-путствовать анемиям различной этиологии, сердечной недостаточности, ды-хательной недостаточности, сопровождающимся развитием гипоксических состояний, нарушением трофики и регенерации тканей.
В ряде случаев воспаление имеет ятрогенную природу и может быть обу-словлено применением лекарственных препаратов. Так, воспаление слизи-стой оболочки желудочно-кишечного тракта нередко возникает на фоне при-менения аспирина, резерпина, бутадиона и стероидных гормонов.

Российская Академия Естествознания приняла участие в выставке BUCH WIEN 2019, (Австрия, Вена , 6-10 ноября 2019 года).

С 12 по 15 октября 2019 г. в г. Сочи состоялся заключительный очный этап VII международного конкурса научно-исследовательских и творческих работ учащихся "СТАРТ В НАУКЕ" и итоговое заседание педагогов высшей и средней школы в рамках научно-практической конференции "Современные проблемы школьного образования".

Российская Академия Естествознания (Международная ассоциация учёных, преподавателей и специалистов) приняла участие в 32-й Московской международной книжной выставке-ярмарке, г. Москва, ВДНХ, 4-8 сентября 2019 года.

Российская Академия Естествознания Приняла участие в выставке HONG KONG BOOK FAIR 2019, (КНР, Гонконг, 17-23 июля 2019 года).

Российская Академия Естествознания Приняла участие в выставке BOOKEXPO AMERICA 2019, (США, Нью-Йорк, 29-31 мая 2019 года).
Тябут Тамара Дмитриевна, профессор кафедры кардиологии и ревматологии Бел МАПО, доктор медицинских наук
Год здоровья. Прочитай и передай другому
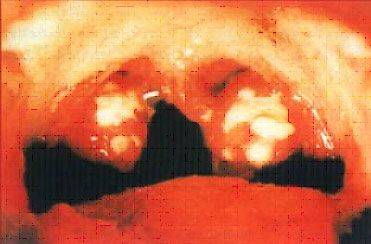
Тонзиллит, вызванный бета-гемолитическим стрептококком.
При наличии хронического тонзиллита в лакунах скапливается большое количество гноя, состоящего из погибших микробов, белых кровяных телец - лейкоцитов, других клеток (гнойно-казеозные пробки). В гнойном содержимом лакун размножаются болезнетворные микробы. Продукты жизнедеятельности микробов из миндалин попадают в кровь и приводят к развитию тонзиллогенной интоксикация, проявляющейся утомляемостью, болями в мышцах и суставах, головными болями, снижением настроения, субфебрилитетом. Миндалины превращаются в хранилище инфекционных агентов, откуда они могут распространяться по организму и быть причиной воспалительных процессов. Частые болезни еще более ослабляют иммунитет, что приводит к дальнейшему развитию тонзиллита. Так формируется порочный круг заболевания.
Хронический тонзиллит опасен осложнениями, связанными с распространением инфекции по организму. К ним относятся паратонзиллярные абсцессы, ·поражение сердца (тонзилогенная миокардиодистрофия, острая ревматическая лихорадка), сосудов, почек.
Тонзиллогенная миокардиодистрофия относится к часто развивающимся, но гораздо реже диагностируемым поражениям сердечной мышцы при хроническим тонзиллите. Она вызывается токсинами бактерий, находящихся в миндалинах, и продуктами местного воспаления и распада тканей.
Клинические признаки тонзиллогенной дистрофии миокарда обусловлены нарушением деятельности вегетативной нервной системы (вегетативной дисфункцией) и нарушением различных видов обмена в сердечной мышце (электролитного, белкового), следствием которых является нарушение образования энергии в сердечной мышце. На ранних этапах развития тонзилогенная миокардиодистрофия проявляется высокой частотой сердечных сокращений - тахикардией, перебоями в работе сердца - экстрасистолией, одышкой при интенсивных физических нагрузках, нарушением общего самочувствия больных. При поздней диагностике появляются признаки сердечной недостаточности, уменьшается объем нагрузки, вызывающей одышку, появляются более тяжелые нарушения ритма и проводимости. При своевременной диагностике и лечении внесердечного фактора - хронического тонзиллита, вызвавшего перечисленные изменения в сердечной мышце, они обратимы и постепенно структура и функции сердечной мышцы
восстанавливаются.
Наибольшую опасность для прогноза и качества жизни пациентов представляет поражение сердца при острой ревматической лихорадке.
Острая ревматическая лихорадка (ОРЛ) - постинфекционное осложнение тонзиллита (ангины) или фарингита, вызванных бета - гемолитическим стрептококком группы А, в виде системного воспалительного заболевания соединительной ткани с преимущественной локализацией патологического процесса в сердечно-сосудистой системе (кардит), суставах (мигрирующий полиартрит), мозге (хорея) и коже (кольцевидная эритема, ревматические узелки), развивающегося у предрасположенных лиц, главным образом молодого возраста (7-15 лет). В Российской Федерации и в РБ заболеваемость ревматической лихорадкой составляет от 0,2 до 0,6 случаев на 1000 детского населения. Первичная заболеваемость ОРЛ в России в начале ХХI века составила 0,027 случая на 1000 населения. Частота впервые выявленной хронической ревматической болезни сердца (ХРБС), которая включает пороки сердца и специфические изменения клапанов (краевой фиброз), выявляемые при ультразвуковом исследовании сердца - 0,097случаев на 1000 населения, в том числе ревматических пороков сердца - 0,076 случаев на 1000 взрослого населения. Имеющиеся статистические различия между частотой первичной заболеваемости острой ревматической лихорадкой и хронической ревматической болезнью сердца свидетельствует о наличии большого количества не диагностированных острых форм болезни.
Временной интервал между перенесенным острым стрептококковым тонзиллитом, фарингитом, обострением хронического тонзиллита и возникновением проявлений острой ревматической лихорадки составляет 3-4 недели. При острой ревматической лихорадке могут поражаться все структуры сердца - эндокард, миокард, перикард. Поражение миокарда (мышцы сердца) встречается всегда. Проявлениями поражения сердца могут быть сердцебиение, одышка, связанная с физической нагрузкой или в покое, боли в области сердца ноющего характера, которые в отличие о стенокардии не имеют четкой связи с физической нагрузкой и могут сохраняться длительный период времени, сердцебиение, перебои в работе сердца, приступообразные нарушения ритма - мерцательная аритмия, трепетание предсердий. Обычно поражение сердца сочетается с суставным синдромом по типу артралгий - болей в крупных суставах (коленных, плечевых, голеностопных, локтевых) или артрита (воспаления) этих же суставов. Для воспаления суставов характерны боль, изменения формы сустава, вызванные отеком, покраснение кожи в области пораженного сустава, местное повышение температуры и нарушение функции сустава в виде ограничения объема движений. Мелкие суставы поражаются гораздо реже. Воспалительный процесс в суставах носит мигрирующий характер и быстро проходит на фоне правильного лечения. Поражение сердца и суставов обычно сопровождается повышением температуры тела, слабостью потливостью, нарушением трудоспособности. У части пациентов встречаются поражения нервной системы, кожные сыпи по типу кольцевидной эритемы и подкожные ревматические узелки.
Для постановки диагноза острой ревматической лихорадки существуют диагностические критерии, которые включают клинические, лабораторные и инструментальные данные, а также информацию о перенесенной инфекции, вызванной бета-гемолитическим стрептококком группы А, его ревматогенными штаммами. Своевременно поставленный диагноз позволяет добиться выздоровления больного при проведении терапии антибиотиками, глюкокортикоидными гормонами, нестероидным противовоспалительными препаратами. Однако, при поздно начатом лечении, несоблюдении пациентами двигательного режима, наличии генетической предрасположенности, не санированной очаговой инфекции (декомпенсированный тонзиллит, кариес) исходом острой ревматической лихорадки может быть хроническая ревматическая болезнь сердца с пороком сердца или без него. Порок сердца возникает как исход воспалительного поражения клапанов сердца. Наличие порока сердца ревматической этиологии требует отнесения пациента к группе высокого риска развития инфекционного эндокардита, наиболее тяжелой формы поражения сердца, связанного с инфекционными агентами.
Острая ревматическая лихорадка относится к заболевания, при которых профилактика имеет важное значение для снижения как первичной заболеваемости, так и повторных эпизодов болезни (повторная острая ревматическая лихорадка).
Первичная профилактика имеет своей целью снижение первичной заболеваемости и включает комплекс медико-санитарных и гигиенических мероприятий, а так же адекватное лечение инфекций, вызванных бета-гемолитическим стрептококком группы А. Первое направление включает мероприятия по закаливанию, знакомство с гигиеническими навыками, санацию хронических очагов инфекции, в первую очередь - хронического тонзиллита и кариеса. Миндалины тщательно санируют повторными полосканиями и промываниями растворами антибактериальных средств, вакуум-аспирацией патологического содержимого лакун. Если это не дает желаемого результата обсуждается вопрос хирургического лечения - удаления миндалин. В каждом конкретном случае выбор тактики лечения определяет врач отоларинголог и терапевт, кардиолог или ревматолог.
Адекватное лечение ангины и фарингита направлено на подавление роста и размножения стрептококка в организме при развитии стрептококкового фарингита, ангины, тонзиллита. Основу лечения составляет антибиотикотерапия в сочетании с противовоспалительными средствами, которые должны проводиться не менее 10 дней с обязательным контролем общего анализа крови, мочи, а по показаниям биохимического анализа крови при возникновении признаков болезни, при окончании лечения и через месяц от появления первых признаков болезни. Лабораторное исследование, проведенное в эти сроки, позволяет правильно поставить диагноз, определить эффективность лечения, и что самое главное, не пропустить начало развития осложнения в виде острой ревматической лихорадки.
Вторичная профилактика имеет своей целью предупреждение развития повторной острой ревматической лихорадки и прогрессирования заболевания у лиц, перенесших ОРЛ. Она проводится у пациентов, не имеющих аллергии к препаратам пенициллинового ряда. Лекарственным средством, используемым для профилактики у взрослых является бензатинбензилпенициллин (экстенциллин, ретарпен) в дозе 2 400 000 ЕД 1 раз в 3 недели внутримышечно. Профилактические режимы зависят от возраста пациента и исхода острой ревматической лихорадки. В соответствии с рекомендациями Ассоциации ревматологов России вторичная профилактика включает следующие режимы:
Наиболее тяжелым и прогностически неблагоприятным заболеванием сердца, связанным с инфекцией считается инфекционный эндокардит - заболевание, характеризующееся развитием воспалительного процесса на клапанном или пристеночном эндокарде, включающее поражение крупных внутригрудных сосудов, отходящих от сердца, возникающее вследствие воздействия микробной инфекции. Наиболее часто это различные бактерии- стрептококки, стафилококки, энтерококки, кишечная палочка, синегнойная палочка и многие другие. Описано 119 различных возбудителей, приводящих к развитию заболевания.
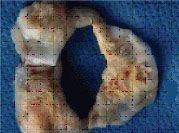
Аортальный клапан
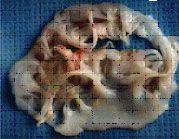
Митральный клапан
Так выглядят клапаны сердца при развитии инфекционного эндокардита.
Наложения из микробов, клеток крови нарушают их функцию,
разрушают клапан и зачастую требуют экстренного хирургического лечения.
Распространенность инфекционного эндокардита в начале 21 века составляла 2- 4 случая на 100 000 населения в год. Отмечается повсеместный рост заболеваемости, наиболее выраженный в старших возрастных группах и составляющий 14, 5 случая на 100 000 населения в возрасте 70-80 лет. Диагностика заболевания сложна. При первом обращении к врачу диагноз ставится только у 19 - 34,2% больных. Средний срок от первичного обращения до постановки диагноза составляет не менее 1,5 - 2 месяцев.
Выделяют группу больных с высоким риском развития инфекционного эндокардита, в которую входят:
- пациенты с ранее перенесенным инфекционным эндокардитом,
- пациенты с протезированными клапанами сердца,
- пациенты с синими врожденными пороками,
- пациенты после хирургических операций на аорте, легочных сосудах
- пациенты с приобретенными пороками сердца, в первую очередь ревматической этиологии (ХРБС).
Кроме этого выделена группа умеренного (промежуточного) риска, объединяющая пациентов со следующими заболеваниями:
- Пролапс митрального клапана, обусловленный миксоматозной дегенерацией или другими причинами с регургитацией 2-3 степени или пролапсы нескольких клапанов
- Нецианотичные врожденные пороки сердца (исключая вторичный ДМПП)
- Бикуспидальный (двухстворчатый)аортальный клапан
- Гипертрофическая кардиомиопатия (идиопатический гипертрофический субаортальный стеноз).
Установлено, что для развития инфекционного эндокардита необходимо попадание возбудителя в кровь. Наиболее частой причиной этого могут быть стоматологические манипуляции, сопровождающиеся повреждением десны и кровоточивостью. При наличии кариеса или заболеваний десен, бактериемия (наличие возбудителя в крови) может возникать достаточно часто.

Среди причин, приводящих к нарушениям родовой деятельности, особое внимание привлекает инфекционная патология беременных, и давно доказано, что инфекционно-воспалительные процессы оказывают негативное влияние на плаценту. Об этом свидетельствуют высокая частота угрозы прерывания беременности, самопроизвольных выкидышей и преждевременных родов у женщин с инфекционными заболеваниями полового аппарата и инфекциями другой локализации[5].
Инфекционная патология женских половых органов часто обуславливает воспалительные заболевания гениталий, хронические тазовые боли, осложненное течение беременности, а также привычное невынашивание, преждевременные роды, плацентарную недостаточность, задержку развития плода, внутриутробное инфицирование плода и новорожденного. Причём, известно, что при беременности организм женщины предрасположен к инвазии патогенных микроорганизмов и последующему их развитию, поэтому, инфекционные заболевания, встречающиеся во время гестационного процесса, подразделяют на: инфекции, передаваемые половым путем, воспалительные заболевания органов малого таза, инфекционные осложнения послеродового периода, а также экстрагенитальные и нозокомиальные инфекции[11].
Современные стремительное распространение оппортунистических инфекций и изменение особенностей микробиологического спектра оказывают негативное влияние на уровень здоровья населения, причём наиболее неблагоприятно это отражается на репродуктивной системе.[7]
И в этой связи в течение последних десятилетий одними из основных проблем акушерства являются инфекции у беременных, особое внимание уделяется изучению влияния инфекционно-воспалительных процессов на течение самого значимого события гестации - непосредственно родового акта, в частности на родовую деятельность; частота аномалий родовой деятельности у женщин, у которых есть урогенитальная хроническая инфекция, существенно превышает средние показатели по отношению ко всем родам, достигая 50%[10].
У детей ранний неонатальный период, при воздействии негативного характера, связанного с нарушением гестационного процесса, в том числе обусловленного внутриутробным инфицированием, характеризуется проявлением критических значений физиологических показателей, которые вызваны не только гемостазиологическими нарушениями в системе мать-плацента-плод, но и выявлением значительного дефицита ряда факторов свертывания крови, физиологических антикоагулянтов и компонентов фибринолиза; также обнаруживается прекращение плацентарного и включение легочного кровообращения, послеродовой гемолиз, которые происходят под воздействием "бактериального стресса" и ряда других сдвигов, создающих предпосылки для крайне негативных и опасных срывов в системе саморегуляции именно в этот периоде жизни[9].
Инфекции, передаваемые половым путём, занимают одно из ведущих мест в развитии невынашивания, причем исследования последних лет показали, что у женщин с синдромом потери плода вирусно-бактериальная колонизация плаценты встречается значительно чаще, чем у женщин с нормальным акушерским анамнезом. Соответственно, данная патология, учитывая ее распространенность, вносит значимый вклад в младенческую и перинатальную смертность[3].
Хроническая плацентарная недостаточность (ХПН), будучи одной из самых распространенных осложнений при беременности, часто сопровождается задержкой внутриутробного роста и развития плода, гипоксией, нарушением функций и структуры его жизненноважных органов, вот почему на данный момент и считается самой главной причиной перинатальной заболеваемости и смертности[17].
Этиологическая основа плацентарной недостаточности весьма разнообразна и зависит от множества факторов, которые принято делить на эндогенные и экзогенные. Эндогенными факторами можно считать морфологические нарушения плаценты, возникающие у будущей матери при генетических, эндокринных, инфекционных, иммунологических заболеваниях, а также под влиянием курения, и других различных вредных факторов окружающей среды, а также заболевания женщины, другого генеза, особенно на ранних сроках беременности; при этом достоверно установлено, что наиболее часто развитие плацентарной недостаточности есть результат инфекционного поражения плаценты беременной женщины.[13]
Особое место среди этиологических факторов занимают нарушения эндокринной системы, в частности заболевания щитовидной железы, диагностика которых в современном мире не представляет труда и является более доступной населению по сравнению с генетическими или иммунологическими исследованиями.[8]
К одной из наиболее часто диагностируемых инфекций мочеполового тракта относится хламидиоз - сексуально-трансмиссивная инфекция, ведущая к развитию воспалительных заболеваний урогенитальной системы и органов малого таза и оказывающая значительное влияние на репродуктивную функцию[17].
По оценкам Всемирной Организации Здравоохранения, хламидиоз занимает второе место после урогенитального трихомониаза среди инфекций, передаваемых половым путем; хламидии выявляются у каждой второй женщины с хроническими воспалительными процессами мочеполовой системы, у 70-80% - с привычным невынашиванием, у 40-50% - с трубным бесплодием. [12].
Урогенитальные микоплазмы относят к числу возбудителей внутриутробной инфекции, вызывающей в плацентах воспалительные, дистрофические и гемодинамические нарушения, которые могут приводить не только к выраженным морфологическим изменениям последа и его оболочек, но и к внутриутробной гибели плода[16].
Снижение функциональной активности эритроцитов в системе мать-плацента при обострении HVS-1,2 является одним из значимых факторов в патогенезе развития ХПН, высокий риск формирования которой имеется у 10% беременных с ранней плацентарной недостаточностью.
Таким образом, наличие недифференцированной формы дисплазии соединительной ткани у беременных с персистирующей инфекцией семейства вирусов герпес является клиническим предиктором риска реализации инфекционного процесса в плаценте с развитием субкомпенсированной фетоплацентарной недостаточности[4].
В случае заражения трихомонадной инфекцией или при активации хронического процесса, до формирования хориоамниотических оболочек, беременность может прерываться в результате самопроизвольного выкидыша. Если же заражение произошло на более поздних сроках, восходящая инфекция развивается редко. При этом, известно, что одно из наиболее частых проявлений урогенитальных инфекций у беременных женщин - фетоплацентарная недостаточность, которая характеризуется соответствующими эхографическими признаками, расстройством маточно-плацентарной и фетоплацентарной гемодинамики, нарушением реактивности сердечно-сосудистой системы плода[14].
Заключение
Отмеченные факты дают основание считать, что при наличии у беременных таких фоновых состояний, как острые и хронические инфекционные заболевания, самопроизвольное и искусственное прерывание предыдущих беременностей, экстрагенитальной патологии, их следует относить к группе риска по развитию плацентарной недостаточности[2].
У беременных с острой или обострением хронической инфекции крайне важно проведение мероприятий, направленных на борьбу с инфекцией и улучшение защитных резервов в системе мать - плацента - плод.
Можно выделить несколько основных направлений лечения беременных при плацентарной недостаточности:
- нормирование гемодинамики в плацентарной системе;
- усиление интенсивности газообмена;
- постоянное наблюдение и своевременный контроль реологических свойств крови;
- постоянная профилактика гиповолемии;
- поддержание онкотического давления крови.
- стабилизация сосудистого тонуса
- нормализация сократительной активности матки
- усиление работы антиоксидантной системы;
- уравновешивание метаболических и обменных процессов между плодом и плацентой [14].
При плацентарной недостаточности инфекционного генеза, наряду с улучшением показателей гемодинамики и метаболизма в системе мать - плацента - плод, большое значение имеют профилактика и лечение острой инфекции или обострения хронической[1].
Таким образом, адекватное и своевременное лечение хронической ПН с использованием современных препаратов способствует повышению вероятности благоприятного исхода беременности и позволяет избежать прогрессирования нарушений в системе мать -плацента - плод[6].
Рецензенты:
Артифексова А.А., д.м.н., профессор, зав. кафедрой патологической анатомии, ГБОУ ВПО НижГМА Минздрава России, г. Нижний Новгород;
Потемина Т.Е., д.м.н., профессор, зав. кафедрой патологической физиологии, ГБОУ ВПО НижГМА Минздрава России, г. Нижний Новгород.
Читайте также:


