Иммуноферментный метод в диагностике инфекционных заболеваний

Иммуноферментный анализ (ИФА) — метод лабораторной диагностики, позволяющий обнаруживать специфические антитела и антигены при самых разных патологиях.
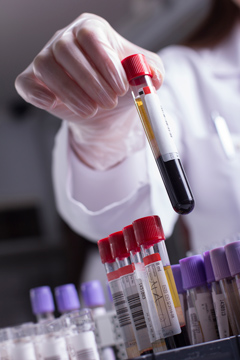
ИФА — один из самых распространенных и точных методов для выявления инфекций, передающихся половым путем, в частности ВИЧ, ВПЧ, гепатита В.

Для того чтобы результаты анализов были максимально достоверными, необходимо правильно подготовиться к их сдаче.

Спецпредложения, скидки и акции помогут существенно сэкономить на медицинском обследовании.
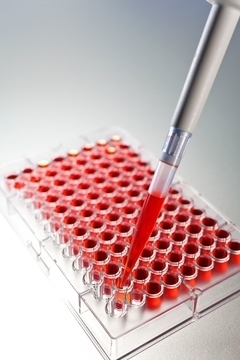
Контроль качества лабораторных исследований, осуществляемый по международным стандартам, — дополнительная гарантия точности результатов анализов.
Современная диагностика в медицине немыслима без высокочувствительных лабораторных анализов. Прежде для установления причин тех или иных симптомов врачи были вынуждены ориентироваться на косвенные признаки болезни, а также проводить многоступенчатые микроскопические исследования в попытке обнаружить возбудителя инфекции. Сегодня достаточно одного-единственного теста — такого как иммуноферментный анализ — чтобы подтвердить или опровергнуть первоначальный диагноз.
Основные понятия и принцип метода иммуноферментного анализа
Существует несколько разновидностей антител, каждая из которых вступает в действие на определенном этапе иммунного ответа. Так, первыми в ответ на проникновение антигена в организм синтезируются иммуноглобулины класса М (IgM). Содержание этих антител наиболее высоко в первые дни инфекционного процесса.
Следом за ними иммунная система выбрасывает в кровь иммуноглобулины класса G (IgG), которые помогают уничтожать антигены до полной победы над инфекцией, а также продолжают циркулировать по сосудам в дальнейшем, обеспечивая иммунитет к повторному заражению. На этом явлении основана вакцинация: благодаря прививкам, содержащим ослабленные антигены микробов и вирусов, в нашей крови появляется большое количество IgG, которые при контакте с реальной угрозой быстро подавляют инфекцию — до того, как она нанесет вред здоровью.
Как узнать, какие именно антигены или антитела присутствуют в организме человека? Когда врач предполагает, что причиной заболевания является определенная инфекция, или желает измерить концентрацию определенного гормона, он назначает пациенту иммуноферментный анализ.
ИФА бывает качественным и количественным. В первом случае подразумевается однозначный ответ: искомое вещество или найдено, или не найдено в образце. В случае с количественным анализом более сложная цепь реакций дает возможность оценить концентрацию антител в крови человека, что в сравнении с результатами предыдущих тестов даст ответ на вопрос о том, как развивается инфекционный процесс.
Бесспорные преимущества ИФА — высокая чувствительность и специфичность метода. Чувствительность — это возможность распознать искомое вещество, даже если его концентрация в образце невысока. Специфичность же подразумевает безошибочность диагностики: если результат положительный, значит, найдены именно те антитело или антиген, которые предполагались, а не какие-то другие.
Высокая степень технологичности проведения иммуноферментного анализа минимизирует влияние человеческого фактора, что снижает вероятность ошибки. Большинство используемых в современных лабораториях тест-систем и реактивов для ИФА выпускаются в промышленных условиях, что гарантирует точный результат.
В случае диагностики инфекционных заболеваний иммуноферментный анализ не может найти возбудителя и определить его специфичные свойства: он лишь указывает на наличие антител в крови у больного, косвенно свидетельствующих о присутствии чужеродного микроорганизма в теле человека.
ИФА — крайне точный, но не дешевый метод, поэтому обращаться к нему нужно с умом, а интерпретацией результатов должен заниматься квалифицированный врач.
Невозможно охватить полный список показаний к проведению ИФА. Вот наиболее распространенные цели анализа:
- Диагностика острых и хронических инфекционных заболеваний:
- IgM и IgG к вирусным гепатитам А, B, C, E, а также антигенов гепатитов В и С;
- IgG к ВИЧ;
- Ig M и IgG к цитомегаловирусной инфекции;
- Ig M и IgG к вирусу Эпштейна-Барр;
- Ig M и IgG к герпетическим инфекциям;
- Ig M и IgG к токсоплазмозу;
- Ig M и IgG к кори, краснухе, сальмонеллезу, дизентерии, клещевому энцефалиту и другим заболеваниям;
- IgG к паразитарным заболеваниям;
- Ig M и IgG к инфекциям, передающимся половым путем;
- IgG к хеликобактерной инфекции.
- Общая оценка показателей иммунитета человека и маркёров некоторых аутоиммунных заболеваний.
- Выявление онкологических маркёров (фактора некроза опухоли, простатспецифического антигена, раково-эмбрионального антигена и других).
- Определение содержания гормонов в сыворотке крови (прогестерона, пролактина, тестостерона, тиреотропного гормона и других).
Основной биоматериал для проведения ИФА — это сыворотка крови: в лаборатории у пациента берут образец крови из вены, из которого в дальнейшем удаляют форменные элементы, затрудняющие проведение анализа. В некоторых других случаях для анализа используется спинномозговая жидкость, околоплодные воды, мазки слизистых оболочек и т.д.
Для того чтобы избежать искажений в результатах, рекомендуется сдавать кровь натощак, а за две недели до исследования (если целью является диагностика хронических, скрыто протекающих инфекционных заболеваний) необходимо отказаться от приема антибиотиков и противовирусных препаратов.
При наличии необходимых реактивов и хорошей организации работы лаборатории результат анализа вы получите в течение 1–2 суток после забора крови. В некоторых случаях, при необходимости получения экстренного ответа, этот срок может быть сокращен до 2–3 часов.
- IgM — наличие этого класса иммуноглобулинов говорит об остром инфекционном процессе в организме. Отсутствие IgM может говорить как об отсутствии конкретного возбудителя в организме, так и о переходе инфекции в хроническую стадию.
- IgA при отрицательном результате теста на IgM чаще всего свидетельствует о хронической или скрыто протекающей инфекции.
- IgM и IgA (совместное присутствие) — два положительных результата говорят о разгаре острой фазы заболевания.
- IgG говорит либо о хронизации заболевания либо о выздоровлении и выработке иммунитета к инфекционному агенту.
В зависимости от содержания анализа в бланке могут быть представлены данные в виде таблицы с перечислением всех антител или антигенов с пометками об отрицательной или положительной реакции, либо будет указано количественное значение результата (отрицательный, слабоположительный, положительный или резко положительный). Последний вариант определяет, сколько антител содержится в анализируемом образце.
Еще один количественный показатель — индекс авидности антител, выраженный в процентах. Он указывает, сколько времени прошло от начала инфекционного процесса (чем выше индекс — тем больше).
Сегодня выпускаются тысячи видов тест-систем ИФА, позволяющих обнаруживать специфические антитела и антигены при самых разных патологиях. Поэтому этот анализ используется практически во всех медицинских отраслях. Диагноз, поставленный с помощью ИФА, — это гарантия назначения адекватной терапии и эффективного лечения заболевания.
Информативность ИФА делает этот анализ важным инструментом в работе многих медицинских центров. Но можно ли доверять такую диагностику государственным лабораториям или лучше самим выбрать, где провести такое исследование?
Диагностика инфекционных заболеваний является одной из самых сложных проблем в клинической медицине. Лабораторные методы исследования при ряде нозологических форм играют ведущую, а в целом ряде клинических ситуаций решающую роль не только в диагностике, но и в определении конечного исхода заболевания.
Диагностика инфекционных заболеваний почти всегда предусматривает использование комплекса лабораторных методов.

- бактериологические;
- серологические;
- метод полимеразной цепной реакции (ПЦР) для обнаружения ДНК или РНК возбудителя инфекционного заболевания в исследуемом материале.
У одних пациентов для диагностики этиологии инфекционно-воспалительного процесса достаточно провести бактериологическое исследование, в других клинических ситуациях решающее значение имеют данные серологических исследований, в третьих, предоставить полезную информацию может только метод ПЦР. Однако наиболее часто в клинической практике врачу-клиницисту необходимо использовать данные различных методов лабораторных исследований.
Бактериологические методы исследования
Бактериологические исследования наиболее часто проводят при подозрении на гнойно-воспалительные заболевания (составляют 40-60% в структуре хирургических заболеваний) с целью их диагностики, изучения этиологической структуры, определения чувствительности возбудителей к антибактериальным препаратам. Результаты бактериологических анализов способствуют выбору наиболее эффективного препарата для антибактериальной терапии, своевременному проведению мероприятий для профилактики внутрибольничных инфекций.
Возбудителями гнойно-воспалительных заболеваний являются истинно-патогенные бактерии, но наиболее часто условно-патогенные микроорганизмы, входящие в состав естественной микрофлоры человека или попадающие в организм извне. Истинно-патогенные бактерии в большинстве случаев способствуют развитию инфекционного заболевания у любого здорового человека. Условно-патогенные микроорганизмы вызывают заболевания преимущественно у людей с нарушенным иммунитетом.
Бактериологические исследования при заболеваниях, вызываемых условно-патогенными микроорганизмами, направлены на выделение всех микроорганизмов, находящихся в патологическом материале, что существенно отличает их от аналогичных исследований при заболеваниях, вызванных истинно патогенными микроорганизмами, когда проводится поиск определенного возбудителя.
Для получения адекватных результатов бактериологического исследования при гнойно-воспалительных заболеваниях особенно важно соблюдать ряд требований при взятии биоматериала для анализа, его транспортировки в лабораторию, проведения исследования и оценки его результатов.
Для идентификации вида возбудителя гнойно-воспалительных заболеваний и определения чувствительности к антибактериальным препаратам бактериологические лаборатории используют комплекс методов. Они включают:
- микроскопическое исследование мазка (бактериоскопия) из доставленного биоматериала;
- выращивание культуры микроорганизмов (культивирование);
- идентификацию бактерий;
- определение чувствительности к антимикробным препаратам и оценку результатов исследования.
Доставленный в бактериологическую лабораторию биоматериал первоначально подвергается микроскопическому исследованию.
Микроскопическое исследование мазка (бактериоскопия), окрашенного по Граму или другими красителями, проводят при исследовании мокроты, гноя, отделяемого из ран, слизистых оболочек (мазок из цервикального канала, зева, носа, глаза и т.д.). Результаты микроскопии позволяют ориентировочно судить о характере микрофлоры, ее количественном содержании и соотношении различных видом микроорганизмов в биологическом материале, а также дает предварительную информации об обнаружении этиологически значимого инфекционного агента в данном биоматериале, что позволяет врачу сразу начать лечение (эмпирическое). Иногда микроскопия позволяет выявить микроорганизмы, плохо растущие на питательных средах. На основании данных микроскопии проводят выбор питательных сред для выращивания микробов, обнаруженных в мазке.
Культивирование микроорганизмов. Посев исследуемого биоматериала на питательные среды производят с целью выделения чистых культур микроорганизмов, установления их вида и определения чувствительности к антибактериальным препаратам. Для этих целей используют различные питательные среды, позволяющие выделить наибольшее количество видов микроорганизмов. Оптимальными являются питательные среды, содержащие кровь животного или человека, а также сахарный бульон, среды для анаэробов. Одновременно производят посев на дифференциально-диагностические и селективные (предназначенные для определенного вида микроорганизмов) среды. Посев осуществляют на стерильные чашки Петри, в которые предварительно заливают питательную среду для роста микроорганизмов.

Микроскопия мазков, окрашенных по Граму
1 - стрептококки; 2 - стафилококки; 3 - диплобактерии Фридленда; 4 - пневмококки
Чашки Петри с посевами инкубируют в термостате при определенных температурных, а для ряда микроорганизмов газовых (например, для выращивания анаэробов создают условия с низким содержанием кислорода) режимах в течение 18-24 ч. Затем чашки Петри просматривают. Количественную обсемененность доставленного биоматериала микрофлорой определяют по числу колониеобразующих единиц (КОЕ) в 1 мл или 1 мг исследуемого образца. При просмотре чашек Петри выявляют некоторые особенности изменения цвета среды, ее просветления в процессе роста культуры. Многие группы бактерий образуют характерные формы колоний, выделяют пигменты, которые окрашивают колонии или среду вокруг них. Из каждой колонии делают мазки, окрашивают по Граму и микроскопируют. Оценивают однородность бактерий, форму и размер, наличие спор или других включений, капсулы, расположение бактерий, отношение к окраске по Граму. Вся эта информация служит важнейшей составляющей для выбора сред и получения в дальнейшем чистой культуры каждого микроорганизма.
Колонии отсевают на плотные, жидкие, полужидкие питательные среды, оптимальные для культивирования определенного вида бактерий.
Выделенные чистые культуры микроорганизмов подвергают дальнейшему изучению в диагностических тестах, основанных на морфологических, ферментативных, биологических свойствах и антигенных особенностях, характеризующих бактерий соответствующего вида или варианта.
Определение чувствительности к антибактериальным препаратам. Чувствительность к антимикробным препаратам изучают у выделенных чистых культур микроорганизмов имеющих этиологическое значение для данного заболевания. Поэтому в направлении на бактериологические анализы требуется указать диагноз заболевания у больного. Определение чувствительности бактерий к спектру антибиотиков помогает лечащему врачу правильно выбрать препарат для лечения больного.
Оценка результатов исследования. Принадлежность условно-патогенных микроорганизмов к естественной микрофлоре организма человека создает ряд трудностей при оценке их этиологической роли в развитии гнойно-воспалительных заболеваний. Условно-патогенные микроорганизмы могут представлять нормальную микрофлору исследуемых жидкостей и тканей или контаминировать их из окружающей среды. Поэтому для правильной оценки результатов бактериологических исследований необходимо знать состав естественной микрофлоры изучаемого образца. В тех случаях, когда исследуемый биоматериал в норме стерилен, как, например, спинномозговая жидкость, экссудаты, все выделенные из него микроорганизмы могут считаться возбудителями заболевания. В тех случаях, когда исследуемый материал имеет собственную микрофлору, как, например, отделяемое влагалища, кал, мокрота, нужно учитывать изменения ее качественного и количественного состава, появление несвойственных ему видов бактерий, количественную обсемененность биоматериала. Так, например, при бактериологическом исследовании мочи степень бактериурии (число бактерий в 1 мл мочи), равная и выше 10 5 , свидетельствует об инфекции мочевых путей. Более низкая степень бактериурии встречается у здоровых людей и является следствием загрязнения мочи естественной микрофлорой мочевых путей.
Установить этиологическую роль условно-патогенной микрофлоры помогают также нарастание количества и повторность выделения бактерий одного вида от больного в процессе заболевания.
Врач-клиницист должен знать, что положительный результат бактериологического исследования в отношении биологического материала, полученного из в норме стерильного очага (кровь, плевральная жидкость, спинномозговая жидкость, пунктат органа или ткани), всегда тревожный результат, требующий немедленных действий по оказанию медицинской помощи.
Серологические методы исследования
В основе всех серологических реакций лежит взаимодействие антигена и антитела. Серологические реакции используются в двух направлениях.
С внедрением в практику лабораторий метода иммуноферментного анализа (ИФА) стало возможным определять в крови больных антитела, относящиеся к различным классам иммуноглобулинов (IgM и IgG), что существенным образом повысило информативность серологических методов диагностики. При первичном иммунном ответе, когда иммунная система человека взаимодействует с инфекционным агентов в первый раз, синтезируются преимущественно антитела, относящиеся к иммуноглобулинам класса М. Лишь позднее, на 8-12 день после попадания антигена в организм, в крови начинают накапливаться антитела иммуноглобулинов класса G. При иммунном ответе на инфекционные агенты вырабатываются также и антитела класса А (IgA), которые играют важную роль в защите от инфекционных агентов кожи и слизистых оболочек.
2. Установление родовой и видовой принадлежности микроба или вируса. В этом случае неизвестным компонентом реакции является антиген. Такое исследование требует постановки реакции с заведомо известными иммунными сыворотками.
Серологические исследования не обладают 100 % чувствительностью и специфич-ностью в отношении диагностики инфекционных заболеваний, могут давать перекрестные реакции с антителами, направленными к антигенам других возбудителей. В связи с этим оценивать результаты серологических исследований необходимо с большой осторожностью и учетом клинической картины заболевания. Именно этим обусловлено использование для диагностики одной инфекции множества тестов, а также применение метода Western-blot для подтверждения результатов скрининговых методов.
В последние годы прогресс в области серологических исследований связан с разработкой тест-систем для определения авидности специфических антител к возбудителям различных инфекционных заболеваний.
Авидность - характеристика прочности связи специфических антител с соответствующими антигенами. В ходе иммунного ответа организма на проникновение инфекционного агента стимулированный клон лимфоцитов начинает вырабатывать сначала специфические IgM-антитела, а несколько позже и специфические IgG-антитела. IgG-антитела обладают поначалу низкой авидностью, то есть достаточно слабо связывают антиген. Затем развитие иммунного процесса постепенно (это могут быть недели или месяцы) идет в сторону синтеза лимфоцитами высокоспецифичных (высокоавидных) IgG-антител, более прочно связывающихся с соответствующими антигенами. На основании этих закономерностей иммунного ответа организма в настоящее время разработаны тест-системы для определения авидности специфических IgG-антител при различных инфекционных заболеваниях. Высокая авидность специфических IgG-антител позволяет исключить недавнее первичное инфицирование и тем самым с помощью серологических методов установить период инфицирования пациента. В клинической практике наиболее широкое распространение нашло определение авидности антител класса IgG при токсоплазмозе и цитомегаловирусной инфекции, что дает дополнительную информацию, полезную в диагностическом и прогностическом плане при подозрении на эти инфекции, в особенности при беременности или планировании беременности.
Метод полимеразной цепной реакции
Полимеразная цепная реакция (ПЦР) являющаяся одним из методов ДНК-диагностики, позволяет увеличить число копий детектируемого участка генома (ДНК) бактерий или вирусов в миллионы раз с использованием фермента ДНК-полимеразы. Тестируемый специфический для данного генома отрезок нуклеиновой кислоты многократно умножается (амплифицируется), что позволяет его идентифицировать. Сначала молекула ДНК бактерий или вирусов нагреванием разделяется на 2 цепи, затем в присутствии синтезированных ДНК-праймеров (последовательность нуклеотидов специфична для определяемого генома) происходит связывание их с комплементарными участками ДНК, синтезируется вторая цепь нуклеиновой кислоты вслед за каждым праймером в присутствии термостабильной ДНК-полимеразы. Получается две молекулы ДНК. Процесс многократно повторяется. Для диагностики достаточно одной молекулы ДНК, то есть одной бактерии или вирусной частицы. Введение в реакцию дополнительного этапа - синтеза ДНК на молекуле РНК при помощи фермента обратной транскриптазы - позволило тестировать РНК-вирусы, например, вирус гепатита С. ПЦР - это трехступенчатый процесс, повторяющийся циклично: денатурация, отжиг праймеров, синтез ДНК (полимеризация). Синтезированное количество ДНК идентифицируют методом иммуноферментного анализа или электрофореза.
В ПЦР может быть использован различный биологический материал - сыворотка или плазма крови, соскоб из уретры, биоптат, плевральная или спинномозговая жидкость и т.д. В первую очередь ЦПР применяют для диагностики инфекционных болезней, таких как вирусные гепатиты В, С, D, цитомегаловирусная инфекция, инфекционные заболевания, передающиеся половым путем (гонорея, хламидийная, микоплазменная, уреаплазменная инфекции), туберкулез, ВИЧ-инфекция и т.д.
Преимущество ПЦР в диагностике инфекционных заболеваний перед другими методами исследований заключается в следующем:
- возбудитель инфекции может быть обнаружен в любой биологической среде организма, в т.ч. и материале, получаемом при биопсии;
- возможна диагностика инфекционных болезней на самых ранних стадиях заболевания;
- возможность количественной оценки результатов исследований (сколько вирусов или бактерий содержится в исследуемом материале);
- высокая чувствительность метода; например чувствительность ПЦР для выявления ДНК вируса гепатита В в крови составляет 0,001 пг/мл (приблизительно 4,0 . 10 2 копий/мл), в то время как метода гибридизации ДНК с использованием разветвленных зондов - 2,1 пг/мл (приблизительно 7,0 . 10 5 копий/мл).
О . А . Верк о вс кий , доктор биологических наук, заведующий отделом иммунологии НПО НАР ВАК
Теоретические и практические достижения ветеринарной науки значительно расширили арсенал методов диагностики и средств специфической профилактики инфекционных болезней крупного рогатого скота. При этом развитие новых подходов к предупреждению инфекционных болезней и изучение механизмов иммунологической защиты животных неразрывно связаны с разработкой и внедрением новых методов и технологий, основанных на современных представлениях об эффекторных механизмах иммунитета, среди которых главное место занимает взаимодействие анти ген-антитело.
Иммуноферментный анализ (ИФА) к настоящему времени прошел путь от новейшей научной разработки до рутинного метода в клинической диагностике. С его помощью можно проводить как массовое обследование стад, так и поставить окончательный диагноз у конкретного животного.
По сравнению с другими методами выявления антигенов и антител профессионально разработанные иммуноферментные тест-системы обладают следующими преимуществами:
• высокой чувствительностью, позволяющей выявлять концентрации белка в диапазоне нг/мл, и специфичностью;
• воспроизводимостью полученных результатов;
• стабильностью при хранении всех необходимых реагентов (до года и более);
• простотой проведения реакции и возможностью использования минимальных объемов исследуемого материала;
• наличием инструментального (в качественном и количественном варианте) учета реакции и возможностью автоматизации всех ее этапов.
При инструментальной оценке результат ИФА может быть качественным (позволяет судить о наличии или отсутствии специфических антител) и полуколичественным (позволяет получить информацию об относительном содержании антител в испытуемых пробах). Оба варианта являются приблизительными, однако они намного точнее методов определения титров антител в реакциях с визуальным учетом.
узаконенным методом диагностики лейкоза, ящура и бруцеллеза крупного рогатого скота.
Специалисты НПО НАРВАК в сотрудничестве с ведущими отечественными и зарубежными учеными внедрили в ветеринарную практику нашей страны ИФА-наборы для диагностики лейкоза и ящура, проводят эксперименты по созданию ИФА-набора для диагностики бруцеллеза. Условия применения данных наборов - любые лаборатории, оснащенные стандартным оборудованием для ИФА. ИФА - диагностика лейкоза
"Набор для выявления антител к вирусу лейкоза крупного рогатого скота (ВЛКРС методом им-муноферментного анализа (ИфА)", выпускаемый в двух вариантах:
• И ФА-набор для проведения массовых скри-нинговых исследований - скринирующий тест;
• ИФА-набор (VeriTest) для подтверждения положительных результатов - подтверждающий (конфирмационный или верификационный) тест.
Как и большинство зарубежных аналогов оба варианта ИФА предназначены для выявления антител к поверхностному гликопротеину др51 ВЛКРС в сыворотке крови и молоке животных.
Использование подтверждающего ИфА-набо-ра VeriTest является очень важным моментом при диагностических исследованиях на лейкоз, поскольку одним из наиболее важных вопросов при проведении ИФА является вопрос о специфичности результатов. Так при применении только скриниру-ющего теста, некоторые пробы, взятые от животных с различной патологией, могут давать ложнополо-жительные результаты вследствие синтеза перекрестно-реагирующих антител. Поэтому возможное существование ложнопозитивных результатов ставит перед лабораторным работником задачу их разграничения с истинным выявлением антител к ВЛКРС. Для решения этой задачи и служит ИФА-набор VeriTest, который применяется для подтверждения положительных результатов скринирующего теста.
Таким образом, алгоритм серологического обследования на лейкоз при совместном применении РИД и ИФА следующий.
1) Животные положительные в РИД считаются инфицированными, в ИФА не проверяются и подлежат выбраковке.
2) Отрицательные результаты в РИД, должны быть перепроверены в ИФА и только после этого животные могут считаться серонегативными.
3) Первичное тестирование проб в ИФА проводится в скринирующем тесте и при отсутствии положительной реакции выдается заключение об отсутствии серологических данных инфицирования ВЛКРС. При положительном результате теста проба подлежит исследованию в подтверждающем тесте. При отрицательном результате подтверждающего теста, проба считается серонегативной по ВЛКРС, положительный результат является основанием для окончательного подтверждения серологического диагноза на лейкоз.
Такая схема проведения диагностических исследование за два последних года с успехом апробирована в ряде ветеринарных лабораторий нашей страны и показан ее практический эффект.
Если имеется возможность, то вместо скринирующего ИФА-набора можно сразу же использовать ИФА-набор VeriTest и тем самым упростить алгоритм серологического обследования на лейкоз и сократить число необходимых анализов. ИФА - диагностика ящура
"Набор для выявления антител к вирусу ящура ЗАВС иммуноферментным методом (ИФА)" предназначен для выявления постинфекционных антител в сыворотке крови крупного рогатого скота.
Набор позволяет обнаружить антитела к неструктурному белку вируса ящура - ЗАВС (в системе используется рекомбинантный белок MSP ЗАВС в качестве антигена), который отсутствует (или скрыт для распознавания клетками иммунной системы) в инактивированных вакцинных препаратах. Поэтому у здоровых или вакцинированных животных антител к ЗАВС белку нет (реакция отрицательная),
а у экспериментально зараженных или спонтанно инфицированных животных (даже ранее вакцинированных), в организме которых присутствовал живой вирус ящура - антитела данной специфичности есть (реакция положительная).
Данное заключение демонстрируют результаты, полученные нами при испытании данного набора в профильной лаборатории ФГУ ВНИИЗЖ (табл.1). Для проверки были использованы сыворотки крови крупного рогатого скота, полученные от. а) животных, переболевших ящуром (в динамике с интервалом 3- 5 суток после заражения); б) от животных, вакцинированных против ящура; в) животных сначала вакцинированных против ящура, затем экспериментально зараженных вирулентным вирусом; г) от клинически здоровых неиммунных животных. Исследования проводили в сравнительном аспекте с набором аналогичной направленности и с параллельным определением активности испытуемых сывороток в реакции микронейтрализации и в стандартном варианте непрямого ЙфА, где в качестве антигена используются структурные белки вириона.
Таким образом, отличительной особенностью ИФА-набора для выявления антител к антигену ЗАВС вируса ящура является его способность дифференцировать здоровых и вакцинированных животных от инфицированных и вирусоносите-лей, поэтому его использование незаменимо при проведении оздоровительных и мониторинговых мероприятий.
ИФА - диагностика бруцеллеза
В течение последних лет ряд зарубежных компаний выпускают ИФА-наборы, предназначенные для выявления антител к возбудителям бруцеллеза крупного рогатого скота, овец и коз (Brucella abortus и Brucella melitensis). В настоящее время в НПО проводятся подобные исследования.
В лабораторных исследованиях обычно используют два варианта ИФА: непрямой и конкурентный. Однако на практике наибольшей ценностью обладает конкурентный ИФА, отличительной особенностью которого является возможность дифференцировать животных инфицированных бруцеллами от животных, вакцинированных вакциной из штамма 19 (и возможно из штамма 82). Метод основан на конкурентном взаимодействии моноклональных антител к о-полисахариду S-LPS антигена В. abortus и сывороточных антител к бруцеллам с S-LPS антигеном В. abortus. При отсутствии в исследуемой сыворотке крови антител к В. abortus или В. melitensis, МкА связывается с иммобилизованным S-LPS антигеном, формируя при этом комплекс антиген-антитело. Полученный иммунный комплекс выявляется после взаимодействия с антивидовым конъюгатом, фермент которого после добавления субстрата, вызывает разложение субстрат-индикаторного раствора и образование окрашенного продукта. Если исследуемая сыворотка содержит антитела к бруцеллам, то они конкурируют с МкА за связывание с сайтами антигена и препятствуют взаимодействию МкА с о-полисахаридом S-LPS антигена, в результате чего интенсивность окраски снижается.
Сыворотка крови животных, вакцинированных вакциной из штамма 19, содержит низкоаффинные антитела, которые не конкурируют с МкА за связывание с антигеном, что приводит к отрицательной реакции. Однако в ряде случаев через 6 месяцев после вакцинации животные могут реагировать положительно.
Нами были проведены предварительные испытания двух тест-систем с использованием охарактеризованных в РА сывороток крови крупного рогатого, полученных из ФГУ ВГНКИ (табл.2).
Проведенные исследования показали, что по чувствительности оба варианта ИФА превосходят РА, однако для подтверждения диагностической ценности конкурентного метода проводятся более расширенные испытания с хорошо охарактеризованной панелью сывороток крови, полученных от больных и вакцинированных животных. Есть предположение, что данная тест-система может быть также использована в медицине для выявления антител к бруцеллам у инфицированных людей.
Читайте также:


