Дисбактериоз микрофлоры в просвете толстого отдела кишечника
Что понимают под дисбактериозом? Какие методы диагностики являются современными и достоверными? Какие лекарственные препараты применяются при дисбактериозе? Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых
Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых достигает 10 14 , что на порядок выше общей численности клеточного состава человеческого организма. Количество микроорганизмов увеличивается в дистальном направлении, и в толстой кишке в 1 г кала содержится 10 11 бактерий, что составляет 30% сухого остатка кишечного содержимого.
В тощей кишке здоровых людей находится до 10 5 бактерий в 1 мл кишечного содержимого. Основную массу этих бактерий составляют стрептококки, стафилококки, молочнокислые палочки, другие грамположительные аэробные бактерии и грибы. В дистальном отделе подвздошной кишки количество микробов увеличивается до 10 7 –10 8 , в первую очередь за счет энтерококков, кишечной палочки, бактероидов и анаэробных бактерий. Недавно нами было установлено, что концентрация пристеночной микрофлоры тощей кишки на 6 порядков выше, чем в ее полости, и составляет 10 11 кл/мл. Около 50% биомассы пристеночной микрофлоры составляют актиномицеты, примерно 25% — аэробные кокки (стафилококки, стрептококки, энтерококки и коринеформные бактерии), от 20 до 30% приходится на бифидобактерии и лактобациллы.
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
До 90-95% микробов в толстой кишке составляют анаэробы (бифидобактерии и бактероиды), и только 5-10% всех бактерий приходится на строгую аэробную и факультативную флору (молочнокислые и кишечные палочки, энтерококки, стафилококки, грибы, протей).
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Площадь внутренней поверхности кишечника составляет около 200 м 2 . Она надежно защищена от проникновения пищевых антигенов, микробов и вирусов. Важную роль в организации этой защиты играет иммунная система организма. Около 85% лимфатической ткани человека сосредоточено в стенке кишечника, где продуцируется секреторный IgA. Кишечная микрофлора стимулирует иммунную защиту. Кишечные антигены и токсины кишечных микробов значительно увеличивают секрецию IgA в просвет кишки.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
В развитии дисбактериоза толстой кишки большую роль играют ятрогенные факторы: применение антибиотиков и сульфаниламидов, иммунодепрессантов, стероидных гормонов, рентгенотерапия, хирургические вмешательства. Антибактериальные препараты значительно подавляют не только патогенную микробную флору, но и рост нормальной микрофлоры в толстой кишке. В результате размножаются микробы, попавшие извне, или эндогенные виды, устойчивые к лекарственным препаратам (стафилококки, протей, дрожжевые грибы, энтерококки, синегнойная палочка).
Клинические проявления чрезмерного роста микроорганизмов в тонкой кишке могут полностью отсутствовать, выступать в качестве одного из патогенетических факторов хронической рецидивирующей диареи, а при некоторых болезнях, например, дивертикулезе тонкой кишки, частичной кишечной непроходимости или после хирургических операций на желудке и кишечнике, приводить к тяжелой диарее, стеаторее и В 12 -дефицитной анемии.
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
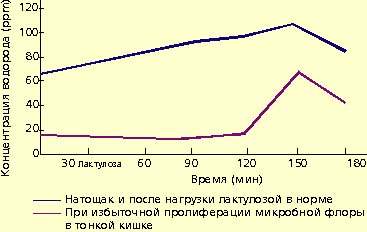 |
| Рисунок 1. Концентрация водорода в выдыхаемом воздухе |
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
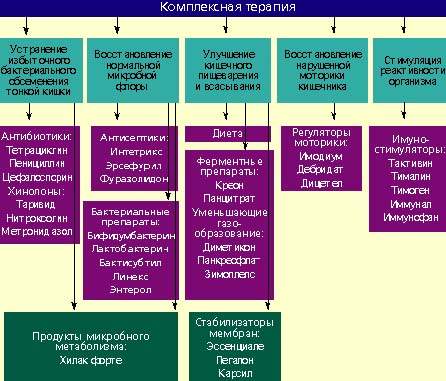 |
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
- устранение избыточного бактериального обсеменения тонкой кишки;
- восстановление нормальной микробной флоры толстой кишки;
- улучшение кишечного пищеварения и всасывания;
- восстановление нарушенной моторики кишечника;
- стимулирование реактивности организма.
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Совсем недавно появились сообщения о возможности лечения острой диареи, ассоциированной с антибактериальной терапией и Cl. difficile, большими дозами пре- и пробиотиков.
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия. Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.
Цель — баланс
Пищеварительный тракт — гетерогенная бактериальная экосистема. Вследствие низкого значения pH желудок здорового человека можно считать стерильной средой.
В кишечнике условия для роста микроорганизмов лучше. В тонком бактерий немного — 104–106/мл (высокое значение pH и быстрый транзит не способствуют увеличению их количества), а в толстом — в 100 000 раз больше.
Кишечник является строго анаэробной системой, богатой питательными веществами, с кислотностью среды от нейтральной до слабощелочной. Его бактериальная экосистема включает от 400 до 500 типов микроорганизмов, которые взаимодействуют. Многие являются компенсалами, помогают расщеплять неперевариваемые соединения, содержащиеся в пище.
У практически здоровых людей около 96% микрофлоры кишечника составляют представители облигатной (т. е. постоянно встречающейся) микрофлоры: бифидо- и лактобактерии, бактероиды, непатогенная кишечная палочка и др.
Вторая группа, куда входят факультативная (непостоянная) и условно-патогенная микрофлора, занимает лишь 2–4% от общего количества микроорганизмов. При определенных условиях (снижение местного, а тем более общего иммунитета) вызывает внутрикишечные и общие нарушения. Факультативная группа представлена микрококками, протеем, стафилококками, клостридиями, цитробактерами и др.
Третью группу составляет транзиторная (случайная) патогенная микрофлора: клостридии, синегнойная палочка, грибы рода Candida. На ее долю приходится 0,001–0,01%.
В процессе постоянного взаимодействия макро- и микроорганизмов формируется уникальная экосистема, находящаяся в состоянии динамического баланса. Существенную роль играют облигатные и факультативные анаэробы: бифидо-, лакто- и энтеробактерии, а также энтерококки. Бифидобактерии создают кислую среду и тем самым препятствуют размножению вредной микрофлоры. Кроме того, обладают выраженным антагонизмом в отношении патогенов, улучшают процессы пищеварения, поддерживают витаминный баланс и иммунный статус, участвуют в синтезе незаменимых аминокислот.
Нарушение бактериоэкологического равновесия в ЖКТ приводит к формированию дисбактериоза (дисбиоза) кишечника.
Нехорошие перемены
Дисбактериоз кишечника — это клинико-лабораторный синдром, возникающий при разных патологических состояниях. Характерны изменения количественного и (или) качественного состава нормофлоры, метаболические и иммунологические нарушения; у некоторых пациентов добавляются симптомы поражения кишечника.
При заболеваниях местного и общего характера изменяется микробный пейзаж толстой кишки. Дисбактериоз регистрируется у большинства пациентов с поражением ЖКТ инфекционной и неинфекционной природы, после острых вирусных и бактериальных инфекций внекишечной локализации, при хронической воспалительной и аллергической патологии, у страдающих злокачественными заболеваниями и лейкозами, на фоне применения цитостатиков и особенно антибиотиков. Антибиотикозависимые дисбиозы стабильны и требуют активной терапии.
Сдвиги в микрофлоре кишечника вторичны — отражают воздействие факторов, изменяющих статус кишечника или внутренний баланс самого микробиоценоза. Нарушение микробного равновесия может осложнять многие патологические состояния, быть атерогенным явлением, связанным с антибактериальной, гормональной и другой терапией, несбалансированным питанием и т. д.
Один из частых вариантов (удельный вес порой достигает 31%) дисбактериоза кишечника — кандидозный, при котором имеет место избыточный рост грибов рода Candida. Он нередко ассоциируется с пищевой аллергией и аллергическими заболеваниями вообще, а также с курением.
Лабораторные поиски
Клиническая картина дисбактериоза кишечника вариабельна, а выраженность симптоматики не всегда напрямую зависит от степени дисбиотических нарушений. Ранними и наиболее специфическими симптомами можно считать повышенное газообразование, нарушение переваривания пищи (кишечная диспепсия), изменение характера стула; при развитии дисбактериоза на фоне колита — болевой синдром, патологические примеси в кале (слизь). В более тяжелых случаях добавляются интоксикация, диарея и обезвоживание, снижение массы тела.
В диагностике и трактовке кишечного дисбактериоза большое значение имеет копрологическое исследование, дающее возможность охарактеризовать пищеварительную, ферментовыделительную, всасывательную и двигательную функции кишечника. В последнее время получили распространение методы, основанные на выявлении метаболитов микроорганизмов, — газожидкостная и ионная хроматография. В лабораториях проводят бактериологические исследования фекалий и посев на питательные среды соскобов со слизистых оболочек.
Золотым стандартом диагностики синдрома избыточного роста бактерий считается интестиноскопия с аспирацией содержимого тонкой кишки и посевом аспирата на питательную среду. Но эта методика сложна, требует общей анестезии и хорошей бактериологической базы с возможностью культивирования аэробов и анаэробов, а результат приходится ждать порядка 10 дней.
Синдром избыточного роста бактерий выявляется также по данным дыхательного теста с меченым Н2 — с лактулозой или галактозой. Бактерии разлагают лактулозу, в результате чего освобождается меченый Н2, концентрация которого затем может быть измерена в выдыхаемом воздухе. В норме лактулоза расщепляется лишь микрофлорой в толстом кишечнике. При дисбиозе и тонкая кишка заселяется микроорганизмами, расщепляющими лактулозу. При этом следует исключить ускоренное продвижение субстрата по тонкой кишке.
Посев дуоденального аспирата тоже подтверждает синдром избыточного роста бактерий: при патологии содержание микроорганизмов >106/мл (общее количество бактерий в просвете тощей кишки не превышает 104–106/мл).
Микрофлора различных отделов пищеварительного тракта значительно отличается количественно и качественно.+
Микробиологическое исследование фекалий лишь косвенно может свидетельствовать о микробном неблагополучии, т. к. состав фекальной микрофлоры отражает ситуацию только в толстой кишке, а точнее — в дистальном отделе.
Настрой на победу
Профилактика и особенно лечение дисбактериоза кишечника должны быть комплексными и предполагать:
- устранение избыточного бактериального обсеменения тонкой кишки;
- восстановление нормальной микробной флоры толстой кишки;
- улучшение кишечного пищеварения и всасывания;
- восстановление нормальной моторики кишечника;
- стимулирование реактивности организма.
Важнейшими нормальными обитателями толстого кишечника человека являются бифидобактерии (вид анаэробных палочковидных грамположительных бактерий) — 3–7% от общей фекальной микрофлоры взрослых. Нужны и лактобактерии.
Восстановлению качества и количества бифидобактерий способствует увеличение в рационе пектинов (растворимых пищевых волокон), а для лактобактерий лучшие продукты — кисломолочные. Антибиотическую активность последних повышают путем добавления никотиновой кислоты (на 1 л — 6–8 мг), тиамина (4–6 мг), токоферола (1–3 мг).
Для профилактики и лечения дисбактериоза широко используются пробиотики и пребиотики.
Пробиотики — это живые микроорганизмы (молочнокислые бактерии, чаще бифидо- или лактобактерии), нормальные обитатели кишечника здорового человека, улучшающие микробный баланс. Обладают антагонистическими свойствами по отношению к патогенам (третья группа): конкурируют за рецепторы на эпителиоцитах, питательные вещества; способны выделять ингредиенты (цитокины, масляную кислоту), ингибирующие рост патогенных бактерий. Монокультуру или комплекс живых микроорганизмов дополняют веществом, стимулирующим их колонизирующую способность и размножение.
Пробиотики содержатся в молочных продуктах со специальной закваской, кукурузных хлопьях, крупах, черном хлебе.
При наличии бродильных процессов в кишечнике надо ограничивать углеводы, пищевые волокна (клетчатку), при гнилостных — белки и жиры.
Каждому, у кого высок риск развития дисбиоза, следует избегать цельного молока, бобовых, а также продуктов, богатых эфирными маслами (чеснок, зеленый лук, репа, редька).
Для стабилизации микрофлоры кишечника в рацион включают морковный сок, сою, дрожжевой, тыквенный, картофельный и рисовый экстракты, молочную сыворотку и молозиво (обладают бифидогенным действием).
Используют растительные компоненты и при стафилококковом дисбактериозе. Полезны лесная земляника, рябина, малина, черника, шиповник, черная смородина. При протейном дисбактериозе нужны абрикосы и черная смородина; при наличии гнилостных бактерий — клюква и абрикосы. Если имеет место избыточный рост грибов рода Candida, стоит налегать на бруснику, стручковый перец, морковь.
При торпидно протекающем дисбактериозе рекомендуют дополнять лечение, подключая эффект от приема эвкалипта, календулы, аира, зверобоя. Когда подтвержден грибковый дисбактериоз с бродильной диспепсией, положительное влияние окажет цикорий растворимый.
Кроме пробиотиков, важное значение в профилактике и лечении дисбактериоза кишечника имеют пребиотики (к ним в основном относят растворимые пищевые волокна класса углеводов: фруктоолигосахариды, галактоолигосахариды). В желудке и тонкой кишке они избегают гидролиза пищеварительными ферментами и достигают толстой кишки в неизменном виде. Там подвергаются ферментации бифидо- и лактобактериями, что приводит к увеличению количества флоры и объема каловых масс. При этом важно подчеркнуть, что фруктоолигосахариды представляют собой энергетический субстрат для представителей нормальной микрофлоры кишечника (бифидо- и лактобактерий). В процессе ферментации образуются короткоцепочечные жирные кислоты (преимущественно уксусная, пропионовая, масляная), которые снижают рН в кишечнике, стимулируют перистальтику.
Укреплению защитного барьера толстой кишки при потреблении пребиотиков способствует и стимуляция выработки в ней слизи. Повышенное слизеобразование энтероцитами может быть следствием снижения рН при возросшем синтезе короткоцепочечных жирных кислот микрофлорой кишечника в ответ на введение пребиотиков. Свойствами пребиотиков в наибольшей степени обладают инулин, лактулоза, лактил, олигосахариды, лактоолигосахариды, хилак форте и др.
Инулин присутствует в клетках цикория, артишока, корней одуванчика, клубней топинамбура, фасоли, петрушки. Наиболее хорошо изучен как бифидогенный фактор — избирательно ускоряет рост и метаболизм бифидобактерий. Прием 5 г/день олигофруктозы или ≤8 г/день инулина обеспечивает значительное изменение состава кишечной микрофлоры, увеличивая численность бифидобактерий и снижая количество патогенов.
Пробиотики и пребиотики могут применяться для профилактики и лечения дисбактериоза кишечника, в т. ч. при назначении эрадикационных схем лечения Helicobacter pylori при гастроэзофагеальной рефлюксной, язвенной болезни желудка и двенадцатиперстной кишки, эрозивных гастро- и дуоденопатиях.
Применение антибиотиков нежелательно, т. к. они могут усугублять дисбиоз кишечника. Целесообразно использовать препараты, минимально влияющие на симбиотическую флору и в тоже время подавляющие рост патогенных микроорганизмов. К таким относятся нитрофураны (нифуроксазид, интетрикс) — т. н. кишечные антисептики.
Пациентам с кишечной диспепсией показаны ферментные препараты. Чаще используют панкреатин (мезим форте, трифермент, креон). При стеаторее и гипомоторной дискинезии кишечника к панкреатину добавляют желчные кислоты (панзинорм), при бродильных расстройствах — гемицеллюлозу (фестал, энзистал, дигестал). Для улучшения процессов всасывания можно назначать мембраностабилизирующие препараты (карсил, эссенциале).
При дисбактериозе, особенно в период реабилитации, показаны иммуномодуляторы (натрия нуклеинат, витамины), растительные адаптогены (элеутерококк, женьшень, эхинацея). Когда отмечена тенденция к лейкопении и требуется усилить эпителизацию слизистой оболочки, можно использовать метилурацил и пентоксил (не более двух недель).
Иван Броновец, профессор кафедры кардиологии и внутренних болезней БГМУ, доктор мед. наук
Медицинский вестник, 12 сентября 2016
Аннотация научной статьи по ветеринарным наукам, автор научной работы — Сабельникова Е. А.
В статье представлены данные отечественной и зарубежной литературы о дисбактериозе кишечника . Очевидно, что дисбиоз кишечника всегда вторичен и его коррекция должна проводиться с учетом причины, вызвавшей нарушение микробного состава кишечной флоры и клинических проявлений данного синдрома. Дана характеристика нормальной кишечной микрофлоры и ее значения для организма человека. Подчеркивается, что резидентная микрофлора оказывает влияние на развитие иммунного ответа слизистой оболочки кишечника, дифференцировку и пролиферацию эпителия, моторику кишечника, активно участвует в пищеварении и всасывании, а также синтезе витаминов и биологически активных веществ. Описаны факторы, приводящие к нарушению микробного состава кишечника, а также методы диагностики и лечения дисбактериоза. Лечебные мероприятия при дисбиозе проводятся с учетом характера и тяжести основного заболева- ния и заключаются в соблюдении диетических рекомендаций и применении препаратов, нормализующих кишечную микрофлору. С целью удаления из просвета кишечника условно патогенной микрофлоры и ее токсинов используются различные энтеросорбенты. Одним из представителей данной группы препаратов является Лактофильтрум . Препарат Лактофильтрум эффективен в лечении больных с заболеваниями кишечника, сопровождающимися дисбактериозом, как в виде монотерапии, так и в комплексе с другими лекарственными средствами.
Похожие темы научных работ по ветеринарным наукам , автор научной работы — Сабельникова Е. А.
КЛИНИЧЕСКИЕ АСПЕКТЫ ДИСБАКТЕРИОЗА КИШЕЧНИКА
Сабельникова Е. А.
Центральный научно-исследовательский институт гастроэнтерологии, Москва
Сабельникова Елена Анатольевна 111123, Москва, шоссе Энтузиастов, д. 86 Тел.: 8 (495) 305 0553 E-mail: sabelnikova_e_a@mail.ru
В статье представлены данные отечественной и зарубежной литературы о дисбактериозе кишечника. Очевидно, что дисбиоз кишечника всегда вторичен и его коррекция должна проводиться с учетом причины, вызвавшей нарушение микробного состава кишечной флоры и клинических проявлений данного синдрома.
Дана характеристика нормальной кишечной микрофлоры и ее значения для организма человека. Подчеркивается, что резидентная микрофлора оказывает влияние на развитие иммунного ответа слизистой оболочки кишечника, дифференцировку и пролиферацию эпителия, моторику кишечника, активно участвует в пищеварении и всасывании, а также синтезе витаминов и биологически активных веществ. Описаны факторы, приводящие к нарушению микробного состава кишечника, а также методы диагностики и лечения дисбактериоза.
Лечебные мероприятия при дисбиозе проводятся с учетом характера и тяжести основного заболевания и заключаются в соблюдении диетических рекомендаций и применении препаратов, нормализующих кишечную микрофлору. С целью удаления из просвета кишечника условно патогенной микрофлоры и ее токсинов используются различные энтеросорбенты. Одним из представителей данной группы препаратов является Лактофильтрум.
Препарат Лактофильтрум эффективен в лечении больных с заболеваниями кишечника, сопровождающимися дисбактериозом, как в виде монотерапии, так и в комплексе с другими лекарственными средствами.
Ключевые слова: дисбактериоз кишечника; лечение дисбиоза; Лактофильтрум.
The article presents data of domestic and foreign literature on intestinal dysbacteriosis. It is evident that intestinal dysbiosis always secondary and its correction should take into account the reasons that caused the violation of the microbial composition of the intestinal flora and the clinical manifestations of this syndrome. The characteristic of the normal intestinal microflora and its significance for the human body. It was emphasized that the resident microflora influences the development of the immune response of the intestinal mucosa, epithelial differentiation and proliferation, motility, is actively involved in the digestion and absorption, and synthesis of vitamins and bioactive substances. It was described factors leading to violation of the microbial composition of intestine, as well as methods of diagnosis and treatment of dysbiosis.
Therapeutic measures for dysbiosis conducted according to the nature and severity of underlying disease and were in compliance with dietary recommendations and the use of drugs, normalizing the intestinal microflora. In order to remove from the intestinal lumen conditionally pathogenic microorganisms and toxins using different chelators. One of the members of this group of drugs is Laktofiltrum.
Laktofiltrum drug effective in treating patients with bowel diseases, accompanied by dysbiosis, as a monotherapy and in combination with other drugs.
Keywords: intestinal dysbiosis; treatment of dysbiosis; Laktofiltrum.
№03/2011 ЭКСПЕРИМЕНТАЛЬНАЯ И КЛИНИЧЕСКАЯ
Несмотря на значительный прогресс в изучении качественного и количественного состава микрофлоры, остается много спорных вопросов, связанных не только с диагностикой, но и с лечением дисбактериоза (дисбиоза) кишечника.
В современном понятии дисбактериоз кишечника представляет собой клинико-лабораторный синдром, связанный с изменением качественного и /или количественного состава микрофлоры кишечника с последующим развитием метаболических и иммунологических нарушений с возможным развитием желудочно-кишечных расстройств [2]. Выраженный сдвиг видового и количественного соотношения микробов прежде всего приводит к подавлению нормальной микрофлоры желудочнокишечного тракта и размножению условно патогенной.
В настоящее время не вызывает сомнения тот факт, что такое патологическое состояние, как дисбактериоз, не является заболеванием, а представляет собой лишь отклонение одного из параметров гомеостаза [3]. Дисбактериоз всегда вторичен, но, являясь по сути микробиологическим феноменом, часто сам выступает в качестве начального этапа
формирования многих заболеваний или же усугубляет течение основного патологического процесса [4]. Тем не менее усилия врачей должны быть в первую очередь направлены на устранение причины, вызвавшей нарушение микрофлоры, а коррекция дисбиотических нарушений должна проводиться при наличии клинических проявлений данного синдрома.
ЗНАЧЕНИЕ НОРМАЛЬНОЙ КИШЕЧНОЙ МИКРОФЛОРЫ
В настоящее время известно, что микробиота кишечника представлена более чем 600 видами микробов, основными из которых являются бифидобактерии и семейство бактероидов. Концентрация бактерий резко возрастает в дистальном отделе тонкой кишки и в толстой кишке составляет 1011 -1012 бактерий на 1 г кишечного содержимого, при этом на бактерии приходится до 60% каловых масс [10; 11]. Аэробные бактерии, представленные кишечными палочками, лактобациллами, энтерококками и др., составляют сопутствующую микрофлору. К остаточной микрофлоре относят стафилококки, клостридии, протей и грибы. Установлено, что значительную часть бактерий составляют не выделенные в культуре, а новые микроорганизмы [12].
Важной деталью является тот факт, что взаимодействие между нормальной микрофлорой и организмом человека происходит в основном на поверхности слизистой оболочки кишечника, видовой состав бактерий которой существенно отличается от состава внутрипросветной микрофлоры [12].
На протяжении жизни человека комбинация преобладающих видов бактерий может меняться в зависимости от питания, образа жизни и возраста [13; 14]. Однако некоторые исследователи полагают, что генетические факторы оказывают больше влияния на видовой состав микробиоты, чем питание или факторы окружающей среды [15]. В опытах на млекопитающих животных было установлено, что на состав микрофлоры, стерильного от рождения потомства, влияют характер родов, тип вскармливании, гигиенические мероприятия и применение лекарственных средств [16, 17]. Одними из первых заселяют кишечник бифидо- и энтеробактерии, которые путем влияния на экспрессию генов хозяина создают подходящую для себя среду обитания и препятствуют росту других бактерий, что и определяет дальнейший состав микробиоты [18; 19].
Нормальная кишечная микрофлора оказывает на организм человека ряд благоприятных воздействий. Одной из важнейших функций кишечной микрофлоры является обеспечение колонизационной резистентности, которая представляет собой совокупность механизмов, обеспечивающих стабильный состав микрофлоры и предотвращение заселение организма хозяина посторонними микроорганизмами. Подобная функция обеспечивается за счет комплекса факторов антагонистической активности, адгезивных свойств различных представителей нормальной флоры и конкуренции с экзогенными микроорганизмами за рецепторы связывания и факторы питания [20]. Воздействие на эпителиальные клетки кишечника заключается в укреплении эпителиального барьера за счет индукции ингибитора комплемента, сокращения плотных контактов в апикальной мембране, блокирования белка плотных контактов и увеличения трансэпителиальной резистентности 23.
Резидентная микрофлора оказывает влияние на развитие иммунного ответа слизистой оболочки, стимулируя синтез иммуноглобулинов и цитокинов 25. Выработка короткоцепочечных жирных кислот влияет на дифференцировку и пролиферацию эпителия, моторику кишечника [27]. Помимо этого нормальная микрофлора активно участвует в пищеварении и всасывании, а также синтезе витаминов и биологически активных веществ 29.
ФАКТОРЫ, ВЛИЯЮЩИЕ НА МИКРОФЛОРУ КИШЕЧНИКА
Факторы, приводящие к нарушению микробного состава кишечника, достаточно многочисленны. Условно их можно разделить на экзогенные и эндогенные. Из экзогенных факторов значение имеют неадекватное питание с дефицитом пищевых волокон и избытком рафинированных продуктов, злоупотребление алкоголем, воздействие бытовых и промышленных загрязнителей, физический и эмоциональный стресс. Значительные нарушения микробиоты с увеличением количества
антибиотикоустойчивых патогенных микроорганизмов возникают при длительном и бесконтрольном приеме антибиотиков широкого спектра действия. Помимо антибактериальных препаратов к дисбиотическим изменениям могут приводить употребление наркотических и местноанестезирующих веществ, прием слабительных, отхаркивающих, психотропных и многих других лекарственных препаратов [31]. К эндогенным факторам можно отнести острые и хронические заболевания желудочно-кишечного тракта (ЖКТ), иммунодефицитные состояния различного происхождения, тяжелые хронические инфекции, заболевания обмена веществ, оперативные вмешательства и возраст (младенческий и старческий). Известно, что почти у всех больных с патологией ЖКТ имеются те или иные проявления дисбактериоза. Нарушения микрофлоры характеризуются снижением числа бифидо- и лактобактерий, нормальной кишечной палочки, увеличением количества энтерококков, стафилококков, протеев, клостридий, энтеробактерий, грибов рода Candida.
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ КИШЕЧНОГО ДИСБИОЗА
Клинические симптомы кишечного дисбактериоза неспецифичны. Как правило, отсутствует прямая зависимость между клиническими проявлениями и степенью дисбиотических изменений.
Так, например, клинические проявления СИБР могут полностью отсутствовать или быть одним из патогенетических факторов хронической рецидивирующей диареи. У ряда больных дисбиотические изменения микрофлоры могут приводить к тяжелой диарее со стеатореей, синдрому нарушенного всасывания и В12-дефицитной анемии. Наличие большого количества эшерихий, клебсиелл, протея, энтерококков, бактероидов и других представителей условно патогенной микрофлоры способствует развитию воспалительных изменений в слизистой оболочке тонкой кишки, повышению ее проницаемости по отношению к пищевым и микробным антигенам. Развитие эндогенных инфекций и эндотоксикозов вследствие массивной бактериальной транслокации чаще всего развивается у больных с тяжелыми травмами, ожоговой болезнью, новорожденных и престарелых людей [8].
Условно патогенные микроорганизмы, в том числе неспорообразующие анаэробные бактерии, не обладают органным тропизмом, поэтому клиническая картина при дисбиозе очень разнообразна и не имеет нозологической специфичности.
Определенный интерес представляет собой достаточно специфичная клиническая картина псевдомембранозного колита, причиной которого является длительное употребление антибиотиков.
Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Газожидкостная хроматография (ГЖХ) представляет собой метод диагностики кишечной флоры по метаболитам (индикан, паракрезол, фенол, 14СО2, аммиак и др.). Спектр определяемых короткоцепочечных жирных кислот (КЖК) позволяет сделать заключение о таксономическом положении всех микробов, присутствующих в исследуемом материале. Преимуществом изучения КЖК является то, что они характеризуют преимущественно анаэробный спектр микроорганизмов, культивирование которых представляет большие технические сложности. ГЖХ может применяться в качестве экспресс-метода, однако его специфичность составляет 50 - 90%, а чувствительность — 25 - 100%.
Метод газовой хроматографии в сочетании с масс-спектрометрией [34] основан на определении компонентов бактериальных клеток, появляющихся в результате их естественного отмирания или атаки компонентов иммунной системы. В качестве маркеров используют минорные липидные компоненты мембран микробов. По их содержанию и количеству можно определить до 170 видов бактерий и грибов [35].
МЕТОДЫ КОРРЕКЦИИ НАРУШЕНИЯ КИШЕЧНОЙ МИКРОФЛОРЫ
Лечебные мероприятия при дисбиозе должны проводиться с учетом характера и тяжести основного заболевания. Обязательным условием является соблюдение диетических рекомендаций.
Все препараты, используемые для коррекции микрофлоры кишечника, принято подразделять на пробиотики, пребиотики и синбиотики.
Пребиотики применяются для стимуляции роста нормальной флоры кишечника. Они состоят из продуктов метаболизма нормальных микроорганизмов и компонентов, способствующих их росту, и представляют собой разновидность углеводов, не расщепляющихся в верхних отделах ЖКТ. Пребиотики не подвергаются гидролизу пищеварительными ферментами человека и адсорбируются в верхних отделах пищеварительного тракта. Хорошо известными препаратами из этой группы являются препараты лактулозы и лекарственные средства, представляющие собой концентрат продуктов метаболизма сахаролитических и протеолитических представителей микрофлоры, способствующих восстановлению нормальной микрофлоры и поддерживающих физиологические способности слизистой оболочки кишечника.
К синбиотикам относятся препараты, содержащие живые микроорганизмы и пребиотики. Как правило, это биологически активные добавки, входящие в состав функционального питания и обогащенные одним или несколькими штаммами представителей родов Lactobacillus и / или Bifidobacterium. В нашей стране используются биовестин-лакто (содержит бифидогенные факторы и биомассу B. bifidum, B. adolescentis, L. plantarum); мальтидофилюс, (маль-тодекстрин и биомасса B. bifidum, L. acidоphilus, L. bulgaricus); бифидо-бак (фруктоолигосахариды
из топинамбура и комплекс из бифидобактерий и лактобацилл) и ламинолакт (комплекс E. faecium Ь-3, изолят соевого белка, морской капусты, растительных экстрактов).
С целью удаления из просвета кишечника условно патогенной микрофлоры и ее токсинов используются также различные энтеросорбенты.
Энтеросорбция, как и другие способы лечения, претерпевает определенную эволюцию. Тенденции в развитии этого направления зависят от технологических возможностей при создании энтеросорбентов, конкурирующих направлений методов детоксикации и метаболической коррекции. В качестве энтеросорбентов, применяемых в медицине, до сих пор в основном используются пористые углеродные адсорбенты, в частности активированные угли разного происхождения. В то же время существует большой класс природных полимеров на основе лигнина, хитина, целлюлозы, глин (алюмосиликаты, цеолиты) и др., имеющих высокие адсорбционные и каталитические свойства.
Лактофильтрум — комплексный препарат, содержащий 355 мг гидролизного лигнина и 120 мг лактулозы.
Лактулоза — синтетический дисахарид, не встречающийся в природе и состоящий из галактозы и фруктозы. В толстой кишке лактуло-за является идеальным питательным субстратом для сахаролитических бактерий, которые растут и размножаются при применении препарата. В то же время соперничество за питательные вещества приводит к угнетению протеолитической флоры, продуцирующей токсины и являющейся
потенциально патогенной. Лактулоза в толстой кишке гидролизуется до моносахаридов (фруктозы и галактозы), а затем — до короткоцепочечных жирных кислот (органических кислот, обладающих низкой молекулярной массой). Это вызывает снижение концентрации среднецепочечных жирных кислот, которые имеют токсические эффекты. В результате гидролиза лактулозы и образования органических кислот снижается рН содержимого толстой кишки, повышается осмотическое давление в просвете кишки, активизируется перистальтика. Лактулоза является источником углеводов и энергии, необходимой для роста бифидобактерий и лактобактерий, что приводит к увеличению их массы.
Сочетание эффективного сорбента и пре-биотика позволило производителям создать уникальный по своим возможностям комплекс Лактофильтрум, объединяющий достоинства лигнинов и лактулозы.
По данным некоторых клинических исследований, Лактофильтрум хорошо зарекомендовал себя у больных с синдромом раздраженного кишечника. Препарат эффективен у взрослых с неустойчивым стулом или со склонностью к запорам, а у детей — при дисбактериозе легкой и средней степени тяжести, развившегося после приема антибактериальных препаратов [36; 37]. Проведенные исследования позволили сделать заключение о возможности применения отечественного препарата Лактофильтрум, обладающего пребиотической активностью, при дисбиозах низкой и средней степени выраженности, особенно с преобладанием запоров в клинической картине, а также после любого курса антибактериальной или антихеликобактерной терапии.
Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Читайте также:


