Чем отличаются микробы от инфекции
Микроорганизмы вокруг нас: бактерии, вирусы, грибы, простейшие, а также гельминты и другие паразиты; их природа и функции. Элементарные знания и правила поведения, помогающие существенно уменьшить вероятность заражения и предотвратить возникновение серьезных патологических процессов в нашем организме.
До сих пор мы рассматривали работу систем и органов человека в отсутствии воздействия болезнетворных микробов (микроорганизмов). В повседневной жизни нас постоянно окружают микробы. Они находятся в воздухе, которым мы дышим, в почве, в воде, на нашей коже и даже внутри нас. Большинство из них относительно безвредны для человека, но много и опасных.
Особенно опасны микроорганизмы, способные вызвать эпидемию, когда распространение инфекционной болезни значительно превышает уровень заболеваемости, обычно регистрируемый в данной местности, или даже шире - пандемию, когда болезнь быстро распространяется на территории ряда стран и континентов. В истории человечества наиболее известны пандемии чумы и холеры.
В VI веке после прошедшей по Европе пандемии чумы погибло 100 миллионов человек. Вторая пандемия, названная "черной смертью", за три года (1347-1350 годы) унесла более 50 миллионов жизней, при этом Европа потеряла четверть своего населения. К счастью, в наши дни чума, и этим гордится и фармакология, и медицина, практически ликвидирована.
Также неоднократно бушевала и холера. Первая зарегистрированная пандемия этого "бича народов" продолжалась с 1817 по 1823 год. Началась она в Индии и затем распространилась по всему миру. На протяжении XIX века пандемии холеры возникали вновь и вновь, охватывая все страны. Отмечены, как минимум, четыре вспышки этой инфекции, длившиеся от 8 до 15 лет каждая. Последняя пандемия холеры длилась 24 года (1902-1926 годы)! Без сомнения, число жертв этих бедствий было огромным. Как считают, не войны и стихийные бедствия помешали населению нашей планеты за 150000 лет существования превзойти 10-миллиардный уровень населенности, а пандемии.
Кроме холеры и чумы, миллионы жизней уносили и другие инфекционные заболевания - дизентерия, брюшной тиф. От последнего только в Петербурге в XIX веке каждый год умирало около 1000 человек.
Однако не только такие угрожающие жизни инфекции заставляют страдать человечество. Вспомним хотя бы грибковые поражения ногтей.
Слово "инфекция" пришло к нам из латинского языка и в переводе означает "заражать". В настоящее время под инфекцией понимают заболевание, вызванное микроорганизмами, к которым относят бактерии, вирусы, грибы и простейшие.
Чуть выше мы уже упоминали, что не все микроорганизмы вызывают заболевания - существуют, и их много, вполне безвредные для человека и животных микробы, которые привыкли мирно сосуществовать, не вторгаясь в чужие сферы жизни. В этой главе мы будем говорить только о способных привести к инфекционной болезни (патогенных по отношению к человеку) микроорганизмах.
Инфекционные заболевания сопровождают человечество с самого его появления, но многие тысячелетия истинная природа инфекций не была известна. Только в конце XIX века французский ученый Луи Пастер открыл причину этих заболеваний - микроорганизмы, и сделал возможным поиск лекарств для борьбы с ними. По иронии судьбы, Л. Пастер только в 60 лет был избран членом Академии наук и не за это открытие, а за работы по кристаллографии, выполненные им еще в молодости.
История открытия возбудителей инфекционных заболеваний изобилует многими яркими страницами. Вот одна из них.
По окончании медицинского факультета Геттингенского университета Роберт Кох получил скромную должность уездного врача. Он быстро завоевал уважение пациентов, и его врачебная практика стала приносить ощутимый доход. В день 28-летия (было это в 1871 году) жена подарила ему микроскоп. Купленный как игрушка, этот микроскоп перевернул всю жизнь Коха. Он увлекся микробиологией и потерял интерес к врачеванию. Его воображение поразили опыты Л. Пастера, утверждавшего, что все болезни вызываются бактериями. Р. Кох занялся поиском возбудителя туберкулеза - тяжелой болезни и сейчас еще уносящей много жизней. Он рассматривал под микроскопом органы человека, умершего от скоротечной чахотки (туберкулеза легких), но увидеть бактерии ему не удавалось. И тогда - гениальное решение - он окрасил исследуемые ткани специальными красителями. Этот год - 1877 - стал историческим для медицины. В окрашенном в синий цвет срезе легочной ткани можно было увидеть множество тоненьких палочек. За эти "палочки", позже названные "палочками Коха", выдающийся ученый, как первооткрыватель возбудителя туберкулеза, был удостоен Нобелевской премии.
Кто же они, наши невидимые "враги", заставляющие иной раз трепетать все человечество и приносящие ему столько бед?
Бактерии - одноклеточные микроорганизмы, жизнь которых подчиняется законам, описанным нами в главе 1.1. Как и все клетки, они размножаются делением. Бактерии отличаются большим разнообразием форм; они бывают шаровидными (кокки), в форме палочки (бациллы), вытянутые и изогнутые (спирохеты, лептоспиры, вибрионы). Бактерии, для роста которых требуется кислород, называют аэробами, а те, которые растут в отсутствии кислорода, - анаэробами. Кроме того, все бактерии подразделяются на грамположительные и грамотрицательные. Что это значит? В 1884 году датский бактериолог, фармаколог и врач Грам предложил окрашивать бактерии красителем розанилином (фуксином). Некоторые бактерии имеют в клеточной мембране специальный белок - пептидогликан. Они окрашиваются по методу Грама, поэтому и названы "грамположительными". Бактерии, в клеточной мембране которых нет такого белка, окрашиванию по Граму не подвергаются и, вследствие этого, получили название "грамотрицательных".
Способность бактерий вызывать инфекционные заболевания называют болезнетворностью, или патогенностью. Патогенными для человека являются те бактерии, которые, попадая в организм, преодолевают барьеры иммунной системы и вырабатывают яды (токсины), отравляющие различные ткани и органы. Бактерии, которые живут внутри нас, относят к естественной микробной флоре человека (например, кишечная флора). Часть их необходима для нашего организма. Они участвуют в переваривании пищи, вырабатывают витамины, помогают бороться с патогенными микробами. Однако другие, их так и называют - условно-патогенными, могут вызвать заболевание лишь в определенных условиях, например, при снижении сопротивляемости организма человека.
Вирусы - внутриклеточные паразиты, являющиеся причиной многочисленных заболеваний человека и животных. Есть вирусы, поражающие даже бактерии, их называют фаги. Вирусы нельзя относить в полном смысле слова к живым существам, т.к. это организмы, не имеющие клеточного строения, но они проявляют некоторые свойства живого: способны размножаться (только в живых клетках), обладают наследственностью и изменчивостью. В клетку вирусы попадают тем же путем, что и питательные вещества. В ней они начинают быстро размножаться и вызывают гибель клетки. Одна вирусная частица дает потомство в тысячи особей, каждая из которых может вновь поразить здоровую клетку. Известно более тысячи разновидностей вирусов, около половины из них опасны для человека. Примерами являются вирусы натуральной оспы, герпеса, аденовирусы (вызывают острые респираторные заболевания, или ОРЗ), гриппа, бешенства, краснухи, полиомиелита и энцефалитов, иммунодефицита человека (ВИЧ), вызывающие СПИД (синдром приобретенного иммунодефицита).
Грибы - одноклеточные или многоклеточные микроорганизмы, большинство которых питается разлагающимися органическими веществами растительного или животного происхождения. Часть их патогенна, другие - условно-патогенны и часто входят в состав естественной микробной флоры человека. При ослаблении иммунитета или при нарушении равновесия между бактериями и грибами в полости рта и в кишечнике (например, при длительном применении антибиотиков или гормональных средств) они могут вызывать различные заболевания. Плесневые грибы вызывают микозы, дрожжевые и дрожжеподобные грибы - кандидозы, дерматофиты - поражают кожу.
Простейшие - микроорганизмы, составляющие подцарство одноклеточных животных. Они широко распространены в природе и, попадая в организм человека, могут паразитировать в нем. Простейшие являются возбудителями амебиаза, лейшманиоза, лямблиоза, малярии и других инфекционных заболеваний.
С открытия роли микроорганизмов в развитии инфекционных заболеваний началась долгая и трудная работа по поиску противомикробных средств. В результате этой многолетней работы медицина сейчас располагает большим арсеналом высокоэффективных лекарств, которые позволяют успешно бороться со многими, ранее неизлечимыми заболеваниями.
Впоследствии родился новый термин "химиотерапия", который предложил один из основоположников иммунологии немецкий ученый П. Эрлих. Химиотерапией стали называть подавление лекарственным средством жизнедеятельности возбудителей инфекции или опухолевых клеток без причинения вреда (в идеале) клеткам человека.
В основе терминов химиотерапия и родившегося от него химиотерапевтические средства лежит избирательность воздействия на чужеродную или ставшую таковой (например, под влиянием вируса) клетку внутри человеческого организма.
Очень важно правильно применять химиотерапевтические средства, так как микроорганизмы легко изменяются (мутируют) и становятся устойчивыми к действию антибиотика, который действовал на них раньше.
Препараты, не обладающие избирательностью действия - антисептики и дезинфицирующие средства, губительно влияют на большинство микроорганизмов и, увы, человеческие клетки, а значит, их, как правило, нельзя применять в виде инъекций.
Главу мы назвали "Противомикробные и противопаразитарные средства", так как рассматриваем в ней не только те лекарства, которые действуют на микроорганизмы, но и те, которые убивают паразитов, не относящихся к микроорганизмам - глистов (гельминтов), вшей, чесоточных клещей.

Каждому из нас известно, что мы постоянно сталкиваемся со множеством разнообразных микроорганизмов. Мы их не видим и часто даже не задумываемся о них.
Действительно, микробы есть везде: в воздухе, в воде, в почве, в организме человека и животных, на всех поверхностях и предметах вокруг нас. Ученым удалось подсчитать, что в теле здорового человека находится около 10 000 видов бактерий, большинство из которых не причиняют нам никакого вреда. В тоже время в природе встречаются как полезные микроорганизмы, так и вредные. Все микроорганизмы можно разделить на бактерии, вирусы и фаги, грибы, дрожжи.



Мы не будем углубляться в полную и глубокую классификацию всех микроорганизмов, остановимся только на том, какие наиболее известные заболевания могут вызывать бактерии, вирусы и грибы.
К наиболее известным бактериальным инфекциям можно отнести: туберкулез, тиф, большинство кишечных инфекций, чуму, холеру, сибирскую язву, дифтерию, коклюш, столбняк, сифилис, гонорею. Стрептококки могут вызывать ангину и рожистое воспаление, стафилококки — различные воспалительные и гнойные процессы. Палочковидные бактерии являются возбудителями сальмонеллеза, дизентерии, брюшного тифа, туберкулеза. Извилистые бактерии ответсвенны за такие болезни как холера, сифилис.
Наиболее известные вирусные инфекции: грипп, ОРВИ, герпетические инфекции, ВИЧ, корь, краснуха, гепатиты, паротит, оспа, лихорадка, полиомиелит, клещевой энцефалит.
Болезни, вызываемые паразитическими грибами называются микозы. Встречаются микозы кожи (дерматомикозы) и микозы внутренних органов. Кератомикозы - поражения рогового слоя кожи. Д ерматофитии - поражения всех слоев кожи и волос. К андидозы - поражения кожи, слизистых, внутренних органов. Трихофития – вызывают прежде всего поражение волос. Глубокие микозы - поражения внутренних органов, вторично - кожи.
Знание механизмов и путей передачи инфекции и воздействие на них являются очень важным фактором для профилактики инфекционных заболеваний.
- алиментарный (фекально-оральный);
- воздушно-капельный;
- контактный;
- гемоконтактный (кровяной);

Алиментарный механизм передачи инфекции через органы системы пищеварения. Различают:
- Пищевой путь – заражение происходит при употреблении пищи. Кишечные инфекции, сальмонеллез, дизентерия может попасть в пищу через немытые руку, через таких переносчиков как мухи, и при нарушениях технологии приготовления пищи.
- Водный путь – выделение возбудителя происходит из кишечника, фактором передачи является вода, в которую попал возбудитель. Типичным примером инфекции с водным путем передачи является холера, которая относится к особо-опасным инфекциям.

Инфицирование происходит при вдыхании воздуха вместе с возбудителем. Основные пути передачи инфекции:
- Капельный путь –инфекция передается от зараженного человека во время чихания или кашля, разговоре на близком расстоянии друг от друга. Таким путем легко можно заразиться, например, гриппом, скарлатиной, ветряной оспой, корью
- Пылевой путь – возможен при длительном сохранении возбудителя в пыли. Микробы могут сохраняться в пыли очень длительное время.
Контактный механизм передачи
Реализуется при контакте восприимчивого организма с источником инфекции. Контакт может быть прямым и опосредованным, в зависимости от этого есть такие пути передачи 
инфекции:
Гемоконтактный (кровяной) механизм передачи
Возможен такой механизм передачи при попадании зараженной возбудителем крови в кровь здорового человека. Есть 3 пути передачи инфекции:
- Гемотрансфузионный путь – связан с переливанием крови и ее компонентов, медицинскими манипуляциями, сопровождающимися повреждением кожи и слизистых при недостаточной стерилизации инструментария. Также встречаются случаи заражения при недоброкачественной обработке инструментов в парикмахерских, салонах татуировок (вирусные гепатиты В, С, ВИЧ СПИД).
- Вертикальный путь – заражение плода от крови матери через плаценту или во время родов (ВИЧ СПИД, вирусные гепатиты).
- Трансмиссивный путь – реализуется через укусы кровососущих насекомых (малярия при укусах комаров, клещевой боррелиоз – укусы клещей, лейшманиоз – москиты, возвратный тиф - вши).
Особенностью некоторых инфекций является наличие нескольких путей передачи.
Как не банально это будет звучать, но профилактика- это основа всего! Как и любые другие болезни, инфекционные заболевания проще не допустить, чем потом лечить.
Для успешного результата необходимо работать в трех самых важных направлениях:
- Уничтожение микроорганизмов: бактерий, вирусов, грибов
- Воздействие на пути передачи инфекции с целью предотвращения заражения человека
- Воздействие на организм человека
Уничтожение микроорганизмов: бактерий, вирусов, грибов
Самый проверенный и эффективный способ уничтожения возбудителей инфекций- это дезинфекция, стерилизация и безусловно-соблюдение правил личной гигиены.
Воздействие на пути передачи инфекции с целью предотвращения заражения человека
При воздушно-капельном используются маски, проветривание, недопущение скопления большого количества людей в помещении
При алиментарном (пищевом) – важную роль играет личная гигиена, мытье рук, продуктов питания, отсутствие мух в помещениях, где идет приготовление пищи
При половом (контактном) – важным моментом профилактики таких инфекций является отсутствие беспорядочной половой жизни с частой сменой партнеров и использование презервативов
При кровяном – в этом случае предотвратить инфекционные заболевания помогут стерильные инструменты в медицинских учреждениях, салонах красоты, маникюрных и педикюрных салонах. Все усилия надо направить на предотвращение нарушения целостности кожи и слизистых оболочек.
Воздействие на организм человека
Прежде всего это общее укрепление иммунитета человека за счет здорового образа жизни и создание иммунитета (невосприимчивости) к определенной инфекции за счет вакцинации.
Каким бы не был метод профилактики, его использование поможет предотвратить заболевание, что особенно важно при неизлечимых инфекциях, таких как ВИЧ СПИД, бешенство и вирусные гепатиты.
Будьте всегда здоровы и счастливы!
Бактериофаги – это вирусы, которые поражают только бактерий. В ходе инфекции они влияют на все процессы жизнедеятельности бактериальной клетки, фактически превращая ее в фабрику по производству вирусного потомства. В конце концов клетка разрушается, а вновь образованные вирусные частицы выходят наружу и могут заражать новые бактерии.
Несмотря на огромное число и разнообразие природных фагов, встречаемся мы с ними редко. Однако бывают ситуации, когда деятельность этих вирусов не остается незамеченной. Например, на предприятиях, где производят сыры, йогурты и другие молочно-кислые продукты, часто приходится сталкиваться с вирусной атакой на бактерии, сбраживающие молоко. В большинстве таких случаев фаговая инфекция распространяется молниеносно, и полезные бактерии гибнут, что приводит к значительным экономическим потерям (Neve et al., 1994).
Именно благодаря прикладным исследованиям в интересах молочной промышленности, направленным на получение устойчивых к бактериофагам штаммов молочно-кислых бактерий, был открыт ряд механизмов, с помощью которых бактерии избегают инфекции. Параллельно были изучены способы, с помощью которых вирусы, в свою очередь, преодолевают бактериальные системы защиты (Moineau et al., 1993).
Кто защищен – тот вооружен
На сегодня известно пять основных, весьма хитроумных механизмов защиты, которые бактерии выработали в непрестанной борьбе с вирусами: изменение рецептора на поверхности клетки; исключение суперинфекции; системы абортивной инфекции; системы рестрикции-модификации и, наконец, системы CRISPR-Cas.
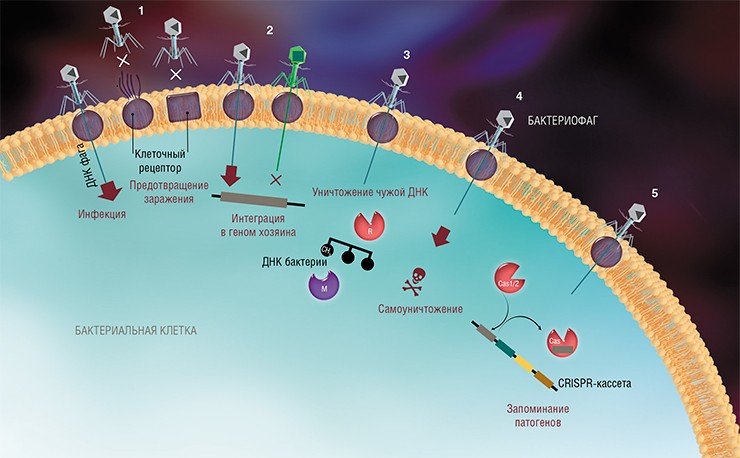
К средствам противовирусной защиты бактерий относятся и системы рестрикции-модификации, в которые входят гены, кодирующие два белка-фермента – рестриктазу и метилазу. Рестриктаза узнает определенные последовательности ДНК длиной 4—6 нуклеотидов и вносит в них двуцепочечные разрывы. Метилаза, напротив, ковалентно модифицирует эти последовательности, добавляя к отдельным нуклеотидным основаниям метильные группы, что предотвращает их узнавание рестриктазой.
Врага нужно знать в лицо
Системы CRISPR-Cas являются уникальным примером адаптивного иммунитета бактерий. При проникновении в клетку ДНК фага специальные белки Cas встраивают фрагменты вирусной ДНК длиной 25—40 нуклеотидов в определенный участок генома бактерии (Barrangou et al., 2007). Такие фрагменты называются спейсерами (от англ. spacer – промежуток), участок, где происходит встраивание, – CRISPR-кассета (от англ. Clustered Regularly Interspaced Short Palindromic Repeats), а сам процесс приобретения спейсеров – адаптацией.
Чтобы использовать спейсеры в борьбе с фаговой инфекцией, в клетке должен происходить еще один процесс, управляемый белками Cas, названный интерференцией. Суть его в том, что в ходе транскрипции CRISPR-кассеты образуется длинная молекула РНК, которая разрезается белками Cas на короткие фрагменты – защитные криспрРНК (крРНК), каждая из которых содержит один спейсер. Белки Cas вместе с молекулой крРНК образуют эффекторный комплекс, который сканирует всю ДНК клетки на наличие последовательностей, идентичных спейсеру (протоспейсеров). Найденные протоспейсеры расщепляются белками Cas (Westra et al., 2012; Jinek et al., 2012).
Системы CRISPR-Cas обнаружены у большинства прокариот – бактерий и архей. Хотя общий принцип действия всех известных систем CRISPR-Cas одинаков, механизмы их работы могут существенно отличаться в деталях. Наибольшие различия проявляются в строении и функционировании эффекторного комплекса, в связи с чем системы CRISPR-Cas делят на несколько типов. На сегодняшний день описаны шесть типов таких неродственных друг другу систем (Makarova et al., 2015; Shmakov et al., 2015).
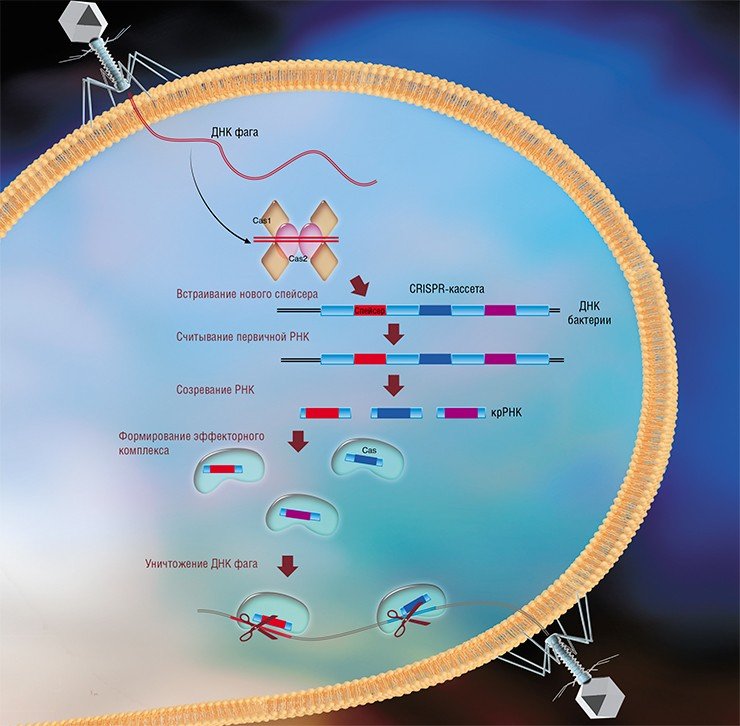
Наиболее изученной является система CRISPR-Cas I типа, которой обладает излюбленный объект молекулярно-биологических исследований – бактерия кишечная палочка (Esсherichia coli). Эффекторный комплекс в этой системе состоит из нескольких небольших белков Cas, каждый из которых отвечает за разные функции: разрезание длинной некодирующей CRISPR РНК, связывание коротких крРНК, поиск, а затем разрезание ДНК-мишени.
Гонка вооружений
Бактериофаги, как факторы среды, вызывают направленные изменения в геноме бактерий, которые наследуются и дают бактериям явное преимущество, спасая от повторных инфекций. Поэтому системы CRISPR-Cas можно считать примером ламарковской эволюции, при которой происходит наследование благоприобретенных признаков (Koonin et al., 2009)
Некоторые бактериофаги реагируют на наличие в бактериальной клетке систем CRISPR-Cas выработкой особых анти CRISPR-белков, способных связываться с белками Cas и блокировать их функции (Bondy-Denomy et al., 2015). Еще одно ухищрение — обмен участков генома вируса, на которые нацелена система CRISPR-Cas, на участки геномов родственных вирусов, отличающихся по составу нуклеотидной последовательности (Paez-Espino et al., 2015).
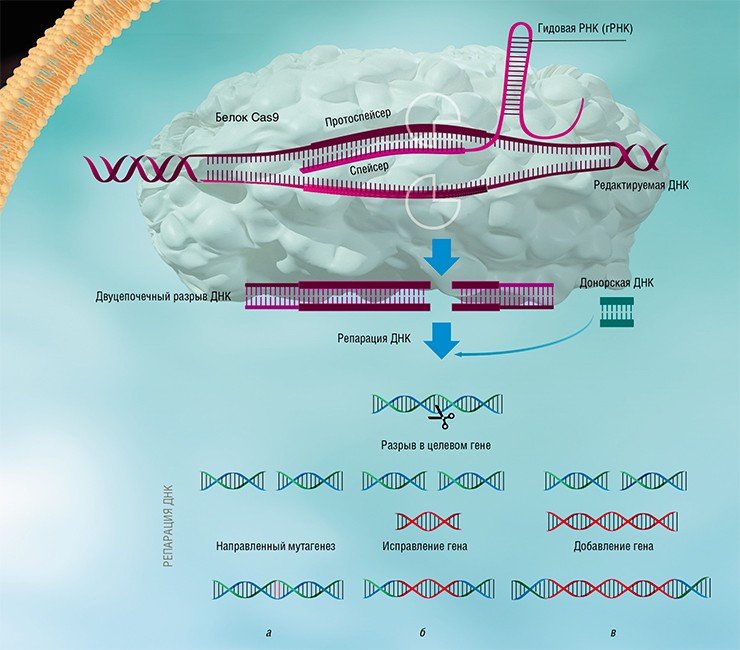
Благодаря постоянному совершенствованию биоинформатических алгоритмов поиска, а также включению в анализ все большего количества прокариотических геномов, открытие новых типов CRISPR-Cas систем является делом недалекого будущего. Предстоит также выяснить и детальные механизмы работы многих недавно открытых систем. Так, в статье, опубликованной в 2016 г. в журнале Science и посвященной анализу системы CRISPR-Cas VI типа, описан белок С2с2, образующий эффекторный комплекс с крРНК, который нацелен на деградацию не ДНК, а РНК (Abudayyeh et al., 2016). В будущем такое необычное свойство может быть использовано в медицине для регулирования активности генов путем изменения количества кодируемых ими РНК.
Изучение стратегий борьбы бактерий с бактериофагами, несмотря на свою кажущуюся фундаментальность и отвлеченность от задач практической медицины, принесло неоценимую пользу человечеству. Примерами этого могут служить методы молекулярного клонирования и редактирования геномов – направленного внесения или удаления мутаций и изменения уровня транскрипции определенных генов.
Благодаря быстрому развитию методов молекулярной биологии всего лишь через несколько лет после открытия механизма действия систем CRISPR-Cas была создана работающая технология геномного редактирования, способная бороться с болезнями, ранее считавшимися неизлечимыми. Доступность и простота этой технологии позволяют рассматривать ее как основу для медицины, ветеринарии, сельского хозяйства и биотехнологий будущего, которые будут базироваться на направленных и безопасных генных модификациях.
Нет никаких сомнений, что дальнейшее изучение взаимодействия бактерий и их вирусов может открыть перед нами такие возможности, о которых мы сейчас даже не подозреваем.
Abudayyeh O. O., Gootenberg J. S., Konermann S. et al. C 2c2 is a single-component programmable RNA-guided RNA-targeting CRISPR effector // Science. 2016. V. 353: aaf5573.
Barrangou R., Fremaux C., Deveau H. et al. CRISPR provides acquired resistance against viruses in prokaryotes // Science. 2007. V. 315. P. 1709–1712.
Bikard D., Marraffini L. A. Innate and adaptive immunity in bacteria: mechanisms of programmed genetic variation to fight bacteriophages // Curr. Opin. Immunol. 2012. V. 1 P. 15–20.
Bondy-Denomy J., Garcia B., Strum S. et al. Multiple mechanisms for CRISPR-Cas inhibition by anti-CRISPR proteins // Nature. 2015. V. 526. P. 136–139.
Calendar R., Abedon S. T. The Bacteriophages // 2nd Ed., Oxford University Press. 2006.
Datsenko K. A., Pougach K., Tikhonov A. et al. Molecular memory of prior infections activates the CRISPR/Cas adaptive bacterial immunity system // Nat. Commun. 2012. V. 3. P. 945
Jiang W., Marraffini L. A. CRISPR-Cas: New Tools for Genetic Manipulations from Bacterial Immunity Systems // Annu. Rev. Microbiol. 2015. V. 69. P. 209–28.
Jinek M., Chylinski K., Fonfara I., et al. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity // Science. 2012. V. 337. P. 816–821.
Koonin E. V., Wolf Y. I. Is evolution Darwinian or/and Lamarckian? // Biol. Direct. 2009. V. 4. P. 42.
Lopez-Pascua L., Buckling A. Increasing productivity accelerates host-parasite coevolution // J. Evol. Biol. 2008. V. 3. P. 853–860.
Makarova K. S., Wolf Y. I., et al. An updated evolutionary classification of CRISPR-Cas systems // Nat. Rev. Microbiol. 2015. V. 11. P. 722–736.
Moineau, S., Pandian S., Klaenhammer T. R. Restriction/modification systems and restriction endonucleases are more effective on lactococcal bacteriophages that have emerged recently in the dairy industry // Appl. Envir. Microbiol. 1993. V. 59. P. 197–202.
Neve H., Kemper U., et al. Monitoring and characterization of lactococcal bacteriophage in a dairy plant // Kiel. Milckwirtsch. Forschungsber. 1994. V. 46. P. 167–178.
Nuñez J. K., Harrington L. B., et al. Foreign DNA capture during CRISPR-Cas adaptive immunity // Nature. 2015a. V. 527. P. 535–538.
Nuñez J. K., Kranzusch P. J., et al. Cas1-Cas2 complex formation mediates spacer acquisition during CRISPR-Cas adaptive immunity // Nat. Struct. Mol. Biol. 2014. V. 21. P. 528–534.
Nuñez J. K., Lee A. S., Engelman A., Doudna J. A. Integrase-mediated spacer acquisition during CRISPR-Cas adaptive immunity // Nature. 2015b. V. 519. P. 193–198.
Paez-Espino D., Sharon I., et al. CRISPR Immunity Drives Rapid Phage Genome Evolution in Streptococcus thermophilus // MBio. 2015. V. 6: e00262–15.
Shmakov S., Abudayyeh O. O., Makarova K. S., et al. Discovery and Functional Characterization of Diverse Class 2 CRISPR-Cas Systems. // Mol. Cell. 2015. V. 60. P. 385–397
Tan D., Svenningsen S. L., Middelboe M. Quorum sensing determines the choice of antiphage defense strategy in Vibrio anguillarum. // mBio 2015. V. 6: e00627–15.
Westra E. R., van Erp P. B., Künne T., et al. CRISPR immunity relies on the consecutive binding and degradation of negatively supercoiled invader DNA by Cascade and Cas3 // Mol. Cell. 2012. V. 46. P. 595–605.
Работа поддержана грантом РФФИ (№ 16-34-01176)
Посоветуйте книгу друзьям! Друзьям – скидка 10%, вам – рубли
Часть вторая
Инфекции, микробы, иммунитет
Историю о том, как лиса пыталась залезть к ним в дом, ёжик слышал уже много раз. Папа тогда изловчился, подпрыгнул и пребольно уколол лисий нос, неосмотрительно засунутый в нору. Ёжик гордился папой, но немножко ему завидовал и даже мечтал о том, чтобы лиса появилась еще раз. – Я ей покажу, пусть только сунется, – шептал ёжик и старался лечь поближе к входу, чтобы первым встретить непрошеную гостью.


Преогромное число окружающих нас микроорганизмов люди именуют просто микробами. Для среднего человека, не имеющего к медицине и биологии особого отношения, все микробы вместе – нечто загадочное и, как правило, весьма вредное. Кое-кто знает о том, что микробы бывают полезными. Типичные примеры знаний о полезности микробов ограничиваются информацией о том, что они (микробы) превращают молоко в кефир, что дрожжи – это тоже микробы и что в кишечнике есть какие-то палочки, помогающие переваривать пищу.
Но всем хорошо известен тот факт, что инфекционные болезни вызываются именно микробами. Правда, в одном случае микроб, вызвавший заболевание, легко переходит от человека к человеку, в другом – это происходит редко, в третьем – не происходит почти никогда. Проще говоря, одни инфекционные болезни – заразные, а другие – нет. И медицинские работники почти повсеместно договорились о том, чтобы называть инфекционными болезнями именно болезни заразные.
Примеры? Пожалуйста. Воспаление легких или язва желудка. В 99 % случаев в основе заболевания – особые микроорганизмы. Но поразив одного человека, они становятся индивидуальной проблемой этого конкретного человека, не представляя угрозы окружающим.

Успешное лечение любой инфекционной болезни невозможно без четкой и достоверной информации об особенностях конкретного микроба, вызвавшего именно эту болезнь. Что же надо знать?
1 Источник инфекции. Кто или что? Кого бояться (избегать)? Это может быть (и, кстати, чаще всего бывает) человек, а также кошки, собаки, птицы, насекомые, некачественная пища, нестерильное лекарство и т. д.
3 Восприимчивость к болезни. При контакте с больным ветряной оспой или краснухой заражаются практически все, кто раньше не болел. При дифтерии может заболеть 1 из 10, при скарлатине – 1 из 5, при кори – 2 из 3.
4 Иммунитет. Имеется ли у человека врожденный иммунитет к конкретной болезни. Если заразились – сколько надо времени для выработки иммунитета; если переболели – можно ли заболеть еще раз.
И источник инфекции, и пути передачи, и восприимчивость, и иммунитет, и самое, пожалуй, главное – способы лечения – все это самым тесным образом связано с биологическими особенностями конкретного микроорганизма.
Что же имеется в виду под этими самыми биологическими особенностями?
Наиболее важно – деление микробов на вирусы и бактерии. Этот факт весьма принципиален, и без четкого понимания разницы между вирусами (вирусными инфекциями) и бактериями (бактериальными инфекциями) любые рассуждения, советы, объяснения и рекомендации относительно инфекционных заболеваний просто не имеют никакого смысла.


Увидеть вирус можно только с помощью электронного микроскопа. Подавляющему большинству врачей и сами вирусы, и электронные микроскопы знакомы лишь по фотографиям в умных медицинских книгах. Но болезни, вызываемые вирусами, имеют настолько характерные симптомы, что ни микроскопов, ни фотографий не надо – все и так ясно.
Принципиальной и наиболее существенной биологической особенностью любого вируса является следующая: вирусы не способны размножаться без помощи клеток других организмов.
Таким образом, вирус проникает внутрь совершенно определенной клетки, и именно эта зараженная клетка превращается как бы в завод по производству вирусов. Понятно, что работать на два фронта (и на вирус, и на организм) клетка не может, а следовательно, не может выполнять свое основное предназначение – отсюда и возникают вполне конкретные симптомы болезни.
Так, например, вирус инфекционного гепатита может существовать и размножаться только в клетках печени и больше нигде. Вирус эпидемического паротита (свинки) предпочитает клетки слюнных желез, вирус гриппа – клетки слизистой оболочки трахеи и бронхов, вирус энцефалита – клетки головного мозга и т. д. В отношении каждого вируса можно перечислить определенные клетки и ткани человеческого организма, которые он (вирус) поражает или может поразить.
Любая клетка организма выполняет целый ряд специфических, только этой клетке присущих функций. После заражения вирусом рано или поздно начинают возникать проблемы. Вирус поразил клетки печени – возникла желтуха и другие признаки печеночной недостаточности. Вирус поразил слизистую оболочку бронхов – появился кашель, в легких – хрипы, учащенное дыхание. Вирус проник в клетки головного мозга – возникли расстройства сознания, судороги, параличи.
Избирательность вирусов приводит к тому, что каждой вирусной инфекции присущи свои, совершенно конкретные симптомы, а симптомы, как теперь становится понятно, будут определяться именно неспособностью группы клеток, поврежденных вирусом, выполнять свои функции.
Итак, становится понятным следующее. Вирус гриппа способен размножаться в клетках слизистых оболочек дыхательных путей. И этот вирус ни при каких обстоятельствах не сможет вызвать воспаление печени, или почек, или сердца. Просто потому, что не сможет размножаться в клетках печени, почек, сердца.
Клетки слизистых оболочек дыхательных путей – настоящий лакомый кусочек для множества вирусов.
Вирусы эти могут отличаться и действительно отличаются друг от друга по строению, степени заразности, тяжести повреждающего воздействия на клетки, устойчивости во внешней среде, способности стимулировать выработку иммунитета и еще по очень большому количеству факторов. Но поскольку все эти вирусы поражают фактически одни и те же клетки, то симптомы болезни будут очень похожи, похожи настолько, что в подавляющем большинстве случаев определить имя вируса просто невозможно. Невозможно без специальных, часто длительных, иногда трудоемких, почти всегда дорогостоящих обследований, проб, анализов.

Именно для таких ситуаций – когда группа вирусов вызывает очень похожие болезни – и существуют специальные медицинские термины, приравненные к диагнозу. И самый типичный такой диагноз – острая респираторная вирусная инфекция (ОРВИ). Диагноз очень удобный, поскольку конкретные действия врачей и родителей зависят не столько от названия конкретного микроба, сколько от того, во-первых, микроб этот – вирус или бактерия, а во-вторых, от того, какие именно клетки данным микробом поражены. Утверждения, что инфекция эта ВИРУСНАЯ да еще и РЕСПИРАТОРНАЯ – совершенно достаточны для выбора правильного и эффективного плана лечения.
Тяжесть вирусной инфекции зависит от множества факторов. Прежде всего, от силы вируса, его способности только повреждать или полностью разрушать конкретную клетку, от количества поврежденных клеток, соответственно – от способности человеческого организма данный вирус нейтрализовать.
И еще один очень важный момент касательно тяжести болезни.
Тяжесть болезни во многом определяется состоянием или, проще говоря, степенью здоровья конкретной клетки.
Клетки слизистой оболочки носа у дочери инженера Марины намного слабее, чем точно такие же клетки у дочери лесника Насти. А клетки слизистой оболочки бронхов у курящего десятиклассника Пети слабее, чем у его некурящего одноклассника Сережи. И существует реальная вероятность того, что ОРВИ у Марины и Пети будет протекать тяжелее, чем у Насти и Сережи.


Бактерии существенно отличаются от вирусов. Во-первых, они значительно крупнее, во-вторых, представляют собой вполне законченный живой организм, который может сам себя обеспечивать и сам себя воспроизводить при наличии соответствующих условий окружающей среды (обнаружение еды, присутствие или отсутствие кислорода, подходящая температура). Попадая в организм человека, некоторые бактерии находят вышеупомянутые условия вполне пригодными для размножения и питания – вот так и возникает определенная болезнь.
До ХХ века борьба врачей с бактериальными инфекциями ничем не отличалась от борьбы с инфекциями вирусными – все усилия сводились к тому, чтобы помочь организму выстоять и справиться с болезнью самостоятельно. К счастью, возможности современной медицины заметно увеличились. Произошло это благодаря созданию нескольких групп лекарственных препаратов, позволяющих убить микроб и не нанести при этом существенного вреда человеку. Про эти лекарства вы, конечно же, слышали – антибиотики (пенициллин, тетрациклин, гентамицин), сульфаниламиды (стрептоцид, бисептол) и кое-что еще.
Мир бактерий удивительно разнообразен, как разнообразно и велико количество вызываемых ими болезней. Бактерии отличаются друг от друга размерами, особенностями строения, размножения и питания, весьма различны условия, при которых они могут нормально существовать. Одни бактерии имеют круглую форму – их называют кокками (стафилококк, пневмококк, стрептококк, менингококк, гонококк), другие – удлиненную, их называют палочками (дизентерийная палочка, коклюшная, кишечная). Бактерии часто имеют не ровную поверхность, а всякие там выросты, жгутики, реснички.
Теперь самое, пожалуй, главное.
Бактерия, какой бы противной и страшной она ни казалась, как правило, не приносит человеческому организму особого вреда.
Но, будучи полноценными живыми существами, бактерии образуют продукты своей жизнедеятельности, которые, в свою очередь, есть не что иное, как самые настоящие яды. Называются эти ядовитые вещества токсинами. Каждой бактерии присущи свои токсины, и именно токсинами, точнее, их специфическим воздействием на организм человека определяются симптомы конкретной болезни.

И количество токсинов, и опасность каждого отдельно взятого токсина у каждой бактерии свои, индивидуальные. В подавляющем большинстве случаев токсины образуются во время гибели бактерии – т. е. находятся они в самой бактериальной клетке и выделяются при ее разрушении. Бактерии в организме человека постоянно разрушаются – во-первых, они и сами по себе живут недолго, во-вторых, на то и иммунитет, чтоб с бактериями бороться, и в-третьих, бактерии разрушаются во время лечения, все теми же антибиотиками, например.
Существует очень небольшое число бактерий, жизнедеятельность которых сопровождается постоянным выделением токсинов – т. е. бактерии способны выделять токсин, но не погибать при этом!
Экзотоксины – самые (!) опасные яды из всех обнаруженных или придуманных к настоящему времени.
Болезни, возбудители которых вырабатывают экзотоксин, называются экзотоксическими. Какие это болезни? Дифтерия, столбняк, ботулизм, газовая гангрена, сибирская язва – все эти названия вы слышали неоднократно, т. е. они (болезни), хоть и экзотоксические, но, к сожалению, не экзотические (вот такой каламбур).
При некоторых инфекциях бактерии способны вырабатывать одновременно и экзо-, и эндотоксины. Тут свои сложности в лечении. Примеры таких болезней – коклюш, холера, некоторые варианты дизентерии. [10]
Опасность экзотоксических инфекций состоит в том, что антибиотики помочь не могут – за то время, что пройдет, пока их назначат (сначала ведь необходимо диагноз поставить), да пока они убьют микроб, может быть уже поздно. Антибиотики свое дело сделали, бактерий нет, но токсины остались. Они-то организм и погубят, если вовремя не ввести лекарство, нейтрализующее токсины (антитоксическую сыворотку).
Именно потому, что при лечении экзотоксических инфекций на антибиотики надежд мало, а с сывороткой не всегда можно успеть, главное – профилактика!
Она не для всех инфекций разработана, но ее (профилактики) принципы вполне понятны: если существует токсин, то необходимо, чтобы в организме человека постоянно (!) циркулировал антитоксин, т. е. противоядие. Именно поэтому детям делают прививки (прежде всего против дифтерии и столбняка) – вводят очень ослабленные токсины, [11] а в результате организм ребенка формирует вполне приличный иммунитет, поскольку вырабатывается антитоксин.


Каждой человеческой клетке присуща своя генетическая информация. Это сложное, на первый взгляд, положение прямо-таки вызывает желание либо перестать читать, либо схватить школьный учебник по биологии, дабы срочно восполнить пробелы в образовании. Но тонкости нам не нужны. Принципиально другое: система иммунитета способна анализировать – отличать своих от чужих. А в основе этого анализа – именно генетическая информация. Что-то попало в организм: генетическая информация совпадает – значит, свой, не совпадает – чужой. Любое вещество, имеющее чужеродную генетическую информацию, называется антигеном.
Система иммунитета вначале обнаруживает антиген, а затем делает все, чтобы этот антиген уничтожить. Для уничтожения конкретного антигена организм вырабатывает особые клетки – они называются антитела. Определенное антитело подходит к определенному антигену как ключ к замку, разве что вероятность повторить или подобрать его в миллионы раз меньше.
Пример. В организм попал вирус кори. Иммунитет определил, что этот вирус генетически отличается от любой другой клетки человека. Следовательно, это антиген. Началась выработка антител, не просто каких-то там антител, а именно антител к вирусу кори. Антитела нейтрализовали вирус, и болезнь закончилась. А иммунитет к конкретной болезни, в нашем примере к кори, остался. Следует знать, что сроки болезни у каждого конкретного ребенка во многом будут определяться скоростью образования и количеством выработанных антител.
Иммунитет к определенным болезням может быть врожденным (часть уже готовых антител достается ребенку от матери) и, соответственно, приобретенным – т. е. таким, который организм выработал самостоятельно.
Приобретенный иммунитет может быть естественным, т. е. вырабатываться вследствие случайной встречи с определенным микроорганизмом, и искусственным, когда антиген вводится в организм сознательно (делается прививка).
Приобретенный иммунитет может быть длительным, почти пожизненным, а может быть кратковременным. От чего это зависит?
Прежде всего, от способности конкретного вируса к изменчивости. Так, вирус кори стабилен, поэтому заболевание приводит к тому, что формируется пожизненный иммунитет. А вирус гриппа все время меняется – т. е. переболели, выработали антитела, а через год прилетел другой вирус, с уже совершенно другой генетической информацией. И выработанные антитела к новому антигену не подходят. Заболели опять…
Применительно к бактериям иммунитет во многом зависит от количества токсинов у конкретного микроорганизма. Так, у коклюшной или дифтерийной палочек токсинов мало, а опасный – вообще один. Поэтому антитела к токсину, один раз образовавшись, способны длительное время поддерживать защиту организма. А у стафилококка токсинов десятки. И сформировать устойчивый и длительный иммунитет организму многократно сложнее.
И еще очень важная теоретическая информация.
Мы уже поняли, что иммунитет – явление специфическое (четкое соответствие конкретного антигена конкретному антителу). Но это не всегда так, поскольку система иммунитета имеет на своем вооружении не только антитела.
Т. е. помимо специфического иммунитета есть еще и иммунитет неспецифический, когда некие вырабатываемые организмом вещества способны воздействовать на самые разнообразные антигены.
Типичный пример: контакт клеток человеческого организма с микробами приводит к тому, что в организме начинает образовываться особый белок – интерферон. Интерферон реагирует на любые вирусы (и гриппа, и кори, и краснухи), тормозит размножение многих бактерий, т. е. его (интерферона) действие неспецифично.
Система неспецифического иммунитета это не только интерферон, это несколько десятков активных веществ, которые человеческий организм способен вырабатывать. Неспецифический иммунитет представлен еще и специальными клетками – нейтрофилами и фагоцитами. Они обезвреживают, поглощают и переваривают пришельцев (тех же бактерий) в то время, пока специфические антитела нейтрализуют токсины.
Да, системы специфического и неспецифического иммунитета обеспечивают постоянство внутренней среды организма и всех, кто внутрь проникает, по мере сил нейтрализуют-уничтожают.
Но для того чтобы с этими системами столкнуться, микроб должен туда, внутрь, в организм попасть.
А внутрь попасть – совсем не просто. Ибо помимо иммунитета общего, так сказать, внутреннего, есть еще и защита внешняя – местный иммунитет.
Читайте также:



