Ботулизм это газовая анаэробная инфекция
НАУЧНЫЕ ДОСТИЖЕНИЯ В ОБЛАСТИ ПРОИЗВОДСТВА АНАТОКСИНОВ
Проблема создания эффективных препаратов для профилактики газовой гангрены насчитывает десятки лет, но и в настоящее время считается актуальной [21, 22]. Проведены многочисленные исследования [3, 16, 23, 24] в целях создания профилактических анатоксинных препаратов против анаэробных инфекций и повышения качества. Однако исследования, посвященные разработке методов получения очищенных сорбированных гангренозных анатоксинов, не вышли за пределы лабораторных экспериментов. В связи с этим потребовалась разработка методов культивирования патогенных клостридий и получения токсинов-анатоксинов в реакторах большой емкости. В конце 1966 г. МЗ СССР было поручено приступить к разработке ассоциированного препарата - секстаанатоксина, предназначенного для профилактики столбняка, ботулизма и газовой гангрены. Разработка технологического процесса реакторного получения ботулинических анатоксинов типов А, В, Е проводилась на базе Уфимского НИИВС, гангренозных анатоксинов - в Московском и Пермском НИИВС. Для успешной реализации этой задачи проведены исследования в следующих направлениях: 1. совершенствование питательных сред для глубинного выращивания Clostridium perfringens типа А и C.oedematiens типа А; 2. определение оптимальных параметров процесса роста и токсинообразования C.perfringens типа А и С.оеdematiens типа А (рН, гН, Dim, L,, потребление углеводов и азотистых веществ, компонентного состава токсинов), обеспечивающих при глубинном выращивании клостридий получение высокоактивных токсинов; 3. отработка оптимальных условий детоксикации анатоксинов перфрингенс и эдематиенс при максимальном сохранении их антигенной активности; 4. исследование различных методов очистки и концентрации гангренозных анатоксинов. Предлагаемая технология реакторного метода приготовления казеиновых гидролизатоа с повышенным содержанием белковых и пептидных фракций разработана на основе найденных оптимальных условий гидролизата казеина (количество казеина, фермента, соляной кислоты, продолжительность процесса, величина рН и температуры). На усовершенствованных питательных средах получены высокоактивные гангренозные токсины. Средние титры токсинов C.perfringens на панкреатической и протеазной, а токсинов C.oedematiens - на пепсинной и кислотной казеиновых средах соответственно составляли 1040,6 и 720 Dlm/мл; 20800 и 10700 Dtm/мл [15, 18]. В результате изучения основных факторов, определяющих процесс токсинообразования при реакторном культивировании C.perfringens типа А штамма ВР6К-28 и C.oedematiens типа А штамма 79 (рН, гН, потребление углеводов и азотистых веществ), установлено, что лимитирование изменений каждого из них и подбор питательных сред с учетом параметров физикохимических сдвигов в среде обеспечивает получение высокоактивных гангренозных токсинов. Впервые установлены компоненты токсина перфрингенс в следующих количествах: лецитиназа - 660 - 2000 Lv/мл; тэта-гемолизин - 2290-12650 ГЕ/мл; коллагеназа - 69,96 - 77,47; гиалуронидаза - 2,0- 10,0; протеиназа - 0,028 - 0,729 ед/мл. Детоксикация нативного токсина перфрингенс оптимальна при дробном добавлении формалина, при котором происходит более интенсивное образование метиленовых связей формальдегида с токсином перфрингенс и снижение токсичности. Формалин добавляется в дозе 0,015% с различными временными интервалами. Общая доза колебалась в пределах 0,6 - 0,7% в зависимости от высоты титра токсина перфрингенс. Данный метод позволяет избежать чрезмерного денатурационного воздействия на токсин и повысить активность нативного анатоксина перфрингенс (а.п.) до 8-14 ЕС/мл против 5 - 7 ЕС/мл по общепринятой схеме [5]. Оптимальным вариантом оказался метод двухэтапной очистки (осаждение соляной кислоты при рН 3,3+0,1 в присутствии гексаметафосфата натрия и фильтрации через гель сефадекса Г-75), обеспечивающий получение а.п. с удельной активностью 300 - 500 ЕС на 1 мг белкового азота. Полученные очищенные гангренозные анатоксины в дозе 100 ЕС полностью сорбировались на геле гидрооксида алюминия (0,4-0,5 мг А^Од). Разработка промышленной технологии получения гангренозных анатоксинов в Московском и Пермском НИИВС завершилась составлением совместного регламента производства. Созданный в период 1966 - 1969 гг. совместно с коллективами Московского и Уфимского НИИВС новый ассоциированный препарат - секстаанатоксин был утвержден Комитетом вакцин и сывороток МЗ СССР и принят к массовому производству. Применение секстаанатоксина для активной иммунизации населения против анаэробных инфекций показало, что наиболее слабым антигеном в составе ассоциированного препарата является а.п. Об этом свидетельствует уровень антитоксина в сыворотке крови после иммунизации людей секстаанатоксином: столбнячный - 3,07; ботулинические типов А, В, Е соответственно - 0,56, 0,6, 0,7; перфрингенс - 0,18: эдематиенс - 0,78 МЕ/мл (средняя геометрическая титров). Одним из путей повышения иммунологической эффективности а.п. является получение препарата из очищенного токсина [10]. В результате проведенных исследований по сравнительной оценке различных методов очистки токсина перфрингенс впервые была предложена следующая технология: осаждение нативного токсина перфрингенс солями хлорида натрия и хлорида цинка, элюция полученного осадка р-ром двузамещенного фосфата натрия, концентрирование элюата ультрафильтрацией, очистка концентрата на углеродном сорбенте марки СКН и обезвреживание очищенного токсина формалином в присутствии L-лизина. Получены препараты с удельной активностью 400 - 450 ЕС на 1 мг белкового азота [8].
| Информация о документе | |
| Дата добавления: | |
| Размер: | |
| Доступные форматы для скачивания: |
Общая характеристика патогенных анаэробных бактерий
Возбудители газовой гангрены
Общая характеристика патогенных анаэробных бактерий
Патогенные анаэробы относятся к семейству Bacillaсеае, роду Clostridium. Анаэробы - обширная группа микроорганизмов, среди которых патогенны для человека: 1) клостридии столбняка; 2) клостридии газовой гангрены (полимикробная инфекция); 3) клостридии ботулизма.
Патогенные анаэробы являются постоянными обитателями кишечника животных и человека, с испражнениями которых выделяются во внешнюю среду. В виде спор они длительно сохраняются в почве, морской и пресной воде.
Патогенные клостридии - крупные палочки размером 4-9x0,6-1,2 мк. Молодые культуры грамположительны. Все клостридии образуют споры овальной или круглой формы, располагающиеся терминально, субтерминально или центрально. Большинство анаэробов подвижны. Жгутики располагаются перитрихиально. Клостридии продуцируют экзотоксины высокой биологической активности.
Устойчивость к факторам окружающей среды. Вегетативные формы анаэробов мало устойчивы. Споры очень устойчивы к физическим и химическим факторам: они переносят кипячение от 15-20 мин до нескольких часов в зависимости от вида бацилл. Устойчивы также к низким температурам и высушиванию. Обычные растворы дезинфицирующих веществ губят их только после длительной экспозиции (12-14 ч). Особенно устойчивы споры возбудителей ботулизма. Экзотоксин С. botulinum обладает высокой устойчивостью - разрушается только при 15-20-минутном кипячении.
Морфология. С. tetani - палочки размером 4-8x0,4-1 мкм с закругленными краями. Подвижны. Жгутики располагаются перитрихиально. Капсул не образуют. Образуют споры шаровидной формы, расположенные терминально, что придает бацилле вид барабанной палочки. Грамположительны.
Культивирование. Возбудитель столбняка - строгий анаэроб. Специальными средами для их выращивания служат: среда Вейнберга , среда Виллиса и Хоббса, среда Китта-Тароцци и др. Возбудители столбняка растут при температуре 35-37°С и рН среды 6,8-7,4. На плотных питательных средах рост появляется на 3-4-й день. Выросшие колонии сероватого цвета, иногда прозрачные с неровной зернистой поверхностью и вытянутыми краями. В высоком столбике агара С. tetani образуют колонии в виде пушинок, иногда колонии бывают темные и напоминают чечевичные зёрна. На кровяных средах вокруг колоний отмечается зона гемолиза. При посеве возбудителей столбняка на среду Кита-Тароцци среда мутнеет. Рост на среде Вильсона-Блера характеризуется почернением среды.
Ферментативные свойства. С. tetani обладают слабой ферментативной активность. Углеводы не расщепляют. Протеолитические свойства выражаются в восстановлении нитратов в нитриты, медленном свёртывании молока и медленном разжижении желатина. С. tetani образует фибрилизин.
Токсинообразование. С. tetani вырабатывают сильный экзотоксин, состоящий из двух компонентов: тетаноспазмина и тетанолизина. Тетаноспазмин (нейротоксин) поражает двигательные клетки нервной ткани, что приводит к спазматическому сокращению мышц. Тетанолизин гемолизирует эритроциты.
Устойчивость к факторам окружающей среды . Вегетативные формы С. tetani при температуре 60-70°С погибают через 20-30 минут. Споры обладают большой устойчивостью, они выдерживают кипячение в течении 1-1,5 часа. В почве и на других предметах споры длительно сохраняются. Прямой солнечный свет убивает их через несколько часов. Дезинфицирующие растворы губят их через 5-6 часов.
Источники инфекции. Возбудители столбняка широко распространены в природе. Многие животные являются носителями этих микроорганизмов, поэтому С. tetani обнаруживают в почве, куда они попадают из кишечника животных и человека. Заболевания столбняком чаще наблюдаются в сельской местности, особенно в районах с развитым животноводством. Споры могут разноситься с пылью, попадая на одежду и другие предметы.
Пути передачи и входные ворота. Входными воротами является поврежденная кожа и слизистые оболочки. Столбняк является раневой инфекцией, и заболеваемость связана с травматизмом (особенно в военное время). Опасны ранения с глубокой травматизацией тканей, в которые заносится земля, инородные тела и т.д. однако для возникновения заболевания иногда достаточно проникновения небольшой занозы.
Иммунитет . Постинфекционного иммунитета нет, так как исход этого заболевания часто смертельный.
Искусственный иммунитет достигается путём введения анатоксина. Иммунитет антитоксический.
Специфическая профилактика. Основана на иммунизации анатоксином, являющимся компонентом АКДС.
Специфическое лечение. Вводят в/м противостолбнячную сыворотку. Хороший результат даёт иммуноглобулин, полученный из крови доноров, иммунизированных против столбняка. Кроме этого вводят антибиотики тетрациклинового ряда и пенициллин.
Материал для исследования
Кусочки ткани с пораженного участка
Инородные тела, попавшие в рану
С профилактической целью исследуют на стерильность перевязочный материал, кетгут, шелк и препараты для подкожного введения
СТОЛБНЯК
Эпидемиология
Столбняк, хотя и ограниченный иммунизацией, распространен по всему миру. В США наиболее часто встречается среди неиммунизированных или не полностью иммунизированных пожилых лиц, а также после таких травм, как колотые раны, аборты или повреждения при контакте с землей.
Патогенез
При низком окислительновосстановительном потенциале в ране, загрязненной спорами Clostridium tetani, происходит прорастание спор, сопровождающееся образованием токсина. Токсин проникает в тело нервной клетки, мигрирует через синапс к пресинаптическому окончанию, блокируя высвобождение ингибирующих нейромедиаторов. Генерализованная мышечная ригидность возникает в результате повышения активности покоя амотонейронов при снижении действия ингибиторов.
Клинические проявления
Диагностика
Диагностика столбняка проводится клинически. Микробы часто не высеваются из ран больных столбняком и обнаруживаются в ранах больных, у которых столбняка нет.
Лечение
Цель лечения - устранение источника образования токсина, нейтрализация несвязанного токсина, предупреждение мышечных спазмов и обеспечение поддерживающей терапии (особенно в отношении дыхательной системы) до и после выздоровления. Больного помещают в тихую изолированную палату для проведения интенсивной терапии. Бензилпенициллин (10-12 млн. ЕД/сут внутривенно в течение 10 дней) вводят для устранения вегетативных форм. Вводят противостолбнячный иммуноглобулин G (TIG) в дозе 3000-6000 ЕД внутримышечно быстро для нейтрализации циркулирующего и несвязанного токсина. Лошадиный столбнячный антитоксин можно ввести в дозе 10 000 ЕД внутримышечно, но к нему часто отмечается гиперчувствительность, и период его полужизни короче, чем у TIG. Для лечения мышечного спазма применяют диазепам, при выраженном спазме показана нейромышечная блокада. При ларингоспазме может понадобиться ИВЛ для устранения гиперактивности симпатической НС. Оптимальная терапия при избыточной симпатической активности не разработана, применяют лабетолол, эсмолол, клонидин и морфина сульфат. Больным проводят активную иммунизацию против столбняка, поскольку естественное течение болезни не стимулирует иммунитет.
Профилактическая схема для взрослых - 3 дозы столбнячного анатоксина, первую и вторую вводят внутримышечно с промежутком в 48 нед, а третью через 6-12 мес после второй. Вспомогательная доза вводится каждые 10 лет. Профилактика при наличии ран: столбнячный анатоксин вводят при любой ране, если: 1) иммунный статус больного неизвестен, 2) в прошлом введено менее 3 доз или 3) прошло более 10 лет после введения 3 доз. При тяжелых и сильно загрязненных ранах иммунизацию проводят, если прошло более 5 лет после последнего эпизода вакцинации. При всех ранах необходимо вводить столбнячный иммуноглобулин 250 мг внутримышечно, если иммунный статус больного неясен или неполноценен; исключения составляют малые, чистые раны.
БОТУЛИЗМ
Эпидемиология
Ботулизм как заболевание человека распространен повсеместно. Пищевой ботулизм возникает при употреблении пищевых продуктов, зараженных образовавшимся в них токсином (чаще эти пищевые продукты имеют домашнее происхождение). Раны, служащие источником болезни, должны быть заражены С1. Botulinum: к ним относятся раны, загрязненные почвой, раны у людей, злоупотребляющих медикаментами, и раны после кесарева сечения. Ботулизм может возникнуть, если ребенок поглощает споры и токсин высвобождается у него в кишечнике. Заражение детей ботулизмом по взрослому типу отмечается в старшем возрасте.
Клинические проявления
Пищевой ботулизм. Инкубационный период составляет 18-36 ч после употребления зараженной токсином пищи. Начало болезни связано с появлением черепномозговой симптоматики, обычно это диплопия, дизартрия и (или) дисфагия. Паралич развивается симметрично, опускается вниз и ведет к дыхательной недостаточности и смерти. До паралича или после его начала могут возникать тошнота, рвота и боли в животе. Характерны головокружение, нарушения зрения, сухость слизистой оболочки полости рта, а также сухость и боли в горле. Лихорадка нетипична.
Часто имеется птоз; фиксированные и расширенные зрачки отмечены у 50% больных. Рвотный рефлекс может быть подавлен, глубокие сухожильные рефлексы нормальны или снижены. Паралитическая непроходимость кишечника, выраженный запор, задержка мочеиспускания - все это характерно.
Раневой ботулизм. Картина этого варианта болезни сходна с наблюдаемой при пищевом ботулизме, но инкубационный период длиннее (10 дней) и не характерны нарушения ЖКТ.
Диагноз
Диагноз ставят по выявлению токсина в сыворотке крови; в то же время в присутствии явной инфекции тест может быть отрицателен, а его выполнение требует особого лабораторного оборудования. Другие биологические среды, в которых может быть обнаружен токсин, - это рвотные массы, желудочный сок и кал. Попытка выделить возбудитель из пищи диагностически несостоятельна.
Лечение
Необходимо мониторирование функций больного, особенно дыхания. При пищевой форме после получения лабораторных проб необходимо сразу же ввести трехвалентный лошадиный антитоксин (тип А, В и Е). Дозировка: два флакона (оба внутривенно или один внутривенно, другой внутримышечно). Повторная доза может потребоваться спустя 24 ч. Могут быть эффективны слабительные. Ценность антибиотиков сомнительна. При раневом ботулизме: обработка раны, бензилпенициллин (для устранения инфекции) и лошадиный антитоксин. Поддерживающая терапия применяется при ботулизме у детей.
ДРУГИЕ КЛОСТРИДИАЛЬНЫЕ ИНФЕКЦИИ
Патогенез
Несмотря на частый высев клостридий из ран при серьезных травмах, частота тяжелых инфекций, обусловленных ими, невелика. В развитии тяжелой болезни определяющими являются два фактора: некроз тканей и низкий окислительновосстановительный потенциал. Клостридиальные инфекции опосредуются токсинами.
Клинические проявления
[i]Пищевые отравления.[/i] Cl perfringens - одна из наиболее частых причин пищевых отравлений в США. Источником служат мясо при повторном его приготовлении, мясо - и птицепродукты. Симптомы появляются через 8-24 ч после употребления пищи и включают боль в эпигастрии, тошноту и водную диарею длительностью 12-24 ч. Лихорадка и рвота нехарактерны.
[i]Колит, связанный с применением антибиотиков.[/i] Продуцирующие токсины штаммы Cl. difficile, обнаруживаемые в кале, - главная причина колита у больных диареей, обусловленной применением антибиотиков. Различные противомикробные средства (включая метронидазол и ванкомицин, используемые для лечения этой инфекции) могут вызвать этот синдром, определяемый как диарея, у которой нет иных причин и возникающей в процессе антибактериального лечения или в течение 4 нед после его прекращения. Стул обычно водянистый, значителен по объему, без больших примесей крови или слизи. У многих больных отмечаются спастические боли в животе, болезненность при пальпации, лихорадка и лейкоцитоз.
[i]Гнойная инфекция[/i] глубоких тканей. Клостридий часто обнаруживают в сочетании с другими микробами или изолированно, но обычно без общих признаков заболевания, вызываемого их токсинами. Сюда относятся: внутрибрюшной сепсис, эмпиема, абсцессы в полости малого таза, подкожные абсцессы, отморожения с газовой гангреной, инфекция культи после ампутации, абсцесс головного мозга, абсцесс предстательной железы, конъюнктивит, инфекция аортальных шунтов. Холецистит вызывается клостридиальной инфекцией, по крайней мере, в 50 % случаев.
[i]Инфекция кожи и мягких тканей. [/i]Локализованная. Проявления безболезненны, без признаков общей интоксикации и отека. Типичные поражения: целлюлит, периректальный абсцесс, диабетические язвы стоп. Газ может находиться в ране и в соседних тканях, но не в мышцах. Гнойный миозит встречается у наркоманов, применяющих героин.
[i]Распространяющийся целлюлит.[/i] Синдром имеет острое начало с быстрым распространением гнойного процесса и газа по фасциям. Некроз мышечной ткани отсутствует, но весьма выражена токсемия, которая может быть фатальной. При осмотре находят выраженную крепитацию, местная боль выражена незначительно. Этот синдром чаще всего встречается среди больных карциномой, особенно при локализации в ситовидной или толстой кишке.
[i]Клостридиальный мионекроз (газовая гангрена).[/i] Встречается при глубоких ранах с некрозом тканей, часто после травмы или операции. Инкубационный период всегда менее 3 сут, часто менее 24 ч. В отличие от распространяющегося целлюлита газовая гангрена начинается с внезапной боли в ране. Имеется локальный отек с незначительным геморрагическим экссудатом. Обязательны токсемия, снижение АД, почечная недостаточность и крепитация.
[i]Клостридиалъная септицемия.[/i] Клостридиальная септицемия встречается нечасто, но она почти всегда фатальна и развивается вслед за клостридиальным инфиЦированием матки (особенно после септического аборта), толстой кишки или желчевыводящих путей. У больных развивается картина сепсиса спустя 13 дня после аборта, с лихорадкой, ознобом, слабостью, головной болью, тяжелой миалгиеи, болями в животе, тошнотой, рвотой и (иногда) диареей. Быстро, вслед за гемолизом, развиваются олигурия, снижение АД, желтуха, гемоглобинурия. Как и при газовой гангрене, больные с клостридиальной септицемией проявляют повышенную настороженность к происходящему. У больных с локализацией инфекции в кишечнике или в желчных путях заболевание часто приобретает системный характер. СреДи проявлений болезни следует назвать лихорадку, озноб, у половины больных внутрисосудистый гемолиз. У онкологических больных Cl. septicum вызывает быструю фатальную септицемию с лихорадкой, тахикардией, снижением АД, болью в животе, тошнотой, рвотой. Только у 20-30 % этих больных развивается гемолиз; смерть наступает в течение 12ч.
Диагностика клостридиальной инфекции должна основываться прежде всего на клинической картине. Наличие газа на рентгенограмме дает врачу ключ к диагнозу, но это же встречается и при смешанной аэробноанаэробной инфекции. Диагноз клостридиального мионекроза можно поставить при исследовании препарата замороженного фрагмента мышцы. Колит, обусловленный Cl. difficile, может быть установлен при уточнении вида токсина в кале путем культуральных исследований на фоне адекватной нейтрализации антитоксином.
Лечение
Бензилпенициллин (20 млн. ЕД/сут) - антибиотик выбора при клостридиальной инфекции тканей. При аллергии к пенициллину могут быть назначены и другие антибиотики, но должна быть оценена чувствительность возбудителя к препаратам. При клостридиальном мионекрозе главным в лечении является дренирование и оперативное вмешательство на инфицированном участке. При быстром распространении инфекции по конечности молсет потребоваться ее ампутация; при мионекрозе мышц передней брюшной стенки иногда необходима повторная хирургическая обработка, а при мионекрозе матки выполняют гистерэктомию. При энтероколите, связанном с Cl. difficile, в качестве лечебной меры отменяют антибиотик, спровоцировавший осложнение. Назначают метронидазол (250 мг 4 раза или 500 мг 3 раза в сутки внутрь) или ванкомицин (125 мг 4 раза в день внутрь) на протяжении 7-10 дней, что смягчает и укорачивает проявление симптомов заболевания. Доза ванкомицина может быть увеличена до 500 мг 4 раза в сутки внутрь при тяжелом течении. В рефракторных случаях или при рецидиве в лечение вносят стратегические изменения: добавляют рифампицин к ванкомицину, уменьшают дозу ванкомицина, переходят от метронидазола или ванкомицина к альтернативным лекарственным средствам.
СМЕШАННЫЕ АНАЭРОБНЫЕ ИНФЕКЦИИ
Клинические проявления
[i]Голова и шея.[/i] Инфекции головы и шеи, вызываемые анаэробами, включают гингивит, воспаление в глотке (включая ангину Людвига), инфекции фасциальных пространств, когда ротоглоточная микрофлора со слизистых оболочек или области стоматологического вмешательства распространяется в область головы и шеи, вызывая, в частности, отит и синусит. Осложнения этих инфекций: остеомиелит костей черепа или челюсти, внутричерепные инфекции (абсцесс головного мозга), медиастинит или плевропульмональная инфекция.
[i]Центральная нервная система.[/i] При применении оптимальных бактериологических методов анаэробы обнаруживают в 85 % случаев абсцессов головного мозга. Доминируют грамположительные анаэробные кокки; фузобактерии и Bacteroides встречаются реже.
[i]Легкие и плевральная полость.[/i] Четыре клинических синдрома связаны с анаэробной плевролегочной инфекцией, возникающей при аспирации: аспирационная пневмония, некротизирующая пневмония, абсцесс легкого и эмпиема. Аспирационная пневмония развивается довольно медленно, с невысокой лихорадкой, слабостью, продуктивным кашлем у больных с предрасположенностью к аспирации. У больных с абсцессом легкого отмечается типичная картина лихорадки, озноб, слабость, похудание, выделение зловонной мокроты, что происходит на протяжении недель. Эмпиема плевры - проявление длительно существующей анаэробной легочной инфекции, клинически напоминает картину абсцесса легкого. Может отмечаться плевритная боль в груди и боль при пальпации участка грудной клетки. Поддиафрагмальный процесс может осложниться эмпиемой плевры.
ВНУТРИБРЮШНЫЕ ПРОЦЕССЫ
[i]Малый таз.[/i] Часто анаэробная инфекция может вызвать тубоовариальный абсцесс, септический аборт, абсцессы в малом тазу, эндометрит, инфекцию послеоперационной раны, особенно после гистерэктомии.
[i]Кожа и мягкие ткани.[/i] Иногда удается выделить анаэробы при крепитирующем целлюлите, синергическом целлюлите, гангрене, некротизирующем фасциите, кожных абсцессах, прямокишечном абсцессе, инфекции подмышечных потовых желез. Синергическая гангрена Мелени (Meleney) - прогрессирующее, очень болезненное заболевание с эритемой, отеком, индурацией, некрозом в центральной зоне. Обычно его вызывают анаэробные кокки и Staph. aureus. Хотя некротизирующий фасциит обычно вызывается стрептококками группы А, он может быть вызван и анаэробами, включая Peptostreptococcus и Bacteroides.
[i]Кости и суставы.[/i] Анаэробный остеомиелит обычно развивается как продолжение инфекции мягких тканей; септический артрит часто имеет гематогенное происхождение.
[i]Бактериемия.[/i] B.fragilis - единственный анаэроб, часто высеваемый из крови. В то время, как клинические проявления анаэробной бактериемии сходны с сепсисом, вызванным грамотрицательными аэробными бактериями, для первой не характерны септический тромбофлебит и септический шок.
Диагностика
Когда инфекция развивается вблизи поверхности слизистых оболочек, обычно заселенных анаэробами, их и следует рассматривать в качестве этиологических факторов. Культуры необходимо специально исследовать на наличие анаэробов, шскольку их лабораторное выделение требует времени, диагностика в ряде случаев может быть предположительной.
Еще в 1861 г. Л. Пастер показал, что процесс маслянокислого брожения вызывается бактериями, которым свойствен один совер- шенно необычный признак - рост при полном отсутствии кислорода.
Это явление Пастер назвал анаэробиозом, что означает жизнь при отсутствии воздуха. Годы Первой мировой войны стали годами интенсивного изучения анаэробных инфекций. В результате были изучены основные возбудители газовой гангрены, унифицирована и упрощена методика работы с ними.
Спорообразующие анаэробы рода Clostridium принадлежат к семейству Bacillaceae и насчитывают свыше 150 видов. Эти бактерии при наличии благоприятных условий способны вызывать у человека газовую гангрену, столбняк, ботулизм, псевдомембранозный язвенный энтероколит, пищевые отравления и другие заболевания,
связанные с клостридиальным поражением различных органов и систем.
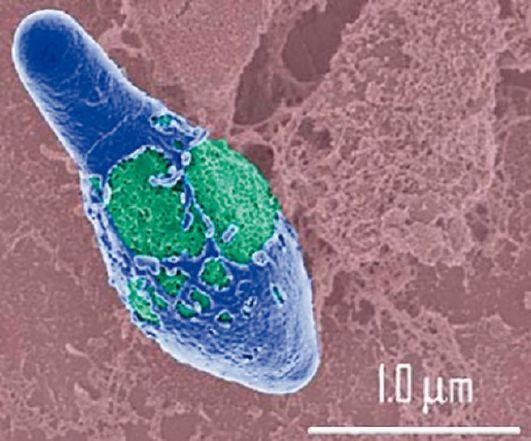
Рис. 16.4. Clostridium botulinum
споры округлой или овальной формы, располагаются в центре клетки субтерминально или терминально в зависимости от видовой принадлежности микроба (рис. 16.4). Поперечник споры обычно больше поперечника клетки, поэтому клетка, содержащая спору, выглядит раздутой и напоминает веретено (от лат. clostridium - веретено). Форма бактерий может сильно изменяться под влиянием различных факторов вплоть до появления клостридий в форме кокков, нитевидных бактерий и т.д. Все они, кроме C. perfringens, подвижны, перитрихи, имеют 15-20 жгутиков. C. perfringens в организме человека или животных может образовывать капсулы.
Патогенные клостридии - грамположительные палочки. Большинство патогенных клостридий способны продуцировать истинные экзотоксины очень большой силы. Например, ботулотоксин не имеет себе равных по силе среди природных биологических ядов.
Биохимические свойства патогенных клостридий различны. Некоторые виды отличаются очень высокой сахаролитической активностью, другие обладают большой протеолитической активностью. Есть патогенные клостридии, которые в биохимическом отношении малоактивны.
16.5.2.1. Возбудители газовой гангрены
Возбудителей газовой гангрены по степени патогенности принято делить на три группы. Первая группа включает наиболее патогенные виды, каждый из которых может вызывать газовую гангрену (C. perfringens, С. novyi и С. septicum). Во вторую группу входят клостридии, обладающие менее патогенными свойствами (С. histolyticum, С. bifermentans, С. sporogenes, C. fallax). Каждый из них также способен самостоятельно вызывать газовую гангрену, но чаще при этом заболевании они встречаются в ассоциации с другими анаэробами. Третья группа представлена маловирулент-
ными клостридиями, не способными вызывать развитие газовой гангрены, однако, присоединяясь к возбудителям первой или вто- рой группы, они существенно ухудшают течение болезни. К ним относятся C. tertium, С. butiricum, C. sordellii и некоторые другие. Газовая гангрена - полимикробное заболевание, в патогенезе которого важную роль играет и сопутствующая микрофлора (стафилококки, стрептококки, энтеробактерии и другие возбудители). Обнаружение патогенных клостридий в раневом отделяемом далеко не всегда свидетельствует о развитии соответствующего заболевания, поэтому правильный этиологический диагноз должен быть основан на совокупности клинических и микробиологических данных.
Клостридии обитают в почве и попадают в рану из внешней среды с инородными телами - пулями, осколками, обрывками одежды, занозами и т.д. Для заболевания характерны быстрое распространение болезненного отека мягких тканей с их разрушением, а также общая интоксикация пораженного организма. Очень часто в погибшей ткани накапливаются газообразные продукты, раневое отделяемое имеет зловонный запах.
Чаще всего газовая гангрена развивается после обширных и глубоких проникающих ранений мягких тканей. В мирное время это следствие автомобильной или железнодорожной катастрофы, травм на производстве, в сельском хозяйстве или в быту, внебольничных абортов, ожогов, обморожений, хирургических операций на желудочно-кишечном тракте, ампутаций, инъекций различных лекарственных препаратов и т.д.
C. perfringens - длинная грамположительная палочка (рис. 16.5). Имеет серовары A, B, C, D и F. В жидких питательных средах, приготовленных из гидролизатов мяса или казеина (рН 7,4), при 37-43 ?С растет быстро (3-8 ч) с бурным газообразованием и изменением рН в кислую сторону. Смесь газов (водород, углекислый газ, аммиак, сероводород, летучие амины, альдегиды, кетоны), выделяющихся из больших объемов растущей культуры, в присутствии огня может дать взрыв. Существует три устойчивых варианта колоний C. perfringens: гладкий (S), слизистый (М) и шероховатый (R), однако при определенных условиях могут появляться колонии смешанного (О) варианта. Колонии, выросшие на поверхности кровяного агара, часто окружены одной или двумя зонами гемолиза и при выдерживании на воздухе приобретают зеленоватую окра-
Рис. 16.5. Clostridium perfringens
ску. Вокруг колоний, вырабатывающих α-токсин (лецитиназу), в желточном агаре образуется зона перламутрового преципитата.
Большинство штаммов обладает протеолитическими свойствами, медленно расплавляя свернутую сыворотку (вареные кусочки мяса) на 2-7-й день. Многие штаммы вырабатывают ферменты, расплавляющие через 24 ч 7% желатин. Характерной для C. perfringens является способность свертывать лакмусовое молоко с образованием сгустка кирпичного цвета и полным просветлением молочной сыворотки. Все штаммы сбраживают с образованием кислоты и газа глюкозу, галактозу, мальтозу, лактозу, левулезу, сахарозу и не ферментируют маннит и дульцит. Некоторые штаммы разлагают глицерин и инулин.
С. septicum - полиморфная грамположительная палочка с суб- терминальными спорами. В зависимости от состава среды она может превращаться в короткие вздутые формы и длинные нити. Последние часто обнаруживаются в трупах животных на поверхности печени, прилегающей к диафрагме. Строгий анаэроб. На поверхности плотных питательных сред только через 48 ч образует блестящие полупрозрачные колонии диаметром до 4 мм с неровными бахромчатыми краями, имеет тенденцию к ползучему росту. Чаще образует R-форму колоний. В глубине 1% агара образует колонии диаметром 1-2 мм с уплотненным центром и радиально отходящими перепутанными нитями. В 2% агаре колонии имеют вид чечевиц, сердца и т.п., иногда с протуберанцами. На кровяном агаре узкая зона гемолиза появляется вокруг колонии только на 2-е сутки. Ферментирует с образованием кислоты глюкозу, мальтозу,
лактозу, галактозу, фруктозу, салицин и не разлагает глицерин и маннит, разжижает желатин и свертывает лакмусовое молоко с образованием кислоты и газа. Очень редко разлагает сахарозу. Не образует индол, не восстанавливает нитраты в нитриты и не вырабатывает большого количества сероводорода.
C. fallax - грамположительная прямая, иногда инкапсулированная палочка с закругленными концами, редко образующая овальные центральные или субтерминальные споры. Перитрих, подвижна в молодых культурах. Строгий анаэроб. На поверхности агара через 1-2 сут образует плоские прозрачные колонии с не- ровным краем диаметром 1-2 мм, которые затем становятся матовыми, с возвышением в центре. На агаре с кровью лошади вокруг колоний имеется узкая зона гемолиза. В глубине агара колонии напоминают мелкие чечевицы, иногда с выростами на краю. Ферментирует глюкозу, мальтозу, лактозу, сахарозу, маннит, салицин, не разлагает крахмал и глицерин, не сбраживает молоко с образованием кислоты. Не образует сероводород, индол, не восстанавливает нитраты в нитриты. Выделяется из ран в 1-4% случаев.
C. sordellii - грамположительная палочка, образующая овальные, центральные и субтерминальные споры на обычных средах. Перитрих, подвижна в свежих культурах. Анаэроб нестрогий. На поверхности питательных сред через 1-2 сут образует слабовыпуклые серовато-белые колонии с неровным краем. На кровяном агаре (эритроциты лошади) колонии окружены узкой зоной гемолиза. В глубине агара колонии имеют форму чечевиц или сердца с выростами по краю.
Ферментирует мальтозу, глюкозу и фруктозу, не разлагает лактозу и сахарозу. Разжижает желатин и свернутую сыворотку, вы- рабатывает сероводород и индол.
Деление патогенных клостридий на варианты связано с их способностью вырабатывать различные по антигенным свойствам ле- тальные и некротические токсины. Например, C. perfringens вырабатывает более десятка различных токсинов и ферментов (α, β, γ, δ, ε, ζ, η, θ, ι, κ, λ, μ).
В развитии типичной картины газовой гангрены наибольшую роль играет лецитиназа (α-токсин), которая обладает летальны- ми, гемолитическими и дермонекротическими свойствами. Этот токсин вызывает не только местные изменения в мышечной ткани - коагуляционный и колликвационный некроз здоровой ткани
(рис. 16.6), но и тяжелую интоксикацию организма больного с выраженным нарушением кровообращения, гемолитической анемией, угнетением эритро- и лейкопоэза, поражением паренхиматозных органов и костного мозга. Некоторую роль в этом разрушительном процессе могут играть другие ферменты (коллагеназа - летальный и некротический фактор, гемолизин, гиалуронидаза, ДНКаза и др.).

Рис. 16.6. Некроз при газовой гангрене
Главные летальные и некротические факторы и токсины типов В, С, D, E и F изучались главным образом в связи с энте- ротоксемиями у человека и животных, а их роль в патогенезе газовой гангрены почти не исследовалась. Типы А и В образуют термолабильный летальный и некротический α-токсин. β-токсин в больших количествах выделяют типы D, в меньших - В (это некротический, гемолитический - лецитиназа С).
Помимо указанных токсинов и ферментов, описаны γ-гемолизин, который вырабатывает только штаммы типа А, δ-токсин, представляющий собой легкоокисляемый кислородом гемолизин, который обнаруживают у некоторых штаммов типа А, и некоторые других.
Особенностью является то, что тип С не вырабатывает ни один из вышеуказанных ферментов. Фильтраты токсигенных штаммов С. septicum содержат по крайней мере несколько активных субстанций, природа и химическая структура которых еще далеко не изучены.
Основной летальный, некротический и гемолитический фактор С. septicum - это кислородостабильный α-токсин. При внутривенном введении его мышам он вызывает быструю гибель животных с явлениями судорог и параличей. Этот фермент не относится к лецитиназам. Кроме α-токсина, штаммы С. septicum вырабатывают β-токсин (ДНКаза), γ-токсин (гиалуронидаза), кислородостабильный δ-гемолизин, имеющий общие антигены с θ-гемолизином C. perfringens.
Все 6 типов C. perfringens способны вызывать газовую гангрену у человека и животных в том случае, если возбудитель вырабатывает
лецитиназу. В экспериментальных условиях весьма чувствительны к заражению голуби, воробьи, тогда как другие животные (кролики, свинки, мыши и т.д.) более устойчивы к заражению. Типичную картину изменения тканей, вызываемыхC. perfringens, можно получить при внутримышечной инъекции морской свинке 0,5 мл свежей культуры гладкой формы этого микроба. Смерть животного наступает в сроки от нескольких часов до нескольких суток.
C. fallax обнаружены при аппендиците, ранениях, хроническом артрите у людей и при гангрене скота. Свежие культуры, изолированные из ран, в первых генерациях бывают патогенными для мышей и морских свинок, однако вирулентность штаммов быстро теряется.
C. sordellii в эксперименте на животных способен вызвать за- болевание, похожее на газовую гангрену, с подкожным желатинозным отеком, иногда розово-красного цвета. Смерть животных происходит обычно за счет действия летального токсина в течение 1-2 дней после введения культуры. Описаны случаи смертельных кишечных заболеваний у человека и рогатого скота.
Среди других клостридий, относительно часто изолируемых из ран, следует упомянуть C. tertium, C. butyricum, которые непатогенны для лабораторных животных, но могут оказывать некоторое влияние на течение газовой гангрены, находясь в ассоциациях с патогенными клостридиями.
Лечение заключается в обработке ран, раннем введении с профилактической целью поливалентной антитоксической очищенной концентрированной сыворотки по 10 тыс. МЕ. С лечебной целью эту дозу увеличивают в 5 раз (по 50 тыс. МЕ каждой сыворотки) и применяют антибиотики. Лечение только одной сывороткой в ряде случаев не дает нужного эффекта, в то время как комплексное применение антитоксической сыворотки антибиотиков сопровождается значительным снижением летальности.
Читайте также:


