Вируса клещевого энцефалита относится к семейству
Клещевой энцефалит (КЭ) - вирусная природно-очаговая инфекция, передающаяся клещами, протекающая слихорадкой, интоксикацией, поражением нервной системы, принимающая иногда хроническое течение.
Этиология -Клещевой энцефалит. Возбудителем Клещевого энцефалита является представителем экологической группы арбовирусов и относится к роду флавивирусов семейства тогавирусов. Это РНК-содержащий вирус, способный выживать в организме клещей при низких температурах. Он нестоек к высоким температурам (при кипячении погибает через 2-3 мин) и к дезинфицирующим средствам.
Эпидемиология -Клещевой энцефалит. Клещевой энцефалит-трансмиссивная инфекция с природной очаговостью. Основным резервуаром и источником вируса в природе являются иксодовые клещи: Ixodes persulcatus, распространенные в восточных регионах страны, и Ixodes ricinus - в западных. Клещи проходят несколько стадий развития - яйцо, личинка, нимфа, имаго (взрослый клещ). Для того, чтобы происходило превращение клеща из одной стадии в другую, необходима кровь теплокровных животных. Начиная со стадии личинки, клещи активно ищут себе прокормителя, как правило, это мелкие лесные животные (зайцы, мыши и др.), птицы.
Однако клещи могут нападать и на крупных животных, в том числе домашний скот (козы, овцы, коровы). Во время кровососания клещ инокулирует вирус животным, вследствие чего развивается вирусемия и они становятся дополнительными резервуарами инфекции. Таким образом, происходит циркуляция вируса: клещ - животное - клещ. Клещи могут передавать вирус потомству. Заражение человека происходит трансмиссивным путем через укусы клеща. Возможна алиментарная передача инфекции при употреблении в пищу сырого молока коз и коров.
Заболеваемость Клещевой энцефалит имеет сезонный характер, соответствующий активности клещей. Максимальный ее подъем наблюдается в мае- июне. Второй, менее выраженный подъем заболеваемости, регистрируется в конце лета - начале осени.
Патогенез -Клещевой энцефалит. Возбудитель при укусе клеща внедряется в организм человека через кожу, репродуцируется в месте внедрения и проникает в кровь. Гематогенно и лимфогенно он попадает в различные внутренние органы, в том числе и в центральную нервную систему, вызывая поражение двигательных нейронов спинного и ствола головного мозга или развитие диффузного менингоэнцефалита.
При алиментарном заражении патологический процесс носит двухфазный характер. Первая фаза характеризуется начальной вирусемией и последующей репликацией вируса в клетках печени, селезенки и других органов. Вторая фаза включает вторичную вирусемию и поражение ЦНС. В клинике этому соответствует течение двухволнового менингоэнцефалита.
В процессе болезни формируется иммунитет, и вирус удаляется из организма человека. У некоторых людей вирус сохраняется в нервной системе в течение всей жизни, обусловливая хронические формы болезни.
Клиника -Клещевой энцефалит. Инкубационный период имеет продолжительность от 1 до 30 дней (чаще 7-14 дней). В подавляющем большинстве случаев у лиц, подвергшихся укусам вирусофорных клещей, развивается инаппарантная форма КЭ и лишь у 2% - клинически выраженная. Клещевой энцефалит начинается внезапно с лихорадки, интоксикации. Температура тел а быстро повышается до 38-39 "С. Больных беспокоят сильная головная боль, слабость, тошнота, иногда рвота, нарушается сон.
Характерен внешний вид больного - кожа лица, шеи, верхней половины грудной клетки, конъюнктивы гиперемированы, склеры инъецированы. Заболевание может завершиться в 3-5 дней. Такая форма болезни называется лихорадочной, является одной из самых частых, но редко диагностируется. Поражение нервной системы при этой форме отсутствует. При прогрессировании болезни с 3-5-го дня развиваются признаки поражения нервной системы. В зависимости от локализации поражения различают следующие формы клещевого энцефалита: менингеальную, менингоэнцефалитическую, полиомиелитическую, пол и радикулоневритическую.
Менинзеальная форма Клещевого энцефалита характеризуется общемозговым синдромом, появлением ригидности мышц затылка, симптомов Кернига, Брудзинского. Изменения цереброспинальной жидкости свидетельствуют о серозном менингите. Заболевание имеет благоприятное течение. Лихорадка длится 10-14 дней, санация ликвора несколько отстает от клинического выздоровления.
Менинзоэнцефалитическая форма протекает значительно тяжелее. Больные становятся вялыми, заторможенными, сонливыми. Усиливаются головная боль, тошнота, рвота. Нередко наблюдаются бред, галлюцинации, психомоторное возбуждение, нарушение сознания. У некоторых больных могут быть судороги, эпилептиформные припадки. Поражаются нервы, иннервирующие лицевую, глазодвигательную мускулатуру, и другие черепные нервы. Могут развиваться нарушения глотания, дыхания. Типичной для клещевого энцефалита является полиомиелитическая форма, проявляющаяся парезами и параличами верхних конечностей и шейно-плечевой мускулатуры. В конце 2-3-й недели возникает атрофия пораженных мышц. Парезы и параличи нижних конечностей встречаются редко.
Полирадикулоневритическая форма протекает с поражением периферических нервов и корешков, с болями по ходу нервных стволов, нарушением чувствительности.
Двухволновый менинзоэнцефалит (двухволновая молочная лихорадка). Первая лихорадочная волна продолжается 3-7 дней, затем период благополучия 7-14 дней и новое повышение температуры тела, сопровождающееся нарастающей интоксикацией, менингеальными и общемозговыми симптомами.
Прозредиентные формы возникают в случаях, когда вирус сохраняется в центральной нервной системе. Инфекционный процесс не завершается и переходит в хроническое течение сразу после острого периода болезни или после длительного латентного периода. Клинически такая форма проявляется чаще эпилептиформными припадками, гипер кинетическими судорогами.
Диагностика -Клещевой энцефалит. Диагноз основывается на эпидемиологических и клинических признаках и подтверждается результатами серологического исследования. РСК, РПГА, РН проводят с парными сыворотками, диагностическим является нарастание титра антител в 4 раза и более. Антитела к вирусу КЭ появляются поздно, поэтому для повторного исследования кровь берут через 3-4 нед, а иногда через 2-3 мес от начала болезни.
Используют ИФА, который позволяет обнаружить антитела к вирусу Клещевого энцефалита в более ранние сроки.
Лечение -Клещевой энцефалит. Больные клещевым энцефалитом с признаками поражения центральной нервной системы нуждаются в тщательном уходе и наблюдении. Проводят профилактику пролежней, следят за мочеиспусканием и дефекацией. Выявляют начальные симптомы расстройства дыхания. В течение первых Здней лечения ежедневно вводят по 6-9 мл донорского иммуноглобулина против клещевого энцефалита.
Используют противовирусные средства - препараты интерферона, рибонуклеазу и другие. Назначают дезинтоксикационную и дегидратационную терапию. При возбуждении, эпилептических припадках используют аминазин, димедрол, фенобарбитал. бензонал. При полиомиелитической форме рано начинают восстановительную терапию. Выздоровление происходит медленно. Все переболевшие клещевым энцефалитом с поражением нервной системы состоят на диспансерном учете у невропатолога.
Профилактика -Клещевой энцефалит. Необходимо соблюдать индивидуальные меры защиты от клещей во время пребывания в лесу, на садовых участках, расположенных вблизи лесных массивов. После их посещения следует проводить само- и взаимоосмотры. Козье и коровье молоко в очагах клещевого энцефалита должно кипятиться. Обнаруженный клещ должен быть немедленно удален в асептических условиях, возможно исследование клеща на наличие в нем антигена вируса Клещевого энцефалита.
Экстренная профилактика проводится иммуноглобулином против клещевого энцефалита. При титре антител в препарате 1:80 и выше иммуноглобулин вводят внутримышечно однократно детям до 12 лет - 1 мл, от 12 до 16 лет- 2 мл и от 16 лет и старше - 3 мл. Лица, отправляющиеся на работу в природные очаги клещевого энцефалита, подвергаются вакцинации.
Антитела класса IgM к вирусу клещевого энцефалита – это специфические противовирусные белки-иммуноглобулины, вырабатываемые иммунной системой в ответ на инфицирование вирусом клещевого энцефалита и свидетельствующие о текущей инфекции.
Результат исследования – полуколичественный.
Антитела класса IgM к вирусу клещевого энцефалита (Encephalitis virus), иммуноглобулины класса M к вирусу клещевого энцефалита.
Синонимы английские
Anti-arboviral Encephalitis IgM, Encephalitis Virus Antibodies, IgM, Tick-borne encephalitis virus IgM (TBE virus IgM).
Иммуноферментный анализ (ИФА).
Ед/мл (единица на милилитр)
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Клещевой энцефалит – это сезонное (весенне-летнее) вирусное заболевание, передающееся в основном с укусом клещей; поражает преимущественно центральную нервную систему.
Возбудитель клещевого энцефалита относится к арбовирусам, семейству флавивирусов, и подразделяется на три подвида: дальневосточный, центральноевропейский и сибирский. Основной переносчик энцефалита – иксодовые клещи. Кроме того, он передается через птиц, грызунов и хищников. Инкубационный период в среднем составляет 3-7 суток. Клинические проявления болезни разнообразны. Выделяют лихорадочную, менингеальную, менингоэнцефалитическую, полиомиелитическую и полирадикулоневритическую формы заболевания. Возможно длительное вирусоносительство в виде латентной, персистентной или хронической инфекции.
В ответ на инфицирование вирусом клещевого энцефалита или на вакцинацию против этого вируса иммунной системой вырабатываются специфические противовирусные антитела – белки-иммуноглобулины. Уже при первых симптомах заболевания в крови появляются иммуноглобулины класса M. Их уровень достигает максимума через 3,5-4,5 недели с момента инфицирования и затем постепенно в течение нескольких месяцев снижается.
Для чего используется исследование?
- Для подтверждения диагноза "клещевой энцефалит" (как текущего, так и недавно перенесенного заболевания).
- Как часть дифференциальной диагностики при поражении центральной нервной системы (инфекционных менингитах и энцефалитах другого происхождения, эпилепсии, асептическом менингите, тромбозе артерий или вен головного мозга, инсульте, внутричерепном кровоизлиянии, фебрильных судорогах, ВИЧ-инфекции, цистицеркозе, саркоидозе, сифилисе, карциноматозе мозговых оболочек, паранеопластическом энцефаломиелите и др.).
Когда назначается исследование?
При подозрении на текущий или перенесенный клещевой энцефалит.
Что означают результаты?
Концентрация: 0 - 100 Ед/мл.
Причины положительного результата
- Ранние стадии клещевого энцефалита (при этом IgG к вирусу клещевого энцефалита не выявляются). В таком случае рекомендуется повторить исследование через 7-10 дней.
- Текущий или недавно перенесенный клещевой энцефалит (в сочетании с положительным тестом на IgG к вирусу клещевого энцефалита) при условии, что не проводилась вакцинация против клещевого энцефалита.
- Недавно проведенная вакцинация против клещевого энцефалита.
Причины отрицательного результата
- Отсутствие недавнего инфицирования и, соответственно, иммунного ответа на вирус клещевого энцефалита (если IgG тоже не выявляются).
- Наличие активного иммунитета вследствие недавно перенесенной инфекции или успешной вакцинации (если тест на IgG к вирусу клещевого энцефалита положительный).
- Слабый иммунный ответ (или его отсутствие) на клещевой энцефалит из-за нарушений иммунной системы (если IgG к вирусу клещевого энцефалита не выявляются).
Что может влиять на результат?
Наличие перекрестно-реагирующих антител к другим возбудителям рода флавивирусов (вируса лихорадки Западного Нила, вируса японского энцефалита и др.).
- Профилактикаклещевого энцефалита осуществляется двумя способами. Во-первых, это вакцинация, которая проводится при риске заражения клещевым энцефалитом, а во-вторых, ревакцинация по эпидемическим показаниям перед сезоном клещевого энцефалита.
- Тем, кто лечился гамма-глобулином в первые дни болезни, через 2-3 месяца необходимо дополнительное серологическое исследование в связи с тем, что такая терапия временно угнетает формирование иммунитета.
Кто назначает исследование?
Инфекционист, невролог, терапевт, врач общей практики.
Среди переносчиков инфекционных заболеваний человека клещи занимают второе место после комаров: на сегодня выявлено не менее трех вирусных, 22 бактериальные и несколько протозойных инфекций, которые переносятся иксодовыми клещами. Ситуация зачастую осложняется тем, что при укусах клещи способны передавать человеку одновременно разные виды бактерий, вирусов и простейших, вызывая смешанные инфекции, часто протекающие в более тяжелых формах. Дополнительный риск заражения возникает из-за возможной циркуляции патогенов в сельскохозяйственных и домашних животных (например, инфекционные агенты могут сохраняться в молочных продуктах), а также при переливаниях крови и трансплантации органов. Наиболее опасными среди инфекций, переносимых клещами, считаются клещевой энцефалит, иксодовый клещевой боррелиоз, эрлихиоз, риккетсиоз и бабезиоз. Для России наиболее социально значимыми инфекционными агентами являются боррелии и конечно же вирус клещевого энцефалита, о котором пойдет речь ниже.
Таежная инфекция
В 30-х гг. XX в. шло интенсивное освоение Дальнего Востока: строились дороги, вырубались леса, из-за напряженных отношений с Японией в тайге дислоцировались крупные военные части. Врачи, работавшие в то время в Приморском крае, стали регулярно сообщать о неизвестной тяжелой болезни, поражающей как местных жителей, так и военных. Заболевание, считавшееся новой разновидностью тяжелого гриппа, сопровождалось резким повышением температуры и часто приводило к параличам и даже гибели заболевших.
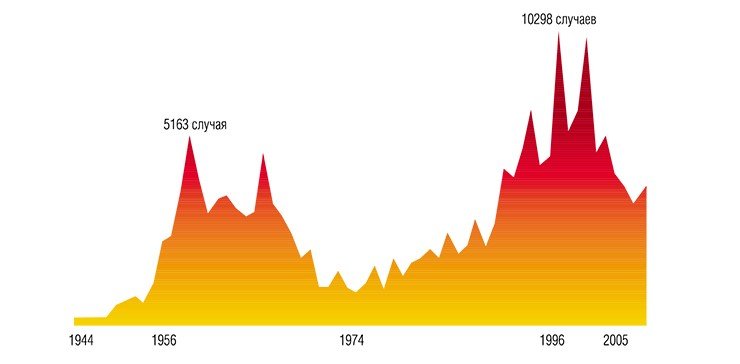
Правильно диагностировать неизвестную болезнь удалось лишь в 1935 г. местному врачу А. Г. Панову. Заболевание оказалось воспалением мозга, т. е. энцефалитом, похожим по симптомам на описанный ранее японский энцефалит. В 1936 г. врачи дальневосточной пастеровской станции пытались выделить возбудителя заболевания, вводя мышам в мозг эмульсию мозга людей, погибших от энцефалита. Но, несмотря на то, что у мышей появлялись признаки заболевания, исследования не увенчались успехом.
В январе 1937 г. военные медики обратились в Наркомздрав СССР, где и было принято решение об организации на Дальний Восток научной экспедиции под руководством Л. А. Зильбера. В тяжелых полевых условиях была развернута настоящая вирусологическая лаборатория. Ученые свою задачу выполнили: патоген, вызывающий тяжелые заболевания центральной нервной системы, был успешно выделен и описан. Кроме того, была четко установлена определяющая роль иксодовых клещей в передаче инфекционного агента. Выяснилось, что источником заражения клещей служили дикие позвоночные животные, на основе чего были разработаны рекомендации по необходимым профилактическим мерам.
К сожалению, это поистине блестящее открытие, ставшее важной вехой в истории вирусологии, не обошлось без жертв среди самих участников научной экспедиции. Так, М. П. Чумаков – будущий академик и создатель Института по изучению полиомиелита – перенес тяжелейшую форму инфекции, перешедшую у него в хроническую пожизненную форму; последствием заболевания у В. Д. Соловьева стала шестимесячная слепота.
Опасный сосед
Что на сегодня известно о вирусе клещевого энцефалита (ВКЭ)? Вирус относится к достаточно старому в эволюционном плане семейству флавивирусов (Flaviviridae), включающему более 70 вирусов животных и человека, в том числе такие опасные, как вирус желтой лихорадки, японского энцефалита, вирус лихорадки Денге и вирус гепатита C.

Лев Александрович ЗИЛЬБЕР (1894—1966) – один из основоположников медицинской науки в СССР. С его именем связаны фундаментальные исследования изменчивости у бактерий и природы иммунитета, организация первых в стране вирусологических центров, создание и экспериментальная разработка вирусо-генетической теории происхождения опухолей, а также совершенно нового направления – иммунологии рака.
За работу по выявлению возбудителя и переносчика весенне-летнего энцефалита в 1937 г. был награжден премией Наркомздрава СССР, но в том же году арестован по ложному обвинению, что экспедиция, которую возглавлял Зильбер, тайно распространяла японский энцефалит на Дальнем Востоке, и освобожден лишь через полтора года. В короткий промежуток времени между освобождением и новым арестом работал над монографией об эпидемических энцефалитах, подготовил несколько статей.
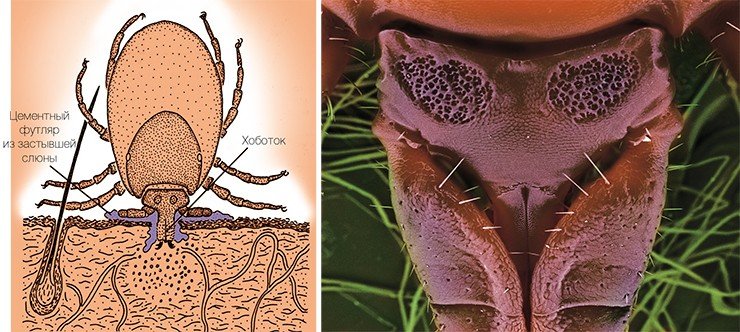
Основным природным резервуаром ВКЭ служат мелкие млекопитающие (полевки, мыши, насекомоядные). Вирус способен заражать животных и размножаться в их организме, однако заболевание протекает у них зачастую без видимого вреда для здоровья. Переносчиками вируса являются клещи, питающиеся кровью лесных зверьков, – европейский лесной клещ, таежный, луговой клещи, а также ряд других, более редко встречающихся видов. ВКЭ может размножаться и в их организме. Точно не известно, был ли вирус первоначально связан только с клещами, или только с позвоночными животными, но в процессе эволюции он приспособился к существованию в организмах как тех, так и других.
В настоящее время вирус клещевого энцефалита встречается в лесных регионах по всей территории Евразии от Атлантического океана до Тихого, причем в целом область его распространения совпадает с ареалами европейского лесного и таежного клещей. В последние десятилетия ареал ВКЭ неуклонно расширяется, что связано с усилением хозяйственной деятельности человека. Так, заброшенные лесные вырубки зарастают мелкими кустарниками и заболачиваются, что создает идеальные условия для обитания мелких млекопитающих и связанных с ними клещей.
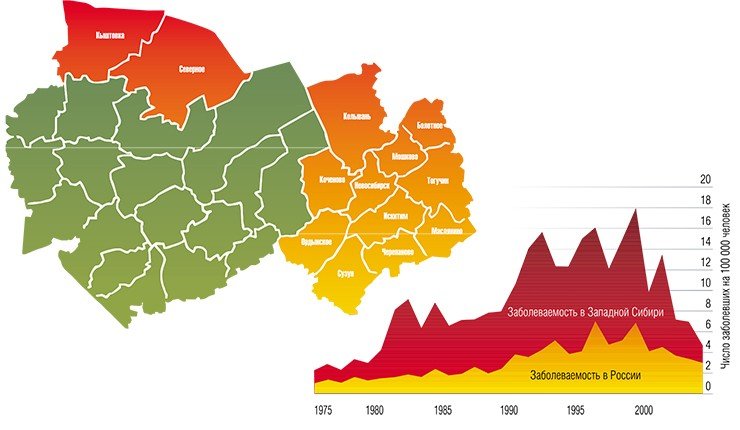
Кроме того, все большее число людей предпочитает проводить свободное время на природе, отдыхая или работая на приусадебных участках. В той же Новосибирской области около 75% населения проживает на территории, условия которой благоприятны для жизни клещей, здесь же сосредоточена и основная масса летних оздоровительных учреждений, зон массового отдыха, садово-дачных участков.
В Институте химической биологии и фундаментальной медицины были исследованы 95 штаммов вируса клещевого энцефалита из коллекции Института систематики и экологии животных СО РАН, выделенных от взрослых особей таежного клеща, собранных с растительности в восточной части Новосибирской области в 1980—2001 гг.
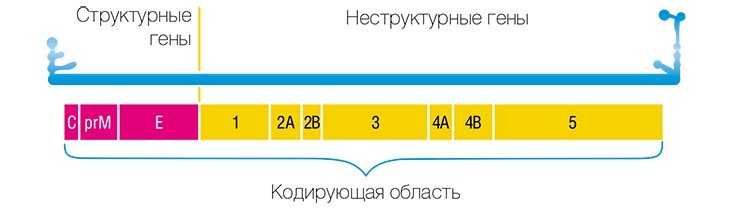
Анализ нуклеотидных последовательностей фрагмента гена Е, кодирующего белок оболочки вируса, показал, что все штаммы соответствуют сибирскому генетическому типу.
С другой стороны, в крови людей, госпитализированных с подозрением на клещевые инфекции, в совместных исследованиях с новосибирскими медиками были обнаружены изоляты ВКЭ, относящиеся к дальневосточному генетическому типу.
Ранее считалось, что этот тип вызывает только тяжелые формы заболевания, тогда как сибирский – преимущественно хронические. Наши исследования, подтвержденные данными других авторов, показали, что вирус дальневосточного генетического типа способен вызывать различные формы клещевого энцефалита, начиная от самых тяжелых и заканчивая стертыми, никак не проявляющимися.
Геном вируса клещевого энцефалита был расшифрован в 1989—1990 гг. практически одновременно в нашей стране (в том числе и в Институте химической биологии и фундаментальной медицины СО РАН (Pletnev et al., 1990)) и за рубежом (Mandl et al., 1989). На сегодня выделено три генетических типа вируса, различающихся по своим свойствам: дальневосточный, сибирский и западноевропейский. Такая привязка генетического типа к географическому местоположению достаточно условна, поскольку в одном регионе могут встречаться штаммы, относящиеся к разным типам.
Для вируса клещевого энцефалита, как и для большинства других вирусных инфекций, не существует высокоспецифических методов лечения – в этом заключается его опасность. Лечение всех вирусных заболеваний направлено в основном на стимуляцию иммунитета и устранение внешних симптомов заболевания, а дальше организм должен сам справляться с инфекцией. ВКЭ опасен еще и тем, что способен вызывать хронические формы заболевания, а его последствиями могут быть параличи и инвалидность. Поэтому важнейшим делом в исследовании этого инфекционного агента является разработка методов диагностики и профилактики заболевания.
Диагностика и профилактика
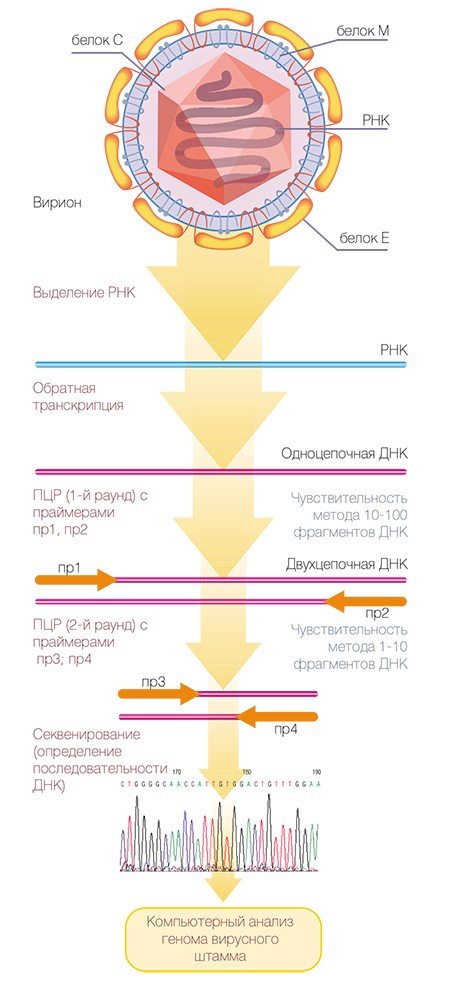
В клинической диагностике вируса клещевого энцефалита наиболее распространены серологические методы, с помощью которых в крови пациента определяют наличие антител, специфических защитных белков, или наличие самого агента. Однако чувствительность этих методов не слишком высока, к тому же существует вероятность ошибки из-за возможных перекрестных реакций с другими патогенами. Кроме того, с их помощью невозможно получить подробную характеристику самого возбудителя (например, определить его генетический тип).
Молекулярно-генетические методы, направленные на специфическое распознавание генетического материала вируса, обладают более высокой чувствительностью. Особенно это относится к методу полимеразной цепной реакции** (ПЦР), благодаря которой можно размножить, а потом идентифицировать ничтожное количество наследственного материала вируса, что позволяет провести диагностику в течение первых дней после заражения. Однако при некоторых обстоятельствах достоинства могут переходить в недостатки: генодиагностика ВКЭ молекулярно-генетическими методами благодаря высокой чувствительности может также приводить к ошибкам, обусловленным многочисленными новыми мутациями вирусных геномов, а кроме того, предъявляет высокие требования к чистоте экспериментов.

Живые вакцины
Живые вакцины – способ стимуляции иммунитета введением в организм ослабленных вирусов, открытый еще в 1796 г. английским врачом Э. Дженнером. С тех пор была получена живая вакцина против вируса желтой лихорадки, отличающаяся от высокопатогенных штаммов многочисленными заменами нуклеотидов в геноме; продолжаются поиски ослабленных штаммов флавивирусов Денге, Западного Нила и Лангат для разработки на их основе живых вакцин.
Были предприняты попытки создания живой вакцины и против вируса клещевого энцефалита. В 1957 г. в качестве такой живой вакцины было решено использовать ослабленный штамм флавивируса Лангат, вызывающий в организме выработку антител, подобных антителам к ВКЭ. Однако выяснилось, что при внутримозговом введении этот штамм сам становится патогенным и вызывает энцефалиты и атрофию участков мозга без внешних клинических проявлений. В дальнейшем были обнаружены ослабленные штаммы самого ВКЭ, но, к сожалению, все они оказались генетически нестабильными.
Вот трагический пример использования живых вакцин против ВКЭ. В 1969 г. от больного, у которого после укуса клеща в течение 4 лет не было клинических проявлений заболевания, но в крови сохранялись высокие титры антител, был выделен ослабленный штамм вируса клещевого энцефалита. Лабораторные исследования выявили его низкую нейровирулентность, после чего были проведены клинические испытания на добровольцах, давшие положительные результаты. В конечном счете ослабленным штаммом ВКЭ было иммунизировано около 650 тыс. человек. Однако 35 вакцинированных получили тяжелые осложнения в виде менингитов и менингоэнцефалитов, причем у 22 из них тяжелые последствия заболевания остались на всю жизнь, а один человек умер. Использование этого штамма в качестве живой вакцины было прекращено (Timofeev, Karganova, 2003).
ДНК-копии
С помощью подобных манипуляций были созданы живые химерные вакцины, содержащие, например, часть генов вируса желтой лихорадки и часть генов других флавивирусов. При этом в функционально важные участки их геномов были введены точечные мутации, вызывающие ослабление патогенности (Pletnev et al., 2006).
Тем не менее в настоящее время применение ослабленных живых вакцин, в том числе и против ВКЭ, ограничено, поскольку существует вероятность превращения ослабленных штаммов в высокопатогенные штаммы дикого типа. Это происходит потому, что в клетке-хозяине отсутствуют системы коррекции мутаций, которые могут возникнуть в вирусной РНК. Гарантией безопасности таких вакцин могла бы служить утрата больших фрагментов вирусных геномов, однако это приводит к значительному снижению жизнеспособности самих вирусов-мутантов.
Нужно отметить, что исследования флавивирусов, как и многих других патогенов, осложняются их высокой инфекционностью, следствием которой являются строгие требования безопасности, а также дороговизной самих вирусных препаратов. И в этом смысле использование неинфекционных ДНК-копий генома ВКЭ является очень перспективным направлением.
В ИХБФМ был получен ряд генно-инженерных ДНК, содержащих в том числе и полноразмерную ДНК-копию генома вируса клещевого энцефалита (Dobrikova et al., 1996). Конструирование подобных стабильных ДНК-копий вирусных геномов открывает широкие возможности для исследования хода размножения вируса в клетках, изучения функций отдельных вирусных белков и их комплексов.
Иммунизация генами
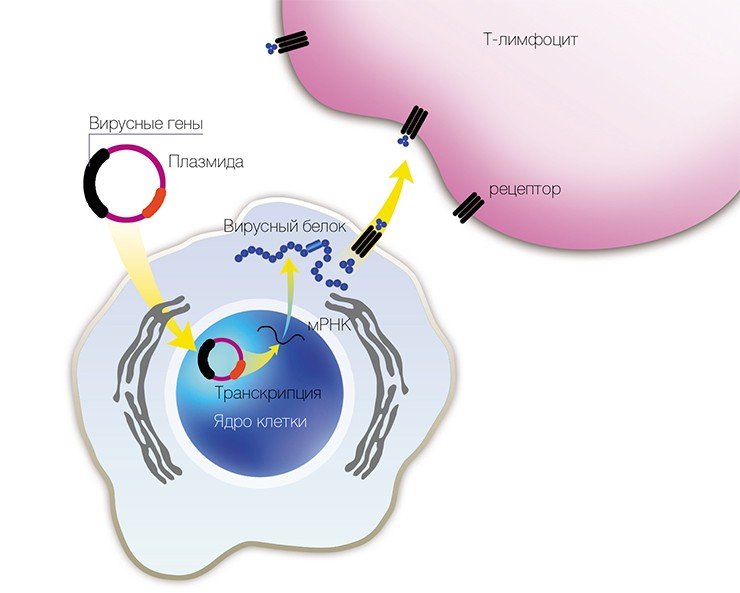
В 1993 г. появился новый подход к профилактике инфекционных заболеваний – генная иммунизация, основанная на прямом введении в организм генно-инженерной ДНК, рекомбинантных плазмид (векторов-переносчиков), содержащих не весь геном, но отдельные гены возбудителя заболевания.
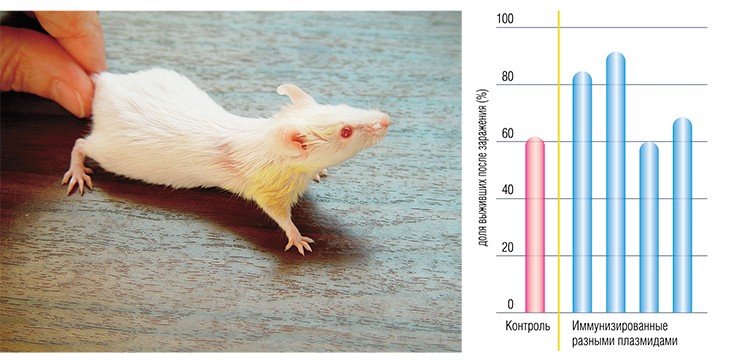
Учеными из ИХБФМ были сконструированы четыре таких плазмиды, содержащие различные гены одного из штаммов вируса клещевого энцефалита. Для оценки эффекта генной иммунизации привитых мышей заражали летальными дозами того же штамма ВКЭ. В результате оказалось, что некоторые плазмиды обладают определенным защитным эффектом.
В качестве вакцин против вирусных заболеваний ученые предполагают использовать генно-инженерные плазмиды, в которые встроены отдельные гены вирусов
Чтобы изучить возможные нежелательные эффекты этих вакцин, плазмиды вводили в различные клеточные культуры. В результате выяснилось, что при увеличении времени культивирования клеток до нескольких месяцев наблюдалась существенная модификация плазмид и встраивание их в хозяйский геном.
Таким образом, несмотря на положительные результаты генной вакцинации, вопрос о применении ДНК-вакцин в настоящее время остается открытым, поскольку препятствием к их использованию также является проблема безопасности. Возможно, преодолеть это препятствие удастся созданием РНК-вакцин с аналогичным принципом действия, для которых не существует риска интеграции в ДНК-геном хозяйской клетки. Но это уже задачи будущих исследований.
Возможно ли полностью избавиться от ВКЭ, например, уничтожив его основных переносчиков, иксодовых клещей? В свое время такая попытка была сделана с использованием печально известного ДДТ, но последствия массовой обработки лесов сильнейшим ядом были поистине ужасающими.

Клещевой (весенне-летний) энцефалит — острая нейровирусная природно-очаговая трансмиссивная инфекция, характеризующаяся лихорадкой, интоксикацией, поражением центральной нервной системы.
Инфекция наиболее распространена в Республике Беларусь в юго-западных (Брестская область) и западных (Гродненская) регионах. В последние года за счет расширения ореала обитания переносчика инфекции – иксодовых клещей, инфицированность которых достигла 30-40%, заболеваемость выросла.
Возбудитель клещевого энцефалита относится к роду Flavivirus семейству Togaviridae, экологической группы Arboviruses. Вирус представляет собой округлые частицы, размером 20-40 нм, содержит РНК, окруженную белковой оболочкой. Выделяют восточные и западные антигенные варианты вирусов, вызывающих различные нозогеографические формы клещевого энцефалита. Вирус культивируется на куриных эмбрионах и клеточных культурах различного происхождении. Из домашних животных наиболее чувствительны к вирусу овцы, козы, поросята и лошади.
Основные проявления эпидемического процесса. Клещевой энцефалит относится к группе природно-очаговых болезней человека. Основным резервуаром и переносчиком вируса в природе являются иксодовые клещи — Ixodes persulcatus, Ixcodes riciniis с трансовариальной передачей инфекции. Дополнительным резервуаром вируса являются грызуны (заяц, еж, бурундук, полевая мышь), птицы (дрозд, щегол, чечетка, зяблик), хищники (волк). Основным путем инфицирования человека является трансмиссивная передача через укусы зараженных клещей. Спустя 5-6 дней после кровососания на инфицированном животном вирус проникает во все органы клеща, концентрируясь в половом аппарате, кишечнике, слюнных железах. Вирус сохраняется в течение всей жизни членистоногого (2 - 4 года), что определяет механизм заражения животных и человека и трансовариальную передачу вируса у клещей. В отдельных очагах болезни инфицированность клещей превышает 20%. Возможна также передача инфекции алиментарным путем при употреблении в пищу сырого молока коз и коров (молочная лихорадка), а также при раздавливании клеща в момент удаления его с тела человека и, наконец, воздушно-капельным путем при нарушении режима работы в лабораториях. Для клещевого энцефалита характерна строгая весенне-летняя (май-июнь) сезонность заболеваемости. Чаще болеют лица в возрасте 20-40 лет. При алиментарном пути заражения характерно наличие семейно-групповых случаев болезни.
Клиника. Инкубационный период длится 7-14 дней с колебаниями от 3 до 21 дня. Более короткий срок инкубации (4 - 6 дней) отмечен при алиментарном заражении. С первых дней течение клещевого энцефалита носит токсико-инфекционный характер. Заболевание начинается остро, с озноба и повышения температуры тела до 38-39°С. Появляются общая слабость, резкая головная боль тошнота и рвота, разбитость, утомляемость, нарушение сна. Беспокоят боли во всем теле и конечностях.
Лечение. В качестве этиотропной терапии применяется противоклещевой донорский иммуноглобулин и рибонуклеаза. Серотерапия проводится в течение лихорадочного периода, обычно 3 дня, человеческим гамма-глобулином, имеющим титр к вирусу клещевого энцефалита не менее 1:80, в дозе 1,5-3 мл 1-2 раза в сутки внутримышечно. Рибонуклеаза вводится на 10 мг в 3 мл изотонического раствора натрия хлорида внутримышечно 4—6 раз в сутки в течение лихорадочного периода и еще 2 дня после снижения температуры.
Профилактика. В природных очагах клещевого энцефалита проводятся мероприятия по защите населения от нападения клещей с использованием противоклещевых комбинезонов, репеллентов (диметил- и дибутилфталаты). При обнаружении присосавшихся клещей после их удаления применяют специфический донорский иммуноглобулин (взрослым по 3 мл внутримышечно). Не рекомендуется использовать в пищу некипяченое молоко. Специфическая профилактика проводится по эпидемическим показаниям за 1-1,5 мес до сезона активности клещей путем применения культуральной концентрированной вакцины. Вакцина вводится подкожно по 1 мл по схеме, включающей первичный курс 4 инъекции с интервалами 7-10, 20-30 дней, 4
6 мес и три ежегодные отдаленные ревакцинации. После проведения полного курса прививок (7 инъекций) иммунитет сохраняется в течение 5 лет, в связи с чем повторные ревакцинации рекомендуется проводить через 4 года лицам, проживающим на эндемичной территории.
Болезнь Лайма (лайм-боррелиоз, клещевой боррелиоз) – это инфекционное заболевание, вызываемое бактериями рода borrelia и передающееся клещами, с преимущественным поражением кожи, нервной системы, опорно-двигательного аппарата и сердца. Больной клещевым боррелиозом для окружающих не заразен. Боррелиоз имеет очень разнообразную клиническую картину, что может затруднять его своевременную диагностику.
Процесс развития болезни Лайма. Заражение клещевым боррелиозом происходит при укусе инфицированным клещом. И не только в лесу, но и в лесопарках внутри города. Боррелии со слюной клеща попадают в кожу и в течение нескольких дней размножаются, после чего они распространяются на другие участки кожи и внутренние органы (сердце, головной мозг, суставы). Боррелии в течение длительного времени (годами) могут сохраняться в организме человека, обусловливая хроническое и рецидивирующее течение заболевания. Хроническое течение болезни может развиться после длительного периода времени.
Инкубационный период клещевого боррелиоза состовляет - от 2 до 30 дней, в среднем - 2 нед. Характерным признаком начала заболевания в 70% случаев является появление на месте укуса клещом покраснения кожи. Красное пятно постепенно увеличивается по периферии, достигая 1-10 см в диаметре, иногда до 60 см и более. Форма пятна округлая или овальная, реже неправильная. Наружный край воспаленной кожи более интенсивно красный, несколько возвышается над уровнем кожи. Со временем центральная часть пятна бледнеет или приобретает синюшный оттенок, создается форма кольца. В месте укуса клеща, в центре пятна, определяется корочка, затем рубец. Пятно без лечения сохраняется 2-3 нед, затем исчезает. Через 1-1,5 мес развиваются признаки поражения нервной системы, сердца, суставов.
Профилактика боррелиоза. Существует ли вакцина от Лайм-боррелиоза? Вакцина от Лайм-боррелиоза была разработана и применялась в США до 2002 года, но затем ее выпуск был прекращен, в основном, по коммерческим причинам. В Европе ведутся разработки вакцин следующего поколения, но разрешенных к применению вакцин в настоящее время нет.
Очень важным моментом становится неспецифическая профилактика клещевого боррелиоза. Основные профилактические мероприятия:
- на прогулки в лес необходимо надевать защищающую одежду - рубашки с длинными рукавами, сапоги, длинные брюки, перчатки, шапки. Заправляйте верхнюю одежду в штаны, а штаны – в носки;
- на одежду лучше заранее нанести средства, отпугивающие насекомых;
- после того, как придете домой, снимите одежду вне жилого помещения и тщательно ее осмотрите, обратив особое внимание на складки, швы, карманы;
- если клещ прикрепился на кожу, его надо аккуратно удалить с помощью пинцета, клеща удаляют выкручивающими движениями за головку;
- если под рукой нет ни пинцета, ни специальных приспособлений для удаления клещей, то клеща можно удалить при помощи нитки. Прочную нитку завязывают в узел, как можно ближе к хоботку клеща, затем клеща извлекают, подтягивая его вверх. Резкие движения недопустимы;
- после удаления клеща кожу в месте его присасывания обрабатывают настойкой йода или спиртом;
Что делать если укусил клещ?
Читайте также:


