Тромбоцитопения у детей при гриппе
Учитывая то обстоятельство, что в литературных источниках недостаточно полно отражены особенности протекания острой формы этого заболевания у детей в различные возрастные периоды жизни, целью нашего исследования мы поставили изучение клинического течения острой ИТП у 100 детей и подростков в трех возрастных группах: 1-я группа - дети в возрасте от 1 месяца до 1 года 6 месяцев (29 больных), 2-я группа - дети раннего и дошкольного возраста (от 1 года 7 месяцев до 7 лет 6 месяцев, 50 детей), 3-я группа - дети школьного возраста (от 7 лет 7 месяцев до 17 лет, 21 больной). Обследование и лечение больных проводилось на базе отделения гематологии областной детской клинической больницы г. Перми. Катамнестическое обследование всех пациентов в течение не менее 6 месяцев подтвердило факт отсутствия перехода заболевания в хроническую форму.
В группе детей первых полутора лет жизни (14 девочек, 15 мальчиков) первые симптомы заболевания у 13 больных появились в возрасте 1 - 3 месяца жизни, у 6 больных - на 4 - 6 месяце, у 4 больных - на 7-12 месяце и у 6 - на 13 - 18 месяце. Острое начало было зафиксировано у 96,5% заболевших, только в одном случае имела место постепенная манифестация. Практически у всех детей (96,5%) в развитии патологии были выявлены провоцирующие факторы. В качестве последних наиболее часто выступали ОРВИ в сроки от 3 до 22 дней (в среднем 14,5 дней) до начала ИТП (41,3%). Вакцининдуцированная ИТП наблюдалась в 34,5% случаев, заболевание при этом начиналось в сроки от 1 до 26 дней после вакцинации. Связь патологического процесса с вакцинацией АКДС + ОПВ зафиксирована у 5 детей, с вакцинацией ВГВ - 2 детей. По одному случаю ИТП зарегистрировано после вакцинации АКДС + ОПВ + ВГВ, после туровой вакцинации ОПВ, а также после прививки против краснухи. Цитомегаловирусная инфекция послужила причиной развития заболевания у 2 больных. На фоне обострения аллергической патологии заболевание развилось также у 2 детей. Не выявленным остался этиологический фактор в одном случае.
Сухая форма заболевания наблюдалась у 69% обследованных, влажная - у 31%. Наиболее часто заболевание манифестировало в форме изолированного кожно-геморрагического синдрома в виде петехий (27,6%) или петехий в сочетании с экхимозами (44,8%). Влажная пурпура на момент начала патологического процесса определялась у каждого четвертого больного.
У 26 из 29 больных кожно-геморрагический синдром носил выраженный характер. Однако, если петехиальная сыпь за весь период заболевания была представлена у всех больных, то экхимозы встречались только у 2/3 пациентов. Геморрагические высыпания на лице отмечались в 83% случаях, геморрагии на слизистой полости рта - в 48,3% больных, а кровоизлияния в склеры - в 10,3%. Носовые кровотечения были отмечены у 6 больных (24,1%), развивались спонтанно, реже - на фоне вирусных инфекций, были, как правило, кратковременными, необильными, не требовали применения инвазивных методов остановки и не приводили к тяжелой анемизации. Кишечные кровотечения в виде появления сгустков алой крови в стуле отмечались у 4 обследованных (13,8%), также были непродолжительными (1-2 дня) и необильными. Десневые кровотечения, а также длительные кровотечения из мест внутримышечных инъекций и забора крови из вены встречались у 2 больных. Периферические лимфоузлы у всех детей, кроме двоих, были не увеличены. Умеренная гепатомегалия (печень +1+2,5 см ниже края реберной дуги) отмечалась у 58,6% обследованных, выраженная гепатомегалия (+3+4 см) - у 13,8%. Более чем у половины детей (58,6%) селезенка не пальпировалась, у 13,8% детей пальпировался ее край, у 27,6% - он выступал из подреберья на 1-2,5 см. Уровень тромбоцитов ниже 30 х 10 9 /л отмечался у 62% больных, у остального количества детей число тромбоцитов находилось в пределах 30 - 60 х 10 9 /л. У 4 больных количество тромбоцитов снижалось до единичных в мазке. Анемия легкой степени тяжести была выявлена у 48,2% больных, средней тяжести - 13,8%. В одном случае наблюдалась тяжелая постгеморрагическая анемия, требовавшая гемотрансфузий.
В группе детей раннего и дошкольного возрастов (n=50) ИТП одинаково часто встречалась у больных обоего пола (26 мальчиков, 24 девочки). Как и в предыдущей возрастной группе, острое начало заболевания выявлялось у большинства детей (96%). Среди этиологических факторов преобладали ОРВИ (44%) и специфические вирусные инфекции - грипп, краснуха, острая ЦМВИ, острая хламидийная инфекция, инфекционный мононуклеоз (18%). Вакцининдуцированная ИТП развивалась значительно реже по сравнению с предыдущей группой (р 9 /л. В остальных случаях наблюдалась умеренная тромбоцитопения (30 - 50 х 10 9 /л). Снижение числа тромбоцитов до единичных в мазке регистрировалось у каждого третьего больного.
В группе детей школьного возраста (n=21) заболевание чаще встречалось у девочек (71,4%). Во всех случая была характерна острая манифестация. Ведущим этиологическим фактором, как и в предыдущих группах, оказывались ОРВИ (42,8%). Однако у каждого третьего больного патологический процесс разворачивался без видимой причины. Среди других провоцирующих факторов фигурировали грипп, бактериальные инфекции, гиперинсоляция, физические травмы, гельминтозы, вакцинация; они выявлялись у единичных больных. Отличительной чертой клинической картины заболевания явилось преобладание у детей влажной формы (76,2%). В начальном периоде ИТП кровотечения регистрировались в 2/3 случаев, при этом у половины больных одновременно были кровотечения нескольких локализаций (носовые + десневые, носовые + почечные).
Обратила на себя внимание умеренная выраженность кожно-геморрагического синдрома у ¼ больных. Геморрагические высыпания на лице были представлены менее чем в половине случаев (43%). Кровоизлияния на слизистой рта наблюдались у 66,7% детей, кровоизлияния в склеры - у 14,3%. Носовые кровотечения были представлены в 66,7% случаев, десневые - у 1/4 больных. С одинаковой частотой (9,5%) регистрировались кишечные, почечные и маточные кровотечения. Инвазивные мероприятия при носовых кровотечениях требовались каждому четвертому ребенку. У одной девочки, заболевшей в возрасте 16 лет, на второй неделе заболевания развилось внутричерепное кровоизлияние, послужившее причиной летального исхода. Умеренное увеличение печени выявлено у 14% детей. Ни у одного из больных селезенка не пальпировалась. Постгеморрагическая анемия осложняла течение заболевания в 2/3 случаев. Среднетяжелый ее характер отмечался у каждого четвертого больного, у остальных детей она была легкой. У всех больных уровень тромбоцитов был ниже 30 х 10 9 /л, причем в 1/3 случаев зарегистрирован практически нулевой их уровень.
Следовательно, отличительными чертами острой ИТП у детей школьного возраста были преобладание заболевания у девочек, большая, по сравнению с другими возрастными группами, частота собственно идиопатических форм, преобладание влажной пурпуры над сухой, наиболее широкий диапазон кровотечений (носовые, десневые, кишечные, почечные, маточные, внутричерепные). Кровотечения нередко носят комбинированный характер, представляя угрозу для жизни больного. Последний фактор, наряду с глубокой тромбоцитопенией, свойственной всем детям, определили тяжесть течения ИТП у детей этого возраста. Развитие гепатолиенального синдрома не характерно.
Таким образом, проведенное исследование выявило наличие многих особенностей течения ИТП у детей рассматриваемых возрастных групп. Практическую значимость подобной работы мы видим в том, что знание специфики протекания заболевания у детей определенного возрастного состава помогает лечащему врачу спрогнозировать его течение и вероятность развития осложнений.

- Главная
- Профилактика
- Болезни крови
- Тромбоцитопеническая пурпура
Тромбоцитопеническая пурпура
Тромбоцитопеническая пурпура – это заболевание, которое характеризуется кровоизлияниями под кожу, повышенной кровоточивостью, возникающих в результате тромбоцитопении – снижения количества тромбоцитов в крови. Поскольку тромбоциты отвечают за свертываемость крови, снижение их количества в крови до 150x10 9 /л приводит к ее низкой свертываемости, поэтому возникают обильные кровотечения. Само название болезни Purpura thrombocytopenica в переводе с латинского означает: purpura - пурпурный цвет, thrombocyte – тромбоциты, от греч. penia – бедность. Синоним: болезнь Верльгофа.
Тромбоцитопеническую пурпуру относят к заболеваниям группы геморрагических диатезов. Встречается эта болезнь с частотой 10-80 случаев на миллион жителей в год. Обнаруживается пурпура чаще всего в детском возрасте, обычно у детей 2-7 лет, но встречается даже у грудных детей. В возрасте до 10 лет мальчики и девочки болеют с одинаковой частотой, после 10 лет – девочки болеют в несколько раз чаще. Начинается пурпура, как правило, после вирусной или бактериальной инфекции.
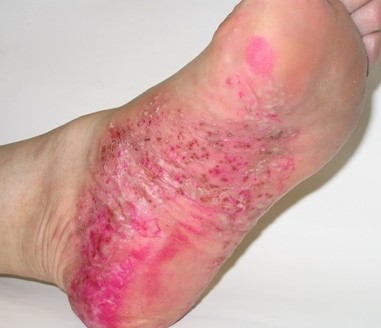
- Кровоизлияния в кожу.
- Бледность кожи.
- Кровотечение из носа.
- Кровоточивость десен.
- Кишечные, желудочные кровотечения.
- У девочек – маточные кровотечения.
- Низкое давление.
- Повышение температуры до 38°С.
- Лимфаденопатия - увеличение лимфатических узлов.
- В 15-20% случаев – увеличение печени и селезенки.
В зависимости от причин и механизма развития различают следующие виды заболевания:
- Идиопатическая тромбоцитопеническая пурпура (болезнь Верльгофа).
- Изоиммунная – из-за повторных переливаний крови или тромбоцитной массы, а также беременностей.
- Врожденная иммунная тромбоцитопеническая пурпура – из-за несовместимости крови матери и ребенка, обычно проходит к 4-5 месяцам жизни ребенка.
- Аутоиммунная тромбоцитопеническая пурпура – сочетается с анемией, системной красной волчанкой и др.
- Симптоматическая – наблюдается при дефиците витамина В12, лучевой болезни, некоторых инфекциях, приеме некоторых сильнодействующих лекарственных препаратов.
Сочетание пурпуры с эндокардитом, малярией, лейшманиозом может осложнить протекание этих инфекционных заболеваний.
Обычно причиной тромбоцитопенической пурпуры служит вирусная инфекция – в 80% случаев это грипп, ветрянка, корь, краснуха. Случается, что болезнь спровоцировала реакция на прививку при вакцинации. Врожденная форма болезни вызвана несовместимостью материнской крови и ребенка, наследственными заболеваниями крови или обмена веществ. Пурпура может возникнуть при лейкозе и других раковых заболеваниях крови.
Диагностика основана на фиксации характерных симптомов – носовых, желудочных, кишечных, маточных кровотечений, бледности кожи, высокой температуре. Проводятся эндотелиальные пробы – их положительный результат свидетельствует о пурпуре. Проведение лабораторных тестов (измерение времени кровотечения, определение степени ретракции сгустка крови и др.) – наиболее надежный способ диагностики тромбоцитопенической пурпуры.
Для дифференциальной диагностики тромбоцитопенической пурпуры от лейкоза, красной волчанки, тромбоцитопатии проводят иммунологические исследования, пункцию красного костного мозга, структурный анализ крови.
Прежде всего, нужно обеспечить ребенку постельный режим. Обычно лечение тромбоцитопенической пурпуры проводят в больнице. При кровотечении десен и слизистой рта пища для ребенка должна быть охлажденной.
Для лечения назначаются глюкокортикоиды и иммунодепрессанты. Рассмотрим их применение поподробнее.
Преднизолон – применяется в течение 2-3 недель в дозировке 2 мг в сутки на каждый килограмм массы тела. Затем идет снижение дозы и отмена препарата. Иногда применяются короткие курсы по 7 дней с дозировкой 3 мг в сутки на каждый килограмм массы тела. Между такими курсами делают перерыв 5-7 дней. В большинстве случаев такая методика помогает, однако у некоторых пациентов после отмены преднизолона может возникнуть рецидив болезни.
Иммуноглобулины – применяются в сочетании с основными препаратами (обычно с глюкокортикоидами). Чаще всего назначается внутривенное введение Ig 0,4 мг/кг в сутки, курс – 5 дней. Если эти препараты не улучшают ситуацию, то применяют цитостатики.
При слабом эффекте глюкокортикоидов и иммуноглобулинов рассматривается целесообразность проведения спленэктомии – операции по удалению селезенки. Как правило, такую операцию проводят детям от 5 лет, помогает она в 70% случаев.
Смертность от тромбоцитопенической пурпуры составляет 1-2% случаев. Основная причина – кровоизлияние в головной мозг. За последние годы в связи с развитием медицины врачам удалось существенно сократить количество летальных исходов заболевания.
Никаких профилактических мер по предупреждению тромбоцитопенической пурпуры не разработано. Профилактика сводится к предотвращению возможных рецидивов. Среди возможных мер профилактики можно выделить особое внимание детям при вакцинации, индивидуальный подход к детям с повышенным риском заболевания. После полного выздоровления от пурпуры пациенты находятся на учете в течение 5 лет, регулярно сдают кровь для анализа количества тромбоцитов. При заболевании другой инфекционной болезнью необходимо проведение тщательного обследования.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Грипп А(H1N1)pdm09, кроме высокой контагиозности, отличается от сезонного гриппа повышенным развитием осложненных форм.
Цель: изучить особенности течения внебольничных пневмоний на фоне гриппа A(H1N1)pdm09.
Материал и методы: приведены особенности течения внебольничных пневмоний на фоне гриппа A(H1N1)pdm09 в период с 2009 по 2016 г. у 169 больных в возрасте от 18 до 85 лет. Диагноз внебольничной пневмонии верифицировался на основании клинико-эпидемиологических данных в момент поступления в стационар, рентгенологических и лабораторных методов диагностики. Критериями тяжести течения являлись: степень дыхательной недостаточности, выраженность интоксикационного синдрома, объем воспалительной инфильтрации, наличие осложнений, декомпенсация сопутствующих заболеваний. У 96 (56,8%) больных регистрировалась тяжелая внебольничная пневмония, у 73 больных (43,2%) – нетяжелая внебольничная пневмония.
Результаты: течение внебольничных пневмоний на фоне гриппа A(H1N1)pdm09 у обследованных нами больных характеризовалось острым началом, проявлялось выраженным интоксикационным синдромом и поражением дыхательных путей, степень проявления которого зависела от тяжести заболевания. В 56,8% случаях пневмонии протекали с тяжелым течением, преимущественно у молодых людей 18–29 лет, имеющих отягощенный преморбидный фон с преобладанием метаболического синдрома, что и определило ведущую роль в развитии тяжелого течения пневмонии на фоне гриппа A(H1N1)pdm09. По данным рентгенологического обследования у больных с тяжелыми пневмониями чаще диагностировались двусторонние пневмонии (64,6%) с тотальным и долевым поражением, в группе больных с нетяжелым течением пневмонии преобладали односторонние пневмонии (83,5%) с преимущественной локализацией в правом легком (68,5%). Особенностью гематологических параметров при тяжелом течении пневмонии был незначительный лейкоцитоз с тромбоцитопенией, которые нарастали по мере более позднего поступления в стационар. В биохимических параметрах при тяжелой пневмонии отмечалось повышение С-реактивного белка (СРБ), креатинина, аспартатаминотрансферазы (АсТ), креатинфосфокиназы (КФК), снижение общего белка, что расценивается как проявление полиорганной недостаточности на фоне эндогенной интоксикации.
Заключение: внебольничные пневмонии на фоне гриппа A(H1N1)pdm09 протекают в тяжелой форме, в основе которой лежит синдром выраженного системного воспалительного ответа.
Ключевые слова: грипп A(H1N1)pdm09, внебольничная пневмония, больные, тяжесть течения, преморбидный фон, лабораторные методы диагностики.
Для цитирования: Сергеева И.В., Демко И.В. Особенности течения внебольничной пневмонии на фоне гриппа A(H1N1)pdm09. РМЖ. 2017;18:1280-1285.
Features of the course of community-acquired pneumonia on a background of influenza A(H1N1)pdm09
Sergeeva I.V., Demko I.V.
Krasnoyarsk State Medical University named after Professor V.F. Voyno-Yasenetsky
Influenza A(H1N1)pdm09, in addition to high contagiousness, differs from seasonal influenza by the increased development of complicated forms.
Aim: to study the features of the course of community-acquired pneumonia on a background of influenza A(H1N1)pdm09.
Patients and methods: 169 patients aged 18 to 85 years were examined between 2009 and 2016. The diagnosis of community-acquired pneumonia was verified on the basis of clinical and epidemiological data at the time of admission to the hospital, X-ray and laboratory diagnostic methods. Criteria for the severity were: the degree of respiratory failure, the severity of the intoxication syndrome, the volume of inflammatory infiltration, the presence of complications, the decompensation of comorbidities. Severe community-acquired pneumonia was registered in 96 (56.8%) patients, in 73 patients (43.2%) - community-acquired pneumonia of moderate severity.
Results: the course of community-acquired pneumonia on a background of influenza A(H1N1)pdm09 in the patients examined by us was characterized by an acute onset, manifested by severe intoxication syndrome and respiratory tract disease, the degree of manifestation of which depended on the severity of the disease. In 56.8% of cases, severe course of pneumonia was registered, mainly in young people aged 18-29 years with a burdened premorbid background with a predominance of metabolic syndrome, which determined its leading role in the development of severe pneumonia on a background of influenza A(H1N1)pdm09. According to the X-ray examination in patients with severe pneumonia, bilateral pneumonia with total and fractional lesion was more often diagnosed (64.6%), unilateral pneumonia prevailed in the group of patients with moderate pneumonia (83.5%) with predominant localization in the right lung (68, 5%). A feature of hematological parameters in severe pneumonia was a slight leukocytosis with thrombocytopenia, which increased depending on the day of admission. In the biochemical parameters of severe pneumonia, there was an increase in C-reactive protein (CRP), creatinine, aspartate aminotransferase (AST), creatine phosphokinase (CPK), total protein reduction, which is regarded as a manifestation of multiple organ on the background of endogenous intoxication.
Conclusion: community-acquired pneumonia against the background of influenza A(H1N1)pdm09 occurs in severe form, which is based on the syndrome of a pronounced systemic inflammatory response.
Key words: influenza A(H1N1)pdm09, community-acquired pneumonia, patients, severity of the course, premorbid background, laboratory diagnostic methods.
For citation: Sergeeva I.V., Demko I.V. Features of the course of community-acquired pneumonia on a background of influenza A(H1N1)pdm09 // RMJ. 2017. № 18. P. 1280–1285.
Статья посвящена особенностям течения внебольничной пневмонии на фоне гриппа A(H1N1)pdm09
Только для зарегистрированных пользователей
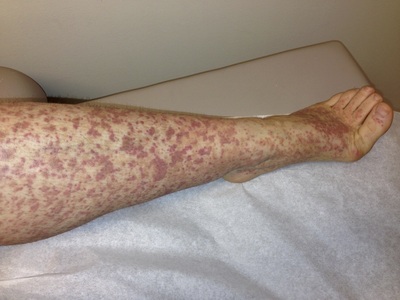
Тромбоцитопения (пурпура) – это заболевание, характеризующееся снижением количества тромбоцитов в периферической крови до показателя 150000 в микролитре. В результате чего повышается ломкость мелких сосудов, а также замедляется процесс остановки кровотечений из них.
Классификация болезни
По продолжительности и тяжести симптомов болезнь можно классифицировать как:
- острую (протекает практически бессимптомно, срок воздействия на организм больного не более полугода);
- хроническую (симптомы проявляются постепенно, заболевание длится более 6 месяцев, длительность лечения может доходить до двух лет).
Формы болезни
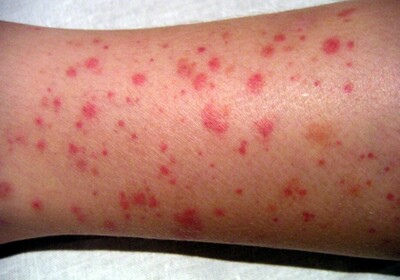
Тромбоциты являются составной частью крови, образующейся в костном мозге из клеток предшественников – мегакариоцитов. Они имеют вид безъядерной плоской пластинки размером от одного до двух микрометров.
Мегакариоциты – это относительно большие клетки, имеющие длинные, заполненные цитоплазмой отростки, которые в ходе созревания, отделяясь от материнской клетки, попадают в кровоток. Эти отростки собственно и являются тромбоцитами. Стоит заметить, что из одной донорской клеточки может образоваться до 8000 тромбоцитов.
За образование мегакариоцитов отвечает гормон – тромбопоэтин, образующийся в печени, почках и мышечной ткани. Стоит отметить, что между количеством красных клеточек и тромбопоэтина существует прямая зависимость: чем больше образуется тромбоцитов, тем сильнее тормозится синтез тромбопоэтина. Эта закономерность позволяет поддерживать количество вышеуказанных элементов на стабильном уровне.
В случае, если на любом из указанных выше этапов происходит сбой, количество тромбоцитов в сыворотке крови снижается, вызывая тромбоцитопению.
С учетом причин и механизмов развития заболевание может принимать следующие формы:
- наследственную;
- продуктивную;
- разрушенную;
- потребления;
- распределения;
- разведения.
Наследственная форма
В большинстве случаев данный вид патологии проявляется при наличии прочих сопутствующих врожденных аномалий. А основными ее причинами являются различного рода генетические нарушения (мутации):
- Синдром Вискота-Олдрича. Вызывается генетическими мутациями, в результате которых происходят изменения размера тромбоцитов в сторону их уменьшения (диаметр красной клеточки не превышает одного микрометра). Из-за аномального изменения структуры клеточки происходит их быстрое разрушение в селезенке (в течение 1-2 часов).
- Аномалия Мея-Хегилина. Крайне редко встречающаяся генетическая аномалия, вызывающая нарушение процесса отделения тромбоцитов от мегакариоцитов. В результате, чего происходит сокращение их количества в сыворотке крови, а также увеличение их диаметра до семи микрометров. Параллельно этому может наблюдаться угнетение образования новых лейкоцитов.
- Амегакариоцитарная тромбоцитопения (врожденная). В большинстве случаев патология встречается у детей в младенческом возрасте. Ее появление связывают с нарушениями в работе костного мозга.
- Синдром Бернара-Сулье. Проявляется в младшем возрасте и лишь в случае, если ребенок унаследовал дефектный ген от одного из родителей. Для этого вида болезни характерно образование функционально дефектных красных клеточек, имеющих к тому же гигантский диаметр более 8 микрометров.
- TAR-синдром. Наиболее редкая причина возникновения отклонения спровоцирована отсутствием обеих лучевых костей.
Продуктивная форма
К данной группе относят патологии, связанные с нарушением процесса образования тромбоцитов в красном костном мозге. К причинам ее возникновения можно отнести:
Форма разрушения
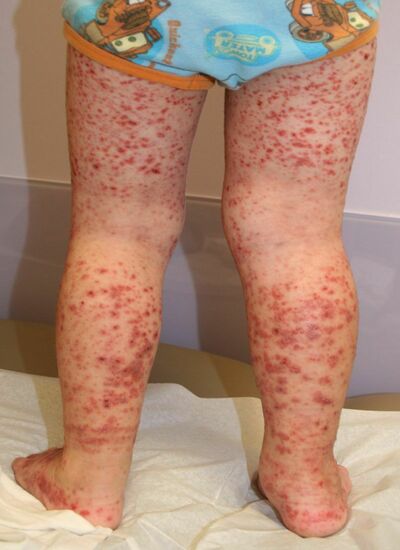
Причиной болезни является усиленное разрушение красных клеточек в селезенке, лимфатических узлах, сосудах и печени. Патология может быть диагностирована:
- у новорожденных;
- у больных, страдающих от синдрома Эванса-Фишера;
- в случае заражения некоторыми видами вирусов;
- в случае приема некоторых видов лекарственных средств;
- при идиопатическом тромбоцитопеническом пурпуре.
Форма болезни у новорожденных
Возникает в случае несоответствия антигенов, расположенных на поверхности тромбоцитов ребенка, антигенам, расположенным на поверхности красных клеточек матери. Иммунные клетки материнского организма, поступая в кровеносную систему ребенка через плаценту, разрушают его собственные тромбоциты. Описанный выше процесс происходит до 20 недели беременности.
Синдром Эванса-Фишера
Синдром возникает, как следствие развития системных аутоиммунных заболеваний –поражение печени и суставов, системная красная волчанка.
Вирусная форма
В процессе размножения вирусных клеток происходит образование специфических антител, провоцирующих разрушение красных клеточек в селезенке. Вирусами способными спровоцировать болезнь являются: корь, краснуха и грипп.
Посттрансфузионная форма
Патология является следствием реакции организма на чужеродные донорские тромбоцитарные клеточки.
Лекарственная форма
Идиопатическая пурпура
Этот вид патологии характеризуется резким снижением количества красных клеточек в периферической крови при неизменном уровне остальных элементов.
Причины возникновения пурпуры
Современная наука не может выявить точную причину возникновения заболевания. Наиболее популярной теорией является комплексное воздействие внешних негативных факторов и наследственной предрасположенности. Негативные факторы, способные спровоцировать появление болезни:
- некоторые виды бактериальных и вирусных инфекций;
- побочные эффекты некоторых прививок;
- негативное воздействие солнечной радиации;
- длительное переохлаждение;
- воздействие некоторых видов лекарственных средств.
Механизм возникновения болезни можно объяснить нахождением на поверхности тромбоцитарных клеток – антигенов, которые в случае наличия каких-либо мутаций провоцируют выработку специфических антител, способных взаимодействовать с антигенами и разрушать клетку-носитель.
В случае наличия эссенциальной формы болезни селезенка вырабатывает антитела к антигенам собственных тромбоцитов, которые, закрепляясь на мембранах красных клеточек, помечают их. Помеченные клеточки, проходя с кровотоком через селезенку, отсеиваются и разрушатся.
Благодаря снижению количества красных клеточек в крови начинается их усиленная выработка клетками печени. Скорость вызревания мегакариоцитов и образования тромбоцитов в костном мозге значительно увеличивается. Однако, с течением времени компенсационные возможности костного мозга ослабляются, провоцируя появление первых признаков болезни.
Форма потребления
Активация клеток происходит в сосудистом русле, запуская механизм свертываемости крови. Благодаря усиленной выработке тромбоцитов костный мозг исчерпывает возможности по их созданию, что собственно является причиной возникновения патологии. В случае, если вовремя не начать терапию, уменьшение уровня тромбоцитов в крови может стать фатальным.
К активации форменных элементов может привести:
- Тромботическая пурпура. Провоцируется недостаточным количеством простациклина в крови. Данный фактор вырабатывается клетками эндотелия, благодаря своим свойствам простациклин мешает склеиванию тромбоцитов. В случае нарушения его выработки происходит точечная активация выработки красных клеточек, способствующих образованию различного рода тромбов, повреждающих сосуды и способствующих развитию внутрисосудистого гемолиза.
- Синдром диссеминированного внутрисосудистого свертывания является последствием сильного поражения внутренних органов, вследствие которых способность организма вырабатывать тромбоциты истощается, благодаря чему происходит образование множественных тромбов, способных оказывать негативное влияние на кровоснабжение и функционирование внутренних органов (в первую очередь, мозга и почек). Как следствие этого состояния происходит усиление выработки веществ, ухудшающих свертываемость крови, которые со временем разрушают образовавшиеся тромбы и восстанавливают нормальное кровообращение. Однако, в некоторых случаях кровь полностью утрачивает способность к свертываемости, что приводит к повышенному риску возникновения кровотечений, способных, кроме всего прочего, привести к летальному исходу.
Гемолитико-уремический синдром
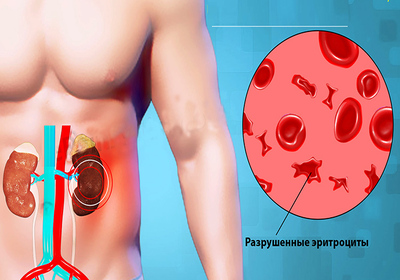
Провоцируется этот синдром различного рода кишечными инфекциями, наследственной предрасположенностью, системными заболеваниями и приемом некоторых видов лекарственных препаратов. Благодаря выделению в кровь токсинов (в случае бактериальных и вирусных инфекций), продуктов распада (в случае системных заболеваний) или различного рода токсических веществ происходит повреждение эндотелиальной ткани сосудистого русла из-за чего происходит активация выработки красных клеточек.
Форма перераспределения
В нормальном состоянии в клеточках селезенки откладывается треть от образуемых тромбоцитов. Как следствие у некоторых видов хронических заболеваний происходит увеличение селезенки в размере. Также увеличивается и способность селезенки депонировать тромбоциты (в некоторых случаях до 100% от общего количества красных клеточек). Увеличение селезенки может быть спровоцировано циррозом, системной волчанкой, онкологией, употреблением алкоголя и некоторыми видами инфекций.
Форма разведения
Развивается у людей, перенесших процедуру переливания большого количества донорской крови, плазмы или иных видов физиологических жидкостей. В итоге концентрация собственных тромбоцитарных клеток снижается до уровня, на котором поддержание нормальной свертываемости крови становится невозможным.
Симптомы
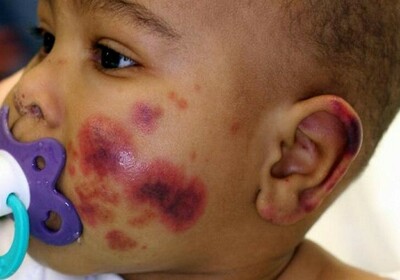
Из-за снижения количества тромбоцитов нарушаются механизмы питания стенок кровеносных сосудов, увеличивая ломкость последних. В определенный момент по причине воздействия каких-либо физических факторов нарушается целостность капилляров, провоцируя сильное кровотечение. Нехватка собственных красных клеточек не дает образоваться тромбоцитарной пробке в поврежденных сосудах, благодаря чему кровь из сосуда изливается в окружающие ткани.
К наиболее часто встречающимся симптомам патологии относят:
- Кровоизлияния под кожу или в слизистые ткани. В результате, чего на теле образуются пятна красного или синего цвета, которые не исчезают при механическом воздействии и не причиняют какого-либо дискомфорта. Размер поражения варьируется от нескольких миллиметров до нескольких сантиметров. Параллельно этому может происходить образование синяков.
- Кровоточивость десен. Проявляется на большой поверхности и не прекращается на протяжении большого промежутка времени.
- Слабость сосудов носоглотки. Причиной носового кровотечения может являться чихание, простудные заболевания, раздражение слизистой носа и микротравмы. Выходящая их носоглотки кровь имеет ярко выраженный артериальный цвет (насыщено красный). Длится кровотечение довольно продолжительное время.
- Проявление крови в моче. Происходит из-за единичных или множественных кровоизлияний в слизистые ткани мочевого пузыря или мочевыводящих путей.
- Внутрижелудочные кровотечения. Являются следствием повышения ломкости сосудов слизистой желудка и кишечника, а причиной возникновения зачастую являются механические травмы.
- Менструальные кровотечения, отличающиеся от обычной интенсивности и длительности.
Диагностика

Базовым симптомом, позволяющим диагностировать наличие патологии у детей и взрослых, является повышение количества тромбоцитов в пробе крови. Однако, для наиболее точной постановки диагноза может потребоваться проведение различного рода дополнительных диагностических процедур, которые можно пройти в большинстве современных медицинских учреждений. К таким анализам относят:
- общий и развернутый анализ крови;
- оценка времени кровотечения по Дьюку;
- забор образца костномозговой ткани (пункция);
- замер времени свертываемости крови;
- генетический анализ (актуален при подозрении на наличие наследственной формы заболевания);
- определение количества антител в пробе крови (исследуется соотношение специфических антител и красных клеточек);
- проведение ультразвуковой диагностики и магнитно-резонансной томографии (дает возможность изучить состояние сосудов и органов, а также определить размер печени и селезенки).
Лечение
Терапию патологии проводит квалифицированный врач-гематолог. Определяющий состав терапии назначается только после проведения всесторонней диагностики и оценки состояния здоровья пациента:
- Легкая тяжесть заболевания (от 50000 до 150000 тромбоцитов на микролитр крови). Стенки капилляров не имеют видимых повреждений, их целостность не нарушена. Значительные по объему кровотечения не наблюдаются. В этой стадии патологию возможно вылечить без применения лекарственных средств. Происходит выявление причины появления болезни. В случае, если причина была устранена, симптомы патологии проходят со временем. Как правило, госпитализация заболевшего не требуется.
- Средняя тяжесть заболевания (от 25000 до 50000 тромбоцитов в микролитре крови). Начинают проявляться кровотечения в ротовую полость и носоглотку. При незначительном воздействии происходит образование синяков и гематом, периодически образуются значительные по размеру кровоподтеки. Существует значительный риск развития внутрижелудочных и внутрикишечных кровотечений. В данном случае, требуется проведение медикаментозной терапии. Лечение проводится в условиях амбулатории.
- Тяжелая степень патологии (количество красных клеточек - 20000 единиц на микролитр и меньше). Могут возникать спонтанные подкожные кровотечения, проявляется геморрагический синдром. В связи с потенциальной опасностью лечение пациента проводится исключительно в условиях стационара.
Медикаментозная терапия

Медикаментозное лечение любой формы патологии направленно на достижение следующих целей:
- купирование кровотечений;
- устранение причины патологии;
- терапия заболевания, спровоцировавшего появление тромбоцитопении.
Наиболее часто для лечения тромбоцитопении используются следующие лекарственные средства:
Немедикаментозная терапия
Лечение заболевания может осуществляться при помощи оперативных и терапевтических методов и мероприятий. Чаще всего врачи-гематологи используют:
- Трансфузионную терапию - переливание больному донорской крови и ее препаратов.
- Резекция селезенки. Селезенка является одним из основных органов, в котором происходит разрушение тромбоцитарных клеток. В особо тяжелых случаях гематолог может прибегнуть к ее полному или частичному удалению, что способствует нормализации уровня тромбоцитов в крови.
- Трансплантация костного мозга. Для того, чтобы избежать отторжения пересаженных клеток, перед проведением процедуры пациенту назначаются препараты, подавляющие клеточный рост.
Терапия при беременности
Лечение патологии у беременных требует аккуратного и грамотного подхода. Зачастую будущим мамам назначают непродолжительные курсы стероидных противовоспалительных препаратов для того, чтобы ускорить рост и формирование плода и спровоцировать досрочное родоразрешение.
В случае неэффективности этого метода применяют внутривенные инъекции иммуноглобулина. За весь период вынашивания плода производят четыре инъекции, и одну сразу после родов. В ситуации, в которой возникает опасность для жизни матери или ребенка прибегают к прямому переливанию донорской крови.
Если вышеуказанные меры не принесли результата, проводится операция по резекции селезенки. Стоит отметить, что операция может быть проведена только в третьем триместре беременности. Наиболее предпочтительным является применение малоинвазивной хирургии.
Вопрос родоразрешения решается индивидуально, исходя из тяжести заболевания и сопутствующих рисков. Наиболее безопасным считается кесарево сечение.
Народные методы лечения
Наиболее эффективным является употребление отвара листьев крапивы, тысячелистника и земляники. Употребляются травы в виде отваров (стакан кипятка, на полстакана листьев).
Также эффективным является употребление кунжутного масла (столовая ложка трижды в день после еды).
Диетическое питание

Больным тромбоцитопенией нет необходимости придерживаться какого-либо конкретного режима питания или отдельной диеты. Однако, для предотвращения возможных осложнений необходимо придерживаться следующих рекомендаций:
- придерживаться принципов рационального питания;
- придерживаться сбалансированного соотношения в рационе всех элементов;
- не употреблять в пищу грубые продукты, чтобы не спровоцировать желудочное кровотечение;
- полностью отказаться от употребления спиртосодержащих напитков и сигарет.
Опасность
Тромбоцитопения несет существенную опасность для здоровья и жизни больного. Болезнь способна привести к возникновению кровоизлияний в мозг (крайне опасно, может привести к летальному исходу), в сетчатку глаза (при неблагоприятном исходе способно привести к потере зрения) или же привести к возникновению анемии.
Профилактика
Профилактика заболевания сводится к постоянному контролю уровня тромбоцитов в крови, а также к выяснению и предотвращению заболеваний, способных спровоцировать ее появление.
Читайте также:


