Токсический гепатит жидкость в брюшной полости
Асцит является следствием цирроза печени в 75%; злокачественных новообразований - в 10%; сердечной недостаточности в 5% случаев.
В клинической картине у пациентов отмечается вздутие живота и прогрессирующее нарастание веса.
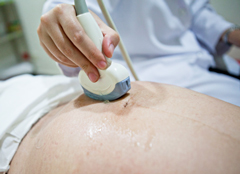
Диагноз основывается на результатах физикального и визуализирующих (рентгенологических, ультразвуковых) методов исследования.
Лечение заключается в назначении бессолевой диеты, диуретиков. Больным может производиться терапевтический лапароцентез, выполняются хирургические вмешательства. Пациенты с асцитом - кандидаты на трансплантацию печени.
Наиболее частым осложнением асцита является спонтанный бактериальный перитонит . Он возникает при инфицировании асцитической жидкости, которое в 90% случаев происходит спонтанно. У больных появляются боли в животе, повышается температура тела.
Для диагностики этого осложнения производится исследование асцитической жидкости. Для лечения спонтанного бактериального перитонита назначаются антибактериальные препараты.
Асцит, который не может быть устранен, или ранний рецидив которого не может быть адекватно предотвращен лечением.
- Асцит, резистентный к диуретикам: асцит, рефрактерный к диете с ограничением натрия и интенсивной терапии диуретиками ( спиронолактон 400 мг/день, фуросемид 160 мг/день в течение не менее 1 недели; диета с ограничением поваренной соли менее 5,2 г/день).
- Асцит, не контролированный диуретиками: асцит, рефрактерный к терапии из-за развития вызванных диуретиками осложнений, которые препятствуют применению эффективных дозировок диуретиков.
Примерно у половины пациентов с циррозом печени асцит развивается в течение 10 лет от начала заболевания. Он обусловлен нарушениями почечной функции, портального и висцерального кровообращения.
Примерно 50% пациентов с цирротическим асцитом умирают в течение 2 лет от начала заболевания. Показатели однолетней выживаемости у больных с асцитом, резистентным к терапии, составляют 50%.
У здоровых мужчин внутриперитонеальная жидкость обнаруживается в меньших количествах, чем у женщин, у которых ее объем составляет примерно 20 мл (в зависимости от фазы менструального цикла). При асците этот объем значительно увеличивается.
Частота возникновения спонтанного бактериального перитонита составляет 15-20%.
Непеченочными причинами асцита могут быть: заболевания сердца ( сердечная недостаточность , констриктивный перикардит), злокачественные новообразования (карциноматоз, псевдомиксома брюшины), заболевания брюшины (инфекционный перитонит), выраженная гипоальбуминемия (нефротический синдром), другие болезни (опухоли и кисты яичников, панкреатит , саркоидоз , системная красная волчанка, микседема).
Факторы риска возникновения асцита:
- Факторы риска при отсутствии патологических процессов в брюшине.
- Портальная гипертензия (градиент концентрации альбумина сыворотка-асцит ≥11 г/л).
- Цирроз печени .
- Алкогольный гепатит.
- Фулминантная печеночная недостаточность.
- Метастазы в печень .
- Хроническая сердечная недостаточность .
- Констриктивный перикардит .
- Синдром Бадда-Киари .
- Обструкция нижней полой вены.
- Гипоальбуминемия (градиент концентрации альбумина сыворотка-асцит 11г/л) и другими причинами (градиент концентрации альбумина сыворотка-асцит 225 мЕ/мл (или выше верхней границы нормы для сыворотки крови).
Клинически различают две формы рефрактерного асцита:
- Асцит с ежедневной потерей менее чем 200 г массы тела (несмотря на ограничения натрия) и прием 400 мг спиронолактона (Верошпирон) или 30 мг амилорида (Амипразид, Арумил, Мидамор), а также 160 мг фуросемида (Лазикс) в течение 2 недель.
- Асцит, который невозможно контролировать; рецидивирующий асцит, обострения которого невозможно предупредить, назначая диуретики в дозах, не вызывающих побочных явлений.
- Основные диагностические критерии гепаторенального синдрома:
- Гепаторенальный синдром развивается у пациентов с хроническими или острыми заболеваниями печени, выраженной печеночной недостаточностью, портальной гипертензией и асцитом.
- Существуют два варианта течения гепаторенального синдрома.
- Синдром первого типа характеризуется прогрессирующим течением: быстрым нарастанием симптомов почечной недостаточности. Диагностика синдрома первого типа производится на основании увеличения почти вдвое содержания сывороточного креатинина (более чем 1,5 мг/дл) или 50%-ным снижением суточного клиренса креатинина (менее 40 мл/мин) в течение 2 недель. Пациенты с синдромом первого типа нуждаются в трансплантации печени. В противном случае синдром заканчивается летально у 90% больных.
- Для синдрома второго типа характерно медленно прогрессирующее течение.
- Отсутствие шока, текущей бактериальной инфекции, данных о приеме нефротоксических препаратов, отсутствие диареи и рвоты, потери жидкости с почками (снижение веса более чем на 500 г в течение нескольких дней у пациентов с асцитом без периферических отеков и более 1 кг/сут у больных с периферическими отеками).
- Отсутствие улучшения почечной функции (сохранение уровня сывороточного креатинина более чем 1,5 мг/дл и суточного клиренса креатинина менее 40 мл/мин) после назначения диуретиков и увеличения объема плазмы за счет введения 1,5 л изотонического раствора.
- Протеинурия менее 500 мг/дл и отсутствие ультразвуковых признаков поражения почечной паренхимы или обструктивной уропатии.
- Дополнительные диагностические критерии гепаторенального синдрома:
- Объем суточной мочи менее 500 мл/сут.
- Концентрация натрия в моче менее 10 мЭкв/л.
- Осмолярность мочи выше, чем осмолярность крови.
- Концентрация натрия в сыворотке крови менее 130 мЭкв/л.
- Количество эритроцитов в моче более 50 в поле зрения.
- Цели лечения
- Улучшение самочувствия.
- Устранение причин асцита.
- Повышение качества жизни.
Постельный режим и ограничение потребления натрия являются эффективными терапевтическими мероприятиями у 10% пациентов с асцитом.
Ограничения в диете и лечение диуретиками оказывают терапевтический эффект у 90% пациентов с асцитом. При отсутствии эффекта или при выраженном асците необходимо стационарное лечение.
Больные с асцитом, не получающие диуретиков, ежедневно экскретируют почками примерно 20 ммоль/сут натрия.
Отрицательный баланс натрия может быть достигнут благодаря ограничению потребления натрия с пищей до 22 ммоль/сут, что затруднительно для больных. Как правило, удается поддерживать количество натрия в пище в количестве 44 ммоль/сут.
В пищевом рационе пациентов с асцитом должны содержаться низкие количества соли (1-1,5 г/сут или 40-60 ммоль/сут).
Ограничения объемов потребления жидкости (до 1 л/сут) показаны больным с цирротическим асцитом при условии гипонатриемии (содержание натрия в сыворотке крови
![]()
Боль в животе, метеоризм, отрыжка и изжога, затрудненное дыхание, отеки ног — все это может свидетельствовать о наличии асцита брюшной полости.
![]()
На ранних стадиях асцит брюшной полости протекает незаметно. Зачастую люди думают, что просто набирают вес.
![]()
Магнитно-резонансная томография органов брюшной полости позволяет распознать опухолевые и воспалительные процессы, увидеть кисты.
![]()
Скидка на магнитно-резонансную томографию в выходные и праздничные дни!
![]()
Ультразвуковое исследование органов брюшной полости позволяет оценить их форму, размеры и расположение, выявить существующие патологии.
![]()
Чем раньше диагностировать асцит и начать лечение, тем выше шансы на выздоровление.
![]()
Спецпредложения, скидки и акции помогут существенно сэкономить на медицинском обследовании.
![]()
![]()
![]()
Асцит, который иногда называют водянкой живота, — это не отдельная болезнь, а осложнение целого ряда самостоятельных заболеваний. И практически все они крайне опасны для здоровья и жизни. Как диагностируют асцит брюшной полости, из-за чего он возникает и можно ли его вылечить?
Асцит: болезнь или симптом?
Патологическое скопление жидкости в брюшной полости называется асцитом. Небольшое количество асцитической жидкости присутствует в полости брюшины всегда. Эта жидкость постоянно перемещается в лимфатические сосуды, а ее место занимает новая, и это совершенно естественный процесс. Но при некоторых нарушениях в работе организма эта жидкость либо начинает вырабатываться в избыточном количестве, либо перестает всасываться. В результате она постепенно накапливается и начинает давить на внутренние органы, ухудшая их функционирование.
Список заболеваний и нарушений, при которых может возникнуть асцит, весьма внушителен. Среди них:
- цирроз печени;
- некоторые онкологические заболевания;
- туберкулез;
- панкреатит;
- сердечная недостаточность;
- эндометриоз, кисты и опухоли яичников;
- внутренние кровотечения;
- заболевания почек;
- недоедание и истощение;
- заболевания эндокринной системы.
Однако, если у человека диагностируют асцит брюшной полости, первыми на подозрении у врачей обычно оказываются цирроз печени (причина 75% случаев асцита), онкологические заболевания (10% случаев) и сердечная недостаточность (5% случаев). На все остальные заболевания вместе взятые приходится лишь 10% случаев асцита брюшной полости.
Конечно, асцит возникает далеко не у всех людей, страдающих вышеуказанными заболеваниями. Однако существуют факторы риска, повышающие шансы развития асцита: алкоголизм, наркомания, гепатиты, ожирение и высокий уровень холестерина, а также сахарный диабет.
Асцит брюшной полости чаще всего развивается постепенно, на протяжении многих месяцев, и потому большинство пациентов очень долго не обращают на него внимания. Зачастую люди просто думают, что набирают вес.
На ранних стадиях заметить асцит действительно сложно: нужно, чтобы собралось не менее литра жидкости. Лишь после этого начинают проявляться типичные симптомы асцита брюшной полости: боль в животе, метеоризм, отрыжка и изжога, затрудненное дыхание, отеки ног. По мере увеличения объема жидкости живот тоже увеличивается, вскоре человеку становится сложно наклоняться. Живот приобретает форму шара, могут появиться растяжки и расширенные вены.
Но для того, чтобы поставить диагноз, мало внешних признаков — необходимо проконсультироваться с врачом.
Она начинается с визуального осмотра и пальпации живота. Опытный врач может диагностировать асцит уже на основании только этих данных, однако для уточнения требуются более точные методы. Недостаточно знать, что у пациента асцит — гораздо важнее выяснить, что его вызвало.
При подозрении на асцит назначается УЗИ брюшной полости и грудной клетки — оно позволяет увидеть как асцит, так и новообразования или изменения в структуре печени. Иногда назначается также и допплерография, показывающая состояние вен.
Рентгенография — еще один метод, широко применяемый в диагностике асцита. Это обследование дает возможность выявить туберкулез или увеличение размеров сердца, которые могут быть причиной скопления жидкости в брюшной полости.
МРТ и КТ — очень точные диагностические методы, которые позволяют увидеть наличие жидкости даже там, где его сложно рассмотреть при УЗИ и рентгенографии.
В некоторых случаях врач может направить пациента на лапароскопию, при которой производится прокол брюшной стенки и скопившаяся жидкость берется на анализ. Проводятся также биохимический анализ крови и анализ мочи.
Лечение асцита всегда начинается с лечения основного заболевания, вызвавшего скопление жидкости.
- При асците, вызванном сердечными заболеваниями, назначают сосудорасширяющие препараты, мочегонные и гликозиды.
- При почечных болезнях показаны низкосолевая диета и ограничение потребления жидкости.
- При нарушениях белкового обмена назначается диета с оптимальным содержанием белка и переливание альбумина.
- При циррозе применяют гепатопротекторы.
В дополнение к этому назначают симптоматическую терапию:
- низкосолевую диету (не более 2 г соли в сутки), а в некоторых случаях — вовсе бессолевой рацион. Если причиной асцита стал цирроз, следует также ограничить потребление жидкости;
- препараты калия и мочегонные средства.
Во время лечения врач следит за изменениями в состоянии пациента и, в особенности, — за его весом. Если выбранные терапевтические меры работают, потеря веса должна составлять около 500 граммов в сутки.
Если консервативные методы по каким-либо причинам не дают ожидаемого результата, показано хирургическое вмешательство. Нередко при асците проводят удаление жидкости путем постепенного дренажа (если ее количество значительно). Хирург делает небольшой прокол в брюшине и вставляет в него дренажную трубку (лапароцентез).
Альтернативой этому болезненному и сопряженному с большими рисками для здоровья методу является установка постоянных катетеров и подкожных портов. В результате асцитическая жидкость удаляется по мере ее накопления. Этот подход значительно облегчает жизнь пациентам, позволяет исключить необходимость повторных проколов, а значит — снизить риск повреждения внутренних органов и воспалений.
Установка системы представляет собой несложную хирургическую операцию, в процессе которой врач вводит конец катетера (изготавливается из гипоаллергенных материалов) в брюшную полость, сам же порт (он изготовлен из титана) устанавливается подкожно в области реберной дуги. Чтобы эвакуировать скопившуюся в брюшной полости жидкость, необходимо проткнуть кожу и силиконовую мембрану камеры порта специальной иглой. Через нее и откачивается асцитическая жидкость. Подобным способом можно ввести лечебные препараты.
Иногда требуется так называемое внутрипеченочное шунтирование, при котором врач создает сообщение между печеночной и воротной веной.
В тяжелых случаях может потребоваться пересадка печени.
Чем раньше асцит будет диагностирован и начнется лечение, тем выше шансы на успех. Избавиться от асцита на ранних стадиях намного проще. Но есть некоторые факторы, которые негативно влияют на эффективность терапии, — это пожилой возраст, сахарный диабет, гипотония, онкологические заболевания (и особенно рак печени), перитонит, а также пониженный уровень альбумина.
Асцит смертельно опасен. Примерно в 50% случаев, если назначение диуретиков не помогает, развитие асцита заканчивается трагически. Особенно опасен асцит при раке — летальный исход вероятен примерно в 60% случаев.
Следует помнить о том, что асцит всегда ухудшает течение основного заболевания, вызывая дыхательную недостаточность, гидроторакс, грыжи, непроходимость кишечника и массу других осложнений.
Даже если асцит удалось вылечить, следует очень внимательно относиться к своему здоровью, так как всегда есть риск рецидивов. Поэтому даже после излечения асцита следует придерживаться назначенной врачом диеты.
Скопление жидкости в брюшной полости может вызывать сильный дискомфорт, но еще до того, как это произойдет, проявляются другие симптомы. Оставлять их без внимания не следует — обязательно обратитесь к врачу.
«Асцит — серьезное осложнение, свидетельствующее о том, что лечение основного заболевания затягивать нельзя. Однако это заболевание зачастую нужно еще правильно диагностировать, ведь многие склонны не обращать внимания на отеки, метеоризм и другие симптомы и откладывать визит к врачу до последнего. Поскольку в этом случае на постановку диагноза остается мало времени, имеет смысл обратить внимание на коммерческие медицинские центры, где вас могут оперативно принять.
Если верить американским врачам, ежегодно только в США от цирроза печени погибает 49 500 человек. В России цирроз печени находится на 7 месте среди причин смерти, всего — 47 200 случаев в год [1] . Отчего возникает эта грозная болезнь, как ее избежать и можно ли повернуть процесс вспять — читайте в нашей статье.
Цирроз печени: характеристика заболевания и стадии его развития
Цирроз печени — хроническое прогрессирующее заболевание, в основе которого постепенная гибель клеток печени (гепатоцитов), избыточное разрастание нефункциональной соединительной ткани и активное деление сохранившихся гепатоцитов. Это ведет к нарушению нормального строения органа, невозможности выполнять функции (развитию печеночной недостаточности) и изменению внутрипеченочного кровотока.
В экономически развитых странах цирроз печени входит в шесть основных причин смерти для возраста 35–60 лет. Ежегодно заболеваемость увеличивается на 3,7% [2] .
Цирроз может стать исходом любого хронического воспаления печеночной ткани. Само же воспаление может быть вызвано множеством причин, начиная от вирусов и заканчивая неправильным питанием. Избыток жиров и легко усваиваемых углеводов в пище ведет к избыточному накоплению жира в гепатоцитах (стеатоз), что может стать причиной развития воспаления (стеатогепатит). Независимо от внешней причины, вызвавшей воспаление (вирусов, лекарств, неправильного питания — подробно об этом далее), в тканях печени активируются так называемые звездчатые клетки, которые начинают синтезировать коллаген, то есть соединительную (фиброзную) ткань, которая, собственно, и нарушает нормальную работу печени.
Получившаяся фиброзная ткань:
- препятствует обмену веществ между кровью и гепатоцитами;
- нарушает питание клеток печени;
- скапливаясь вокруг мелких сосудов, усиливает сопротивление току крови, что повышает давление в системе воротной вены (переносящей кровь от органов брюшной полости в печень);
- нарушает отток желчи.
Эти изменения приводят к печеночной недостаточности и портальной гипертензии — повышению давления в системе воротной вены.
В развитии болезни выделяются 3 стадии:
- Начальная: на фоне выраженных патоморфологических изменений симптомы минимальны.
- Стадия выраженных клинических проявлений, когда разворачивается типичная картина заболевания.
- Терминальная: появляются необратимые изменения во всех органах и системах, что приводит к летальному исходу.
Основные осложнения цирроза печени:
Основные причины развития цирроза:
- злоупотребление алкоголем (по данным разных источников от 30 до 80% случаев) [3] ;
- хронические вирусные гепатиты (В, С) — до 40% случаев;
- болезни желчных путей, приводящие к застойным явлениям;
- химические и лекарственные интоксикации;
- хронический дефицит белков и витаминов в пище;
- крайне редко — врожденные нарушения обмена веществ.
Исходя из причин возникновения циррозы делятся на:
- алкогольный;
- вирусный;
- лекарственно индуцированный;
- метаболический — вызванный генетически обусловленными аномалиями обмена веществ;
- первичный билиарный цирроз;
- вторичный билиарный цирроз;
- застойный;
- аутоиммунный;
- криптогенный (причина не установлена).
Крайне трудно провести грань между начавшимся фиброзом и развитием цирроза печени. Несмотря на то, что гистологически (при исследовании биоптата печеночной ткани) выделяют 4 степени фиброза, появление развернутой клинической картины, как правило, говорит о финальной стадии процесса фиброзирования: циррозе — состоянии окончательно необратимом.
Далее проявляется комплекс симптомов, которые врачи называют диспептическим:
К этим признакам может присоединяться ноющая боль и тяжесть в правом подреберье.
Поскольку печень — главный орган, синтезирующий белки организма, в том числе и белки, регулирующие свертываемость крови, по мере прогрессирования болезни развивается геморрагический синдром:
- кровоточивость десен;
- носовые, маточные кровотечения;
- беспричинные гематомы (синяки);
- точечные подкожные кровоизлияния в виде сыпи (экхимозы);
- желудочные, кишечные кровотечения;
- кровотечения из варикозно расширенных вен пищевода.
Постепенно снижается вес, вплоть до кахексии (т. е. истощения). Из-за асцита начинает расти живот, появляются отеки на ногах, лице — из-за дефицита белка. Накопление токсинов вызывает энцефалопатию.
В зависимости от состояния больного выделяют четыре стадии печеночной энцефалопатии:
Врач при обследовании больного циррозом может увидеть:
- увеличение печени и селезенки;
- желтуху;
- сосудистые звездочки и расширенные вены на передней брюшной стенке;
- геморрагические высыпания;
- ярко-красные ладони (пальмарную эритему);
- признаки гормональных расстройств (гинекомастия, атрофия яичек).
При первых же симптомах нужно обратиться к врачу-терапевту, который порекомендует основные лабораторные исследования и с их результатами переадресует пациента к гастроэнтерологу, по возможности — специализирующемуся на болезнях печени (врачу-гепатологу). При появлении признаков печеночной энцефалопатии необходима консультация невролога.
Единственный радикальный метод лечения цирроза печени — трансплантация органа. Вовремя начатая медикаментозная терапия позволяет замедлить процесс и поддержать нарушенные функции.
По возможности необходимо устранить причину цирроза: отказаться от алкоголя, провести противовирусную терапию. Очень важен щадящий образ жизни без чрезмерных физических и психоэмоциональных нагрузок, полноценный сон.
Необходимо строго соблюдать диету: ограничить животные белки, восполняя их недостаток молочными продуктами, белки которых легче усваиваются. Суточное количество белка должно быть не менее 60 г, а при отсутствии печеночной энцефалопатии — 80–100 г. Суточная калорийность — 1800–2500 ккал. Если говорить о калорийности в целом, она тем выше, чем моложе пациент и чем выше его физическая активность. Обязательно наличие в рационе пищевых волокон, клетчатки: овощей, фруктов, цельных злаков, отрубей. Пищевые волокна не только способствуют развитию нормальной микрофлоры, которая активно участвует в пищеварении, но и способны всасывать токсические вещества. Питание 5–6-разовое. При появлении отеков ограничивается соль.
Используемые группы медикаментов:
Цирроз печени — опасное заболевание. Но если выявить проблему на ранних стадиях, можно надолго замедлить его развитие. Внимательное отношение к своему здоровью и регулярные обследования помогут улучшить качество и продолжительность жизни при обнаруженном фиброзе.
![]()
![]()
Воспалительные процессы в печени могут привести к циррозу.
, MD, Sidney Kimmel Medical College at Thomas Jefferson University
Last full review/revision January 2018 by Steven K. Herrine, MD
Этиология
Причиной асцита могут быть заболевания печени, обычно хронические, но иногда и острые, также асцит может быть обусловлен причинами, не связанными с патологией печени.
Печеночные причины включают следующие:
Портальная гипертензия (которая составляет > 90% всех случаев заболеваний печени), обычно вследствие цирроза печени
Обструкцию печеночной вены (например, синдром Бадда – Киари)
При тромбозе воротной вены асцит обычно не возникает, за исключением случаев сопутствующего гепатоцеллюлярного повреждения.
Внепеченочные причины включают следующие:
Генерализованную задержку жидкости, связанную с системными заболеваниями (например, сердечная недостаточность, нефротический синдром, тяжелая гипоальбуминемия, констриктивный перикардит)
Заболевания брюшины (например, карциноматозный или инфекционный перитонит, утечка желчи, вызванная хирургическим вмешательством или другими медицинскими процедурами)
Более редкие причины – это почечный диализ, панкреатит, системная красная волчанка и эндокринные нарушения (например, микседема)
Патофизиология
Механизмы комплексные и выяснены не до конца. Факторы включают расширение сосудов внутренних органов, спровоцированное выделением оксида азота, изменение сил Старлинга в портальных сосудах (низкое онкотическое давление из-за гипоальбуминемии и повышенное портальное венозное давление), патологическую задержку натрия в почках (концентрация натрия в моче обычно 5 мЭкв/л) и, возможно, повышенную продукцию лимфы в печени.
Механизмы, которые, вероятно, участвуют в задержке натрия почками, включают активацию ренин-ангиотензин-альдостероновой системы; повышение симпатического тонуса; внутрипочечное шунтирование с оттоком крови от коркового слоя; повышенное образование оксида азота и изменения в формировании или метаболизме АДГ, кининов, простагландинов и предсердного натрий-уретического фактора. Спланхническая артериальная вазодилатация может служить триггером, определенные роли и взаимодействия этих патологических изменений остаются неуточненными.
Клинические проявления
Малые количества асцитической жидкости не вызывают каких-либо симптомов. Умеренное ее количество приводит к увеличению объема живота и прибавке в весе. Большое количество жидкости может вызвать неспецифическое чувство распирания, но реальная боль встречается редко и предполагает другую причину острой абдоминальной боли. Если асцит приводит к высокому стоянию диафрагмы, то может возникнуть одышка. Симптомы спонтанного бактериального перитонита (СБП) могут включать появление новых жалоб на дискомфорт в животе и лихорадку.
Клинические признаки асцита включают притупление звука при перкуссии живота и ощущение флюктуации при физикальном исследовании. Объемы 1 500 мл могут не выявляться при объективном обследовании. Массивный асцит вызывает напряжение брюшной стенки и уплощение пупка. При заболеваниях печени или брюшины обычно наблюдается изолированный асцит, либо он диспропорционален перифирическим отекам; при системных заболеваниях (например, при сердечной недостаточности) обычно встречается обратная ситуация.
Диагностика
УЗИ или КТ, если очевидных физикальных признаков недостаточно
Часто исследование параметров асцитической жидкости
Диагноз может основываться на физикальном осмотре в случае большого количества жидкости, но визуальные методы исследования более чувствительны. УЗИ и КТ определяют гораздо меньшие объемы жидкости (100–200 мл), чем физикальный осмотр. Также должно возникать подозрение на СБП, если у пациента имеется асцит с абдоминальной болью, лихорадкой или наблюдается необъяснимое ухудшение состояния.
Диагностический абдоминальный парацентез следует проводить в любых нижеперечисленных случаях:
впервые диагностированного асцита;
Причина его возникновения не известна.
подозрении на СБП.
Эвакуируется и анализируется приблизительно 50–100 мл жидкости для общего внешнего осмотра, определения содержания белка, подсчета клеток и определения их видов, посева на культуру, и при клинических показаниях проводятся цитология и специальные исследования на кислотоустойчивые микроорганизмы и/или амилазу. По контрасту с асцитом, обусловленным воспалением или инфекцией, асцит при портальной гипертензии характеризуется чистой соломенного цвета жидкостью с низким содержанием белка и полиморфонуклеарных лейкоцитов ( 250 клеток/ μ мкл) и, что наиболее надежно, высоким сывороточно-асцитическим альбуминовым градиентом (СААГ), который представляет собой разницу уровня сывороточного альбумина и уровня альбумина асцитической жидкости. СААГ ≥ 1,1 г/дл относительно специфичен для асцита, вызванного портальной гипертензией. Если асцитическая жидкость мутная и количество полиморфонуклеарных лейкоцитов > 250 клеток/ мкл , то это указывает на СБП, в то время как жидкость с примесью крови дает основания предполагать опухоль или туберкулез. Редкий, подобный молоку (хилезный) асцит является чаще всего признаком лимфомы или окклюзии лимфатического протока.
Лечение
Диета с ограничением потребления натрия
Иногда спиронолактон, возможно, с добавлением фуросемида
Иногда терапевтический парацентез
(См. также Практическое руководство Американской ассоциации по изучению заболеваний печени у взрослых пациентов с асцитом по причине цирроза [AASLD practice guideline Management of Adult Patients with Ascites Due to Cirrhosis]).
Диета с ограничением натрия (2000 мг/день) – это первый и наиболее безопасный метод лечения асцита, связанного с портальной гипертензией. Диуретики должны применяться в случае, если диета с ограничением натрия в течение нескольких дней оказалась неэффективной. Обычно эффективен спиронолактон (в пероральной дозе от 50 мг 1 раз/день до 200 мг 2 раза/день). Петлевой диуретик (например, фуросемид 20–160 мг обычно 1 раз/день или 20–80 мг 2 раза/день) должен быть добавлен при неэффективности спиронолактона. Так как спиронолактон может вызывать задержку калия, а фуросемид, наоборот, способствует его выведению, комбинация этих препаратов часто приводит к оптимальному диурезу с низким риском отклонений в содержании калия. Ограничение в приеме пациентом жидкости показано только при лечении гипонатриемии (сывороточный натрий 120 мЭкв/л).
Изменения веса тела пациента и количества натрия в моче отражают реакцию на лечение. Уменьшение веса примерно на 0,5 кг/день является оптимальным, так как асцитная жидкость не может выводится быстрее. Более агрессивный диурез уменьшает объем внутрисосудистой жидкости, особенно когда периферические отеки отсутствуют; это истощение может вызвать почечную недостаточность или электролитный дисбаланс (например, гипокалиемию), что может спровоцировать портосистемную энцефалопатию. Неадекватное уменьшение количества натрия в диете – обычная причина персистирующего асцита.
Альтернативой является терапевтический парацентез. Удаление 4 литров/день безопасно; многие клиницисты назначают внутривенное введение бессолевого альбумина (примерно 40 г при проведении парацентеза) для предотвращения циркуляторных нарушений. Даже однократный тотальный парацентез может быть безопасным. Лечебный парацентез сокращает время пребывания больного в стационаре с относительно малым риском развития электролитного дисбаланса или почечной недостаточности; тем не менее пациентам требуется постоянный прием мочегонных, а также у них имеется тенденция к задержке жидкости быстрее, чем у тех, кому парацентез не проводился.
Методы аутологичной инфузии асцитической жидкости (например, LeVeen брюшинно-венозный шунт) часто вызывают осложнения и, как правило, больше не используются. Трансъюгулярное внутрипеченочное портосистемное шунтирование (ТВПШ) может снизить портальное давление и оказывает положительный эффект на резистентный к другим методам лечения асцит, ноТВПШ – инвазивный метод, который может вызвать осложнения, включающие портосистемную энцефалопатию и ухудшение гепатоцеллюлярной функции.
(См. также Практическое руководство Американской ассоциации по изучению заболеваний печени - "Роль трансяремного внутрипеченочого портосистемного шунта в лечении портальной гипертензии" [the American Association for the Study of Liver Diseases practice guideline The Role of Transjugular Intrahepatic Portosystemic Shunt (TIPS) in the Management of Portal Hypertension: Update 2009])
Основные положения
Асцит – это наличие свободной жидкости в брюшной полости, чаще обусловленное портальной гипертензией, а иногда другими печеночными и внепеченочными причинами.
При умеренном количестве жидкости может отмечаться увеличение окружности живота и массы тела, а большое количество жидкости приводит к растяжению живота, ощущению распирания и одышке; клинические признаки могут отсутствовать, если количество асцитической жидкости составляет
- Портальная гипертензия (градиент концентрации альбумина сыворотка-асцит ≥11 г/л).
Читайте также: