Последствия лечения гепатита с пегинтроном
Т.Н. Лопаткина, ММА им. И.М. Сеченова
Изучение эффективности противовирусной терапии (ПВТ) хронического гепатита С (ХГС) и внедрение перспективных методов лечения в последнее десятилетие позволило повысить уровень устойчивого ответа с 6% при использовании препаратов интерферона альфа-2Ь (ИФН альфа-2b А) в стандартном режиме (3 млн ME 3 раза в неделю в течение 6 мес) до 61% при комбинированной терапии ПегИФН альфа-2b и Рибавирином в течение 12 мес 1.
Двадцатилетний опыт лечения ХГС противовирусными препаратами показал недостаточную эффективность монотерапии интерфероном альфа (ИФНа): при 6-месячном курсе устойчивый биохимический и вирусологический ответ с отсутствием RNA HCV в сыворотке крови спустя 6 мес после окончания ПВТ отмечался лишь у 6-10% больных ХГС, вызванного различными генотипами вируса гепатита С (HCV). Увеличение продолжительности лечения ИФН альфа-2b в стандартном режиме 3 млн ME 3 раза в неделю до 12 мес позволило в среднем добиваться устойчивого ответа у 15-30% пациентов 9. Строгий подбор "идеального" кандидата для ПВТ с учетом низкой вирусной нагрузки, не 1-го генотипа HCV, молодого возраста, женского пола и небольшой массы тела пациента; отсутствием синдрома перегрузки железом, признаков цирроза печени при морфологическом ее исследовании и коинфекции другими вирусами (ВИЧ, HBV, вирусами герпесгруппы и др.), непродолжительного срока заболевания обеспечивал более высокий устойчивый ответ (30-40%) в группе больных, получавших монотерапию ИФНα.
С середины 90-х годов прошлого века предпочтение в лечении ХГС стали отдавать комбинированной терапии ИФНα и рибавирином - синтетическим аналогом нуклеозидов (коммерческое название Рибавирин). В работах ряда авторов [3, 10] показано, что можно прогнозировать успех лечения ХГС на основании результатов определения уровней RNA HCV после первого месяца лечения. А. Bellobuono и соавт. [10] рандомизировали 60 больных ХГС после первого месяца монотерапии ИФНα в стандартном режиме на три группы: продолжавших лечение ИФНа 3 млн ME 3 раза в неделю, если у них исчезла RNA HCV в сыворотке; получавших ИФНα в стандартном режиме в сочетании с Рибавирином 1000 мг/сут или двойную дозу ИФНα (6 млн ME 3 раза в неделю) - если спустя месяц после ПВТ отсутствовал ранний вирусологический ответ на монотерапию.
После 4 недель терапии 20% пациентов имели вирусологический ответ, а 80% пациентов остались позитивными по RNA HCV. Устойчивый ответ наблюдался у 42% больных с ранним вирусологическим ответом, у 42% - без раннего вирусологического ответа, получавших ИФНа и Рибавирин и только у 4% пациентов, получавших двойную дозу ИФНα (р = 0,006). Авторы отметили эффективность включения в терапию ИФНа Рибавирина и недостаточную эффективности удвоения дозы ИФНа, если не наблюдалось исчезновения RNA HCV на ранних этапах терапии. Превалирование при ХГС пациентов с 1Ь генотипом HCV и наличие у них низкого ответа на монотерапию ИФНа позволили рекомендовать комбинированное применение ИФНα и Рибавирина как терапию выбора при первоначальном лечении, а также для лечения не ответивших больных или с обострением после монотерапии. Отмечено, что комбинированная терапия Рибавирином и ИФНα в высоких дозах превосходит результаты монотерапии высокими дозами ИФНα у больных ХГС, инфицированных генотипом lb HCV[11].
S. Pol и соавт. [11] рандомизировали 307 пациентов с ХГС 1Ь генотипа в 3 группы: А - получавших 6 млн ME ИФНα 3 раза в неделю в течение 6 мес и 3 млн ME 3 раза в неделю в последующие 6 мес; В - 10 млн ME ИФНα 3 раза в неделю в течение 3 мес, 6 млн ME 3 раза в неделю - 3 мес, 3 млн ME 3 раза в неделю в течение последующих 6 мес; С - ИФНα по схеме группы А в комбинации с Рибавирином в течение 4,6 или 12 мес. Устойчивый вирусологический ответ спустя 6 мес после окончания ПВТ достоверно чаще отмечен в группе С, чем в группах А или В (32,8%, 16,9% и 14,1% соответственно, р 10,6 мг/кг Рибавирина
3 млн. ME ИФН альфа-2b А +
> 10,6 мг/кг Рибавирина
Включенные
в лечение
> или = 80%
полученного
лечения *
Включенные
в лечение
> или = 80%
полученного
лечения *

Хронический вирусный гепатит С (ХВГС) – заболевание, имеющее высокую медико-социальную значимость и связанное с высокой распространенностью, трудностями диагностики, лечения и серьезными осложнениями. ХВГС страдают около 170 млн. человек в мире. ХВГС – самая частая причина пересадки печени и заболеваемости гепатоцеллюлярным раком. Ежегодно от осложнений терминальной стадии цирроза печени, ассоциированного с ВГС, умирают около 500 тыс. человек [1].
Учитывая большое число инфицированных пациентов и вероятное увеличение распространенности ХВГС в будущем, на протяжении следующих нескольких десятилетий в России можно ожидать постоянного роста заболеваемости, смертности и затрат на лечение. Однако эту тенденцию можно изменить, если больные ХВГС будут обеспечены противовирусными препаратами.
В России имеется большое число больных с установленным диагнозом ХВГС, однако частота противовирусной терапии относительно низкая по сравнению с другими европейскими странами [1]. Низкая частота противовирусной терапии обусловлена различными причинами. Главная из них – низкая доступность противовирусных препаратов для пациентов.
С момента открытия интерферонов именно α-интерферон стал одним из главных агентов противовирусной терапии ХВГС. Затем в практику вошла его комбинация с ребетолом (рибавирином), позднее появились пегилированные аналоги α-интерферон (ПЕГ-ИФН-α), которые также применяются в сочетании с ребетолом [3]. Стандартом лечения ХВГС, вызванного, например, вирусом 1-го генотипа, служит применение ПЕГ-ИФН-α и ребетола (рибавирина) в течение 48 недель, что обеспечивает устойчивый вирусологический ответ (УВО) приблизительно у 40–76 % пациентов. Эту терапию может себе позволить не каждый пациент, из-за её дороговизны.
Появление новых недорогих противовирусных препаратов может привести к увеличению доли больных, получающих противовирусную терапию и, самое главное, снизить затраты на лечение.
Было интересно выявить эффективность клинического применения пегинтрона и альгерона, а так же сравнить их эффективность между собой для лечения хронического вирусного гепатита С у больных находящихся на лечении в областной клинической инфекционной больнице и в областном центре по профилактике и борьбе со СПИД и инфекционными заболеваниями г. Воронежа.
Цель исследования: оценка эффективности клинического применения пегинтрона и альгерона в комплексной терапии больных ХГС, находящихся на лечении в областной клинической инфекционной больнице и в областном центре по профилактике и борьбе со СПИД и инфекционными заболеваниями г. Воронежа.
Задачи исследования
1) изучить влияние комбинированной противовирусной терапии препаратами пегинтрон и ребетол на лабораторные параметры у больных с ХВГС.
2) оценить эффективность комбинированного использования противовирусной терапии отечественными препаратами альгерон и ребетол у пациентов с ХВГС на фоне базисного лечения.
3) исследовать сравнительную эффективность комбинированной противовирусной терапии препаратами пегинтрон и ребетол с препаратами альгерон и ребетол у пациентов с ХВГС.
Материалы и методы исследования
Первая группа – 25 историй болезни за 2014 год, из которых 12 мужчин и 13 женщин в возрасте от 24 до 57 лет. У 15 пациентов генотип 1в, у 10 пациентов – 3а.
Первая группа пациентов получали комбинированную противовирусную терапию: ПегИнтрон (Шеринг-Плау, Бельгия) 120-150 мкг п/к 1 раз в неделю (в зависимости от массы тела) + ребетол 800-1200 мг/сут per os, разделенной на 2 приема (назначался в зависимости от массы тела).
Вторая группа – 25 историй болезни за 2015 год, из которых 13 мужчин и 12 женщин в возрасте от 27 до 54 лет. У 12 пациентов был генотип 1в HCV, у 13 пациентов – 3а.
Вторая группа пациентов получали комбинированную противовирусную терапию: альгерон (BIOCAD, Россия) 100-150 мкг п/к 1 раз в неделю (в зависимости от массы тела) + ребетол 800-1200 мг/сут per os, разделенной на 2 приема (назначался в зависимости от массы тела).
Помимо общеклинических методов обследования, у всех больных проводилось полное серологическое обследование на маркеры вирусных гепатитов В, С, D с использованием методов ИФА и молекулярной диагностики (ПЦР). ПЦР-диагностика проводилась в режиме real-time, чувствительность использованных тест-систем (РНК HCV Амплисенс) составляла 50 копий/мл. У каждого пациента определялся также генотип HCV и количественное определение РНК HCV в крови. Всем больным выполнялись ФГС и УЗИ органов брюшной полости утром натощак. Для выявления фиброза печени всем больным была также проведена фиброэластометрия ткани печени на фиброскане (Fibroscan FS-502, Echosens, Франция).
У всех обследованных до начала терапии отсутствовали изменения со стороны системы кроветворения, функции почек, щитовидной железы, отмечали нормальный уровень тиреотропного гормона в плазме.
Эффективность терапии в двух группах оценивали по степени выраженности и динамики лабораторных показателей нежелательных явлений противовирусной терапии (уровень лейкоцитов, тромбоцитов, нейтрофилов и гемоглобина). При достижении критических значений требуется модификация дозы или отмена препаратов.
Общепринятым методом оценки эффективности лечения ХВГС является достижение вирусологического ответа. Вирусологические критерии оценки эффективности – основные показатели успешности противовирусного лечения гепатита С. Вирусологическими критериями оценки эффективности лечения являются: быстрый вирусологический ответ (БВО) – РНК ВГС ниже уровня детекции анализатора через 4 недели лечения; ранний вирусологический ответ (РВО); частичный РВО – снижение уровня РНК ВГС от исходного значения на 2 log10 или более (≥100 раз) через 12 недель лечения и полный РВО – отсутствие детекции РНК ВГС через 12 недель лечения.
Таким образом, во время лечения необходимо определять быстрый и ранний вирусологический ответ.
Существует большая вероятность достижения УВО при достижении быстрого вирусологического ответа, чем при частичном РВО или при замедленном вирусологическом ответе на лечение.
Быстрый и полный ранний вирусологические ответы могут рассматриваться в качестве предикторов устойчивого вирусологического ответа. При отсутствии достижения РВО вероятность получения УВО составляет ≤ 3 %. В таком случае необходимо прекратить лечение.
Результаты исследования и их обсуждение
Сравнительный анализ частоты достижения биохимического ответа не выявил статистически достоверных различий между группами [4]. В процессе проводимого лечения у пациентов первой группы, получавших пегинтрон и ребетол отмечена лейкопения до 3,7±0,05×109/л и 3,4±0,02×109/л (р
Актуальность. Проблема этиотропного лечения хронического вирусного гепатита С (ХВГС), несмотря на большое количество исследований, по-прежнему остается актуальной и до конца не решена.
Эффективность лечения по данным разных исследователей не превышает 46-51% у больных ХВГС с 1-м генотипом и 70-80% у больных ХВГС с не 1-м генотипом 4. Так же ограничивают их применение высокая стоимость препаратов и большое количество побочных эффектов от проводимой терапии. Целью проведения этиотропной терапии ХВГС является подавление вирусной репликации, эрадикация вируса из организма и, соответственно, прекращение инфекционного процесса. Даже отсутствие вирусологического эффекта при специфической терапии приводит к замедлению прогрессирования заболевания, стабилизации или регрессии патологических изменений в печени, предупреждению формирования цирроза печени и первичной гепатоцеллюлярной карциномы, а также повышению качества жизни.
Оценку эффективности специфического лечения осуществляют на основании нескольких критериев: вирусологического (исчезновение рибонуклеиновой кислоты (РНК) вируса из сыворотки крови), биохимического (стойкая нормализация уровня ферментов печени) и морфологического (уменьшение индекса гистологической активности и стадии фиброза).
В целом около 5% больных [1,5] вынуждены отказаться от специфического противовирусного лечения в начале курса из-за многочисленных побочных эффектов, а 20% не доводят его до конца.
Побочные эффекты интерферона (ИФН) и рибавирина иногда вынуждают временно или постоянно снижать их дозы или отменять препараты. Некоторыми исследователями [5] показано, что для достижения устойчивого вирусологического ответа (УВО) необходимо получение не менее 2/3 дозы ИФН и рибавирина, поэтому эффективность комбинированной противовирусной терапии (КПВТ) напрямую зависит от наличия побочных эффектов и возможностью их коррекции.
Некоторые побочные эффекты не требуют медикаментозной терапии, так как носят легкий или среднетяжелый характер, другие - тяжелый и угрожающий жизни характер, при этом необходима специфическая коррекция. Как правило, после окончания терапии большинство побочных эффектов полностью исчезает без применения симптоматической терапии.
Проблема побочных эффектов на фоне проводимой КПВТ остается до конца не изученной, несмотря на проведенные многочисленные исследования.
Основными побочными явлениями, описанными в литературе, являются: гематологические изменения; гриппоподобный, диспепсический, неврологический и астеновегетативный синдромы; аутоиммунные поражения; снижение массы тела; выпадение волос; огрубение кожи; аллергические реакции различной степени выраженности; местная реакция в области введения интерферонов.
Таким образом, проблема побочного действия комбинированного противовирусного лечения ХВГС, его влияние на достижение УВО является актуальной в настоящее время.
Целью данного исследования было изучение побочных явлений КПВТ в зависимости от схемы лечения, сопутствующих заболеваний, влияние на достижение УВО. Для достижения поставленной цели были сформулированы следующие задачи: оценить переносимость КПВТ пациентами с различными схемами терапии, выявить частоту побочных эффектов КПВТ и взаимосвязь их с достижением УВО.
Материалы и методы. В исследование были включены 50 пациентов с установленным диагнозом ХВГС, которые получали КПВТ. Диагноз был подтвержден согласно общепринятым методикам.
Из исследования исключались пациенты с микст-инфекцией (вирусный гепатит В, ВИЧ-инфекция) а так же наличием сопутствующей патологии печени (первичный билиарный цирроз, болезнь Вильсона-Коновалова, синдром Бадда-Киари, гемохроматоз, аутоиммунный гепатит, дефицит альфа-1 антитрипсина) и предшествующего специфического противовирусного лечения по поводу ХВГС, больные с наличием любого из общепринятых противопоказаний для проведения КПВТ.
Продолжительность лечения составила 48 недель для пациентов, инфицированных генотипом 1в вирусного гепатита С или при наличии у больного цирроза печени; 24 недели для пациентов, инфицированных генотипом 2 и 3а. Согласно рекомендациям по ведению пациентов с ХВГС, КПВП включала комбинацию стандартного (Интрон или Альтевир 3 млн МЕ 3 раза в неделю) или пегилированного (ПегИнтрон 120 мкг или Пегасис 180 мкг в неделю) ИФН и рибавирина в дозировке 800-1200 мг в зависимости от массы тела.
Устойчивый вирусологический ответ (УВО) определялся как отсутствие РНК вируса в сыворотке крови спустя 24 недели после окончания КПВТ. Больные находились под наблюдение в течение терапии на базе Воронежской областной клинической инфекционной больницы и поликлиник Воронежа. Все пациенты были разделены на 2 группы: получающие в составе КПВТ стандартные ИФН – 52,0% (26 человек) или пегилированные ИФН – 48,0% (24 человек). Пациенты были сопоставимы по возрасту и полу: средний возраст составил 40,3 ±10,4, количество мужчин - 57,1%, женщин 42,9%. Распределение по группам показано в табл. 1.
Таблица 1. Характеристика пациентов в исследуемых группах
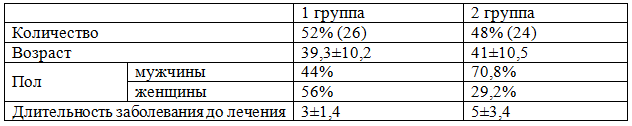
При анализе полученных результатов использовались описательные методы математической статистики с применением пакета программ Microsoft Excel 2010. Достоверность различий оценивалась методами непараметрической статистики, статистически значимыми считались различия результатов при р≤0,05.
Результаты. При анализе эпидемиологических данных выяснено, что в большинстве случаев (34% случаев) ХВГС выявлен случайно, без клинических проявлений. Одинаковое количество пациентов (по 8 человек - 19,2%) обследовались по поводу диспепсических жалоб и длительного повышения печеночных ферментов. У 30 % пациентов в анамнезе отмечались неоднократные операции или переливание крови; употребление внутривенных наркотиков - у 16% человек. Длительность заболевания до начала противовирусной терапии составила в 1 группе 3±1,4 лет, во 2 группе 5±3,4лет. Степень фиброза по Metavir в среднем составил в 1 группе 1±0,85 балла, во второй группе выше - 1,9±1,5 баллов.
Соотношение генотипов вируса гепатита С, определенных до начала КПВТ, показано в табл. 2.
Таблица 2. Соотношение генотипов вирусного гепатита С
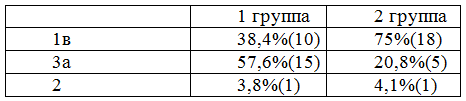
Среди всех пациентов УВО определялся в большинстве случаев - 80,0%, при применении обоих видов терапии, но при этом достоверных различий между группами по этому признаку не выявлено. Эффективность терапии в 1 группе составила 75,1%, во 2 группе - 78,2%. Отсутствие вирусологического ответа в половине случаев связано с отменой препаратов из-за развития выраженных побочных эффектов (прогрессирование неврологической симптоматики с развитием энцефалопатии в 1 группе, длительная некупируемая лихорадка во 2 группе).
Частота побочных эффектов в общей выборке была достаточно высокой - 72,3% среди всех пациентов, при этом в 1 и 2 группе нежелательные явления встречались с одинаковой частотой (69,1% и 73% соответственно).
На протяжении всей терапии у большинства пациентов встречался астеновегетативный синдром в виде выраженной слабости, усталости, нарушения сна, при этом значительно чаще эти проявления отмечали пациенты 2 группы - принимающие пегилированные ИФН (30,7%), что в 2,1 раза чаще, чем во 1 группе (66,6%). Снижение настроения, появление раздражительности, неконтролируемой агрессии при опросе отмечали 23,0% пациентов 1 группы и 25,0% пациентов 2 группы. Данные жалобы чаще встречались на 24±2 неделе терапии. Описанная в литературе депрессия, индуцированная КПВТ, среди данной выборки не встречалась. Для выявления депрессии у всех пациентов применялся опросник Цунга в начале и при завершении КПВТ.
Гриппоподобный синдром, проявляющийся лихорадкой до 38±0,85?С, миалгией, артралгией, выявлен достоверно чаще в у пациентов 1 группы (38,4%), чем у 2 группы (30,1%). Длительность лихорадки составляла в среднем 14±2 недель, первый подъем температуры всегда сопровождал начало КПВТ. Лихорадка купировалась применением препаратов НПВС в стандартных дозировках.
Жалобы со стороны желудочно-кишечного тракта в виде снижения аппетита, тошноты, периодической диареи, боли, вздутия в животе отмечались у 34,6% пациентов 1 группы, что в 2,08 раза чаще, чем во 2 группе (16,6%) .Желтуха на фоне КПВТ встречалась у 2 человек в каждой группе (по 8,3% и 7,6% соответственно).
Снижение веса в среднем на 10,5±5,1 кг, регистрируемое к концу КПВТ, встречалась в 2,3 раза чаще у пациентов 1 группы (19,2%) чем у пациентов среди пациентов 2 группы (8,3%).
Выпадение волос, жалобы на сухость кожи, зуд кожи регистрировались редко: в 1 группе у 2 человек (7,6%среди группы), во 2 группе чаще - у 3 человек(12,5%).
Обострение имеющихся сопутствующих соматических заболеваний встречались в обеих группах приблизительно с одинаковой частотой (30,1% и 27,6% соответственно). Чаще всего встречались обострения хронического панкреатита, язвенной болезни желудка, сахарного диабета.
Частота манифестации впервые выявленных соматических заболеваний на фоне проведения КПВТ имеет прямую корреляционную связь с используемыми препаратами, то есть значительно чаще выявляется при применении ИФН короткого действия, чем пролонгированных форм. При этом в 1 группе на фоне КПВТ манифестировали псориаз (7,6%), аутоиммунный тиреодит (15,3%). А во 2 группе выявлялись гипотиреоз и сахарный диабет (по 4,1% пациентов).
Гематологические осложнения встречались в обеих группах. Анемия, регистрируемая в виде снижения гемоглобина ниже 110г/л, встречалась чаще всего в середине терапии (24±3недели КПВТ). Во второй группе анемия выявлена достоверно чаще – в 2,4раза чаще (38,4%случаев), чем в 1 группе (16% случаев). Эритропоэтин для коррекции анемии применялся в 4 случаях (8%), у остальных коррекции анемии не требовалось.
Среди пациентов обеих групп при наличии анемии УВО встречается в 49,7% случаев, при отсутствии анемии достоверно реже (в 1,35 раз) - у 36,6% пациентов. Таким образом, наличие анемии, в сочетании с другими факторами можно считать предиктором эффективности КПВТ.
Напротив, частота тромбоцитопении на фоне КПВТ коррелировала с отсутствием УВО. Пациенты со снижением уровня тромбоцитов в 1,8 раз реже достигали УВО. Среди всех пациентов тромбоцитопения встречалась только у 8,0% пациентов, что реже, чем по литературным данным. В обеих группах частота данного побочного действия была одинаковой.
Выводы
1. Эффективность терапии с применением препаратов пегилированных или стандартных интерферонов оказалась сходной.
2. Гематологические нежелательные эффекты выявлены достоверно чаще при использовании пегилированных ИФН в составе противовирусной терапии.
3. Гриппоподобный на фоне КПВТ встречались достоверно чаще у пациентов, получающих стандартные ИФН.
4. Астеновегетативный синдром зарегистрирован чаще у пациентов на фоне терапии пегилированными ИФН.
5. Выявлена зависимость между достижением устойчивого вирусологического ответа и величиной снижения уровня гемоглобина.
Список использованных источников:
1. Беляева Н.М., Турьянов М.Х., Рабинович Э.З. Комбинированная терапия гепатита С рибавирином и альфа-интерфероном: Пособие для врачей. - М.: РМАПО. – 2002.
2. Громова Н.И. и Богомолов Б.П. Клиническая эффективность этиотропной терапии хронического вирусного гепатита С// Клин. мед. - 2003.-№1. - С.48.
3. Ивашкин В.Т. Комбинированное лечение хронического гепатита В// Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 1998. №5. С. 57-60.
4. Ferenci P., Fried M., Shiffman M. et al. Predicting sustained virological responses in chronic hepatitis C patients treated with peginterferon alfa-2a// J. Hepatol. – 2005. – Vol. 43. – P. 425–433.
5. Fried M.W. Side effects of therapy of hepatitis C and their management. Hepatology. 2002. - P.237-244
6. Князькина О.В., Каган Ю.Д., Скачков М.В. Микробиоценоз кишечника у больных хроническим вирусным гепатитом С и его лечение// Врач-аспирант, №3.4(52), 2012. – С.579-586.
7. Пирогова И.Ю., Пышкин С.А. Неинвазивная диагностика стадии фиброза у пациентов с хроническими гепатитами В и С// Врач-аспирант, №2(45), 2011. – С. 21-27.
8. Попов С.С., Попов С.Ф. Динамика биохимических показателей гепато-билиарной системы рабочих основных цехов металлургического завода, инфицированных вирусами гемоконтактных гепатитов В и С// Врач-аспирант, №6(55), 2012. – С.55-61.
9. Рихсиева Г.М. Особенности клинико-иммунологических показателей детей, больных острыми вирусными гепатитами А и В, родившихся от матерей, злоупотребляющих алкоголем// Врач-аспирант, №4.4(47), 2011. – С. 675-681.
10. Рюмин А.М., Корочкина О.В., Соболевская О.Л. Закономерности естественного течения хронического гепатита В// Врач-аспирант, №4.1(53), 2012. – С. 214-223.
- КЛЮЧЕВЫЕ СЛОВА: вирусный гепатит, гепатит С, Альгерон, Пегинтрон
В начале своего выступления профессор А.А. Шульдяков отметил, что нельзя недооценивать влияние инфекции, вызванной вирусом гепатита C (ВГC), на течение жизни пациентов с хроническим гепатитом C (ХГС). Совсем недавно завершился ряд больших эпидемиологических исследований, результаты которых показали, что инфицирование вирусом значительно сокращает продолжительность жизни больных. Хроническая ВГС-инфекция повышает смертность от печеночных и внепеченочных заболеваний 1 .
Основной задачей лечения ХГC является элиминация вируса и, как следствие, увеличение продолжительности жизни и улучшение ее качества.
Достижение больными ХГС устойчивого вирусологического ответа (УВО), который расценивается как отрицательный результат обнаружения РНК ВГС через 24 недели после проведенного курса противовирусной терапии, связано со снижением смертности от всех причин.
Таким образом, цель стартовой терапии ВГС-инфекции – снижение смертности от всех причин, но в первую очередь от заболеваний, связанных с поражением печени.
Среди ранее не леченных пациентов выделяют самые тяжелые группы больных, нуждающихся в неотложной терапии. В группы с высоким риском тяжелых осложнений входят больные с фиброзом (стадии F3–F4), циррозом, криоглобулинемией (2-й и 3-й типы), тяжелым поражением почек (протеинурией, нефротическим синдромом, мембранозно-пролиферативным гломерулонефритом), а также пациенты после трансплантации.
Группа пациентов высокого приоритета для лечения ВГС-инфекции, но с возможностью на непродолжительное время отложить терапию включает больных с фиброзом печени стадии F2, коинфекцией с ВИЧ или вирусом гепатита В, иными сопутствующими заболеваниями печени, синдромом хронической усталости, сахарным диабетом и др.
Последние 15 лет в гепатологии отмечены выдающимися достижениями в области лечения ХГС, в том числе 1-го генотипа. Если в начале этого века эффективность терапии составляла 42–46% в плане достижения УВО, то с 2013 г., с появлением препаратов прямого противовирусного действия, она достигла 90–100%.
Основные группы современных противовирусных препаратов прямого действия – ингибиторы протеазы, ингибиторы полимеразы, ингибиторы NS5A. Они характеризуются так называемым прямым противовирусным действием, при этом блокируют ключевые внутриклеточные этапы размножения вируса. К преимуществам препаратов прямого противовирусного действия, используемым в терапии ВГC-инфекции, относятся эффективность, упрощенные схемы и мониторинг, высокий уровень безопасности, удобство использования. Однако, применяя препараты прямого противовирусного действия, необходимо учитывать первичную и вторичную резистентность вируса к ним, неодинаковую эффективность в отношении различных генотипов вируса, латентные резервуары вируса, безопасность и переносимость препаратов и их комбинаций, особенно у пациентов с циррозом печени, различия в эффективности препаратов. Не следует забывать и о возможном нарушении пациентами режима приема лекарственных средств, неадекватном назначении терапии, сопутствующих заболеваниях. Но самым главным лимитирующим фактором для широкого использования в клинической практике препаратов с прямым противовирусным действием остается их очень высокая стоимость.
Эффективным подходом к решению одной из проблем терапии ВГС-инфекции является определение перед началом лечения резистентности вируса к препаратам, что должно быть закреплено в соответствующих рекомендациях. Необходимо также учитывать возможность межлекарственных взаимодействий, которые могут обусловливать увеличение токсичности препаратов или снижение их эффективности. Это особенно актуально при использовании этих лекарственных средств у ВИЧ-инфицированных лиц, вынужденных принимать пожизненно по меньшей мере три антиретровирусных препарата. В то же время, как отметил профессор А.А. Шульдяков, все недостатки прямых противовирусных препаратов меркнут на фоне их цены. Несмотря на высокую распространенность ХГС в мире, стоимость препаратов для лечения данного заболевания чрезвычайно высока. Например, 12-недельный курс лечения препаратами зарубежных компаний обойдется пациенту в 84 000–95 000 долларов. Существующие в России реалии таковы, что в ближайшее время прямые противовирусные препараты по государственным программам закупаться не будут. В связи с этим в качестве терапии первой линии ХГС оправдано использование пегилированного интерферона (ПЭГ-ИФН) альфа в сочетании с рибавирином.
Лечение ХГС с использованием ИФН достаточно затруднительно, поскольку требует более продолжительных сроков и инъекционного введения, сопровождается более выраженными нежелательными явлениями, сопряжено со сложным мониторингом в процессе терапии. Несмотря на это, за прошлые годы достигнуты положительные результаты в терапии ВГC-инфекции препаратами ИФН.
В ряде исследований доказана эффективность комбинации ПЭГ-ИФН с ИФН-альфа и рибавирином в лечении ХГС у больных в зависимости от генотипа. Больные ХГС даже со сложным для терапии 1-м генотипом при благоприятных предикторах в течение 24 недель достигали быстрого вирусологического ответа (БВО) в 90% случаев. Значение имеет и то, что ПЭГ-ИФН-альфа хорошо изучены, в том числе в плане отдаленных побочных эффектов, широко используются для лечения ХГС и знакомы практикующим врачам.
Учитывая уникальные свойства препарата, эксперты Всемирной организации здравоохранения присвоили ему новое международное непатентованное наименование – цепэгинтерферон альфа-2b. Торговое название лекарственного средства – Альгерон.
Противовирусной эффективности препарата Альгерон в терапии ХГС посвящен ряд исследований.
В многоцентровом открытом рандомизированном сравнительном исследовании участвовали 150 взрослых больных ХГС, ранее не леченных препаратами ИФН. Пациенты были стандартно стратифицированы по четырем признакам – возрасту, полу, генотипу и вирусной нагрузке. Больных рандомизировали на три группы. В двух основных группах больные получали Альгерон в дозе 1,5 или 2,0 мкг/кг один раз в неделю в комбинации с рибавирином (800–1400 мг/сут), в группе активного контроля – ПЭГ-ИФН-альфа-2b (ПегИнтрон) 1,5 мкг/кг один раз в неделю в комбинации с рибавирином (800–1400 мг/сут). После 12 недель терапии оценивали эффективность лечения путем определения частоты достижения БВО (после четырех недель) и раннего вирусологического ответа (после 12 недель). По прошествии 24 недель после последнего приема препаратов у пациентов оценивали УВО.
При изучении распределения генотипов ВГC среди пациентов отмечалось преобладание генотипов 1b и 3a, что характерно для Российской Федерации.
Оценка раннего вирусологического ответа показала, что в группе Альгерона 1,5 мкг/кг ранний ответ наблюдался у 100% пациентов с 2-м и 3-м генотипом ХГC. У пациентов с 1-м генотипом этот показатель достигал 88,5%. В группе Альгерона 2,0 мкг/кг ранний вирусологический ответ зарегистрирован у 92,6% пациентов
с 1-м генотипом и у 95,7% – с 2-м и 3-м генотипом. На основании этих данных была выбрана терапевтическая доза Альгерона 1,5 мкг/кг, которую впоследствии получали все пациенты в группах Альгерона. Сопоставимые результаты получены в группе больных, принимавших ПегИнтрон.
Частота достижения УВО среди всех пациентов независимо от генотипа в группе Альгерона составила 75%, в группе ПегИнтрона – 68% (p > 0,05). У пациентов с 2-м или 3-м генотипом, использовавших Альгерон, УВО отмечался в 83% случаев. В группе сравнения этот показатель составил 81,8%. Среди пациентов с 1-м генотипом УВО наблюдался в 67,9 и 57,1% случаев соответственно (p > 0,05).
По мнению профессора А.А. Шульдякова, отсутствие БВО – не приговор для продолжения лечения. Как показали результаты исследования, даже в отсутствие БВО на терапию цепэгинтерфероном альфа-2b 55,6% больных удалось достичь УВО. При отсутствии БВО необходимо дальнейшее снижение вирусологической нагрузки. Следует продолжать терапию в соответствии с рекомендациями по лечению ХГС для достижения УВО.
Оценка безопасности терапии больных ХГС препаратами Альгерон и ПегИнтрон продемонстрировала, что наиболее частой нежелательной реакцией на лечение было появление гриппоподобного синдрома. В целом частота нежелательных явлений в обеих группах не имела статистически значимых различий. Результаты исследования подтвердили высокую эффективность и безопасность отечественного препарата Альгерон в подавлении репродукции вируса гепатита С 2 .
Как известно, коинфекция вирусом гепатита С и ВИЧ достаточно распространена. Доказано, что наличие ХГС определяет заболеваемость и смертность ВИЧ-инфицированных больных.
В рандомизированном исследовании эффективности и безопасности терапии цепэгинтерфероном альфа-2b (Альгерон) участвовали пациенты, инфицированные ВГС и ВИЧ. Больные были равномерно распределены в группы по генотипу вируса, массе тела, возрасту, сопутствующей антиретровирусной терапии. 140 пациентов были рандомизированы на две равные группы Альгерона и ПегИнтрона. Результаты исследования показали, что общее количество пациентов, достигших раннего вирусологического ответа, среди коинфицированных пациентов, получавших Альгерон, составило 90%. В группе сравнения этот показатель составил 81,4%. Следует отметить, что лечение ВИЧ-инфицированных больных – сложная задача, обусловленная многообразием вирусных агентов, угнетением иммунной системы. Поэтому такие пациенты, как правило, показывают невысокие результаты вирусологического ответа.
Результаты исследования свидетельствуют о высокой противовирусной активности Альгерона, как минимум не уступающей зарегистрированному по этому показанию препарату ПегИнтрон, а также позволяют рассчитывать, что у абсолютного большинства пациентов эффект от терапии будет стойким.
В заключение профессор А.А. Шульдяков констатировал, что не всегда имеется возможность использовать препараты с прямым противовирусным действием. В этих случаях надо выделять группы больных, нуждающихся в неотложной терапии, и обеспечивать их доступными интерфероновыми схемами. Конечно, необходим мониторинг ближайших перспектив на обеспечение препаратами прямого противовирусного действия для определения групп больных, у которых лечение интерфероновыми схемами может быть отложено на незначительное время.
Появление отечественного препарата Альгерон существенно облегчает схему терапии у больных ХГС, которые нуждаются в неотложном лечении. По сравнению с зарубежными аналогами этот препарат экономически выгоднее.
Читайте также:


