Патоморфология хронического гепатита с
Вирусный гепатит— вирусное заболевание, характеризующееся преимущественно поражением печени и пищеварительного тракта.
Этиология и эпидемиология. Возбудителями гепатита являются вирусы А (HAV), В (HBV) и дельта (HDV).
HAV — РНК-содержащий вирус гепатита А — вызывает вирусный гепатит А. Путь передачи инфекции фекально-оральный от больного человека или вирусоносителя (инфекционный гепатит). Инкубационный период составляет 15—45 дней. Для этого типа гепатита характерны эпидемические вспышки (эпидемический гепатит). Течение гепатита А, как правило, острое, поэтому он не ведет к развитию цирроза печени.
HBV вызывает вирусный гепатит В, для которого характерен чрескожный механизм передачи: переливание крови, инъекции, татуировка (сывороточный гепатит). Источником инфекции служит больной человек или вирусоноситель. Инкубационный период продолжается 25—180 дней (гепатит с длительным инкубационным периодом). Вирусный гепатит В, который может быть как острым, так и хроническим, широко распространен во всех странах мира, причем отмечается тенденция к его учащению.
Вирусный гепатит В
Этиология. Вирусом гепатита В считают ДНК-содержащий вирус (частица Дейна), включающий три антигенные детерминанты: 1) поверхностный антиген (HBsAg); 2) сердцевидный антиген (HBcAg), с которым связывают патогенность вируса; 3) HBeAg, который расценивают как маркер ДНК-полимеразы. Антигены вируса В можно выявить в тканях с помощью гистологических (окраски альдегидфуксином, орсеином) или иммуиогистохимических методов (ис-, пользование антисывороток к HBsAg, HBcAg, HBeAg).
Классификация. Различают следующие клиникоморфологические формы вирусного гепатита: 1) острую циклическую (желтушную); 2) безжелтушную; 3) некротическую (злокачественную, фульминантную, молниеносную); 4) холестатическую; 5) хроническую. При первых четырех формах речь идет об остром гепатите.
Патологическая анатомия. При острой циклической (желтушной) форме вирусного гепатита морфологические изменения зависят от стадии заболевания (стадии разгара и выздоровления).
Встадию разгара заболевания (1 —2-я неделя желтушного периода) печень (данные лапароскопии) становится увеличенной, плотной и красной, капсула ее напряжена (большая красная печень).
Портальная и внутридольковая строма диффузно инфильтрирована лимфоцитами и макрофагами с примесью плазматических клеток, эозинофильных и нейтрофильных лейкоцитов. Число звездчатых ретикулоэндотелиоцитов значительно увеличено. Клетки инфильтрата выходят из портальной стромы в паренхиму дольки и разрушают гепатоциты пограничной пластинки, что ведет к появлению перипортальных ступенчатых некрозов. В различных отделах долек много переполненных желчью капилляров.
В стадию выздоровления (4—5-я неделя заболевания) печень приобретает нормальные размеры, гиперемия ее уменьшается; капсула несколько утолщена, тусклая, между капсулой и брюшиной встречаются небольшие спайки.
При микроскопическом исследовании находят восстановление балочного строения долек, уменьшение степени некротических и дистрофических изменений. Выражена регенерация гепатоцитов, много двуядерных клеток во всех отделах долек. Лимфомакрофагальный инфильтрат в портальных трактах и внутри долек становится очаговым. На месте сливных некрозов гепатоцитов находят огрубение ретикулярной стромы и разрастание коллагеновых волокон. Пучки коллагеновых волокон обнаруживают также в перисинусоидальных пространствах.
При безжелтушной форме гепатита изменения печени по сравнению с острой циклической формой выражены меньше, хотя при лапароскопии находят картину большой красной печени (возможно поражение лишь одной доли). Микроскопическая картина иная: баллонная дистрофия гепатоцитов, очаги их некроза, тельца Каунсильмена встречаются редко, резко выражена пролиферация звездчатых ретикулоэндотелиоцитов; воспалительный лимфо-макрофагальный и нейтрофильный инфильтрат хотя и захватывает все отделы долек и портальные тракты, но не разрушает пограничную пластинку; холестаз отсутствует.
Для некротической (злокачественной, фульминантной или молниеносной) формы вирусного гепатита характерен прогрессирующий некроз паренхимы печени. Поэтому печень быстро уменьшается в размерах, капсула ее становится морщинистой, а ткань — серо-коричневой или желтой. При микроскопическом исследовании находят мостовидные или массивные некрозы печени. Среди некротических масс встречаются тельца Каунсильмена, скопления звездчатых ретикулоэндотелиоцитов, лимфоцитов, макрофагов, нейтрофилов. Резко выражен стаз желчи в капиллярах. Гепатоциты определяются лишь в сохранившейся паренхиме на периферии долек, они в состоянии гидропической или баллонной дистрофии. В участках, где некротические массы резорбированы и обна жена ретикулярная строма, просветы синусоидов резко расширены, полнокровны; там же видны многочисленные кровоизлияния.
Если больные не погибают в острый период от печеночной комы, у них формируется постнекротический крупноузловой цирроз печени.
Холестатическая форма гепатита встречается преимущественно у лиц пожилого возраста. В основе ее лежат внутрипеченочный холестаз и воспаление желчных протоков. При лапароскопии находят изменения, подобные большой красной печени, но печень с очагами желто-зеленой окраски и подчеркнутым дольковым рисунком. При микроскопическом исследовании преобладают явления холестаза: желчные капилляры и желчные протоки портальных трактов переполнены желчью, желчный пигмент накапливается как в гепа-тоцитах, так и в звездчатых ретикулоэндотелиоцитах. Холестаз сочетается с воспалением желчных протоков <холангиты, холангиолиты).Гепатоциты центральных отделов долек в состоянии гидропической или баллонной дистрофии, встречаются тельца Каунсильмена. Портальные тракты расширены, инфильтрированы преимущественно лимфоцитами, макрофагами, нейтрофилами.
Хроническая форма вирусного гепатита представлена активным или персистирующим гепатитом (возможен и лобулярный гепатит).
Для хронического активного гепатита характерна клеточная инфильтрация портальной, перипортальной и внутридольковой склерозированной стромы печени. Особенно характерно проникновение инфильтрата из лимфоцитов, макрофагов, плазматических клеток через пограничную пластинку в печеночную дольку, что ведет к повреждению гепатоцитов. Развиваются дистрофия (гидропическая, баллонная) и некроз гепатоцитов (деструктивный гепатит), осуществляемый эффекторными клетками иммунной системы (иммунный цитолиз). Некрозы могут быть ступенчатыми, мостовидными и субмассивными (мультилобулярными). Степень распространенности .некроза является критерием степени активности (тяжести) заболевания. Деструкция гепатоцитов сочетается с очаговой идя диффузной пролиферацией звездчатых ретикулоэндотелиоцитов и клеток холангиол. При этом регенерация паренхимы печени оказывается несовершенной, развиваются склероз и перестройка ткани печени.
Хронический активный гепатит, как правило, прогрессирует в постнекротический крупноузловой цирроз печени.
Хронический персистирующий гепатит характеризуется инфильтрацией лимфоцитами, гистиоцитами и плазматическими клетками склеро-зированных портальных полей. Редко очаговые гистиолимфоцитарные скопления встречаются внутри долек, где отмечаются гиперплазия звездчатых рети-кулоэндотелиоцитов и очаги склероза ретикулярной стромы. Пограничная пластинка, как и структура печеночных долек, как правило, сохранена. Дистрофические изменения гепатоцитов выражены минимально или умеренно (гидропиче-ская дистрофия), некроз гепатоцитов встречается редко. Хронический персистирующий гепатит очень редко прогрессирует в цирроз печени и только в тех случаях, когда трансформируется в активный гепатит.
Внепеченочные изменения при вирусном гепатите проявляются желтухой и множественными кровоизлияниями в коже, серозных и слизистых оболочках, увеличением лимфатических узлов, особенно брыжеечных, и селезенки за счет гиперплазии ретикулярных элементов. При остром гепатите довольно часто возникает катаральное воспаление слизистой оболочки верхних дыхательных путей и пищеварительного тракта. В эпителии почечных канальцев, мышечных клетках сердца и нейронах ЦНС находят дистрофические изменения. При хрониче ском активном гепатите развиваются системные поражения экзокринных желез (слюнных, желудка, кишечника, поджелудочной ж'елезы) и сосудов (васкулиты, гломерулонефрит).
Смерть при вирусном гепатите наступает от острой (некротическая форма) или хронической (хронический активный гепатит с исходом в цирроз) печеночной недостаточности. В ряде случаев развивается гепаторенальный синдром.
Патоморфология хронического гепатита
Хронический гепатит (ХГ) – хроническое воспалительное заболевание печени продолжительностью 6 и более месяцев, морфологически характеризующееся дистрофией и некрозами гепатоцитов, воспалительной инфильтрацией с преобладанием лимфоцитов преимущественно портальных трактов, фиброзом.
В 1994 г. на Международном конгрессе гастроэнтерологов в Лос-Анджелесе была принята новая классификация хронического гепатита:
Хронический гепатит В
Хронический гепатит В и D
Хронический гепатит С
Криптогенный гепатит (хронический гепатит неклассифицированный как вирусный или аутоиммунный)
Хронический лекарственный гепатит
Хронический наследственный гепатит:
а) при недостаточности α1-антитрипсина
б) при болезни Вильсона-Коновалова
Современная классификация хронического гепатита требует от клиницистов и патоморфологов учитывать три категории его оценки : этиологический фактор, степень активности процесса, стадию заболевания.
Следует также отметить, что в настоящей классификации отсутствует хронический алкогольный гепатит, включенный в Международной классификации болезней (МКБ) в состав хронической алкогольной болезни (печеночной формы).
Среди различных этиологических вариантов первичных ХГ наибольшее значение придается вирусным гепатитам В, В и D , С. При этом следует помнить, что перечень вирусных форм этим не ограничивается. Появились публикации о ХГ G , E и даже А, что ранее полностью отрицалось.
Для определения этиологии ХГ патоморфологи используют прямые и непрямые (косвенные) морфологические маркеры – совокупность изменений в клетках и тканях органа, которые возникают при внедрении и под воздействием этиологического фактора, а их обнаружение позволяет установить этиологию процесса. К прямым маркерам относят этиологические агенты или их компоненты, выявляемые в тканях (клетках), а к непрямым – характерные для определенной этиологии тканевые или клеточные изменения.
Прямые морфологические маркеры этиологии ХГ
К прямым морфологическим маркерам вирусных ХГ относят частицы вируса и его антигены, для выявления которых необходимо использование электронно-микроскопического, иммуногистохимического и/или иммунофлюоресцентного методов.
При лекарственном и алкогольном ХГ прямые маркеры отсутствуют, а заключение делается на основе анамнестических данных при наличии непрямых маркеров заболевания.
При постановке диагноза аутоиммунного ХГ необходимо учитывать избирательный эффект иммунодепрессивной терапии и обнаружение в сыворотке крови больных высокого уровня иммуноглобулинов и аутоантител, включая антитела к специфическому печеночному протеину (LSP).
При наследственном ХГ, развивающемся преимущественно в младенческом и раннем детском возрасте, могут определяться следующие основные клинико-лабораторные признаки: 1) снижение активности сыворотки против трипсина – недостаточность 1-антитрипсина ; 2) чрезмерное накопление меди в различных тканях с концентрацией церулоплазмина в сыворотке крови меньше чем 1:3 ммоль/л – наследственное аутосомно-рецессивное заболевание с первичным дефектом печени ( болезнь Вильсона-Коновалова ).
Непрямые морфологические маркеры этиологии ХГ
I . Вирусные гепатиты:
Среди вирусных гепатитов непрямые маркеры выделены при ХГ В и С, патоморфологическая диагностика остальных форм возможна только при выявлении прямых маркеров.
Для ХГ В морфологическими маркерами являются :
1) “матово-стекловидные” гепатоциты – крупные клетки с бледноэозинофильной мелкозернистой цитоплазмой со смещенным к периферии ядром; при иммуногистохимическом и иммунофлюоресцентном исследовании в их цитоплазме обнаруживается HbsAg ;
2) “песочные ядра” – хроматин располагается по периферии, центральная просветленная часть ядра представлена мелкогранулярными эозинофильными включениями; при иммуногистохимическом и иммунофлюоресцентном исследовании в ней обнаруживается HbcAg ;
3) тельца Каунсильмена – четко отграниченные гомогенные, эозинофильные образования без ядер или с их остатками, возникающие в результате коагуляционного некроза печеночных клеток;
4) белковая гидропическая дистрофия гепатоцитов до баллонной;
5) очаги колликвационного некроза (фокальные интралобулярные; ступенчатые – очаговые некрозы перипортальных зон печеночных долек, чередующиеся с сохранными участками, как правило, инфильтрированными воспалительными клеточными элементами, периферия печеночной долька и разрушенная пограничная пластинка портального тракта прибретают извитой, ступенчатый вид; мостовидные – протяженные некротические “дорожки”, соединяющие соседние структуры: порто-портальные, порто-центральные, центро-центральные и транслобулярные; субмассивные – некрозы, захватывающие большую часть одной или нескольких долек; массивные – обширные некрозы ткани печени до целой доли);
6) лимфогистиоцитарная инфильтрация с примесью плазматических клеток и полиморфноядерных лейкоцитов.
Для ХГ С косвенными морфологическими маркерами являются :
1) сочетание жировой дистрофии гепатоцитов с гидропической (преобладает жировая);
2) тельца Каунсильмена;
3) гетерогенность гепатоцитов;
4) лимфоцитарная инфильтрация портальных трактов и долек с образованием лимфоидных фолликулов, иногда с реактивными центрами;
5) активация синусоидальных клеток с образованием цепочек лимфоцитов внутри синусоидов;
6) поражение желчных протоков (деструкция, пролиферация, склероз).
II . Аутоиммунный (“люпоидный”) гепатит
Аутоиммунный гепатит (АГ) впервые был описан H . Kunkel с соавт. в 1951 г. у молодых женщин. В связи с частым обнаружением LE -клеточного феномена в сочетании с системными поражениями заболевание было названо “люпоидным” гепатитом.
В сыворотке крови больных обнаруживаются аутоантитела: антиядерные, аутоантитела против мембранных аутоантигенов гепатоцитов, включая LSP . Кроме них выявляются антитела против вирусных антигенов (кори, краснухи). Антиген LSP способен индуцировать реакцию гиперчувствительности замедленного типа. Доказана связь развития АГ с иммунопатологическими реакциями с участием антигенов HLA - A , HLA - B 8, HLA - B 12, DRW 3 у молодых женщин до 30 лет. Эти данные указывают на роль Х-ромосомы и половых гормонов, главным образом эстрогенов, в патогенезе АГ. При этой форме ХГ эффективна иммунодепрессивная терапия.
Морфологическими маркерами АГ являются :
1. частое обнаружение LE -клеточного феномена – полиморфноядерные лейкоциты и макрофаги с внутрицитоплазматическим фагоцитированным поврежденным клеточным ядром;
2. внепеченочные поражения, свойственные системной красной волчанке;
3. выраженная воспалительная инфильтрация печени с преобладанием плазматических клеток;
4. преобладание признаков высокой степени активности с частым развитием мостовидных некрозов;
5. образование гепатоцитами в перипортальных зонах гландулярных (железистых) структур;
6. воспаление мелких желчных протоков и холангиол портальных трактов;
7. лимфоциты инфильтрата нередко образуют в портальных трактах лимфоидные фолликулы;
III . Хронические гепатиты лекарственной этиологии
Медикаменты, вызывающие поражение печени (гепатотоксины), делят на истинные и гепатотоксины идиосинкразии. Истинные гепатотоксины, в свою очередь, подразделяют на две группы: прямого и опосредованного действия. В настоящее время препараты первой группы истинных гепатоксинов не применяются – хлороформ, карботетрахлорид и др. Гепатотоксины опосредованного действия могут быть цитотоксическими, холестатическими и канцерогенными.
Вирусные гепатиты являются инфекционной патологией человека, характеризующейся преимущественным поражением ткани печени, обусловленного её воспалением, и сопровождающееся развитием дистрофических и некротических процессов в сочетании с инфильтрацией стромы (Серов В.В., Лапиш К., 1989). При использовании современных высокочувствительных методов лабораторной диагностики этиологическая расшифровка хронических вирусных гепатитов возможна в 97% случаев (Ивашкин В.Т. и соавт., 2001).
В последнее время увеличилось число инфицированных гепатитами В и С, что представляет определённую опасность инфицирования для врачей-патологоанатомов, судебно-медицинских экспертов, врачей хирургических специальностей, а так же других медицинских работников, участвующих в проведении инвазивных методов диагностики и лечения инфицированных гепатитами больных. Учитывая вышеизложенное нам представилось интересным установить частоту инфицированности и определить демографические особенности HCY и HBY инфекции при случайно выявленном инфицировании по материалам проводимых судебно-медицинских исследований и особенности патоморфологии печени и почек у этих лиц.
Для решения поставленной цели нами сплошным методом было проведено исследование крови от трупов лиц, подвергшихся судебно-медицинскому исследованию в областном бюро судебно-медицинской экспертизы. Исследовалась кровь от трупов лиц в возрасте от 18 до 55 лет. Забор крови производился без учёта причин смерти. Период с момента наступления смерти до забора крови не превышал 24 часов. Жидкая кровь от трупов забиралась в стерильные герметично упакованные пенициллиновые флаконы и направлялась в лабораторию иммуноферментного анализа областной клинической больницы для выявления суммарных антител к вирусу гепатита В и С.
Всего был осуществлён забор от 350 трупов. Среди инфицированных, преобладали умершие насильственной смертью, что составило 72% (99 случаев). Инфицированные гепатитами в возрастной группе от 15 до 24 лет составили 16%, в возрасте от 24 до 35 лет - 52%, от 35 до 44 лет – 20%, старше 45 лет – 12% наблюдений. Среди инфицированных вирусными гепатитами преобладали мужчины (85%), женщины составили 15%.
В результате проведённого исследования было выявлено, что суммарные антитела были обнаружены в 38,1% наблюдений. При проведении иммунологического обследования у 14 человек из 15 инфицированных гепатитом С был выявлен следующий набор маркеров: анти-HCV, анти-HCV core, анти-HCV NS (минимум 1 NS из трех у всех был положителен). У одного инфицированного присутствовали только суммарные антитела к HCV. Среди 15 человек, инфицированных гепатитом С, 5 явились носителями антител HbsAg.
При оценке патоморфологических изменений печени нами учитывались такие параметры, как степень активности, стадия хронизации, выраженность дистрофических изменений гепатоцитов (жировая, гидропическая дистрофия), наличие алкогольного гиалина, телец Каунсильмена, лимфоцитов в синусоидах, лимфоидных фолликулов в портальных трактах, изменения ядер гепатоцитов.
При оценке патоморфологических изменений почек учитывались такие изменения, как клеточная пролиферация клубочков, утолщение базальной мембраны, фиброз. В канальцах учитывалась выраженность дистрофии, атрофии, отложения солей кальция, пигмента. В интерстиции оценивали наличие и выраженность фиброза, клеточной инфильтрации, формирование лимфоидных фолликулов, отёка, полнокровия, кровоизлияний. В состоянии сосудов учитывали такие параметры, как утолщение стенок артерий и артериол, выраженность фиброза и фиброэластоза.
В ходе проведённого микроскопического исследования печени по степени активности гепатитов были выделены основные 3 группы: 1-ая с выраженной степенью активности (40 случаев); 2-ая с умеренной степенью активности (44 случая); 3-я группа со слабой степенью активности (64 случая). В группе с выраженной степенью активности отмечено 14 наблюдений с развитием цирроза печени; в зависимости от степени хронизации наибольшее количество наблюдений приходилось на 4 степень.
Патоморфологические изменения почек в этой группе проявились в виде пролиферации мезангиального матрикса, воспалительных изменений интерстиция, васкулитов, сморщивания клубочков, перигломерулярного и интерстициального склероза, атрофии канальцев, частичного их некроза, и дистрофических изменений эпителия.
В группе с умеренной степенью активности гепатита наибольшее количество наблюдений пришлось на 1-ю степень хронизации (36 наблюдений). Было выявлено поражение клубочков в виде пролиферации мезангиального матрикса и сморщивания клубочков. Изменения канальцев выражались в их атрофии, дистрофических изменениях эпителия и незначительном поражении стромы за счёт воспалительных изменений.
В группе со слабой степенью активности гепатита (64 наблюдения) преобладала слабая степень хронизации (51 случай). Изменения почек в этой группе проявлялись наличием тромбоцитов в клубочках, пролиферацией мезангиального матрикса, васкулитом, сморщиванием клубочков, атрофией канальцев, умеренными воспалительными изменениями интерстиция.
Изменения печени у исследуемого контингента проявлялись воспалением, дистрофией гепатоцитов, а так же некрозами и формированием фиброза. Указанные изменения обнаруживались при различной степени активности гепатита и стадии фиброза.
Как следует из представленных данных, репликация вируса при хронических гепатитах в ткани почек была выявлена в половине исследуемых случаев и не зависела от серологического профиля гепатита. Воспаление и дистрофические изменения развивались в структуре клубочков, канальцев, сосудах и интерстиции. Выраженность патоморфологических изменений почек у инфицированных вирусными гепатитами не зависела от активности воспалительного процесса в печени.

Цирроз печени является исходом хронического гепатита. Так, в среднем, после заражения вирусом гепатита С цирроз печени развивается через 30 лет. При этом, если инфицирование произошло у женщины до 40 лет, то цирроз развивается через 42 года, а если у мужчины после 40 лет, то через 13 лет.
Классификация по этиологическим, морфологическим критериям представлена на слайде. По степени выраженности печеночной недостаточности цирроз делится на компенсированный, субкомпенсированный и декомпенсированный.
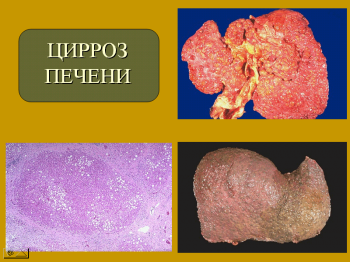
Морфологические формы цирроза печени. Справа вверху крупноузловой цирроз, справа внизу – мелкоузловой. На левой нижней фотографии изображена гистологическая картина мелкоузлового цирроза печени. Отчетливо виден узел из регенерирующих гепатоцитов, окруженный соединительной тканью, среди которой определяется фокус лимфоцитарной инфильтрации. Гепатоциты с признаками жировой дистрофии.
Важными осложнениями цирроза печени являются портальная гипертензия и печеночная недостаточность. Портальная гипертензия сопровождается открытием порто-кавальных анастомозов и, как следствие, кровотечением из варикозно расширенных вен пищевода, геморроидальных вен; асцитом; развитием хронического венозного полнокровия в селезенке и далее спленомегалии, гиперспленизма, анемии, тромбоцитопении.

Эти осложнения развиваются на фоне прогрессирующей печеночной недостаточности, основные признаки которой представлены на данном слайде. Особо необходимо отметить нарушения белоксинтезирующей функции печени, приводящие к недостаточному образованию факторов свертывания крови и, как результат, гипофибриногенемии, гипопротромбинемии. Кровотечение из варикозно расширенных вен пищевода на фоне нарушения белоксинтезирующей функции печени приводит к летальному исходу в 25 % случаев.

Следующим смертельно опасным осложнением хронических вирусных гепатитов В и С является первичный рак печени. Подтверждением данного тезиса является высокая сочетаемость опухолей человека с вирусными гепатитами и циррозами печени. При формировании у больного цирроза печени, обусловленного вирусным гепатитом С, каждый последующий год увеличивает шанс развития гепатоцеллюлярного рака на 3-10 %. Другими словами, минимум через 10 лет и максимум через 33 года у больных с циррозом печени вирусной этиологии будет злокачественная опухоль.
Механизм формирования гепатоцеллюлярного рака при вирусных гепатитах связывают со встраиванием вируса гепатита В в геном клетки и повышением пролиферативной активности гепатоцитов в процессе регенерации печени (вирусные гепатиты В и С).

Различают три макроскопические формы первичного рака печени: узловую, массивную и диффузную.
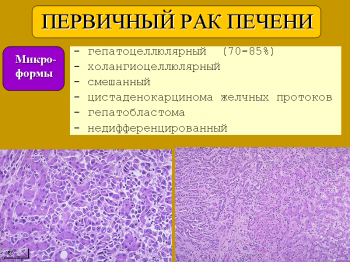
Микроскопически среди первичного рака печени выделяют происходящий из гепатоцитов – гепатоцеллюлярный, из эпителия желчных протоков – холангиоцеллюлярный и несколько более редких форм – цистаденокарцинома, гепатобластома, недифференцированный. Характерными признаками гепатоцеллюлярного рака (слева) являются: наличие трабекулярных и ацинарных структур, напоминающих первичные трабекулы, продукция желчи, широкие поля эозинофильной гранулярной цитоплазмы, продукция гликогена, отсутствие секреции слизи. Для холангиоцеллюлярного рака (справа) характерны микроскопические признаки высокодифференцированной аденокарциномы с признаками продукции слизи и отсутствием внутриклеточных скоплений желчного пигмента.
Наибольшее клиническое значение для рака печени имеют гематогенные метастазы в легкие и кости, лимфогенные – в околопортальные лимфатические узлы, брюшину; развитие печеночной недостаточности и, как следствие, гепатаргии; кровотечение в брюшную полость; кахексия.
Выводы и заключение
Таким образом, течение большинства патологических процессов в печени при вирусных гепатитах стереотипно. Основные звенья формирования патологии печени при вирусных гепатитах следующие: острый гепатит, переход его в хронический гепатит (вирусные гепатиты B, C, D, G), формирование цирроза печени и затем гепатоцеллюлярного рака. Скорость формирования цирроза определяется активностью в печени патологического процесса.
Знание врачами морфологической стадии и активности заболевания определяет прогноз и, соответственно, выбор терапии для данной категории больных. В этом и состоит значение изучения морфологии печени при вирусных гепатитах.

Хронический микст-гепатит С+В предсталяет собой серьезную проблему в связи с разнообразной, но более тяжелой по сравнению с моногепатитами С и В, клинической картиной и неоднозначностью в подходах к терапии [1-4, 7, 8, 10]. Так, относительно хронического гепатита С, при хронической микст-инфекции HCV+HBV, реже наблюдается минимальная степень активности (18 % против 33 %) и чаще - умеренная (44% против 27 %), что в целом характеризует течение хронического микст-гепатита С+В как более тяжелое. Распределение пациентов с гепатитом С+В по стадии заболеваний, или по выраженности фиброза, имеет тот же профиль, что и при гепатите С, c явным преобладанием случаев со слабовыраженным портальным фиброзом (70 %), тем не менее, при микст-гепатите чаще отмечается конечная стадия заболевания - цирроз печени [6, 9].
Цель исследования - на основе анализа клинических синдромов, биохимических тестов и результатов патоморфологического исследования биопсии печени пациентов с хроническим микст-гепатитом С+В выделить различные патоморфогенетические варианты инфекционно-вирусного процесса.
Материал и методы исследования
Исследовано 112 пациентов в возрасте от 16 до 69 лет с маркерами хронических гепатитов С и В, преобладали мужчины (74 пациента). Изучали эпидемиологический анамнез, клиническую картину, результаты клинико-биохимического, серологического, молекулярно-биологического и патоморфологического исследований. Анализировали анамнез, пути возможного заражения вирусами гепатита С и В: парентеральное употребление наркотических веществ, гемотрансфузии, хирургические вмешательства. Выявляли токсические факторы: алкоголь, лекарственную гиперпрогмазию, профессиональные вредности, учитывали наличие патологии желудочно-кишечного тракта и паразитарной инвазии.
Диагноз хронического микст-гепатита С+В верифицирован на основании данных эпидемиологического анамнеза, клинико-инструментальных данных, результатов биохимического, иммуносерологического анализа, ПЦР-диагностики и изучения биопсии печени, что позволило идентифицировать маркеры HCV- и HBV-инфекции, установить степень активности и стадию заболевания. Исследования выполнены с информированного согласия пациентов и в соответствии с этическими нормами Хельсинкской Декларации (2000).
Результаты исследования и их обсуждение
Анализ эпидемиологического анамнеза выявил факторы риска заражения вирусами гепатитов С и В: переливание крови и ее компонентов, донорство, парентеральное введение лекарственных препаратов, наркоманию с парентеральным введением наркотических веществ, инвазивные методы исследования и лечения, профессиональный контакт с кровью. Перенесенный острый вирусный гепатит в анамнезе имел место у 34 % пациентов. Среди факторов дополнительного гепатотоксического воздействия - лекарственная гиперпрогмазия (33 %), злоупотребление алкоголем (18 %), сочетанное употребление этанола и наркотических веществ (4 %). У 41 % пациентов имелась патология желудочно-кишечного тракта, у 24 % - патология других органов и систем.
В соответствии с особенностями клинического течения заболевания и результатами комплексного клинико-патоморфологического исследования пациентов выделено три варианта хронического микст-гепатита С+В: типичный (с преобладанием типичных симптомов поражения печени) - 61 % случаев, холестатический - 25 % и вариант с выраженными внепеченочными проявлениями - 14 % пациентов.
Спектр серологических маркеров вирусных гепатитов В и С при всех клинических вариантах не имел существенных различий, во всех наблюдениях регистрировались суммарные HCVAb, в большинстве случаев - антитела к NS-антигенам HCV и набор антигенов и антител HBV, при этом отличительной особенностью серологического спектра холестатического варианта было более редкое выявление HBsAg и более частое обнаружение HВeAg. По данным ПЦР-диагностики, в целом среди всех пациентов доминировала репликация HCV (68 % случаев) по сравнению с репликацией HBV - 52 % случаев.
При типичном варианте в образцах крови с помощью ПЦР в 77 % случаев обнаружена РНК HCV и в 57 % - ДНК HBV, одновременная репликация HCV и НBV - в 30 % случаев. Важно отметить, что при холестатическом варианте хронического микст-гепатита C+B достоверно (р
Читайте также:


