Парвовирус у ребенка анализы
ДНК-содержащий вирус, который обладает склонностью поражать клетки-предшественники эритроцитов и эндотелий сосудов, способен вызывать интенсивную эритему щек и сетчатую эритему конечностей у детей, самолимитирующееся поражение суставов у взрослых, хроническую анемию у людей с иммунодефицитами и водянку плода.
Возбудитель инфекционной эритемы (пятой болезни), эритровирус В19.
Parvovirus B19, Parvo B19, Erythrovirus B19, Fifth Disease test.
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Амниотическую жидкость, венозную кровь, ликвор, слюну, мазок из зева (ротоглотки), биоптат.
Общая информация об исследовании
Парвовирус В19 – ДНК-содержащий вирус из семейства Parvoviridae, который вызывает инфекционную эритему, поражение суставов и хроническую анемию. Эта инфекция распространена, антитела выявляются у 60 % европейского населения. Влияние вируса на организм зависит от гематологического и иммунного статуса инфицированного. Парвовирус В19 размножается в клетках костного мозга, преимущественно разрушая эритробласты и ретикулоциты, а также обладает склонностью поражать эндотелий сосудов.
Вирусом заражаются воздушно-капельным путем или в редких случаях при переливании крови и ее компонентов. Инкубационный период составляет от нескольких дней до 2-3 недель. Парвовирус проникает в кровоток в среднем через 7-14 дней после инфицирования. Острая инфекция часто протекает по типу легкой простуды, сопровождаясь общей слабостью, температурой 37-38 °C, головной болью, диспепсией, или протекает скрыто, не вызывая каких-либо симптомов.
У детей парвовирус вызывает инфекционную эритему – характерное покраснение обеих щек и возвышающуюся сетчатую сыпь на туловище и конечностях. Высыпания в некоторых случаях могут сохраняться или возникать снова в течение нескольких недель и усиливаться при воздействии солнечных лучей, интенсивном воздействии тепла или стрессе. Инфекционную эритему иногда называют пятой болезнью, так как она входит в шестерку самых распространенных заболеваний, сопровождающихся сыпью у детей.
У взрослых при парвовирусной инфекции могут возникать болезненные отеки суставов, покраснение кистей и стоп, которые обычно самостоятельно проходят через несколько недель.
Парвовирус В19 опасен для людей с железодефицитной анемией, серповидно-клеточной анемией, талассемией. Инфицирование вирусом при данных гематологических заболеваниях способно значительно ухудшить течение болезни в связи с интенсивным разрушением эритроидного ростка красного костного мозга, развитием апластического криза.
У людей с иммунодефицитами на фоне ВИЧ/СПИДа после трансплантанции органов, химиотерапии парвовирусная инфекция может привести к неэффективности лечения хронической анемии.
При инфицировании во время беременности вирус иногда может проникать к плоду и вызывать анемию, миокардит. В редких случаях парвовирус В19 становится причиной невынашивания плода (до 9 % случаев при инфицировании во втором триместре), преждевременных родов, водянки новорождённого (в 10-20 % случаев) и мертворождения. Наибольшую угрозу инфекция представляет в первом и втором триместрах беременности.
В большинстве случаев инфекция проходит без лечения и не вызывает значительных последствий. Детям специфическая диагностика парвовируса В19 назначается редко. Особое внимание уделяется людям из группы риска – иммуноскомпрометированным, беременным, больным хроническими формами анемии. Молекулярно-генетическое исследование позволяет обнаружить активную инфекцию в крови до появления антител и является высокочувствительным и специфическим методом ее диагностики.
Для чего используется исследование?
- Для дифференциальной диагностики причин инфекционной эритемы у детей или полиартропатий у взрослых.
- Для диагностики причин острой или хронической анемии у пациентов с иммунодефицитами (у ВИЧ-инфицированных, реципиентов донорских органов).
- Для диагностики причин водянки у новорождённых.
- Для диагностики парвовирусной инфекции у беременных и оценки риска патологии плода.
- Для уточнения причин транзиторного апластического криза у больных с врождёнными формами гемолитической анемии.
Когда назначается исследование?
- При тяжелой или персистирующей анемии у людей с иммунодефицитами.
- При наличии данных о контакте беременной с инфицированными парвовирусом.
- При ухудшении состояния пациентов с различными хроническими формами анемий.
- При инфекционной эритеме у детей.
- При суставном синдроме и полиартропатиях неясного генеза.
Что означают результаты?
Референсные значения: отрицательно.
Причины положительного результата
- Парвовирусная инфекция в период виремии (острая или персистирующая инфекция)
Причины отрицательного результата
- Отсутствие инфекции
- Парвовирусная инфекция в период выздоровления и сероконверсии
Отрицательный результат полностью не исключает инфицирования данным вирусом. Для уточнения диагноза необходимо одновременно определять наличие специфических антител.
Что может влиять на результат?
При содержании вирусных частиц в крови ниже детектируемого уровня возможен ложноотрицательный результат.
- Для периода активной инфекции характерно снижение уровня ретикулоцитов в крови.
- Инфицирование в период беременности в большинстве случаев не представляет угрозы для ребенка, однако требует тщательного мониторинга состояния плода.
- Для людей с иммунодефицитами ввиду нарушения продукции антител единственным анализом, подтверждающим наличие инфекции, может оказаться ПЦР.
Кто назначает исследование?
Гематолог, ревматолог, инфекционист, педиатр, акушер-гинеколог.
Литература
- Lamont RF, Sobel JD, Vaisbuch E, Kusanovic JP, Mazaki-Tovi S, Kim SK, Uldbjerg N, Romero R. "Parvovirus B19 infection in human pregnancy". BJOG: an International Journal of Obstetrics and Gynaecology - January 2011 - 118(2): 175–86.
- Servey JT, Reamy BV, Hodge J. "Clinical presentations of parvovirus B19 infection". Am Fam Physician — 2007 - 75(3): 373–376.
Как врач общей практики может диагностировать инфекцию, вызванную парвовирусом В19? В чем заключается опасность этой инфекции для детей с гематологическими заболеваниями?
Хотя другие представители данного рода вирусов поражают собак, кошек, лисиц и даже медведей гризли, штамм В19 патогенен только для людей и размножается исключительно в предшественниках эритроцитов человека.
Антитела-IgG к этим вирусам выявляются приблизительно у 50% подростков, достигших 15 лет, и более чем у 90% пожилых людей [2]. Ежегодно вираж серологических проб происходит у 1,5% женщин детородного возраста. Повышение заболеваемости отмечается каждые три-четыре года, обычно в конце зимы, весной и в начале лета.
Большинство специалистов считают, что данная инфекция передается воздушно-капельным путем, хотя, в отличие от других вирусных заболеваний, в данном случае репликации возбудителя в носоглотке не обнаружено. Парвовирус В19 не выделяется ни с мочой, ни с калом.
Подобно тому как выпускаемые в Бордо изысканные вина в 1855 году были разделены на пять сортов, еще в прошлом веке экзантемы у детей были разбиты на пять групп. Инфекционная эритема получила название пятой болезни, корь — первой, скарлатина — второй, краснуха — третьей, болезнь Филатова-Дьюка — четвертой; в настоящее время четвертая болезнь не признается отдельным заболеванием [3]. Впоследствии была описана младенческая розеола (roseola infantum).
 |
| Рисунок 2. Вторичная эритематозная пятнисто-папулезная сыпь появляется на туловище и конечностях через несколько дней после первичных высыпаний. Она варьирует по выраженности и продолжительности, может носить транзиторный характер, рецидивируя на протяжении нескольких недель |
Инфекционной эритемой поражаются преимущественно дети в возрасте 4-10 лет. В течение двух-пяти дней и до появления сыпи клинические симптомы неспецифичны и могут включать насморк, фарингит, головную боль, тошноту, понос и общее недомогание, а также лихорадку. В это время ребенок наиболее заразен.
Затем появляются кожные симптомы; это означает, что ребенок уже не заразен. Сначала на обеих щеках появляется ярко-красная сыпь, при этом вокруг рта кожа бледная, что похоже на следы от пощечин. Удивительно то, что у заболевших взрослых кожа щек не изменяется.
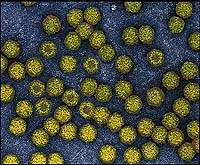 |
| Рисунок 3. Парвовирус В19: у инфицированных им детей, страдающих сопутствующими гематологическими заболеваниями, могут развиться осложнения |
Такую сыпь трудно выявлять у детей-негров, для которых своевременная диагностика может иметь особое значение, если у них одновременно наблюдается серповидноклеточная анемия. Установлению диагноза помогают жалобы на зуд в подошвах. Действительно, зуд, особенно на подошвах, может быть самым выраженным симптомом заболевания, хотя неясно, чем объяснить такую связь. У взрослых в результате инфицирования парвовирусом В19 часто наблюдаются боли в суставах и артрит. Эти же явления встречаются приблизительно у 10% детей с инфекционной эритемой.
Хотя артрит обычно вскоре проходит, у небольшой части детей он принимает затяжной характер, при этом его можно спутать с юношеским ревматоидным артритом (с болезнью Стилла [Still]). Как бы то ни было, парвовирус В19 в отдаленные сроки не вызывает деструкции суставов [4].
Во время этих кризов (которые у ребенка часто могут быть первым проявлением гематологической патологии, до этого хорошо компенсированной) быстро развиваются симптомы анемии: бледность, утомляемость, одышка и спутанность сознания. На поздней стадии развиваются застойная сердечная недостаточность и некроз костного мозга, что может привести к смерти. Однако переливание крови в начале криза обычно позволяет добиться полного выздоровления у большинства детей.
Если ребенок принадлежит к одной из указанных групп высокого риска и заболевает инфекционной эритемой, то врач общей практики должен направить его на консультацию к гематологу для точной постановки диагноза. По крайней мере, у ребенка следует провести общий анализ крови и микроскопию мазка.
Гематологические изменения во время инфекции, вызванной парвовирусом В19, могут наблюдаться и у детей, которые ранее были здоровы.
Как и при многих вирусных инфекциях, часто наблюдаются в разной степени выраженные нейтропения и тромбоцитопения; эти признаки не имеют почти никакого диагностического значения. В литературе сообщалось о возможной связи инфекции, вызываемой вирусом В19, с идиопатической тромбоцитопенической пурпурой [6], а также с пароксизмальной холодовой гемоглобинурией (при которой гемолитическая анемия начинает развиваться под воздействием холода).
Наибольшую тревогу вызывает то, что ребенок с инфекционной эритемой может заразить свою беременную мать при отсутствии у нее специфического иммунитета [7]. Плод весьма подвержен воздействию парвовируса В19, особенно между 20 и 28 неделями внутриутробного развития.
Как и у детей с сопутствующими гематологическими заболеваниями, вирус поражает клетки-предшественники эритроцитов, что ведет к глубокой анемии. Это может вызвать неиммунный отек плода (из-за застойной сердечной недостаточности) и его гибель.
Из всех беременных, впервые заражающихся данной инфекцией на указанном сроке (при этом только у 30% из них выражены клинические симптомы), у 10% женщин наступает гибель плода [8]. Обнадеживает то, что у выживших младенцев, родившихся от матерей, которые были инфицированы парвовирусом В19 во время беременности, не отмечается повышенной частоты врожденных пороков развития, неврологической патологии или задержки развития.
Что же должен предпринять врач общей практики, если есть подозрение, что беременная заразилась парвовирусом? Путем определения специфических противовирусных антител можно подтвердить факт инфицирования только через некоторое время: антитела-IgM появляются через десять дней после попадания вируса в организм, а антитела-IgG — через две недели. У такой беременной необходимо регулярно проводить ультразвуковое исследование, чтобы не пропустить развитие отека плода, при котором следует решать вопрос о раннем фетальном переливании крови [9].
В литературе имеются относительно немногочисленные сообщения о возможной связи В19-парвовирусной инфекции у детей с рядом патологических состояний: нефропатиями, энцефалитом, узелковым периартериитом, системной красной волчанкой, болезнью Кавасаки, миокардитом, гепатитом и с другими васкулитными синдромами. Ни в одном из этих сообщений не прослеживается четкой причинно-следственной связи.
Создать такую вакцину вполне реально. Белок оболочки вируса — это сильный стимулятор гуморальной иммунной реакции, что делает вакцину в высшей степени эффективной [11]. Необходимо использовать конъюгаты и вспомогательные вещества (адъюванты). Может быть применен рекомбинантный белок оболочки вируса.
Вакцинацию целесообразно будет проводить у молодых женщин и детей с гематологическими заболеваниями, однако в настоящее время спорным остается вопрос о введении универсальной вакцины против кори, эпидемического паратита, краснухи и парвовирусной инфекции.
Возбудитель – парвовирус В19, относящийся к семейству Parvoviridae, представляет собой безоболочечный ДНК-содержащий вирус диаметром 18–26 нм. Капсид состоит их двух полипептидных белков 84 кДа и 58 кДа (VP1 и VP2). Оба структурных белка кодируются в одной и той же рамке считывания генома вируса. Кроме того, в геноме кодируется основной неструктурный белок NS-1, который необходим для репликации вируса. Вирус очень термостабилен и может выдерживать нагревание в 60.
Источник инфекции – больной человек или носитель. Пути передачи: воздушно- капельный, парентеральный (особенно при переливании эритромассы), трансплацентарный. Факторами передачи вируса являются слюна, кровь, донорские органы и ткани. Инкубационный период – 1–3 недели. Фаза виремии длится от 3 до 7 дней и сопровождается головной болью, зудом, болью в мышцах и лихорадкой, но может протекать и бессимптомно (у 20% пациентов). Примерно через 2 недели после заражения может появиться инфекционная эритема (чаще – у детей) или краснухоподобная сыпь. В дальнейшем появляются боли в суставах (у 60% пациентов), респираторные симптомы (в 22% случаев), диарея (15–35%). Артропатии, которые в 2 раза чаще встречаются у женщин, чем у мужчин, обычно исчезают через 2–4 недели, однако при персистирующей форме могут отмечаться в течение нескольких лет.
У лиц с достаточной иммунорезистентностью угнетение эритропоэза в результате репликации вируса (обычно 1–4 недели) протекает субклинически, однако у лиц со сниженной иммунорезистентностью может привести к апластической анемии, и, как осложнение, к апластическому кризу. Репликация вируса сопровождается тромбоцитопенией. С парвовирусом В19 ассоциированы заболевания в виде дисфункции печени и миокардита, он может вызывать поражение мозга.
Парвовирус В19 может передаваться плоду через плаценту. При заражении плода до 20 недели беременности, инфекция способна привести к тяжелой острой или хронической анемии, самопроизвольному аборту. При заражении во втором триместре беременности развивается водянка плода. Около 80% беременностей протекают без осложнений.
Восприимчивость населения к парвовирусу В19 высокая. Обычно через 10 дней после заражения выявляются АТ IgM, что сопровождается появлением описанных ранее симптомов, через 30–60 дней АТ IgM уже не выявляются. Через 2–3 недели с момента инфицирования начинается образование АТ IgG, они остаются в организме длительно (годами). По мере развития заболевания на фоне анемии может прогрессировать тромбоцитопения (особенно у новорожденных детей и у лиц с иммунодефицитными состояниями).
Показания к обследованию
- Анемия беременных, не поддающаяся терапии с использованием препаратов железа;
- тромбоцитопения;
- инфекционная эритема с суставным синдромом;
- гепатит неясной этиологии;
- гепатоспленомегалия;
- наличие отягощенного акушерского анамнеза (перинатальные потери);
- скрининг беременных из группы высокого риска (тромбоцитопения, анемия неясного генеза, апластический криз, артропатии, краснухоподобная сыпь, УЗИ-признаки многоводия, водянки плода);
- наличие в анамнезе переливания крови или тромбоцитарной массы;
- симптоматика врожденной инфекции, сопровождающаяся анемией и тромбоцитопенией;
- дети первого года жизни с гидроцефальным синдромом, менингоэнцефалитом, гепатитом неясной этиологии.
Дифференциальная диагностика. Краснуха, корь, ЦМВИ (мононуклеозоподобная форма), ВИЧ–инфекция, псевдотуберкулез (мононуклеозоподобный синдром), железодефицитная анемия.
Материал для исследования
- Кровь, плазма/сыворотка крови, лимфоциты периферической крови, СМЖ – обнаружение ДНК;
- cыворотка/плазма крови, СМЖ – определение АТ.
Этиологическая лабораторная диагностика включает выявление ДНК возбудителя и определение вирусоспецифических АТ к антигенам парвовируса В19.
Сравнительная характеристика методов лабораторной диагностики. Определение в сыворотке крови АТ IgM и IgG к АГ парвовируса В19 проводится преимущественно методом ИФА. Исследование применяется для перинатального скрининга и диагностики парвовирусной инфекции. С учетом кратковременности выявления АТ IgM в крови для оценки риска инфицирования плода и новорожденного основополагающей является детекция ДНК вируса методом ПЦР.
Выявление ДНК при диагностике парвовирусной инфекции В19 может быть проведено в плазме крови и СМЖ в качественном или количественном формате. Дополнительным методом лабораторной диагностики является ИБ, который позволяет определять АТ к отдельным белкам-антигенам парвовируса В19. Результаты применения ИБ дают возможность уточнять стадию заболевания, выявить персистирующую форму инфекции.
Показания к применению различных лабораторных исследований. При диагностике острой и врожденной инфекции методом выбора является выявление ДНК парвовируса В19 в плазме крови и СМЖ.
Для скрининга беременных в группах риска каждый триместр целесообразно определять специфические АТ IgM и IgG, появление которых (наличие сероконверсии) указывает на первичное заражение, представляющее наибольшую угрозу для плода.
Особенности интерпретации результатов лабораторных исследований. Обнаружение ДНК парвовируса В19 в плазме крови и СМЖ подтверждает активное течение инфекции и свидетельствует о репликации вируса. Для установления факта первичной инфекции или рецидива заболевания целесообразно провести определение АТ IgM и IgG. Однократный отрицательный результат обнаружения ДНК парвовируса В19 в клетках крови не исключает репликацию вируса в мозге, костном мозге, ЖКТ, что обосновывает дополнительные исследования для определения АТ IgM и IgG. При обнаружении IgM можно делать заключение о первичной инфекции. Нарастание уровня IgG в динамике (через 2–3 недели) свидетельствует об активно текущей инфекции. Выявление в иммуноблоте АТ IgG к белку NS-1 парвовируса В19 указывают на репликацию парвовируса В19.
Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
Copyright ФБУН Центральный НИИ Эпидемиологии Роспотребнадзора, 1998 - 2020

! Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
| Стоимость услуги: | 650 руб.* Заказать |
Мазок из ротоглотки. Натощак или через 4 часа после еды, (не полоскать рот, не пить).
Слюна. Трехкратное полоскание полости рта физиологическим раствором.
Амниотическая жидкость. Условия подготовки определяются лечащим врачом.
Метод исследования: ПЦР.
ПОКАЗАНИЯ К ИССЛЕДОВАНИЮ:
- Обследование беременных из группы высокого риска (тромбоцитопения, анемия неясного генеза, апластический криз, артропатии, краснухоподобная сыпь, УЗ-признаки многоводия, водянки плода),
- Обследование лиц с тромбоцитопенией, инфекционной эритемой с суставным синдромом, гепатоспленомегалией,
- Обследование детей с симптомами врожденной инфекции,
- Исследование амниотической жидкости для подтверждения внутриутробного инфицирования плода.
ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ:
Референсные значения (вариант нормы):
| Параметр | Референсные значения |
|---|---|
| ДНК Parvovirus B19 (качественное исследование) | Не обнаружено |
Выявление ДНК парвовируса свидетельствует об инфицировании.
" ["serv_cost"]=> string(3) "650" ["cito_price"]=> NULL ["parent"]=> string(2) "25" [10]=> string(1) "1" ["limit"]=> NULL ["bmats"]=> array(3) < [0]=>array(3) < ["cito"]=>string(1) "N" ["own_bmat"]=> string(2) "12" ["name"]=> string(10) "Слюна" > [1]=> array(3) < ["cito"]=>string(1) "N" ["own_bmat"]=> string(2) "12" ["name"]=> string(43) "Амниотическая жидкость" > [2]=> array(3) < ["cito"]=>string(1) "N" ["own_bmat"]=> string(2) "12" ["name"]=> string(52) "Мазок/отделяемое ротоглотки" > > >
| Тип | В офисе |
|---|---|
| Слюна | |
| Амниотическая жидкость | |
| Мазок/отделяемое ротоглотки |
Мазок из ротоглотки. Натощак или через 4 часа после еды, (не полоскать рот, не пить).
Слюна. Трехкратное полоскание полости рта физиологическим раствором.
Амниотическая жидкость. Условия подготовки определяются лечащим врачом.
Метод исследования: ПЦР.
ПОКАЗАНИЯ К ИССЛЕДОВАНИЮ:
- Обследование беременных из группы высокого риска (тромбоцитопения, анемия неясного генеза, апластический криз, артропатии, краснухоподобная сыпь, УЗ-признаки многоводия, водянки плода),
- Обследование лиц с тромбоцитопенией, инфекционной эритемой с суставным синдромом, гепатоспленомегалией,
- Обследование детей с симптомами врожденной инфекции,
- Исследование амниотической жидкости для подтверждения внутриутробного инфицирования плода.
ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ:
Референсные значения (вариант нормы):
| Параметр | Референсные значения |
|---|---|
| ДНК Parvovirus B19 (качественное исследование) | Не обнаружено |
Выявление ДНК парвовируса свидетельствует об инфицировании.
Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
Copyright ФБУН Центральный НИИ Эпидемиологии Роспотребнадзора, 1998 - 2020

! Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
Информация только для специалистов в сфере медицины, фармации и здравоохранения!

Т.М. Чернова, к.м.н., М.Ф. Дубко, к.м.н. Санкт-Петербургский государственный педиатрический медицинский университет Минздрава России
В статье впервые представлен случай парвовирусной В19-инфекции у ребенка, протекавшей в виде кардита и миозита. В клинике отмечалось стремительное прогрессирование симптомов острого рабдомиолиза с резким повышением в крови уровня креатинфосфокиназы, лактатдегидрогеназы, миоглобина, ферритина и тропонина 1. Ультразвуковое исследование позволило выявить диффузные воспалительные изменения мышц верхних и нижних конечностей с множественными очагами дезорганизации мышечной ткани. Количественным методом ПЦР определен высокий уровень ДНК PVВ19, что позволило верифицировать парвовирусную В19-инфекцию. Быстрый клинический и лабораторный ответ у наблюдаемой пациентки явился результатом адекватной комплексной терапии, в том числе за счет раннего применения препаратов с противовирусным и иммуномодулирующим действием.
Парвовирусная В19-инфекция (PVB19) - широко распространенное заболевание, встречающееся преимущественно в детском возрасте. В международной классификации болезней десятого пересмотра (МКБ 10) парвовирусная инфекция имеет коды:
• В08.3 - эритема инфекционная (пятая болезнь);
• B97.6 - парвовирусы как причина болезней, классифицированных в других рубриках;
• B34.3 - парвовирусная инфекция неуточненная.
В 1995 г. возбудитель был классифицирован как еrythrovirus в связи с его тропизмом к предшественникам эритроцитов в костном мозге и селезенке, на поверхности которых имеется P-антиген - мембранный рецептор, облегчающий проникновение вируса внутрь клеток. В дальнейшем доказана его экспрессия на поверхности зрелых эритроцитов, мегакариоцитов, гранулоцитов, эндотелиальных и гладкомышечных клеток сосудов, гепатоцитов и других клеток [1]. У лиц с генетически детерминированной недостаточностью P-рецепторов парвовирусная инфекция не развивается [2].
Геном PVB19 представлен одноцепочечной ДНК (5596 нуклеотидов), кодирующей структурные белки VP1 и VP2 и неструктурный белок NS1. Возбудитель подвержен значительной изменчивости, что подтверждается данными иммуноферментного анализа (ИФА), полимеразной цепной реакции (ПЦР) и методом секвенирования. Обычно мутации происходят в последовательностях, кодирующих VP1 и VP2, тогда как область NS1 стабильна. В то же время изменчивость парвовируса B19 не объясняет различия в клинических проявлениях инфекции, которые зависят не только от свойств самого вируса, но и возраста, гематологического и иммунологического статуса инфицированного человека [3].
В крови ДНК PVB19 определяется в высоких концентрациях на первой неделе заболевания и быстро исчезает с появлением специфических IgM (10-12-е сутки после инфицирования), которые циркулируют в течение 3-4 месяцев и более. Антитела класса IgG обнаруживаются через 5-7 дней после появления IgM, высокоавидные IgG обеспечивают пожизненный иммунитет к инфекции. Низкий уровень ДНК-вируса (ниже 100 МЕ/мл) может определяться в сыворотке крови иммунокомпетентных лиц в течение 1-3 лет после перенесенной острой инфекции [4, 5]. При иммунной дисфункции и недостаточном количестве нейтрализующих антител в редких случаях возможно формирование персистирующей и хронической инфекции. Маркером персистирующей инфекции является выявление в крови специфических IgG к вирусному белку NS1 через 6 недель после инфицирования. При хронической инфекции у больных отмечается постоянная виремия, наличие вирусной ДНК в костномозговых клетках, может наблюдаться длительное тяжелое угнетение всех трех ростков кроветворения [6].
Репликация возбудителя сопровождается лизисом инфицированных клеток и приводит к незначительному снижению продукции эритроцитов и уровня гемоглобина в течение 7-10 суток, что не влияет на самочувствие больного. В ряде случаев возможны субфебрильная лихорадка, слабость, головная боль, насморк, першение в горле, миалгии, слабовыраженные ретикулоцито- лимфоцито-, нейтро- и тромбоцитопения. Появление в крови специфических IgM к вирусному белку VP2 и IgG к вирусному белку VP1 способствуют элиминации PVB19 из организма.
Таким образом, в большинстве случаев заболевание протекает в бессимптомной или стертой формах и практически не диагностируется. Это подтверждается данными эпидемиологических исследований - 40-60% населения серопозитивны уже к 30 годам и до 90% лиц старше 60 лет имеют антитела к парвовирусу B19 при отсутствии клинических проявлений заболевания в анамнезе [7]. У больных с гемолитической анемией и гемоглобинопатиями (серповидноклеточная анемия, наследственный микросфероцитоз, талассемии, ферментопатии) разрушение клеток-предшественников эритроцитов при репликации PVB19 и нарушение эритропоэза обычно приводит к транзиторному апластическому кризу.
Предполагается, что типичные клинические проявления парвовирусной инфекции - инфекционная эритема и артрит - развиваются у лиц с иммунной дисфункцией и обусловлены осаждением иммунных комплексов (ИК) в коже и синовиальных оболочках суставов, так как начало симптомов совпадает с появлением в крови IgM и IgG против вирусных структурных белков. Доказано, что при парвовирусной B19-инфекции существует корреляция между клиническими особенностями и специфичностью иммуноглобулинов: у пациентов с инфекционной эритемой преимущественно индуцируются IgG-антитела против кератина, тогда как при артрите - преимущественно против коллагена типа II [8].
Артропатии у детей наблюдаются достаточно редко (8-10% случаев), возникают на фоне сыпи, после ее исчезновения или могут быть основным клиническим проявлением инфекции. Характерно симметричное поражение мелких суставов рук и ног (голеностопные, межфаланговые и пястно-фаланговые), коленные или тазобедренные суставы вовлекаются редко. В области поражения отмечается отечность, болезненность, которая может затруднять самостоятельное передвижение, возможна локальная гипертермия. Течение артропатий при PVB19-инфекции доброкачественное, продолжительность процесса обычно не превышает 2-3 недель. Возможно затяжное течение без деструкции и дегенеративных изменений суставов [9].
PVB19 является одной из наиболее распространенных причин вирусных миокардитов, что обусловлено экспрессией P-антигена кардиомиоцитами. Кроме того, недавно установлена способность вируса реплицироваться в клетках эндотелия коронарных сосудов [10]. Как следствие, развивается спазм коронарной артерии, ишемия миокарда и нарушение функции сердечно-сосудистой системы в целом. У детей парвовирусные миокардиты в основном характеризуются транзиторным нарушением сердечной деятельности и способностью к полному восстановлению. Редкие случаи выраженных нарушений функции левого желудочка с формированием тяжелой декомпенсированной сердечной недостаточности без трансплантации заканчиваются неблагоприятно [11]. В то же время имеются сообщения о выздоровлении детей с декомпенсированными миокардитами после длительной комплексной терапии (экстракорпоральная мембранная детоксикация, диуретики, ингибиторы ангиотензинпревращающего фермента, иммунодепрессанты, глюкокортикоиды) [12].
В настоящее время известно, что парвовирусная B19-инфекция может протекает в виде васкулита, гломерулонефрита, гепатита, менингита, энцефалита, тромбоцитопении, нейтропении. Обнаружена связь инфекции с идиопатической тромбоцитопенической пурпурой, пурпурой Шенлейна - Геноха, гемофагоцитарным синдромом. Кроме того, описаны случаи периферической нейропатии (плечевой плексит, парезы двигательных черепных нервов), обусловленные PVB19. Имеется сообщение об обнаружения ДНК PVB19 в мышечных биоптатах у двух пациентов с воспалительной миопатией [13, 14, 15].
Атипичные формы инфекции, протекающие без характерной инфекционной эритемы, представляют значительные трудности для диагностики. В связи с этим приводим клиническое наблюдение случая парвовирусной В19-инфекции у ребенка, протекавшей в виде кардита и миозита.
Девочка 7 лет поступила в клинику СПбГПМУ с жалобами на лихорадку в течение 5 дней, выраженную слабость, сильные боли в мышцах.
Из анамнеза жизни известно, что девочка от 2-й беременности, протекавшей с угрозой прерывания на ранних сроках. Роды срочные, вес при рождении - 3220 г, длина - 50 см. Оценка по шкале Апгар 8/9 баллов.
Растет и развивается по возрасту. На диспансерном учете на состояла. Привита по возрасту в соответствии с Национальным календарем профилактических прививок. Перенесенные инфекционные заболевания: ветряная оспа, редкие ОРЗ (последнее 4 месяца назад).
Настоящее заболевание началось остро с повышения температуры тела до 38,0 С, снижения аппетита, катаральных симптомов не было. На 4-й день сохранялась фебрильная лихорадка, появились боли в эпигастральной области, однократная рвота, отечность лица. Осмотрена педиатром, назначены пробиотик, энтеросорбент. На следующий день продолжала лихорадить до 37,8 С, наросла общая слабость, стала вялой, сонливой, отказывалась от еды, жаловалась на боли в спине, верхних и нижних конечностях, в связи с чем была госпитализирована.
При поступлении состояние средней тяжести, в сознании, очень вялая. Кожа обычной окраски, мраморность, сыпи нет. Слизистая задней стенки глотки слабо гиперемирована. Небные миндалины I-II степени, налетов нет. Периферические лимфоузлы - не увеличены. Тоны сердца ясные, ритмичные, тахикардия до 140 ударов в минуту. Дыхание жесткое, хрипов нет, одышка до 44 в минуту. Живот мягкий, безболезненный. Печень, селезенка не пальпируются. Стула не было. Мочится достаточно. Менингеальные симптомы отрицательные. При обследовании в клиническом анализе крови: лейкоциты - 10,6 х 109/л, нейтрофилез до 76%, тромбоцитопения до 92 х 109/л, СОЭ 3 мм/час. В биохимическом анализе крови: аспартатаминотрансфераза (АСТ) - 161 Ед/л (норма до 38), лактатдегидрогеназа (ЛДГ) - 555 Ед/л (норма до 220). Общий анализ мочи - без патологии.
В течение ночи нарос отек лица, появился акроцианоз. С подозрением на миокардит по тяжести состояния переведена в реанимационное отделение (6-й день болезни).
Диагноз острого кардита подтвержден по результатам инструментального исследования - Rg-графии органов грудной полости (умеренное увеличение размеров сердца, сглаженность талии) и ЭХО-кардиографии (гипертрофия левого и правого желудочков, без нарушения сократительной способности и диастолической дисфункции, сепарация листков перикарда жидкостью по задней стенке ЛЖ до 19 мм), а также лабораторных данных - повышение уровня натрийуретического пептида (NT-proBNP) до 7020 (норма до 125,0).
Кроме того, в течение первых 5 дней наблюдения прогрессировали симптомы миопатии – отек кистей, стоп и голеней, резкая болезненность мышц конечностей при пальпации, невозможность самостоятельных движений. Учитывая выраженный болевой синдром, диффузное снижение мышечного тонуса и мышечной силы конечностей до 1-2 баллов, проведено МРТ-исследование (исключены объемные образования и воспалительные процессы в головном и спинном мозге). По данным электронейромиографии (ЭНМГ) исключена полинейропатия. В то же время при ультразвуковом исследовании выявлены диффузные воспалительные изменения мышц верхних и нижних конечностей (выраженный отек подкожной жировой клетчатки, повышенная васкуляризация мышц, множественные очаги дезорганизации мышечной ткани до 1-2 мм в диаметре). При динамическом наблюдении в крови наблюдались признаки нарастающего рабдомиолиза в виде значительного повышения содержания клеточных ферментов (КФК до 113571 Ед/л (норма до 168), КФК-МВ до 273,4 Нг/мл (норма до 3,4), АЛТ до 742 Ед/л (норма до 55), АСТ до 2459 Ед/л, ЛДГ до 3769 Ед/л), а также ферритина до 302 мкг/л (норма до 120), миоглобина до 9283,4 нг/мл (норма до 65,8) и тропонина 1 до 0,51 нг/мл (норма до 0,01). В клиническом анализе крови на фоне нарастания лейкоцитоза до 20,8х109/л и СОЭ до 26 мм/час наблюдалось снижение количества эритроцитов до 2,8 х 1012/л, гемоглобина до 76 г/л, тромбоцитов до 81 х 109/л. В моче - транзиторные признаки инфекционной нефропатии (белок до 3 г/л, эритроциты - до 5-8 в поле зрения, гиалиновые цилиндры до 2-4).
В процессе дифференциального диагноза был получен отрицательный результат иммуноблота на антинуклеарные антитела и антитела при полимиозите, что позволило исключить и аутоиммунный генез рабдомиолиза. С целью выявления этиологической причины воспалительной миопатии проведено лабораторное исследование на инфекционные возбудители. Учитывая фебрильную лихорадку, боли в животе, боль в мышцах, кардиопатию, лабораторные маркеры рабдомиолиза, ребенок был обследован на энтеровирусную инфекцию, иерсиниозы, герпесвирусные инфекции - результаты отрицательные. Количественным методом ПЦР в крови выявлена ДНК PVВ19 (5,2 х 103 МЕ/мл), что в сочетании с клиническими проявлениями (выраженные анемия и тромбоцитопения) позволило диагностировать парвовирусную В19-инфекцию.
Получала комплексную этиопатогенетическую терапию, которая включала рекомбинантный человеческий интерферон-альфа ректально (Виферон), иммуноглобулин человека внутривенно два введения через 3 дня, метилпреднизолон 3 дня, фосфокреатин, ибупрофен, проводилась коррекция электролитных нарушений и диуреза. На фоне лечения через 2 дня перестала лихорадить, с 3-го дня отмечалось улучшение самочувствия, аппетита, с 6-го дня зафиксирована стабилизация миолиза и сердечно-сосудистой деятельности, начала самостоятельно переворачиваться и садиться в постели, переведена в педиатрическое отделение кардиоревматологического профиля. Со второй недели к терапии добавлены комплекс витаминов группы B, массаж, лечебная физкультура. На третьей неделе (4-я неделя болезни) движения восстановились в полном объеме, начала самостоятельно ходить. По результатам контрольного лабораторного и инструментального обследования отмечались остаточные признаки мышечного и сердечного вовлечения. Выписана в удовлетворительном состоянии на 25-й день наблюдения с диагнозом: парвововирусная В19-инфекция, смешанная форма (кардит, миозит). Осложнение: острый рабдомиолиз, интраинфекционная нефропатия.
Острый миозит является достаточно редкой патологией детского возраста и возникает в основном как осложнение гриппа. При этом выраженность проявлений варьирует от легкой миалгии до тяжелого рабдомиолиза с развитием декомпенсации миокарда и нарушением мышечных функций. Мы наблюдали первый случай парвовирусной В19-инфекции у ребенка, протекавшей в виде сочетанного поражения сердца и скелетной мускулатуры.
Парвовирус B19 как причина миозита регистрируется крайне редко. В настоящее время в зарубежной литературе имеются лишь единичные сообщения о данной патологии. В связи с малым количеством наблюдений патогенез миопатии при парвовирусной В19-инфекции остается неясен. Так, в двух случаях у детей миозит развился во время сыпи (стадия продуцирования антител и образования ИК), что позволило авторам предположить иммунокомплексную природу миолиза [16, 17]. Однако Ishikawa A. с соавт. наблюдали случай нарастания мышечной слабости и КФК в крови у ребенка с легкими симптомами респираторной инфекции, контактного с больной инфекционной эритемой сестрой [18]. Несмотря на отсутствие экзантемы, диагноз был подтвержден выявлением в крови специфических IgM и ДНК PVB19, а острый рабдомиолиз был расценен как возможное проявление парвовирусной B19-инфекции.
В приведенном наблюдении начало кардита и миопатии у ребенка в первые дни заболевания также свидетельствовало против иммунокомплексной природы поражения. К тому же введение иммуноглобулина во время активной циркуляции вируса в крови так и не привело к развитию иммуноопосредованных симптомов (сыпи и артропатии) [19].
До настоящего момента прямых доказательств роли PVB19 в развитии миозита не получено. Однако быстрый клинический и лабораторный ответ у наблюдаемой пациентки явился результатом адекватной комплексной терапии, в том числе за счет раннего применения препаратов с противовирусным и иммуномодулирующим действием. Это может служить косвенным доказательством прямого вирусного эффекта в развитии миопатии.
Таким образом, PVB19 следует рассматривать как потенциальный причинный фактор у пациентов с миозитом, особенно при отсутствии инфекционной эритемы. Для выявления истинных механизмов поражения мышечных клеток необходимы углубленные исследования, в том числе с проведением биопсии пораженных мышц.
Литература
Читайте также:
- Кто создает вирусы гриппа
- Ихтиоз это вирусное заболевание
- Как принимать арбидол при ротавирусе
- Прививка от гриппа французская ваксигрипп отзывы
- Можно ли гулять при энтеровирусе
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции

