Наркоз и токсический гепатит
Причины, симптомы, диагностика, осложнения и лечение болезни.
Токсический гепатит – это заболевание печени, острого или хронического течения, развивающееся в результате попадания в организм химических или других вредных веществ (лекарственные препараты, алкоголь, токсины грибов), токсического действия их на клетки печени, сопровождающее воспалением клеток и их смертью, и проявляющееся увеличением печени в размерах, болью в правом подреберье и прогрессирующей желтухой.
Причины токсического гепатита

Попадание в организм вредных веществ может быть случайным, профессиональным (деятельность работы) или умышленным (желаемым). Вредные вещества, которые попадают в организм и поражают печень, называются печёночными ядами. Они попадают в организм по разным путям. Через пищеварительный тракт: рот ? желудок ? кровь ? печень. Через дыхательную систему: нос ? легкие ?кровь ? печень. Через кожу яды тоже могут проникнуть в кровь, а потом и в печень. Проникая в кровь одни печёночные яды, могут оказывать прямое действие на печёночную клетку (гепатотропные яды), нарушая её функцию и жизнедеятельность. Другие виды ядов, нарушающие кровообращение в мелких сосудах питающих печень, это приводит к недостатку кислорода в клетках и их смерть, с последующим нарушением функции органа.
Печёночные яды имеют разное происхождение:

1. Лекарственные препараты, в дозах назначенных лечащим врачом, обладают лечебным эффектом, при однократном принятии большой (токсической) дозы одного из препаратов этих групп, происходит токсическое повреждение печени и развитие острого токсического гепатита.

- сульфаниламидные препараты: Бисептол, Сульфадиметоксин
- противовирусные: Интерферон, Амантадин;
- противотуберкулёзные: Фтивазид, Тубазид;жаропонижающие: Парацетамол, Аспирин
- противосудорожные: Фенобарбитал и другие.
2. Промышленные яды попадают в организм при вдыхании или через кожу, при попадании в организм больших доз, развивается острое поражение печени с гибелью её клеток и замещением жировыми клетками, при многократном попадании малых доз, развивается хронический токсический гепатит.
- мышьяк – выделяется на металлургических комбинатах;
- фосфор – содержится в фосфорных удобрениях, применяется для обработки металла
- пестициды – используются в сельском хозяйстве, для уничтожения сорняков
- хлорированные углеводороды– компоненты нефти.
- альдегиды (например: ацетальдегид) используется в промышленном хозяйстве для получения уксусной кислоты
- фенолы – содержатся в антисептиках используемые для дезинфекции, содержится в консервах
- инсектициды – используются в сельском хозяйстве, для борьбы с вредными насекомыми

3. Алкоголь - хроническое и чрезмерное употребление алкоголя, в особенности плохого качества приводят к токсическим поражениям печени. 20-40 грамм спирта в сутки для мужчин, и до 20 грамм для женщин, считаются безопасными дозами, в более высоких дозах, он оказывает, токсический эффект.
Весь принятый алкоголь из пищеварительного тракта с кровью поступает в печень. В печени происходит активная обработка поступившего алкоголя. Основным компонентом преобразования алкоголя в печени является его взаимодействие с ферментом алкоголь дегидрогеназа. В результате такого ферментативного преобразования распада алкоголя приводит к образованию ацетальдегида. Ацетальдегид является достаточно токсичным веществом, под действием которого, происходит нарушения различных химических реакций в печени (в частности и жирового обмена). Происходит накопление жирных кислот и замещение печёночных клеток жировой тканью.
4.Растительные яды (яды сорняков: горчак, крестовник; яды грибов: бледная поганка), обладают гепатотропным действием (действуют прямо на печёночную клетку, нарушая её жизнедеятельность и замещение её жировой тканью), в результате чего развивается клиника острого токсического гепатита.
Симптомы токсического гепатита
Признаки острого токсического гепатита:

В лёгких случаях может протекать почти без симптомов, обнаруживается лишь при групповом обследовании (например: употребление ядовитых грибов).
В более тяжелых случаях может проявиться в виде следующих симптомов:
- Боли в правом подреберье, возникают внезапно, через 2-5 дней после проникновения гепатотропного яда в организм, являются результатом растяжение капсулы увеличенной печенью (из-за острого воспалительного процесса в ней);
- Признаки интоксикации организма: повышение температуры тела >38 0 С, общая слабость, отсутствие аппетита, тошнота, рвота (может быть с кровью), боли в суставах;
- Кровотечения из носа, дёсен, мелкие точечные кровоизлияния на коже, эти проявления являются результатом, разрушающего действия токсина на стенки сосудов;
- Влияние на психику больного в виде возбуждённости или заторможенности, нарушение ориентации в пространстве, тремора, так как яды имеют способность оказывать токсический эффект и на нервные клетки;
- Прогрессирующая желтуха, темная моча, светлый кал (жирный, блестящий) появляется одновременно с признаками интоксикации, и является результатом нарушения оттока желчи по мелким внутрипечёночным желчевыводящим путям;
- Увеличение печени в размере, в результате острого воспаления печёночных клеток и замещение их жировой тканью (жировая дистрофия печени)
Признаки хронического токсического гепатита:

- Периодические боли в правом подреберье, средней интенсивности, усиливающие после приёма пищи;
- Тяжесть в правом подреберье, связано с увеличением печени;
- Субфебрильная температура тела 37-37,5 0 С;
- Тошнота, рвота, снижение аппетита, горечь во рту, вздутие живота, понос, эти проявления развиваются в результате нарушения оттока желчи;
- Утомляемость, снижение работоспособности;
- Кожный зуд, чешется кожа из-за скопления желчных кислот;
- Увеличение печени и селезёнки.
Эти симптомы могут на время утихать (ремиссия), и опять проявляться (обостряться).
Осложнения токсического гепатита
В лёгких случаях токсический гепатит полностью излечивается. В остальных случаях может осложниться одним из следующих заболеваний:
1. Печеночная недостаточность, является результатом гибели печёночных клеток, замена их жировыми клетками и нарушение её функций, проявляется следующими симптомами:
- Отеки (в результате нарушения белкового обмена);
- Желтуха
- Кровотечения (снижается выработка факторов свёртывания крови);
- Похудание организма (из-за недостатка насыщения организма белками, жирами, углеводами, энергией, вырабатываемые печенью);
- Печёночная энцефалопатия (психические и нервно-мышечные нарушения), развивается в результате нарушения токсической функции печени;
2. Печёночная кома, прогрессирующие нарушение печени и центральной нервной системы (нарушение сознания, рефлексов, судороги и другие), результатом может быть смерть;
3. Цирроз печени, хроническое заболевание, в результате которого происходит смерть клеток печени и замещение их соединительной тканью.
Лечение токсического гепатита

В первую очередь необходимо предотвратить контакт с ядом. Чтобы предотвратить попадание яда в кровь, а в дальнейшем и в печень, необходимо его удалить из желудка (в тех случаях, когда он попал в пищеварительный тракт), путём искусственно вызванной рвоты. Принять удобную позу для рвоты (полусидящее положение с наклоном головы вперёд), с помощью раздражения корня языка, в результате надавливания на него пальцем (но это применяется не во всех случаях). Для ослабления воздействия яда на стенки желудка, можно выпить отвар семян льна, принять внутрь активированный уголь. При наличии повышения температуры, можно применять холодные компрессы на лоб. Пока всё это мы делаем, срочно вызываем скорую медицинскую помощь, или срочно обратиться в специализированное медицинское учреждение (отделение токсикологии).
При проявлении признаков острого токсического гепатита необходимо больного срочно госпитализировать, где будут проводиться под наблюдением лечащего врача, следующие методы лечения:
Лечение токсического гепатита
- Постельный режим
- Зондовое промывание желудка для очищения желудка от оставшегося яда, попавшего в желудок.
- Выведение ядов из организма (активированный уголь,капельницы с растворами электолитов), гемосорбция, плазмоферез (очищение крови от токсических веществ). Активированный уголь, всасывает на своей поверхности токсины, оставшиеся в желудке, предотвращая их попадание в кровь.
- Витаминотерапия - применение витаминов группы В и С.
- Гепатопротекторы (Лиф 52, Гептрал, Эссенциале). Эти препараты активно участвуют в процессах размножения клеток печени и их восстановлении после повреждения. Лиф 52 назначается по 2 таблетки 3 раза в день, продолжительность приёма индивидуальна, в зависимости от степени поражения печени.
- Желчегонные препараты (Холосас, Холензим). Вместе с желчь из печени выводится часть токсических веществ. Желчегонные препараты активизируют этот процесс.
- Антидоты (при отравлении грибами, Атропин). Химические вещества, которые специфически воздействуют на токсические агенты или на рецепторы клеток, препятствуя токсическому повреждению.
Гепатопротекторы растительного происхождения для лечения токсического гепатита
Гепатопротекторы – повышают устойчивость печени к вредным воздействиям (лекарств, алкоголя, растительных и химических ядов). Ускоряют восстановление поврежденных клеток. Усиливают обезвреживающую функцию печени.
Диета при токсическом гепатите
Употребление алкоголя и курения категорически запрещено. Питаться нужно маленькими порциями и часто, таким образом, улучшается выведение желчи. Пища не должна быть жирной, жаренной, солёной, с отсутствием приправ, быть богата витаминами и растительной клетчаткой. Основными продуктами в рационе должны быть, свежие овощи и фрукты (различные салаты), бобовые (фасоль, горох). Употреблять только сливочные и растительные масла.Употреблять в пищу только легкоусвояемое мясо (курица, кролик). Полностью отказаться от копчёностей, консервов, острых и жирных блюд. Делать разгрузочные дни, один день в неделю употреблять только овощи или фрукты. Лицам работающих на промышленных предприятиях, с воздействием вредных веществ, необходимо ежедневное употребление молочных продуктов.
Учреждение здравоохранения
"25-я центральная районная поликлиника
Московского района г. Минска"
Поражение печени может произойти из-за накопления жира в ее клетках или их воспаления. При первых симптомах заболевания необходимо приступить к лечению.
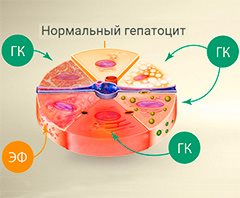
В борьбе с воспалением клеток печени (гепатоцитов) помогают препараты, содержащие глицирризиновую кислоту (ГК) и эссенциальные фосфолипиды (ЭФ).
Чтобы добиться должного эффекта от лечения, стоит выбирать препараты, прошедшие клинические исследования.

- оптимальный состав активных компонентов;
- противовоспалительное действие;
- благоприятный профиль безопасности;
- безрецептурный отпуск из аптек.

Стоит помнить: комплексный подход в лечении печени — наиболее результативный.

Чтобы не переплачивать за лечение, стоит выбирать препараты, обладающие фиксированной доступной ценой.
Печень – крупнейшая многофункциональная железа в пищеварительной системе и один из важнейших органов обмена веществ, обеспечивающий полноценную работу всего человеческого организма. Ее заболевания в большинстве своем протекают в скрытой форме и бурно проявляются уже на серьезных стадиях. При малейших симптомах поражения печени следует обратиться к врачу.
Лучше всего, конечно, беречь этот чувствительный, но лишенный болевых рецепторов орган и уделять внимание мерам профилактики. Имейте в виду, что восстановить печень значительно сложнее, чем нанести ей вред.
Виды и причины поражения печени
Итак, печень – самая крупная железа в организме. На нее ложится огромная нагрузка по синтезу гормонов и ферментов, по нейтрализации токсинов в крови, по многим обменным процессам в организме. При этом печень крайне подвержена самым разным воздействиям. По этой причине список возможных поражений достаточно широк:
Определить, что больна именно печень, бывает довольно сложно. Сам этот орган лишен нервных окончаний и не посылает болевых сигналов в мозг. Боли появляются на поздних стадиях тяжелых патологий, когда печень сильно увеличена и давит на печеночную капсулу. Поводом проверить печень может быть появление следующих симптомов:
- потеря аппетита, вялость, раздражительность;
- тошнота, горечь во рту;
- склонность к аллергии;
- желтуха – окрашивание кожи и белков глаз в желтый цвет, мочи – в коричневый, за счет повышенной выработки билирубина;
- тянущие боли в правом подреберье;
- изменение консистенции стула, изменение массы тела;
- повышенный уровень холестерина;
- нарушение пищеварения, связанное с недостатком ферментов.
В диагностике заболеваний печени используются анализы крови и мочи, УЗИ, компьютерная или магнитно-резонансная томография, лапароскопия, биопсия.
В зависимости от природы поражения печени, назначается медикаментозное лечение. Оно обязательно должно сопровождаться соблюдением специальной диеты и борьбой с вредными привычками. В тяжелых случаях (цирроз, рак) зачастую необходимо хирургическое вмешательство. В качестве примера приведем некоторые иллюстрации методов лечения:
К выбору средств народной медицины следует подходить крайне осторожно и ни в коем случае не применять их для самолечения, пренебрегая походом к врачу. Помните, что противопоказания есть не только у современных химических препаратов, но и у традиционных натуральных средств. Даже самые безобидные, казалось бы, методы народной медицины при неправильном применении могут серьезно усугубить протекание болезни. Дело в том, что ни один природный компонент в естественном виде не содержится изолированно, а сопутствующие ему биологически активные вещества могут нанести вред. Безопасные лечебные пропорции должны быть тщательно изучены, а эффективность действующих веществ нуждается в клиническом подтверждении. Именно поэтому так важно предварительно проконсультироваться с врачом. Скорее всего, он назначит вам именно лекарственный препарат, а нее его альтернативу, относящуюся к средствам народной медицины.
Прежде всего, необходимо сократить влияние поражающих факторов, которые так же разнообразны, как и заболевания печени. Беспорядочные половые связи, алкоголь, курение, работа на вредных производствах, бездумное применение лекарств без назначения врача, несвежие или заведомо вредные для здоровья продукты – все это следует исключить.
Если вы уже перенесли гепатит или любые другие заболевания печени, необходимо как минимум дважды в год проходить обследование и постоянно соблюдать диету. Показаны легкие физические нагрузки, прогулки на свежем воздухе, санаторно-курортное лечение, поддерживающая лекарственная терапия.
Для восстановления гепатоцитов показан прием гепатопротекторов. Их основой могут быть следующие действующие вещества:
- Глицирризиновая кислота – оказывает противовоспалительное, антиоксидантное и антифибротическое действие. Клинические исследования подтвердили клинический эффект и благоприятный профиль безопасности глицирризиновой кислоты при лечении алкогольной и неалкогольной жировой болезни печени. Достоверно зафиксированы факты уменьшения воспаления, степени фиброза.
- Эссенциальные фосфолипиды – основа структуры клеточных и внутриклеточных мембран, оказывают цитопротекторное действие, нормализуют белковый и липидный обмены, предотвращают снижение уровня ферментов и других активных веществ в печени, восстанавливают печеночную функцию. Данные биологически активные вещества присутствуют в большинстве наиболее известных гепатопротекторов, но являются скорее средством профилактики, а не лечения. Стоит также отметить, что в сочетании с глицирризиновой кислотой существенно повышается ее биодоступность, а значит и терапевтическое воздействие последней.
По данным агентства Synovate Comcon, препарат на основе глицирризиновой кислоты и фосфолипидов занимает первое место по назначению терапевтами для лечения заболеваний печени в крупнейших городах России. Кроме того, глицирризиновая кислота включена в рекомендации Азиатско-Тихоокеанской ассоциации по изучению печени (APASL) для лечения заболеваний печени и разрешена для применения Европейским медицинским агентством (EMA).
В России данный состав с 2010 года включен в Перечень жизненно необходимых и важнейших лекарственных препаратов для медицинского применения в качестве препарата для лечения заболеваний печени. Стоит отметить, что стоимость лекарственного средства на основе этих действующих веществ зафиксирована в Государственном реестре предельных отпускных цен, что гарантирует доступную цену.
Экспериментальные модели токсического гепатита вызывали внутрижелудочным и интраперитонеальным введением раствора тетрахлорметана. Для оценки тяжести поражения печени были применены биохимический и морфологический методы исследования. На основании полученных данных на обеих моделях подтвержден токсический гепатит. Наиболее тяжелые поражения печени возникают при интраперитонеальном введении тетрахлорметана. Внутрижелудочное введение тетрахлорметана позволяет снизить уровень летальности (до 10 %), избежать нарушения целостности кожных покровов и уменьшить проявление болевого синдрома у животных.
Ключевые слова: тетрахлорметан, гепатит.
Актуальность. Доклинические исследования перспективных гепатопротекторов проводятся, как правило, на классической модели токсического хронического гепатита, вызванного внутрижелудочным или интраперитонеальным введением 50 % масляного раствора тетрахлорметана [3]. Четыреххлористый углерод оказывает прямое повреждающее действие на печень посредством образования ковалентных связей с клеточными макромолекулами, что, в свою очередь, приводит к выраженному повреждению мембран гепатоцитов, активации процессов липопероксидации, дисбалансу в работе ферментативного звена антиоксидантной системы организма, нарушению метаболизма липидов, белков, углеводов 4. Основными механизмами действия уже известных или изучаемых гепатопротекторов являются стабилизация клеточных мембран, антиоксидантный, детоксицирующий, противовоспалительный, антихолестатический, антифибротический, регенерирующий эффекты и др. [1, 2, 8]. Вследствие этого, для получения объективных результатов необходимо, чтобы выбранная методика наиболее полно отражала процессы повреждения печени.
Цель исследования: провести сравнительную характеристику моделей токсического хронического гепатита, вызванных внутрижелудочным и интраперитонеальным введением 50 % масляного раствора тетрахлорметана на основании биохимических и морфологических показателей.
50 % масляный раствор тетрахлорметана в дозе 2,0 мл/кг вводили 40 крысам, которые были разделены на 2 группы по 20 особей в каждой. У первой группы животных токсический гепатит вызывали внутрижелудочным введением тетрахлорметана 2 раза в неделю в течение 3-х недель. Забор материала (сыворотки крови и образцов тканей печени) осуществляли путем декапитации под эфирным наркозом на 20-й день от начала эксперимента. Второй группе масляный раствор тетрахлорметана вводили интреперитонеально 1 раз в неделю в течение 4-х недель, забор материала проводили на 23-й день эксперимента. Группа контроля (интактные животные) состояла из 10-ти крыс.
Активность перекисного окисления липидов (ПОЛ) в тканях печени оценивали по содержанию малонового диальдегида (МДА) в реакции с тиобарбитуровой кислотой. О состоянии антиоксидантной системы судили по активности антиокислительного фермента глутатионпероксидазы (ГПО).
Для светооптического морфологического исследования вырезали образцы из большой доли печени, фиксировали в 10 % растворе нейтрального формалина, подвергали стандартной обработке с последующей заливкой в парафиновые блоки. Срезы толщиной 5–7 мкм окрашивали гематоксилином Лилл-Майера и 1 % эозином, а также проводили гистохимическое окрашивание для выявления соединительной ткани по Ван Гизону пикрофуксином. Морфометрический анализ срезов был проведен при ×400 увеличении микроскопа с использованием окулярной сетки на 289 точек. Подсчет проводили в 15-ти полях зрения каждого препарата. В тканевом микрорайоне печени подсчитывали объемную плотность гепатоцитов с дистрофическими и некротическими изменениями, синусоидов, соединительной ткани, определяли объемную плотность каждого структурного компонента.
Статистическая обработка результатов включала подсчет среднеарифметических значений (M) и их ошибки (m). Для выявления достоверности полученных значений применяли тест множественных сравнений Дункана (Duncan’s test, ANOVA) с использованием пакета компьютерных программ Statistica 6.0. Отличия считали достоверными при р
Государственная лицензия ФГБОУ ВО НГМУ Минздрава России
на образовательную деятельность:
серия ААА № 001052 (регистрационный № 1029) от 29 марта 2011 года,
выдана Федеральной службой по надзору в сфере образования и науки бессрочно
Свидетельство о государственной аккредитации ФГБОУ ВО НГМУ Минздрава России:
серия 90А01 № 0000997 (регистрационный № 935) от 31 марта 2014 года
выдано Федеральной службой по надзору в сфере образования и науки
на срок по 31 марта 2020 года
Адрес редакции: 630091, г. Новосибирск, Красный проспект, д. 52
тел./факс: (383) 229-10-82, адрес электронной почты: mos@ngmu.ru
Средство массовой информации зарегистрировано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзор) —
Свидетельство о регистрации СМИ: ПИ № ФС77-72398 от 28.02.2018.
 |
|
08.02.2016 11.01.2016 28.12.2015
Цель исследования. Оценить изменение иммунологических показателей у крыс с хроническим токсическим гепатитом под влиянием адопции аллогенного ликвора, обладающего различной степенью иммунотропной активности. Материал и методы исследования. В работе приведены данные, полученные от 32 крыс линии Brown Norway, весом 160-180г. Оперативное вмешательство осуществлялось под гексеналовым наркозом (доза - 70мг./кг., внутрибрюшинно). Для воспроизведения модели хронического токсического гепатита (ХТГ) был использован гелиотрин, вводимый внутрибрюшинно в дозе 50 мг/кг массы тела один раз в неделю в течение 35 дней [2]. Адопция цереброспинальной жидкости (ЦСЖ) в III желудочек мозга проводилась раз в сутки согласно стандартной стереотопографии на аппарате WPI (Berlin, Germany) [6]. Количественное определение показателей иммунного статуса проводили с использованием набора дифференцировочных маркеров (Sandoz Pharma AG, Switzerland). Статистическая обработка результатов проводилась с расчетом критерия Стъюдента, различия считали достоверными при значении p≤0,05. Полученные результаты и их обсуждение. В проведенных ранее экспериментах было показано, что крысы Brown Norway (BN) с ХТГ имеют достоверно сниженные показатели иммунного статуса по сравнению с нормальными показателями интактных крыс. Примечательно, что при двукратном (в среднем) снижении количества клеток оцениваемых лейкоцитарных элементов, процентное соотношение показателей иммунограммы не изменялось. Вероятно, число всех типов клеток лейкоцитарного звена уменьшилось за счет генерализованного угнетения метаболической функции печени и последующего подавления центральных звеньев иммунорегуляции, что подтверждается исследованиями отдельных авторов [10]. В этой связи, проведено три серии экспериментов направленных на определение степени вовлеченности иммунокомпетентного микроокружения гипоталамуса в механизмы супрессирования иммунной системы при ХТГ. Задачей первой экспериментальной группы крыс являлось изучение влияния адопции аллогенного ликвора, полученного от интактных крыс линии Sprague Dawley (SD) на показатели иммунного статуса при ХТГ. Полученные данные свидетельствуют, что ни один из оцениваемых показателей, за исключением общего пула лимфоцитов, каких-либо значимых количественных изменений не претерпел, количество нейтрофилов, мононуклеаров, В-лимфоцитов, Т-лимфоцитов, NK-клеток и лейкоцитов в целом незначительно колебалось в ту или иную сторону. Лишь абсолютное число лимфоцитов в периферической крови животных изучаемой группы достоверно возросло на 9% в сравнении с их количеством в крови контрольной группы крыс с ХТГ, но без манипуляций с составом ЦСЖ. (табл.1). Таблица 1. Влияние адопции аллогенного ликвора на иммунный статус крыс с ХТГ показатели иммунитета (×10 6 /L) крысы с ХТГ (контроль) ХТГ + адопция интактной ЦСЖ ХТГ + адопция ЦСЖ от крыс с ХТГ крысы без ХТГ + адопция ЦСЖ от крыс с ХТГ Примечания: во всех сравниваемых группах n = 8 a - достоверно по отношению к контрольной группе крыс b - достоверно по отношению к группе крыс с адопцией аллогенной интактной ЦСЖ * - достоверно по отношению к группе интактных крыс Таким образом, исследованиями продемонстрировано, что аллогенная адопция ЦСЖ полученной от интактных крыс, не оказывает значимого влияния на показатели активности иммунной системы крыс с моделью ХТГ. По данным ряда авторов, стимуляция центральных звеньев иммунорегуляции ведет к избирательной модуляции нарушенных звеньев периферической иммунной системы, возвращая супрессированные либо гиперактивированные механизмы реализации иммунных процессов к физиологически нормальным значениям [5]. Казалось бы, внутрижелудочковое введение нормальной ЦСЖ, имеющей физиологичный состав иммунотропных компонентов и обладающей способностью модулировать подавленную активность центра поддержания иммунного гомеостаза, должно ослабить интенсивность иммуносупрессии у крыс с токсическим гепатитом, однако этого не произошло. Отсутствие какого-либо воздействия адопции ЦСЖ на активность иммунитета экспериментальной группы крыс, возможно, обусловлено неспособностью периферической иммунной системы прореагировать на смену вектора центральной эфферентной импульсации (в условиях "искусственной оптимизации" состава ЦСЖ), за счет тотального подавления анаболических (пластических) процессов в организме реципиентов ЦСЖ, имеющих печеночную дисфункцию. Результаты, полученные во второй серии экспериментов, направленных на изучении роли ликвора полученного от аллогенных крыс-доноров, на которых за 14 дней до забора ЦСЖ была воспроизведена аналогичная модель ХТГ, демонстрируют, что животные изучаемой группы с ХТГ (реципиенты ЦСЖ) подверглись значительному снижению показателей иммунного статуса, вследствие адопции ликвора. Так, количество лейкоцитов в изучаемой группе было достоверно снижено в сравнении с контрольной группой крыс с ХТГ (без адопции ЦСЖ) и в сравнении с группой крыс (первой экспериментальной серии) с ХТГ и с адопцией ЦСЖ от интактных животных линии SD. Аналогичные изменения были характерны и в отношении нейтрофилов и клеток мононуклеарного ряда. Общий пул лимфоцитов, включая Т- и В-популяции и натуральные киллеры, также подвергся значительному снижению числа клеток в периферической крови. Анализ показателей иммунограммы позволяет предполагать, что адопция аллогенной ЦСЖ в гипоталамическое ликворное микроокружение крыс реципиентов ЦСЖ ведет к угнетению активности иммуноцитов периферической крови за счет сбоя центральных механизмов поддержания иммунного гомеостаза. Указанное подавление иммунитета крыс реципиентов ликвора, полученного от особей с моделью патологии усугубленной с течением времени, возможно, обусловлено замещением собственного ликвора, донорским ликвором, с составом биоактивных субстанций (главным образом цитокинов) истощенным моделью токсического гепатита более прогрессировавшего у крыс доноров ЦСЖ. Таким образом, адопция "декомпенсированного" ликвора от крыс с прогрессировавшей с течением времени моделью токсического гепатита индуцирует ускорение повреждения функций периферической иммунной системы реципиентов ЦСЖ, за счет экспериментально спровоцированной дезрегуляции механизмов поддержания иммунного гомеостаза в гипоталамусе, как результат адопции "декомпенсированного" (истощенного) ликвора. С другой стороны, возможен и иной механизм снижения активности периферической иммунной системы. По утверждению ряда авторов, угнетение периферических иммунных процессов может являться результатом компенсаторного действия центральных иммунотропных импульсов, направленных на предотвращение цитокиновой гиперсекреции в условиях патологии [4;9]. В третьей серии экспериментов оценивалось влияние адопции аллогенной ЦСЖ от крыс с моделью ХТГ на состояние иммунной системы изначально интактных крыс. Анализ полученных данных позволяет судить о том, что аллогенная адопция ЦСЖ от крыс с моделью патологии ведет к повышению показателей иммунограммы у крыс реципиентов ЦСЖ. В частности, общее количество лейкоцитов повысилось на 13% в сравнении с тем же показателем у интактных крыс. Число нейтрофилов, клеток мононуклеарного ряда и общий пул лимфоцитов также статистически значимо возросли. Среди клеток лимфоцитарного ряда достоверное увеличение клеточности имело место среди В-популяции лимфоцитов и натуральных киллеров. В то же время, общее число Т-лимфоцитов и, в частности, их хелперная и эффекторная субпопуляции не проявили значимого увеличения, однако тенденция к повышению числа клеток наблюдалась для обеих оцениваемых субпопуляций Т-клеток. Таким образом, показано, что центральное введение ЦСЖ, полученной от доноров с моделью гепатита, стимулирует рост показателей активности периферической иммунной системы. Возможным механизмом действия адоптированной ЦСЖ является адаптационное усиление интенсивности иммунорегуляторных импульсов со стороны центра поддержания иммунного гомеостаза в гипоталамусе. Указанная интенсификация иммуностимулирующих гипоталамических импульсов, возможно, обусловлена составом адоптированной ЦСЖ, свидетельствующим о глубоком подавлении активности периферической иммунной системы, вызванном моделью токсического гепатита в организме донора ЦСЖ. Вероятно, обедненный цитокиновый состав адоптированной ЦСЖ индуцирует компенсаторное повышение концентрации цитокинов в ЦСЖ и, следовательно, периферической крови реципиентов ликвора, т.е. происходит активация иммунной системы экспериментальной группы крыс без ХТГ, обусловленная искусственно спровоцированной ложной афферентной сигнализацией в центр поддержания иммунного гомеостаза. Предложенная гипотетическая схема стимуляции иммунитета изначально интактных крыс реципиентов ЦСЖ согласуется с утверждением отдельных авторов о том, что введение различных иммунологически активных субстанций в ІІІ желудочек мозга позволяет изменять вектор иммунотропных влияний гипоталамуса в желаемом направлении [7;8]. Заключение.
Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу. Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Copyright © Иммунитет и инфекции
|


