Напряженность иммунитета при гриппе
Донник Ирина Михайловна
Директор ГНУ Уральского научно-исследовательского ветеринарного института (УрНИВИ).
Член-корреспондент РАСХН, профессор
Шилова Евгения Николаевна
Зав. отделом инфекционной патологии ГНУ УрНИВИ Кандидат ветеринарных наук, доцент
В последние годы большое внимание уделяется профилактике высокопатогенного гриппа птиц, как инфекции, представляющей возможную угрозу человечеству. Одним из наиболее эффективных средств профилактики гриппа А птиц является иммунопрофилактика. Вакцинация, не препятствуя инфицированию птицы, защищает ее от клинического проявления заболевания, увеличивая порог вирусной инфекции, необходимый для инфицирования привитой птицы, а также воздействует на эпизоотический процесс, ограничивая пути передачи и распространение инфекции (Ямникова С.С, Смоленский В.И., Хохлачев О.Ф. и др., 2007).
Как известно, эффективность применения вакцины оценивают по трём показателям: уровню поствакцинального иммунитета, выраженного в установлении протективных титров антител, заболеваемости и смертности птиц при экспериментальном или полевом инфицировании. Согласно "Инструкции по применению вакцины против гриппа птиц инактивированной эмульгированной" (2006), данная вакцина должна вызывать не менее чем у 80 % вакцинированных птиц накопление в крови антител к вирусу гриппа птиц в титре 1/16 со штаммом вируса, имеющего иную антигенную форму, иммунитет формируется в течение 28 дней после вакцинации.
Установлено, что интенсивность иммунного ответа у животных и птиц может отличаться на разных территориях, в случае, если на организмы влияют разные факторы внешней среды, в т.ч. и неблагоприятная экологическая обстановка (Бектимиров Т.А., Горбунов М.А., Никитюк Н.М. и др., 2001).
В связи с этим, нами проведены исследования напряженности и длительности иммунитета при вакцинации взрослых гусей против гриппа птиц А.
Материалы и методы:
Нами проведена экспериментальная вакцинация разных видов домашней птицы против гриппа птиц А. Птицу содержали в опытных вольерах вивария. Рацион был стандартным на основе комбикорма. Ведение препарата организовывали в отдельном помещении, вынесенном за пределы птицепредпри-ятий.
Вакцинацию гусей проводили разработанной в ФГУ ВНИ-ИЗЖ инактивированной эмульгированной вакциной против гриппа птиц из шт. H5N1 (производство ОАО "Покровский комбинат биопрепаратов"). Вакцину вводили согласно наставлению: подкожно, в дозе 0,5 мл. на голову. Вакцинацию проводили трехкратно, с интервалом в 1 мес.
Для получения сыворотки кровь у гусей брали из яремной вены каждые 10 дней после вакцинации.
Уровень поствакцинальных антител в сыворотке экспере-ментальной птицы определяли в реакции торможения гемаг-глютинации (РТГА) с использованием стандартного диагностического набора
Дополнительно у опытной и контрольной птицы определяли гематологические и иммунологические показатели. В цельной крови выявляли содержание гемоглобина (гемометром Сали), количество эритроцитов и лейкоцитов [И.А. Болотников, Ю.В. Соловьев, 1980]. Подсчет эритроцитов и лейкоцитов осуществляли одновременно в камере Горяева по методике Фриед и Лукачевой в модификации Болотникова И.А Для характеристики клеточного и гуморального иммунитета (проводили количественное определение Т- и В- лимфоцитов [Л.С. Колабская, 1980].
Исследования проводились в течение 2005-2007 гг.
После проведенной вакцинации установлено, что уже через 10 дней во всех пробах сыворотки крови птиц выявляются антитела в протективных титрах. При этом разброс разведений, в которых обнаружены антитела, составляет от минимального
- 1/16 до максимального - 1/256 (у 25 % птиц титры составили
1/16, у 8,3% - 1/32, у 16,6% - 1/64, у 16,6% - 1/128, у 33,3%
Однако уже через 30 дней после введения вакцины у гусей отмечено снижение титров антител, при этом у 33% гусей выявлены антитела ниже протективного титра (разведение 1/8). Таким образом, однократное введение вакцины не вызывало полноценную иммунную защиту у 67% птицы через 30 дней после первичной вакцинации.
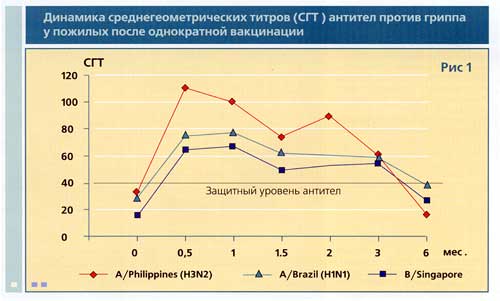
Первую ревакцинацию птицепоголовья провели через 30 дней (третья декада). Анализ показал, что через 10 дней после ревакцинации было отмечено значительное снижение напряженности иммунитета у гусей (рис. 1). При этом у 33% птиц антитела совсем не выявляли, у 17%титр был ниже протективного (1/8), у 50 % в титре 1/16 - 1/32. То есть, повторное введение вакцины через 30 дней после предыдущей вакцинации (четвертая - пятая декада) искусственно снижает напряженность иммунитета вплоть до исчезновения антител, и птица в этот период становилась не иммунной к возбудителю гриппа птиц.
Через 14-21 день после ревакцинации (шестая декада) отмечали рост титра антител, при этом все 100% вакцинированных птиц имели специфические гемагглютинины в протек-тивных концентрациях (1/16-1/128). Таким образом, после рекомендуемой наставлением однократной ревакцинации у птиц есть
После второй ревакцинации (седьмая декада) снижение концентрации антител не происходило, напротив, были отмечены максимальные титры (1/64-1/128), которые удерживались в течение месяца (70-100-й день опыта).
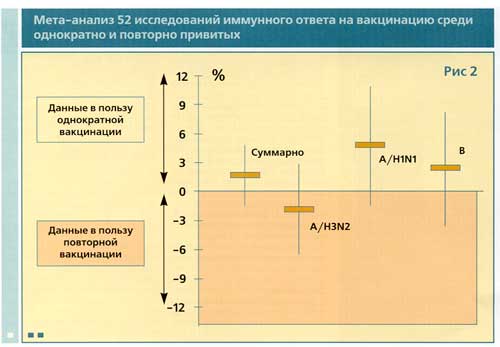
Начиная со 110-го дня опыта (одиннадцатая - двенадцатая декада), отмечено снижение концентрации антител к вакцинному антигену (рис.2). Также установлено, что в экспериментальной группе вакцинированных против ГП птиц ежемесячно отмечалось наличие, в среднем, 30-40% птиц, не имеющих иммунной защиты к вакцинному антигену, а, следовательно, к возбудителю гриппа птиц А. У остальных птиц концентрация специфических гемагглютининов оставалась низкая, но достаточная для защиты от заболевания (1/16-1/64).
К концу периода наблюдения (через 12 мес. после начала вакцинации) протективные титры сохранялись у 50% поголовья, средняя концентрация антител составила 1/42.
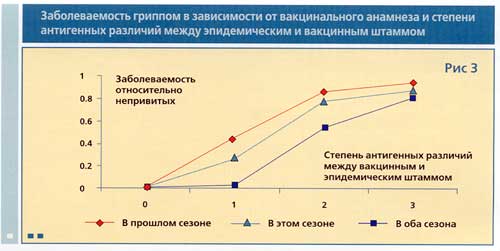
Обобщая полученные данные, можно отметить, что, в целом, всех птиц данной популяции можно было условно разделить на три группы: с высоким уровнем антителообразования, со средним и с низким. При этом, если у птиц после первой вакцинации отмечались высокие титры антител, то и на протяжении всего периода наблюдения они продолжали оставаться высокими (1/128-1/512). Количество таких птиц в экспериментальной популяции было, в среднем, 15% (рис.3).
У гусей, которые после первой вакцинации показывали низкие значения напряженности иммунитета, после 1 и 2 ревакцинации уровень антител продолжал оставаться низким и, спустя 4-5 мес. после начала опыта, исчезал совсем. Данная группа птиц более половины срока наблюдения оставалась неиммунной после трехкратной вакцинации, их количество составляло, в среднем, 37%. Поголовье птицы, которое показывало средние уровни антителообразования (1/16-1/64), составляло, в среднем, 48%.
При проведении биохимических и гематоиммунологичес-ких исследований установлено, что у гусей перед вакцинацией отмечено низкое содержание у-глобулинов, средние значения данного показателя составили 17,6% от среднего содержания (при норме 35-37%). Также у гусей отмечено достаточно низкое содержание тимоцитов и В-клеток (34% и 21 % соответственно), изменение их соотношения (Т/В составило 2,1 у.е.), что свидетельствует об иммунологической недостаточности.
Проведенные исследования показали, что полноценный иммунный ответ на введение вакцины отмечен только после трехкратного введения вакцины с интервалом 30 дней, концентрация защитных антител у птиц удерживалась при этом до 12 мес. в протективных титрах. также необходимо отметить, что в популяции, в среднем, до 40% птиц не формируют иммунитет против ГП.
Заключение: Таким образом, исследованиями установлено, что при вакцинации гусей трехкратно с интервалом 1 мес, в среднем, 37-50% поголовья показывают низкий иммунный ответ на введение вакцины, что выражается отсутствием антител либо уровнем антител ниже протективного уровня (1/8). Данные исследования являются предварительными, поскольку проведены на ограниченном поголовье экспериментальной птицы и требуют дальнейших производственных опытов.
1. Вакцинация - профилактика гриппа птиц/ Ямникова С.С, Смоленский В.И., Хохлачев О.Ф., Власов Н. 2007
2. Вирусные болезни животных/ В.Н. Сюрин, А.Я. Са-муйленко, Б.В.Соловьев, Н.В.Фомина. - М.: ВНИИТиБП, 1998. - С.324-336.
3. Грипп птиц. Стратегия противодействия/ Э. Д. Джава-дов, Ф.И. Полежаев и др.// Ж. Ветеринария. - N°6. - 2006. -С. 3-6.
4. Испытание вакцины против высокопатогенного гриппа птиц в эксперименте/ Э.ДДжавадов, Э.М. Амдий, А. С. Дубовой и др.//Ж. Птица и птицепродукты. - N°3. - 2006.
5. Смирнов A.M. История и реальность вируса гриппа птиц штамма H5N1/А.М.Смирнов, М.А. Шесточенко, В.А. Исаченко - М.: Издательство РАСХН, 2006. - 100 с.
Динамика напряженности поствакцинального иммунитета у экспериментальной птицы при гриппе А
И.М.Донник, Е.Н. Шилова
Уральский научно-исследовательский ветеринарный институт
При вакцинации против гриппа птиц гусей три раза с интервалом 1 мес, в среднем, 37-50% поголовья показывают низкий иммунный ответ на введение вакцины, что выражается отсутствием антител либо уровнем антител ниже протективного уровня (1/8).
Ключевые слова: грипп А, специфическая профилактика, иммунитет, антитела, мониторинг
УДК 619:615.371:6169215:57083.3:636 028:6365
Dynamics of intensity immunity at a fu А at an experimental poultry
The Urals State Scientifc-Research Institute of the Veterinary Medicine
At vaccination against a flu of birds of geese three times with an interval of 1 month, on the average, 37-50 % of a poultry show the low immune answer to introduction of a vaccine that is expressed by absence of antibodies or a level of antibodies of below protective level (1/8).
Key words: immunity, flu A, poultry, vaccination
Сведения об авторах:
Донник Ирина Михайловна
Директор ГНУ Уральского научно-исследовательского ветеринарного института (УрНИВИ). Член-корреспондент РАСХН, д.б.н., профессор
Шилова Евгения Николаевна
Зав. отделом инфекционной патологии ГНУ УрНИВИ Кандидат ветеринарных наук, доцент
- ответственная за переписку с редакцией Адрес: 620142, г.Екатеринбург, ул.Белинского, 112а, Тел. (343)257-20-44, факс (343)257-82-63 Адрес: 620142, г.Екатеринбург, ул.Белинского, 112а, Тел. (343)257-20-44, факс (343)257-82-63
Материал опубликован 03 октября 2019 в 11:32.
Обновлён 03 октября 2019 в 11:32.
В рамках мониторинга часть сотрудников – группа из 150 человек – перед вакцинацией сдала кровь на напряженность иммунитета*. О том, для чего нужны такие исследования, рассказывает заместитель главного врача по эпидобеспечению, главный эпидемиолог Ставропольского края Николай Пелих:
- Подобная практика существует давно, примерно столько же, сколько производятся вакцины. Ежегодно в серологическом контроле иммуногенных свойств вакцин участвуют медицинские работники различных лечебных учреждений. Результаты такого мониторинга позволяют из года в год улучшать вакцины, т.е. повышать их защитные свойства, снижать реактогенность (то есть сводить к минимуму негативные ощущения после прививки) и устранять побочные эффекты. Сотрудники лечебных учреждений лучше, чем кто-либо понимают необходимость таких рутинных исследований и имеют возможность сами компетентно оценить результаты своего обследования и на их основании сделать прогноз вероятности заболевания, вызываемого тем или иным штаммом вируса гриппа в предстоящем эпидемическом сезоне.
- Для этого делается анализ крови на напряженность иммунитета - определяется концентрация специфических антител, вырабатываемых организмом на вакцину. Необходимо иметь три образца крови: один – до введения вакцины, и два – после. После вакцинации в организме начинают вырабатываться антитела, их количество со временем нарастает и достигает защитного уровня через три-четыре недели. В это время кровь берётся на анализ повторно. Цель – определить, способна ли данная вакцина создавать специфический иммунитет, препятствующий заражению гриппом. Через полгода после прививки производится еще один забор крови – чтобы проследить, как долго и на каком уровне антитела сохраняются в организме.
Эпидемиолог пояснил, что в редких случаях антитела могут появиться в недостаточном количестве, не достигающем защитного уровня. Причины возможны две: 1) особенность иммунной системы (ослабленное состояние); 2) несостоятельность самой вакцины, что практически невероятно. Первая причина покажет низкий уровень антител в единичных случаях, вторая – в большинстве.
- Есть мнение, что прививки бесполезны, поскольку мы все равно не знаем, какой штамм распространится в этом году. Это не так, - констатирует Николай Пелих. - На самом деле штаммы не так часто мутируют настолько, чтобы вакцинация стала неэффективной, всего лишь раз в несколько лет, да и распространение получает обычно не один, а два-три штамма, так что в большинстве случаев вакцинация дает существенные преимущества тем, кто ее прошел.
В Ставропольской психиатрической больнице вакцинации от гриппа подлежит весь персонал, начиная от главного врача и заканчивая техслужащими. В этом году предполагается привить более 750 человек. Группе добровольцев, участвующих в исследованиях, прививки уже сделали. Вакцинация остальных будет проведена в начале октября, а в середине месяца пройдет вакцинация пациентов.
- Чтобы вакцинация была эффективной, должно быть привито определенное число людей, иначе инфекция все равно будет распространяться. Для нашей больницы это 85% персонала, - комментирует Николай Леонидович.
Эпидемиолог категорически опровергает слухи относительно вредности прививок.
- С одной стороны, конечно, никто не может дать гарантии, что в этом году грипп не мутирует в пандемический штамм и вы не заразитесь, с другой – статистика из года в год подтверждает: люди, не прошедшие вакцинацию, справляются с болезнью намного тяжелее, чаще возникают осложнения, которые могут негативно сказываться на здоровье долгие годы, а в некоторых случаях приводят к инвалидности и даже к смерти.
Тем не менее выбор – делать прививку (с минимальной вероятностью переболеть гриппом в легкой форме) или не делать (и рисковать здоровьем и даже жизнью) - за вами.
СПРАВКА
Прививочный препарат Совигрипп – отечественная разработка вакцины против гриппа в виде раствора, поставляется в форме ампул или шприцев одноразового назначения. Действующее вещество – гликопротеины, полученные из актуальных штаммов вирусов гриппа типов А и В. Вспомогательные вещества - фосфатно-солевой буферный раствор и адъювант Совидон. Отсюда и название.
*Серологический контроль – исследование сыворотки крови на наличие в ней противогриппозных поствакцинальных антител.
*Напряженность иммунитета – концентрация специфических антител в крови, которые вырабатываются организмом в ответ на введение вакцины. По результатам теста на напряженность иммунитета оценивается уровень реакции организма на тот или иной возбудитель инфекции. Другими словами, напряженность иммунитета показывает способность организма защищаться от заражения определенным возбудителем.
Вакцинопрофилактика гриппа№5 (17) Сентябрь-октябрь 2001
|
Эффективность вакцины Ваксигрип у детей школьного возраста А.Л. Заплатников 1 , Н.А. Коровина 1 , Е.И. Бурцева 2 , Л.Н. Власова 2 , В.Т. Иванова 2 , В.И. Далечин 1 , Г.А. Мингалимова 1 , А.Н. Слепушкин 2 Грипп, нанося огромный ущерб как здоровью населения, так и экономике страны в целом, продолжает оставаться одной из актуальных медицинских и социально-экономических проблем отечественного здравоохранения [9]. При этом доказано, что в настоящее время имеется действенный способ профилактики гриппа - активная специфическая иммунизация [3, 15]. Создание эффективных и безопасных гриппозных вакцин стало возможным после фундаментальных исследований по изучению эпидемиологии заболевания, расшифровки морфологического и антигенного строения вируса гриппа, а также определения биологической роли различных структур возбудителя. Так было установлено, что рецепторсвязывающая активность вируса гриппа обеспечивается специализированной гликопротеидной субъединицей оболочки - гемагглютинином (ГА) [13]. Предполагается, что другой суперкапсидный гликопротеид вируса гриппа, нейраминидаза (НA), способствует повышению его вирулентности, а также принимает участие в высвобождении дочерних вирионов из инфицированной клетки [16]. ГА и НA содержат штаммоспецифические антигенные детерминанты вирусов гриппа и инициируют формирование специфической иммунной защиты организма в ответ на гриппозную инфекцию [10]. При этом гуморальная иммунная защита в основном обусловлена синтезом специфических антител к ГА и НА. Антитела к гемагглютинину (анти-ГА), препятствуя прикреплению вируса к мембранным рецепторам клеток-мишеней и нейтрализуя вирусную инвазивность, способствуют повышению специфической резистентности организма к возбудителю гриппа [10]. В свою очередь антитела к нейраминидазе (анти-НА) нарушают процессы репликации вируса, что играет существенную роль в снижении тяжести гриппозной инфекции и предотвращении развития постгриппозных осложнений [6, 10]. Развитие эффективного противогриппозного гуморального иммунитета у привитых людей, так же как и у пациентов при естественной инфекции, связано с адекватной продукцией специфических анти-ГА и анти-НА [10]. Среди широкого круга зарегистрированных и разрешенных к применению в РФ гриппозных вакцин инактивированная гриппозная сплит вакцина Ваксигрип ("Авентис Пастер", Франция) показала высокую эффективность и хорошую переносимость как у взрослых, так и у детей [1, 5, 7, 8]. В многочисленных работах подробно изучены процессы формирования поствакцинального иммунитета к гемагглютининам, входящим в состав вакцины Ваксигрип [1, 7, 8, 12, 14 и др.]. В то же время особенности развития гуморального иммунитета к нейраминидазам при иммунизации Ваксигрипом, несмотря на очевидную важность данного компонента в формировании эффективной поствакцинальной защиты, исследованы в значительно меньшей степени. Поэтому целью настоящей работы являлось комплексное изучение реактогенности, иммуногенности и клинико-эпидемиологической эффективности гриппозной вакцины Ваксигрип, а также особенностей формирования специфического поствакцинального иммунитета к обоим поверхностным антигенам вируса гриппа - гемагглютинину и нейраминидазе. В условиях массовой противогриппозной активной иммунопрофилактики гриппа у школьников (Сергиево-Посадский р-н Московской обл., эпидсезон 2000-2001 гг.) было проведено открытое рандомизированное контролируемое исследование по изучению переносимости, иммуногенности и профилактической эффективности гриппозной инактивированной сплитвакцины Ваксигрип. Осенью 2000 г. после предварительного уточнения клинико-анамнестических данных и в соответствии с рекомендациями Хельсинской декларации по соблюдению этических норм и прав пациентов был проведен отбор 183 школьников в возрасте 7-16 лет, ранее (в 1997 г.) иммунизированных вакциной Ваксигрип. У всех исследуемых изучали напряженность поствакцинального иммунитета к антигенам вирусов гриппа А/Йоганнесбург/82/96(H1N1), А/Нанчанг/933/95(H3N2), В/Пекин/184/93, входивших в состав гриппозных вакцин в эпидемическом сезоне 1997-1998 гг. Методом случайной рандомизации из 183 школьников были отобраны 135 человек и распределены на 2 группы. Из них 70 детей в предэпидемический период гриппа сезона 2000-2001 гг. были привиты вакциной Ваксигрип (основная группа), а 65 детей в эпидсезон 2000-2001 гг. не были иммунизированы и составили контрольную группу. Группы были сопоставимы по возрасту, полу и состоянию здоровья детей. С начала декабря 2000 г. и до конца апреля 2001 г. за детьми, включенными в исследование, проводился клинический, серологический и вирусологический мониторинг. Закончили исследование 127 детей (67 - в основной и 60 - в контрольной группе). Клиническая часть исследования включала динамический контроль за состоянием здоровья детей и, в случае необходимости, оказание им медицинской помощи. Особое внимание уделяли изучению переносимости детьми вакцины Ваксигрип. Реактогенность вакцины оценивалась на основании результатов активного динамического наблюдения за привитыми в течение 5 дней после иммунизации. При этом учитывались как местные (болезненность, гиперемия и инфильтрация в месте инъекции), так и общие реакции (повышение температуры тела, недомогание, головная боль, слабость, ощущение "разбитости", миалгия, артралгия и др.). Установлено, что только у 1 (1,5%) ребенка иммунизация Ваксигрипом сопровождалась нетяжелой общей реакцией в виде субфебрильной температуры, недомогания, головной боли. Симптомы сохранялись в течение 2-х дней с последующим самостоятельным купированием без применения жаропонижающих и анальгетиков. У остальных детей, привитых Ваксигрипом, поствакцинальный период протекал гладко и не требовал обращения за медицинской помощью. Активное наблюдение за вакцинированными в течение 5 дней после прививки позволило у 12,5% детей выявить местные реакции в виде легкой, локализованной в месте инъекции гиперемии, без инфильтрации и других признаков воспаления, не сопровождавшиеся жалобами и не требовавшие терапии. Характер изменений специфического противогриппозного иммунитета в результате вакцинации определяли на основании динамического выявления антител к ГА и НА. Антигемагглютинины (анти-ГА) сыворотки крови определяли при помощи реакции торможения гемагглютинирующей активности (РТГА) с использованием 0,75% взвеси эритроцитов человека 0 (1) группы крови, а антинейраминидазные антитела (анти-НА) - в лектин-тесте с 3% взвесью эритроцитов морской свинки. Постановку РТГА и лектин-теста проводили стандартными методами с использованием вирусов гриппа, подобным вакцинным штаммам эпидемического сезона 2000-2001 (А/Новая Каледония/20/ 99(H1N1), А/Панама/2007/99 (H3N2), В/Яманаши/166/98) [2, 4]. Для анализа иммуногенности вакцины Ваксигрип перед вакцинацией и через 4 недели после нее у детей были взяты пробы капиллярной крови. Иммуногенность вакцины Ваксигрип определяли на основании числа диагностических приростов титров специфических антител к гемагглютинину и нейраминидазе в 4 и более раз, а также по динамике величин средних геометрических титров антител (СГТ) в парных сыворотках и проценту детей, у которых после вакцинации регистрировали защитный титр специфических противогриппозных антител (1:40 и выше). Уровень инфицированности исследуемого контингента эпидемическими штаммами вирусов гриппа определяли титрованием парных сывороток в РТГА с антигенами вирусов гриппа А и В, имевших эпидемическую активность в период наблюдения. Первичный забор крови осуществляли перед началом эпидемического подъема заболеваемости гриппом (конец декабря 2000 г.), последующий - после завершения эпидсезона (конец апреля 2001 г.). Достоверным признаком перенесенной инфекции считали нарастание титров антител в парных сыворотках не менее чем в 4 раза. Дополнительно у заболевших детей с клиническим диагнозом "грипп" для уточнения этиологии проводили вирусологическое исследование носоглоточных смывов, отобранных в первые 3 дня заболевания с последующим заражением культуры клеток МDСК по методике описанной ранее [12]. Для оценки профилактической эффективности вакцины Ваксигрип использовали сравнительный анализ заболеваемости гриппом в исследуемых группах с определением индекса эпидемиологической эффективности. Полученные результаты обрабатывали с помощью методов вариационной статистики с определением критерия достоверности Стьюдента t. Таким образом, представленные результаты свидетельствуют о высокой иммуногенной активности гемагглютининов и нейраминидаз инактивированных вирусов гриппа, входивших в состав вакцины Ваксигрип эпидсезона 2000-2001 гг. Применение Ваксигрипа сопровождалось полноценным формированием защитных уровней антител к обоим поверхностным антигенам всех вакцинных штаммов вируса гриппа у подавляющего большинства привитых и определило развитие у них высокоэффективного противогриппозного поствакцинального иммунитета. Благодаря этому среди школьников, иммунизированных Ваксигрипом, только 8 (11,9%) были инфицированы вирусами гриппа, в то время как в контрольной группе инфицирование вирусом гриппа встречалось достоверно чаще - у 16 детей и подростков (26,7%) (pВаксигрипом только у 2 из 8 инфицированных школьников заболевание сопровождалось клиническими проявлениями в виде нетяжелого катара дыхательных путей, а у остальных детей грипп протекал бессимптомно и выявлялся лишь на основании ретроспективного иммунологического обследования. Среди школьников, иммунизированных вакциной Ваксигрип, в отличие от детей и подростков контрольной группы, не было ни одного случая заболевания гриппом с тяжелым или осложненным течением (pПри вирусологической и серологической расшифровке этиологии гриппа установлено, что как у привитых, так и в контрольной группе заболевание достоверно чаще вызывал вирус гриппа В. Так, в основной группе из 8 случаев инфицирования детей вирусами гриппа, 7 были обусловлены вирусом гриппа В. В этиологической структуре гриппа у школьников контрольной группы также преобладал вирус гриппа В - в 11 случаях из 16. В 1 случае заболевание вызывалось микст-инфекцией (вирус гриппа A(H1N1) + вирус гриппа В). В целом индекс эпидемиологической эффективности вакцинации Ваксигрипом составил 2,2 (pВаксигрип при ее использовании в педиатрической практике. Таким образом, хорошая переносимость, низкая реактогенность, высокая иммуногенность и эпидемиологическая эффективность изучаемого препарата позволяют рекомендовать инактивированную гриппозную сплит вакцину Ваксигрип для применения у детей и подростков при проведении плановой активной иммунизации против гриппа. ВАКСИГРИП |
№3 (27) май/июнь 2003 г.