Национальный центр по гриппу воз
Региональная лабораторная сеть по гриппу является частью Глобальной системы эпиднадзора за гриппом и принятия ответных мер (ГСЭГО) и действует в следующем составе:
- национальные лаборатории по гриппу в 50 странах Региона; 52 лаборатории (в 41 государстве-члене) официально признаны ВОЗ в качестве национальных центров по гриппу (НЦГ);
- сотрудничающий центр ВОЗ по справочной информации и исследованиям в области гриппа (СЦ ВОЗ) при Национальном институте медицинских исследований, Лондон, Соединенное Королевство;
- 2 референс-лаборатории ВОЗ по гриппу Н5 (Институт Пастера, Париж, Франция, и Федеральное государственное научно-исследовательское учреждение, Государственный научно-исследовательский центр вирусологии и биотехнологии ВЕКТОР, Новосибирск, Российская Федерация);
- головная контрольная лаборатория ВОЗ при Национальном институте биологических стандартов и контроля, Поттерс-Бар, Соединенное Королевство.
Национальные центры по гриппу являются национальными учреждениями, признанными ВОЗ и уполномоченными министерствами здравоохранения для участия в работе ГСЭГО ВОЗ. Основной ролью национальных центров является проведение эпиднадзора за сезонным гриппом и оказание поддержки в составлении ежегодных рекомендаций ВОЗ по составу вакцины.
Национальные центры также предупреждают ВОЗ о необычных вспышках гриппа или гриппоподобных заболеваний, а также о выявлении несубтипируемых или медленно реагирующих изолятов вируса при исследовании с использованием диагностических реагентов ВОЗ, полученных по каналам ГСЭГО. Таким образом, национальные центры находятся на передовой линии относительно реагирования на вспышки, вызываемые новыми вирусами гриппа или другими возбудителями респираторных инфекций, такими как вирусы птичьего гриппа A(H5N1) и A(H7N9) и коронавирус ближневосточного респираторного синдрома (БВРС-КоВ).
НЦГ в 30 странах Европейского союза и Европейского экономического пространства также принимают участие в работе Сети европейских референс-лабораторий по гриппу человека (ERLI-Net) Европейской сети эпиднадзора за гриппом (EISN), которая координируется Европейским центром профилактики и контроля заболеваний (ECDC).
В мире существует 5 сотрудничающих центров ВОЗ по справочной информации и исследованиям в области гриппа. Эти центры получают вирусы гриппа из НЦГ различных стран мира, проводят подробный антигенный и генетический анализ вирусов и делятся результатами с предоставившим вирус гриппа национальным центром и ВОЗ.
Эти результаты формируют основу для ежегодных рекомендаций ВОЗ о составе вакцины против сезонного гриппа для Северного и Южного полушарий. Результаты используются также при проведении непрерывной глобальной оценки рисков, определяющей, обладают ли известные в настоящее время вирусы гриппа потенциалом, способным вызвать пандемию гриппа.
СЦ ВОЗ при Национальном институте медицинских исследований в Лондоне (Соединенное Королевство) в сотрудничестве с ЕРБ ВОЗ получает и анализирует вирусы гриппа из большинства НЦГ в Европейском регионе ВОЗ, проводит обучение для сотрудников НЦГ Европейского региона по лабораторным методам, включая диагностику, анализ данных, оценку риска и другие важные функции, поддерживает ответные действия на вспышки и предоставляет данные для еженедельных и годовых отчетов по эпиднадзору за гриппом.
Сотрудничающий центр ВОЗ по эпиднадзору, эпидемиологии и борьбе против гриппа при
Центрах по контролю и профилактике заболеваний США (подразделение по гриппу в составе Национального центра по иммунизации и другим респираторным заболеваниям) ежегодно готовит и распространяет обновленные наборы реагентов для диагностики гриппа среди всех НЦГ и других сотрудничающих лабораторий.
Эти комплекты, включающие в себя эталонные антисыворотки и контрольные антигены, необходимы для выявления циркулирующих вирусов гриппа A(H3N2), A(H1N1) и B, а также для серологических анализов. Реагенты, специфичные для таких вирусов птичьего гриппа, как A(H5N1) и А(H7N9), можно получить по запросу.
Сеть референс-лабораторий ВОЗ по гриппу H5 была создана в 2004 г. в ответ на потребности общественного здравоохранения, связанные с инфицированием птичьим гриппом A(H5N1) человека и необходимости поддержки готовности лабораторий к пандемии.
Пять лабораторий этой сети участвуют в проведении оценки риска и реагировании, обеспечивая надежную лабораторную диагностику гриппа у людей, особенно в тех случаях, когда есть подозрение на птичий грипп А(Н5) или наличие других вирусов гриппа с пандемическим потенциалом.
Одна из 4 существующих в мире, головная контрольная лаборатория ВОЗ в Соединенном Королевстве вносит свой вклад в производство безопасных и эффективных вакцин против гриппа путем отбора и разработки кандидатных вакцинных вирусов. Лаборатория формально принадлежит к национальному регулирующему органу Соединенного Королевства и играет важную роль в разработке, регулировании и стандартизации вакцин против гриппа.
ЕРБ ВОЗ поддерживает работу региональной лабораторной сети по гриппу путем организации ежегодных совещаний по эпиднадзору за гриппом, проведения учебных мероприятий, предоставления технических руководств и программ внешнего контроля качества. ЕРБ ВОЗ проводит эту работу в сотрудничестве с СЦ ВОЗ при Национальном институте медицинских исследований в Лондоне, Соединенное Королевство, Европейским центром профилактики и контроля заболеваний (ECDC), а также Сетью европейских референс-лабораторий по гриппу человека (ERLI-Net), с участием экспертов из НЦГ стран Региона.
Вирусологи из национальных центров по гриппу (НЦГ) в Варшаве (Польша), Бухаресте (Румыния), Санкт-Петербурге (Российская Федерация) и Женеве (Швейцария) приняли участие в специализированных учебных курсах, которые были организованы сотрудничающим центром ВОЗ по справочной информации и исследованиям в области гриппа при Институте Фрэнсиса Крика (Лондон, Соединенное Королевство).
НЦГ играют ключевую роль в эпиднадзоре за гриппом на национальном и региональном уровне. Функции НЦГ включают следующие: сбор образцов вирусов, циркулирующих в их странах; проведение предварительного анализа этих образцов; отправка репрезентативных клинических образцов и изолированных вирусов в сотрудничающие центры ВОЗ для проведения расширенного антигенного и генетического анализа. Разработка ежегодных рекомендаций ВОЗ по составу вакцин против гриппа и проводимые ВОЗ оценки риска сезонного гриппа во многом базируются на результатах этого анализа.
1-2-недельные учебные курсы, адаптированные к конкретным потребностям вышеуказанных НЦГ, охватывали различные аспекты лабораторной диагностики и вирусологического надзора за гриппом. Главная цель этих курсов заключалась в том, чтобы повысить знания и навыки участников в сфере выявления и характеризации циркулирующих вирусов сезонного гриппа человека.
Участники курсов – по 2 из каждого НЦГ – дали очень высокую оценку качеству обучения и выразили готовность использовать приобретенные знания и навыки для повышения потенциала своих НЦГ в характеризации циркулирующих вирусов гриппа.
Ana Rita Gonçalves Cabecinhas и Patricia Suter-Boquete из НЦГ в Женеве заявили следующее: “Обучение совместно с сотрудниками других НЦГ было очень полезным, так как это дало нам хорошую возможность обменяться информацией о различных аспектах эпиднадзора за гриппом и о соответствующих стратегиях наших стран.” Они подчеркнули, что такое взаимодействие помогает укрепить сотрудничество между НЦГ.
"Наша группа состояла из четырех человек, которые одновременно проводили анализ, и нам это очень понравилось", – продолжили они. – "Группа была достаточно маленькой, чтобы дать всем возможность принять активное участие в проведении анализа".
Учебный курс для сотрудников НЦГ в Варшаве был посвящен методам выделения вируса гриппа в клеточной культуре и идентификации подтипа гемагглютинина полученных вирусных изолятов с помощью реакции ингибирования гемагглютинации (ИГ). Кроме того, участники курса прошли обучение по вирусологическим исследованиям, используемым для оценки восприимчивости вирусов гриппа к лекарственным средствам.
Учебный курс для сотрудников НЦГ в Женеве и Бухаресте был посвящен методам проведения реакции микронейтрализации вируса гриппа (тест на снижение бляшкообразования). Эта реакция используется в качестве альтернативы теста ингибирования гемагглютинации для изучения антигенных свойств и инфекционности вирусов гриппа. Переход на реакцию микронейтрализации (РМН) помогает устранить эффекты неантигенного характера, обусловленные изменениями аффинности рецепторов вирусов гриппа, что может затруднить интерпретацию результатов теста ингибирования гемагглютинации.
Учебный курс для сотрудников НЦГ в Санкт-Петербурге был посвящен методам секвенирования следующего поколения (NGS), используемым для полногеномной характеризации вирусов гриппа. Участники прошли обучение по лабораторным процедурам, используемым для подготовки библиотек NGS, и по методам разработки и внедрения экономически эффективного протокола проведения секвенирования. Они также ознакомились с преимуществами и недостатками различных программных пакетов, используемых для анализа данных, полученных благодаря методам секвенирования следующего поколения.
Сотрудничающий центр ВОЗ при Институте Фрэнсиса Крика регулярно проводит учебные курсы для вирусологов из НЦГ из всех частей мира. Он адаптирует каждый учебный курс к конкретным потребностям участников и берет на себя оплату всех лабораторных расходов.
Обучение финансируется за счет Плана реализации вклада партнеров в Механизм обеспечения готовности к пандемическому гриппу в период 2013–2017 гг., целью которого является укрепление потенциала НЦГ и вирусологического эпиднадзора за гриппом в Европейском регионе ВОЗ, а также за счет программы ЕРБ ВОЗ по борьбе с особо опасными патогенами в рамках ежегодного обучения специалистов по вирусологии гриппа.
Аннотация научной статьи по прочим медицинским наукам, автор научной работы — Соминина Анна Адольфовна, Грудинин М. П., Еропкин М. Ю., Смородинцева Е. А., Писарева М. М.
Представлен анализ развития эпидемии гриппа сезона 2010-2011 гг. Установлена ведущая роль вирусов гриппа A(H1N1)pdm09 и B Викторианской линии в структуре эпидемической заболеваемости при небольшом участии вируса A(H3N2). По антигенным свойствам выделенные в России вирусы оказались родственными штаммам, введенным в состав вакцин. Дрейф-варианты вируса A(H1N1)pdm09, выделенные в Астрахани и Санкт-Петербурге, были признаны сотрудничающим центром (СЦ) ВОЗ в Лондоне в качестве родоначальников трех новых генетических групп возбудителя.
Похожие темы научных работ по прочим медицинским наукам , автор научной работы — Соминина Анна Адольфовна, Грудинин М. П., Еропкин М. Ю., Смородинцева Е. А., Писарева М. М.
Development of Influenza Surveillance in Russia in the System of the WHO National Influenza Center
Analysis of development influenza activity season 2010-2011 is presented. Significant participation of influenza A(H1N1)pdm09 virus and influenza B of Victoria lineage virus in the epidemic morbidity structure with minor participation of A(H3N2) virus was revealed. The influenza viruses isolated in Russia according to antigenic properties were similar to the strains included in the vaccine composition. Drift variants of influenza A(H1N1)pdm09 viruses isolated in Astrakhan and St.-Petersburg were recognized using WHO CC in London as representatives of three new genetic groups.
(FluMist) derived from cold - adapted A/Ann АгЬог/6/60. Virology. 2003; 306: 18-24.
11. Jin H., Zhou H., Lu В., Kemble J. Imparting temperature sensitivity and attenuation in ferrets to A/Puerto Rico/8/34 influenza virus by transferring the genetic signature for temperature sensitivity from cold-adapted A/Ann Arbor/6/60. J. Virol. 2004; 78: 995-8.
12. Kendal A. P., Maasab H. F., Alexandrova G. I., Ghendon Y. Z. Development of cold-adapted recombinant live attenuated influenza A vaccines in the USA and USSR. Antiviral Res. 1981; 1: 339-65.
13. Klimov A. I., Kiseleva I. V, Alexandrova G. I., Сох N. J. Genes coding for polymerase proteins are essential for attenuation of the cold-adapted A/Leningrad/134/17/57 (H2N2) influenza virus. International Congress Series. 2001; 1219: 955-59.
14. Maassab H. Adaptation and growth characterization of influenza virus at 25oC. Nature. 1967; 213: 612-4.
15. ReedL. I., Muench H. A simple method of estimation fifty per cent endpoints. Am. J. Hyg. 1938; 27: 493-97.
А. А. Соминина, М. П. Грудинин, М. Ю. Еропкин, Е. А. Смородинцева, М. М. Писарева, А. Б. Комиссаров, Н. И. Коновалова, Д. М. Даниленко, Т. М. Гудкова, О. И. Киселев
Развитие надзора за гриппом в России в системе национального
центра ВОЗ по гриппу
ФГБУ НИИ гриппа Минздравсоцразвития России, Санкт-Петербург
Представлен анализ развития эпидемии гриппа сезона 2010-2011 гг. Установлена ведущая роль вирусов гриппа A(H1N1)pdm09 и B Викторианской линии в структуре эпидемической заболеваемости при небольшом участии вируса A(H3N2). По антигенным свойствам выделенные в России вирусы оказались родственными штаммам, введенным в состав вакцин. Дрейф-варианты вируса A(H1N1)pdm09, выделенные в Астрахани и Санкт-Петербурге, были признаны сотрудничающим центром (СЦ) ВОЭ в Лондоне в качестве родоначальников трех новых генетических групп возбудителя.
Ключевые слова: грипп, заболеваемость, ПЦР, ИФ, генетический анализ
Development of Influenza Surveillance in Russia in the System of the WHO National
A. A. Sominina, M. P. Grudinin, M. Yu. Eropkin, E. A. Smorodintseva, M. M. Pisareva, A. B. Komissarov, N. I. Konovalova, D. M. Danilenko, T. M. Gudkova, and O. I. Kiselev
Federal State Research Institute of Influenza, Ministry of Health and Social Development of the Russian Federation, St.
Analysis of development influenza activity season 2010-2011 is presented. Significant participation of influenza A(H1N1)pdm09 virus and influenza B of Victoria lineage virus in the epidemic morbidity structure with minor participation of A(H3N2) virus was revealed. The influenza viruses isolated in Russia according to antigenic properties were similar to the strains included in the vaccine composition. Drift variants of influenza A(H1N1)pdm09 viruses isolated in Astrakhan and St.-Petersburg were recognized using WHO CC in London as representatives of three new genetic groups.
Key words: influenza, morbidity, polymerase chain reaction, IFA, genetic analysis
Грипп - инфекция, известная со времен Гиппократа (V век до н. э.), которая не имеет себе равных по скорости глобального распространения. Некоторые субтипы возбудителя, в частности A(H5N1), отнесены к особо опасным в связи с высокой (около 60%) летальностью заболевших. Этот вирус пока не приобрел свойственной вирусам гриппа способности к трансмиссии среди людей, поскольку имеет прямое происхождение от вируса H5N1 птиц, но оказался способным преодолевать барьер хозяина и при тесном контакте инфицировать человека [12]. В последнее время в двух лабораториях США и Нидерландов показана возможность приобретения такого свойства в результате последовательного пассирования вируса H5N1 на лабораторных животных (хорьках) или реассортации генов вирусов гриппа A(H5N1) и A(H1N1) [11]. С учетом важности проблемы гриппа по инициативе акад. А. А. Смородинцева в России в марте 1967 г. был организован ВНИИ гриппа,
одним из основных направлений деятельности которого был определен надзор за гриппом и ОРВИ в стране [7]. Быстро и четко организованная деятельность института при поддержке со стороны Министерства здравоохранения СССР привела к его признанию на международном уровне и созданию на базе института Национального центра по гриппу (НЦГ), признанного ВОЗ в 1971 г. одним из участников Глобальной сети надзора за гриппом (GISN). Важный вклад в это направление деятельности в свое время внесли проф. Т. Я. Лузянина и сотр., проф. Ю. Г. Иванников и сотр., затем его продолжили акад. О. И. Киселев, проф. А. А. Соминина, канд. мед. наук Л. Е. Камфорин, д-р мед. наук И. Г. Маринич, в настоящее время оно развивается с привлечением современных методов молекулярной диагностики, антигенного и филогенетического анализа, что дает ценную информацию для понимания эволюции возбудителей гриппа и позволяет контроли-
Соминина Анна Адольфовна, д-р мед. наук, проф., зав. каф.; e-mail: anna@influenza.spb.ru
ровать появление мутаций, ответственных за признак высокой патогенности для человека.
Материалы и методы
Лабораторный надзор. Лабораторный надзор за гриппом осуществлялся в соответствии с нормативными [4] и методическими документами [6].
Выделение вирусов гриппа в ОБ проводили в клеточной культуре MDCK, полученной из Центра CDC (Атланта, США) и переданной из института, а в НЦГ - одновременно в двух системах (куриные эмбрионы и клетки MDCK). Для типирования возбудителей в ОБ использовали специфические диагностические кроличьи сыворотки (ООО “Предприятие по производству диагностических препаратов”). Антигенный анализ выделенных возбудителей осуществляли в НЦГ в РТГА с использованием крысиных сывороток к референс-штаммам вирусов гриппа, а также сывороток из набора для идентификации вирусов гриппа, полученного из CDC по линии ВОЗ. В работе использовали референс-вирусы А/Калифорния/07/09 (H1N1)pdm09, A/sw/Iowa/15/30(Hsw1N1), A/Южная Каролина/20/10 (H1N1)pdm09, А/Брисбен/10/07(Н3№), А/Висконсин/ 15/09(H3N2), А/Перт/16/09(Н3Ш), А/Виктория/208/
09(H3N2), А/Род-Айленд/1/10(Н3№), В/Малайзия/ 2506/04, В/Брисбен/60/08 и российские изоляты.
Контроль популяционного иммунитета. Анализ популяционного иммунитета осуществляли в ОБ путем исследования в РТГА сывороток от 100 взрослых здоровых доноров крови с определением процента серопозитивных лиц и среднегеометрических титров (СГТ) антител у населения различных городов страны. Определение проводили дважды в год: в предэпидемический (октябрь) и постэпидемический (апрель) периоды.
Генетический анализ. Для первичного скрининга клинических образцов использовали ПЦР-тест-системы “АмплиСенс” (ЦНИИ эпидемиологии, Москва), а также праймеры и контрольные образцы для типирования и субтипирования вирусов гриппа A и В, любезно предоставленные специалистами CDC (Атланта, США). Определение нуклеотидной последовательности молекулы HA1 было проведено с использованием ABI PRISM 3100-Avant Genetic Analyzer (“Applied Biosystems”, США). BigDye Terninator Cycle Sequencing Kit v3.1 был использован для анализа последовательностей. С помощью программ Vector NTI 8 и MEGA 2.1 предсказывали первичные аминокислотные последовательности гемагглютинина, нейра-минидазы и М2-белка. При построении филогенетических древ были использованы также нуклеотидные и аминокислотные последовательности гемагглютинина, нейраминидазы и М2-белка, представленные в Международной базе данных GenBank.
Эпидемиологический надзор осуществляли на основании сообщений из 49 ОБ в соответствии с приказом Роспотребнадзора[4].
Результаты и обсуждение
Популяционный иммунитет. За предшествующий пандемический сезон (2009-2010) в России переболело около 8,5% населения, вакцинировано сезонной тривакциной 34,4 млн человек, вакциной против пандемического гриппа - около 29 млн человек. В итоге процент серопозитивных лиц к вирусу гриппа A(H1N1)pdm09 повысился с 3,1 в октябре 2009 г. до 36,2 в октябре 2010 г. Вместе с тем около 63,8% здорового взрослого населения оставалось неиммунным по отношению к пандемическому вирусу гриппа и около 29,6 и 26,5% людей не имели защитных титров антител к вирусам гриппа A(H3N2) и В, что позволяло ожидать развития эпидемии смешанной этиологии с участием вирусов A(H1N1)pdm09, A(H3N2) и В.
Мониторинг гриппа и ОРВИ. За анализируемый период в 46 ОБ методом ПЦР было обследовано 49 934 больных гриппом и другими ОРВИ, методом ИФ -35 726 больных. После осеннего подъема заболеваемости в сентябре-октябре 2010 г., связанного с усилением циркуляции возбудителей ОРВИ негриппозной этиологии, среди которых более чем в 20% случаев выявляли вирусы парагриппа, РСВ и аденовирусы, в начале сезона 2010-2011 гг. методом ПЦР еще регистрировали единичные случаи сезонного гриппа A(H1N1), однако в последующий период этот возбудитель больше не обнаруживали. Вирус гриппа A(H3N2), однако, продолжал циркулировать среди населения начиная с конца ноября 2010 г. В декабре частота его регистрации возросла до 4,6-5,7%, но интенсивность циркуляции на протяжении всего последующего периода носила умеренный характер. Напротив, активность
вируса гриппа A(HlNl)pdm09 в прошедшем сезоне была весьма высокой. Рост частоты регистрации заболеваний, вызванных этим возбудителем, наметился в конце декабря. В январе 2011 г. по результатам ПЦР она достигла 18,2-27%, а в феврале - 33,8-35,6% с сохранением активности до конца марта в пределах
19,5-36% от числа обследованных, хотя по результатам ИФ в марте она снизилась до 2,2-7,6%, что лучше коррелировало с данными о снижении заболеваемости. Вирусы гриппа В появились в самом начале сезона, но диагностировались в небольшом (0,2-1,9) проценте случаев до начала зимы. В декабре интенсивность их циркуляции повысилась (до 2,8-5,9% по результатам ПЦР и 2,1-3,4% по результатам ИФ) и достигла максимума в январе (до 8,9-21,3 и 7,4-7,5% по результатам ПЦР и ИФ) с последующим постепенным снижением в феврале-апреле. В марте-июне в ОБ регистрировали единичные случаи гриппа A(H1N1) pdm09 и В. Интеграция данных лабораторной диагностики и эпидемиологических показателей показала, что первая волна подъема заболеваемости, зарегистрированная в ряде городов России, начиная с 47-49-й недели, была связана с присоединением вирусов гриппа A(H3N2) и В к активно циркулировавшим в этот период аденовирусам и вирусам парагриппа. Второй, более выраженный, эпидемический рост заболеваемости в январефеврале был обусловлен преимущественной циркуляцией пандемического вируса A(HlNl)pdm09 при социркуляции вирусов гриппа В и в меньшей степени - A(H3N2). По сравнению с пандемическим сезоном (2009-2010) заболеваемость за последний сезон в целом несколько снизилась (с 8,5 до 6,6% от численности населения), как и показатели госпитализации (с 2,6 до 23% от числа заболевших ОРВИ). Количество летальных исходов, в 95,7% случаев, обусловленных вирусом A(HlNl)pdm09, уменьшилось в 2010-2011 гг. по сравнению с пандемией 2009-2010 гг. с 634 до 232 случаев (по данным ОБ). Следует отметить, что в структуре заболеваемости ОРВИ достаточно высокой была роль возбудителей ОРВИ: по результатам ИФ в целом за сезон частота детекции вирусов парагриппа составила 9,4%, аденовирусов - 5,7%, РСВ - 2,9%, а по результатам ПЦР - 4,2, 4 и 1,5% случаев от числа обследованных больных соответственно. Циркуляция вирусов парагриппа, РСВ и аденовирусов снизилась в период эпидемии, но вновь возросла в постпандемический период.
Выделение вирусов гриппа было проведено в 27 ОБ, исследованы
материалы от 9565 больных. За весь сезон был выделен 561 вирус гриппа, в том числе 297 штаммов A(HlNl)pdm09, 18 штаммов A(H3N2) и 246 вирусов гриппа В.
Наиболее эффективной (частота выделения ll,9-25,6%) была работа вирусологов ОБ в Астрахани, Воронеже, Калининграде, Краснодаре, Москве, Новосибирске и Туле. Первые вирусы гриппа В были выделены в Новосибирске (на 50-й неделе), гриппа A(H3N2) - в Чите (на 51-й неделе), вируса гриппа A(HlNl)pdm09 - в Астрахани (на 4-й неделе 2011 г.). Частота выделения вирусов гриппа A(HlNl)pdm09, A(H3N2) и В за неделю на пике в целом по стране составила 10, 2,3 и 7,5% соответственно, т. е. была ближе к данным ИФ-анализа в тот же период (14,4, 2,2 и 7,5% соответственно), чем к данным ПЦР (36, 5,7 и 21,3% соответственно) (рис. 1). По данным се-
Рис. 1. Результаты ИДР-диагиостики и выделения вирусов гриппа в сезон 2010-2011 гг.
A/Belgorod/12/2009 __| |A/Nizhny Novgorod/02/2009 A/Nizhny Novgorod/01/2009 -A/Belgorod/11/2009 |— A/Voronezh/01 /2009 j— A/Saint-Petersburg/48/2009 ^A/Saint-Petersburg/82/2009 A/Orenburg/IIV2974/2009
A/Saint-Petersburg/44/2009 A/Saratov/06/2009 A/Lviv/N6/2009
— A/Saratov/01 /2009 A/Pskov/02/2009 A/Saint-Petersburg/75/2009 A/Belgorod/02/2010 A/Petrozavodsk/02/2009

Министерство здравоохранения Республики Беларусь

О заболеваемости ОРВИ в мире и республике

О заболеваемости острыми респираторными вирусными инфекциями в мире и республике.
Согласно информации Глобальной сети наблюдения за гриппом Всемирной организации здравоохранения и Flu News Europe в странах Северного полушария с умеренным климатом активность гриппа продолжает повышаться.
В Европейском регионе продолжается рост активности гриппа с коциркуляцией обоих типов вирусов гриппа А, но преобладанием A(H1N1)pdm09 над A(H3N2). Количество выявленных вирусов гриппа В оценивается как небольшое.
В большинстве стран Европейского региона интенсивность эпидемического процесса оценивается как средняя или высокая, с широким уровнем географического распространения:
- низкая в Исландии Норвегии, Швеции, Дании, Англии, Ирландии, Бельгии, Нидерландах, Австрии, Азербайджане, Узбекистане;
- средняя – в Шотландии, Португалии, Испании, Германии, Чехии, Словакии, Польше, Болгарии, Словении, Сербии, Молдове, Литве, Латвии, Республики Беларусь, РФ;
- высокая – во Франции, Италии, Венгрии, Румынии, Греции.
Вирусы гриппа A(H1N1)pdm09 доминируют в большинстве стран Европейского региона.
По данным Федерального центра по гриппу Российской Федерации заболеваемость гриппом и острыми респираторными инфекциями увеличилась во всех округах по населению в целом и, особенно среди детей школьного возраста и взрослых.
В Республике Беларусь в настоящее время, как и прогнозировал Национальный центр по гриппу и другим острым респираторным заболеваниям, отмечается сезонная заболеваемость острыми респираторными инфекциями и гриппом средней интенсивности на ожидаемых для данного времени года уровнях. В текущем сезоне заболеваемость соответствует среднемноголетним показателям.
ДИНАМИКА ЗАБОЛЕВАЕМОСТИ ОРИ В КОНТРОЛЬНЫХ ГОРОДАХ РЕСПУБЛИКИ БЕЛАРУСЬ
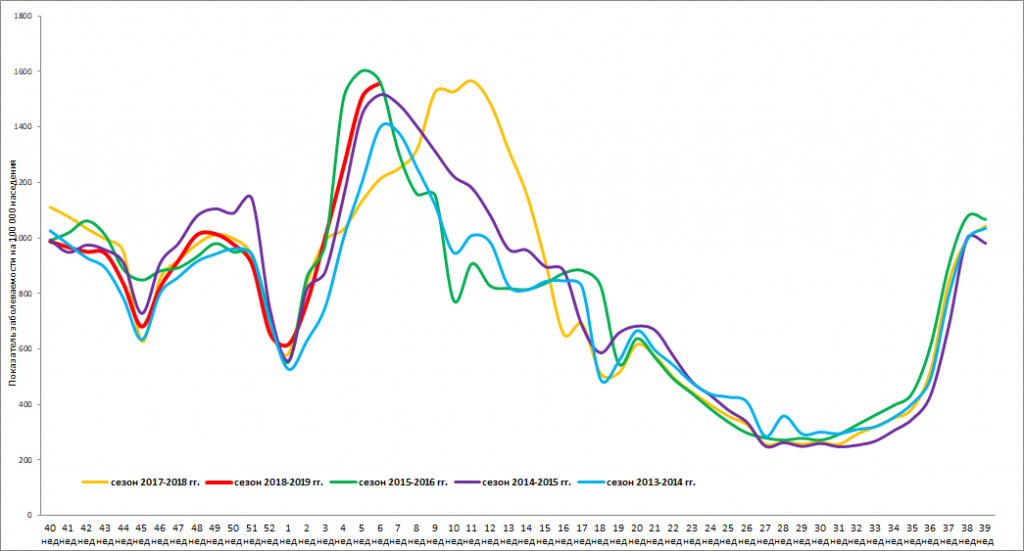
Среди заболевших преобладает детское население – 66,7%.
На протяжении ряда последних сезонов в нашей стране заболеваемость респираторными инфекциями, в том числе гриппом, характеризуется средней интенсивностью.
В структуре циркулирующих респираторных вирусов увеличилась доля вирусов гриппа типа А, среди которых превалировал A(H1N1)pdm09. Результаты молекулярно-биологических лабораторных исследований, проводимых в рамках эпидемиологического слежения за респираторными инфекциями, не выявили доминирующих возрастных групп пациентов, от которых выделены вирусы гриппа А(H1N1) pdm09.
Продолжают активно циркулировать респираторные вирусы не гриппозной этиологии (вирусы парагриппа, аденовирусы, бокавирусы, риновирусы, метапневмовирусы), которые в некоторых случаях, как и вирусы гриппа, становятся причиной развития пневмоний. Однако определяющее значение в этиологической структуре лабораторно подтвержденных пневмоний имеет бактериальная флора.
Все пациенты с острыми респираторными инфекциями и гриппоподобными заболеваниями, от которых были выделены вирусы гриппа, не были привиты от гриппа.
Циркуляция вирусов гриппа А (H1N1, H3N2) ожидаема для стран Северного полушария, включая Республику Беларусь. Начиная с 2010 г. аналоги вируса с антигенной структурой А (H1N1)pdm09 входят в состав всех противогриппозных вакцин, включая вакцины, применяемые в 2018 г.
В Европейском регионе большинство циркулирующих вирусов A(H1N1)pdm09 и A(H3N2) соответствуют вакцинным компонентам, что позволяет дать предварительную оценку о высокой эффективности использованной для профилактики гриппа вакцины.
Эпидемиологическая ситуация по заболеваемости острыми респираторными инфекциями находится на постоянном контроле Министерства здравоохранения Республики Беларусь.
Вместе с тем в целях предупреждения заболевания острыми респираторными инфекциями каждому человеку необходимо выполнять простые профилактические меры.
Сократите риск возможного заражения респираторными вирусами:
- избегайте тесных контактов с людьми, имеющими признаки респираторного заболевания;
- сократите время пребывания в местах скопления людей;
- мойте руки с мылом регулярно и тщательно, особенно после посещения улицы и общественного транспорта;
- применяйте средства для обеззараживания рук (гигиенический салфетки, бактерицидные гели);
- промывайте полость носа и рта особенно после посещения улицы и общественного транспорта;
- проветривайте, увлажняйте воздух и делайте влажную уборку помещений, в которых находитесь.
Повышайте защитные силы организма:
- ведите здоровый образ жизни,
- соблюдайте режим полноценного сна,
- соблюдайте режим питания и физической активности.
- прикрывайте рот и нос салфеткой (платком), когда чихаете или кашляете;
- используйте одноразовые бумажные салфетки (платки), которые выбрасывайте сразу после использования;
- при отсутствии салфетки (платка) кашляйте или чихайте в сгиб локтя;
- не трогайте руками нос, рот и глаза.
В случае заболевания острой респираторной инфекцией и гриппом следуйте следующим рекомендациям:
- при первых симптомах заболевания постарайтесь остаться дома,
- при необходимости – обратиться к врачу и строго соблюдать все его рекомендации;
- соблюдайте постельный режим,
- максимально ограничить свои контакты с домашними, особенно детьми, чтобы не заразить их,
- часто и регулярно проветривайте помещение,
- все лекарственные средства применяйте ТОЛЬКО по назначению врача.
- Дети с признаками острой респираторной инфекции должны оставаться дома и не посещать дошкольные учреждения и школы.
Читайте также:


