Миокардит при хроническом гепатите с

Дата публикации: 08.11.2016 2016-11-08
Статья просмотрена: 164 раза
При хронических вирусных гепатитах с умеренной степенью лабораторной активности функциональные изменения сердца проявляются развитием концентрического ремоделирования миокарда. У больных хроническим вирусным гепатитом высокой степени активности функциональные изменения сердца характеризуются развитием концентрической гипертрофии миокарда. Включение в комплекс лечения больным с хроническими гепатитами препаратов ингибитора ангиотензинпревращающего фермента улучшает функциональное состояние миокарда обоих желудочков сердца.
Ключевые слова: хронический гепатит, функциональные показатели миокарда, лечение
Актуальность: При хронических заболеваниях печени (ХЗП), к которым относятся хронические гепатиты (ХГ) и цирроз печени (ЦП) нарастают изменения сократительной функции миокарда, по мере прогрессирования основного заболевания. Происходит перестройка общей гемодинамики с преобладанием гиперкинетического типа, что приводит к развитию недостаточности кровообращения [1, с. 4; 2, с. 15].
Многие авторы указывают на наличие у больных с ХЗП, особенно ЦП на снижение сосудов (ОПСС), увеличение ударного объема (УО) при снижении показателей сократимости миокарда левого желудочка. Гиперкинетический тип гемодинамики компенсаторно усиливает кровоток в условиях повышенного артериовенозного шунтирования в печени [3, с. 530].
В ответ на это изменяются функции сердца, развивается ремоделирование миокарда. Ремоделирование — динамический процесс изменения толщины миокарда, размера и формы камер сердца, дисфункции правого желудочка (ПЖ) и левого желудочка (ЛЖ) [4, с. 80].
Прогрессированию ремоделирования ЛЖ и ПЖ и развитию сердечной недостаточности способствует повреждение митохондрий кардиомиоцитов, сопровождающееся образованием активных радикалов кислорода [5, с. 957].
Цель исследования. Изучить динамику функциональных показателей левого и правого желудочков у больных хроническими заболеваниями печени и динамику показателей в процессе лечения.
Материал иметоды. Исследования проведены у 42 больных ХГ вирусной этиологии (HBV, HCV, HBV+HCV), 28 мужчин (66,6 %) и 14 женщин (33,3 %), в возрасте от 20 до 67 лет. В соответствии с заболеванием больные были поделены на 2 группы: ХГ умеренной степени лабораторной активности (ХГ II ст. акт.) — 20 (33,3 %), ХГ высокой степени лабораторной активности (ХГ III ст. акт.) — 22 (25 %).
Для ПЖ оценивались: толщина передней стенки ПЖ в диастолу ТСПЖд, в норме — 5мм; индекс относительной толщины стенки в диастолу (ИОТСд), норма — 0,73± 0,09; индекс сферичности линейный диастолический (ИС), норма 0,3±0,04; миокардиальный стресс (МС), норма — 0–11,07. Контрольную группу для определения норм параметров ремоделирования миокарда составили 20 практически здоровых лиц.
Наряду с этим изучалось влияние курсовой дозы ингибитора ангиотензинпревращающего фермента периндоприла (престариум) на динамику функциональных изменений сердца у 21 больного. Периндоприл назначался по 2 мг 1 раз в сутки в течение 90 дней, сначала в стационаре, затем в амбулаторных условиях.
Результаты исследования иих обсуждение. Результаты проведенных исследований показали, что у больных ХГ отмечается четкая тенденция функциональных изменений в миокарде.
У больных ХГ в патологический процесс вовлекались как правые, так и левые отделы сердца. В группе с ХГ II ст. акт. (n=20) после проведения УЗДКГ после поступления в стационар было отмечено повышение КДР — 5,24±0,08; КСР — 3,44±0,07; КДО — 136,0±1,9; КСО — 56,6±2,3; УО — 73,3,3±0,22; ТЗСЛЖд, — 1,2±0,053; ТМЖПд. — 1,33±0,45. Изменение этих эхокардиографических параметров было статистически достоверно выше, по сравнению с показателями в контрольной группе. Отмечалось также повышение массы миокарда левого желудочка ММЛЖ — 167,5±1,7, ИММЛЖ — 96,8±1,4 и ИОТСЛЖ. Наряду с изменениями в ЛЖ в патологический процесс вовлекались правые отделы — ТСПЖ — 5,9±0,3; ИОТСПЖ — 0,84±0,06; а также некоторое снижение ИС — 0,24±0,56, что отражает процесс изменения геометрии ПЖ по типу концентрического ремоделирования (при этом индекс миокардиального стресса оставался в пределах нормы). Данные результаты указывают на развитие концентрического ремоделирования сердца.
Анализ результатов больных с ХГ III ст. акт. (n=22) позволил отметить нарастание систолической и диастолической перегрузок ЛЖ и ПЖ. Для некоторых параметров изменения были незначительными по сравнению с предыдущей группой — КДР — 6,01±0,09; КДО — 136,0±1,9, ТЗСЛЖ — 1,34±0,03, ОТСЛЖ -. 0,56±0,05. Для других параметров — КСР — 4,3±0,04. КСО — 59,0±1,32, ИС — 0,42±0,2 и МС — 11,4 изменения были статистически достоверно больше, чем у больных ХГ II ст. активности. Миокард больных ХГ III ст. активности имел тенденцию к развитию концентрической гипертрофии ЛЖ, о чем свидетельствует увеличение ММЛЖ — 171,2±2,03 и ИММЛЖ — 99,9±1,8.
Также как у больных умеренной степени лабораторной активности наблюдались изменения правых отделов сердца. Были утолщение стенки ПЖ, увеличение индекса относительной толщины стенки ПЖ, ИС и повышение МС выше нормы. Как отмечалось выше, ЭхоКГ проводилось у подавляющего числа больных дважды до и после лечения, а также на 90 день амбулаторного наблюдения и лечения.
Анализ результатов повторного исследования на 14 день на фоне комплексного метаболического лечения показал, что в целом отмечалось незначительное улучшение работы сердца. Регистрировалось снижение КДО, КСО, ИС и МС; некоторое увеличение УО. В группе больных ХГ II ст. акт. КДО — 130,0±0,9; КСО — 51,2±1,3; ИС — 0,28±0,026; МС — 4,6±0,2. В группе ХГ III ст. акт. КДО — 136,4±0,36; КСО — 58,0±0,09; ИС — 0,39±0,018; МС — 12,2±2,1. УО — 80,1±0,3.
Данные исследуемых больных на 90 день представлены на рисунке 1.
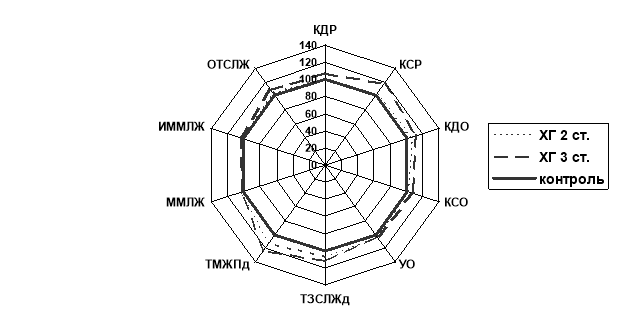
Рис. 1. Динамика кардиогемодинамических параметров на фоне курсового лечения и_АПФ периндоприлом больных ХГ
Регистрировалось снижение КДО, КСО, ИС и МС практически до контрольных цифр. Наблюдалось некоторое недостоверное увеличение УО. В группе больных ХГ II ст. акт. КДО — 128,0±0,4; КСО — 44,8±0,9; ИС — 0,46±0,07; МС — 0,98±0,9. В группе ХГ III ст. акт. КДО — 134,1±0,21; КСО — 48,0±0,05; ИС — 0,49±0,02; МС — 5,9±0,8, УО — 77,1±0,3.
При изучении влияния препарата из группы (периндоприла) на гемодинамику сердца показал, что на фоне метаболической терапии в стационаре и лечения в течение 90 дней и-АПФ периндоприлом в группах больных наблюдалась отчетливая положительная динамика с клинически значимым изменением параметров функциональной перестройки.
Выводы:
- У больных хроническим вирусным гепатитом с умеренной степенью лабораторной активности функциональные изменения сердца проявляются развитием концентрического ремоделирования миокарда.
- У больных хроническим вирусным гепатитом высокой степени активности функциональные изменения сердца характеризуются развитием концентрической гипертрофии миокарда.
- Перинодоприл в дозе 2,0 мг 1 раз в сутки в течение 90 дней улучшает функциональное состояние миокарда обоих желудочков сердца.
- Казюлин А. Р. /Особенности состояния сердечно-сосудистой системы у больных с заболеваниями органов пищеварения //Автореф. дис. …д-р мед. наук. — М., 2010.- с.36
- Шерлок Ш., Дули Д. /Заболевания печени и желчных путей // Пер. с англ. — М.: Гэотар Москва, 1999. — с. 415.
- Ide T., Tsutsui H., Hayashidani S. et al. /Mitochondrial DNA Damage and Dysfunction Associated With Oxidative Stress in Failing Hearts After Myocardial Infarction // Circ. Res. — 2001. — V. 88. — P.529–535
- Амосова Е. Н., Лыховский О. И., Сапожников А. Р., Сидорова Л. Л. /Состояние внутрисердечной гемодинамики у больных диффузными поражениями печени //Матеріали XIV з'їзду терапевтів України. — К., 2008. — С. 80–81.
- Levy D., Svage D., Garrison R. I. et al. /Echocardiography criteria for left ventricular hypertrophy (the Framingham Heart Study) // Am. J. Cardiology. -2007. — Vol.59. — P.956–960.
Аннотация научной статьи по клинической медицине, автор научной работы — Белобородова Э. И., Челнова И. П., Белобородова Е. В., Челнов В. Г., Тюкалова Л. И.
Целью исследования явилось изучение состояние миокарда у больных хроническим вирусным гепатитом (ХВГ). Постановка диагноза проводилась методом ИФА, методом ПЦР, по биоптату печени с установлением степени активности и стадии хронизации процесса. Для выявления структурно-функциональных изменений миокарда были проведены исследования: регистрация ЭКГ, сцинтиграфия миокарда с 99m Tc-пирофосфата, ультразвуковое исследование сердца в М-,Ви импульсном допплеровском режимах. Выполнена однофотонная эмиссионная компьютерная томография с лейкоцитами, меченными 99m Tc-НМРАО. У 29% больных ХВГ выявлены патологические типы геометрии левого желудочка. У 26% случаев при вирусном гепатите С (ХГС) и 21% при вирусном гепатите В (ХГВ) при допплерографии трансмитрального потока обнаружено нарушение расслабления левого желудочка. Степень выраженности диастолической дисфункции зависела от наличия вируса гепатита С. У трети больных ХГС и ХГВ отмечалось накопление 99m Tc-пирофосфата в миокарде. Изменение параметров, характеризующих геометрию миокарда, а также признаков диастолической дисфункции, даже без изменения систолических показателей, при эхокардиодопплерографии свидетельствуют о вовлечении в патологический процесс миокарда.
Похожие темы научных работ по клинической медицине , автор научной работы — Белобородова Э. И., Челнова И. П., Белобородова Е. В., Челнов В. Г., Тюкалова Л. И.
The aim was to study condition of myocardium in patients with chronic viral hepatitis (CVH). Establishing diagnosis was performed using EIA method, PCR, obtaining liver biopsy sample and determining degree of activity and process chronization stage. To detect structural and functional myocardial changes we performed following tests: ECG, myocardial scintigraphy using 99m Tc pyrophosphate, ultrasound heart examination using and M,B and pulse Doppler mode. SPECT with 99m Tc-НМРАО marked leucocytes was also performed. 29% of CVH pаtients revealed abnormal left ventricle configuration. Doppler imaging of transmitral flow showed that 26% with type C hepatitis (CVC) and 21% with type B (CVB) viral hepatitis showed left ventricular relaxation failure. Diastolic dysfunction degree of activity depended on the presence of type C viral hepatitis . Third of patients with CVC and CVB showed accumulation of 99m Tc pyrophosphate in myocardium. Changes in parameters characterizing myocardial shape and also changes in signs of diastolic dysfunction even without stroke volume index variation testify to the myocardial involvement in the pathological process.
СТРУКТУРНО-ФУНКЦИОНАЛЬНОЕ ПОРАЖЕНИЕ МИОКАРДА У БОЛЬНЫХ ХРОНИЧЕСКИМ ВИРУСНЫМ ГЕПАТИТОМ
Э.И. Белобородова, И.П. Челнова, Е.В. Белобородова, В.Г. Челнов, Л.И. Тюкалова, И.Л. Пурлик, Д.В. Чвырина, С.Г. Шкорлупа
ГОУ ВПО Сибирский государственный медицинский университет Росздрава, Томск E-mail: tatiana05@sibmail.com
STRUCTURAL AND FUNCTIONAL MYOCARDIAL DAMAGE IN PATIENTS WITH CHRONIC VIRAL HEPATITIS
E.I. Beloborodova, I.P. Chelnova, E.V. Beloborodova, V.G. Chelnov, L.I. Tyukalova, I.L. Purlik, D.V. Chvirina, S.G. Shkorlupa
Siberian State Medical University, Tomsk
Целью исследования явилось изучение состояния миокарда у больных хроническим вирусным гепатитом (ХВГ). Постановка диагноза проводилась методом ИФА, методом ПЦР, по биоптату печени с установлением степени активности и стадии хронизации процесса. Для выявления структурно-функциональных изменений миокарда были проведены исследования: регистрация ЭКГ, сцинтиграфия миокарда с "^-пирофосфата, ультразвуковое исследование сердца в М-, В- и импульсном допплеровском режимах. Выполнена однофотонная эмиссионная компьютерная томография с лейкоцитами, меченными "^-НмРАО. У 29% больных ХВГ выявлены патологические типы геометрии левого желудочка. У 26% случаев при вирусном гепатите С (ХГС) и 21% при вирусном гепатите В (ХГВ) при допплерографии трансмитрального потока обнаружено нарушение расслабления левого желудочка. Степень выраженности диастолической дисфункции зависела от наличия вируса гепатита С. У трети больных
ХГС и ХГВ отмечалось накопление 99тТс-пирофосфата в миокарде. Изменение параметров, характеризующих геометрию миокарда, а также признаков диастолической дисфункции, даже без изменения систолических показателей, при эхокардиодопплерографии свидетельствуют о вовлечении в патологический процесс миокарда. Ключевые слова: вирусный гепатит, эхокардиодопплерография, сцинтиграфия миокарда, однофотонная эмиссионная компьютерная томография, тропонин в плазме, поражение миокарда.
The aim was to study condition of myocardium in patients with chronic viral hepatitis (CVH). Establishing diagnosis was performed using EIA method, PCR, obtaining liver biopsy sample and determining degree of activity and process chronization stage. To detect structural and functional myocardial changes we performed following tests: ECG, myocardial scintigraphy using 99mTc-pyrophosphate, ultrasound heart examination using d M-, B- and pulse Doppler mode. SPECT with 99mTc-НМРАО marked leucocytes was also performed. 29% of CVH pаtients revealed abnormal left ventricle configuration. Doppler imaging of transmitral flow showed that 26% with type C hepatitis (CVC) and 21% with type B (CVB) viral hepatitis showed left ventricular relaxation failure. Diastolic dysfunction degree of activity depended on the presence of type C viral hepatitis. Third of patients with CVC and CVB showed accumulation of 99mTc-pyrophosphate in myocardium. Changes in parameters characterizing myocardial shape and also changes in signs of diastolic dysfunction even without stroke volume index variation testify to the myocardial involvement in the pathological process.
Key words: viral hepatitis, echo Doppler imaging, myocardial scintigraphy, SpECT, troponin in plasma, myocardial damage.
Хронические вирусные гепатиты (ХВГ) занимают значительное место в структуре заболеваний органов пищеварения, оставаясь серьезной социально-экономической и клинико-эпидемиологической проблемой здравоохранения всех стран мира 3. При инфицировании вирусом гепатита С и В у многих больных на различных стадиях прогрессирования процесса в печени развиваются поражения других органов и систем, которые могут протекать как латентно, так и в виде ярких клинических синдромов или самостоятельных заболеваний.
Среди внепеченочных проявлений ХВГ поражение сердца, во многом определяющее прогноз заболевания, составляет от 8 до 18,4% 6. В то же время, лишь у 18% больных сердечные признаки сразу расцениваются как проявление системного поражения вирусом гепатита. Можно согласиться с авторами, которые считают, что патология миокарда остается зачастую нераспознанной, маскируясь другими поражениями. До сих пор у исследователей нет однозначного мнения о патоморфологической основе кардиальных проявлений ХВГ [9, 10].
В связи с тем, что эндомиокардиальная биопсия подтверждает клинический диагноз миокардита в 17-37% случаев, проведение чреззондовой трансвенозной биопсии при поражении миокарда у больных ХВГ не отвечает современным деонтологическим требованиям к диагностике. Кроме того, риск самой инвазивной процедуры, связанной с зондированием сердца и взятием биопсии, достаточно велик и превышает зачастую риск данного заболевания для жизни [11, 12]. Все это диктует необходимость поиска более совершенных, малоинвазивных, специфичных методов диагностики поражений сердца у больных ХВГ.
Современная кардиология располагает малоинвазивными, высокоспецифичными методами оценки поражения миокарда при жизни. К ним относятся методы ядерной медицины, которые дают возможность оценить патофизиологические процессы, происходящие в пораженном органе, а также ультразвуковые и лабораторные тесты определения в крови маркеров повреждения миокарда.
Цель исследования - изучить состояние миокарда у больных хроническим вирусным гепатитом.
Материал и методы
Обследовано 38 пациентов с хроническим вирусным гепатитом. В зависимости от этиологии вирусного гепатита выделили подгруппу А, представленную больными хроническим вирусным гепатитом С (ХГС) - 28 человек и подгруппу В - 10 пациентов с хроническим вирусным гепатитом В (ХГВ). Подавляющее большинство больных были молодого возраста - до 30 лет (71,0%) и преобладали мужчины (76,3%).
Критериями исключения явились: возраст старше 40 лет, беременность, прием лекарственных препаратов (нестероидных противовоспалительных, гормональных контрацептивов), сопутствующие заболевания, которые могли повлиять на результаты проводимых исследований. До исследования больные не получали какой-либо этиотроп-ной противовирусной терапии. Клинически и амнести-чески у больных были исключены злоупотребления алкоголем и гепатотоксическими веществами. Для суждения о нормальных параметрах изучаемых показателей обследовано 20 здоровых лиц (контрольная группа), сопоставимых по возрастным и половым характеристикам с пациентами основной группы.
Всем больным проводилось стандартное общеклиническое обследование крови с определением общего белка, белковых фракций, аланинаминотрансферазы, аспар-татаминотрансферазы, щелочной фосфатазы, тимоловой пробы, общего билирубина и его фракций, глюкозы, С-реактивного протеина, серомукоидов по стандартным методикам. Всем больным проводилось ультразвуковое исследование органов брюшной полости. Этиологическая верификация диагноза проводилась методом ИФА, тест-наборами Elisa. Верификация репликативной фазы развития вируса, что было выявлено у всех больных, проводилась методом ПЦР. Морфологическая верификация диагноза была проведена всем больным по анализу био-птата печени с установлением степени активности и стадии хронизации процесса. Сцинтиграфическое исследование сердца было проведено всем обследуемым в одинаковых условиях, через 120 минут после введения 370 МБк "“Т^пирофосфата. Полученные сцинтиграммы обрабатывали с помощью пакета прикладных программ. Пятерым пациентам с выявленным диффузным накоп-
лением меченных "^-фосфатных комплексов однократно была выполнена однофотонная эмиссионная компьютерная томография с лейкоцитами, меченными 99mTc-НМРАО. Ультразвуковое исследование сердца проводилось в М-, В- и импульсном допплеровском режимах по стандартной методике. Определение уровня тропонина Т в плазме крови осуществили на автономном анализаторе “Elecsys 1010” при помощи метода электрохимолю-минисценции с использованием тест-систем от фирмы Roche (Швейцария).
Статистический анализ полученных данных проводился при помощи пакетов статистических программ STATISTICA 6.0; БИОСТАТИСТИКА 4.03, 1998. Применяли методы описательной статистики. Для анализа соответствия вида распределения признака по закону нормального распределения использовали критерий W-тест Шапиро-Уилка, а также метод графического представления выборок на фоне кривой Гаусса. Статистическую значимость при сравнении двух независимых количественных переменных при распределении признака, отличающегося от нормального, оценивали, используя U-тест Манна-Уитни. Для определения взаимосвязи между переменными при несоответствии нормальному закону распределения или балльных оценках вычисляли коэффициенты корреляции - R Спирмена. Статистически значимыми считали различия при p Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Ао, см 2,99 (2,83; 3,07) 3,03 (2,83; 3,18) 3,07 (2,74;3,23)
ЛП, см 3,0 (2,88; 3,07) 3,19 (3,0; 3,39) 3,14 (3,03; 3,21)
ПЖ, см 2,14 (1,87; 2,31) 2,07 (1,84; 2,25) 2,15 (1,93; 2,33)
ТМЖП, см 0,84 (0,82; 0,89) 0,93 (0,88; 1,0)** 0,96 (0,90; 1,0)**
КДР, см 4,72 (4,71; 4,74) 4,89 (4,61; 5,12) 5,26 (4,67; 5,3)
КСР, см 2,91 (2,89; 2,93) 3,09 (2,83; 3,24) 3,27 (2,74;3,33)
КДО, мл 113,07 (102,5; 114,3) 108,5 (97,55; 122,5) 133,0 (108,0; 137,0)
КСО, мл 36,0 (35,35; 36,80) 37,0 (31,1; 43,1) 43,2 (31,0; 45,1)
ТЗСЛЖ, см 0,84 (0,81; 0,88) 0,88 (0,82; 1,0) 0,91 (0,88; 0,93)
ИММЛЖ, г/м2 86,30 (80,05; 94,95) 102,79 (86,63; 114,5)** 97,59 (88,96; 118,28)*
ИОТ, отн. ед. 0,36 (0,35; 0,37) 0,37 (0,35; 0,40)* 0,38 (0,34; 0,39)
различия при сравнении с группой контроля статистически значимы (р Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Показатели Группа контроля, Подгруппа А (ХГС), Подгруппа В (ХГВ),
Нормальная геометрия ЛЖ 20 (100%) 21 (75,0%) 8 (80,0%)
Концентрическое ремоделирование ЛЖ - 3 (10,71%) 1 (10,0%)
Эксцентрическая ГЛЖ - 4 (14,29%) 1 (10,0%)
Примечание: межгрупповые различия статистически не значимы (р>0,05).
Распределение типов ДФ ЛЖ у больных ХВГ и здоровых лиц
Подгруппы обследованных Истинно Напряжение Ригидная Псевдонормальный
нормальный тип АПМ ДДФ тип
Подгруппа А (ХГС), п=26 9 (34,62%') 9 (34,62%) 3 (11,54%) 5 (19,23%'')
Подгруппа В (ХГВ), п=7 2 (25,0') 4 (50,0%) 1 (12,50%) -
Подгруппа контроля, п=20 20 - - -
Примечание: ' - различия при сравнении с группой контроля статистически значимы (р Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
2. У 29% больных хроническим вирусным гепатитом выявлены патологические типы геометрии левого желудочка. Они статистически значимо чаще встречаются у лиц, инфицированных вирусом гепатита С.
3. В 26% случаев при хроническом вирусном гепатите С
и 21% при хроническом вирусном гепатите В при допплерографии трансмитрального потока обнаруживается нарушение расслабления левого желудочка. Степень выраженности диастолической дисфункции в большей степени установлена при хронической пер-систенции в организме вируса гепатита С.
4. У 43% больных ХГС и у 40,0% лиц с ХГВ было отмечено накопление 99тТс-пирофосфата в миокарде. Чаще процесс носил диффузный характер и имел среднюю степень интенсивности, выявленную достоверно чаще при хроническом гепатите С.
5. Поражение миокарда при хроническом течении вирусного процесса не сопровождается некрозом кар-диомиоцитов и носит дистрофический характер.
1. Подымова С.Д. Болезни печени: руководство для врачей. -М. : Медицина, 1993. - 543 с.
2. Сорисон С.Н. Вирусные гепатиты. - СПб. : Теза, 1998. -325 с.
3. Змызгова А.В. Интерферонотерапия вирусных гепатитов. -Новосибирск : Б.и., 2002. - 32 с.
4. Ивашкин В.Т., Буеверов А.О., Грязин А.Е. Механизмы устойчивости вируса гепатита С к противовирусным препаратам // Молекулярная медицина. - 2004. - № 2. - С. 18-23.
5. Чубенко С.С. Внепеченочные проявления хронических вирусных гепатитов // Рос. журнал гастроэнтерологии, гепа-тологии, колопроктологии. - 2002. - № 1(12). - С. 14-16.
6. Абдурахманов Д.Т., Русских А.В. Внепеченочные проявления хронической ИБУ-инфекции // Клиническая фармакология и терапия. - 2003. - № 12. - С. 18-22.
7. Дерюгин М.В., Бойцов С.А. Хронические инфекционно обусловленные миокардиты как проблема в практике кардиолога // Сердце. - 2004. - № 4. - С. 172-180.
8. Ерямкина О.Л., Виноградова И.Б., Бригиневич Б.Е. Внепеченочные проявления хронических ИБУ и ИСУ инфекций // Рус. мед. журнал. - 2006. - С. 6-8.
9. Крель П.Е., Апросина З.Г. Миокардит при хронически ак-
тивном гепатите // Клиническая медицина. - 1989. - № 7.
10. Ягода А.В., Шнюкова Т.Г. Состояние сердечно-сосудистой системы при хронических вирусных гепатитах // Рос. журнал гастроэнтерологии, гепатологии, колопроктологии. -2001. - № 5. - С. 89-93.
11. Атрощенко Е.С. Кардиомиопатия инфицированного гене-за: воспалительные и аутоиммунные механизмы формирования сердечной недостаточности // Рос. кардиол. журнал.
- 2003. - № 6. - С. 29-35.
12. Бойцов С.А., Дерюгин М.В. Современные возможности не-
ревматического миокардита // Consilium Medicum. - 2003.
13. Zignego A.I., Brechot Е.Р. Extra hepatic manifestations of HCV-infection facts and controversies // Hepatology. - 1999. -№ 31. - С. 369-376.
14. Беленков Ю.Н. Ремоделирование левого желудочка: комплексный подход. Сердечная недостаточность // Кардиология. - 2002. - № 4. - С. 161-163.
15. Сазонова С.И. Сцинтиграфическая диагностика воспалительных процессов в сердце : дис. . канд. мед. наук: 05.25.03.

Оглавление диссертации Конышева, Александра Александровна :: 2013 :: Москва
Положения, выносимые на защиту.
Глава 1. Обзор литературы:.
1.1. Основные диагностические критерии цирротической кардиомиопатии.
1.2. Толщина стенок и объем камер сердца.
1.3. Систолическая дисфункция левого желудочка у больных циррозом печени.
1.4. Диастолическая дисфункция левого желудочка у больных циррозом печени.
1.5. Электрофизиологические нарушения.
1.6. Механизмы развития цирротической кардиопатии.
1.6.1. Систолическая дисфункция.
1.6.2. Диастолическая дисфункция.
1.6.3. Электрофизиологические нарушения.
Глава 2. Материал и методы.
2.2. Лабораторные и инструментальные методы обследования.
2.2.1. Клинический анализ крови.
2.2.2. Биохимическое исследование.
2.2.3. Вирусологическое исследование.
2.2.5. УЗИ органов брюшной полости.
2.2.6. Эластометрия печени.
2.2.7. Биопсия печени.
2.3. Статистическая обработка результатов.
Глава 3. Результаты.
3.1. Клинико-морфологическая характеристика обследованных больных.
3.2. Анализ данных электрокардиографии.
3.2.1. Основные параметры электрокардиографии.
Электрическая ось сердца.
3.2.2. Удлинение интервала С^Тс.
3.3. Анализ данных эхокардиографии.
3.3.1. Основные параметры, регистрируемые при эхокардиографии.
3.3.2. Гипертрофия миокарда.
3.3.3. Диастолическая функция.
3.4. Многофакторный анализ.
Глава 4. Обсуждение результатов.
4.1. Удлинение интервала (^Тс.
4.2. Систолическая функция миокарда.
4.3 Гипертрофия миокарда и диастолическая дисфункция.
Введение диссертации по теме "Внутренние болезни", Конышева, Александра Александровна, автореферат
Заболевания печени остаются одной из актуальных проблем современной медицины. По данным Всемирной организации здравоохранения (ВОЗ) треть населения мира инфицирована различными видами гепатотропных вирусов. Несмотря на снижение заболеваемости острым гепатитом, число больных хроническим гепатитом возрастает. Также отмечено снижение количества заболевших вирусным гепатитом В и увеличение больных гепатитом С. В мире насчитывается более 200 млн. носителей вируса гепатита С (HCV) (3% населения Земного шара) (ВОЗ), в том числе более 2 миллионов в России (Онищенко Г. Г., 2002). На долю хронического вирусного гепатита С (ХГС) приходится более 70% всех хронических заболеваний печени. HCV является этиологическим фактором 40% случаев цирроза печени и 60-70% - гепатоцеллюлярной карциномы (EASL International Conference of Hepatitis С, Paris, 1999).
В 1953 году H.Kowalski и соавт. впервые описали удлинение интервала QT у пациентов с циррозом печени. В последующем было показано, что у больных циррозом печени наблюдаются увеличение сердечного выброса и частоты сердечных сокращений (ЧСС) в сочетании с вазодилатацией и снижением АД, снижение сократимости миокарда и систолической функции левого желудочка, особенно при физической нагрузке, гипертрофия миокарда с диастолической дисфункцией левого желудочка, электрофизиологические нарушения. Выявленные изменения сердечнососудистой системы нельзя было объяснить воздействием алкоголя или другими известными причинами [88; 97].
Поражение сердца при циррозе печени может длительное время оставаться бессимптомным. Иногда оно проявляется только после трансплантации печени. Резкое ухудшение функции сердца с развитием сердечной недостаточности после трансплантации печени наблюдается в 7
15% случаев (третье место среди причин летальных исходов) [124]. Описаны случаи развития левожелудочковой недостаточности в раннем послеоперационном периоде у больных, ранее не страдавших сердечнососудистыми заболеваниями.
В исследовании на большой группе больных показано, что при циррозе печени вирусной (НСУ) этиологии происходит поражение сердца, проявляющееся удлинением интервала С>Тс, увеличением толщины межжелудочковой перегородки и задней стенки левого желудочка, ухудшением функции диастолического расслабления (отношение Е/А).
Впервые проведено сравнение поражения сердечно-сосудистой системы у больных циррозом печени и хроническим гепатитом. В предшествующих исследованиях группы сравнения составляли здоровые добровольцы, что не позволяло полностью исключить влияние самого вируса гепатита С на формирование поражения сердца.
Впервые показано, что снижение фильтрационной фракции натрия у больных циррозом печени сопровождается увеличением толщины межжелудочковой перегородки и задней стенки левого желудочка.
Впервые изучен вклад анемии в формирование поражения сердца при циррозе печени. Показано, что анемия может приводить к гипертрофии миокарда и диастолической дисфункции как у больных гепатитом, так и циррозом печени, но является не единственным фактором развития поражения сердца.
Результаты настоящей диссертационной работы свидетельствуют о необходимости ранней диагностики поражения сердца у больных циррозом печени вирусной этиологии, особенно при декомпенсации заболевания печени. С этой целью необходимо проведение электрокардиографии с расчетом длительности интервала С*Тс по формуле Базетта, а также эхокардиографии. При эхокардиографии необходимо оценивать толщину межжелудочковой перегородки и задней стенки левого желудочка, то есть наличие гипертрофии миокарда, а также определять диастолическую функцию левого желудочка по отношению Е/А.
Портальная гипертензия, приводящая к увеличению активности ренин-ангиотензин-альдостероновой системы, может способствовать развитию поражения сердца у больных циррозом печени. Задержка натрия и анемия могут способствовать гипертрофии миокарда и формированию диастолической дисфункции. В связи с этим у больных циррозом печени необходимо оценивать наличие анемии и задержки натрия.
У больных циррозом печени следует тщательно оценивать риск применения различных фармакологических препаратов. Некоторые из них (петлевые диуретики, гепарин, противогрибковые средства) могут вызывать удлинение интервала (^Т, одного из элементов поражения сердца при циррозе печени.
Положения, выносимые на защиту
1. У больных циррозом печени вирусной (НСУ) этиологии происходит удлинение интервала С)Тс по сравнению с таковым у больных гепатитом. Удлинение интервала С)Тс >440 мс встречалось у больных циррозом печени (38%) достоверно чаще, чем у больных гепатитом (6,1%).
2. Гипертрофия и диастолическая дисфункция левого желудочка у больных циррозом печени отмечаются чаще, чем у больных хроническим гепатитом.
3. Декомпенсация цирроза печени приводит к увеличению частоты удлинения интервала С)Тс, гипертрофии миокарда и диастолической дисфункции левого желудочка.
4. Портальная гипертензия, анемия и задержка натрия способствуют формированию поражения сердца у больных циррозом печени.
Изучить частоту и характер поражения сердца при циррозе печени, вызванном вирусом гепатита С, и роль портальной гипертензии, анемии и задержки натрия в его развитии.
1. Сравнить частоту и характер электрокардиографических и эхокардиографических признаков поражения сердца у больных циррозом печени и хроническим гепатитом С.
2. Оценить зависимость частоты поражения сердца от тяжести цирроза печени.
3. Изучить роль анемии, портальной гипертензии и задержки натрия в развитии поражения сердца.
Читайте также:


