Математическая модель вирусной инфекции
Ученые Самарского национального исследовательского университета и Автономного университета Барселоны разработали математическую модель распространения опасных вирусных инфекций. Разработке посвящена статья, опубликованная в журнале Американского института математических наук Mathematical Biosciences and Engineering (MBE). В публикации рассматриваются различные аспекты распространения инфекций среди животных, но, по мнению ученых, данную модель можно применить и к инфекционным заболеваниям человека, в том числе к коронавирусу.
Модель учитывает множество факторов и постоянно изменяющихся данных, в том числе, например, уровни смертности и рождаемости, отсутствие или наличие иммунитета после выздоровления, сокращение кормовой базы или уменьшение запасов еды, а также явление “мнимого исчезновения”. Динамика процессов описывается взаимосвязанными системами дифференциальных уравнений. Особый акцент в своих исследованиях ученые сделали на математическом моделировании критических ситуаций, возникающих по мере распространения болезни в популяции. Модель демонстрирует возможность и неконтролируемого развития событий в случае взрывного характера распространения вируса.
“В распространении вирусной инфекции можно выделить два различных процесса. Когда речь идет о развитии болезни внутри одного организма, то может иметь место явление “мнимого исчезновения”, когда обнаружить возбудителей заболевания не удается только потому, что время взятия биологического материала для анализов – например, крови, плазмы, тканей – соответствовало периоду мнимого исчезновения. Это перекликается с тем, что у некоторых людей, которых считали выздоровевшими от коронавируса, через некоторое время обнаруживали рецидивы болезни, – отметила профессор Самарского университета Елена Щепакина. – Второй процесс – это распространение инфекции в популяции, особи которой подвержены заболеванию, при этом не имеет значения, идет ли речь о популяции микроорганизмов, животных или людей. Одной из особенностей наших исследований является анализ критических значений параметров и моделирование критических явлений”.
По словам профессора, пояснить понятие критического режима и критических явлений можно на примере из теории горения. Процесс горения может протекать плавно и безопасно, но при изменении параметров горения, когда они заходят за пределы допустимых значений, этот процесс может приобрести очень опасный характер, сопровождаемый так называемым тепловым взрывом.
“Критический режим разделяет режимы опасного и безопасного горения. Именно для моделирования подобных явлений и применяются такие специальные математические объекты как “траектории-утки” и их обобщения – “каскады уток” и “черные лебеди”, – сказала Щепакина. – Применительно к модели распространения вирусной инфекции, которая предложена и изучена в нашей статье, это означает принципиальную возможность неконтролируемого развития событий. Поэтому мы считаем, что никакая предосторожность в текущей ситуации по коронавирусу не может быть излишней”.
Как отметила Щепакина, опубликованная в MBE научная работа входит в целую серию статей, написанных учеными Самарского университета на тему математического моделирования биологических процессов. Теоретические основы этих прикладных исследований изложены в ряде монографий, вышедших в известных научных издательствах как в России (“Наука” и “Физматлит”), так и за рубежом (Springer и SIAM). Авторству самарских ученых принадлежит и выдвинутая около 15 лет назад гипотеза о мнимом исчезновении, касающаяся изменений популяций микроорганизмов.
“Мы выдвинули чисто теоретическую гипотезу, суть которой состоит в следующем. В некоторых микробиологических сообществах может иметь место явление, которые мы назвали эффектом мнимого исчезновения: популяция микроорганизмов может сокращаться до исчезающе малых размеров, а по прошествии некоторого времени ее размеры нарастают, причем взрывным образом, при этом временные промежутки, соответствующие мнимому исчезновению, могут превосходить промежутки, на которых популяция имеет значительные размеры, на несколько порядков”, – рассказала Щепакина.
К этой гипотезе с одобрением отнесся известный микробиолог профессор Майкл Прентис (Michael Prentice), возглавлявший отделение медицинской микробиологии в Национальном университете Ирландии.
“Он привлек наше внимание к известным данным об изменениях в популяции морских фагов, которые полностью подтвердили справедливость гипотезы. В соавторстве с Майклом Прентисом была опубликована первая работа на эту тему, после этого вышли еще несколько статей по данной тематике, а буквально на днях мы получили сообщение, что еще одна статья будет опубликована в специальном выпуске журнала Australian and New Zealand Industrial and Applied Mathematics Journal, который будет посвящен юбилею Грэма Уэйка, известного специалиста по математическому моделированию инфекционных заболеваний из новозеландского университета Мэсси”, – сказала Щепакина.
Пресс-служба Самарского национального исследовательского университета
Полный текст:
В данной работе проведен анализ публикаций международных баз данных HighWire, PubMed, Google Scholar в период с 1981 по 2016 год, предложена оригинальная классификация моделей. Все основные математические модели, разработанные для вируса иммунодефицита человека категоризированы на 2 уровня: организменный и популяционный. Организменный уровень делится на модели взаимодействия вируса и человека (изучение репликации вируса иммунодефицита человека, кинетика вирусной популяции в процессе развития заболевания, молекулярные механизмы взаимодействия с иммунными клетками) и модели ингибирующего действия антиретровирусных препаратов (имитационные модели различных терапевтических схем, выработка мутаций резистентности, вирус иммунодефицита человека в клеточных резервуарах, лечение как профилактическое мероприятие). Популяционный уровень можно разделить на модели распространения вируса иммунодефицита человека среди населения (циркуляция различных генотипов вируса, анализ структуры человеческой популяции по возрасту, полу и контингентам риска, тенденции развития в разных географических территориях, изучение факторов, способствующих распространению вирусной инфекции) и управленческие модели, позволяющие наиболее эффективно использовать ресурсы здравоохранения для противодействия эпидемии (анализ профилактической работы, оценка экономических издержек скрининговых, лечебных мероприятий, прогнозирование социально-экономических последствий). Рассмотрены наиболее значимые достижения каждой из представленных групп, выделены не решенные на сегодняшний день проблемы.
660028, Красноярск, ул. Ладо Кецховели, 71–36
644099, Омск, ул. Ленина, 12.
1. Daelemans D., Costes S.V., Cho E.H., Erwin-Cohen R.A., Lockett S., Pavlakis G.N. In vivo HIV-1 rev multimerization in the nucleolus and cyto- plasm identified by fluorescence resonance energy transfer. J. Biol. Chem., 2004, Vol. 279, No. 48, pp. 50167–50175.
2. Tsiang M., Jones G.S., Hung M., Mukund S., Han B., Liu X., Babaoglu K. Affinities between the Binding Partners of the HIV-1 Integrase Dimer-Lens Epithelium-derived Growth Factor (IN Dimer-LEDGF) Complex. J. Biol. Chem., 2009, Vol. 284, pp. 33580–33599.
3. Goonetilleke N., Liu M.K., Salazar-Gonzalez J.F., Salazar G.M.G., Weinhold K.J., Moore S. The first T cell response to transmitted/founder virus contributes to the control of acute viremia in HIV-1 infection. J. Exp. Med., 2009, Vol. 206, pp. 1253–1272.
4. Salimi H., Roche M., Webb N., Gray L.R., Chikere K., Sterjovski J., Ellett A. Macrophage-tropic HIV-1 variants from brain demonstrate altera- tions in the way gp120 engages both CD4 and CCR5. J. Leukoc. Biol., 2013, Vol. 93, pp.113–126.
5. Schlub T.E., Grimm A.J., Smyth R.P., Cromer D., Chopra A., Mallal S. Fifteen to twenty percent of HIV substitution mutations are associated with recombination. J. Virol., 2014, Vol. 88, pp. 3837–3849.
6. Song H., Pavlicek J.W., Cai F., Bhattacharya T., Li H., Iyer S.S., Bar K.J. Impact of immune escape mutations on HIV-1 fitness in the context of the cognate transmitted/founder genome. Retrovirology, 2012, Vol. 9, pp. 89–103.
7. Rodrigo A.G., Shpaer E.G., Delwart E.L., Iversen A.K.N., Gallo M.V., Brojatsch J., Hirsch M.S. Coalescent estimates of HIV-1 generation time in vivo. Proc. Nati. Acad. Sci., USA, 1999, Vol. 96, pp. 2187–2191.
8. Burg D., Rong L., Neumann A.U., Dahari H. Mathematical modeling of viral kinetics under immune control during primary HIV-1 infection. J. Theor. Biol., 2009, Vol. 259, No. 4, pp. 751–759.
9. Alizon S., Magnus C. Modelling the course of an HIV infection: insights from ecology and evolution. Viruses, 2012, Vol. 4, No. 10, pp. 1984– 2013.
10. Pawelek K.A., Liu S., Pahlevani F., Rong L. A model of HIV-1 infection with two time delays: mathematical analysis and comparison with patient data. Math. Biosci., 2012, Vol. 235, No. 1, pp. 98–109.
11. Smith N., Mlcochova P., Watters S.A., Aasa-Chapman M.M., Rabin N., Moore S. Proof-of-principle for immune control of global HIV-1 reacti- vation in vivo. Clin. Infect. Dis., 2015, Vol. 61, pp. 120–128.
12. Zarei H., Kamyad A.V., Heydari A.A. Fuzzy modeling and control of HIV infection. Comput. Math. Methods Med., 2012, Vol. 2012, pp. 1–17.
13. Dolezal J., Hraba T. Mathematical modelling of chemotherapy in HIV infection. Folia Biologica, 1994, Vol. 40, No. 3, pp. 103–111.
14. Donahue D.A., Sloan R.D., Bjorn D.K. Stage-Dependent Inhibition of HIV-1 Replication by Antiretroviral Drugs in Cell Culture. Antimicrob. Agents Chemother., 2010, Vol. 54, No. 3, pp. 1047–1054.
15. Vergu E., Mallet A., Golmard J.-L. Available clinical markers of treatment outcome integrated in mathematical models to guide therapy in HIV infection. J. Antimicrob. Chemother., 2004, Vol. 53, pp. 140–143.
16. Fung I.C.-H., Gambhir M., Sighem A., de Wolf F., Garnett G.P. The clinical interpretation of viral blips in HIV patients receiving antiviral trea- tment: are we ready to infer poor adherence? J. Acquir. Immune Defic. Syndr., 2012, Vol. 60, No. 1, pp. 5–11.
17. Perelson A.S., Deeks S.G. Drug effectiveness explained: the mathematics of antiviral agents for HIV. Sci. Transatlantional Med., 2011, Vol. 3, No. 91, pp. 30.
18. Supervie V., García-Lerma J.G., Heneine W., Blower S. HIV, transmitted drug resistance, and the paradox of preexposure prophylaxis. Proc. Nati. Acad. Sci., USA, 2010, Vol. 107, pp. 12381–12386.
19. Guo D., Zhang G., Wysocki T.A., Wysocki B.J., Gelbard H.A., Liu X.M. Endosomal trafficking of nanoformulated antiretroviral therapy facilitates drug particle carriage and HIV clearance. J. Virol., 2014, Vol. 88, pp. 9504–9513.
20. Petravic J., Martyushev A., Reece J.C., Kent S.J., Davenport M.P. Modeling the timing of antilatency drug administration during HIV treatment. J. Virol., 2014, Vol. 88, pp. 14050–14056.
21. Glaubius R.L., Parikh U.M., Hood G., Penrose K.J., Parikh U.M., Mellors J.W., Bendavid E., Abbas U.L. Deciphering the effects of injectable pre-exposure prophylaxis for combination HIV prevention. Open Forum Infect. Dis., 2016, Vol. 10, pp. 1093–1127.
22. Frank M., Kleist M., Kunz A., Harms G., Schütte C. Quantifying the impact of nevirapine-based prophylaxis strategies to prevent mother-to-child transmission of HIV-1: a combined pharmacokinetic, pharmacodynamic, and viral dynamic analysis to predict clinical outcomes. Antimicrob. Agents Chemother., 2011, Vol. 55, No. 12, pp. 5529–5540.
23. Беляков Н.А., Розенталь В.В., Дементьева Н.Е., Виноградова Т.Н., Сизова Н.В. Моделирование и общие закономерности циркуляции суб- типов и рекомбинантных форм ВИЧ // ВИЧ-инфекция и иммуносупрессии. 2012. Т. 4, № 2. С. 7–18. [Belyakov N.A., Rosental V.V., Dementjeva N.E., Vinogradova T.N., Sizova N.V. Mathematical modelling and general trends of circulation of HIV subtypes and recombinant forms. HIV Infection and Immunosuppressive Disorders, 2012, Vol. 4, No. 2, рр. 7–18 (In Russ.)].
24. May R., Anderson R.M. Transmission dinamics of HIV infection. Nature, 1987, Vol. 326, pp. 137–142.
25. Романюха А.А., Носова Е.А. Модель распространения ВИЧ-инфекции в результате социальной дезадаптации // Управление большими системами, 2011. Выпуск 34. М.: ИПУ РАН. С. 227–253. [Romanyukha A.A., Nosova E.A. Model of the spread of HIV infection as a result of social disadaptation. Management of Large Systems, 2011, Issue 34, Moscow: IPP RAS, рр. 227–253 (In Russ.)].
27. Greenhalgh D., Hay G. Mathematical modelling of the spread of HIV/AIDS amongst injecting drug users. Math. Med. Biol., 1995, Vol. 14, No. 1, pp. 11–38.
28. Vickerman P., Ndowa F., O’Farrell N., Steen R., Alary M., Delany-Moretlwe S. Using mathematical modelling to estimate the impact of periodic presumptive treatment on the transmission of sexually transmitted infections and HIV among female sex workers. Sex. Transm. Infect., 2010, Vol. 86, pp. 163–168.
29. Sighem A., Vidondo B., Glass T.R., Bucher H.C., Vernazza P., Gebhardt M. Resurgence of HIV infection among men who have sex with men in Switzerland: mathematical modelling study. PLoS, 2012, Vol. 7, No. 9, pp. e44819.
30. Quinlivan E.B., Patel S.N., Grodensky C.A., Golin C.E., Tien H., Hobbs M.M. Modeling the impact of Trichomonas vaginalis infection on HIV transmission in HIV-infected individuals in medical care. Sex. Transm. Dis., 2012, Vol. 39, No. 9, pp. 671–677.
31. Ronn M., Garnett G., Hughes G. et al. Lymphogranuloma venereum, HIV and high-risk behaviour: findings from LGV enhanced surveillance and mathematical modeling. Sex. Transm. Infect., 2011, Vol. 87, pp. A48.
32. Mills H.L., Cohen T., Colijn C. Modelling the performance of isoniazid preventive therapy for reducing tuberculosis in HIV endemic settings: the effects of network structure. J. R. Soc. Interface, 2011, Vol. 8, pp. 1510–1520.
33. Akra O.M., Oyejola B.A. Mathematical modeling of the epidemiology and the transmission dynamics of HIV/AIDS infections in Nigeria. Afr. J. Med. Sci., 2010, Vol. 39, рр. 73–80.
34. Benotsch E.G., Mikytuck J.J., Pinkerton S.D. Sexual risk and HIV acquisition among men who have sex with men travelers to Key West, Florida: a mathematical modeling analysis. AIDS Patient Care STDs., 2006, Vol. 20, No. 8, pp. 549–556.
36. Розенталь В.В., Беляков Н.А., Пантелеева О.В. Подходы к прогнозированию эпидемии ВИЧ-инфекции // ВИЧ-инфекция и иммуносупрессии. 2010. Т. 2, № 3. С. 7–15. [Rozental V.V., Beliakov N.A., Panteleeva O.V. Аpproaches to forecasting of HIV epidemic. HIV Infection and Immunosuppressive Disorders, 2010, Vol. 2, No. 6, рр. 7–15 (In Russ.)].
38. Rollins N., Mahy M., Becquet R., Kuhn L., Creek T., Mofenson L. Estimates of peripartum and postnatal mother-to-child transmission probabi- lities of HIV for use in Spectrum and other population-based models. Sex. Transm. Infect., 2012, Vol. 88, рр. 44–51.
39. Нешумаев Д.А., Малышева М.А., Шевченко Н.М., Кокотюха Ю.А, Мейрманова Е.М., Уланова Т.И., Загрядская Ю.Е. Моделирование динамики эпидемии ВИЧ-инфекции с использованием частоты встречаемости ранних случаев заражения // ВИЧ-инфекция и иммуносупрессии. 2016. Т. 8, № 2. С. 53–60. [Neshumayev D.A., Malysheva M.A., Shevchenko N.M., Kokotyukha Yu.A., Meyrmanova Е.M., Ulanova T.I., Zagryadskaya Yu.Е. Modeling the dynamics of HIV epidemic based on the incidence of early HIV cases. HIV Infection and Immunosuppressive Disorders, 2016, Vol. 8, No. 2, рр. 53–60 (In Russ.)].
41. Бобрик А.В. Профилактика ВИЧ среди потребителей наркотиков в российских городах. Анализ экономической эффективности // Российский семейный врач. 2002. Т. 4, № 6. С. 30–36. [Bobrik A.V. Prevention of HIV among drug users in Russian cities. Analysis of economic efficiency. Russian Family Doctor, 2002, Vol. 4, No. 6, рр. 30–36 (In Russ.)].
42. Boily M.-C., Lowndes C.M., Vickerman P., Kumaranayake L., Blanchard J., Moses S., Ramesh B.M., Pickles M. Evaluating large-scale HIV pre- vention interventions: study design for an integrated mathematical modelling approach. Sex. Transm. Infect., 2007, Vol. 83, pp. 582–589.
43. Heaton L.M., Bouey P.D., Fu J., Stover J., Fowler T.B., Lyerla R. Estimating the impact of the US President’s emergency plan for AIDS relief on HIV treatment and prevention programmes in Africa. Sex. Transm. Infect., 2015, Vol. 91, pp. 615–620.
44. Wilson D.P., Fairley C.K., Sankar D., Williams H., Keen P., Read T.R. Replacement of conventional HIV testing with rapid testing: mathematical modelling to predict the impact on further HIV transmission between men. Sex. Transm. Infect., 2011, Vol. 87, pp. 588–593.
45. Cambiano V., Ford D., Mabugu T., Napierala M.S., Miners A., Mugurungi O. Assessment of the potential impact and cost-effectiveness of self-testing for HIV in low-income countries. J. Infect. Dis., 2015, Vol. 212, pp. 570–577.
46. Coco A. The cost-effectiveness of expanded testing for primary HIV infection. Ann. Fam. Med., 2005, Vol. 3, No. 5, pp. 391–399.
47. Лонг Э.Ф., Брандо М.Л., Гелвин К.М., Виниченко Т., Толе С.П., Шварц А. Оценка эффективности и экономической эффективности стратегии расширенной антиретровирусной терапии в Санкт-Петербурге, Россия // AIDS. 2006. Т. 20. С. 2207–2215. [Long E.F., Brandeau M.L., Galvin K.M., Vinichenko T., Tole S.P., Schwartz A. Effectiveness and cost-effectiveness of strategies to expand antiretroviral the- rapy in St. Petersburg, Russia. AIDS, 2006, Vol. 20, рр. 2207–2215 (In Russ.)].
48. Stover J. Influence of mathematical modeling of HIV and AIDS on policies and programs in the developing world. Sex. Transm. Dis., 2000, Vol. 27, No. 10, pp. 572–578.
50. Galletly C.L., Pinkerton S.D. Preventing HIV transmission via HIV exposure laws: applying logic and mathematical modeling to compare statu- tory approaches to penalizing undisclosed exposure to HIV. J. Law. Med. Ethics., 2008, Vol. 36, No. 3, pp. 577–584.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
Ученые Самарского национального исследовательского университета и Автономного университета Барселоны опубликовали статью в журнале Американского института математических наук Mathematical Biosciences and Engineering (MBE). В публикации рассматриваются различные аспекты распространения инфекций среди животных. По мнению ученых, эту же модель можно применить и к инфекционным заболеваниям человека, в том числе к коронавирусу.

Началось всё с того, что около 15 лет назад самарские ученые выдвинули гипотезу о "мнимом исчезновении", касающуюся изменений популяций микроорганизмов. "В некоторых микробиологических сообществах может иметь место явление, которые мы назвали эффектом мнимого исчезновения: популяция микроорганизмов может сокращаться до исчезающе малых размеров, а по прошествии некоторого времени ее размеры нарастают, причем взрывным образом, при этом временные промежутки, соответствующие мнимому исчезновению, могут превосходить промежутки, на которых популяция имеет значительные размеры, на несколько порядков", - рассказала профессор Самарского университета Елена Щепакина.
К этой гипотезе с одобрением отнесся известный микробиолог профессор Майкл Прентис (Michael Prentice), возглавлявший отделение медицинской микробиологии в Национальном университете Ирландии. "Он привлек наше внимание к известным данным об изменениях в популяции морских фагов, которые полностью подтвердили справедливость гипотезы. В соавторстве с Майклом Прентисом была опубликована первая работа на эту тему, после этого вышли еще несколько статей по данной тематике, а буквально на днях мы получили сообщение, что еще одна статья будет опубликована в специальном выпуске журнала Australian and New Zealand Industrial and Applied Mathematics Journal, который будет посвящен юбилею Грэма Уэйка, известного специалиста по математическому моделированию инфекционных заболеваний из новозеландского университета Мэсси", - сообщила Щепакина.
На основе этих исследований и была создана математическая модель, которая учитывает множество факторов и постоянно изменяющихся данных, в том числе, например, уровни смертности и рождаемости, отсутствие или наличие иммунитета после выздоровления, сокращение кормовой базы или уменьшение запасов еды, а также явление "мнимого исчезновения". Особый акцент в своих исследованиях ученые сделали на математическом моделировании критических ситуаций, возникающих по мере распространения болезни в популяции. Она демонстрирует возможность и неконтролируемого развития событий в случае взрывного характера распространения вируса.
По словам профессора, пояснить понятие критического режима и критических явлений можно на примере из теории горения. Процесс горения может протекать плавно и безопасно, но при изменении параметров, когда они заходят за пределы допустимых значений, этот процесс может приобрести очень опасный характер, сопровождаемый так называемым тепловым взрывом.
Опубликованная в MBE научная работа входит в целую серию статей, написанных учеными Самарского университета на тему математического моделирования биологических процессов. Теоретические основы этих прикладных исследований изложены в ряде монографий, вышедших в известных научных издательствах как в России ("Наука" и "Физматлит"), так и за рубежом (Springer и SIAM).
Елена Щепакина, профессор Самарского университета:
— В распространении вирусной инфекции можно выделить два различных процесса. Когда речь идет о развитии болезни внутри одного организма, то может иметь место явление "мнимого исчезновения", когда обнаружить возбудителей заболевания не удается только потому, что время взятия биологического материала для анализов — например, крови, плазмы, тканей — соответствовало периоду мнимого исчезновения. Это перекликается с тем, что у некоторых людей, которых считали выздоровевшими от коронавируса, через некоторое время обнаруживали рецидивы болезни. Второй процесс — это распространение инфекции в популяции, особи которой подвержены заболеванию, при этом не имеет значения, идет ли речь о популяции микроорганизмов, животных или людей. Одной из особенностей наших исследований является анализ критических значений параметров и моделирование критических явлений.

Издание The Washington Post опубликовало на прошлой неделе математические модели распространения вируса при различных сценариях ограничений людей в социальных контактах, а также при открытой модели распространения вируса.
В начале материала приводится интерактивный график распространения коронавирусной инфекции в США, который представлен экспоненциальной кривой. В течение первых недель с момента первого инфицирования в стране число заболевших нарастало в геометрической прогрессии – сначала медленно, а затем по нарастающей.
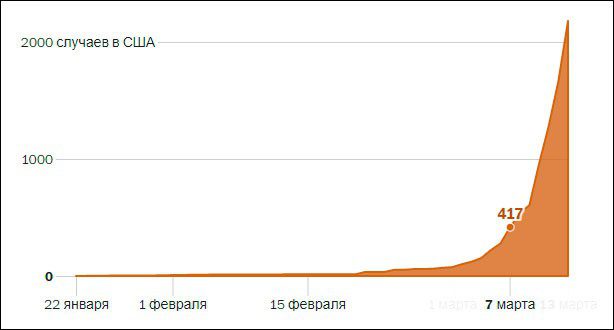
Скриншот, когда в США было 400+ заболевших — примерно как в России по состоянию на 23 марта. Интерактивный график см. по ссылке на оригинал статьи в первом абзаце.
Без каких-либо мер вирус продолжил бы распространяться по стране в геометрической прогрессии еще в течение нескольких месяцев, пишет автор. Однако в США, как и в других странах, власти начали проводить предупредительные меры, что должно помочь остановить столь быстрое распространение вируса.
Журналист Харри Стивенс (Harry Stevens) – автор материала — на примере населенного пункта в 200 жителей предлагает рассмотреть варианты распространения вируса. При построении математической модели журналист допустил ряд упрощений. Например, в модели не учитывались случаи смерти от вируса, а также было принято допущение, что заболевает каждый, кто контактировал с заболевшим.

Свободное распространение инфекции на примере малого городка в 200 жителей.
Далее рассматривается вариант распространения вируса при введении принудительного карантина – как это было сделано в Китае. Там, напомним, в январе в ряде городов были закрыты все въезды и выезды, а также построены специальные больницы для пациентов с подозрением на заражение инфекцией.
Как оказалось, полностью изолировать больное население от здорового невозможно – люди общаются со своими семьями, работают в соседних городах, доставляют товары и пр. В итоге инфекция всё равно поражает подавляющее большинство жителей, однако в более растянутом промежутке времени.
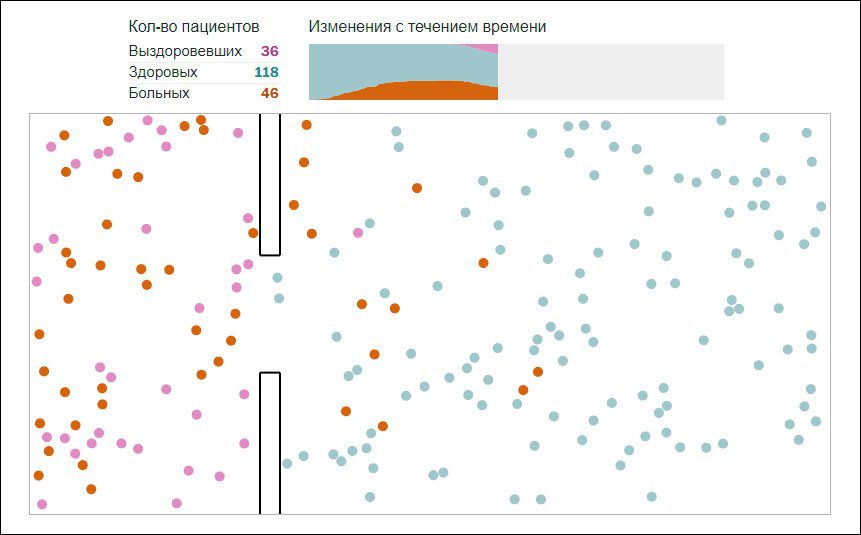
Имитация карантина. Скриншот. Каждый раз новая симуляция показывает разное число заболевших, но это всё равно бОльшая часть жителей городка.
Но есть еще один способ замедлить распространение вируса – ограничение социальных контактов человека, т.е. отказ от посещения массовых мероприятий, пользования общественным транспортом, соблюдение дистанции при общении и пр.
Люди всё равно будут перемещаться и контактировать, пишет автор. У некоторых работа связана непосредственно с контактами с людьми, кто-то просто будет игнорировать предписания либо же жизненные обстоятельства сложатся так, что человеку придется контактировать с другими.
В этом случае автор предлагает рассмотреть два варианта – в контактах ограничены три четверти населения и семь восьмых населения.
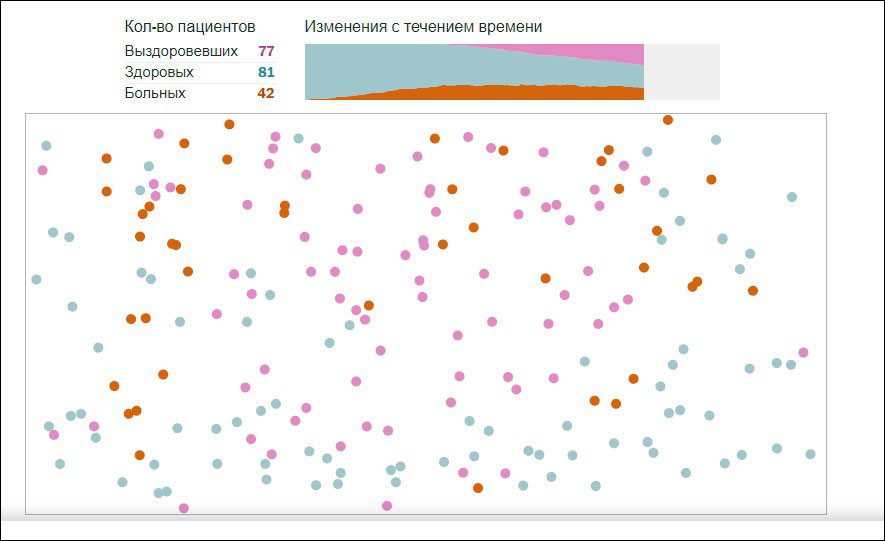
Умеренное дистанцирование. Вирус всё равно поражает минимум половину населения. 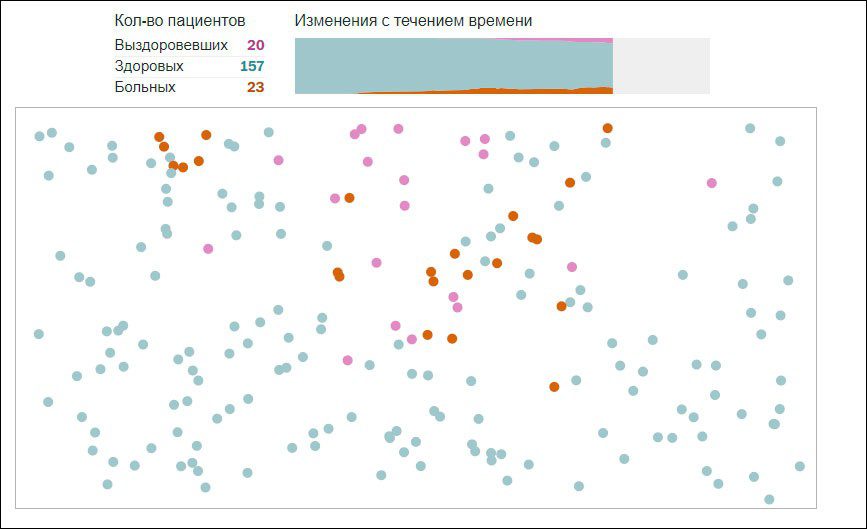
Экстенсивное социальное дистанцирование. Пораженных болезнью меньше четверти населения.
В своём исследовании автор делает вывод, что лучше всего с эпидемией справится экстенсивное социальное дистанцирование, когда социальные контакты поддерживает только один из восьми жителей. Но даже умеренное дистанцирование справится лучше, чем попытка карантина, пишет журналист.
Смотрите на видео, как выглядит цифровая модель экстенсивного дистанцирования:
— Пока мы не можем говорить о каком-то ярко выраженном сценарии для нашей страны. Если ориентироваться на показатели заражения, смертности и выздоровления, то Россия на текущий момент близка к Восточной Европе и Скандинавии. Опасные тенденции, характерные для стран Западной Европы и США, не наблюдаются.
Коронавирусом в мире поражены практически все государства, но явно негативная картина наблюдается примерно в десяти странах. В их число Россия не входит и, при условии соблюдения необходимых мер безопасности, не войдёт.
Если же внимательнее проанализировать официальную статистику смертей от COVID-19, то более половины всех случаев приходится на Италию, Испанию и США.
— Какие существуют математические модели для прогнозов по распространению вирусов и для эпидемий в общем?
— Математический аппарат для моделирования эпидемий очень разнообразен. Самые простые, но и наименее точные модели основаны на экстраполяции имеющихся данных по заболеваемости с помощью методов регрессии, то есть изучения влияния одной или нескольких независимых переменных на зависимую переменную. Более убедительные модели описывают причинно-следственные связи возникновения и развития заболеваний в форме последовательности промежуточных состояний.
— В СМИ сейчас активно обсуждается математическая модель SEIR, доработанная для пандемии COVID-19. Что можете сказать о её точности? Какие модели использует ваша команда?
— Упомянутая вами модель SEIR рассматривает всего четыре возможных состояния человека: S — здоровый, E — заражённый в инкубационном периоде или бессимптомный, I — заражённый в активной стадии болезни и R — умерший или выздоровевший с иммунитетом (в зависимости от интерпретации). Вместе с коллегами, Сергеем Ивановым и Василием Леоненко, сотрудниками Национального центра когнитивных разработок Университета ИТМО, мы разработали эпидемиологические модели с более чем двадцатью состояниями, учитывающими разнообразие структуры социальных контактов. В целом количество состояний определяет степень детализации, необходимую для описания путей распространения того или иного заболевания.
— Можно ли говорить о том, то ваша модель расчётов наиболее эффективна?
— Какие факторы имеют самый большой вес при расчётах? Готовность системы здравоохранения, плотность населения, ответственность граждан, решительные действия властей?
— На этот вопрос нет однозначного ответа. В целом для возбудителей, передающихся воздушно-капельным и контактно-бытовым путём, к которым относится и COVID-19, основными являются факторы биологической природы заболевания: вирулентность, продолжительность инкубационного и инфекционного периодов, уровень смертности. Также важны свойства популяции, в которой протекает болезнь: общая численность, уровень иммунитета, возрастная структура и количество контактов.
Эпидемиологических моделей недостаточно для количественного анализа факторов, ведь распространение инфекции — социальный процесс. Особенно это важно для коронавируса, поскольку его распространяют в основном бессимптомные носители.
— Используются какие-то дополнительные модели?
— Параллельно с эпидемиологической моделью используется модель, описывающая повседневную жизнь и активность населения, так называемое виртуальное общество. Такую модель мы разработали в Институте дизайна и урбанистики Университета ИТМО для Санкт-Петербурга при поддержке Российского научного фонда. Она позволяет воспроизвести распределение плотности населения города в течение суток и оценить структуру контактов между людьми на дому, на работе, в магазине, в транспорте.
— Существуют ли модели расчётов эффективности разных по строгости режимов: ограничения передвижения, самоизоляции, карантина и ЧС?
— Подобные расчёты выполняются разными научными коллективами и обычно не совпадают количественно. При этом они демонстрируют понятную тенденцию — чем меньше контактов, тем меньше заражённых. Однако на основе модели виртуального общества можно управлять различными социальными механизмами таких контактов.
— Как влияет социальная активность отдельного человека на общую картину?
— Приём разделения на группы эффективно работает даже против суперраспространителей и нарушителей карантина. Они будут неспособны заметно повлиять на эпидемиологическую обстановку в целом. Однако в силу недостаточной изученности коронавируса сложно определить характеристики структуры социальных связей, ограничивающей развитие эпидемии. При этом, судя по аналогичным случаям и опыту других стран, принимаемые в России меры позволяют надеяться на лучшее.
— Как рассчитываются последствия? Когда будет пик, спад эпидемии в России?
Эпидемия идёт на спад, когда каждый заражённый инфицирует менее одного здорового. Этот процесс неизбежен, в первую очередь, в силу биологических причин, таких как постепенная иммунизация общества или ослабление самого вируса, которому для своего выживания и распространения убивать своего носителя совершенно невыгодно.
— Есть ли модели расчёта появления подобных бедствий, их предупреждения? Может ли ваша работа помочь устранить такие угрозы на старте?
— Сам факт появления таких бедствий заранее выявить достаточно сложно. Обычно для этого используются весьма общие модели эволюции сложных систем. Они описываются нелинейными дифференциальными уравнениями и способны иногда демонстрировать хаотическое поведение, которое и считается началом какого-либо бедствия: эпидемии, финансового кризиса или революции. Основное внимание уделяют раннему обнаружению так называемых критических точек, когда система находится в переходном состоянии и достаточно лёгкого толчка, чтобы отправить её в кризис, который не остановить.
— Прежде всего, в ситуации с COVID-19 ярко проявилась проблема противопоставления личности и общества. Во всех странах предписания по самоизоляции выполняются не всеми и не всегда. При этом консолидация общества в части минимизации социальных связей позволяет компенсировать действия нарушителей, и эпидемия распространяется в значительно меньших масштабах. Однако никому не следует расслабляться, так как от таких действий страдают именно нарушители, которые первыми становятся жертвами инфекции.
Другая тенденция, с которой мы столкнулись, следует из логики науки о глобальных системах. Она описывает каскады критических эффектов, возникающих в нескольких связанных сложных системах. Например, когда быстрое распространение эпидемии через социальные связи порождает снижение логистической активности и одновременную перегрузку цифровых сетей.
Читайте также:


