Лечение гепатита с пегинтроном и рибавирином отзывы

Хронический вирусный гепатит С (ХВГС) – заболевание, имеющее высокую медико-социальную значимость и связанное с высокой распространенностью, трудностями диагностики, лечения и серьезными осложнениями. ХВГС страдают около 170 млн. человек в мире. ХВГС – самая частая причина пересадки печени и заболеваемости гепатоцеллюлярным раком. Ежегодно от осложнений терминальной стадии цирроза печени, ассоциированного с ВГС, умирают около 500 тыс. человек [1].
Учитывая большое число инфицированных пациентов и вероятное увеличение распространенности ХВГС в будущем, на протяжении следующих нескольких десятилетий в России можно ожидать постоянного роста заболеваемости, смертности и затрат на лечение. Однако эту тенденцию можно изменить, если больные ХВГС будут обеспечены противовирусными препаратами.
В России имеется большое число больных с установленным диагнозом ХВГС, однако частота противовирусной терапии относительно низкая по сравнению с другими европейскими странами [1]. Низкая частота противовирусной терапии обусловлена различными причинами. Главная из них – низкая доступность противовирусных препаратов для пациентов.
С момента открытия интерферонов именно α-интерферон стал одним из главных агентов противовирусной терапии ХВГС. Затем в практику вошла его комбинация с ребетолом (рибавирином), позднее появились пегилированные аналоги α-интерферон (ПЕГ-ИФН-α), которые также применяются в сочетании с ребетолом [3]. Стандартом лечения ХВГС, вызванного, например, вирусом 1-го генотипа, служит применение ПЕГ-ИФН-α и ребетола (рибавирина) в течение 48 недель, что обеспечивает устойчивый вирусологический ответ (УВО) приблизительно у 40–76 % пациентов. Эту терапию может себе позволить не каждый пациент, из-за её дороговизны.
Появление новых недорогих противовирусных препаратов может привести к увеличению доли больных, получающих противовирусную терапию и, самое главное, снизить затраты на лечение.
Было интересно выявить эффективность клинического применения пегинтрона и альгерона, а так же сравнить их эффективность между собой для лечения хронического вирусного гепатита С у больных находящихся на лечении в областной клинической инфекционной больнице и в областном центре по профилактике и борьбе со СПИД и инфекционными заболеваниями г. Воронежа.
Цель исследования: оценка эффективности клинического применения пегинтрона и альгерона в комплексной терапии больных ХГС, находящихся на лечении в областной клинической инфекционной больнице и в областном центре по профилактике и борьбе со СПИД и инфекционными заболеваниями г. Воронежа.
Задачи исследования
1) изучить влияние комбинированной противовирусной терапии препаратами пегинтрон и ребетол на лабораторные параметры у больных с ХВГС.
2) оценить эффективность комбинированного использования противовирусной терапии отечественными препаратами альгерон и ребетол у пациентов с ХВГС на фоне базисного лечения.
3) исследовать сравнительную эффективность комбинированной противовирусной терапии препаратами пегинтрон и ребетол с препаратами альгерон и ребетол у пациентов с ХВГС.
Материалы и методы исследования
Первая группа – 25 историй болезни за 2014 год, из которых 12 мужчин и 13 женщин в возрасте от 24 до 57 лет. У 15 пациентов генотип 1в, у 10 пациентов – 3а.
Первая группа пациентов получали комбинированную противовирусную терапию: ПегИнтрон (Шеринг-Плау, Бельгия) 120-150 мкг п/к 1 раз в неделю (в зависимости от массы тела) + ребетол 800-1200 мг/сут per os, разделенной на 2 приема (назначался в зависимости от массы тела).
Вторая группа – 25 историй болезни за 2015 год, из которых 13 мужчин и 12 женщин в возрасте от 27 до 54 лет. У 12 пациентов был генотип 1в HCV, у 13 пациентов – 3а.
Вторая группа пациентов получали комбинированную противовирусную терапию: альгерон (BIOCAD, Россия) 100-150 мкг п/к 1 раз в неделю (в зависимости от массы тела) + ребетол 800-1200 мг/сут per os, разделенной на 2 приема (назначался в зависимости от массы тела).
Помимо общеклинических методов обследования, у всех больных проводилось полное серологическое обследование на маркеры вирусных гепатитов В, С, D с использованием методов ИФА и молекулярной диагностики (ПЦР). ПЦР-диагностика проводилась в режиме real-time, чувствительность использованных тест-систем (РНК HCV Амплисенс) составляла 50 копий/мл. У каждого пациента определялся также генотип HCV и количественное определение РНК HCV в крови. Всем больным выполнялись ФГС и УЗИ органов брюшной полости утром натощак. Для выявления фиброза печени всем больным была также проведена фиброэластометрия ткани печени на фиброскане (Fibroscan FS-502, Echosens, Франция).
У всех обследованных до начала терапии отсутствовали изменения со стороны системы кроветворения, функции почек, щитовидной железы, отмечали нормальный уровень тиреотропного гормона в плазме.
Эффективность терапии в двух группах оценивали по степени выраженности и динамики лабораторных показателей нежелательных явлений противовирусной терапии (уровень лейкоцитов, тромбоцитов, нейтрофилов и гемоглобина). При достижении критических значений требуется модификация дозы или отмена препаратов.
Общепринятым методом оценки эффективности лечения ХВГС является достижение вирусологического ответа. Вирусологические критерии оценки эффективности – основные показатели успешности противовирусного лечения гепатита С. Вирусологическими критериями оценки эффективности лечения являются: быстрый вирусологический ответ (БВО) – РНК ВГС ниже уровня детекции анализатора через 4 недели лечения; ранний вирусологический ответ (РВО); частичный РВО – снижение уровня РНК ВГС от исходного значения на 2 log10 или более (≥100 раз) через 12 недель лечения и полный РВО – отсутствие детекции РНК ВГС через 12 недель лечения.
Таким образом, во время лечения необходимо определять быстрый и ранний вирусологический ответ.
Существует большая вероятность достижения УВО при достижении быстрого вирусологического ответа, чем при частичном РВО или при замедленном вирусологическом ответе на лечение.
Быстрый и полный ранний вирусологические ответы могут рассматриваться в качестве предикторов устойчивого вирусологического ответа. При отсутствии достижения РВО вероятность получения УВО составляет ≤ 3 %. В таком случае необходимо прекратить лечение.
Результаты исследования и их обсуждение
Сравнительный анализ частоты достижения биохимического ответа не выявил статистически достоверных различий между группами [4]. В процессе проводимого лечения у пациентов первой группы, получавших пегинтрон и ребетол отмечена лейкопения до 3,7±0,05×109/л и 3,4±0,02×109/л (р

В настоящее время стандартом противовирусной терапии (ПВТ) хронического гепатита С (ХГС) является комбинация пегилированного интерферона – альфа (Пег – ИНФ – альфа) и рибавирина, обеспечивающая 40–50 % в частоте достижения СВО при инфицировании HCV 1 генотипа при продолжительности лечения в течение 48 недель и 70–90 % при инфицировании HCV 2 и 3 генотипов и проведения лечения в течение 24 недель [1, 3, 4, 5, 7].
Цель исследования: определение частоты устойчивого вирусологического ответа у больных хроническим гепатитом С при применении различных схем комбинированной противовирусной терапии.
Материалы и методы исследования
В исследование включены взрослые пациенты в возрасте 18–58 лет с хроническим гепатитом С, вызванным HCV генотипов 1, 2, 3, которые ранее не получали противовирусного лечения.
Критериями включения в исследование являлись: серологическое подтверждение гепатита С положительным результатом антител к HCV методом ИФА, качественное и количественное определение РНК HCV с помощью ПЦР, отсутствие изменений со стороны органов кроветворения, почек, щитовидной железы, количество нейтрофилов более 3,0х109/л, тромбоцитов более 100х109/л, гемоглобина более 120 г/л для женщин и более 130 г/л для мужчин, нормальные уровни креатинина и тиреотропного гормона.
Критериями исключения являлись: ВИЧ-инфекция, туберкулез, проводившаяся ранее ПВТ по поводу ГС, системная иммуномодулирующая или противоопухолевая терапия в течение предшествующих 6 мес., пациенты с сахарным диабетом, психическими расстройствами, иммунологически обусловленными заболеваниями, декомпенсированным циррозом печени, тяжелыми хроническими декомпенсированными заболеваниями, страдающие алкоголизмом и наркоманией, беременные и кормящие женщины, мужчины, имеющие беременных половых партнерш.
Этиологическую верификацию гепатитов проводили с помощью серологических методов с определением анти-HCV core, неструктурных белков NS3, NS4, NS5, молекулярно-биологических методов – полимеразной цепной реакции на аппарате Термоциклер для амплификации нуклеиновых кислот IQ5 CUCLER в реальном времени с определением генотипа вируса и вирусной нагрузки. Определяли также степень фиброза (по шкале METAVIR – F0, F1, F2, F3 , F4) методом ультразвуковой эластометрии печени. Противовирусную эффективность оценивали по наличию быстрого вирусологического ответа – уменьшение виремии в 100 раз и более (> 2 log10) от исходного уровня через 4 недели терапии, раннего вирусологического ответа – уменьшение виремии в 100 раз и более (> 2 log10) от исходного уровня через 12 недель терапии, непосредственного вирусологического ответа – отсутствие РНК-HCV по окончании курса противовирусной терапии (через 24 и 48 недель в зависимости от генотипа вируса гепатита С).
Результаты исследования и их обсуждение
В клиническое исследование включены 293 больных с хроническим вирусным гепатитом С. Больные разделены на четыре группы. Первая группа – 21 больной с 1 генотипом хронического гепатита С получал стандартную терапию пегинтроном в дозе 1,5 мкг/кг/нед. и рибавирином 10,6 мг/кг/сут. Вторая группа – 28 больных со 2–3 генотипами хронического гепатита С получали стандартную терапию пегинтроном в дозе 1,5 мкг/кг/нед. и рибавириом 10,6 мг/кг/сут. Третья группа – 116 больных с 1 генотипом хронического гепатита С получали терапию альтевиром в дозе 3 млн МЕ 3 раза в неделю и рибавирином 10,6 мг/кг/сут. Четвертая группа – 128 больных со 2–3 генотипами хронического гепатита С получали терапию альтевиром в дозе 3 млн МЕ 3 раза в неделю и рибавирином 10,6 мг/кг/сут. Курс лечения пациентов с 1 генотипом составил – 48 недель, а пациентов со 2–3 генотипами – 24 недели.
По полу больные были распределены следующим образом: среди пациентов первой группы было 23 мужчины (46 %) и 26 женщин (54 %). Среди пациентов второй группы было 13 мужчин (46 %) и 15 женщин (54 %). В третьей группе – 48 мужчин (41 %) и 68 женщин (59 %), в четвертой группе – мужчин – 40 (31 %), женщин – 88 (69 %). Во всех группах доминировали пациенты женского пола.
Среди пациентов первой группы высокая вирусная нагрузка (более 400000 МЕ/МЛ) регистрировалась у 9 пациентов (43 %), низкая вирусная нагрузка у 12 больных (57 %). Во второй группе у 7 (25 %) больных отмечалась высокая вирусная нагрузка и у 21 больного (75 %) низкая вирусная нагрузка. В третьей группе пациентов высокая вирусная нагрузка зарегистрирована у 53 (46 %) пациентов и низкая вирусная нагрузка у 63 (54 %) пациентов. В четвертой группе соответственно 49 (38 %) и 79 (62 %) больных. Во всех группах у большинства больных выявлена низкая вирусная нагрузка.
Оценка степени фиброза печени при хроническом вирусном гепатите С принципиально важна в клинической практике для определения прогноза и показаний к лечению. Кроме того, у этих больных нередко морфологические критерии используются для оценки результатов лечения. Перед началом противовирусной терапии в первой группе обследовано 17 (81 %) пациентов: у 2 человек (11 %) выявлен фиброз F0 степени, F1 степени – у 5 (29 %), F2 степени – у 6 больных (36 %), 3 пациента имели фиброз F3 (18 %), и F4 степени выявлен у 1 больного (6 %). Во второй подгруппе обследовано 2 (85 %) пациентов, выявлен фиброз F0 степени – у 4 больных (17 %), F1 степени – 5 больных (21 %), F2 степени – 8 (33 %), F3 степени – 5 (21 %), F4 степени – 2 (8 %). В третьей группе обследовано 92 (79 %) пациентов: у 18 человек (20 %) выявлен фиброз F0 степени, F1 степени – у 19 (21 %), F2 степени – у 26 больных (27 %), 21 пациент имел фиброз F3 (23 %) и F4 степени выявлен у 8 больных (9 %). В четвертой группе обследовано 97 (76 %) пациентов, выявлен фиброз F0 степени – у 16 больных (16 %), F1 степени – 18 больных (19 %), F2 степени – 34 (25 %), F3 степени – 20 (21 %), F4 степени – 9 (9 %) (рисунок 10). Во всех группах преобладали больные с фиброзом F1 и F2.
Группы были сопоставимы по полу, генотипам, вирусной нагрузке, выраженности фиброза печени .
У пациентов оценивали быстрый вирусологический ответ – через 4 недели от начала лечения. На фоне лечения через 4 недели в первой группе HCV РНК не определялась у 10 больных (47 %), у 10 пациентов (47 %) отмечалось снижение вирусной нагрузки на 2 log: быстрый вирусологический ответ достигнут у 20 пациентов (95 %) первой группы. Во второй группе больных при оценке быстрого вирусологического ответа HCV РНК не определялась у 20 больных (71 %), у 6 пациентов (21 %) отмечалось снижение вирусной нагрузки на 2 log: быстрый вирусологический ответ достигнут у 26 пациентов (92 %) второй группы. В третьей группе на фоне лечения через 4 недели HCV РНК не определялась у 52 больных (45 %), у 55 пациентов (47 %) отмечалось снижение вирусной нагрузки на 2 log: быстрый вирусологический ответ достигнут у 107 пациентов (92 %) третьей группы. В четвертой группе больных при оценке быстрого вирусологического ответа HCV РНК не определялась у 101 больного (79 %), у 24 пациентов (19 %) отмечалось снижение вирусной нагрузки на 2 log: быстрый вирусологический ответ достигнут у 125 пациентов (98 %) четвертой группы.
При анализе раннего вирусологического ответа (через 12 недель от начала терапии) в первой группе пациентов полная элиминация HCV РНК произошла у 19 (90 %) пациентов, снижение вирусной нагрузки на 2 log и более достигнуто у 2 пациентов; таким образом, ранний вирусологический ответ достигнут у 21 больного первой группы (100 % случаев). Во второй группе больных при оценке раннего вирусологического ответа HCV РНК не определялась у 24 пациентов (86 %), у 4 пациентов (14 %) отмечалось снижение вирусной нагрузки на 2 log: ранний вирусологический ответ достигнут у 28 пациентов (100 % случаев) второй группы. В третьей группе через 12 недель от начала терапии полная элиминация HCV РНК произошла у 93 (80 %) пациентов, снижение вирусной нагрузки на 2 log и более достигнуто у 11 пациентов (10 %); таким образом, ранний вирусологический ответ достигнут у 104 больных третьей группы (90 % случаев). В четвертой группе больных при оценке раннего вирусологического ответа HCV РНК не определялась у 117 пациентов (91 %), у 3 пациентов (3 %) отмечалось снижение вирусной нагрузки на 2 log: ранний вирусологический ответ достигнут у 120 пациентов (94 % случаев) четвертой группы.
При оценке непосредственного вирусологического ответа через 48 недель от начала терапии в первой группе пациентов оказалось, что полная элиминация HCV РНК достигнута у 17 (81 %) пациентов. Два пациента сняты по медицинским показаниям, в связи с развитием на 24-й неделе терапии неспецифического язвенного колита и аутоиммунного тиреоидита. Отказ от противовирусной терапии у 1 больного на 25-й неделе, вирусологический прорыв зарегистрирован на 24-й неделе лечения у одного пациента; таким образом, непосредственный вирусологический ответ на 48-й неделе терапии достигнут у 17 больных первой группы (81 % случаев). Во второй группе больных при оценке непосредственного вирусологического ответа на 24-й неделе терапии HCV РНК не определялась у 24 пациентов (85 % случаев). Вирусологический прорыв выявлен у 3 пациентов на 24-й неделе терапии, аутоиммунный тиреоидит на 14-й неделе диагностирован у одного пациента. Во второй группе непосредственный вирусологический ответ на 24-й неделе достигнут у 24 пациентов (85 % случаев).
При оценке непосредственного вирусологического ответа через 48 недель от начала терапии в третьей группе пациентов оказалось, что полная элиминация HCV РНК достигнута у 78 (67 %) пациентов. Вирусологический прорыв на 24-й неделе лечения выявлен у 15 больных, развитие депрессии на 24 и 35-й неделе диагностирован у 2 пациентов, отказ от продолжения лечения у 8 больных; таким образом, непосредственный вирусологический ответ на 48-й неделе терапии достигнут у 67 % больных первой группы (78). В четвертой группе больных при оценке непосредственного вирусологического ответа на 24-й неделе терапии HCV РНК не определялась у 113 пациентов (88 % случаев). Вирусологический прорыв выявлен у 2 пациентов на 24-й неделе терапии, аутоиммунный тиреоидит на 16-й неделе диагностирован у одного пациента, у 3 пациентов развитие психоза на фоне употребления психоактивных веществ. В четвертой группе непосредственный вирусологический ответ на 24 недели достигнут в 88 % случаев (113 пациентов).
При оценке устойчивого вирусологического ответа, проведенного через 6 месяцев после завершения терапии, в первой группе пациентов на контроль эффективности лечения обратилось 76 % пациентов (13 из 17 больных). Полная элиминация HCV РНК достигнута у 11 (85 %) пациентов. У двух пациентов зарегистрирован вирусологический прорыв 15 %. Во второй группе больных при оценке устойчивого вирусологического ответа на контроль эффективности лечения обратилось 86 % пациентов (21 из 24 больных). HCV РНК не определялась у 18 пациентов (86 % случаев). Вирусологический прорыв выявлен у 3 пациентов (14 % случаев).
При оценке устойчивого вирусологического ответа в третьей группе пациентов на контроль эффективности лечения обратилось 69 % пациентов (54 из 78 больных). Полная элиминация HCV РНК достигнута у 40 (74 %) пациентов. Рецидив заболевания выявлен у 14 (26 %) больных. В четвертой группе больных на контроль эффективности лечения обратилось 59 % пациентов (67 из 113 больных). Устойчивый вирусологический ответ достигнут у 52 пациентов (77 % случаев). У 15 пациентов выявлен рецидив заболевания в 22 % случаев.
Выводы
1. Лечение пегинтроном в сочетании с рибавирином у пациентов с 1 генотипом хронического гепатита С позволяет достигнуть устойчивого вирусологического ответа в 85 % случаев.
2. Лечение пегинтроном в сочетании с рибавирином у пациентов со 2–3 генотипами хронического гепатита С позволяет достигнуть устойчивого вирусологического ответа в 86 % случаев.
3. Лечение альтевиром в сочетании рибавирином у пациентов с 1 генотипом хронического гепатита С позволяет достигнуть устойчивого вирусологического ответа в 74 % случаев.
4. Лечение альтевиром в сочетании рибавирином у пациентов со 2–3 генотипами хронического гепатита С позволяет достигнуть устойчивого вирусологического ответа в 77 % случаев.
Рецензенты:
Т.Н. Лопаткина, ММА им. И.М. Сеченова
Изучение эффективности противовирусной терапии (ПВТ) хронического гепатита С (ХГС) и внедрение перспективных методов лечения в последнее десятилетие позволило повысить уровень устойчивого ответа с 6% при использовании препаратов интерферона альфа-2Ь (ИФН альфа-2b А) в стандартном режиме (3 млн ME 3 раза в неделю в течение 6 мес) до 61% при комбинированной терапии ПегИФН альфа-2b и Рибавирином в течение 12 мес 3.
Двадцатилетний опыт лечения ХГС противовирусными препаратами показал недостаточную эффективность монотерапии интерфероном альфа (ИФНа): при 6-месячном курсе устойчивый биохимический и вирусологический ответ с отсутствием RNA HCV в сыворотке крови спустя 6 мес после окончания ПВТ отмечался лишь у 6-10% больных ХГС, вызванного различными генотипами вируса гепатита С (HCV). Увеличение продолжительности лечения ИФН альфа-2b в стандартном режиме 3 млн ME 3 раза в неделю до 12 мес позволило в среднем добиваться устойчивого ответа у 15-30% пациентов 7. Строгий подбор "идеального" кандидата для ПВТ с учетом низкой вирусной нагрузки, не 1-го генотипа HCV, молодого возраста, женского пола и небольшой массы тела пациента; отсутствием синдрома перегрузки железом, признаков цирроза печени при морфологическом ее исследовании и коинфекции другими вирусами (ВИЧ, HBV, вирусами герпесгруппы и др.), непродолжительного срока заболевания обеспечивал более высокий устойчивый ответ (30-40%) в группе больных, получавших монотерапию ИФНα.
С середины 90-х годов прошлого века предпочтение в лечении ХГС стали отдавать комбинированной терапии ИФНα и рибавирином - синтетическим аналогом нуклеозидов (коммерческое название Рибавирин). В работах ряда авторов [3, 10] показано, что можно прогнозировать успех лечения ХГС на основании результатов определения уровней RNA HCV после первого месяца лечения. А. Bellobuono и соавт. [10] рандомизировали 60 больных ХГС после первого месяца монотерапии ИФНα в стандартном режиме на три группы: продолжавших лечение ИФНа 3 млн ME 3 раза в неделю, если у них исчезла RNA HCV в сыворотке; получавших ИФНα в стандартном режиме в сочетании с Рибавирином 1000 мг/сут или двойную дозу ИФНα (6 млн ME 3 раза в неделю) - если спустя месяц после ПВТ отсутствовал ранний вирусологический ответ на монотерапию.
После 4 недель терапии 20% пациентов имели вирусологический ответ, а 80% пациентов остались позитивными по RNA HCV. Устойчивый ответ наблюдался у 42% больных с ранним вирусологическим ответом, у 42% - без раннего вирусологического ответа, получавших ИФНа и Рибавирин и только у 4% пациентов, получавших двойную дозу ИФНα (р = 0,006). Авторы отметили эффективность включения в терапию ИФНа Рибавирина и недостаточную эффективности удвоения дозы ИФНа, если не наблюдалось исчезновения RNA HCV на ранних этапах терапии. Превалирование при ХГС пациентов с 1Ь генотипом HCV и наличие у них низкого ответа на монотерапию ИФНа позволили рекомендовать комбинированное применение ИФНα и Рибавирина как терапию выбора при первоначальном лечении, а также для лечения не ответивших больных или с обострением после монотерапии. Отмечено, что комбинированная терапия Рибавирином и ИФНα в высоких дозах превосходит результаты монотерапии высокими дозами ИФНα у больных ХГС, инфицированных генотипом lb HCV[11].
S. Pol и соавт. [11] рандомизировали 307 пациентов с ХГС 1Ь генотипа в 3 группы: А - получавших 6 млн ME ИФНα 3 раза в неделю в течение 6 мес и 3 млн ME 3 раза в неделю в последующие 6 мес; В - 10 млн ME ИФНα 3 раза в неделю в течение 3 мес, 6 млн ME 3 раза в неделю - 3 мес, 3 млн ME 3 раза в неделю в течение последующих 6 мес; С - ИФНα по схеме группы А в комбинации с Рибавирином в течение 4,6 или 12 мес. Устойчивый вирусологический ответ спустя 6 мес после окончания ПВТ достоверно чаще отмечен в группе С, чем в группах А или В (32,8%, 16,9% и 14,1% соответственно, р 10,6 мг/кг Рибавирина
3 млн. ME ИФН альфа-2b А +
> 10,6 мг/кг Рибавирина
Включенные
в лечение
> или = 80%
полученного
лечения *
Включенные
в лечение
> или = 80%
полученного
лечения *
Актуальность. Проблема этиотропного лечения хронического вирусного гепатита С (ХВГС), несмотря на большое количество исследований, по-прежнему остается актуальной и до конца не решена.
Эффективность лечения по данным разных исследователей не превышает 46-51% у больных ХВГС с 1-м генотипом и 70-80% у больных ХВГС с не 1-м генотипом 3. Так же ограничивают их применение высокая стоимость препаратов и большое количество побочных эффектов от проводимой терапии. Целью проведения этиотропной терапии ХВГС является подавление вирусной репликации, эрадикация вируса из организма и, соответственно, прекращение инфекционного процесса. Даже отсутствие вирусологического эффекта при специфической терапии приводит к замедлению прогрессирования заболевания, стабилизации или регрессии патологических изменений в печени, предупреждению формирования цирроза печени и первичной гепатоцеллюлярной карциномы, а также повышению качества жизни.
Оценку эффективности специфического лечения осуществляют на основании нескольких критериев: вирусологического (исчезновение рибонуклеиновой кислоты (РНК) вируса из сыворотки крови), биохимического (стойкая нормализация уровня ферментов печени) и морфологического (уменьшение индекса гистологической активности и стадии фиброза).
В целом около 5% больных [1,5] вынуждены отказаться от специфического противовирусного лечения в начале курса из-за многочисленных побочных эффектов, а 20% не доводят его до конца.
Побочные эффекты интерферона (ИФН) и рибавирина иногда вынуждают временно или постоянно снижать их дозы или отменять препараты. Некоторыми исследователями [5] показано, что для достижения устойчивого вирусологического ответа (УВО) необходимо получение не менее 2/3 дозы ИФН и рибавирина, поэтому эффективность комбинированной противовирусной терапии (КПВТ) напрямую зависит от наличия побочных эффектов и возможностью их коррекции.
Некоторые побочные эффекты не требуют медикаментозной терапии, так как носят легкий или среднетяжелый характер, другие - тяжелый и угрожающий жизни характер, при этом необходима специфическая коррекция. Как правило, после окончания терапии большинство побочных эффектов полностью исчезает без применения симптоматической терапии.
Проблема побочных эффектов на фоне проводимой КПВТ остается до конца не изученной, несмотря на проведенные многочисленные исследования.
Основными побочными явлениями, описанными в литературе, являются: гематологические изменения; гриппоподобный, диспепсический, неврологический и астеновегетативный синдромы; аутоиммунные поражения; снижение массы тела; выпадение волос; огрубение кожи; аллергические реакции различной степени выраженности; местная реакция в области введения интерферонов.
Таким образом, проблема побочного действия комбинированного противовирусного лечения ХВГС, его влияние на достижение УВО является актуальной в настоящее время.
Целью данного исследования было изучение побочных явлений КПВТ в зависимости от схемы лечения, сопутствующих заболеваний, влияние на достижение УВО. Для достижения поставленной цели были сформулированы следующие задачи: оценить переносимость КПВТ пациентами с различными схемами терапии, выявить частоту побочных эффектов КПВТ и взаимосвязь их с достижением УВО.
Материалы и методы. В исследование были включены 50 пациентов с установленным диагнозом ХВГС, которые получали КПВТ. Диагноз был подтвержден согласно общепринятым методикам.
Из исследования исключались пациенты с микст-инфекцией (вирусный гепатит В, ВИЧ-инфекция) а так же наличием сопутствующей патологии печени (первичный билиарный цирроз, болезнь Вильсона-Коновалова, синдром Бадда-Киари, гемохроматоз, аутоиммунный гепатит, дефицит альфа-1 антитрипсина) и предшествующего специфического противовирусного лечения по поводу ХВГС, больные с наличием любого из общепринятых противопоказаний для проведения КПВТ.
Продолжительность лечения составила 48 недель для пациентов, инфицированных генотипом 1в вирусного гепатита С или при наличии у больного цирроза печени; 24 недели для пациентов, инфицированных генотипом 2 и 3а. Согласно рекомендациям по ведению пациентов с ХВГС, КПВП включала комбинацию стандартного (Интрон или Альтевир 3 млн МЕ 3 раза в неделю) или пегилированного (ПегИнтрон 120 мкг или Пегасис 180 мкг в неделю) ИФН и рибавирина в дозировке 800-1200 мг в зависимости от массы тела.
Устойчивый вирусологический ответ (УВО) определялся как отсутствие РНК вируса в сыворотке крови спустя 24 недели после окончания КПВТ. Больные находились под наблюдение в течение терапии на базе Воронежской областной клинической инфекционной больницы и поликлиник Воронежа. Все пациенты были разделены на 2 группы: получающие в составе КПВТ стандартные ИФН – 52,0% (26 человек) или пегилированные ИФН – 48,0% (24 человек). Пациенты были сопоставимы по возрасту и полу: средний возраст составил 40,3 ±10,4, количество мужчин - 57,1%, женщин 42,9%. Распределение по группам показано в табл. 1.
Таблица 1. Характеристика пациентов в исследуемых группах
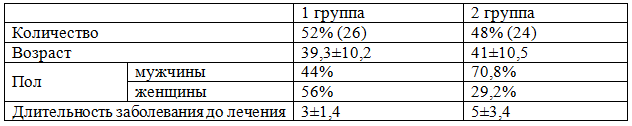
При анализе полученных результатов использовались описательные методы математической статистики с применением пакета программ Microsoft Excel 2010. Достоверность различий оценивалась методами непараметрической статистики, статистически значимыми считались различия результатов при р≤0,05.
Результаты. При анализе эпидемиологических данных выяснено, что в большинстве случаев (34% случаев) ХВГС выявлен случайно, без клинических проявлений. Одинаковое количество пациентов (по 8 человек - 19,2%) обследовались по поводу диспепсических жалоб и длительного повышения печеночных ферментов. У 30 % пациентов в анамнезе отмечались неоднократные операции или переливание крови; употребление внутривенных наркотиков - у 16% человек. Длительность заболевания до начала противовирусной терапии составила в 1 группе 3±1,4 лет, во 2 группе 5±3,4лет. Степень фиброза по Metavir в среднем составил в 1 группе 1±0,85 балла, во второй группе выше - 1,9±1,5 баллов.
Соотношение генотипов вируса гепатита С, определенных до начала КПВТ, показано в табл. 2.
Таблица 2. Соотношение генотипов вирусного гепатита С
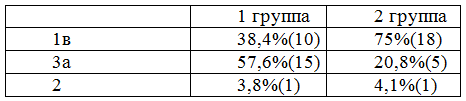
Среди всех пациентов УВО определялся в большинстве случаев - 80,0%, при применении обоих видов терапии, но при этом достоверных различий между группами по этому признаку не выявлено. Эффективность терапии в 1 группе составила 75,1%, во 2 группе - 78,2%. Отсутствие вирусологического ответа в половине случаев связано с отменой препаратов из-за развития выраженных побочных эффектов (прогрессирование неврологической симптоматики с развитием энцефалопатии в 1 группе, длительная некупируемая лихорадка во 2 группе).
Частота побочных эффектов в общей выборке была достаточно высокой - 72,3% среди всех пациентов, при этом в 1 и 2 группе нежелательные явления встречались с одинаковой частотой (69,1% и 73% соответственно).
На протяжении всей терапии у большинства пациентов встречался астеновегетативный синдром в виде выраженной слабости, усталости, нарушения сна, при этом значительно чаще эти проявления отмечали пациенты 2 группы - принимающие пегилированные ИФН (30,7%), что в 2,1 раза чаще, чем во 1 группе (66,6%). Снижение настроения, появление раздражительности, неконтролируемой агрессии при опросе отмечали 23,0% пациентов 1 группы и 25,0% пациентов 2 группы. Данные жалобы чаще встречались на 24±2 неделе терапии. Описанная в литературе депрессия, индуцированная КПВТ, среди данной выборки не встречалась. Для выявления депрессии у всех пациентов применялся опросник Цунга в начале и при завершении КПВТ.
Гриппоподобный синдром, проявляющийся лихорадкой до 38±0,85?С, миалгией, артралгией, выявлен достоверно чаще в у пациентов 1 группы (38,4%), чем у 2 группы (30,1%). Длительность лихорадки составляла в среднем 14±2 недель, первый подъем температуры всегда сопровождал начало КПВТ. Лихорадка купировалась применением препаратов НПВС в стандартных дозировках.
Жалобы со стороны желудочно-кишечного тракта в виде снижения аппетита, тошноты, периодической диареи, боли, вздутия в животе отмечались у 34,6% пациентов 1 группы, что в 2,08 раза чаще, чем во 2 группе (16,6%) .Желтуха на фоне КПВТ встречалась у 2 человек в каждой группе (по 8,3% и 7,6% соответственно).
Снижение веса в среднем на 10,5±5,1 кг, регистрируемое к концу КПВТ, встречалась в 2,3 раза чаще у пациентов 1 группы (19,2%) чем у пациентов среди пациентов 2 группы (8,3%).
Выпадение волос, жалобы на сухость кожи, зуд кожи регистрировались редко: в 1 группе у 2 человек (7,6%среди группы), во 2 группе чаще - у 3 человек(12,5%).
Обострение имеющихся сопутствующих соматических заболеваний встречались в обеих группах приблизительно с одинаковой частотой (30,1% и 27,6% соответственно). Чаще всего встречались обострения хронического панкреатита, язвенной болезни желудка, сахарного диабета.
Частота манифестации впервые выявленных соматических заболеваний на фоне проведения КПВТ имеет прямую корреляционную связь с используемыми препаратами, то есть значительно чаще выявляется при применении ИФН короткого действия, чем пролонгированных форм. При этом в 1 группе на фоне КПВТ манифестировали псориаз (7,6%), аутоиммунный тиреодит (15,3%). А во 2 группе выявлялись гипотиреоз и сахарный диабет (по 4,1% пациентов).
Гематологические осложнения встречались в обеих группах. Анемия, регистрируемая в виде снижения гемоглобина ниже 110г/л, встречалась чаще всего в середине терапии (24±3недели КПВТ). Во второй группе анемия выявлена достоверно чаще – в 2,4раза чаще (38,4%случаев), чем в 1 группе (16% случаев). Эритропоэтин для коррекции анемии применялся в 4 случаях (8%), у остальных коррекции анемии не требовалось.
Среди пациентов обеих групп при наличии анемии УВО встречается в 49,7% случаев, при отсутствии анемии достоверно реже (в 1,35 раз) - у 36,6% пациентов. Таким образом, наличие анемии, в сочетании с другими факторами можно считать предиктором эффективности КПВТ.
Напротив, частота тромбоцитопении на фоне КПВТ коррелировала с отсутствием УВО. Пациенты со снижением уровня тромбоцитов в 1,8 раз реже достигали УВО. Среди всех пациентов тромбоцитопения встречалась только у 8,0% пациентов, что реже, чем по литературным данным. В обеих группах частота данного побочного действия была одинаковой.
Выводы
1. Эффективность терапии с применением препаратов пегилированных или стандартных интерферонов оказалась сходной.
2. Гематологические нежелательные эффекты выявлены достоверно чаще при использовании пегилированных ИФН в составе противовирусной терапии.
3. Гриппоподобный на фоне КПВТ встречались достоверно чаще у пациентов, получающих стандартные ИФН.
4. Астеновегетативный синдром зарегистрирован чаще у пациентов на фоне терапии пегилированными ИФН.
5. Выявлена зависимость между достижением устойчивого вирусологического ответа и величиной снижения уровня гемоглобина.
Список использованных источников:
1. Беляева Н.М., Турьянов М.Х., Рабинович Э.З. Комбинированная терапия гепатита С рибавирином и альфа-интерфероном: Пособие для врачей. - М.: РМАПО. – 2002.
2. Громова Н.И. и Богомолов Б.П. Клиническая эффективность этиотропной терапии хронического вирусного гепатита С// Клин. мед. - 2003.-№1. - С.48.
3. Ивашкин В.Т. Комбинированное лечение хронического гепатита В// Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 1998. №5. С. 57-60.
4. Ferenci P., Fried M., Shiffman M. et al. Predicting sustained virological responses in chronic hepatitis C patients treated with peginterferon alfa-2a// J. Hepatol. – 2005. – Vol. 43. – P. 425–433.
5. Fried M.W. Side effects of therapy of hepatitis C and their management. Hepatology. 2002. - P.237-244
6. Князькина О.В., Каган Ю.Д., Скачков М.В. Микробиоценоз кишечника у больных хроническим вирусным гепатитом С и его лечение// Врач-аспирант, №3.4(52), 2012. – С.579-586.
7. Пирогова И.Ю., Пышкин С.А. Неинвазивная диагностика стадии фиброза у пациентов с хроническими гепатитами В и С// Врач-аспирант, №2(45), 2011. – С. 21-27.
8. Попов С.С., Попов С.Ф. Динамика биохимических показателей гепато-билиарной системы рабочих основных цехов металлургического завода, инфицированных вирусами гемоконтактных гепатитов В и С// Врач-аспирант, №6(55), 2012. – С.55-61.
9. Рихсиева Г.М. Особенности клинико-иммунологических показателей детей, больных острыми вирусными гепатитами А и В, родившихся от матерей, злоупотребляющих алкоголем// Врач-аспирант, №4.4(47), 2011. – С. 675-681.
10. Рюмин А.М., Корочкина О.В., Соболевская О.Л. Закономерности естественного течения хронического гепатита В// Врач-аспирант, №4.1(53), 2012. – С. 214-223.
Читайте также:


